
 |
Effet de la matière organique sur les propriétés physiques et chimiques des sols sableux de la région de Ouargla( Télécharger le fichier original )par Naima KOULL Université Kasdi Merbah Ouargla Algérie - Magister 2007 |
CHAPITRE I: Résultats et interprétations
d'analyses des matériaux
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
CHAPITRE I: Résultats et interprétations d'analyses des matériaux utilisés |
Tableau 05: Résultats des analyses des M.O (fumier bovin et fumier ovin)
|
Caractéristiques de la M.O |
Valeurs |
|||
|
M.O (fumier) bovin |
M.O (fumier) ovin |
|||
|
MS (%) |
34,12 |
41,11 |
||
|
pHeau (1/5) |
6,83 |
6,39 |
||
|
CE à 25°C (1/5) (dS/m) |
13,59 |
14,17 |
||
|
M.O (%) |
69,81 |
57,32 |
||
|
CO (%) |
40,59 |
33,21 |
||
|
N total (%) |
1,57 |
1,48 |
||
|
C/N |
25,85 |
22,43 |
||
|
Na+ (ppm) |
87,50 |
90,00 |
||
|
K+ (ppm) |
57,50 |
60,00 |
||
|
Ca++ (ppm) |
26,42 |
61,00 |
||
|
Mg++ (ppm) |
41,96 |
23,08 |
||
|
Cellulose (%) |
11,00 |
24,00 |
||
|
C. Composés humiques totaux (%o) (MEFTAH, 1988) |
- |
21,40 |
||
|
C. Acide humique (%o) |
- |
14,85 |
||
|
C. Acide fulvique (%o) |
- |
6,55 |
||
|
CHAPITRE I: Résultats et interprétations d'analyses des matériaux utilisés |
||||
B- Résultats et interprétations d'analyse du sol initial
Avant de répondre à la question posée précédemment s'il y a vraiment des paramètres du sol qui seront modifiées par l'apport du fumier, il est indispensable d'avoir les analyses initiales du sol que nous avons utilisé.
Le sol utilisé dans notre expérimentation a une texture sableuse avec 51,15% de sable fin, 31,04% de sable grossier et 17,81% de limon et argile. Les résultats d'analyses du sol sont présentés dans le tableau (06).
Tableau 06: Résultats d'analyses du sol initial (avant expérimentation)
|
Caractéristiques du sol |
Valeurs |
||
|
Sable grossier (%) |
31,04 |
||
|
Sable fin (%) |
51,15 |
||
|
Granulométrie |
Limon grossier (%) |
12,71 |
|
|
Limon fin (%) |
3,10 |
||
|
Argile (%) |
2,00 |
||
|
pHeau (1/2,5) |
8,72 |
||
|
Calcaire total (%) |
0,75 |
||
|
CE à 25°C (1/5) (dS/m) |
4,30 |
||
|
M.O (%) |
0,30 |
||
|
CO (%) |
0,17 |
||
|
Azote |
Total (%) |
0,02 |
|
|
Assimilable ppm |
21,00 |
||
|
C/N |
8,50 |
||
|
Complexe |
Na+ |
1,38 |
|
|
adsorbant |
K+ |
0,39 |
|
|
méq/100 g du sol |
Ca++ |
4,66 |
|
|
Mg++ |
1,03 |
||
|
C.E.C (méq/100 g de sol) |
7, 85 |
||
|
Capacité de rétention en eau (%) |
29,96 |
||
Les résultats d'analyses nous ont permis de constater que notre sol est très alcalin, non calcaire et salé. Il est très pauvre en matière organique et en azote. Le rapport C/N est faible. La capacité d'échange cationique de ce sol est assez faible (7, 85méq/ 100g de terre).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
CHAPITRE II: Résultats et
interprétations d'analyse du sol
durant
l'expérimentation
II-1- Le pH
Dans les régions arides, les sols sont généralement alcalins (7,5< pH <8,5) (DAOUD et HALITIM, 1994).
Les résultats de mesure du pH, dans les sols à différents traitements sont présentés dans le tableau (07).
Tableau 07: Valeurs du pH dans les différents traitements
|
Traitements |
Prélèvements |
Moyennes |
Analyses |
|||||||||
|
P1 |
P2 |
P3 |
P4 |
P5 |
P6 |
P7 |
P8 |
|||||
|
MOB |
D0 |
8,64 |
8,21 |
8,18 |
8,20 |
8,27 |
8,37 |
8,39 |
8,36 |
8,33 |
8,14 |
Effet M.O S Effet D T.H.S Effet P T.H.S Interaction M.O*D H.S Interaction M.O*P T.H.S Interaction D*P T.H.S |
|
D1 |
8,65 |
8,05 |
8,04 |
8,10 |
8,14 |
8,16 |
8,12 |
8,22 |
8,20 |
|||
|
D2 |
8,40 |
7,99 |
7,96 |
7,99 |
8,03 |
8,02 |
8,06 |
8,13 |
8,07 |
|||
|
D3 |
8,37 |
7,75 |
7,76 |
7,84 |
7,95 |
7,88 |
7,98 |
8,05 |
7,95 |
|||
|
MOO |
D0 |
8,84 |
8,15 |
8,20 |
8,31 |
8,33 |
8,38 |
8,38 |
8,38 |
8,37 |
8,10 |
|
|
D1 |
8,85 |
7,96 |
7,99 |
8,07 |
8,06 |
8,05 |
8,08 |
8,14 |
8,15 |
|||
|
D2 |
8,59 |
7,85 |
7,81 |
7,78 |
7,91 |
7,93 |
8,01 |
8,01 |
7,99 |
|||
|
D3 |
8,69 |
7,85 |
7,79 |
7,76 |
7,73 |
7,73 |
7,62 |
7,89 |
7,88 |
|||
|
Moyennes |
8,63 |
7,98 |
7,97 |
8,01 |
8,05 |
8,07 |
8,09 |
8,15 |
8,12 |
Interaction M.O*D*P T.H.S |
||
C.V M.O: 0, 60% C.V D: 0, 80% C.V P: 0, 50%
A première vue, et suivant les valeurs du coefficient de variation (C.V), nous pouvons dire que notre essai pour ce paramètre est d'une grande précision. Le pH est influencé de façon significative par le type de M.O. La comparaison des moyennes a permis d'obtenir deux groupes homogènes. Celui (a)présenté par le fumier bovin (M.O.B) avec un pH moyen de 8,14 et l'autre (b) par le fumier ovin (M.O.O) avec 8,10 en moyenne (Tableau 07).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
A partir des résultats présentés (Tableau 07), nous remarquons que le pH diminue au fur et à mesure qu'on augmente la dose de la M.O, ce qui fait sortir son effet très hautement significatif sur la valeur du pH (Fig. 07).
TURIÈS et al (2000) n'ont trouvé aucune variation significative pour le pH de l'amendement organique des sols sableux.
L'interaction des deux facteurs matière organique et dose de la matière organique (M.O*Dose) présente des différences hautement significatives entre les diverses combinaisons (M.O*Dose). Les boites à moustaches "box plot" (Fig.08) représentent bien ces différences. Nous remarquons que la diminution du pH avec l'augmentation des doses des matières organiques est plus importante dans les sols amendés avec le fumier ovin. Chose expliquée par la légère acidité de la matière organique ovine (cf. Tableau 05). Les résultats obtenus montrent que le pH du sol passe de 8,33 obtenue avec la dose (D0) à 7,95 avec la dose (D3) pour les sols fertilisés avec la M.O bovine et de 8,37 avec (D0) à 7,88 avec (D3) pour les sols amendés avec la M.O ovine (Fig. 07 ). La corrélation entre pH du sol et doses des matières organiques est très bonne et significative (0,98<r<0,99). La comparaison des moyennes illustre quatre groupes homogènes (a, b, c et d) pour chaque M.O, qui sont formés respectivement par D0, D1, D2 et D3.
|
8,5 |
||||||
|
8,4 8,3 8,2 8,1 8 7,9 7,8 |
||||||
|
7,7 DO D1 D2 D3 Doses |
||||||
|
MOO MOB |
||||||
Fig.07 : Evolution du pH en fonction du type et doses
de la
matière organique

|
E.T 0,02 E.T 0,02 E.T 0,04 E.T E.T |
||||||||||||||
|
0,02 E.T |
0,03 E.T |
|||||||||||||
|
0,04 0,02 E.T |
||||||||||||||
|
0,04 |
||||||||||||||
|
D0 D1 D2 D3 D0 D1 D2 D3 |
||||||||||||||
|
M.O.B |
M.O.O |
|||||||||||||
Fig.08 : Box plot " boites à moustaches"
d'évolution du pH à
différentes doses de la
M.O
Aussi l'analyse de la variance des résultats montrent un effet très hautement significatif du facteur temps sur le pH (Fig.09) qui connait une diminution au début de la période expérimentale puis augmente à partir du quatrième prélèvement P4 (quatre semaines d'expérimentation). Le test de Newman-Keuls a révélé six groupes homogènes pour la M.O.B et quatre groupes homogènes et deux autres intermédiaires pour la M.O.O (Annexe 01).
La diminution du pH est due principalement à la libération des groupements acides de cet amendement (SCHINZER et KHAN, 1985 in CHAMAYOU et LEGROS, 1989). Selon MUSTIN (1987), le pH dépend de la concentration en ions H+ provenant de l'oxydation du carbone de la matière organique.
|
8,8 |
||||||
|
8,7 8,6 8,5 8,4 8,3 8,2 8,1 8 7,9 7,8 |
||||||
|
P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||
|
MOO MOB |
||||||
Fig.09 : Evolution du pH en fonction du temps et du
type de
matière organique
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
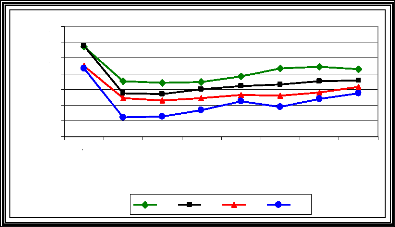
L'interaction entre les trois facteurs à savoir la matière organique, la dose de la matière organique et le temps (M.O*D*P) illustre un effet très hautement significatif sur le pH (Tableau 07, Fig.10 et Fig.11). Au premier prélèvement, les valeurs du pH sont très voisines pour toutes les doses et pour chaque type de M.O, ce qui fait sortir l'absence d'effet M.O sur le pH au début du cycle de développement de la matière organique. Le pH décroît au 2ème prélèvement dans tous les sols; choses expliquée par la libération des acides organiques des M.O. On remarque qu'en D1 et D3 la diminution est plus importante pour les sols amendés avec le fumier ovin, elle est due peut être à la différence en proportion des acides libérés.
pH
8,9
8,7
8,5
8,3
8,1
7,9
7,7
7,5
1 2 3 4 5 6 7 8
D0 D1 D2 D3
Prélèvements
Fig. 10: Evolution du pH en fonction du temps à
différentes doses de
la M.O bovine
|
8,9 8,7 8,5 8,3 8,1 7,9 7,7 |
|||||||
|
7,5 1 2 3 4 5 6 7 8 Prélèvements |
|||||||
|
D0 D1 D2 D3 |
|||||||
Fig.11 : Evolution du pH en fonction du temps à
différentes doses de
la M.O ovine
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
En ce qui concerne le mélange sol-M.O bovine, le pH va accroître à partir du 3ème prélèvement (trois semaines de l'expérimentation) alors que cette augmentation est limitée aux doses D0 et D1 pour les sols fumés avec la M.O ovine. L'accroissement est justifié par la dégradation des acides organiques. Le pH en D2 des sols fertilisés avec la M.O.O augmente à partir de la quatrième semaine (P4) d'autre part en D3, le pH est en diminution continue jusqu'au P7 (10 semaines du début de l'expérimentation) pour atteindre la valeur de 7,62. Le changement du pH entre les deux types de M.O peut être expliqué par l'acidité de la M.O.O et la différence en rapport C/N (cf. Tableau 05). Selon DUCHAUFEUR (1977), les M.O à C/N bas se décomposent vite et libèrent une forte proportion d'azote minéral (ammonification).
Les comparaisons des moyennes à différentes doses des deux matières organiques révèlent pour la dose D0 un seul groupe homogène englobe les deux matières organiques, alors que pour les deux prélèvements P1 et P4 deux groupes (a et b) ont été illustrés. Ils sont représentés respectivement par la M.OB et la M.O.O. Concernant les autres doses D1, D2 et D3, la M.O.B forme un groupe (a) et la M.O.O un groupe (b) à partir du deuxième prélèvement. En ce qui concerne la dose D3, la M.O.O forme un groupe (a) et la M.O.B un groupe (b) pour les deux prélèvements P1 et P2. À partir du 4ème prélèvement la M.O.B forme le groupe (a) et la M.O.O le groupe (b). Pour le prélèvement P3 (la dose D3) , un seul groupe (a) englobe les deux matières organiques (Annexe 01).
Conclusion
L'apport organique a diminué le pH du sol, sans pour autant le rendre neutre. La diminution paraîtnette après deux semaines du départ de l'expérimentation. La matière organique ovine a diminué le pH plus que la matière organique bovine, avec un minimum de diminution obtenu en D3 (7,62) et avec une moyenne de 7,88. Ce décroissement est du à la libération des acides organiques des matières organiques apportées.
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
La conductivité électrique permet d'obtenir une estimation de la teneur globale en sels dissous; elle ne s'applique qu'aux terres salées et aux terres à taux de fertilisation très élevé. (AUBERT, 1978).
Il est bien connu qu'une fertilisation organique contribue à la mise en valeur des sols influencés par la salinité (MONNIER, 1965, HENIN et al, 1969, HALITIM, 1973...). Ces effets dépendent de la nature et de la quantité de la matière organique utilisée.
Dans notre travail expérimental nous avons effectué un suivie de la teneur en sels dissous à l'aide de la conductivité électrique dans les sols à différentes doses de matières organiques. Les résultats sont présentés dans le tableau (08).
Tableau 08 : Valeurs de la conductivité électrique (mS/cm) dans les différents traitements
|
Traitements |
Prélèvements |
Moyennes |
Analyses |
|||||||||
|
P1 |
P2 |
P3 |
P4 |
P5 |
P6 |
P7 |
P8 |
|||||
|
M.O.B |
D0 |
4,08 |
6,22 |
6,74 |
6,84 |
6,83 |
6,85 |
7,14 |
7,45 |
6,52 |
6,47 |
Effet M.O N.S Effet D T.H.S Effet P T.H.S Interaction M.O*D T.H.S Interaction M.O*P N.S Interaction D*P T.H.S |
|
D1 |
3,76 |
6,59 |
7,35 |
7,45 |
7,53 |
7,53 |
7,62 |
7,76 |
6,95 |
|||
|
D2 |
3,8 |
5,96 |
6,38 |
6,53 |
6,84 |
7,09 |
7,8 |
7,48 |
6,49 |
|||
|
D3 |
3,29 |
4,59 |
5,61 |
6,29 |
6,55 |
6,65 |
6,69 |
7,68 |
5,92 |
|||
|
M.O.O |
D0 |
3,75 |
4,79 |
5,95 |
6,03 |
5,99 |
6,44 |
6,37 |
6,31 |
5,70 |
6,27 |
|
|
D1 |
3,35 |
5,98 |
6,32 |
6,86 |
6,82 |
7,56 |
7,81 |
7,83 |
6,57 |
|||
|
D2 |
3,66 |
6,62 |
7,39 |
7,66 |
7,75 |
7,73 |
7,72 |
7,41 |
6,99 |
|||
|
D3 |
3,30 |
4,59 |
5,79 |
6,27 |
6,57 |
6,68 |
6,74 |
6,73 |
5,83 |
|||
|
Moyennes |
3,62 |
5,67 |
6,44 |
6,74 |
6,86 |
7,07 |
7,24 |
7,33 |
6,37 |
Interaction M.O*D*P S |
||
C.V M.O: 18, 90% C.V D: 8, 00% C.V P: 6, 10%
L'analyse de la variance montre l'effet non significatif du type de matière organique sur la conductivité électrique avec une moyenne de 6,47 et 6,27mS/cm respectivement pour la
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
matière organique bovine et ovine (Tableau 08). Le coefficient de variation est de (18,90%) ce qui masquerait probablement les différences éventuelles entre les différents traitements.
La conductivité électrique varie de façon très hautement significative avec les doses de la matière organique. Elle augmente avec l'apport de la matière organique, par ailleurs elle décroît avec l'augmentation des doses de la matière organique pour atteindre 5,83 et 5.92 mS/cm en (D3) respectivement dans les sols ayant subit une fertilisation avec la matière organique ovine et bovine (Fig.12). MALLOUHI (1979) a indiqué que dans les sols salés, la matière organique fraîche améliore la stabilité structurale et par conséquence facilite le lessivage des sels. Ce qui confirme les résultats de notre essai.
Le test de Newman-Keuls a révélé, pour l'interaction M.O*Dose, trois groupes homogènes (a, b et c). Les groupes (a et b) sont représentés respectivement par (D2) (6,99 mS/cm) et (D1) (6,57 mS/cm). C regroupe les doses (D3) avec (5,83 mS/cm) et (D0) avec (5,70 mS/cm) concernant la fertilisation avec la matière organique ovine. En ce qui concerne les sols amendés avec la matière organique bovine, le groupe (b) associe (D0) (6,52mS/cm) et (D2) (6,49mS/cm) et les groupes (a et c) sont formés successivement par les doses (D1) (6,95mS/cm) et (D3) (5,92mS/cm) (Annexe 02).
|
7,5 |
||||||
|
7 |
||||||
|
4,5 D0 D1 D2 D3 Doses de matière organique |
||||||
|
MOB MOO |
||||||
Fig.12 : Evolution de la C.E (mS/cm) en fonction du
type et doses
de la matière organique
Les résultats de la conductivité électrique, représentés sous forme de boites à moustaches (Fig.13), montrent l'effet très hautement significatif de l'interaction des deux
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
facteurs à savoir la matière organique et la dose de la matière organique (M.O*Dose). La conductivité électrique accroît avec l'apport de la matière organique. Elle est plus élevée dans les sols amendés avec le fumier bovin (6,95mS/cm avec la dose D1). Par contre elle est en diminution continue et ceci en fonction des doses de la matière organique. En ce qui concerne la fertilisation avec le fumier ovin, le décroissement de la conductivité électrique n'est enregistré qu'avec la dose (D3). Ces différences résultent aux effets des matières organiques sur la structure du sol, leurs salinités (cf. Tableau 05) et leurs degrés de décomposition.
|
E.T |
||||||||||||||||||||
|
E.T |
||||||||||||||||||||
|
E.T 0,26 0,37 E.T |
||||||||||||||||||||
|
E.T |
||||||||||||||||||||
|
E.T 0,37 E.T 0,35 E.T 0,27 0,21 0,31 |
||||||||||||||||||||
|
D0 D1 |
D2 D D |
D1 D2 D3 |
||||||||||||||||||
|
M.O.B |
M.O.O |
|||||||||||||||||||
Fig.13 : Box plot " boites à moustaches"
d'évolution de la C.E
(mS/cm) à différentes doses de la
M.O
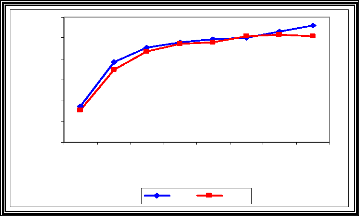
La figure (14) montre que la conductivité électrique est en augmentation incessante pendant toute la période expérimentale, ce qui fait sortir l'effet très hautement significatif du facteur temps sur ce paramètre (tableau 08). Une bonne corrélation existe entre la conductivité électrique et le facteur temps (r (M.O.O)=0.83, r (M.O.B)=0,85). Cette croissance de la conductivité électrique est la conséquence de la minéralisation des matières organiques apportées.
Le test de Newman-Keuls a révélé en fonction du temps cinq groupes homogènes et deux autres intermédiaires pour les deux types des matières organiques (Annexe 02).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
P1 P2 P3 P4 P5 P6 P7 P8
8
7
6
CE (mS/cm)
5
4
3
2
Prélèvements
MOB MOO
Fig.14 : Evolution de la C.E (mS/cm) en fonction du
temps et du
type de matière organique
A l'égard des résultats (Tableau 08, Fig.15 et 16), l'interaction des trois facteurs à savoir la matière organique, la dose de la matière organique et le temps (M.O*D*P) agit de façon significative sur la conductivité électrique. Une bonne corrélation positive présente entre la conductivité électrique et les différentes doses de la matière organique et le temps (0,68<r<0,93). Nous remarquons aussi que l'augmentation de la conductivité électrique est importante entre le premier et le deuxième prélèvement ceci s'explique par une minéralisation rapide de la matière organique. TOUTAIN (1979) a indiqué que dans les sols sahariens, la matière organique étant détruite rapidement en climat chaud sous irrigation. A partir de la deuxième semaine, le taux de l'accroissement de la conductivité électrique du sol devient faible.
La comparaison des moyennes de l'interaction des trois facteurs M.O*D*P a révélé un seul groupe homogène qui associe les deux fumiers, à différentes doses, à travers les prélèvements à l'exception de quelques cas où nous avons deux groupes homogènes, comme c'est le cas en (D2) dans le troisième et le quatrième prélèvements. Le fumier ovin forme un groupe (a) et le fumier bovin un autre groupe (b) (Annexe02).
Conclusion
La matière organique a augmenté la teneur en sels dissous. Elle peut atteindre 6,99mS/cm en D2 pour les sols amendés avec la matière organique ovine. Cet accroissement provient de la minéralisation de ces matières organiques. La conductivité électrique diminue
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
avec l'augmentation de la dose. Ceci s'expliquent par l'effet des matières organiques sur la structure qui se traduit par la facilité du lessivage des sels.
|
8,5 |
||||||
|
7,5 6,5 5,5 4,5 3,5 2,5 |
||||||
|
1 2 3 4 5 6 7 8 Prélèvements |
||||||
|
D0 D1 D2 D3 |
||||||
Fig.15 : Evolution de la C.E (mS/cm) en fonction du
temps à différentes doses
de la M.O bovine
|
8,5 |
||||
|
7,5 6,5 5,5 4,5 3,5 2,5 |
||||
|
1 2 3 4 5 6 7 8 Prélèvements |
||||
|
D0 D1 D2 D3 |
||||
Fig.16 : Evolution de la C.E (mS/cm) en fonction du
temps à différentes doses
de la M.O ovine
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
II-3- La capacité de rétention en eau (humidité équivalente) (H.É)
L'eau joue un rôle considérable; elle est d' abord un facteur fondamental de la genèse du sol et son évolution et elle est considérée comme un vecteur des éléments nutritifs et un produit indispensable à la vie des plantes.
La capacité de rétention en eau est la quantité d'eau capable d'être conservée par un sol en place (GAUCHER, 1968). DUCHAUFFOUR (1965) a précisé que la capacité au champ est une valeur approchée par excès de la capacité de rétention.
Le terme humidité équivalente désigne l'humidité mesurée au laboratoire sur l'échantillon égale à l'humidité du sol à la capacité de rétention au champ (RICHARD et WADLEI GH, 1952 in JOURDAN, 1983).
Dans notre cas, nous avons étudié l'humidité à la capacité de rétention au champ (humidité équivalente) du sol à différents types et à différentes doses de matières organiques dans le temps (différents prélèvements) dont les mesures sont faites sur l'échantillon au
laboratoire par la méthode de Bouyoucos. Les résultats sont présentés dans le tableau (09). Tableau 09: Valeurs d'humidité équivalente en (%) dans les différents traitements.
|
Traitements |
Prélèvements |
Moyennes |
Analyses |
|||||||||
|
P1 |
P2 |
P3 |
P4 |
P5 |
P6 |
P7 |
P8 |
|||||
|
M.O.B |
D0 |
29,80 |
29,49 |
29,37 |
28,98 |
28,87 |
27,7 |
27,56 |
27,4 |
28,64 |
32,25 |
Effet M.O T.H.S Effet D T.H.S Effet P T.H.S Interaction M.O*D T.H.S Interaction M.O*P T.H.S Interaction D*P T.H.S |
|
D1 |
31,18 |
31,59 |
33,32 |
31,41 |
30,75 |
30,38 |
30,56 |
30,59 |
31,22 |
|||
|
D2 |
32,87 |
33,18 |
33,71 |
33,99 |
34,21 |
34,50 |
35,46 |
35,59 |
33,18 |
|||
|
D3 |
33,59 |
35,58 |
36,15 |
36,24 |
36,37 |
36,56 |
36,62 |
36,69 |
35,98 |
|||
|
M.O.O |
D0 |
30,08 |
29,96 |
29,40 |
29,04 |
28,65 |
28,54 |
28,38 |
27,7 |
28,96 |
34,63 |
|
|
D1 |
33,28 |
33,64 |
34,18 |
34,22 |
34,40 |
34,63 |
35,02 |
35,69 |
34,36 |
|||
|
D2 |
34,98 |
35,22 |
35,42 |
35,55 |
35,58 |
35,73 |
36,24 |
37,37 |
35,76 |
|||
|
D3 |
38,69 |
39,08 |
39,29 |
39,56 |
39,77 |
39,89 |
39,65 |
39,66 |
39,45 |
|||
|
Moyennes |
32,05 |
33,46 |
33,82 |
33,62 |
33,57 |
33,49 |
33,68 |
33,84 |
33,44 |
Interaction M.O*D*P T.H.S |
||
C.V M.O : 1,10% C.V Dose : 2,40% C.V P : 1,30%
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
Le type de matière organique apportée agit de façon très hautement significative sur l'humidité à la capacité de la rétention au champ de sol. Le coefficient de variation est faible, il est de 1,10 %. L'analyse de variance a révélé deux groupes homogènes (a et b) représentés respectivement par la matière organique ovine avec une humidité équivalente de 34,63% et la matière organique bovine avec 32,25% d'humidité en moyenne (Tableau 09).
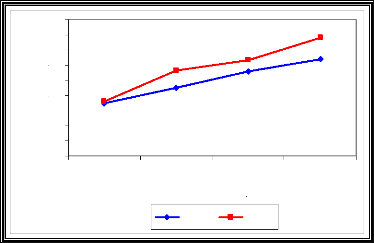
L'humidité équivalente est influencée d'une manière très hautement significative par les doses des matières organiques apportées (Tableau 09). Les valeurs d'humidité vont dans le même sens que l'accroissement des doses des deux matières organiques (Fig.17). Une forte relation positive existe entre la dose de matière organique et la capacité de rétention en eau (r= 0,99). Ce qui fait sortir l'effet très hautement significatif de la combinaison M.O*Dose sur l'humidité équivalente. Une forte corrélation existe aussi entre cette dernière et la dose de matière organique (r (M.O.O)=0.98, r (M.O.B)=0,99). L'humidité passe ainsi de 28,64% et 28,96% en (D0) à 35,98% et 39,45% respectivement pour les sols engraissés avec le fumier bovin et ovin (Fig.17, Fig.18). Les différences enregistrées entre les deux fertilisations peuvent être expliquées par l'écart de la composition en cellulose entre les deux matières organiques (cf. Tableau 05). Ce dernier à caractère hydrophile qui se traduit par un gonflement affectant un épaississement pouvant être de l'ordre de 20-30% (PREVOT, 1970).
D0 D1 D2 D3
42,5
40
37,5
35
HE (%)
32,5
30
27,5
25
22,5
20
Doses de matières organiques
MOB MOO
Fig.17 : Evolution de l'H.É (%) en fonction du
type et doses de la
matière organique
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
||||||||||||||
|
E.T |
||||||||||||||
|
0,21 |
||||||||||||||
|
E.T |
||||||||||||||
|
E.T 0,24 E.T |
||||||||||||||
|
0,31 0,48 E.T |
E.T |
|||||||||||||
|
E.T 0,37 0,35 0,37 E.T 0,27 |
||||||||||||||
|
D0 D1 D2 D3 D0 D1 D2 D3 |
||||||||||||||
|
M.O.B |
M.O.O |
|||||||||||||
Fig.18: Box plot " boites à moustaches"
d'évolution de l'H.É (%) à
différentes doses de
la M.O
L'analyse statistique de l'interaction des deux facteurs à savoir la matière organique et la dose de la matière organique et grâce au test de Newman-Keuls a engendré quatre groupes homogènes (a, b, c et d) pour chaque matière organique. Ils sont formés par ordre de (D3), (D2), (D1) et (D0).
DRIDI et TOUMI (1999) ont trouvé des résultats contradictoire par rapport à nos mesures et que le fumier ne change pas de façon déterminante la réserve en eau.
Dans notre travail nous avons constaté que l'humidité à la capacité de rétention au champ du sol augmente pendant toute l'expérimentation, ce qui confirme l'effet très hautement significatif du facteur temps et l'interaction M.O*P sur l'humidité équivalente (Tableau 09). Elle diffère d'un sol à l'autre, l'humidité passe donc de 34,35 % et 31,86 % au premier prélèvement (8ème jours de l'expérimentation) à 35,11 % et 32,64 % au dernier prélèvement (87 jours de l'expérimentation) respectivement dans les sols amendés avec le fumier ovin et le fumier bovin (Fig.19). Une bonne corrélation existe entre l'humidité (matière organique ovine) et le temps (prélèvements) (r (M.O.O)=0,91, r (M.O.B)=0,48).
MONNIER et GRAS (1965) et HILLEL (1974) ont indiqué que la matière organique retient d'autant mieux l'eau qu'elle est humifiée. Selon VANGHAN et MALCOLM (1985), elle dépend de la présence des groupements fonctionnels spécialement carboxyles où les
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
molécules d'eaux entourent les atomes d'hydrogènes. Il est bien connu que le taux d'acide fulvique de la matière organique augmente de plus en plus qu'elle est humifiée et par conséquence la quantité d'eau absorbée par la matière organique augmente. Ce qui confirme nos résultats dont l'humidité augmente pendant le cycle d'évolution des matières organiques apportées. L'accroissement de la capacité de rétention en eau du sol par rapport aux témoins au début de l'expérimentation est expliqué par l'affinité des composantes de matières organiques (cellulose et acide fulvique) à l'eau (cf. Tableau 05). Hénin et al (1970) ont indiqué que l'incorporation de la matière organique dans le sol, augmente la quantité d'eau retenue et la capacité s'accroît jusqu'à 30%.
L'analyse de la variance de l'interaction M.O*P a révélé trois groupes homogènes (a, b et c) pour chaque amendement. Le groupe (a) est représenté par P3 (22ème jours de l'expérimentation), le groupe (c) par P1 (8ème jours de l'expérimentation) et (b) par l'ensemble des prélèvements restants pour la matière organique bovine. En ce qui concerne le fumier ovin les groupes (a et c) sont formés respectivement par P8 (87 jours de l'expérimentation) et P1 (8ème jours de l'expérimentation), le troisième groupe (b) englobe l'ensemble des prélèvements de P2 (15ème jours de l'expérimentation) à P7 (70ème jours de l'expérimentation) (Annexe 03).
|
36 |
||||||
|
35 34 33 32 31 30 |
||||||
|
P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||
|
MOB MOO |
||||||
Fig.19 : Evolution de l'H.É (%) en fonction du
temps et du type de
matière organique
L'interaction M.O*D*P influe aussi de façon très hautement significative sur l'humidité équivalente. Les coefficients de variations sont de 1,10% pour la matière
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
organique, 2,40% pour les doses et 1,30% pour le facteur temps. La différence est bien distincte entre les témoins (D0) et les autres doses. A partir des résultats (Tableau 09, Fig. 20 et Fig21), nous remarquons que l'humidité diminue en (D0), chose expliquée par la dégradation de la matière organique initiale existante dans le sol de départ. La figure (20) montre un accroissement de l'humidité avec (D1) jusqu'à la 3ème semaine (22ème jours de l'expérimentation), ensuite elle décroît vers la fin de l'expérimentation (87 jours de l'expérimentation).
Une très bonne corrélation positive existe entre l'humidité à la capacité de rétention au champ des sols, la dose des matières organiques et le temps (0,80<r<0,92). Elle passe de 32,87% à 35,59% en (D2), et de 33,59% à 36,69% en (D3) pour les sols additionnés de la matière organique bovine, et de 33,28% à 35,69% en (D1), de 34,98% à 37,37% en (D2) et de 38,69% à 39,66% en (D3) concernant les sols amendés avec la matière organique ovine. Le plus important accroissement est enregistré en (D1) de la fertilisation avec le fumier ovin (r=0,92). Par contre DEMBEBE et al (1999) ont montré que l'apport du fumier avec des doses qui varient entre 2,5 et 10 t/ha entraîne un léger accroissement de la rétention en eau du sol sableux. DUTHIL (1973) a indiqué que la capacité du sol pour l'eau est liée à sa teneur en matière organique, en raison du caractère hydrophile extraîmement accusé des colloïdes qui la compose.
L'analyse de la variance de l'interaction des trois facteurs : la matière organique, la dose de la matière organique et le temps a révélé, en général, deux groupes homogènes celui de la matière organique ovine (a) et celui de la matière organique bovine (b) (Annexe 03).
|
41 |
||||||
|
39 37 35 33 29 |
||||||
|
31 |
||||||
|
1 2 3 4 5 6 7 8 Prélèvements |
||||||
|
D0 D1 D2 D3 |
||||||
Fig.20 : Evolution de l'H.É (%) en fonction du temps à différentes doses de la 47
M.O bovine
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
||||||||
|
41 |
||||||||
|
39 31 29 27 25 |
||||||||
|
33 |
||||||||
|
1 2 3 4 5 6 7 8 Prélèvements |
||||||||
|
D0 D1 D2 D3 |
||||||||
Fig.21 : Evolution de l'H.É (%) en fonction du
temps à différentes doses
de la M.O ovine
Conclusion
La capacité de rétention en eau du sol est améliorée par l'amendement organique avec un maximum obtenu pour les sols amendés avec le fumier ovin en (D3), avec 39,45%. La matière organique ovine améliore mieux la rétention en eau que la matière organique bovine. Cette amélioration provienne du caractère hydrophile des matières organiques.
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
La capacité d'échange cationique exprime l'aptitude d'un matériau à retenir des cations sous forme échangeable. C'est une propriété des sols à la fois utile et intéressante (CALVET, 2003).
D'après BOCKMAN et al (1990), certains sols (particulièrement sableux légers), ont une faible capacité d'échange en cations. L'application de la matière organique à ce type de sol contribue donc à l'augmentation de la capacité d'échange cationique de ces terres (CHARREAU, 1975).
Les résultats de la capacité d'échange cationique obtenus dans notre travail sont présentés dans le tableau (10).
Tableau 10 : Valeurs de la capacité d'échange cationique (méq/100g de sol) dans les différents traitements
|
Traitements |
Prélèvements |
Moyennes |
Analyses |
|||||||||
|
P1 |
P2 |
P3 |
P4 |
P5 |
P6 |
P7 |
P8 |
|||||
|
M.O.B |
D0 |
7,67 |
7,52 |
7,35 |
7,18 |
6,99 |
6,90 |
6,25 |
5,17 |
6,88 |
10,05 |
Effet M.O T.H.S Effet D T.H.S Effet P T.H.S Interaction M.O*D T.H.S Interaction M.O*P T.H.S Interaction D*P T.H.S |
|
D1 |
7,92 |
9,00 |
11,58 |
12,58 |
10,67 |
8,50 |
8,02 |
6,42 |
9,34 |
|||
|
D2 |
10,5 |
11,75 |
12,75 |
13,67 |
12,65 |
12,17 |
10,83 |
6,48 |
11,35 |
|||
|
D3 |
12,67 |
13,42 |
14,75 |
15,83 |
13,25 |
12,58 |
11,50 |
7,17 |
12,65 |
|||
|
M.O.O |
D0 |
7,75 |
7,70 |
7,65 |
7,60 |
7,42 |
7,23 |
6,75 |
5,50 |
7,20 |
11,37 |
|
|
D1 |
8,58 |
8,83 |
9,17 |
9,73 |
10,00 |
14,00 |
12,75 |
7,17 |
10,03 |
|||
|
D2 |
12,58 |
13,03 |
14,00 |
15,25 |
16,75 |
15,00 |
13,00 |
8,66 |
13,54 |
|||
|
D3 |
13,39 |
14,00 |
15,00 |
15,53 |
18,12 |
17,92 |
14,33 |
9,33 |
14,70 |
|||
|
Moyennes |
10,12 |
10,65 |
11,53 |
12,17 |
11,98 |
11,79 |
10,43 |
6,99 |
10,71 |
Interaction M.O*D*P T.H.S |
||
C.V M.O: 1, 10 % C.V D: 8, 90% C.V P: 5, 80%
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
La capacité d'échange cationique présente une différence très hautement significative avec le type de matière organique apportée. La comparaison des moyennes a permis de distinguer deux groupes homogènes (a et b), le premier groupe (a) représenté par la matière organique ovine avec 11,37 méq/100g de sol et l'autre (b) par la matière organique bovine avec 10,05 méq/100g de sol dont le coefficient de variation est de 1,10% (Tableau 10).
D'après les analyses statistiques, le facteur dose a aussi un effet très hautement significatif sur la capacité d'échange cationique du sol (Tableau 10), ainsi que l'interaction M.O*Dose. La capacité d'échange cationique augmente, d'après les résultats obtenus, au fur et à mesure qu'on augmente la dose de la matière organique (Fig.22). Une bonne corrélation existe entre la dose de la matière organique et la capacité d'échange cationique du sol (r= 0,98). Celle-ci passe de 6,88 méq/100g de sol en (D0) à 12,65 méq/100g de sol en (D3) pour le mélange (sol-M.O bovine) et de 7,2 méq/100g de sol en (D0) à 14,70 méq/100g de sol en (D3) pour la fertilisation avec la matière organique ovine, soit une augmentation de l'ordre de 100 % pour les deux types de matières organiques apportées.
|
16 |
||||||
|
14 12 10 8 6 4 2 0 :C (meq/100g de sol) DIV 40)0301V4C |
||||||
|
D0 D1 D2 D3 Doses de matières organiques |
||||||
|
MOB MOO |
||||||
Fig.22 : Evolution de la C.E.C (méq/100g de sol)
en fonction du
type et doses de la matière organique
Nos résultats confirment ceux trouvés par TOURIES et al (2000) qui ont indiqué que la fertilisation organique conduit à une augmentation de la capacité d'échange cationique (cas des sols sableux).
L'augmentation de la capacité d'échange cationique de la matière organique est due à l'existence des groupements carboxyles (-COOH) (CHARREAU, 1975 et BAIZE, 2000).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
L'analyse statistique montre grâce au test de Newman-keuls l'existence de quatre groupes homogènes (a, b, c et d) par l'application des doses des deux types de matières organiques. Ils sont représentés respectivement par D3, D2, D1 et D0. La figure (23) montre que les deux fumiers ont contribué dans l'augmentation de la capacité d'échange cationique du sol. Mais cette contribution était relativement faible pour la fertilisation avec la matière organique bovine, soit 12,65 méq/100g de sol en (D3) contre 13,54 méq/100g de sol en (D2) et 14,70 méq/100g de sol en (D3) pour le deuxième type d'amendement.
|
E.T 0,64 E.T E.T 0,78 E.T 0,33 E.T |
||||||||||||||||||
|
E.T 0,46 0,33 |
||||||||||||||||||
|
0,55 |
||||||||||||||||||
|
E.T 0,25 |
||||||||||||||||||
|
E.T |
||||||||||||||||||
|
D0 D1 D2 D3 D0 D1 D2 D3 |
||||||||||||||||||
|
M.O.B |
M.O.O |
|||||||||||||||||
Fig.23 : Box plot " boites à moustaches"
d'évolution de la C.E.C
(méq/100g de sol) à
différentes doses de la M.O
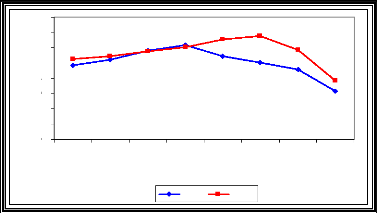
La capacité d'échange cationique présente des différences très hautement significatives dans le temps (Tableau 10). Elle est influencée de façon très hautement significative par l'interaction des deux facteurs qui sont la matière organique et le temps (M.O*P). Concernant la fertilisation par le fumier ovin, elle accroît au début de l'essai de 10,57méq/100g de sol en P1 (une semaine de l'expérimentation) à 13,54 méq/100g de sol en (P6) (après deux mois de l'expérimentation) ensuite elle diminue à 7,67 méq/100g de sol en (P8) (après trois mois de l'expérimentation). En ce qui concerne le fumier bovin, la capacité d'échange cationique passe de 9,69 méq/100g de sol en (P1) à 12,32 méq/100g de sol en (P4) (après un mois de l'expérimentation) puis elle diminue à 6,31méq/100g de sol en (P8) (Fig.24). L'analyse de la variance a illustré quatre groupes homogènes pour l'amendement ovin, six groupes homogènes et deux autres intermédiaires pour le fumier bovin (Annexe 04).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
P1 P2 P3 P4 P5 P6 P7 P8
16
14
CEC (meq/100g de sol)
12
10
8
6
4
2
0
Prélèvements
MOB MOO
Fig.24 : Evolution de la C.E.C (méq/100g de sol)
en fonction du
temps et du type de matière organique
L'effet de l'interaction des trois facteurs à savoir, la matière organique, la dose de matières organiques et le temps (M.O*D*P) sur la capacité d'échange cationique des sols parait très hautement significatif. Les figures (25 et 26) montrent qu'en (D0) (sans apport de matière organique), la capacité d'échange cationique est en diminution continue pendant toute la période d'essai. Ceci s'explique par la minéralisation continue de la matière organique du sol initial. Selon MUSTIN (1987), plus le sol est riche en matière organique stable plus sa capacité d'échange est élevée. Tant que la matière organique de notre sol est mature, elle se dégrade en décroissant la capacité d'échange du sol. La différence entre les deux amendements est non significative pour les témoins.
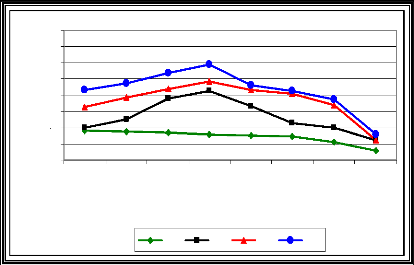
A partir des résultats présentés dans la figure (25), la capacité d'échange cationique accroît pour les doses (D1, D2 et D3) jusqu'au quatrième prélèvement (P4). Elle passe respectivement de 7,92, 10,5 et 12,67méq/100g de sol à 12,58, 13,67 et 15,83méq/100g de sol puis elle diminue respectivement pour les mêmes doses à 6,42, 6,48 et 7,17 méq/100g de sol à la fin de l'essai (après trois mois de l'expérimentation). La figure (26) qui concerne la matière organique ovine montre que pour les doses (D2 et D3), la capacité d'échange cationique passe de 12,58 et 13,39 méq/100g de sol au premier prélèvement à 16,75 et 18,12méq/100g de sol en (P5) ensuite elle décroît à 8,66 et 9,33méq/100g de sol pour P8 respectivement en D2 et D3. La valeur maximale est enregistrée en (D3) au cinquième prélèvement avec 18,12méq/100g de sol. Le fumier en cours d'humification comme toute les autres sources de
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
la matière organique (DELAS, 1971) a augmenté sensiblement la capacité d'échange cationique des sols. Selon BAIZE (2000), la capacité d'échange cationique augmente avec le degré d'humification. Elle présente une grande variation avec le mode d'humification de la matière organique (BONNEAU et COLL, 1968 in MUSTIN, 1987). Ce qui peut expliquer les différences entre les deux types de matières organiques utilisées.
TURIÈS et al (2000) ont montré pour ce type de sol (sableux) une relation étroite entre la teneur en carbone et la capacité d'échange cationique. Donc nous pouvons expliquer la diminution de la capacité d'échange cationique par le décroissement de carbone organique (matière organique) du sol par la minéralisation. TOUTAIN (1979) a indiqué que dans les sols sahariens, la matière organique est détruite rapidement en climat chaud sous irrigation.
La comparaison des moyennes de la capacité d'échange cationique pour l'interaction des trois facteurs (M.O*D*P) a révélé en (D0) un seul groupe homogène (a) qui englobe les deux types de matières organiques pendant la période expérimentale. Pour la dose (D1), en (P1, P2 P5 et P8) un seul groupe homogène (a) est montré, deux autres (a et b) en P6 et P7 sont présentés, par ordre, pour la matière organique ovine et bovine. Pour les prélèvements P3 et P4, la matière organique bovine forme un groupe (a) et l'autre (ovine) un groupe (b). En ce qui concerne les doses D2 et D3 la matière organique ovine présente un premier groupe (a) et la matière organique bovine un deuxième groupe (b) à l'exception de P1, P2, P3 et P4 en (D3) où un seul groupe est illustré (Annexe 04).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
CEC (meq/100g de sol)
20
18
16
14
12
10
4
6
8
1 2 3 4 5 6 7 8
D0 D1 D2 D3
Prélèvements
Fig. 25: Evolution de la C.E.C (méq/100g de sol)
en fonction du temps à
différentes doses de la M.O
bovine
|
20 |
||||||
|
18 16 14 12 10 8 6 4 CEC (meq/100g de sol) is -P |
||||||
|
1 2 3 4 5 6 7 8 Prélèvements |
||||||
|
D0 D1 D2 D3 |
||||||
Fig.26 : Evolution de la C.E.C (méq/100g de sol)
en fonction du temps à
différentes doses de la M.O
ovine
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
Conclusion
Les résultats de la capacité d'échange cationique montrent que l'apport organique améliore de façon très hautement significative la capacité d'échange cationique en libérant des composés organiques générateurs d'éléctronégativité et permettant de fixer les cations. L'augmentation parait nette dans les sols ayant subis une fertilisation avec la matière organique ovine. On observe un décroissement de la capacité d'échange cationique à partir du cinquième prélèvement (sixième semaine de l'expérimentation) à cause de la dégradation de la matière organique et par conséquence un manque de cites électronégatives oü se fixent les cations.
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
Le complexe colloïdal du sol a la propriété d'absorber des ions, notamment des éléments minéraux indispensables à la nutrition des végétaux. Ces éléments sont remplaçables par d'autres au niveau du complexe absorbant; on dit qu'ils sont échangeables (AUBERT, 1978).
II-5-1- Le calcium
Les résultats du dosage du calcium échangeable sont présentés dans le tableau (11).
Tableau 11 : Valeurs du calcium échangeable (méq/100g de sol) dans les différents traitements
|
Traitements |
Prélèvements |
Moyennes |
Analyses |
|||||||||
|
P1 |
P2 |
P3 |
P4 |
P5 |
P6 |
P7 |
P8 |
|||||
|
M.O.B |
D0 |
4,12 |
4,12 |
4,00 |
3,96 |
3,83 |
3,82 |
3,40 |
2,77 |
3,75 |
6,37 |
Effet M.O T.H.S Effet D T.H.S Effet P T.H.S Interaction M.O*D H.S Interaction M.O*P T.H.S Interaction D*P T.H.S |
|
D1 |
4,35 |
5,07 |
7,57 |
8,52 |
7,02 |
5,01 |
4,65 |
3,53 |
5,71 |
|||
|
D2 |
6,53 |
7,47 |
8,59 |
9,34 |
8,79 |
8,56 |
7,51 |
3,48 |
7,54 |
|||
|
D3 |
8,25 |
8,76 |
10,25 |
11,02 |
9,26 |
8,75 |
7,59 |
4,07 |
8,49 |
|||
|
M.O.O |
D0 |
4,20 |
4,18 |
4,40 |
4,13 |
4,10 |
4,00 |
3,94 |
3,10 |
3,97 |
7,38 |
|
|
D1 |
4,50 |
4,58 |
4,97 |
5,38 |
5,67 |
9,90 |
9,10 |
4,30 |
6,05 |
|||
|
D2 |
8,30 |
8,35 |
9,35 |
10,62 |
12,20 |
10,50 |
9,18 |
5,49 |
9,25 |
|||
|
D3 |
9,00 |
9,25 |
10,25 |
10,72 |
13,17 |
13,18 |
10,30 |
6,00 |
10,18 |
|||
|
Moyennes |
6,15 |
6,47 |
7,39 |
7,85 |
8,02 |
7,94 |
6,96 |
4,09 |
6,88 |
Interaction M.O*D*PT .H.S |
||
C.V M.O: 2, 10 % C.V D: 14, 10% C.V P: 8, 80%
L'analyse de la variance a révélé un effet très hautement significatif du type de matières organiques sur le taux de calcium échangeable. La matière organique ovine améliore mieux la teneur en calcium échangeable que la matière organique bovine avec une moyenne respectivement de 7,38 méq Ca++/100g de sol contre 6,37 méq Ca++/100g de sol pour le fumier bovin (Tableau 11). Deux groupes homogènes ont été illustrés, celui de la matière organique ovine (a) et celui de la matière organique bovine (b).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
Le calcium est influencé par l'apport organique à différents traitements ainsi que l'interaction M.O*Dose de façon hautement significative. Le calcium augmente avec l'accroissement de la dose de la matière organique apportée (Fig.27 et 28). Le taux de calcium échangeable passe de 3,75 à 8,49 méq Ca++/100g de sol et de 3,97 à 10,18 méq Ca++/100g de sol en moyenne quand la dose croit de (D0) à (D3) successivement pour le fumier bovin et ovin. Ce résultat est dû à la quantité de matière apportée. Une forte corrélation existe entre le calcium échangeable et la dose de la matière organique (r=0,98).
Le test de Newman-keuls a montré quatre groupes homogènes (a, b, c et d) représentés respectivement par D3, D2, D1 et D0 pour l'interaction M.O*Dose.
|
12 |
||||
|
10 8 6 4 2 0 Ca++ (meo/100g de sol) D I\ ) 4 0) OD 0 IN |
||||
|
D0 D1 D2 D3 Doses de matières organiques |
||||
|
MOB MOO |
||||
Fig.27 : Evolution du Ca++
échangeable (méq/100g de sol) en fonction
du type et doses de
la matière organique
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation
|
E.T 0 59 E.T E.T 0,75 0,46 E.T |
||||||||||||||||||
|
E.T E.T 0,33 |
||||||||||||||||||
|
0,41 |
||||||||||||||||||
|
0,54 |
||||||||||||||||||
|
E.T 0,21 |
||||||||||||||||||
|
E.T 0,20 |
||||||||||||||||||
|
D0 D1 D2 D3 D0 D1 D2 D3 |
||||||||||||||||||
|
M.O.B |
M.O.O |
|||||||||||||||||
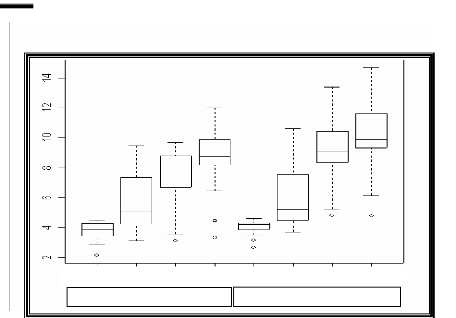
Fig.28 : Box plot " boites à moustaches"
d'évolution du Ca++
échangeable (méq/100g de
sol) du sol à différentes doses de la M.O
Pour l'interaction M.O*P, l'effet est très hautement significatif. Le taux de calcium échangeable augmente jusqu'au quatrième prélèvement pour atteindre 8,21 méq Ca++/100g de sol ensuite il diminue à 3,47 méq Ca++/100g de sol au dernier prélèvement concernant la matière organique bovine. Le calcium échangeable accroît continuellement jusqu'à 9,39 méq Ca++/100g de sol au sixième prélèvement puis il décroît à 4,72 méq Ca++/100g de sol à la fin de l'essai pour les sols engraissés avec le fumier ovin (Fig.29).
Prélèvements
Ca (m éq/
MOB MOO

|
10 9 8 7 6 5 4 3 2 1 0 |
|
|
P1 P2 P3 P4 P5 P6 P7 P8 |
Ca++ (meq/100g de sol)
Fig.29 : Evolution du Ca++
échangeable (méq/100g de sol) en fonction du
temps et du type
de matière organique
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
L'analyse de la variance de l'interaction des deux facteurs à savoir la matière organique et le facteur temps a engendré cinq groupes homogènes (a, b, c, d et e) pour la matière organique bovine. Ils sont formés respectivement par P4, P3 et P5, P6, P1 et P7, et P8 et un groupe intermédiaire (cd) présenté par P2. Par ailleurs, six groupes homogènes (a, b, c, d, e et f) sont révélés pour la matière organique ovine. Ils sont présentés successivement par P6, P5, P7, P3, P2 et P1, et P8, un autre groupe intermédiaire (cd) est présenté par P4 (Annexe05).
La teneur en calcium présente des différences très hautement significatives par la combinaison M.O*D*P. A partir des résultats présentés dans le tableau (11) et figures (30 et 31), le calcium échangeable a connu une diminution en (D0) en fonction du temps. Nous avons trouvé précédemment que la capacité d'échange cationique décroît dans les témoins et par conséquence le calcium échangeable décroît.
La figure (30) montre que la teneur en calcium augmente respectivement de 4,35, 6,53 et 8,25 méq Ca++/100g de sol en D1, D2 et D3 à 8,52, 9,34 et 11,02 méq Ca++/100g de sol après quatre semaines (P4) d'expérimentation ensuite elle décroît vers la fin de l'essai à 3,53, 3,48 et 4,07 méq Ca++/100g de sol pour les mêmes doses. En revanche, le décroissement, en D1 et D3 (Fig.31), n'apparaît qu'après deux mois (P6). Le calcium échangeable passe ainsi de 9,90, 13,18méq Ca++/100g de sol à 4,30 et 6 méq Ca++/100g de sol par ordre en D1 et D3 après qu'il avait été de l'ordre de 4,5 et 9 méq Ca++/100g de sol au début du cycle (P1).
L'analyse statistique de la combinaison des trois facteurs qui sont la matière organique, la dose de la matière organique et le temps (M.O*D*P) a révélé en (D0) un seul groupe homogène (a) qui englobe les deux types de matières organiques pendant la période expérimentale. Pour la dose (D1), deux groupes homogènes sont enregistrés, la matière organique bovine forme le groupe (a) et la matière organique ovine le groupe (b) pour les trois prélèvements P3, P4 et P5. Pour les deux prélèvements P6 et P7, la matière organique bovine forme le groupe (b) et la matière organique ovine le groupe (a). Un seul groupe homogène (a)qui englobe les deux types de fumier est indiqué pour P1, P2 et P8. En ce qui concerne les doses D2 (de P1à P8) et D3 (de P5 à P8) la matière organique ovine forme un premier groupe (a) et la matière organique bovine un deuxième groupe (b). Pour les prélèvements (de P1 à P4) un seul groupe (a) est illustré en (D3) (Annexe 05).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
||||||||
|
14 |
||||||||
|
12 10 8 6 4 2 0 Ca++ (meq/100g de sol) _.. _.. _ O N.) -D. 0) 00 c) N.1 -I |
||||||||
|
P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||||
|
D0 D1 D2 D3 |
||||||||
Fig.30 : Evolution du Ca++
échangeable (méq/100g de sol) en fonction du
temps à
différentes doses de la M.O bovine
|
14 |
||||||
|
12 10 6 4 2 Ca++ (meq/100g de sol) _.. _.. _ N) -1=. CY) CO 0 IV -1 |
||||||
|
8 |
||||||
|
1 2 3 4 5 6 7 8 Prélèvements |
||||||
|
D0 D1 D2 D3 |
||||||
Fig.31 : Evolution du Ca++
échangeable (méq/100g de sol) en fonction du temps
à
différentes doses de la M.O ovine
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
II-5-2- Le magnésium (Mg++)
Les résultats du dosage du magnésium sont présentés dans le tableau (12)
Tableau 12 : Valeurs du magnésium échangeable (méq/100g de sol) dans les différents traitements
|
Traitements |
Prélèvements |
Moyennes |
Analyses |
|||||||||
|
P1 |
P2 |
P3 |
P4 |
P5 |
P6 |
P7 |
P8 |
|||||
|
M.O.B |
D0 |
1,03 |
0,96 |
0,94 |
0,91 |
0,90 |
0,88 |
0,86 |
0,76 |
0,91 |
1,09 |
Effet M.O H.S Effet D T.H.S Effet P T.H.S Interaction M.O*D H.S Interaction M.O*P T.H.S Interaction D*P T.H.S |
|
D1 |
1,13 |
1,29 |
1,32 |
1,32 |
1,05 |
0,94 |
0,94 |
0,88 |
1,11 |
|||
|
D2 |
1,29 |
1,30 |
1,32 |
1,41 |
1,08 |
0,97 |
0,94 |
0,90 |
1,15 |
|||
|
D3 |
1,31 |
1,33 |
1,35 |
1,40 |
1,16 |
1,02 |
0,99 |
0,95 |
1,19 |
|||
|
M.O.O |
D0 |
1,04 |
1,01 |
1,00 |
0,96 |
0,92 |
0,90 |
0,87 |
0,76 |
0,93 |
1,28 |
|
|
D1 |
1,37 |
1,39 |
1,42 |
1,45 |
1,46 |
1,47 |
1,15 |
0,90 |
1,33 |
|||
|
D2 |
1,41 |
1,49 |
1,52 |
1,56 |
1,51 |
1,49 |
1,18 |
0,95 |
1,39 |
|||
|
D3 |
1,50 |
1,57 |
1,58 |
1,60 |
1,61 |
1,63 |
1,26 |
1,00 |
1,47 |
|||
|
Moyennes |
1,26 |
1,29 |
1,31 |
1,33 |
1,21 |
1,16 |
1,02 |
0,89 |
1,18 |
Interaction M.O*D*P T.H.S |
||
C.V M.O: 7, 90 % C.V D: 12, 40% C.V P: 3, 40%
La teneur en magnésium échangeable présente des différences hautement significatives en fonction du type de matière organique. Cette teneur varie de 1,09 méq Mg++/100g de sol dans les sols amendés avec le fumier bovin à 1, 28 méq Mg++/100g de sol dans les sols engraissés avec le fumier ovin (Tableau 12). L'analyse statistique a engendré deux groupes homogènes (a et b) représentés successivement par la matière organique ovine et bovine.
Le taux de magnésium échangeable a été influencé de façon très hautement significative par la dose de la matière organique apportée (Tableau 12). L'influence de l'interaction M.O*Dose était hautement significative. Nous avons constaté que l'interaction a augmenté la teneur en magnésium échangeable de 0,92 méq Mg++/100g de sol en moyenne au (D0) à 1,19 et 1,47 méq Mg++/100g de sol en (D3) respectivement dans les sols engraissés
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
avec le fumier bovin et ovin (Fig.32). Le Mg++échangeable va dans le même sens qu'on accroît la dose de matières organiques apportées (Fig.33). Une très bonne corrélation positive entre le Mg++ échangeable et la dose de la matière organique était constaté (r=0,91). L'accroissement du taux de magnésium est plus remarquable pour la matière organique ovine.
|
1 ,6 |
||||||
|
1,4 1,2 1 0,8 0,6 0,4 0,2 0 Mg++ (meq/100g de sol) PP PP.." .." : ) Iv 41 0) 00 -% IV 41 C |
||||||
|
D0 D1 D2 D3 Matières organiques |
||||||
|
MOB MOO |
||||||
Fig.32 : Evolution du Mg++
échangeable (méq/100g de sol) en fonction
du type et doses de
la matière organique
|
E.T E.T 0,02 E.T E.T 0,01 E.T 0,05 0,01 |
|||||||||||||||||
|
E.T 0,06 |
|||||||||||||||||
|
0,02 |
|||||||||||||||||
|
E.T |
E.T |
||||||||||||||||
|
0,02 |
|||||||||||||||||
|
0,03 |
|||||||||||||||||
|
D0 D1 D2 D3 D0 D1 D2 |
|||||||||||||||||
|
D M.O.B |
M.O.O |
||||||||||||||||
Fig.33 : Box plot " boites à moustaches"
d'évolution du Mg++ échangeable
(méq/100g de
sol) à différentes doses de la M.O
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
Le test de Newman-keuls pour la combinaison M.O*Dose a manifesté deux groupes homogènes. Le premier groupe (a) enclave les trois niveaux de dose (D1, D2 et D3) avec respectivement 1,14, 1,15 et 1,19 méq Mg++/100g de sol, par contre le deuxième groupe (b) est représenté uniquement par le témoin (D0) avec 0,91 méq Mg++/100g de sol pour la fertilisation avec le fumier bovin. D'autre part, quatre groupes ont illustrés pour la deuxième fertilisation ; trois groupes homogènes (a, b et c) qui contiennent successivement les doses D3 (1,47 méq Mg++/100g de sol), D1 (1,33 méq Mg++/100g de sol) et D0 (0,99 méq Mg++/100g de sol) et un groupe intermédiaire (ab) représenté par la dose D2 avec 1,39 méq Mg++/100g de sol.
L'analyse de la variance a montré un effet très hautement significatif du temps sur la teneur en magnésium échangeable (Tableau 12). Ce dernier est influencé, aussi de façon très hautement significative, par l'interaction M.O*P. Cette teneur augmente de 1,19méq Mg++/100g de sol obtenu avec la matière organique bovine et 1,33 méq Mg++/100g de sol avec la matière organique ovine au premier prélèvement pour atteindre 1,26 méq Mg++/100g de sol (M.O.B) et 1,39 méq Mg++/100g de sol (M.O.O) après un mois du départ. Ensuite elle décroît pendant les deux mois restants à 0,87méq Mg++/100g de sol (M.O.B) et 0,90 méq Mg++/100g de sol (M.O.O) (Fig.34). Une relation négative entre le magnésium et le temps (r (M.O.B)= -0,88 et r (M.O.O)= -0,7) a été constatée.
Le test de Newman-keuls de l'interaction des deux facteurs étudiés à savoir la matière organique et le temps a révélé sept groupes d'évolution de magnésium pour les sols amendés avec le fumier bovin dont cinq homogènes (a, b, c, e et f) qui contiennent respectivement les prélèvements P4 (1,26 méq Mg++/100g de sol), P1 (1,19 méq Mg++/100g de sol), P5 (1,05 méq Mg++/100g de sol), P6 et P7 (0,90 et 0,93 méq Mg++/100g de sol) et P8 (0,87 méq Mg++/100g de sol), et deux groupes intermédiaires; un premier groupe (ab) formé par P3 (1,23 méq Mg++/100g de sol) et un deuxième groupe (b et c) formé par P2 (1,22 méq Mg++/100g de sol). En revanche, quatre groupes homogènes seulement ont révélé pour la fertilisation avec la matière organique ovine. Le groupe (a) englobe les cinq prélèvements P4 (1,39 méq Mg++/100g de sol), P3 (1,38 méq Mg++/100g de sol), P5 (1,38 méq Mg++/100g de sol), P6 (1,37 méq Mg++/100g de sol) et P2 (1,37 méq Mg++/100g de sol), les autres groupes (b, c et d) sont présentés successivement par P1 (1,33 méq Mg++/100g de sol), P7 (1,12 méq Mg++/100g de sol), P8 (0,90 méq Mg++/100g de sol) (Annexe 06).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
Prélèvements
MOB MOO

|
1,6 1 0,8 0,6 0,4 0,2 0 |
|
|
P1 P2 P3 P4 P5 P6 P7 P8 |
Mg++ (meq/100g de sol)
Fig.34 : Evolution du Mg++
échangeable (méq/100g de sol) en fonction du
temps et du type
de matière organique
L'interaction des trois facteurs à savoir, la matière organique, la dose de la matière organique et le temps (M.O*D*P) a aussi un effet très hautement significatif sur la teneur en magnésium échangeable (tableau 12, Fig.35 et 36). Comme c'était le cas pour le calcium, la teneur en magnésium échangeable (Fig.35 et 36) est en diminution continue en fonction du temps pour la dose (D0). Elle passe ainsi de 1,03 méq Mg++/100g de sol à 0,76 méq Mg++/100g de sol à la fin de l'essai. Le facteur M.O est non significatif par contre l'effet temps est très hautement significatif.
La figure (35) montre que le taux de magnésium croit de 1,13, 1,29 et 1,31 méq Mg++/100g de sol au premier prélèvement à 1,32, 1,41 et 1,40 méq Mg++/100g de sol après un mois de l'expérimentation (P4) respectivement avec les doses (D1, D2 et D3). Il diminue ensuite pendant les deux mois qui suit pour arriver par le même ordre à 0,88, 0,90 et 0,95méq Mg++/100g de sol au dernier prélèvement (P8). La différence n'est pas significative entre les trois doses.
La figure (36) montre l'accroissement de la teneur en magnésium jusqu'au sixième prélèvement (deux mois de l'expérimentation). Cette teneur passe de 1,37 méq Mg++/100g de sol en (P1) à 1,47 méq Mg++/100g de sol en (P6) avec la dose D1 et de 1,50 méq Mg++/100g de sol en (P1) à 1,63 méq Mg++/100g de sol en (P6) avec la dose D3. Le magnésium échangeable croit de 1,41 méq Mg++/100g de sol en (P1) à 1,56 méq Mg++/100g du sol en
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
(P4) avec la dose D2. Il décroît pour atteindre à la fin de l'expérimentation (P8) 0,90, 0,95 et 1,00 méq Mg++/100g de sol respectivement avec les doses D1, D2 et D3.
La comparaison des moyennes de l'interaction des trois facteurs étudiés (M.O*D*P) dans les différents prélèvements a révélé deux groupes homogènes (a et b) qui contiennent successivement la matière organique ovine et bovine à l'exception de P2 et P3 et P8 en D1, P8 en D2 et D3 dont un seul groupe les deux matières organiques est illustré (Annexe 06).
|
2 |
||||||
|
1,75 1,5 1,25 1 0,75 0,5 0,25 0 Mg++ (meq/100g de sol) c, c, N) P --.1 N) ...-- --.1 C) C.71 C.71 C.71 -- |
||||||
|
P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||
|
D0 D1 D2 D3 |
||||||
Fig.35 : Evolution du Mg++
échangeable (méq/100g de sol) en fonction du temps
à
différentes doses de la M.O bovine
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
|||||||
|
2 |
|||||||
|
1,75 1,5 1,25 1 0,75 0,5 0,25 0 Mg++ (meq/100g de sol) C...) C...) N.) P -.I N.) C) C.71 C71 C71 - |
|||||||
|
1 2 3 4 5 6 7 8 Prélèvements |
|||||||
|
D0 D1 D2 D3 |
|||||||
Fig.36 : Evolution du Mg++
échangeable (méq/100g de sol) en fonction du temps
à
différentes doses de la M.O ovine
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
II-5-3- Le sodium (Na+)
Les résultats de dosage du sodium échangeable sont présentés dans le tableau (13)
Tableau 13 : valeurs du sodium échangeable (méq/100g de sol) dans les différents traitements
|
Traitements |
Prélèvements |
Moyennes |
Analyses |
|||||||||
|
P1 |
P2 |
P3 |
P4 |
P5 |
P6 |
P7 |
P8 |
|||||
|
M.O.B |
D0 |
2,00 |
1,95 |
1,90 |
1,77 |
1,75 |
1,70 |
1,63 |
1,25 |
1,74 |
2,04 |
Effet M.O H.S Effet D T.H.S Effet P T.H.S Interaction M.O*D N.S Interaction M.O*P T.H.S Interaction D*P T.H.S |
|
D1 |
2,00 |
2,09 |
2,14 |
2,20 |
2,17 |
2,15 |
1,95 |
1,65 |
2,04 |
|||
|
D2 |
2,10 |
2,15 |
2,25 |
2,32 |
2,25 |
2,25 |
2,00 |
1,75 |
2,13 |
|||
|
D3 |
2,15 |
2,20 |
2,35 |
2,50 |
2,30 |
2,28 |
2,20 |
1,79 |
2,22 |
|||
|
M.O.O |
D0 |
2,00 |
2,00 |
1,98 |
2,10 |
1,85 |
1,75 |
1,60 |
1,35 |
1,81 |
2,13 |
|
|
D1 |
2,14 |
2,15 |
2,18 |
2,20 |
2,25 |
2,30 |
2,00 |
1,60 |
2,10 |
|||
|
D2 |
2,20 |
2,30 |
2,31 |
2,35 |
2,40 |
2,37 |
2,10 |
1,87 |
2,24 |
|||
|
D3 |
2,25 |
2,37 |
2,42 |
2,45 |
2,60 |
2,44 |
2,17 |
1,93 |
2,33 |
|||
|
Moyennes |
2,11 |
2,15 |
2,19 |
2,22 |
2,19 |
2,15 |
1,96 |
1,65 |
2,08 |
Interaction M.O*D*P T.H.S |
||
C.V M.O: 2, 90 % C.V D: 3, 30% C.V P: 2, 50%
A partir des résultats obtenus lors de notre expérimentation, la teneur en sodium échangeable est influencée de façon hautement significative par le type de matière organique. La comparaison des moyennes a permis d'obtenir deux groupes homogènes, un premier groupe (a) formé par le fumier ovin avec une moyenne de 2,13 méq Na+/100 g de sol et un deuxième groupe (b) est présenté par le fumier bovin avec 2,04 méq Na+/100 g de sol (Tableau 13). Le coefficient de variation est de 2,9%.
Le facteur dose de la matière organique a aussi un effet très hautement significatif sur le taux de sodium. Ce dernier augmente au fur et à mesure qu'on accroît la dose de la matière organique (Tableau 13). L'interaction M.O*Dose présente des différences non significatives entre les différentes combinaisons M.O*Dose. L'effet dose est justifié par la quantité de la matière organique apportée, alors que la non signification de l'interaction
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
M.O*Dose est du aux rapprochement dans les teneurs des fumiers en sodium (cf. Tableau 05).
La figure (38) montre les teneurs du sol en sodium échangeable qui sont proches pour la même dose des deux fumiers. Nous remarquons que l'accroissement du sodium avec l'augmentation de la dose est faible et très voisin pour les deux matières organiques. Le sodium passe ainsi de 1,74 méq Na+/100 g de sol et 1,81 Na+/100 g de sol en D0 à 2,22 méq Na+/100 g de sol et 2,33 méq Na+/100 g de sol en D3 respectivement pour les sols amendés avec le fumier bovin et ovin (Fig.37). Une bonne corrélation existe entre le sodium et la dose de la matière organique (0,94<r<0,97).
|
2,4 |
||||||
|
2,2 2 1,8 1,6 1,4 1,2 1 |
||||||
|
D0 D1 D2 D3 Doses de matières organiques |
||||||
|
MOB MOO |
||||||
Fig.37 : Evolution du Na+ échangeable
(méq/100g de sol) en fonction
du type et doses de la matière
organique
|
ET 0,03 E.T E.T E.T 0,07 E.T 0,06 E.T 0,02 |
||||||||||||||||
|
0,03 |
||||||||||||||||
|
0,02 |
E.T |
|||||||||||||||
|
E.T |
0,05 |
|||||||||||||||
|
0,02 |
||||||||||||||||
|
D0 D1 D2 D3 D0 D1 D2 D3 |
||||||||||||||||
|
M.O.B |
M.O.B |
|||||||||||||||
Fig.38 : Box plot " boites à moustaches"
d'évolution du Na+ échangeable
(méq/100g de
sol) à différentes doses de la M.O
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
La comparaison des moyennes du teneur en sodium échangeable pour la combinaison M.O*Dose a illustré quatre groupes (a, b, c et d) qui sont présentés par ordre par D3 avec 2,22 et méq Na+/100 g de sol, D2 avec 2,13 et méq Na+/100 g de sol, D1 avec 2,04 et méq Na+/100 g de sol et D0 avec 1,74 et méq Na+/100 g de sol pour les sols amendés avec la matière organique bovine et par D3 avec 2,33 et méq Na+/100 g de sol, D2 avec 2,24 et méq Na+/100 g de sol, D1 avec 2,10 et méq Na+/100 g de sol et D0 avec 1,81 et méq Na+/100 g de sol pour la fertilisation avec le fumier ovin.
L'analyse de la variance des résultats a montré un effet très hautement significatif du temps sur le taux de sodium échangeable (Tableau 13), ainsi que l'interaction M.O*P. Le sodium augmente de 2,06 et 2,15 méq Na+/100 g de sol aux premier temps pour atteindre alternativement 2,20 méq Na+/100 g de sol en P4 pour la fertilisation bovine et 2,30 méq Na+/100 g de sol en P5 pour la fertilisation ovine. Il décroît ensuite à 1,61 et 1,69 méq Na+/100 g de sol en P8 par ordre dans les sols additionnés de la matière organique bovine et ovine (Fig.39).
Le test de Newman-keuls de l'interaction (M.O*P) a dévoilé quatre groupes homogènes, concernant la fertilisation bovine. Le premier groupe (a) est composé par les deux prélèvements P4 (2,20 méq Na+/100 g de sol) et P3 (2,16 méq Na+/100 g de sol), le deuxième groupe (b) englobe les quatre prélèvements P5 (2,12 méq Na+/100 g de sol), P2 et P6 (2,10 méq Na+/100 g de sol) et P1 (2,06 méq Na+/100 g de sol), les groupes (c et d) sont présentés respectivement par P7 (1,95 méq Na+/100 g de sol) et P8 (1,61 méq Na+/100 g de sol). En ce qui concerne la deuxième fertilisation, sept groupes ont été enregistrés, cinq homogènes (a, c, d, e et f) sont formés alternativement par P5 (2,20 méq Na+/100 g de terre), P2 (2,22méq Na+/100 g de sol) et P6 (2,21 méq Na+/100 g de sol), P1 (2,15 méq Na+/100 g de sol), P7(1,97 méq Na+/100 g de sol) et P8 (1,69 méq Na+/100 g de sol), et deux groupes intermédiaires (ab et bc) sont présentés par ordre par P4 (2,28 méq Na+/100 g de sol) et P3 (2,25méq Na+/100 g de sol).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
||||||||
|
2,4 |
||||||||
|
2,2 2 1,8 1,6 1,4 1,2 1 a+ (meq/100g de SO1) n) r A N) -4). -0) CO N) N) .1 |
||||||||
|
P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||||
|
MOB MOO |
||||||||
Fig.39 : Evolution du Na+ échangeable
(méq/100g de sol) en fonction du
temps et du type de matière
organique
L'interaction des trois facteurs à savoir la matière organique, la dose de la matière organique et le temps (M.O*D*P) a influencé, aussi de façon très hautement significative sur ce paramètre (Tableau 13). Les figures (40 et 41) montrent que le taux de sodium échangeable est en diminution continue en (D0), ceci passe de 2 méq Na+/100 g de sol à 1,35 méq Na+/100 g de sol (pour la matière organique ovine) et 1,25 méq Na+/100 g de sol (pour la matière organique bovine). Les résultats présentés dans la figure (40) montre qu'en D1, D2 et D3 le sodium échangeable croit par ordre de 2, 2,10 et 2,15 méq Na+/100 g de sol (en P1) à 2,20, 2,32 et 2,50 méq Na+/100 g de sol au quatrième prélèvement puis diminue à 1,65, 1,79 et 1,75 méq Na+/100 g de sol. La figure (41) indique que l'accroissement du sodium est continu jusqu'au cinquième prélèvements en D2 et D3, le sodium passe successivement de 2,20 et 2,25 méq Na+/100 g de sol en (P1) à 2,40 et2, 60 méq Na+/100 g de sol puis à 1,87 et 1,93 méq Na+/100 g de sol en (P8).
L'analyse statistique de l'interaction (M.O*D*P) a fait ressortir deux groupes homogènes. Le groupe (a) formé par la matière organique ovine et le groupe (b) présenté par la matière organique bovine en D0 (pour P2, P3, P4, P5 et P8), en D1 (pour P1et P6) en D2 (pour P1, P2, P5, P6 P7 et P8) et en D3 (pour P1, P2, P5, P6 et P8). En ce qui concerne les autres combinaisons D*P, un seul groupe englobe les deux amendements a été révélé (Annexe 07).
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
||||||||
|
2,8 |
||||||||
|
2,6 2,4 2,2 2 1,8 1,6 1,4 1,2 1 Na+ (meq/100g de sol) 1\3 1\3 N3 is --% -N3 -41, Cr) CO r3 r3 41, co C |
||||||||
|
P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||||
|
D0 D1 D2 D3 |
||||||||
Fig.40 : Evolution du Na+ échangeable
(méq/100g de sol) en fonction du temps
à différentes
doses de la M.O bovine
|
2,8 2,6 2,4 2,2 2 1,8 1,6 1,4 1,2 1 Na+ irmeo/1008 de soil iv iv iv Is IV -P |
||||||
|
1 2 3 4 5 6 7 8 Prélèvements |
||||||
|
D0 D1 D2 D3 |
||||||
Fig.41 : Evolution du Na+ échangeable
(méq/100g de sol) en fonction du
temps à différentes
doses de la M.O ovine
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
II-5-4- Le potassium (K+)
La teneur des sols en potassium diffère d'après la composition minéralogique de la roche mère et l'intensité des pertes, par exportation, le lessivage et l'érosion (HALILAT, 1993 et HALILAT et al, 2000).
D'après BOCKMAN et al (1990), la majeure partie du potassium présent dans le sol est incluse dans les composés minéraux insolubles. Il est inaccessible aux plantes. Une fumure régulière assure une bonne alimentation des cultures.
Les résultats ayant donnés suite au dosage du K+ échangeable, sont exposés dans le tableau (14).
Tableau 14 : valeurs du potassium échangeable (méq/100g de sol) dans les différents traitements
|
Traitements |
Prélèvements |
Moyennes |
Analyses |
|||||||||
|
P1 |
P2 |
P3 |
P4 |
P5 |
P6 |
P7 |
P8 |
|||||
|
M.O.B |
D0 |
0,39 |
0,37 |
0,34 |
0,33 |
0,33 |
0,32 |
0,31 |
0,28 |
0,33 |
0,40 |
Effet M.O S Effet D T.H.S Effet P T.H.S Interaction M.O*D H.S Interaction M.O*P T.H.S Interaction D*P T.H.S |
|
D1 |
0,40 |
0,45 |
0,50 |
0,49 |
0,39 |
0,35 |
0,34 |
0,30 |
0,40 |
|||
|
D2 |
0,43 |
0,47 |
0,50 |
0,53 |
0,40 |
0,36 |
0,36 |
0,33 |
0,42 |
|||
|
D3 |
0,47 |
0,50 |
0,51 |
0,53 |
0,43 |
0,38 |
0,37 |
0,36 |
0,44 |
|||
|
M.O.O |
D0 |
0,39 |
0,39 |
0,38 |
0,37 |
0,35 |
0,33 |
0,31 |
0,27 |
0,34 |
0,48 |
|
|
D1 |
0,51 |
0,52 |
0,54 |
0,54 |
0,55 |
0,56 |
0,43 |
0,31 |
0,49 |
|||
|
D2 |
0,53 |
0,56 |
0,57 |
0,58 |
0,56 |
0,53 |
0,44 |
0,33 |
0,51 |
|||
|
D3 |
0,55 |
0,59 |
0,60 |
0,61 |
0,62 |
0,61 |
0,51 |
0,36 |
0,56 |
|||
|
Moyennes |
0,46 |
0,48 |
0,49 |
0,50 |
0,45 |
0,43 |
0,38 |
0,32 |
0,44 |
Interaction M.O*D*P T.H.S |
||
C.V M.O: 13, 10 % C.V D: 9, 90% C.V P: 4, 40%
Les analyses statistiques ont montrés que le type de matière organique a un effet significatif sur la teneur en potassium échangeable. Ce dernier passe en moyenne de 0,40méq
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
K+/100g de sol pour la matière organique bovine à 0,48méq K+/100g de sol pour la matière organique ovine (Tableau 14).
L'analyse de la variance du facteur matière organique a fait ressortir deux groupes homogènes, dont la matière organique ovine forme le premier groupe (a) et la matière organique bovine le groupe (b). Le coefficient de variation est de 13,1%.
La teneur en potassium présente des différences très hautement significatives avec le facteur dose de la matière organique et hautement significative avec l'interaction M.O*Dose (Tableau 14). Elle a tendance à augmenter avec la dose de la matière organique ramenée à notre sol (Fig.43). Le potassium est au maximum en (D3) avec 0,44 et 0,56 méq K+/100g de sol respectivement pour les sols amendés avec le fumier bovin et ovin, après avoir été 0,33 méq K+/100g de sol en moyenne en (D0) (Fig.42). Une forte corrélation positive entre la dose de matière organique et le potassium est constatée (r=0.93).
L'analyse statistique de l'interaction M.O*Dose et grâce au test de Newman-keuls a révélé quatre groupes pour la fertilisation bovine; trois homogènes (a, b et c) présentés par ordre par D3 avec 0,44 K+/100g de sol, D1 avec 0,40méq K+/100g de sol et D0 avec 0,33méq K+/100g de sol et un seul groupe intermédiaire (ab) enregistré en D2 avec 0,42méq K+/100g du sol. En revanche pour la matière organique ovine, trois groupes homogènes (a, b et c) ont été ressorti, les groupes (a et c) sont présentés alternativement par D3 (0,56méq K+/100g de sol) et D0 (0,34méq K+/100g de sol), le groupe (b) unit les deux doses D2 (0,51méq K+/100g de sol) et D1 (0,49méq K+/100g de sol).
|
0,6 |
||||||
|
0,55 0,5 0,45 0,4 0,35 0,3 0,25 0,2 K+ (meq/100g de sol) o o 0 0 J al w 01 -P 01 01 01 |
||||||
|
D0 D1 D2 D3 Doses de matière organique |
||||||
|
MOB MOO |
||||||
Fig.42 : Evolution du K+ échangeable
(méq/100g de sol) en fonction du
type et doses de la matière
organique
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
||||||||||||||||||||
|
E.T E.T 0,01 E.T 0,02 |
||||||||||||||||||||
|
E.T E.T E.T 0,01 0,02 0,01 0,01 |
||||||||||||||||||||
|
E.T 0,01 |
||||||||||||||||||||
|
E.T |
||||||||||||||||||||
|
0,01 |
||||||||||||||||||||
|
D0 D1 D2 D3 D0 D1 D2 D3 |
||||||||||||||||||||
|
M.O.B |
M.O.O |
|||||||||||||||||||
Fig. 43 : Box plot " boites à moustaches"
d'évolution du K+ échangeable
(méq/100g de
sol) à différentes doses de la M.O
Le potassium évolue de façon très hautement significative pendant la période expérimentale. Les valeurs moyennes de l'essai passent de 0,50 méq K+/100g de sol (en P4) à 0,32 méq K+/100g du sol (en P8) après avoir été de l'ordre de 0,46 méq K+/100g de sol en (P1) (Tableau 14). L'interaction M.O*P aussi a un effet très hautement significatif sur ce paramètre qui accroît de 0,42 méq K+/100g de sol (en P1) à 0,47 méq K+/100g de sol (en P4). Il diminue ensuite à 0,32 méq K+/100g de sol (en P8) pour les sols additionnés de fumier bovin. Le fumier ovin a augmenté le potassium de 0,49méq K+/100g de sol (en P1) à 0,52 méq K+/100g de sol en (P3 et P4), puis il passe à 0,32 méq K+/100g de sol en (P8) (Fig.44). Une relation négative entre le potassium et le temps (r (M.O.B)= -0,8 et r (M.O.O)= -0,69).
L'analyse statistique du facteur temps a révélé six groupes pour les sols ayant une fertilisation bovine; les deux groupes (a et e) englobent respectivement les prélèvements (P4 et P3) avec (0,47et 0,46 méq K+/100g de sol) et (P6 et P7) avec 0,35méq et 0,34méq K+/100g de sol. Les groupes (b, c, d et f) sont formés par ordre par P2 avec 0,45 méq K+/100g de sol, P1 (0,42 méq K+/100g de sol), P5 (0,39 méq K+/100g de sol) et P8 (0,32 méq/100g de sol). Quatre groupes homogènes ont été illustrés (a, b, c et d) pour la matière organique ovine, les groupes (b, c et d) sont présentés alternativement par P1 (0,49méq K+/100g de sol), P7 (0,42 méq K+/100g de sol) et P8 (0,32 méq K+/100g de sol). Les prélèvements P3 et P4 (0,52 méq
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
K+/100g de sol) et P5 et P2 (0,51 méq K+/100g de sol) forment le groupe (a), un autre groupe intermédiaire (ab) présenté par P6 (0,50méq K+/100g de sol).
|
0 ,55 |
||||||
|
0,5 0,45 0,4 0,35 0,3 0,25 0,2 IC (meq/100g de sol) 0 0 o c D iv P la P -41. P "c J 01 C.4 01 41. 01 01 C |
||||||
|
P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||
|
MOB MOO |
||||||
Fig.44 : Evolution du K+ échangeable
(méq/100g de sol) en fonction
du temps et du type de matière
organique
L'effet de l'interaction des trois facteurs à savoir, la matière organique, la dose de la matière organique et le temps (M.O*D*P) parait très hautement significatif sur le potassium échangeable (tableau 14). Les figures (45 et 46) montrent que le potassium diminue en (D0) (comme Ca++, Na+ et Mg++). Il passe de 0,39méq/100g du sol en (P1) à 0,28 méq K+/100g de sol en (P8).
D'après la figure (45), le potassium croit pour les trois doses D1, D2 et D3 successivement de 0,40, 0,43 et 0,47 méq K+/100g de sol (en P1) à 0,50 méq K+/100g de sol avec (D1) (en P3), 0,53 méq K+/100g de sol pour (D2 et D3) en (P4) ensuite il diminue à 0,30, 0,33 et 0,36 méq K+/100g de sol (en P8) par ordre en D1, D2 et D3.
La figure (46) indique que le potassium échangeable accroît de 0,51, 0,53 et 0,55 méq K+/100g de sol (P1) à 0,56 méq/100g de sol (en P6), 0,58 méq/100g de sol (en P4) et 0, 62 méq K+/100g de sol (en P5) alternativement pour D1, D2 et D3 puis décroît à 0,31, 0,33 et 0,36 méq K+/100g de sol en (P8) respectivement pour les même doses. L'augmentation de la teneur en potassium peut être expliquée par la fixation des ions K+ provenant de la minéralisation des matières organiques sur le complexe absorbant et la diminution par le décroissement de la capacité d'échange cationique qui a été montré précédemment. La
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
différence enregistrée entre les deux fertilisants est due à l'écart en capacité d'échange cationique des sols de deux fertilisations.
|
0,7 |
||||||
|
0,6 0,5 0,4 0,3 0,2 IC+ (meq/100g de sol) PPPPPS N c...) -P Cli 0) .- |
||||||
|
P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||
|
D0 D1 D2 D3 |
||||||
L'analyse statistique de l'interaction des trois facteurs à savoir la matière organique, la dose de la matière organique et le temps a fait ressortir un seul groupe homogène qui englobe les deux amendements pour les témoins pendant l'essai. Par ailleurs, deux groupes homogènes (a et b) ont été révélé pour les doses D1, D2 et D3, le groupe (a) formé par la matière organique ovine et celui du groupe (b) présenté par la matière organique bovine (de P1 à P7) un seul groupe englobe les deux amendements enregistré au dernier prélèvement p
Fig.45 : Evolution du K+ échangeable
(méq/100g de sol) en fonction du temps à
différentes
doses de la M.O bovine
|
0 |
||||||||
|
,7 ,6 ,5 ,4 ,3 K+ (meq/100g de sol) - 5 "oa -4 in a) - |
||||||||
|
0,2 P1 P2 P3 P4 P5 P6 P7 P8 Prélèvements |
||||||||
|
D0 D1 D2 D3 |
||||||||
|
CHAPITRE II: Résultats et interprétations d'analyse du sol durant l'expérimentation |
||||||||
Conclusion
L'apport organique à notre sol se traduit par une augmentation des cations échangeables à savoir le calcium (Ca++), le magnésium (Mg++), le sodium (Na+) et le potassium (K+). L'accroissement parait claire après cinq semaines de la mise en place de l'essai. Nos résultats confirment ceux obtenus par TURIES et al (2000), qui ont indiqué que la fertilisation organique entraîne une augmentation des cations échangeables en augmentant la teneur en carbone organique, ce qui est bien connu d'ailleurs (BOISSON, 1977, MOREAU, 1983, WILCZYNSKI et al, 1993 et FELLER, 1994).
Nous avons remarqué que chaque fois les meilleurs résultats sont obtenus avec la matière organique ovine en D3 avec 10,18 méq Ca++ /100g de sol, 1,47 méq Mg++/100g de sol, 2,33méq de Na+/100g de sol et 0,56 méq K+/100g de sol contre 8,49 méq/100g de sol, 1,19 méq/100g de sol, 2,22 méq/100g de sol et 0,44 méq/100g de sol pour la matière organique bovine successivement pour le calcium, le magnésium, le sodium et le potassium. L'accroissement est toutefois suivi par une diminution vers la fin de la période expérimentale à cause de la diminution de la capacité d'échange cationique de sol par la dégradation de la matière organique.
Chapitre III: Etude de quelques corrélations
A partir des résultats précédents, nous avons remarqué que le pH tend à diminuer chaque fois qu'on augmente la dose d'apport de la matière organique. Il joue par conséquent un rôle principal dans la dynamique et l'évolution de la matière organique. Il ressort à travers l'étude des corrélations que le pH est pratiquement corrélé avec la majorité des paramètres étudiés à savoir la conductivité électrique, l'humidité équivalente, la capacité d'échange cationique et les cations échangeables (Ca++, Mg++, Na+ et K+).
a) Relation entre le pH et la conductivité électrique
L'étude de la relation entre ces deux paramètres, montre une corrélation négative de l'ordre de r= - 0,49, où nos analyses montrent que la conductivité électrique du sol tend à augmenter, chose qui est opposée au pH qui décroît avec l'apport organique. Cette relation entre le pH et la conductivité électrique est illustrée par la courbe de régression (Fig.47).
b) Relation entre le pH et la capacité de rétention en eau (humidité équivalente)
La relation entre le pH et la capacité de rétention en eau du sol pour les différents traitements est inversement proportionnelle avec une bonne corrélation négative de l'ordre de r= -0,63. Chaque fois que la teneur en eau retenue par le sol augmente, nous avons une diminution du pH avec l'accroissement des doses des matières organiques. La courbe de régression illustre bien cette relation (Fig.48).
c) Relation entre le pH et les cations échangeables
La relation entre le pH et chaque cation échangeable est négative (r (Ca++)= -0,62), r (Mg++)= -0,42, r (Na+)= -0,50 et r (K+)= -0,45). Nos analyses indiquent que la teneur de chaque cation échangeable augmente avec les doses des matières organiques apportées alors que le pH diminue. Les figures (50, 51, 52 et 53) illustrent respectivement les relations existantes entre le pH et le calcium, le pH et le magnésium, le pH et le sodium et le pH et le potassium.
Chapitre III: Etude de quelques corrélations
L'étude de la relation entre la C.E.C et l'humidité équivalente montre une très forte corrélation positive (r= 0,74). A partir des résultats précédents, nous avons remarqué que la capacité de rétention en eau du sol et la capacité d'échange cationique tendent à augmenter à chaque fois qu'on augmente la dose d'apport de la matière organique. Les résultats ont montré ainsi que la matière organique retient mieux l'eau et sa capacité d'échange cationique augmente qu'elle est humifié. Il est évident, que chaque fois que l'humidité équivalente augmente il y a un accroissement de la capacité d'échange cationique. La figure (49) illustre bien cette relation.
La relation entre la conductivité électrique et l'humidité équivalente est non significative (r= 0,05) (Tableau 15). Alors que AYER et WESTCOT (1988) ont trouvé théoriquement que la rétention en eau du sol est en fonction croissante de la conductivité électrique de la solution du sol.
La droite de régression (Fig.54) illustre l'intensité de la relation qui existe entre le calcium et la capacité de rétention au champ du sol (r= 0,73). Des corrélations positives entre l'humidité équivalente et les deux cations, le magnésium (r= 0,58) et le potassium (r= 0,61) (Fig.55 et 57). A partir de la figure (56) on remarque une forte relation positive entre l'humidité équivalente et le sodium échangeable(r= 0,61) qui serait due à l'affinité du sodium vis-à-vis de l'eau (GRIM, 1953).
A partir de nos résultats, nous avons remarqué que la C.E.C tend à augmenter en fonction de la dose de la matière organique apportée à notre sol. Il est évident, qu'à chaque fois qu'on accroît la quantité apportée, nous aurons une élévation des taux des cations à savoir le calcium, le magnésium, le sodium et le potassium qui vont être fixer sur le complexe adsorbant. Chose confirmée par l'étude de la relation entre le C.E.C et ces cations qui relève : - une très forte corrélation avec la teneur en calcium (r= 0,99) (Fig.58).
- une forte corrélation avec la teneur en magnésium (r= 0,77) (Fig.59).
- une forte corrélation avec la teneur en sodium (r= 0,85) (Fig60).
Chapitre III: Etude de quelques corrélations - une forte corrélation avec la teneur en potassium (r= 0,80) (Fig.61).
Tableau 15 : Matrice de corrélation.
|
pH |
C.E |
H.É |
C.E.C |
Ca++ |
Mg++ |
Na+ |
K+ |
||||||
|
pH |
1 |
||||||||||||
|
C.E |
-0,49 |
1 |
|||||||||||
|
H.É |
-0,63 |
0,05 |
1 |
||||||||||
|
C.E.C |
-0,62 |
0,01 |
0,74 |
1 |
|||||||||
|
Ca++ |
-0,62 |
0,066 |
0,73 |
0,99 |
1 |
||||||||
|
Mg++ |
-0,42 |
-0,16 |
0,59 |
0,77 |
0,70 |
1 |
|||||||
|
Na+ |
-0,50 |
-0,14 |
0,61 |
0,85 |
0,80 |
0,80 |
1 |
||||||
|
K+ |
-0,45 |
-0,17 |
0,61 |
0,80 |
0,73 |
0,92 |
0,82 |
1 |
|||||
|
8 |
= |
0,05 |
1 |
Corrélé Bien corrélé Très bien corrélé |
|||||||||
pH
6
4
2
9
8
7
5
3
0
1
7,5 8 8,5 9 9,5
CE(mS/cm)
Y=-2,38x + 25,70 ,3832x + 25707R2 = 0,24
02449
Fig.47 : Relation entre le pH et la conductivité électrique

Y= -8,08x + 99,24 R2 = 0,40
y = 8,0
7,5 8 8,5 9 9,5
pH
|
HO (%) |
45 40 35 30 25 20 15 10 5 0 |
Fig. 48: Relation entre le pH et l'humidité équivalente
Chapitre III: Etude de quelques corrélations
Calcium (meg/100g)
16
14
12
10
4
2
8
6
0
Y = -6,39 x + 58,7 y = -63965x + 58
R2 = 0,38
R2
7,5 8 8,5 9 9,5
pH
Fig.50 : Relation entre le pH et le calcium
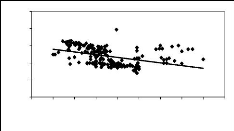
Magnesium (meq/100g)
2,5
0,5
1,5
2
0
1
7,4 7,6 7,8 8 8,2 8,4 8,6 8,8 9 9,2
pH
Y= -0,4x + 4,44 y = -0,403x + R2 = 0,18R
Fig.51 : Relation entre le pH et le magnésium
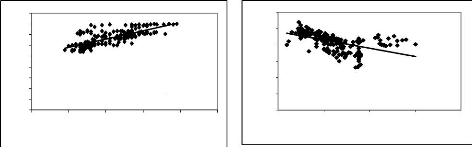
45
40
35
30
25
20
He (%)
15
10
5
0
Y= 0,77x + 25,37 R2 = 0,54
y 0,76
0 5 10 15 20 25
CEC (méq/100g)
3
2,5
2
1,5
1
Sodium (meg/100g)
0,5
0
Y= -0,51x + 6,21 R2 = 0,25
5084 62 2
7,5 8 8,5 9 9,5
pH
Fig. 49: Relation entre l'humidité équivalente et Fig.52 : Relation entre le pH et le sodium
la capacité d'échange cationique
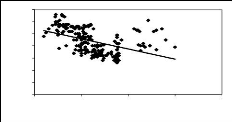
Potassiun (m6q100g)
0,7
0,6
0,5
0,4
0,3
0,2
0,1
0
7,5 8 8,5 9 9,5
pH
Y= -0,17x + 1,79
y = -01659x +
R2 = 0,20
R2
Fig.53 : Relation entre le pH et le potassium
Chapitre III: Etude de quelques corrélations
|
45 40 35 30 25 |
|||
|
H6 (%) |
|||
|
20 15 10 5 |
Y= 0,91x + 27, 36 R2 = 0,54 |
||
|
0 |
0 5 10 15 20
Calcium (méq/100g)

Y= 0, 83x + ,05 y = 08328x
R2 = 0,98
0 5 10 15 20 25
CEC (méq/100g)
16

14

12

10

8

6

4

Calcium (meq/1 00g)
2
0
Fig. 54: Relation entre l'humidite equivalente et le calcium
|
45 40 35 30 25 |
||||
|
H6 (%) |
||||
|
20 |
Y= 7, 84x + 24,3 R2 = 0,34 |
|||
|
10 5 0 |
3 |
|||
0 0,5 1 1,5 2 2,5
Magnésium (méq/100g)
Fig. 54: Relation entre l'humidite equivalente et le magnesium
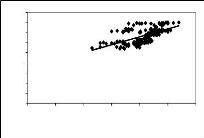
0 0,5 1 1,5 2 2,5 3
Sodium (méq/100g)
He (%)
45
40
35
30
25
20
15
10
5
0
Y= 7,74x + 17,45 R2 = 0,37
7
Fig. 56: Relation entre l'humidite equivalente et le sodium
|
45 |
||||
|
35 |
||||
|
H6 (%) |
30 |
|||
|
25 |
||||
|
20 |
Y= 21,40x + 24,20 R2 = 0,37 |
|||
|
15 |
||||
|
10 5 0 |
||||
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7
Potassium (méq/100g)
Fig.57 : Relation entre l'humidite equivalente et le potassium
Fig. 58: Relation entre la capacite d'echange cationique et le calcium

Y= 0,06x +0,54
R2 = 0,59 y =
0,0
,
0 5 10 15 20 25
CEC (méq/100g)
2,5
2
1,5
1
Magnesium (meo/100g)
0,5
0
Fig.59: Relation entre la capacite d'echange cationique et le magnesium
Y= 0,06x + 1,33
R2 = 0,71 y = 00

0 5 10 15 20 25
CEC (méq/100g)

3
2,5
2
1,5
1
Sodium (m6q/1 00g)
0,5
0
Fig.60 : Relation entre la capacite d'echange cationique et le sodium
Y= 0,02x + 0,18
R2 = 0,63
00
0 5 10 15 20 25
CEC (méq/100g)
0,7
Potassium (m6q/100g)
0,6
0,5
0,4
0,3
0,2
0,1
0
Fig. 61: Relation entre la capacite d'echange cationique et le potassium

En Algérie, les zones arides représentent près de 95% du territoire national dont 80%dans le domaine hyperaride. Ces chiffres traduisent à eux seul l'intérêt de ces régions. La mise en valeur de ces surfaces et leur aménagement est d'une importance capitale pour l'avenir économique du pays.
Les sols des régions arides sont réputés pour être dans leur ensemble pauvre en matière organique. En effet, leurs caractéristiques aussi bien physiques que chimiques sont très particulières et posent des problèmes agronomiques (aptitude culturale faible par exemple) et environnementaux à savoir l'érosion et le ruissellement. De ce fait, il est impératif de raisonner convenablement les apports organiques comme amendement pour améliorer la situation dégradée de ces sols. C'est dans ce contexte que nous avons essayé de déterminer l'effet de deux amendements organiques (fumier bovin et ovin) sur quelques propriétés physiques et chimiques d'un sol sableux. Notre expérimentation a été réalisée dans des pots en conditions climatiques sahariennes de la région de Ouargla.
Durant cet essai, il s'est avéré que sous l'effet des amendements, les propriétés physiques et chimiques du sol paraissent améliorer mise à part la salinité.
L'analyse de l'ensemble des paramètres étudiés permet de tirer les conclusions suivantes :
L'apport organique à des doses croissantes fait diminuer de façon hautement significative le pH. La faible valeur du pH est de l'ordre de 7,73 est obtenue par la dose D3 (113,4 T/h) de fumier ovin après deux mois du départ ensuite elle augmente à 7,89 à la fin de l'expérimentation.
En ce qui concerne la conductivité électrique, la matière organique a augmenté la salinité du sol grâce à la minéralisation de ces constituants organiques. La conductivité électrique croit pendant l'essai, mais elle diminue avec l'accroissement de la dose de matières organiques. C'est donc l'effet de la matière organique sur la structure du sol en améliorant le lessivage des sels dissous. La plus forte salinité est de 7,83 mS/cm. Celle-ci est obtenue avec la dose D1 (37,8 T/h) à la fin de l'expérimentation pour la fertilisation avec le fumier ovin.
La capacité de rétention en eau du sol a présenté des différences très hautement significatives avec les différents traitements de matières organiques. La matière organique accroît la capacité de rétention en eau du sol pendant toute la période expérimentale dont le grand pourcentage est enregistré avec le fumier ovin en D3 avec 39,45% en moyenne.
L'étude de la capacité d'échange cationique a montré que l'utilisation des fumiers comme amendement est très positive. On constate une amélioration très hautement significative de la capacité d'échange cationique en fonction de la dose de matière organique et par conséquence une amélioration des cations échangeables : le calcium, le magnésium, le sodium et le potassium. Le meilleur résultat est obtenue avec le traitement de la dose (D3) de la matière organique ovine avec 18,12méq/100g de sol.
Les résultats obtenus font apparaître deux phases distinctes de l'influence de la matière organique sur les propriétés du sol, notamment le pH, la capacité d'échange cationique et les cations échangeables :
· Une première période, varie de quatre à cinq semaines, caractérisée par un changement rapide des propriétés du sol;
· Une deuxième phase caractérisée par un recul dans les caractéristiques du sol.
Au terme de cette étude, la comparaison que nous avons faite concernant les deux types de matières organiques et les traitements nous permet de dire que nos matières organiques influent sur les propriétés du sol avec une importance relative plus grande pour le fumier ovin. Les propriétés du sol sableux paraient relativement corrigées à l'exception de la salinité qui augmente. Cependant l'amélioration est limitée dans le temps.
En ce qui concerne la dose, nous nous limiterons à dire que la dose 113,4 T/h (D3) a donné les meilleurs résultats mais elle est probablement élevée.
L'irrigation étant indispensable pour les sols dans les régions arides, celle-ci peut, si elle est raisonnée, contribuer à résoudre le problème de l'augmentation de la salinité, mais à condition que la surface irriguée soit bien drainée.
La fertilisation organique est donc très intéressante pour les sols sableux en améliorant en général ses propriétés à savoir le pH, la capacité de rétention en eau du sol, la capacité d'échange
cationique et les cations échangeables. Même si ces modifications sont limitées dans le temps, on pense que l'apport organique régulier et raisonné peut maintenir cette amélioration.
Des progrès plus fins sont encore possibles en matière d'améliorer les propriétés des sols sableux, par la mise en place de stratégie de fertilisation. A partir des données d'essai expérimentaux, de longue durée pour une amélioration non limitée afin de rendre notre Sahara une région à potentiel agricole élevé et permanent.

Abiven S., 2004. Relation entre caractéristiques des matières organiques apportées, dynamique de leur décomposition et l'évolution de la stabilité structurale du sol. L'agro compagne. Rennes. INRA.262p.
AFNOR., 1977. Aliments des animaux. Dosage des cendres brutes.NFV.18-101.2p. AFNOR., 1992. Sol : reconnaissances et essais. Norme française. 16p.
AFNOR., 1993. Produits agricoles et alimentaires. Détermination de la cellulose brute. NF V 03-040. 12p.
AFNOR., 1996. Sol : reconnaissance et essais. Norme française. 15p.
Aubert G., 1978. Méthodes d'analyses des sols. Edit.C.R.D.P.Marseille.189p.
Ayers RS. et Westcot D.W., 1988. La qualité d'eau en agriculture. Bulletin FAO d'irrigation et de drainage. N° 29 FAO. Rome. 180p.
Baize D., 2000. Guide des analyses en pédologie. Chois. Expression. Présentation. Interpritation. 2ème Ed. INRA. Paris. 257p.
Balesdent J., 1996. Un point sur l'évolution des réserves organiques des sols en France. Etude et gestion des sols. INRA.(afes). Vol 3 N°4. Paris. pp 245-260.
Barry J.P., Faurel L., Baumgatner N., Belin B., Celles J.C. et Kada A., 1968. Carte de la végétation de l'Algérie, feuille de Ghardaia (1/500 000). Inst de cart de l'Univ d'Alger.
Barry J.P., Faurel L., Baumgatner N., Belin B., Celles J.C. et Kada A., 1973. Notice du feuille de Ghardaia : carte de la végétation de l'Algérie à 1/500 000. . Mém. Soc. Inst. Nat. Afr N°11.1254p.
Birch H., 1988. The effect of soil drying on humus and nitrogen availability. Plant and soil, 10. pp 9-32.
Bockman O.C., Karsted O., Lie O.H. et Richard I., 1990. Agriculture et fertilization-les engrais leur avenir. Edit. Taugen Grafiste. Centre. Oslo.258p.
Boissezon P., 1977. Essai de determination du role des matières organiques dans la capacité d'échange des sols ferraliques. Science du sol. Vol 2. pp 61-68.
Bodet J.M., Hacala S., Aubert C. et Texigr C., 2001. Fertiliser avec les engrais de ferme. IE.ITVAI, ITCF, ITP. Paris.104p.
Calvet R., 2003. Le sol propriétés et fonctions. Tome 1. Constitution et structure, phénomènes aux interfaces. Edit. France Agricole. 455p.
Callot G., Chamayou H., Maertens C. et Salsac L., 1982. Les interactions sols racines. Incidences sur la nutrition minérale. INRA. Paris. 325p.
Castany G., 1983. Principes et méthodes de l'hydrogéologie. Ed.DUNOD. Paris. pp 33 -228.
Chamayou H. et Legros J.P., 1989. Les bases physiques, chimiques et minéralogiques de la science du sol. Technique vivante. Presses universitaires de France. Paris. pp 212-213.
Charreau G., 1975. Matière organique et biochimique du sol dans les zones tropicales sèches d'Afrique occidenlale. Bullet. Pédol. FAO. N° 27. Rome. pp 303-323.
Dambébé Y., Somé L., Zomboudré G. et Diabri S., 1999. Irrigation de complement du riz pluvial sur des sols sableux conditionnés avec de la matière organique au Sud-Ouest du Burkina Faso. Sécheresse. 10 (2). pp 143-149.
Daoud Y. et Halitim A., 1994. Irrigation et salinisation au Sahara Algérien. Sécheresse. 5(3). pp151-160.
Davet P., 1996. Vie microbienne du sol et production végétale. INRA. Paris. 383p.
Delas J., 1971. Évolution des propriétés d'un sol sableux sous l'influence d'apport massif et répété de matières organiques de différentes origines. Ann. Agr.vol 5 (22). pp 585-610.
Donahy R., 1958. Nature des solset croissance végétale. Ed.D'organisation. Paris. 312p.
Douadi F. et Sahraoui K., la palmeraie de l'ITAS. Etude et possibilité d'aménagement. Mém. Ing. ITAS. Ouargla.
Dresh J., 1975. Mémoires et documents. Serv. Doct et de Cart. Géogra. Ed CNRS.Vol 17. 291p.
Dridi B. et Toumi C., 1999. Influence d'amendements organiques et d'apport de boues sur les propriétés d'un sol cultivé. Etude et gestion des sols, 6(1).pp 7-14.
Dubief J., 1950. Évaporation et coefficient climatiques au sahara. Tra. Inst. Rech. Sci. Paris. Tome 6.344p.
Dubief J., 1963. Le climat du sahara. Mém. Inst. Rech. Saha. Alger. Tome I. 298p.
Dubost D., 1991. Écologie, aménagement et développement agricole des oasis algériennes. Thèse. Doct. Univ. Géo et Amén. Univ François Rablais. Tours. 290p.
Dubost D., 1992. Aridité, agriculture et développement : le cas des oasis Algériennes. Sécheresse. 2(3). pp85-96.
Duchaufour Ph., 1965. Précis de pédologie. Masson. Paris. 481p.
Duchaufeur Ph., 1977. Pédologie. Pédogenèse et classification. Edit. Masson. Paris. Tome 1. 477p.
Duchaufour Ph., 1979. Pédologie, constituants et propriétés du sol. Ed Masson. Paris. 480p.
Duchaufour Ph., 1995. Abréges pédologie : sol, végétation, environnement. 4èmeEd. Masson. Paris.324p.
Durant J.H., 1954. Les sols d'Algérie. S.E.S. Alger. 244p.
Durant J.H., 1959. Les sols rouges et les croûtes en Algérie. SES. Alger. 187p.
Durand J.H., 1983. Les sols irrigables. Etude pédologique. Edit. Imprimerie. Boudin. Paris.339p.
Duthil J., 1973. Elément d'écologie et d'agronomie. Tome II. Exploitation et amélioration du milieu. Ed.J.B. Baillière. Paris. 265p.
Dutil P., 1971.Contribution à l'étude des sols et des paléosols du sahara. Thèse doct d'état. Faculté des sciences de l'université de Strasbourg. 346p.
Feller C., 1994. La matière organique dans les sols tropicaux à argile 1 :1 : recherche de compartiments organiques fonctionnels. Une approche granulométrique. Thèse de Doctoral. Univ. Strasbourg (ULP).190p.
Gary M., Zenshi P., Thamas Sims-George J. et Vance F., 1994. Soil and environmental quality. CRC. Press. 313p.
Gaucher G., 1968. Traité de pédologie, agricole, le sol et ces caractéristiques agronomiques.éd DUNOD. Paris. 578p.
Gobet J.M., Aragno M. et Mathey W., 1998. Le sol vivant, bases de pédologie des sols. Ed. Presses Polytechnique et Universitaire. Ramandes. 519p.
Grim R.E., 1953. Cly mineralogy. Toronto. Londres. 384p.
Grissa H. et Ben Khedher M., 2000. Culture Maraîchère. Principes de base en agriculture biologique. Centre Technique de l'agriculture biologique.33p.
Hadjaidji-Ben Seghir F., 2002. Contribution à l'étude de l'avifaune nicheuse de la palmeraie de la cuvette de Ouargla. Mémoire magistère. Inst.N.A. EL Harrech. Alger.187p.
Halilat M.T., 1993. Etude de la fertilisation azoté et potassique sur le blé dure (variété Aldura) on zones sahariennes (région de Ouargla). Mémoire. Magis. Batna. 130p.
Halilat M.T., 1998. Étude expérimentale de sable additionné d'argile, comportement physique et organisation en conditions salines et sodiques. Thèse. Doct. I.N.R.A. I.N.A. Paris. Grigon. 229p.
Halilat M.T., Dogar M.A. et Badraoui M., 2000. Effet de l'azote, du potassium et de leur interaction sur la nutrition du blé sur sol sableux du désert algérien. Revue. Homme, terre et eaux. Vol.30 (115). pp 32-39.
Halitim A., 1973. Étude expérimentale de l'alimentation des sols sodiques de l'Algérie. Thèse Doct.U.E.R.des sciences biologiques.170 p.
Halitim A., 1988. Sols de régions arides d'Algérie. Alger. 384p.
Hamdi-Aissa B. et Ferodoff N., 1997. Salt affected soil functioning at the Ouargla Oasis (Northern Sahara of Algéria) In: International Symposium on Sustunable Management of Salt affected Soil. Ed. EL Gala.A. Blum. W.E.H. ISSS-FAO. pp 153-154.
Hamdi Aissa B. et Girard M., 2000. Utilisation de la télédétection en régions sahariennes pour l'analyse et l'exploitation Spatiale des pédopaysages. Sécheresse. Vol 11(3). pp 179-188.
Hamdi-Aissa B., 2001. Le fonctionnement actuel et passé des sols du Nord Sahara (cuvette de Ouargla). Thèse. Doct. Inst. Nati. Agr. Grignon. 194p.
Hakimi M., 1976. Contribution à la prospective d'une agriculture irriguée dans les régions Nord Sahariennes. Première conférence régionale Afro-Asiatique de la C.I.I.D. 45p.
Henin S. et al., 1970. Le profil cultural, l'état physique du sol et ses conséquences agronomiques. Ed. Masson et C.I.E. 128p.
Hillal D., 1974. L'eau et le sol : principes et processus physiques. Poly Académie. Press. Neuyourk.357p.
Jacquin F., Mallouhi N. et Gallati., 1979. Étude sur l'intensité du transfert de matière organique sous l'influence de la salinité. C.R.A.D. So. Paris. Pp 1229-1231.
Jourdan O., 1983. Contribution à l'étude de la capacité de rétention en eau des sols, cas de deux sols MALGACHES. Thèse. Doct. 136p.
Lahmar F., 1992. Cartographie des sols de l'exploitation de INFSAS (Ouargla). Etude pédologique et thématique. Mém. Ing. INFSAS. Ouargla.50p.
Lasnier-Lachaise L., 1973. Agronomie nouvelle. Flammarion. Paris. 284p.
LE Houerou H.N., 1995. Bioclimatologie et biogéographie des steppes arides du Nord de l'Afrique (diversité biologique, développement et désertification). Options méditerranéennes. Série B.N°10. montpellier.396p.
Mallouhi N., 1979. Contribution à l'étude d'évolution du compost urbain dans les sols salés carbonatés. Thèse. Doct. Ing. 104p.
Margat J., 1990. Les gisements d'eau souterraine. La recherche. pp221, 590-596.
Margat J., 1992. Quelles ressources en eau les grands Aquifères offrent-ils ? Observatoire du Sahara et du Sahel, le craie.14p.
Meftah H., 1988. Influence d'un apport de litière de volailles et de fumier ovin en sol saharien nu et irrigué de la région de Ouargla, dynamique du carbone et humification. Thèse. Ing. Uni. Ouargla. 58p.
Monniers G., 1965. Action des matières organiques sur la stabilité structurale des sols. Ann. Agron. 16 (4 et 5). pp 327-534.
Moreau R., 1983. Evolution des sols sous différents modes de mise en culture en Côte d'Ivoire forestière et pré forestière. Cah. O.R.S.T.O.M. Sér. Pédol. 20 (4). pp 311-325.
Morril L.G., Mahilum B.C. et Mohiuddin S.H., 1982. Organic compounds in soils: sorption, degradation and persistence. Science. Publisher. 326p.
Mustin M., 1987.Le composte, gestion de la matière organique. Ed. François Dubusc. Paris. 954p.
O.N.M., 2006. Données météorologiques de Ouargla.4p.
Oustani M., 1993. Contribution à l'étude de l'influence certains amendements organiques (palmes de dattier, crottes du dromadaire) sur les propriétés biologiques et chimiques d'un sol salé de la région de Ouargla. Thèse d'Ing. INFSAS. Ouargla. 128p.
Ozenda P., 1983. Flore du sahara. Ed. Centre. Nati. Rech. Sci. Paris.622p.
Parr J.F., 1973. Nature and significance of inorganic transformation in tile drained soil. Soil and fertilizers. N°32. pp 411-415.
Passager P., 1957.Ouargla (Sahara constantinois). Etude géographique et médicale. Arch. Inst. Pasteur.Alger.35 (2) : pp 99-200.
Pochon J. et Deberjac H., 1958. Traité de microbiologie du sol. Application agronomique. Ed. DUNOD. Paris. 685p.
Poget M., 1980. Les relations sol végétation dans les steppes Sud-algéroises. O.R.S.T.O.M. Paris. 555p.
PNUD-UNESCO., 1972. Projet Reg 100. Étude des ressources en eau du Sahara septentrionalRaport sur les résultats du projet. U.N.E.S.C.O. Paris.20p.
Prévot A.R., 1970. Humus, biogenèse biochimie biologie. Edit. Tourelle. Saint-Mandé.342p.
Ribiero R.M., Moureaux C. et Novicoff A., 1976. Etude comparative de l'altération microbienne des différents minéraux constituants d'une diabase. Cah. O.R.S.T.O.M.Vol XIV. N°2. pp 161-168.
Rognon P., 1994. Les principaux sols du Maghreb. In « Désertification et aménagement ». Med. Compus N°8. Cours de séminaire Mednin (Tunisie). Agadir (Maroc. Caen).pp 89-112.
Rouvilois-Brigol M., 1975. Le pays de Ouargla (Sahara Algérien). Variation et organisation d'un espace rural en milieu désertique. Ed. Publ. Dépar. Géol. Univ. Sorbonne. Paris. Tome 2.316p.
Sarag ., 1985. Étude méthodologique de la matière organique des sols. Cas de matière organique des sols de semi-aride du Hodna. Ann. Inst. Agr. d'Alger. 9(1). pp 100-125.
Sahnoune M., 1986. Contribution à l'étude des litières de volailles comme amendement organique en culture maraîchère sous trois étages bioclimatiques. Thèse. Mag. I.N.A. Alger. 65p.
Soltner D., 2003. Les bases de la production végétale. Tome I. Le sol et son amélioration. Collection Sciences et Techniques Agricoles.23ème. Ed. Paris. 472p.
Thuriès L., Arrufat A., Dubois M., Feller C., Herrmann P., Larré-Larrouy M.C., Martin C., Pansu M., Rémy J.C. et Viel M., 2000. Influence d'une fertilisation organique et de la solarisation sur la productivité maraîchère et les propriétés d'un sol sableux sous abri. Etude et gestion du sol. 7 (1). pp 73-88.
Toutain G., 1979. Élément d'agronomie saharienne De la recherche au développement. I.N.R.A. Paris.276p.
Vanghan D. et Malcolm R.E., 1985. Soil organic matter and biological activity. Development in plant and soil sciences. Martinus Nijhaff. Vol. 16. 469p.
Vilain H., 1999. Méthodes expérimentales en agronomie (pratique et analyse). Edit : Tec et Doc. Paris.337p.
Wilczynki A.W., Renger M., Jozefaciuk G., Hajnos M. et Sokoloska Z., 1993. Surface area and C.E.C as related to qualitative and quantitative change of forest soil organic matter after liming. Zpflanz Bodenk. 156 (3). pp 235-238.

Annexe
Annexe (01)
Tableau d'analyse de variance du pH
|
D.D.L |
C.M |
TEST. F |
E.T |
C.V |
|
|
Var.tôt.S-Bloc1 |
5 |
0,02 |
|||
|
Var.facteur1 (M.O) |
1 |
0,07 |
33,04 |
||
|
Var.Blocs |
2 |
0,00 |
0,10 |
||
|
Var.residuelle 1 |
2 |
0,00 |
0,05 |
0,60% |
|
|
Var.tôt.s-bloc2 |
23 |
0,23 |
|||
|
Var.facteur 2 (D) |
3 |
1,69 |
422,97 |
||
|
Var.inter.M.O*D |
3 |
0,04 |
10,29 |
||
|
Var.tot.S-Blocs 1 |
5 |
0,02 |
3,79 |
||
|
Var.residuelle 2 |
12 |
0,00 |
0,06 |
0,80% |
|
|
Var.totale |
191 |
0,18 |
|||
|
Var.facteur 3 (P) |
7 |
1,12 |
792,65 |
||
|
Var.inter.M.O*P |
7 |
0,08 |
53,46 |
||
|
Var.inter.D*P |
21 |
0,02 |
12,35 |
||
|
Var.inter.M.O*D*P |
21 |
0,01 |
9,03 |
||
|
Var.tot.S-Blocs 2 |
23 |
0,23 |
163,07 |
||
|
Var.residuelle 2 |
112 |
0,00 |
0,04 |
0,50% |
Tableau des groupes homogènes du pH
|
Facteur |
Groupes homogènes |
|||
|
M.O.B |
M.O.O |
|||
|
Matière organique (M.O) |
a |
B |
||
|
Dose (D) |
D0 |
a |
a |
|
|
D1 |
b |
b |
||
|
D2 |
c |
c |
||
|
D3 |
d |
d |
||
|
Prélèvements (P) |
P1 |
a |
a |
|
|
P2 |
f |
e |
||
|
P3 |
f |
e |
||
|
P4 |
e |
de |
||
|
P5 |
d |
cd |
||
|
P6 |
d |
c |
||
|
P7 |
c |
c |
||
|
P8 |
b |
b |
||
|
Interaction |
D0 |
P1+P4 |
b |
a |
|
P2+P3+P5+P6+P7+P8 |
a |
a |
||
|
D1 |
P1 |
a |
b |
|
|
P2+P5+P6+P7+P8 |
b |
a |
||
|
P3+P4 |
a |
a |
||
|
D2 |
P1 |
b |
a |
|
|
P2 à P8 |
a |
b |
||
|
D3 |
P1+P2 |
b |
a |
|
|
P3 |
a |
a |
||
|
P4 à P8 |
a |
b |
||
92
Annexe
Annexe (02)
Tableau d'analyse de variance de la C.E
|
D.D.L |
C.M |
TEST. F |
E.T |
C.V |
|
|
Var.tôt.S-Bloc1 |
5 |
1,32 |
|||
|
Var.facteur1 (M.O) |
1 |
1,79 |
1,23 |
||
|
Var.Blocs |
2 |
0,94 |
0,65 |
||
|
Var.residuelle 1 |
2 |
2,00 |
1,46 |
1,21 |
18,90% |
|
Var.tôt.s-bloc2 |
23 |
2,15 |
|||
|
Var.facteur 2 (D) |
3 |
9,56 |
36,43 |
||
|
Var.inter.M.O*D |
3 |
7,30 |
14,11 |
||
|
Var.tot.S-Blocs 1 |
5 |
1,32 |
5,02 |
||
|
Var.residuelle 2 |
12 |
0,26 |
0,51 |
8,00% |
|
|
Var.totale |
191 |
1,77 |
|||
|
Var.facteur 3 (P) |
7 |
36,30 |
241,65 |
||
|
Var.inter.M.O*P |
7 |
0,19 |
1,28 |
||
|
Var.inter.D*P |
21 |
0,46 |
3,08 |
||
|
Var.inter.M.O*D*P |
21 |
0,30 |
1,97 |
||
|
Var.tot.S-Blocs 2 |
23 |
2,15 |
14,33 |
||
|
Var.residuelle 2 |
112 |
0,15 |
0,39 |
6,10% |
Tableau des groupes homogènes de la C.E
|
Facteur |
Groupes homogènes |
|||
|
M.O.B |
M.O.O |
|||
|
Matière organique (M.O) |
||||
|
Dose (D) |
D0 |
b |
c |
|
|
D1 |
a |
b |
||
|
D2 |
b |
a |
||
|
D3 |
c |
c |
||
|
Prélèvements (P) |
P1 |
f |
f |
|
|
P2 |
e |
e |
||
|
P3 |
d |
d |
||
|
P4 |
c |
c |
||
|
P5 |
bc |
bc |
||
|
P6 |
ab |
ab |
||
|
P7 |
a |
a |
||
|
P8 |
a |
a |
||
|
Interaction |
D0 |
P2+P8 |
a |
b |
|
P1+P3 à P7 |
a |
a |
||
|
D1 |
P3 |
a |
b |
|
|
P1+P1+P4 à P8 |
a |
a |
||
|
D2 |
P4+P3 |
b |
a |
|
|
P1+P2+P5 à P8 |
a |
a |
||
|
D3 |
P1 à P7 |
a |
a |
|
|
P8 |
a |
b |
||
93
Annexe
Annexe (03)
Tableau d'analyse de variance de l'H.É
|
D.D.L |
C.M |
TEST. F |
E.T |
C.V |
|
|
Var.tôt.S-Bloc1 |
5 |
59,82 |
|||
|
Var.facteur1 (M.O) |
1 |
297,66 |
2287,42 |
||
|
Var.Blocs |
2 |
0,59 |
4,56 |
||
|
Var.residuelle 1 |
2 |
0,13 |
0,36 |
1,10% |
|
|
Var.tôt.s-bloc2 |
23 |
95,24 |
|||
|
Var.facteur 2 (D) |
3 |
619,40 |
978, 74 |
||
|
Var.inter.M.O*D |
3 |
8,53. |
13,48 |
||
|
Var.tot.S-Blocs 1 |
5 |
59,82 |
94,53 |
||
|
Var.residuelle 2 |
12 |
0,63 |
0,80 |
2,40% |
|
|
Var.totale |
191 |
12,42 |
|||
|
Var.facteur 3 (P) |
7 |
5,84 |
29,23 |
||
|
Var.inter.M.O*P |
7 |
1,29 |
6,45 |
||
|
Var.inter.D*P |
21 |
2,96 |
14,82 |
||
|
Var.inter.M.O*D*P |
21 |
2,22 |
11,13 |
||
|
Var.tot.S-Blocs 2 |
23 |
95,24 |
476,42 |
||
|
Var.residuelle 2 |
112 |
0,20 |
0,45 |
1,30% |
Tableau des groupes homogènes de l'H.É
|
Facteur |
Groupes homogènes |
|||
|
M.O.B |
M.O.O |
|||
|
Matière organique (M.O) |
b |
a |
||
|
Dose (D) |
D0 |
d |
d |
|
|
D1 |
c |
c |
||
|
D2 |
b |
b |
||
|
D3 |
a |
a |
||
|
Prélèvements (P) |
P1 |
c |
c |
|
|
P2 |
b |
b |
||
|
P3 |
a |
b |
||
|
P4 |
b |
b |
||
|
P5 |
b |
b |
||
|
P6 |
b |
b |
||
|
P7 |
b |
b |
||
|
P8 |
b |
a |
||
|
Interaction |
D0 |
P1+P2+P3+P4+P6+P7+P8 |
b |
a |
|
P5 |
a |
a |
||
|
D1 |
P1 |
a |
a |
|
|
P2 à P8 |
b |
a |
||
|
D2 |
P1 à P6 + P8 |
b |
a |
|
|
P7 |
a |
a |
||
|
D3 |
P1 à P8 |
b |
a |
|
94
Annexe
Annexe (04)
Tableau d'analyse de variance de la C.E.C
|
D.D.L |
C.M |
TEST. F |
E.T |
C.V |
|
|
Var.tôt.S-Bloc1 |
5 |
16,93 |
|||
|
Var.facteur1 (M.O) |
1 |
83,78 |
5866,05 |
||
|
Var.Blocs |
2 |
0,41 |
28,87 |
||
|
Var.residuelle 1 |
2 |
0,01 |
0,12 |
1,10% |
|
|
Var.tôt.s-bloc2 |
23 |
60,24 |
|||
|
Var.facteur 2 (D) |
3 |
419,43 |
456,47 |
||
|
Var.inter.M.O*D |
3 |
10,51 |
11,44 |
||
|
Var.tot.S-Blocs 1 |
5 |
16,93 |
18,42 |
||
|
Var.residuelle 2 |
12 |
0,92 |
0,96 |
8,90% |
|
|
Var.totale |
191 |
11,43 |
|||
|
Var.facteur 3 (P) |
7 |
68,58 |
179,15 |
||
|
Var.inter.M.O*P |
7 |
10,65 |
27,82 |
||
|
Var.inter.D*P |
21 |
5,70 |
14,89 |
||
|
Var.inter.M.O*D*P |
21 |
3,79 |
9,91 |
||
|
Var.tot.S-Blocs 2 |
23 |
60,24 |
157,35 |
||
|
Var.residuelle 2 |
112 |
0,38 |
0,62 |
5,80% |
Tableau des groupes homogènes de la C.E.C
|
Facteur |
Groupes homogènes |
|||
|
M.O.B |
M.O.O |
|||
|
Matière organique (M.O) |
b |
a |
||
|
Dose (D) |
D0 |
d |
d |
|
|
D1 |
c |
c |
||
|
D2 |
b |
b |
||
|
D3 |
a |
a |
||
|
Prélèvements (P) |
P1 |
e |
c |
|
|
P2 |
cd |
c |
||
|
P3 |
b |
b |
||
|
P4 |
a |
b |
||
|
P5 |
c |
a |
||
|
P6 |
de |
a |
||
|
P7 |
f |
b |
||
|
P8 |
g |
d |
||
|
Interaction |
D0 |
P1 à P8 |
a |
a |
|
D1 |
P1+P2+P5+P8 |
a |
a |
|
|
P6+P7 |
b |
a |
||
|
P3+P4 |
a |
b |
||
|
D2 |
P1 à P8 |
b |
a |
|
|
D3 |
P1 à P4 |
a |
a |
|
|
P5 à P8 |
b |
a |
||
95
Annexe
Annexe (05)
Tableau d'analyse de variance du Ca++ échangeable
|
D.D.L |
C.M |
TEST. F |
E.T |
C.V |
|
|
Var.tôt.S-Bloc1 |
5 |
9,85 |
|||
|
Var.facteur1 (M.O) |
1 |
48,60 |
2391,30 |
||
|
Var.Blocs |
2 |
0,31 |
15,14 |
||
|
Var.residuelle 1 |
2 |
0,02 |
0,14 |
2,10% |
|
|
Var.tôt.s-bloc2 |
23 |
41,68 |
|||
|
Var.facteur 2 (D) |
3 |
291,60 |
308,35 |
||
|
Var.inter.M.O*D |
3 |
7,76 |
8,20 |
||
|
Var.tot.S-Blocs 1 |
5 |
9,85 |
10,42 |
||
|
Var.residuelle 2 |
12 |
0,95 |
0,97 |
14,10% |
|
|
Var.totale |
191 |
8,04 |
|||
|
Var.facteur 3 (P) |
7 |
42,57 |
792,65 |
||
|
Var.inter.M.O*P |
7 |
9,30 |
53,46 |
||
|
Var.inter.D*P |
21 |
4,76 |
12,35 |
||
|
Var.inter.M.O*D*P |
21 |
3,45 |
9,03 |
||
|
Var.tot.S-Blocs 2 |
23 |
41,68 |
163,07 |
||
|
Var.residuelle 2 |
112 |
0,37 |
0,61 |
8,80% |
Tableau des groupes homogènes du Ca++ échangeable
|
Facteur |
Groupes homogènes |
|||
|
M.O.B |
M.O.O |
|||
|
Matière organique (M.O) |
b |
a |
||
|
Dose (D) |
D0 |
d |
d |
|
|
D1 |
c |
c |
||
|
D2 |
b |
b |
||
|
D3 |
a |
a |
||
|
Prélèvements (P) |
P1 |
d |
e |
|
|
P2 |
cd |
e |
||
|
P3 |
b |
d |
||
|
P4 |
a |
cd |
||
|
P5 |
b |
b |
||
|
P6 |
c |
a |
||
|
P7 |
d |
c |
||
|
P8 |
e |
f |
||
|
Interaction |
D0 |
P1 à P8 |
a |
a |
|
D1 |
P1+P2+P8 |
a |
a |
|
|
P3+P4+P5 |
a |
b |
||
|
P6+P7 |
b |
a |
||
|
D2 |
P2+P3 |
a |
a |
|
|
P1+P4+P5+P6+P7+P8 |
b |
a |
||
|
D3 |
P1+P2+P3+P4 |
a |
a |
|
|
P5 à P8 |
b |
a |
||
96
Annexe
Annexe (06)
Tableau d'analyse de variance du Mg++ échangeable
|
D.D.L |
C.M |
TEST. F |
E.T |
C.V |
|
|
Var.tôt.S-Bloc1 |
5 |
0,36 |
|||
|
Var.facteur1 (M.O) |
1 |
1,76 |
200,20 |
||
|
Var.Blocs |
2 |
0,01 |
1,45 |
||
|
Var.residuelle 1 |
2 |
0,01 |
0,09 |
7,60% |
|
|
Var.tôt.s-bloc2 |
23 |
0,32 |
|||
|
Var.facteur 2 (D) |
3 |
1,58 |
73,15 |
||
|
Var.inter.M.O*D |
3 |
0, 15 |
6,86 |
||
|
Var.tot.S-Blocs 1 |
5 |
0,36 |
16,63 |
||
|
Var.residuelle 2 |
12 |
0,02 |
0,15 |
12,40% |
|
|
Var.totale |
191 |
0,07 |
|||
|
Var.facteur 3 (P) |
7 |
0,58 |
357,32 |
||
|
Var.inter.M.O*P |
7 |
0,09 |
56,26 |
||
|
Var.inter.D*P |
21 |
0,02 |
13,78 |
||
|
Var.inter.M.O*D*P |
21 |
0,01 |
7,66 |
||
|
Var.tot.S-Blocs 2 |
23 |
0,32 |
195,20 |
||
|
Var.residuelle 2 |
112 |
0,00 |
0,04 |
3,40% |
Tableau des groupes homogènes du Mg++ échangeable
|
Facteur |
Groupes homogènes |
|||
|
M.O.B |
M.O.O |
|||
|
Matière organique (M.O) |
b |
a |
||
|
Dose (D) |
D0 |
b |
c |
|
|
D1 |
a |
b |
||
|
D2 |
a |
ab |
||
|
D3 |
a |
a |
||
|
Prélèvements (P) |
P1 |
b |
b |
|
|
P2 |
bc |
a |
||
|
P3 |
ab |
a |
||
|
P4 |
a |
a |
||
|
P5 |
c |
a |
||
|
P6 |
e |
a |
||
|
P7 |
e |
c |
||
|
P8 |
f |
d |
||
|
Interaction |
D0 |
P1à P8 |
a |
a |
|
D1 |
P2+P3+P8 |
a |
a |
|
|
P1+ P4 à P7 |
b |
a |
||
|
D2 |
P1 à P7 |
b |
a |
|
|
P8 |
a |
a |
||
|
D3 |
P1 à P7 |
b |
a |
|
|
P8 |
a |
a |
||
97
Annexe
Annexe (07)
Tableau d'analyse de variance du Na+ échangeable
|
D.D.L |
C.M |
TEST. F |
E.T |
C.V |
|
|
Var.tôt.S-Bloc1 |
5 |
0,11 |
|||
|
Var.facteur1 (M.O) |
1 |
0,46 |
124,92 |
||
|
Var.Blocs |
2 |
0,06 |
15,31 |
||
|
Var.residuelle 1 |
2 |
0,00 |
0,06 |
2,90% |
|
|
Var.tôt.s-bloc2 |
23 |
0,29 |
|||
|
Var.facteur 2 (D) |
3 |
0,01 |
428,98 |
||
|
Var.inter.M.O*D |
3 |
0,01 |
1,67 |
||
|
Var.tot.S-Blocs 1 |
5 |
0,11 |
24,49 |
||
|
Var.residuelle 2 |
12 |
0,00 |
0,07 |
3,30% |
|
|
Var.totale |
191 |
0,08 |
|||
|
Var.facteur 3 (P) |
7 |
0,93 |
341,27 |
||
|
Var.inter.M.O*P |
7 |
0,01 |
4,82 |
||
|
Var.inter.D*P |
21 |
0,04 |
13,96 |
||
|
Var.inter.M.O*D*P |
21 |
0,01 |
14,45 |
||
|
Var.tot.S-Blocs 2 |
23 |
0,29 |
107,22 |
||
|
Var.residuelle 2 |
112 |
0,00 |
0,05 |
2,50% |
Tableau des groupes homogènes du Na+ échangeable
|
Facteur |
Groupes homogènes |
|||
|
M.O.B |
M.O.O |
|||
|
Matière organique (M.O) |
b |
a |
||
|
Dose (D) |
D0 |
d |
d |
|
|
D1 |
c |
c |
||
|
D2 |
b |
b |
||
|
D3 |
a |
a |
||
|
Prélèvements (P) |
P1 |
b |
d |
|
|
P2 |
b |
c |
||
|
P3 |
a |
bc |
||
|
P4 |
a |
ab |
||
|
P5 |
b |
a |
||
|
P6 |
b |
c |
||
|
P7 |
c |
e |
||
|
P8 |
d |
f |
||
|
Interaction |
D0 |
P1+P6 |
a |
a |
|
P2+P3+P4+P5+P7+P8 |
b |
a |
||
|
D1 |
P2à P7+P8 |
a |
a |
|
|
P1+P6 |
b |
a |
||
|
D2 |
P3+P4 |
b |
a |
|
|
P1+P2+ P5 à P8 |
b |
a |
||
|
D3 |
P3+P4+P7 |
a |
a |
|
|
P1+P2+P5+P6+P8 |
b |
a |
||
98
Annexe
Annexe (08)
Tableau d'analyse de variance du K+ échangeable
|
D.D.L |
C.M |
TEST. F |
E.T |
C.V |
|
|
Var.tôt.S-Bloc1 |
5 |
0,06 |
|||
|
Var.facteur1 (M.O) |
1 |
0,29 |
87,49 |
||
|
Var.Blocs |
2 |
0,00 |
1,33 |
||
|
Var.residuelle 1 |
2 |
0,00 |
0,06 |
13,10% |
|
|
Var.tôt.s-bloc2 |
23 |
0,05 |
|||
|
Var.facteur 2 (D) |
3 |
0,22 |
166,56 |
||
|
Var.inter.M.O*D |
3 |
0,02 |
10,79 |
||
|
Var.tot.S-Blocs 1 |
5 |
0,06 |
31,81 |
||
|
Var.residuelle 2 |
12 |
0,00 |
0,04 |
9,90% |
|
|
Var.totale |
191 |
0,01 |
|||
|
Var.facteur 3 (P) |
7 |
0,09 |
250,47 |
||
|
Var.inter.M.O*P |
7 |
0,01 |
34,10 |
||
|
Var.inter.D*P |
21 |
0,00 |
8,81 |
||
|
Var.inter.M.O*D*P |
21 |
0,00 |
5,38 |
||
|
Var.tot.S-Blocs 2 |
23 |
0,05 |
123,38 |
||
|
Var.residuelle 2 |
112 |
0,00 |
0,02 |
4,40% |
Tableau des groupes homogènes du K+ échangeable
|
Facteur |
Groupes homogènes |
|||
|
M.O.B |
M.O.O |
|||
|
Matière organique (M.O) |
b |
a |
||
|
Dose (D) |
D0 |
c |
c |
|
|
D1 |
b |
b |
||
|
D2 |
ab |
b |
||
|
D3 |
a |
a |
||
|
Prélèvements (P) |
P1 |
c |
b |
|
|
P2 |
b |
a |
||
|
P3 |
a |
a |
||
|
P4 |
a |
a |
||
|
P5 |
d |
a |
||
|
P6 |
e |
ab |
||
|
P7 |
e |
c |
||
|
P8 |
f |
d |
||
|
Interaction |
D0 |
P1 à P8 |
a |
a |
|
D1 |
P3+P8 |
a |
a |
|
|
P1+P2+P4+P5+P6+P7 |
b |
a |
||
|
D2+D3 |
P1 à P7 |
b |
a |
|
|
P8 |
a |
a |
||
99

