|
République Algérienne Démocratique
et Populaire
Ministère de l'Enseignement Supérieur et de la
Recherche Scientifique
Institut des Sciences de la Mer et de
l'Aménagement du Littoral

Mémoire de Fin d'Etudes
En vue de l'obtention
du Dipl8me d'Etudes Universitaires Appliquées
en Sciences de la
Mer
Theme :
DETERMINATION
DE LA POLLUTION RESIDUELLE
D'UNE STATION
D'EPURATION
PAR LAGUNAGE NATUREL
"CAS DE LA LAGUNE DE BENI-MESSOUS"
Réalisé par : Encadré :
Mr TARMOUL Fateh Mr DRICHE M.
Melle SADI Meriem
Juillet 2007
emerciements
Avant tout, nous remercions Allah, Dieu le
Miséricordieux, l'Unique,
le Puissant, .... pour son guide et sa
protection ;
Nous tenons a remercier vivement Mr Driche, pour la
confiance
qu'il nous a accordé en acceptant de nous encadrer
;
pour sa disponibilité tout au long de l'élaboration de ce
mémoire
de fin d'études, pour son aide, ses critiques et ses
suggestions,
qui ont été pour nous d'un grand apport ;
Nous exprimons notre gratitude a l'ensemble de nos
enseignants
qui ont si soigneusement partagé leurs
connaissances
en sciences de la mer, passion qui nous a tous réuni a
l'ISMAL ;
Sans oublier tous les autres employés de
l'institut,
particulièrement ceux de la bibliothèque ;
Nos remerciements vont aussi, a Mr Mechti,
Mr et Mme Belkacemi
et Mr Makhzoumi du
Ministère des Ressources en Eau ; a Mr Lazili
et
Mme Bouchefer de l'Office Nationale de l'Assainissement (ONA)
;
qui nous ont tous si bien accueilli et aimablement aidé ;
Un grand merci, pour Mesdames, Djermane K., Himrane S. et
Ouakli N.
du laboratoire central de l'O NA qui n'ont ménagé
aucun effort
pour nous assister durant notre stage au sein de leur
établissement,
ainsi que pour leur hospitalité et leurs
encouragements ;
Enfin, que tous ceux qui ont contribué de prés ou
de loin a la réalisation
de ce mémoire, puissent trouver ici,
toute notre reconnaissance.
atert & Aeriem
Did&cace/3
A mes tres, tres chers parents, source d'amour et
d'affection ;
A mes tres chers sceurs et frere, Nabila, Fatma, Namia, Amel,
El Djouher
et Moussa qui comptent énormément pour moi
;
A Toufik et Hacene ;
Aux boutchoux, neveux, Hani et Amine Younes et niece,
Amira ;
A mes cousins, Sid Ahmed, Madina, Soraya, Nadia, notre Mohamed
et
leur papa et maman ;
A ma deuxième Famille, Zahia, Nacer, Amina et
Amir ;
A tous mes autres proches ;
A mes chers amis Said, Walid, Walido, Fethi, Fethi,
Imed, Hamid, Khaled,
Youcef, Mohamed, Noufel, Sid Ali, Faysal, Ferhat,
Mounir, Ibrahim, Sid Ali,
Rachid, Taha, Redouane, Kamel, Ramdan, Billel,
Djamel, Hamza, Ibrahim,
Mohamed, Kamel, Hacene, Mourad, Mehdi, Hamza, Abd
Essamed,
Redouane, Samir, Lotfi, Mohamed, Walid, Nabil, Lakhder, Amine,
Abdou,
Oussama, Ali, Krimo, Ibrahim, Lounes, Larbi, Lotfi, Bachir,
Aboubeker
Karima, Faiza, Nawel, Amina 1, Amina 2, Amina 3, Nadjet,
Narimane,
Fayrouz, Meriem, ... mais surtout, surtout a Lamine, Mehdi et
Imene
a qui je tient plus particulièrement ; j'espere que je n'ai
oublié personne ;
A toutes les personnes qui m'ont soutenu et
encouragé
tout au long de cette année ;
A vous tous qui m'aimez ;
Je dédie ce modeste travail.

Did&cace/3
Je dedie ce memoire :
A mes tres chers parents qui
veillent a ma reussite et bonheur ;
A mon unique sceur, Yasmine
A mes deux freres
adores, Charif et Lokman ;
A tous mes autres proches ;
A mes chers amis, Meriem, Soumeya, Imène,
Nadjet, Amina, Narimane,
Adnane, Walid, Samir et Tarik ainsi
qu,à tous ceux qui me connaissent
a l,ISMAL et
avec qui j,ai passé trois années inoubliables
;
A Fateh, mon binome avec qui travail rime avec
serieux
et bonne humeur ;
Tous simplement, a tous ceux que j,aime et
qui m,aiment.
keriem
5ommdirP
Introduction générale 01
1ère PARTIE : ÉTUDE BIBLIOGRAPHIQUE
Chapitre 1 : Généralités sur les eaux
usées
Introduction 03
1.1. Définition 03
1.2. Origine et composition des eaux usées 03
1.2.1. les eaux usées domestiques 03
1.2.2. les eaux industrielles 03
1.2.3. les eaux agricoles 04
1.2.4. les eaux pluviales 04
1.3. Caractéristiques des eaux usées 04
1.3.1. Les paramètres physico-chimiques 04
1.3.1.1. La température 04
1.3.1.2. Le potentiel d'Hydrogène (pH) 05
1.3.1.3. La turbidité et les matières en suspension
05
1.3.1.4. La demande biologique en oxygène (DBO5) 06
1.3.1.5. La demande chimique en oxygène (DCO) 06
1.3.1.6. Les matières oxydables (MO) 06
1.3.1.7. Le carbone organique total (COT) 06
1.3.1.8. L'azote et le phosphore 07
1.3.1.8.1. L'azote 07
1.3.1.8.2. Le phosphore 08
1.3.1.9. Les oligoéléments et les toxiques
minéraux 08
1.3.2. Les paramètres bactériologiques 08
1.3.2.1. Les coliformes totaux (CT) 08
1.3.2.2. Les coliformes fécaux (CF) 09
1.3.2.3. Les Streptocoques fécaux 09
1.3.2.4. Les Clostridiums sulfito-réducteurs 09
1.4. L'équivalent habitant 10
1.5. Les normes algériennes de rejet d'effluents 10
Conclusion 10
Chapitre 2 : Traitement des eaux usées
Introduction 12
2.1. Les étapes et procédés de traitement
des eaux usées 12
2.1.1. Les prétraitements 12
2.1.1.1. Dégrillage 12
2.1.1.2. Dessablage 13
2.1.1.3. Dégraissage - Déshuilage 13
2.1.2. Les traitements primaires 13
2.1.2.1. Coagulation - Floculation 13
2.1.2.2. Décantation 13
2.1.2.3. Filtration 14
2.1.3. Les traitements secondaires (Biologiques) 14
2.1.3.1. Traitements anaérobies 14
2.1.3.2. Traitements aérobies 14
2.1.3.2.1. Les lits bactériens 15
2.1.3.2.2. Les boues activées 15
2.1.3.2.3. Le lagunage 15
2.1.4. Les traitements tertiaires 15
2.1.4.1. L'élimination de l'azote 16
2.1.4.2. L'élimination du phosphore 16
2.1.4.3. La désinfection 17
2.1.4.4. Le traitement des odeurs 17
2.2. Réutilisation des eaux usées 17
2.2.1. L'industrie 17
2.2.1.1. Lavage et transport industriel des matériaux
17
2.2.1.2. Refroidissement industriel 18
2.2.2. L'irrigation 18
2.2.3. Les usages municipaux 18
2.3. L'épuration des eaux usées en Algérie
18
2.3.1. Volumes des eaux usées en 2004 18
2.3.2. Programme des stations d'épuration pour le court
terme (2006-2010) 19
Conclusion 21
Chapitre 3 : Le lagunage naturel
Introduction 23
3.1. Définition 23
3.2. Principe de fonctionnement 23
3.3. Les différents types de lagunage 24
3.3.1. Le lagunage naturel 24
3.3.1.1. Étangs anaérobies 25
3.3.1.2. Étangs aérobies 25
3.3.1.3. Étangs facultatifs 25
3.3.2. Le lagunage aéré 26
3.4. Influence des conditions climatiques sur les performances du
lagunage 26
3.4.1. La durée du jour et l'intensité de
l'ensoleillement 26
3.4.2. La température 26
3.4.3. Le régime et l'orientation des vents dominants dans
la région 26
3.4.4. L'évaporation 27
3.4.5. La pluviométrie 27
3.5. Exploitation du lagunage 27
3.6. Contraintes d'exploitation 27
3.7. Avantages et inconvénients du lagunage 28
3.7.1. Avantages 28
3.7.2. Inconvénients 28
Conclusion 28
2ème PARTIE : ÉTUDE EXPÉRIMENTALE
Chapitre 4 : Description de la zone d'étude
Introduction 29
4.1. Étude du lagunage naturel de Béni-Messous
29
4.1.1. Localisation géographique 29
4.1.2. Dimensionnement et caractéristiques des lagunes
30
4.1.3. Caractéristiques des eaux usées 31
4.1.4. Temps de séjour dans les lagunes 31
4.2. Étude géologique de la région de
Béni-Messous 32
4.3. Étude hydrologique de la région de
Béni-Messous 32
4.4. Étude démographique de la population
concernée 32
4.5. Description des conditions climatiques 33
4.5.1. Température 33
4.5.2. Ensoleillement 34
4.5.3. Vents 34
4.5.4. Pluviométrie 35
4.5.5. Évaporation 36
Conclusion 36
Chapitre 5 : Matériels et méthodes
Introduction 37
5.1. Prélèvement et échantillonnage 37
5.2. Conditionnement des échantillons 37
5.3. Conservation des échantillons 38
5.4. Application au lagunage naturel de Béni-Messous
38
5.5. Analyses et modes opératoires 39
5.5.1. Paramètres insitu 39
5.5.1.1. La température de l'eau 39
5.5.1.2. Le potentiel d'Hydrogène (pH) 39
5.5.2. Paramètres mesurés au laboratoire 40
5.5.2.1. Matières en suspension (MES) 40
5.5.2.2. Demande chimique en oxygène (DCO) 42
5.5.2.3. Demande biologique en oxygène (DBO5) 43
5.6. Classes de qualité des eaux 44
Conclusion 45
Chapitre 6 : Résultats et interprétations
Introduction 46
6.1. La température 46
6.2. Le potentiel d'hydrogène (pH) 47
6.3. Les matières en suspension (MES) 47
6.4. Détermination de la pollution résiduelle
49
6.4. La demande chimique en oxygène (DCO) 49
6.5. La demande biologique en oxygène (DBO5) 51
6.7. La qualité de l'eau rejetée par la lagune de
Béni-Messous ...52
Conclusion 52
Conclusion générale 53
Bibliographie
Annexes
Liste des tableaux et des figures
Tableau 1 : Les valeurs limites des paramètres de
rejet dans un milieu récepteur 11
Tableau 2 : Volume des eaux usées par région
hydrographique - 2004 19
Tableau 3 : Répartition spatiale des rejets des
eaux usées (amont des barrages,
rejets en mer, rejets en chott et sebkhas) 19
Tableau 4 : Nombre et état des STEP par type de
procédé 21
Tableau 5 : Dimensions et caractéristiques des
quatre bassins du lagunage naturel
de Béni-Messous 31
Tableau 6 : Répartition annuelle des vents sur huit
directions dans la région
de Béni-Messous (ONM, 1960-2004) 35
Tableau 7 : Valeurs typiques de DCO 43
Tableau 8 : Valeurs typiques de DBO5 44
Tableau 9 : Classement des eaux de surfaces stagnantes et
courantes d'après leur
qualité 45
Tableau 10 : Températures, profondeurs et surface
de contact air-eau des quatre

bassins du lagunage de Béni-Messous 46
Figure 1 : Origines, traitements et devenirs des eaux
usées 22
Figure 3 : Schéma d'un lagunage à trois
bassins 24
Figure 4 : Localisation géographique du lagunage
naturel de Béni-Messous 29
Figure 5 : Photo satellite du lagunage naturel de
Béni-Messous 30
Figure 6 : Schéma du lagunage naturel de
Béni-Messous 30
Figure 7 : Profil de variation des températures
moyennes de l'air 33
Figure 8 : Profil de l'ensoleillement mensuel moyen dans
la région de Béni-Messous 34
Figure 9 : Profil de variation de l'ensoleillement 34
Figure 10 : Répartition annuelle des vents sur huit
directions de la région
de Béni-Messous (en %) 35
Figure 11 : Précipitations annuelles dans la
région de Béni-Messous 35
Figure 12 : Profil
évaporations-précipitations de la région de
Béni-Messous 36
Figure 13 : Températures des bassins de la station
d'épuration par lagunage naturel
de Béni-Messous 46
Figure 14 : Potentiel d'hydrogène (pH) des bassins
de la station d'épuration
par lagunage naturel de Béni-Messous 47
Figure 15 : Teneur en matières en suspension (MES)
dans les bassins de la station d'épuration du lagunage de
Béni-Messous 48
Figure 16 : Rendements d'épuration en MES des
quatre bassins de la station
d'épuration par lagunage naturel de Béni-Messous
48
Figure 17 : DCO des bassins de la station
d'épuration par lagunage naturel
de Béni-Messous 50
Figure 18 : Rendement en DCO des bassins de la station
d'épuration par lagunage
naturel de Béni-Messous 50
Figure 19 : DBO5 des bassins de la station
d'épuration par lagunage naturel
de Béni-Messous 51

Parce qu'elle est source de vie, l'eau est fragile
Parce
qu'elle est source de prospérité, l'eau est
convoitée
Parce qu'elle semble inépuisable, l'eau est
gaspillée
Parce qu'elle semble inaltérable, l'eau est
polluée




Introduc:tion I3~n~riEII~

L'Algérie est un pays riche en ressources naturelles
telles que les ressources fossiles et les minerais de phosphates et de fer.
Cependant, elle accuse un important déficit en ressources hydriques.
En effet, avec l'expansion des villes, l'industrialisation et
l'évolution des modes de consommation, en sus, d'un climat de plus en
plus aride que connais le pays, les eaux potables s'épuisent plus
rapidement, augmentant le volume des eaux usées collectées de
plus de 35 Hm3 chaque année pour atteindre environs 689
Hm3 en 20101. Actuellement, les eaux usées ne sont
épurées qu'à 40 %2 et rejetées, le plus
souvent, sans traitements et de façon directe en milieu naturel.
Face à la pénurie d'eau, due essentiellement
à la baisse régulière du volume des précipitations
depuis ces dernières décennies, et dans un souci de
préservation des ressources d'eau encore saines et de protection de
l'environnement et de la santé publique, l'Algérie adopte alors,
un programme riche en matière d'épuration des eaux usées
par la mise en service, à l'horizon 2010, de 194 stations
d'épuration3.
Grâce à des procédés
physico-chimiques ou biologiques, ces stations ont pour rôle de
concentrer la pollution contenue dans les eaux usées sous forme de
résidus appelés boues, valorisable en agriculture et de rejeter
une eau épurée répondant à des normes bien
précises, qui trouve quant-à-elle, une réutilisation dans
l'irrigation, l'industrie et les usages municipaux.
Les procédés d'épuration utilisés
en Algérie, dont l'objectif principal est d'éliminer la pollution
organique sont à4 :
- 54 % procédé à boues activées ;
- 36 % lagunage naturel ;
- 10 % lagunage aéré.
Parallèlement au procédé à boues
activées et au lagunage aéré, qui sont de caractère
intensif, le lagunage naturel présente par ses nombreux avantages, une
alternative idéale pour notre pays, en réunissant toutes les
conditions favorables à son bon fonctionnement.
C'est dans le but de l'étude de ce
procédé biologique et peu onéreux, faisant intervenir les
micro-algues et les bactéries dans l'épuration des eaux
usées, que s'inscrit ce présent mémoire où nous
essayons de détailler, un tant soit peu, le principe de fonctionnement
d'une station par lagunage naturel avec l'évaluation de ses
performances.
1 3 Source : Rapport : Étude de réutilisation
des eaux usées épurées à des fins agricoles ou
autres sur tout le territoire national, Mission 1 : Reconnaissance et collecte
des données de base / Établi par la Direction de l'Assainissement
et de la Protection de l'Environnement (DAPE)/ Ministère des Ressources
en Eau (MRE) : Juillet 2006.
2 4 Source : Idem, Mission 2 : Schéma directeur/ idem/
idem : Février 2007.


Le développement intense des micro-algues dans les
différents bassins d'une station d'épuration par lagunage naturel
génère une forte production de biomasse, communément,
considérée avec la pollution. Il s'agit alors, dans ce document,
d'évaluer la pollution résiduelle qui correspond à la part
additionnelle de pollution.
Nous prenons, également, soin de décrire les
principaux paramètres de pollution des eaux usées ainsi que leurs
analyses.
Comme étude de cas, Nous avons choisi de travailler sur
la lagune de Béni-Messous s'implantant en parallèle à
l'Oued de Béni-Messous, à 5 km de son embouchure dans le littoral
algérois (baie d'El Djamila).
Notre travail se présente en deux volets :
· Une première partie bibliographique qui regroupe
le nécessaire des connaissances théoriques en rapport avec notre
thème et cela en trois chapitres :
> Le premier chapitre est consacré, d'une part,
à la connaissance de la constitution et l'origine des eaux usées,
et d'autre part, à la description des paramètres de pollution qui
les caractérisent et aux normes de rejets en vigueur en
Algérie.
> Le second expose les divers traitements que doivent
subirent les eaux usées avant d'être rejetées en milieu
naturel, les différents usages possibles des eaux usées
traitées et enfin l'état général de
l'épuration en Algérie.
> Le troisième chapitre présente le
procédé du lagunage naturel à travers sa
définition, son principe de fonctionnement, ses différents types,
son exploitation et ses avantages et inconvénients.
· Une deuxième partie expérimentale qui
s'intéresse à l'étude du cas de la lagune de
Béni-Messous, en trois autres chapitres :
> La présentation de la zone d'étude, ainsi
que des conditions climatiques qui influent sur le bon fonctionnement du
lagunage font l'objet du quatrième chapitre.
> Le cinquième chapitre est consacré aux
méthodes d'analyse des paramètres de pollution globaux :
température, pH, MES, DCO et DBO5 des eaux usées des bassins de
la station d'épuration par lagunage naturel de Béni-Messous.
> Le sixième chapitre présente les
résultats des analyses et leurs interprétations. Nous terminerons
par une conclusion générale.




Introduction :
Les cours d'eau ont une capacité naturelle
d'autoépuration. Celle-ci a pour effet de consommer de l'oxygène
; ce qui n'est donc pas sans conséquences sur la faune et la flore
aquatiques. Lorsque l'importance d'un rejet excède cette
capacité, la détérioration de l'environnement peut
être durable. Il est donc indispensable d'épurer les eaux
usées avant de les rejeter en milieu naturel.
En effet, les zones privées d'oxygène par la
pollution entrainent la mort de la faune et de la flore ou créent des
barrières infranchissables, empêchant notamment la migration des
poissons. La présence excessive de phosphates, en particulier, favorise
le phénomène d'eutrophisation ; c'est-à-dire, la
prolifération d'algues qui nui à la faune aquatique, peut rendre
la baignade dangereuse et perturbe la production d'eau potable.
1.1. Définition :
Les eaux usées sont toutes les eaux qui parviennent
dans les canalisations d'eaux usées dont les propriétés
naturelles sont transformées par les utilisations domestiques, les
entreprises industrielles, agricoles et autres. On englobe, aussi, les eaux de
pluie qui s'écoulent dans ces canalisations (BLIEFERT et PERRAUD,
2001).
1.2. Origine et composition des eaux usées :
Suivant l'origine des substances polluantes, on distingue quatre
catégories d'eaux usées :
1.2.1. Les eaux usées domestiques :
Elles proviennent des différents usages domestiques de
l'eau. Elles sont essentiellement porteuses de pollution organique. Elles se
répartissent en eaux ménagères, qui ont pour origine les
salles de bains et les cuisines, et sont généralement
chargées de détergents, de graisses, de solvants, de
débris organiques,
etc. et en eaux vannes ; il s'agit des
rejets des toilettes chargés de diverses matières organiques
azotées et de germes fécaux (GOMELLA et GUERREE, 1978).
1.2.2. Les eaux industrielles :
Elles sont très différentes des eaux
usées domestiques. Leurs caractéristiques varient d'une industrie
à l'autre. En plus de matières organiques, azotées ou
phosphorées, d'après GAUJOUS (1995), elles peuvent
également contenir :
· des graisses (industries agroalimentaires,
équarrissage) ;
· des hydrocarbures (raffineries) ;
· des métaux (traitements de surface,
métallurgie) ;
· des acides, des bases et divers produits chimiques
(industries chimiques divers, tanneries) ;
· de l'eau chaude (circuit de refroidissement des centrales
thermiques) ;
· des matières radioactives (centrales
nucléaires, traitement des déchets radioactifs).
Dans certains cas, avant d'être rejetées dans
les réseaux de collecte, les eaux industrielles doivent faire l'objet
d'un prétraitement de la part des industriels. Elles ne sont
mêlées aux eaux domestiques que lorsqu'elles ne présentent
plus de danger pour les réseaux de collecte et ne perturbent pas le
fonctionnement des usines de dépollution.
1.2.3. Les eaux agricoles :
L'agriculture est une source de pollution des eaux qui n'est
pas du tout négligeable car elle apporte les engrais et les pesticides.
Elle est la cause essentielle des pollutions diffuses (BONTOUX, 1993).
Les épandages d'engrais nitratés et
phosphatés, sous une forme ou en quantité, telle qu'ils ne
seraient pas finalement retenus par le sol et assimilés par les plantes,
conduisent à un enrichissement en matières azotées ou
phosphatées des nappes les plus superficielles et des eaux des cours
d'eau ou des retenues. Parmi les polluants d'origine agricole, il faut tenir
compte aussi des détergents se dispersant lors des applications de
traitement des cultures (GOMELLA et GUERREE, 1978).
1.2.4. Les eaux pluviales :
Elles peuvent, elles aussi, constituer une source de
pollution importante des cours d'eau, notamment pendant les périodes
orageuses. L'eau de pluie se charge d'impuretés au contact de l'air
(fumées industrielles), puis, en ruisselant, des résidus
déposés sur les toits et les chaussées des villes (huiles
de vidange, carburants, résidus de pneus et métaux lourds...)
(BONTOUX, 1993).
Dans les zones urbaines, les surfaces construites rendent les
sols imperméables et ajoutent le risque d'inondation à celui de
la pollution.
1.3. Caractéristiques des eaux usées :
L'évaluation de la qualité de l'eau
nécessite de nombreuses analyses, incluant le dosage de multiples
paramètres physico-chimiques et bactériologiques. Ces analyses
sont réalisées par des méthodes dont les protocoles sont
bien définis.
1.3.1. Les paramètres physico-chimiques :
Selon GAUJOUS (1995), la pollution résulte de
l'introduction dans un milieu de substances conduisant à son
altération. Elle se traduit généralement par des
modifications des caractéristiques physico-chimiques du milieu
récepteur. La mesure par analyse de ces derniers (au niveau du rejet, du
milieu naturel ou du milieu pollué) permet de l'étudier.
1.3.1.1. La température :
La température est un facteur écologique
important du milieu. Son élévation peut perturber fortement la
vie aquatique (pollution thermique). Certains rejets présentent des
écarts de température importants avec le milieu récepteur
: ce sont par exemple, les eaux de refroidissement des centrales
nucléaires thermiques induisant ainsi une forte perturbation du milieu.
La température est mesurée par thermosonde (ou par
thermomètre) (GAUJOUS, 1995).
Il est important de connaitre la température de l'eau
avec précision. En effet, celle-ci joue un rôle dans la
solubilité des sels et surtout des gaz, dans la détermination du
pH, pour la connaissance de l'origine de l'eau et des mélanges
éventuels, etc. (RODIER et al, 1996).
1.3.1.2. Le potentiel d'Hydrogène (pH) :
Le pH est un paramètre qui permet de mesurer
l'acidité, l'alcalinité ou la basicité d'une eau (GOMELLA
et GUEREE, 1978). Sa mesure doit s'effectuer sur place de
préférence par la méthode potentiométrique. La
mesure électrique, quoique délicate, peut seule donner une valeur
exacte, car elle est indépendante du potentiel d'oxydoréduction,
de la couleur du milieu, ou de la turbidité et des matières
colloïdales (RODIER et al, 1996).
En milieu côtier et estuarien, certains rejets
industriels ou les apports d'eaux de ruissellement sont la cause de variation
du pH qui s'avère être, dans ce cas, un indice de pollution
(AMINOT et CHAUSSEPIED, 1983).
Les organismes sont très sensibles aux variations du
pH, et un développement correct de la faune et de la flore aquatique
n'est possible que si sa valeur est comprise entre 6 et 9.
L'influence du pH se fait également ressentir par le
rôle qu'il exerce sur les autres éléments comme les
métaux dont il peut diminuer ou augmenter la disponibilité et
donc la toxicité.
1.3.1.3. La turbidité et les matières en
suspension :
La turbidité est inversement proportionnelle à la
transparence de l'eau. Elle est mesurée :
· soit visuellement par la hauteur d'eau à travers
laquelle on ne distingue plus un objet (disque de Secchi, fil de platine) ;
elle est alors exprimée en mètre.
· soit électroniquement
(néphélométrie) par comparaison avec une gamme de solution
de référence (silice, mastic, formazine) ; elle est alors
exprimée en mg/l de silice, de mastic, ... ou en unité (NTU,
Nephelometric Turbidity Unit, ou JTU -Jackson ou FTU, Formazine-) (GAUJOUS,
1995).
La turbidité varie suivant les matières en
suspension (MES) de l'eau :
La détermination des matières en suspension
(MES) est essentielle pour évaluer la répartition de la charge
polluante entre pollution dissoute et pollution sédimentable, car le
devenir de ces deux composantes est très différent, tant dans le
milieu naturel que dans les systèmes d'épuration.
Dans une eau usée urbaine, prés de 50 % de la
pollution organique se trouve sous forme de MES. Les résultats pour les
eaux usées industrielles sont très variables, il est de
même pour les eaux naturelles où la nature des MES est souvent
minérale et leur taux est relativement bas, sauf en période de
crue des cours d'eau.
La composition des MES peut être
appréciée par analyse directe : plus souvent, elle est obtenue
par différence des caractéristiques des eaux brutes et des eaux
filtrées. Les erreurs sur les valeurs résultantes sont alors
élevées (BONTOUX, 1993). Les MES sont exprimées en
mg/l.
1.3.1.4. La demande biologique en oxygène (DBO5) :
La demande biochimique en oxygène DBO, exprimée
en mg d'oxygène par litre, permet l'évaluation des
matières organiques biodégradables dans les eaux (BONTOUX, 1993).
Plus précisément, ce paramètre mesure la quantité
d'oxygène nécessaire à la destruction des matières
organiques grâce aux phénomènes d'oxydation par voie
aérobie.
Pour la mesurer, on prend comme référence la
quantité d'oxygène consommée au bout de 5 jours ; c'est la
DBO5.
BERNE et CORDONNIER (1991) définissent la DBO5 comme
étant la quantité d'oxygène consommée par les
bactéries, à 20°C à l'obscurité et pendant 5
jours d'incubation d'un échantillon préalablement
ensemencé, temps qui assure l'oxydation biologique d'une fraction de
matière organique carbonée.
La DBO5 est un paramètre intéressant pour
l'appréciation de la qualité des eaux : dans les eaux pures elle
est inférieure à 1 mg d'(O2)/l, et quand elle dépasse les
9 mg/l l'eau est considérée comme étant impropre (GOMELLA
et GUERREE, 1978).
1.3.1.5. La demande chimique en oxygène (DCO) :
La demande chimique en oxygène (DCO), exprimée
en mg d'(O2)/l, correspond à la quantité d'oxygène
nécessaire pour la dégradation par voie chimique est dans des
conditions définies de la matière organique ou inorganique
contenue dans l'eau (GROSCLAUDE, 1999). Elle représente donc, la teneur
totale de l'eau en matières oxydables.
1.3.1.6. Les matières oxydables (MO) :
C'est un paramètre utilisé par les agences de
l'eau pour caractériser la pollution organique de l'eau, il se
définit à partir de la DBO5 et de la DCO selon la formule
suivante (BADIA-GONDARD, 2003) :
MO = (2×DBO5 + DCO)/3
1.3.1.7. Le carbone organique total (COT) :
Le carbone organique est constitué d'une grande
diversité de composés organiques à plusieurs états
d'oxydation, dont certains sont susceptibles d'être oxydés par des
procédés chimiques ou biologiques. Ces fractions sont
caractérisées par la demande chimique en oxygène (DCO) et
la demande biologique en oxygène (DBO).
Certaines matières organiques échappent
à ces mesures ; dans ce cas, le dosage du COT est mieux adapté.
Il est indépendant de l'état d'oxydation de la matière
organique et ne mesure pas les éléments inorganiques tels que
l'azote et l'hydrogène qui peuvent êtres pris en compte par la DCO
et la DBO.
La détermination porte sur les composés
organiques fixés ou volatils, naturels ou synthétiques,
présents dans les eaux résiduaires (cellulose, sucres, huiles,
etc.). Suivant que l'eau a été préalablement
filtrée ou non, on obtiendra le carbone dissous (COD) ou le carbone
total (COT). Cette mesure permet de faciliter l'estimation de la demande en
oxygène liée aux rejets, et d'établir
éventuellement une corrélation avec la DBO et la DCO.
Les méthodes de dosage du carbone organique utilisent
toutes le même principe, qui consiste à oxyder le carbone
organique en dioxyde de carbone. Cette oxydation peut être obtenue par
combustion, irradiation UV, oxydation chimique ou par tous autres
procédés appropriés. Le dioxyde de carbone est ensuite
mesuré, soit directement, par un analyseur infrarouge ou par toutes
méthodes covenant à son dosage, soit réduit en
méthane et analysé par un décanteur à ionisation de
flamme (RODIER et al, 1996).
1.3.1.8. L'azote et le phosphore :
Les teneurs en azote et en phosphore sont également
des paramètres très importants. Les rejets excessifs de phosphore
et d'azote contribuent à l'eutrophisation des lacs et des cours
d'eau.
1.3.1.8.1. L'azote :
Dans les eaux usées domestiques, l'azote est sous
forme organique et ammoniacale, on le dose par mesure du N-NTK (Azote Totale
Kjeldahl) et la mesure du N-NH4. La concentration du N-NTK est de l'ordre de 15
à 20% de celle de la DBO. L'apport journalier est compris entre 10 et
15g par habitant (GROSCLAUDE, 1999).
Azote Kjeldahl = Azote ammoniacal + Azote organique (GAUJOUS,
1995).
L'azote organique, composant majeur des protéines, est
recyclé en continu par les plantes et les animaux.
L'azote ammoniacal est présent sous deux formes en
solution, l'ammoniac NH3 et l'ammonium NH4+, dont les proportions
relatives dépendent du pH et de la température. L'ammonium est
souvent dominant ; c'est pourquoi, ce terme est employé pour designer
l'azote ammoniacal (AMINOT et CHAUSSEPIED, 1983). En milieu oxydant, l'ammonium
se transforme en nitrites puis en nitrates ; ce qui induit une consommation
d'oxygène (GAUJOUS, 1995).
· Nitrites (NO2-) :
Les ions nitrites (NO2-) sont un stade
intermédiaire entre l'ammonium (NH4+) et les ions nitrates
(NO3-). Les bactéries nitrifiantes (nitrosomonas)
transforment l'ammonium en nitrites. Cette opération, qui
nécessite une forte consommation d'oxygène, est la nitritation.
Les nitrites proviennent de la réduction bactérienne des
nitrates, appelée dénitrification.
4 NH4+ + 7 O2 (Nitrosomonas) 4 NO2- + 6
H2O + 4 H+
Les nitrites constituent un poison dangereux pour les
organismes aquatiques, même à de très faibles
concentrations. Sa toxicité augmente avec la température. Ils
provoquent une dégradation de l'hémoglobine du sang des poissons
qui ne peut plus véhiculer l'oxygène. Il en résulte la
mort par asphyxie (SEVRIN-REYSSAC et al, 1995). Chez les nourrissons,
l'inaptitude du sang à transporter l'oxygène est la
méthémoglobinémie (GAUJOUS, 1995).
· Nitrates (NO3-) :
Les nitrates constituent le stade final de l'oxydation de
l'azote organique dans l'eau. Les bactéries nitratantes (nitrobacters)
transforment les nitrites en nitrates.
Cette réaction appelée nitratation s'accompagne
aussi d'une consommation d'oxygène (SEVRIN-REYSSAC et al, 1995).
2 NOi + O2 (Nitrobacters) 2 NO3-
Les nitrates ne sont pas toxiques ; mais des teneurs
élevées en nitrates provoquent une prolifération algale
qui contribue à l'eutrophisation du milieu. Leur potentiel danger reste
néanmoins relatif à leur réduction en nitrates.
Azote global = Azote Kjeldahl + Nitrites + Nitrates
(SEVRIN-REYSSAC et al, 1995). 1.3.1.8.2. Phosphore :
Le phosphore est présent dans l'eau sous plusieurs
formes : phosphates, polyphosphates, phosphore organique ... ; les apports les
plus importants proviennent des déjections humaines et animales, et
surtout des produits de lavage. Les composés phosphorés sont
indésirables dans les réservoirs de distribution d'eau potable,
parce qu'ils contribuent au développement d'algues et plus
généralement du plancton aquatique.
Agents d'eutrophisation gênant dans le milieu naturel,
les phosphates n'ont pas d'incidence sanitaire et les polyphosphates sont
autorisés comme adjuvants pour la prévention de l'entartrage dans
les réseaux (BONTOUX, 1993).
1.3.1.9. Oligo-éléments et les toxiques
minéraux :
Les oligo-éléments sont toujours
présents dans l'eau en quantités très faibles. Leur
présence est généralement indispensable au
développement des êtres vivants, et leur absence peut entrainer
des carences. A plus fortes concentrations, ils deviennent toxiques.
La plupart sont désignés comme étant
"métaux lourds", bien que tous ne soient pas des métaux ; ces
éléments sont soumis à des normes, particulièrement
en eau potable, mais aussi en rejets industriels, pour les boues
d'épuration valorisable en agriculture, pour les épandages de
boues de curage de rivières ... (GAUJOUS, 1995).
1.3.2. Les paramètres bactériologiques :
Les bactéries sont couramment recherchées dans
l'eau, principalement comme témoins de contamination fécale
(GAUJOUS, 1995).
L'OMS (1979) a choisi plusieurs témoins
répondant à certaines exigences ; il s'agit des coliformes, des
streptocoques fécaux du groupe D de LANCFIELD (1933), et parfois les
Clostridium perfringens.
La raison de ce choix réside dans le fait que la
numération de ces bactéries est beaucoup plus simple est rapide
entre 24 et 48h, que celle des germes pathogènes ;
généralement plusieurs jours avec nécessité
d'identification sérologique (GAUTHIER et PIETRI, 1989).
1.3.2.7. Les coliformes totaux (CT) :
Les coliformes sont des bâtonnets, anaérobies
facultatifs, gram (-) non sporulants permettant l'hydrolyse du lactose à
35°C (OMS, 1979).
Les coliformes regroupent les genres Echerichia, Citrobacter,
Entérobacter, Klébsiella, Yersinia, Serratia (RODIER et al, 1996
; JOLY et REYNAUD, 2003).
La recherche et le dénombrement de l'ensemble des
coliformes (coliformes totaux), sans préjuger de leur appartenance
taxonomique et de leur origine, est capital pour la vérification de
l'efficacité d'un traitement désinfectant et est d'un
intérêt nuancé pour déceler une contamination
d'origine fécale (RODIER et al, 1996).
1.3.2.8. Les coliformes fécaux (CF) :
Les coliformes fécaux, ou coliformes
thérmotolérants, sont un sous groupe des coliformes totaux
capables de fermenter le lactose à une température de 44°C.
Ce sont des bâtonnets Gram (-), aérobies et facultativement
anaérobies ; non sporulants, on les désigne souvent sous le nom
d'Eschericia Coli bien que le groupe comporte plusieurs souches
différentes (Citrobacter freundii, Entérobacter
aérogènes, Klebsiella pneumoniiae ...etc.) (OMS, 1979 ; RODIER et
al, 1996 ; JOLY et REYNAUD, 2003).
La recherche et le dénombrement des coliformes
fécaux est un examen proposé en raison d'une concordance
statistique entre leur présence et l'existence d'une contamination
fécale quasi certaine (RODIER et al, 1996).
1.3.2.9. Les Streptococcus fécaux :
Sont considérées comme streptocoques
fécaux, toutes les bactéries Gram (+) de forme oblongue ou de
cocci sphériques légèrement ovales (OMS, 1979). Ils se
disposent, le plus souvent, en diplocoques ou en chainettes (LECLERC et al,
1995 ; JOLY et REYNAUD, 2003).
Selon la classification sérologique de Lancefield
(1933), 5 espèces sont reconnues parmi les streptocoques fécaux
(streptocoques du groupe D). Il s'agit de : S.bovis, S.equinus, S.avium,
S.faecalis et S.faecium, car les autres streptocoques ont une origine
fécale douteuse.
Ils sont des témoins de contamination fécale
assez résistant, y compris dans les milieux salés (GAUJOUS,
1995). Ils peuvent aussi se multiplier dans les milieux présentant des
pH allant jusqu'à 9.6, on peut par conséquent les utiliser comme
indicateurs d'organismes pathogènes qui ont une résistance
similaire au pH élevé (OMS, 1979).
1.3.2.10. Les Clostridium sulfito-réducteurs :
Ils peuvent être considérés comme des
germes fécaux ; ce sont aussi des germes telluriques, et de ce fait,
aucune spécificité d'origine fécale ne peut être
attribuée à leur mise en évidence. Dans une telle optique
d'interprétation, il y a intérêt à ne chercher que
les espèces les plus susceptibles d'être fécales, c'est le
cas en particulier de Clostridium perfringens (RODIER et al, 1996). Les
Clostridium perfringens sont des bâtonnets anaérobies, Gram(+),
sporulants et qui réduisent les sulfites en sulfures en 24 à 48
heures (OMS, 1979).
Ils sont excrétés par l'homme et les animaux, on
les trouve régulièrement dans les matières fécales
humaines, leur densité est la suivante (OMS, 1979) :
· Excréments humains 106 à 108 /g ;
· Eaux usées non traitées 103 /ml.
Ils sont employés comme indicateurs dans l'étude
des pollutions littorales pour un certain nombre de raisons (OMS, 1979) :
· Ils se trouvent en abondance dans les eaux usées
qui sont principalement d'origine humaine ;
· Ils ne se multiplient pas dans les sédiments ;
· Ils survivent longtemps dans les sédiments, ce qui
permet de déceler une pollution ancienne ou intermittente (RODIER et al,
1996).
1.4. L'équivalent habitant (EH) :
Un équivalent habitant correspond à la pollution
quotidienne que génère un individu. Chacun est sensé
utiliser 180 à 300 l d'eau par jour.
La quantité de pollution journalière produite
par un individu est estimée à 57 g de matières oxydables
(MO), 90 g de matières en suspension (MES), 15 g de matières
azotées (MA), et 4 g de matières phosphorées (MP). Enfin,
la concentration des germes est généralement de l'ordre de 1
à 10 milliards de germes pour 100 ml (BADIA- GONDARD, 2003).
1.5. Les normes algériennes de rejet d'effluents :
Les eaux usées collectées, dans les
réseaux urbains ou les eaux usées directement émises par
les industries, ne doivent être rejetées dans un milieu
récepteur naturel (rivière, lac, littoral marin, ou terrain
d'épandage) que lorsqu'elles correspondent à des normes
fixées par voie réglementaire.
Le Décret exécutif n° 93-160 du 10 Juillet
1993, du Journal Officiel de la République Algérienne
réglementant les rejets d'effluents liquides dans son chapitre I,
article 2 (voir annexe 1), définit un rejet comme tout
déversement, écoulement, jets, dépôts directs ou
indirects d'effluents liquides dans le milieu naturel et fixe, en son annexe,
les valeurs limites de ce rejet.
Ces mêmes valeurs viennent d'être
renforcées par un nouveau texte réglementaire ; le Décret
Exécutif n° 06-141 du 20 Rabie El Aouel 1427 correspondant au 19
Avril 2006, section 1, article 3 (voir annexe 2). Les valeurs limites maximales
de rejet d'effluents fixées par ces deux décrets sont
regroupées dans le tableau 1.
Conclusion :
Collectées par le réseau d'assainissement, les
eaux usées contiennent de nombreux éléments polluants,
provenant de la population, des activités commerciales, industrielles et
agricoles et des phénomènes naturels.
Les eaux usées se caractérisent par des
paramètres physico-chimiques et bactériologiques, qui permettent
de déterminer leur éventuelle origine et de connaitre
l'importance de leur charge polluante.
Avant qu'elles ne soient rejetées dans le milieu
naturel et ne le dégradent, elles doivent impérativement
obéir à des normes établies pour protéger les
milieux récepteurs contre la pollution. Pour cela, elles sont
acheminées vers une station d'épuration où elles subissent
plusieurs phases de traitement.
Tableau 1 : Les valeurs limites des paramètres de
rejet dans un milieu récepteur (Journal Officiel de la République
Algérienne, 2006)
PARAMÈTRES
|
UNITÉS
|
VALEURS LIMITES
|
Température
|
°C
|
30
|
pH
|
-
|
6,5 à 8,5
|
MES
|
mg/l
|
35
|
DBO5
|
mg/l
|
35
|
DCO
|
mg/l
|
120
|
Azote Kjeldahl
|
mg/l
|
30
|
Phosphates
|
mg/l
|
02
|
Phosphore total
|
mg/l
|
10
|
Cyanures
|
mg/l
|
0,1
|
Aluminium
|
mg/l
|
03
|
Cadmium
|
mg/l
|
0,2
|
Fer
|
mg/l
|
03
|
Manganèse
|
mg/l
|
01
|
Mercure total
|
mg/l
|
0,01
|
Nickel total
|
mg/l
|
0,5
|
Plomb total
|
mg/l
|
0,5
|
Cuivre total
|
mg/l
|
0,5
|
Zinc total
|
mg/l
|
03
|
Huiles et Graisses
|
mg/l
|
20
|
Hydrocarbures totaux
|
mg/l
|
10
|
Indice Phénols
|
mg/l
|
0,3
|
Fluor et composés
|
mg/l
|
15
|
Étain total
|
mg/l
|
02
|
Composés organiques chlorés
|
mg/l
|
05
|
Chrome total
|
mg/l
|
0,5
|
(*) Chrome III +
|
mg/l
|
03
|
(*) Chrome VI +
|
mg/l
|
0,1
|
(*) Solvants organiques
|
mg/l
|
20
|
(*) Chlore actif
|
mg/l
|
1,0
|
(*) PCB
|
mg/l
|
0,001
|
(*) Détergents
|
mg/l
|
2
|
(*) Tensioactifs anioniques
|
mg/l
|
10
|
|
(*) Valeurs fixées par le Décret exécutif
n° 93-160 du 10 Juillet 1993.



Introduction :
Il ne faut pas confondre le traitement des eaux, qui a pour
fonction de les transformer en eau potable, et l'assainissement des eaux
usées rejetées par le consommateur après utilisation.
L'assainissement des eaux usées a pour objectif de collecter puis
d'épurer les eaux usées avant de les rejeter dans le milieu
naturel, afin de les débarrasser de la pollution dont elles sont
chargées.
2.1. Les étapes et procédés de
traitement des eaux usées :
La dépollution des eaux usées nécessite
une succession d'étapes faisant appel à des traitements
physiques, physico-chimiques et biologiques. En dehors des plus gros
déchets présents dans les eaux usées, l'épuration
doit permettre, au minimum, d'éliminer la majeure partie de la pollution
carbonée.
Selon le degré d'élimination de la pollution et
les procédés mis en oeuvre, plusieurs niveaux de traitements sont
définis : les prétraitements, le traitement primaire et le
traitement secondaire. Dans certains cas, des traitements tertiaires sont
nécessaires, notamment lorsque l'eau épurée doit
être rejetée en milieu particulièrement sensible.
A titre d'illustration, les rejets dans les eaux de baignade,
dans des lacs souffrant d'un phénomène d'eutrophisation ou dans
des zones d'élevage de coquillages sont concernés par ce
troisième niveau de traitement. Les traitements tertiaires peuvent
également comprendre des traitements de désinfection. La
réduction des odeurs peut encore être l'objet d'attentions
particulières.
2.1.1. Les prétraitements :
Les eaux brutes doivent généralement subir,
avant leur traitement proprement dit, un prétraitement qui comporte un
certain nombre d'opérations, uniquement physiques ou mécaniques.
Il est destiné à extraire de l'eau brute, la plus grande
quantité possible d'éléments dont la nature ou la
dimension constitueront une gêne pour les traitements ultérieurs.
Il s'agit principalement des déchets volumineux (dégrillage), des
sables et graviers (dessablage) et des graisses
(dégraissage-déshuilage) (DEGREMONT, 1978).
2.1.1.1. Dégrillage :
Au cours du dégrillage, les eaux usées passent
au travers d'une grille dont les barreaux, plus ou moins espacés,
retiennent les matières les plus volumineuses charriées par l'eau
brute, qui pourraient nuire à l'efficacité des traitements
suivants ou en compliquer leur exécution.
Le dégrillage permet aussi de protéger la
station contre l'arrivée intempestive des gros objets susceptibles de
provoquer des bouchages dans les différentes unités de
l'installation. Les éléments retenus sont, ensuite,
éliminés avec les odeurs ménagères (DEGREMONT,
1978).
2.1.1.2. Dessablage :
Le dessablage a pour but d'extraire des eaux brutes les
graviers, les sables et les particules minérales plus ou moins fines, de
façon à éviter les dépôts dans les canaux et
conduites, à protéger les pompes et autres appareils contre
l'abrasion et à éviter de surcharger les stades de traitements
suivants.
L'écoulement de l'eau, à une vitesse
réduite, dans un bassin appelé "dessableur" entraine leur
dépôt au fond de l'ouvrage. Les sables
récupérés, par aspiration, sont ensuite essorés,
puis lavés avant d'être soit envoyés en décharge,
soit réutilisés selon la qualité du lavage (DEGREMONT,
1978).
2.1.1.3. Dégraissage - Déshuilage :
Le déshuilage est une opération de
séparation liquide-liquide, alors que le dégraissage est une
opération de séparation solide-liquide (à la condition que
la température de l'eau soit suffisamment basse, pour permettre le
figeage des graisses). Ces deux procédés visent à
éliminer la présence des corps gras dans les eaux usées,
qui peuvent gêner l'efficacité du traitement biologique qui
intervient en suite (DEGREMONT, 1978).
2.1.2. Le traitement primaire :
Le traitement "primaire" fait appel à des
procédés physiques, avec filtration et décantation plus ou
moins aboutie, éventuellement assortie de procédés
physicochimiques, tels que la coagulation- floculation :
2.1.2.1. Coagulation - floculation :
La turbidité et la couleur d'une eau sont
principalement causées par des particules très petites, dites
particules colloïdales. Ces particules, qui peuvent rester en suspension
dans l'eau durant de très longues périodes, peuvent même
traverser un filtre très fin. Par ailleurs, puisque leur concentration
est très stable, ces dernières n'ont pas tendance à
s'accrocher les unes aux autres. Pour les éliminer, on a recours aux
procédés de coagulation et de floculation.
La coagulation a pour but principale de déstabiliser
les particules en suspension, c'est-à-dire de faciliter leur
agglomération. En pratique, ce procédé est
caractérisé par l'injection et la dispersion rapide de produits
chimiques : sels minéraux cationiques.
La floculation a pour objectif de favoriser, à l'aide
d'un mélange lent, les contacts entre les particules
déstabilisées. Ces particules s'agglutinent pour former un floc
qu'on peut facilement éliminer par les procédés de
décantation et de filtration (DES JARDINS, 1990).
2.1.2.2. Décantation :
La décantation est un procédé qu'on
utilise dans, pratiquement, toutes les usines d'épuration et de
traitement des eaux (DES JARDINS, 1990). Son objectif est d'éliminer les
particules dont la densité est supérieure à celle de l'eau
par gravité. La vitesse de décantation est en fonction de la
vitesse de chute des particules, qui elle-même est en fonction de divers
autres paramètres parmi lesquels : grosseur et densité des
particules (VILAGINES, 2003).
Les matières solides se déposent au fond d'un
ouvrage appelé "décanteur" pour former les boues "primaires". Ces
dernières sont récupérées au moyen de
systèmes de raclage. L'utilisation d'un décanteur lamellaire
permet d'accroitre le rendement de la décantation. Ce type d'ouvrage
comporte des lamelles parallèles inclinées, ce qui multiplie la
surface de décantation et accélère donc le processus de
dépôt des particules. La décantation est encore plus
performante lorsqu'elle s'accompagne d'une floculation préalable
(DEGREMONT, 1978).
2.1.2.3. Filtration :
La filtration est un procédé physique
destiné à clarifier un liquide, qui contient des matières
solides en suspension en le faisant passer à travers un milieu poreux.
Les solides en suspension, ainsi retenus par le milieu poreux, s'y accumulent ;
il faut donc nettoyer ce milieu de façon continue ou de façon
intermittente.
La filtration, habituellement précédée
des traitements de coagulation-floculation et de décantation, permet
d'obtenir une bonne élimination des bactéries, de la couleur, de
la turbidité et, indirectement, de certains goûts et odeurs (DES
JARDINS, 1990).
2.1.3. Le traitement secondaire (Biologique) :
Dans la grande majorité des cas, l'élimination
des pollutions carbonées et azotées s'appuie sur des
procédés de nature biologique, basés sur la croissance de
micro-organismes aux dépens des matières organiques
"biodégradables" qui constituent pour eux des aliments.
Les micro-organismes, les plus actifs, sont les
bactéries qui conditionnent en fonction de leur modalité propre
de développement, deux types de traitements (VILAGINES, 2003) :
2.1.3.1. Traitements anaérobies :
Les traitements anaérobies font appel à des
bactéries n'utilisant pas de l'oxygène, en particulier, aux
bactéries méthanogènes qui conduisent, comme leur nom
l'indique, à la formation du méthane à partir de la
matière organique, et à un degré moindre de CO2.
Ce type de fermentation est appelé digestion en
hydrologie. C'est une opération délicate qui demande une
surveillance importante. En effet, la température doit être
maintenue à un niveau très stable et suffisamment
élevé. Il faut aussi éviter les écarts brutaux de
pH et les substances inhibitrices du développement bactérien,
à titre d'exemple : les cyanures, les sels de métaux lourds et
les phénols.
Ce système est davantage utilisé pour le
traitement des effluents urbains, que pour le traitement des effluents
industriels généralement toxiques pour les bactéries
(VILAGINES, 2003).
2.1.3.2. Les traitements aérobies :
Les bactéries utilisées exigent un apport
permanant d'oxygène. On distingue trois méthodes essentielles
:
2.1.3.2.1. Les lits bactériens :
Le principe de fonctionnement d'un lit bactérien,
quelques fois appelé filtre bactérien ou filtre percolateur,
consiste à faire ruisseler l'eau à traiter, préalablement
décantée, sur une muse de matériau de grande surface
spécifique servant de support aux microorganismes épurateurs, qui
y forment un feutrage ou un film plus ou moins épais, sous lequel une
couche anaérobie peut de développer sous la couche
aérobie, si son épaisseur est importante (DEGREMONT, 1978).
2.1.3.2.2. Les boues activées :
Les boues activées constituent le traitement
biologique aérobie le plus répondu (OMS, 1979). Le
procédé consiste à provoquer le développement d'une
culture bactérienne dispersée sous forme de flocons (boues
activées), dans un bassin brassé et aéré (bassin
d'aération) et alimenté en eau à épurer. Dans ce
bassin, le brassage a pour but d'éviter les dépôts et
d'homogénéiser le mélange des flocons bactériens et
de l'eau usée (liqueur mixte) ; l'aération peut se faire à
partir de l'oxygène de l'eau, du gaz enrichi en oxygène, voire
même d'oxygène pur, a pour but de dissoudre ce gaz dans la liqueur
mixte, afin de répondre aux besoins des bactéries
épuratrices aérobies.
Après un temps de contact suffisant, la liqueur mixte
est envoyée dans un clarificateur appelé parfois décanteur
secondaire, destiné à séparer l'eau épurée
des boues. Ces dernières sont recyclées dans le bassin
d'aération pour y maintenir une concentration suffisante en
bactéries épuratrices.
L'excédent (boues secondaires en excès) est
extrait du système et évacué vers le traitement des boues
(DEGREMONT, 1978)
2.1.3.2.3. Le lagunage :
Le lagunage est un système biologique
d'épuration, qui consiste à déverser les eaux usées
dans plusieurs basins successifs de faible profondeur, où des
phénomènes naturels de dégradation font intervenir la
biomasse qui transforme la matière organique. La matière
polluante, soustraite aux eaux usées, se retrouve en grande partie dans
la végétation et les sédiments accumulés, et en
faible partie dans l'atmosphère sous forme de méthane et d'azote
gazeux (GRAUSCLAUDE, 1999).
2.1.4. Les traitements tertiaires :
Les traitements tertiaires regroupent tous les traitements
complémentaires visant à affiner la qualité de l'effluent
ayant subis les traitements physiques, physico-chimiques et biologiques. Leur
utilisation s'impose lorsque la nature des milieux récepteurs recevant
l'eau dépolluée l'exige (DEGREMONT, 1978) :
· Les zones sujettes aux phénomènes
d'eutrophisation ;
· Les eaux de baignade ;
· Besoins agricoles;
· Recharge de nappes aquifères ;
· Pisciculture ;
· Usage domestique allant jusqu'à la consommation
humaine.
Les traitements tertiaires englobent, principalement,
l'élimination de l'azote, l'élimination du phosphore et la
désinfection, mais aussi le traitement des odeurs.
2.1.4.1. L'élimination de l'azote :
Les stations d'épuration classiques, prévues
pour éliminer les matières carbonées, n'éliminent
que des quantités réduites d'azote présent dans les eaux
usées. Pour satisfaire aux normes de rejet en zones sensibles, des
traitements complémentaires doivent être mis en place.
L'élimination de l'azote est, le plus souvent, obtenue
grâce à des traitements biologiques, de
"nitrification-dénitrification".
Les procédés physiques et physico-chimiques
d'élimination de l'azote (électrodialyse, résines
échangeuses d'ions, "strippage" de l'ammoniaque) ne sont pas
utilisés dans le traitement des eaux résiduaires urbaines, pour
des raisons de rendement et de coût (BECHAC et al, 1987).
2.1.4.2. L'élimination du phosphore :
L'élimination du phosphore, ou
"déphosphatation", peut être réalisée par des voies
physico-chimiques ou biologiques.
En ce qui concerne les traitements physico-chimiques,
l'adjonction de réactifs, comme des sels de fer ou d'aluminium, permet
d'obtenir une précipitation de phosphates insolubles et leur
élimination par décantation. Ces techniques engendrent une
importante production de boues.
La déphosphatation biologique consiste à
provoquer l'accumulation du phosphore dans les cultures bactériennes des
boues. Les mécanismes de la déphosphatation biologique sont
relativement complexes, et leur rendement variable (en fonction notamment de la
pollution carbonée et des nitrates présents dans les eaux
usées). Dans les grosses installations d'épuration, ce
procédé est souvent couplé à une
déphosphatation physico-chimique, pour atteindre les niveaux de rejets
requis (SATIN et SELMI, 1999).
2.1.4.3. La désinfection :
Les traitements primaires et secondaires ne détruisent
pas complètement les germes présents dans les rejets domestiques.
C'est pourquoi, la désinfection de l'eau s'impose.
La désinfection est un traitement qui permet de
détruire ou d'éliminer les micro-organismes susceptibles de
transmettre des maladies ; ce traitement n'inclut pas nécessairement la
stérilisation qui est la destruction de tous les organismes vivants dans
un milieu donné.
On peut procéder à la désinfection en
ajoutant à l'eau une certaine quantité d'un produit chimique,
doté de propriétés germicides. Les produits chimiques les
plus utilisés sont : le chlore (Cl2), le dioxyde de chlore(ClO2),
l'ozone (O3), le brome (Br2), l'iode (I2) et le permanganate de potassium
(KMnO4).
On peut également désinfecter l'eau grâce
à des moyens physiques : ébullition, ultrasons, ultraviolets (UV)
ou rayon gamma (DES JARDINS, 1990).
Les ultraviolets sont de plus en plus utilisés, car
ils présentent l'avantage de ne pas entrainer l'apparition de
sous-produits de désinfection. Cependant, ils nécessitent un
investissement important.
2.1.4.4. Le traitement des odeurs :
La dépollution des eaux usées produit des
odeurs, qui sont parfois perçues comme une gêne par les riverains
des stations d'épuration. Les principales sources de mauvaises odeurs
sont les boues et leur traitement, ainsi que les installations de
prétraitement.
Le seuil de tolérance de ces nuisances olfactives est
subjectif et aucune norme en matière d'émissions malodorantes
n'existe. Cependant, les exploitants de stations d'épuration cherchent
à limiter les odeurs dégagées par les traitements.
La conception des stations est le premier
élément permettant de limiter l'émission d'odeurs dans le
voisinage. Il faut, par exemple, veiller à réduire les surfaces
d'échange entre l'air et les eaux usées.
Ainsi, les ouvrages les plus odorants sont souvent
regroupés pour concentrer l'émission d'effluves
nauséabonds. Leur couverture est aussi une manière
d'atténuer les émissions malodorantes.
Des installations de désodorisation chimique ou
biologique sont également mises en place, au sein des stations
d'épuration. La désodorisation chimique est la technique la plus
utilisée. Les gaz malodorants sont captés puis envoyés
dans des tours de lavage, où un liquide désodorisant est
pulvérisé. Ces lavages peuvent comporter de la soude, de l'acide
et/ou de l'hypochlorite de sodium (eau de javel), réactifs qui captent
ou neutralisent les mauvaises odeurs (MARTIN et LAFFORT, 1991).
2.2. Réutilisation des eaux usées :
L'importance des coûts d'amener des eaux pour
l'alimentation des villes, jointe à celle de leur évacuation, qui
va de pair avec la raréfaction des ressources en eau, conduit un peu
partout dans le monde, et pas seulement dans les zones arides ou semi arides,
à se poser la question de la réutilisation des eaux
usées.
Après dépollution, les eaux usées
constituent "une ressource de seconde main", qui trouve principalement son
utilité dans :
2.2.1. L'industrie :
2.2.1.1. Lavage et transport industriel des matériaux
:
Dans beaucoup d'industries, le lavage et le transport des
matériaux sont très peu exigeants en qualité de l'eau.
C'est pourquoi les eaux usées épurées sont
utilisées pour (VALIRON, 1983) :
· Le lavage des matières premières (charbon,
gravier, etc.) et leur transport (craie par exemple) ;
· Le transport des déchets (cendres d'une centrale
thermique) ;
· Le lavage d'entretien (wagon, sols, bouteilles, etc.).
2.2.1.2. Refroidissement industriel :
De nombreuses industries utilisent les opérations de
refroidissement qui consomment une part très importante des eaux. C'est
le cas dans (VALIRON, 1983) :
· Les centrales électriques et nucléaires (la
production d'électricité) ;
· La pétrochimie ;
· La chimie ;
· L'industrie du caoutchouc ;
· L'industrie automobile.
2.2.2. L'irrigation :
Dans le cas de l'irrigation, les eaux usées sont
utilisées soit brutes, soit après traitement biologique (boues
activées ou lagunage le plus souvent). Leur intérêt
réside dans le fait que :
· Les eaux brutes contiennent des nutriments qui
accroissent notablement les rendements agricoles, ce qui soulage de
l'utilisation des engrais artificiels très couteux ;
· Les autres sources d'eau utilisable en irrigation se
raréfient en raison de leur potabilité tant recherchée.
2.2.3. Les usages municipaux :
Les usages municipaux peuvent couvrir une assez large gamme
d'utilisations, qui ne requiert pas d'eau de qualité potable, comme par
exemple (VALIRON, 1983) :
· L'arrosage des parcs et jardins publics ;
· Le lavage des rues ;
· La lute contre les incendies ;
· Le nettoyage des engins de collecte des ordures
ménagères.
2.3. L'épuration des eaux usées en
Algérie : 2.3.1. Volumes des eaux usées en 2004 :
Le calcul des volumes des eaux usées (EU) pour
l'année 2004 a été effectué par la Direction de
l'Assainissement et de la Protection de l'Environnement (DAPE) du
Ministère des Ressources en Eau (MRE), et ce, dans le cadre de la
mission 1 de l'étude de la réutilisation des eaux usées
à des fins agricoles ou autres sur tout le territoire national.
Le tableau 2, ci-après, présente les volumes des
eaux usées générées par région
hydrographique pour l'ensemble de la population urbaine et rurale du pays. Le
tableau 3 donne la répartition spatiale des rejets des eaux
usées.
Tableau 2 : Volume des eaux usées par
région hydrographique - 2004.
Région Hydrographique
(RH)
|
Population
totale
|
Taux
de raccordement
à l'égout
|
Volume
consommé
|
Volume
eaux usées
|
|
%
|
Hm3/an
|
Hm3/an
|
Algérois - Soummam -
Hodna (ASH)
|
10 304 025
|
87
|
370
|
259
|
Oranie - Chott Chergui (OCC)
|
5 457 100
|
92
|
123
|
92
|
Cheliff - Zahez (CZ)
|
4 222 089
|
83
|
113
|
74
|
Constantinois - Seybous
Mellegue (CSM)
|
8 400 449
|
88
|
209
|
148
|
Sahara
|
3 470 899
|
81
|
257
|
157
|
TOTAL
|
31 854 563
|
87
|
1 073
|
731
|
|
Tableau 3 : Répartition spatiale des rejets des
eaux usées (amont des barrages, rejets en mer, rejets en chott et
sabkhas).
|
VOLUME DES EAUX USÉES (Hm3/AN)
|
Milieu récepteur
final des EU
|
RH ASH
|
RH OCC
|
RH CZ
|
RH CSM
|
RH Sahara
|
Pour toute
l'Algérie
|
Total rejeté
|
259
|
74
|
148
|
92
|
157
|
731
|
Barrage
|
55
|
61
|
62
|
36
|
7
|
221
|
Mer
|
193
|
6
|
52
|
49
|
-
|
301
|
Chott ou Sabka
|
11
|
7
|
34
|
7
|
150
|
209
|
|
EU épurées
|
110
|
6
|
43
|
52
|
13
|
223
|
EU réutilisées
|
7
|
-
|
2
|
2
|
-
|
11
|
|
2.3.2. Programme des stations d'épuration pour le court
terme (2006-2010)1 :
Au cours de ces dernières années, le
Ministère des Ressources en Eau (MRE) à entrepris la mise en
oeuvre d'un important programme d'investissement concernant la
réalisation de 84 stations d'épuration (STEP) et la
réhabilitation de 15 autres, dont deux en exploitation. Ceci portera le
nombre actuel des STEP existantes et en exploitation de 46 à 138 avant
la fin 2008. À noter aussi que 56 STEP sont actuellement en cours
d'étude ou en étude de réhabilitation, et dont le
lancement des travaux est prévu pour le moyen terme (2007-2010), ce qui
permettra d'atteindre un parc de 194 STEP à l'horizon 2010.
1 Situation Juin 2006 - Source DAPE
Les STEP mentionnées répondent à des
exigences impératives imposées par le MRE et qui consistent en la
protection :
· De la santé publique à proximité des
grands rejets d'eaux usées urbaines (exutoires des grandes villes) ;
· Des ressources en eau conventionnelles mobilisées
(barrages et nappes) ;
· Des ressources en eau non conventionnelles (dessalement
de l'eau de mer) contre la contamination par les rejets urbains ;
· Du littoral, et par conséquent les eaux de
baignade à fin de protéger la santé publique. Et respect
des amendements de la convention de Barcelone pour la protection de la
méditerranée.
La totalité des villes abritant plus de 100.000 habitants
sont dotées de STEP ou le seront avant 2010.
Pour répondre à ces obligations, les
traitements primaires sont de plus en plus abandonnés au profit des
traitements secondaires, qui exploitent largement les filières
biologiques, à savoir, les boues activées et le lagunage (naturel
et aéré) visant les objectifs de qualité exigés par
l'OMS, notamment :
DBO5 < 20 à 40 mg/l ;
DCO < 90 à 120
mg/l ;
MES < 20 à 30 mg/l.
· STEP à boues activées :
Cent six (106) STEP seront en service avant 2010 et
fonctionneront par boues activées ; soit plus de 54 % du nombre total de
STEP (194) prévus à cet horizon. Les capacités
installées varient de 200 m3/jour pour l'agglomération
de H'Nancha (Souk Ahras) à 150.000 m3/jour pour la STEP de
Baraki (Alger).
· Lagunage :
Quatre vingt huit (88) STEP de type lagunage dont 20 de type
aéré seront en service avant 2010 ; soit 46 % du nombre total de
STEP (194) prévus à cet horizon. Les capacités
installées varient de 320 m3/jour pour l'agglomération
d'Émir Abdel Kader (Ain Temouchent) à 42 000 m3/jour
pour la STEP de Ouargla.
Le rendement moyen des STEP est variable selon leur
état, qu'elles soient bien ou mal entretenues. Les STEP, dont la gestion
et l'exploitation sont bien prises en charge, atteignent un rendement de plus
de 95 %.
Le tableau 4 présente le nombre et l'état des STEP
par procédé.
Tableau 4 : Nombre et état des STEP par type de
procédé.
Procédé
|
État
|
Nombre
|
Boues activées
|
En exploitation
Dont six (6) en travaux de réhabilitation et une (1) en
étude de réhabilitation
|
29
|
|
18
|
|
11
|
|
6
|
|
6
|
|
36
|
Sous total
|
106
|
Lagunage naturel et aéré
|
En exploitation
|
12
|
|
33
|
|
22
|
|
1
|
|
-
|
|
20
|
Sous total
|
88
|
Total
|
194
|
|
Conclusion :
Les eaux usées sont toutes les eaux qui sont de nature
à contaminer les milieux dans lesquelles elles seront
déversées. C'est pourquoi, dans un souci de respect de ces
différents milieux, des traitements sont réalisés sur ces
effluents (collectés par le réseau d'assainissement). Ces
derniers sont débarrassés de leurs plus grands déchets, au
cours des prétraitements, jusqu'aux infimes polluants, au cours des
traitements tertiaires.
Les traitements secondaires biologiques, boues activées,
lagunage naturel et aéré sont les traitements les plus
fréquemment utilisés en Algérie.
Le recours aux traitements tertiaires reste minoritaire et
réservé aux traitements poussés des effluents, du fait
qu'il présente de nombreux inconvénient, à savoir :
· Des coûts d'investissement importants ;
· Les ultraviolets (UV) ne sont applicables que pour de
faibles quantités d'eau ;
· La surchloration peut s'avérer
cancérigène.
Le lagunage naturel est un mode épuratoire
écologique, rustique et peu onéreux du fait de son fonctionnent
non mécanisé, qui donne des résultats satisfaisants et qui
s'avère adapté pour la réutilisation des eaux
épurées.
Nous essayons dans notre étude de vérifier
(contrôler) l'efficacité du lagunage naturel dans la
dépollution des eaux usées ; pour pouvoir ensuite évacuer,
sans risques, les eaux traitées dans le milieu naturel et
éventuellement envisager leur réutilisation.
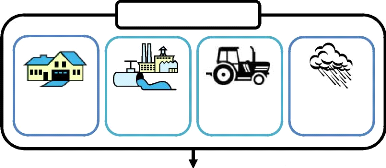
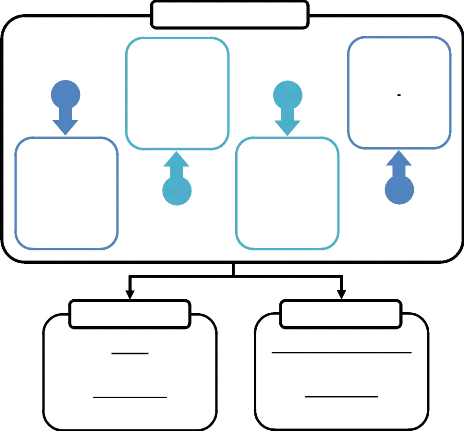
La figure 1 illustre les diverses origines des eaux
usées, les différents traitements effectués sur ces
effluents au sein d'une station d'épuration et enfin leur devenir.
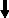
Origine
Domestique
Origine
Industrielle
EAUX USÉES BRUTES
Origine
Agricole
Origine
Pluviale
RÉSEAU D'ASSAINISSEMENT

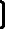

STATION D'ÉPURATION
-
PRÉTRAITEMENTS
Coagulation/
Floculation
TRAITEMENTS
SECONDAIRES
Éliminations :
Azote
Phosphore
1
3
Décantation
-
Filtration
Désinfection
-
Désodorisation
Dégrillage
Traitements
Anaérobies
-
Dessablage
2
-
4
-
Déshuilage
TRAITEMENTS
PRIMAIRES
Traitements
Aérobies
TRAITEMENTS
TERTIAIRES
BOUES
Rejets :
Lacs, Oueds, Mer,
...
-
Réutilisations :
Irrigation, Industrie, ...
EAUX ÉPURÉES
Valorisation en Agriculture :
Boues
Humifiées
-
Récupération :
Traitements
Secondaires
Figure 1 : Origines, traitements et devenir des eaux
usées.


Introduction :
Parmi les divers procédés d'épuration
des eaux usées, dont l'application dépend des
caractéristiques des eaux à traiter et du degré de
dépollution souhaité, figure le lagunage naturel.
Moyen rustique d'épuration des eaux usées, il se
distinct des autres techniques de traitement réputées intensives
par de nombreux avantages. Ce procédé écologique, simple
et peu onéreux se base sur les phénomènes responsables de
l'autoépuration des cours d'eau.
3.1. Définition :
Le lagunage est une technique biologique d'épuration
des eaux usées, où le traitement est assuré par une
combinaison de procédés aérobies et anaérobies,
impliquant un large éventail de micro-organismes (essentiellement des
algues et des bactéries). Les mécanismes épuratoires et
les micro-organismes qui y participent sont, fondamentalement, les mêmes
que ceux responsables du phénomène d'autoépuration des
lacs et des rivières (PEARSON, 2005).
3.2. Principe de fonctionnement :
Le lagunage se présente comme une succession de
bassins (minimum 2 et généralement 3) peu profonds (le plus
souvent rectangulaires) dits lagunes. La surface et la profondeur de ces
lagunes influencent le type de traitement (aérobie ou anaérobie)
et confèrent un rôle particulier à chacune d'entre-elles.
L'épuration par lagunage consiste à faire passer des effluents
d'eau usée par écoulement gravitaire de lagune en lagune
où la pollution est dégradée par (VALIRON, 1983) :
· L'activité bactérienne ;
· L'activité photosynthétique et
l'assimilation des substances minérales ;
· Le pouvoir germicide de la lumière et de certaines
algues.
Les matières en suspension de l'eau brute
décantent dans le bassin de tête. Les bactéries assimilent
la pollution dissoute, et l'oxygène nécessaire à cette
dépollution, est assuré par l'action chlorophyllienne de
végétaux qui participent aussi à la synthèse
directe de la matière organique :
· les microphytes ou algues microscopiques ; ce sont
essentiellement des algues vertes ou bleues difficilement séparables
;
· les macrophytes ou végétaux
macroscopiques, qui comprennent des formes libres (ex. lentilles d'eau) ou
fixées (ex. roseaux). Les jacinthes d'eau peuvent s'enraciner ou non.
Les végétaux supérieurs jouent un rôle de support et
doivent normalement permettre d'augmenter la quantité de
bactéries et d'algues épuratrices. (DEGREMONT, 1989).
Les microphytes sont consommés par le zooplancton, et les
macrophytes filtrent l'eau en sortie avant rejet.
L'ensemble de ces phénomènes apparait dans
plusieurs bassins en séries, ce qui autorise l'étagement des
phénomènes épuratoires.

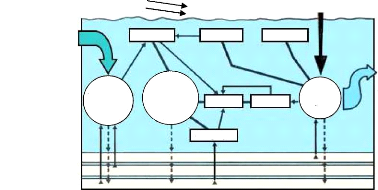
Le processus épuratoire qui s'établit dans une
lagune est particulièrement intéressant, car c'est un
phénomène vivant, un cycle naturel qui se déroule
continuellement. La figure 2 schématise les principaux cycles
biologiques se développant dans une lagune.
ENTRÉE
DE
L'ÉFFLUENT
bactéries
matières organiques
VENTS
microphages
ÉNERGIE SOLAIRE
macrophytes
microphytes
décomposeurs
(bactéries
champignons)
consommateurs
animaux
carnivores herbivores
producteurs
végétaux
détritiphages
sels minéraux solubles
matières organiques
solubles
détritus
SORTIE
DE
L'ÉFFLUENT
TRAITÉ
macrophytes
microphytes
consommateurs
sels
minéraux
résidus organiques
Figure 2 : Cycles biologiques d'une lagune
(d'après CEMAGREF dans DEGREMONT, 1989).
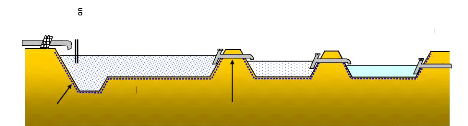
La figure 3 illustre un exemple de lagunage constitué de
trois bassins (de surface et profondeur décroissante) disposés en
série.
Eau Usée
Brute Digue
carrossable
egrillage
phoIde
Eau Usée
Épurée
Bassin n°1 Bassin n°2 Bassin
n°3
Étanchéité
Tuyau en T
Figure 3 : Schéma d'un lagunage à trois
bassins. 3.3. Les différents types de lagunage :
Selon que les lagunes soient artificiellement
aérées ou pas, on distingue deux types de lagunages :
3.3.1. Le lagunage naturel :
Ce sont des bassins artificiels et
imperméabilisés, de faible profondeur pouvant recevoir des
effluents bruts ou prétraités et où la recirculation des
boues biologiques décantées n'est pas réalisée, et
la concentration de la biomasse épuratrice reste faible.
Alimentées d'effluents à traiter, les lagunes naturelles sont
nommées étangs de stabilisation (KOLLER, 2004), que l'on classe
en fonction des filières de développement des bactéries en
trois catégories : anaérobies, aérobies ou facultatifs
(mixtes).



Différents assemblages de ces bassins sont possibles en
fonction des conditions locales, des exigences sur la qualité de
l'effluent final, du débit à traiter, ...
A titre d'exemple, si l'on souhaite un degré de
réduction plus élevé des organismes pathogènes, on
dispose les bassins en série comme suit : étang anaérobie,
facultatif puis anaérobie (CHAIB, 2004).
Le lagunage naturel peut être utilisé, en
traitement complet des effluents ou en traitement tertiaire, pour affiner la
qualité de l'eau traitée par une boue activée (
ex. la désinfection) (DEGREMONT,
1978).
3.3.1.1. Étangs anaérobies :
Les étangs anaérobies sont
caractérisés par un manque d'oxygène dissous causé
par une forte DBO5 (100-400 g/m3/jour), et les solides en suspension
s'y déposent facilement ; ils forment sur le fond une couche où
les bactéries anaérobies décomposent la matière
organique. Un des résultats est la production de gaz :
l'hydrogène sulfuré (H2S) et le méthane (CH4) qui
s'échappent vers la surface sous forme de bulles.
Typiquement, ces lagunes ont une profondeur de 2 à 5 m
et le temps de séjour de l'effluent y est de 3 à 5 jours. Ils
reçoivent des effluents bruts et mènent à des
réductions de la DBO5 de 40 à 60 % et des solides en suspension
de 50 à 70 %.
En générale, on n'y trouve pas de micro-algues
à cause des conditions défavorables à leur croissance
(SEVRIN-REYSSAC et al, 1995).
3.3.1.2. Étangs aérobies :
Les étangs aérobies ou de maturation sont peu
profonds (0,8 à 1,2 m) où la lumière peut
pénétrer et favorisant le développement d'algues vertes.
Par leur action photosynthétique, les algues produisent de
l'oxygène qui permet le développement de bactéries
épuratrices aérobies (DEGREMONT, 1978).
Le temps de séjour dans ces étangs est beaucoup
plus long, de 12 à 18 jours ou plus, et permet un traitement d'effluent
déjà partiellement épuré (SEVRIN-REYSSAC et al,
1995). Ces étangs sont caractérisés par (ANRH,
1996)1 :
· Charge (Kg DBO5/ha/jour) : 111 à 112 ;
· Rendement (% de DBO5) : 80 à 95 % ;
· Concentration en algues (mg/l) : 100.
3.3.1.3. Étangs facultatifs :
D'une profondeur de 1 à 2 m et un temps de
séjour de 4 à 6 jours (SEVRIN-REYSSAC et al, 1995), ces
étangs fonctionnent dans des conditions telle que la partie
supérieure entretient un milieu aérobie, riche en algues et en
micro-organismes aérobies, alors que le fond, couvert de
sédiments organiques, est le siège de fermentation
anaérobie ; entre ces deux zones règne un milieu de transition
favorable aux bactéries facultatives (BEAUDRY, 1984).
1 ANRH : Agence Nationale des Ressources Hydrauliques.
Les fermentations benthiques donnent lieu à un
dégagement de méthane (CH4), de dioxyde de carbone (CO2),
d'hydrogène sulfuré (H2S) et d'ammoniac, ainsi que de
composés organiques de faible masse moléculaire.
Ce produit alimente la flore des zones supérieures et
les composés minéraux dégagés entretiennent les
algues ; une certaine fraction de ces algues meurent et se sédimentent,
venant s'ajouter au lit de boues (BEAUDRY, 1984).
3.3.2. Le lagunage aéré :
Ce sont de vastes bassins constituant un dispositif
très proche du procédé à boues activées
à faible charge. On y effectue une épuration biologique
bactérienne comme celle qui se pratique naturellement dans les
étangs, en apportant de l'extérieur par insufflation d'air ou
oxygénation au moyen d'aérateurs de surface, l'oxygène
nécessaire au maintien des conditions aérobies des
bactéries épuratrices.
Bien que théoriquement elle ne s'impose pas, une
recirculation de l'eau traitée et parfois des boues biologiques en
tête de lagune est souvent pratiquée. Elle permet
d'améliorer le mélange complet et d'assurer une meilleure
répartition de la biomasse.
Il est rare, en raison de la concentration relativement
élevée en matières en suspension, que l'on puisse rejeter
directement l'effluent traité à l'exutoire sans
décantation finale (KOLLER, 2004).
3.4. Influence des conditions climatiques sur les
performances du lagunage :
Le microclimat est le climat local auquel sont soumises les
lagunes, il résulte de l'action de plusieurs facteurs qui jouent un
rôle important dans l'implantation du lagunage naturel ; ce sont
principalement :
3.4.1. La durée du jour et l'intensité de
l'ensoleillement :
La durée du jour conditionne, dans une certaine
mesure, la vitesse de multiplication du phytoplancton. L'intensité de
l'ensoleillement a une influence sur l'activité photosynthétique
des végétaux. Si le ciel reste couvert pendant plusieurs jours,
surtout en été alors que le phytoplancton est abondant, la
production de l'oxygène due à la photosynthèse pendant la
journée devient moins importante, ce qui risque d'entrainer une
désoxygénation passagère (SEVRIN-REYSSAC et al, 1995).
3.4.2. La température :
Les écarts de température exercent une
influence sur le bon fonctionnement des systèmes de lagunage naturel. La
croissance des algues est favorisée par une température
élevée. Lorsqu'ils sont bien ensoleillés et bien
oxygénés, les bassins aérobies ne dégagent pas
d'odeur. Un ciel nuageux, plusieurs jours de suite, affaiblit le
phénomène de photosynthèse créant ainsi des zones
anaérobies dont les produits de fermentation conduisent à de
mauvaises odeurs. La température intervient aussi dans le calcul du
dimensionnement des installations ; les moyennes mensuelles des cinq
dernières années doivent alors être connues (ANRH,
1996).

3.4.3. Le régime des vents dominants dans la
région et leur orientation :
Les vents dominants sont ceux dont la direction est la plus
fréquente. Ce régime des vents étant connu pour une
région donnée, nous permet de fixer l'implantation du
système de telle sorte à éviter le rabattement sur les
habitations des mauvaises odeurs susceptibles de provenir de l'installation, et
de ne pas avoir des effets néfastes sur l'ouvrage (dégradation
des digues par batillage) (ANRH, 1996).
3.4.4. L'évaporation :
L'évaporation est un facteur très important.
Elle est très intense en période estivale (10 à 15 mm/j).
Conjuguée à une infiltration importante, elle peut être
néfaste et doit donc être prise en considération lors des
calculs de dimensionnement des bassins (ANRH, 1996).
3.4.5. La pluviométrie :
Elle devrait également être connue pour le calcul
de la hauteur des digues, afin d'éviter tout risque éventuel
d'inondation (ANRH, 1996).
3.5. Exploitation du lagunage :
L'exploitation des lagunes aérobies ou facultatives
n'exige que peu d'expertise, puisque le préposé à cette
tâche ne peut influencer les paramètres fondamentaux à
l'exception de la hauteur d'eau.
Il devrait néanmoins, à intervalles
réguliers, prendre des mesures de certaines variables telles que le
débit d'arrivée, la hauteur d'eau, la charge organique, la
turbidité, la température et la DBO de l'effluent ; il doit
prendre note des phénomènes anormaux ou singuliers qui peuvent
influer sur le comportement de l'étangs : prolifération
inusité des algues, gel, perte inexpliquée de niveau, etc.
Dans le cas des étangs aérés, il
convient de vérifier le fonctionnement des dispositifs d'aération
et la concentration en oxygène dissous de l'effluent. En revanche, il
faut porter une attention particulière à l'entretien
général de l'étang, des digues, de la clôture et du
terrain compris dans l'enceinte (BAUDRY, 1984).
3.6. Contraintes d'exploitation :
Parmi les contraintes d'exploitation, il faut signaler les
suivantes :
· Passage de l'exploitant une à deux fois par
semaine ;
· Suppression des mauvaises herbes ;
· Suppression des rongeurs ;
· Suppression des matières flottantes ;
· Limitation de la prolifération d'insectes par
l'emploi judicieux d'insecticides ;
· Très faible technicité requise pour
l'exploitant ;
· Très faible consommation énergétique
(voire nulle) ;
· Curage contraignant et coûteux des boues, tous les
1 à 5 ans, dans le bassin de tête, tous les 10 à 20 ans
dans tous les bassins.

3.7. Avantages et inconvénients du lagunage :
3.7.1. Avantages :
Le lagunage naturel présente de nombreux avantages par
rapport aux procédés classiques :
· Excellente élimination de la pollution
microbiologique ;
· Faibles coûts d'investissement et de fonctionnement
;
· Raccordement électrique inutile ;
· Très bonne intégration paysagère
;
· Valorisation aquacole et agricole de la biomasse
planctonique produite et des effluents épurés ;
· Boues peu fermentescibles ;
· Bonne élimination de l'azote (70 %) et du
phosphore (60 %).
3.7.2. Inconvénients :
A l'inverse, le lagunage naturel présente les
inconvénients suivants :
· Variation saisonnière de la qualité de
l'eau en sortie ;
· En cas de mauvais fonctionnement, risque d'odeurs, de
moustiques, de rongeurs ;
· Emprise au sol importante ;
· Difficultés d'extraction des boues ;
· Pas de réglage possible en exploitation ;
· Sensibilité aux effluents septiques et
concentrés.
Conclusion :
Le lagunage est fortement dépendant des conditions
climatiques (essentiellement de la température), et la qualité
des rejets peut donc varier selon les saisons. L'emprise au sol est
relativement importante. Les coûts d'investissement sont non seulement
dépendants du prix du terrain, mais aussi de la nature du sol. Sur un
sol perméable, il sera indispensable d'ajouter un revêtement
imperméable, et dans ce cas, l'investissement peut s'avérer
onéreux, voire difficilement abordable.
Malgré ces défauts, le lagunage reste une
technique efficace (également pour l'azote, le phosphore et germes
pathogènes) bon marché, ne nécessitant pas de construction
en dur (génie civil simple) et s'intégrant parfaitement au
paysage. De plus, aucun apport d'énergie n'est requis si le terrain est
en pente.
Au sein du lagunage naturel et par les processus biologiques
qu'ils créent, les organismes jouent un rôle distinct mais
complémentaire dans l'épuration des eaux usées en formant
un parfait équilibre biologique naturel.
Le Zooplancton

Les Bactéries
|
|
ÉQUILIBRE
|
|
Les Algues
|
|
Les plantes aquatiques




Introduction :
Le lagunage naturel est l'une des techniques les plus
appropriées de traitement des eaux usées pour notre pays,
à caractère semi-aride, réunissant toutes les conditions
favorables à son exploitation.
Nous avons choisi, pour évaluer l'efficacité de
cette technique, de baser le présent mémoire sur l'étude
de la station d'épuration par lagunage naturel de
Béni-Messous.
Toutefois, Il est essentiel de bien connaitre la zone
d'étude afin de déterminer et cerner les principaux facteurs
influençant le traitement des eaux usées, et de ce fait, la
qualité des eaux usées épurées. Ainsi, nous nous
intéresserons à l'environnement du site : situation
géographique, conditions climatiques et structures sociales locales
ainsi qu'aux caractéristiques des eaux usées à traiter.
D'autant plus que, c'est en fonction de ces derniers, que se fait le choix
même de l'implantation du lagunage naturel.
4.1. Étude du lagunage naturel de Béni-Messous
: 4.1.1. Localisation géographique :
La station de lagunage, dont fait l'objet notre étude,
se situe dans la commune de Béni-Messous, du coté Ouest de la
wilaya d'Alger. Elle se trouve à 5 Km de l'embouchure de l'oued de
Béni Messous qui origine à l'Est de la commune de
Bouzaréah, traverse les communes de Béni-Messous et
Chéraga et débouche du coté Ouest dans la baie d'EL
Djamila au niveau de la plage « Les Dunes ». (voir figure 4).
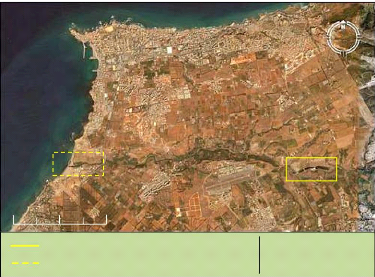
Baie
D'EL Djamila
1939 km
Implantation du lagunage de Béni-Messous Embouchure de
l'Oued de Béni-Messous
Chéraga
Ain Benian
cp : 36° 46'50.00» N X, :
02° 56'50.00» E
y : Latitude
k : Longitude
Figure 4 : Localisation géographique du lagunage
naturel de Béni-Messous
(Google Earth, 2007).
Constituée de quatre bassins en série et
occupant environ 13 hectares, la station d'épuration par lagunage
naturel de Béni-Messous s'implante entre la commune de Ain Benian et
celle de Chéraga ; à proximité du chemin wilayal, CW
n°11 et adjacente à des terres agricoles. (voir figure
5).

Figure 5 : Photo satellite du lagunage naturel de
Béni-Messous (Google Earth, 2007). 4.1.2. Dimensionnement et
caractéristiques des lagunes :
Le plan schématique du lagunage naturel de
Béni-Messous, représenté par la figure 6, présente
la série des quatre bassins, en parallèles à l'Oued de
Béni-Messous, ainsi qu'un déversoir (dispositif contre les fortes
crues) à l'extrémité gauche du premier et du
deuxième bassin. Avant d'être acheminées vers le premier
bassin de la station, les eaux usées brutes passent par un
dégrilleur.
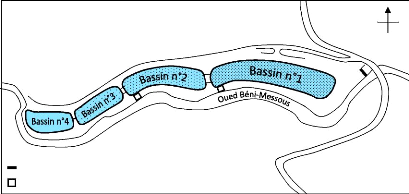
· Déversoir
Dégrilleur
·
·
CW n°11
N
Figure 6 : Schéma du lagunage naturel de
Béni-Messous.
Une étude topographique, sur terrain du site, a permis
de dimensionner les lagunes. Les résultats des mesures ainsi que les
caractéristiques de chacune d'entre-elles sont regroupés dans le
tableau 5.


Tableau 5 : Dimensions et caractéristiques des
quatre bassins du lagunage naturel
de Béni-Messous. (DHEEWA,
2001)1.
|
Bassin
n°
|
Longueur
(m)
|
Largeur
(m)
|
Profondeur
(m)
|
Surface
(m2)
|
Volume
(m3)
|
Caractéristiques
|
|
1
|
300
|
60
|
3,5
|
18000
|
63000
|
- Appelé lagune de décantation. - Contient un
déversoir pour l'évacuation des eaux usées en cas de
fortes crues.
|
|
2
|
175
|
40
|
2
|
7000
|
14000
|
- Contient aussi un déversoir. - Son rôle principal
est
la minéralisation des boues.
|
|
3
|
95
|
40
|
1,5
|
3800
|
5700
|
- Permet aussi la minéralisation des boues.
|
|
4
|
80
|
38
|
1 5
,
|
3040
|
4560
|
- Son rôle est l'affinage de l'épuration.
|
4.1.3. Caractéristiques des eaux usées :
Selon les données fournies par la DHEEWA2
(2001), les eaux usées parvenant à la station par lagunage
naturel de Béni-Messous sont caractérisées par :
|
Débit moyen des eaux usées urbaines
|
8336 m3/j
|
|
Débit des eaux industrielles
|
940 m3/j
|
|
Débit moyen total des eaux
|
9276 m3/j
|
|
Débit moyen horaire des eaux
|
387 m3/h
|
|
Débit de pointe des eaux usées
|
773 m3/j
|
|
DBO5 (charge journalière)
|
5439 Kg/j
|
|
DCO (charge journalière)
|
8640 Kg/j
|
4.1.4. Temps de séjour dans les lagunes :
Le temps de séjour (TS) désigne le temps
nécessaire que doivent séjourner les eaux usées dans
chaque bassin pour permettre leur épuration. Si l'on considère
l'écoulement des eaux comme un écoulement laminaire, on admettra
que le débit est constant. Le temps de séjour pourra être
calculé grâce à l'équation suivante :
TS = V/Q
Où :
TS : Temps de séjour (j) ;
V : Volume du bassin (m3) ;
Q : Débit moyen d'entrée des eaux usées
(m3/j).
1 2 DHEEWA : Direction de l'Hydraulique et de
l'Économie de l'Eau de la Wilaya d'Alger.


Les lagunes de Béni-Messous ont chacune, en
correspondance à leurs volumes différents, un temps de
séjour propre. Ci-après sont regroupés, les temps de
séjour des quatre lagunes ainsi que le temps de séjour global
:
|
Bassin n°
|
Temps de séjour (j)
|
|
1
|
7
|
|
2
|
2
|
|
3
|
1
|
|
4
|
1
|
|
TOTAL
|
11
|
4.2. Étude géologique de la région de
Béni-Messous :
Les sols de la région se composent de marnes bleues, de
grés et de schistes métamorphiques. Les grès et poudingues
carténniens, qui affleurent d'Alger à la commune de Béni
Messous, reposent sur les schistes cristallophylliens du massif ancien de
Bouzaréah et plongent vers le sud sous les marnes bleues plais
anciennes. Ce sont des grés grossiers, peu fissurés, qui
débutent par un poudingue mal cimenté remaniant sur 1 à 2
mètres des éléments du massif ancien et qui renferment des
lits de gravier discontinus.
Le sol comprend également des sables dunaires fins, par
endroits légèrement argileux et cimentés à la base
en un gré calcaire constituant de petites corniches. L'épaisseur
de cet ensemble n'excède pas 50 mètres.
Les conditions géologiques sont particulièrement
identiques dans toute la région considérée. Les
dépôts alluvionnaires, qui comblent le fond des vallons, sont
essentiellement argileux et très peu perméables. Seuls les
grés et poudingues carténniens sont perméables. Ces
derniers sont atteints à 50 mètres de profondeur. Les profils et
sondages réalisés à proximité du site laissent
apparaitre les couches supérieures du sous-sol composé
essentiellement de sables.
4.3. Étude hydrologique de la région de
Béni-Messous :
Le substratum rattaché aux nappes phréatiques du
sahel est caractérisé par une bonne
perméabilité.
Les grés et poudingues carténiennes qui
affleurent d'Alger à la commune de BéniMessous contiennent une
nappe qui s'épanche par quelques petites sources descendant vers l'Oued
Béni Messous. Cette nappe, liée dans la zone de l'affleurement
à la nappe phréatique des terrains anciens, se met en charge vers
le sud sous les marnes bleues. De petites nappes libres existent, elles sont
alimentées exclusivement par la pluviométrie et s'écoulent
vers la mer.
4.4. Étude démographique de la population
concernée :
Selon les données recueillies lors du Recensement
Général de la Population et de l'Habitat (RGPH) de 2004 pour les
communes concernées par l'Oued de Béni-Messous (auquel est
rattaché le lagunage naturel), le nombre d'habitant pour chaque commune
est :

|
Commune
|
|
Nombre d'habitant
|
|
Béni-Messous
|
|
19407
|
|
Chéraga
|
|
66991
|
|
Dély Ibrahim
|
|
34361
|
|
Bouzaréah
|
|
75797
|
|
TOTAL
|
196556
|
4.5. Description des conditions climatiques :
Dans un système lagunaire, le climat affecte, de
façon directe, les processus biologiques qui s'y déroulent, et
par conséquent, le rendement épuratoire des lagunes.
Le climat est une synthèse de la variation des
conditions atmosphériques d'une région sur une période
d'environs 10 ans. Elle est réalisée à l'aide de moyennes
établies à partir de mesures statistiques (annuelles et
mensuelles) se basant sur les données atmosphériques locales.
A l'aide des données climatiques recueillies entre 1995
et 2005 par l'Office National de la Météorologie (ONM), pour la
région de Béni-Messous (voir annexe 3), nous pouvons
étudier les principales conditions climatiques intervenant dans le bon
fonctionnement du lagunage naturel, à savoir : la température,
l'ensoleillement, les vents, la pluviométrie et l'évaporation.
4.5.1. Température :
Deux saisons dominent dans la région de
Béni-Messous ; une saison chaude qui s'étale de Juin à
Octobre où les températures moyennes de l'air varient entre
20°C et 27°C et se rafraichissent en Novembre
et une autre saison qui débute en Décembre et s'achève en
Mars où les températures moyennes varient entre
11°C et 18°C.
Sur la figure suivante nous pouvons apprécier la variation
moyenne des températures maximales et minimales entre 1995 et 2005.
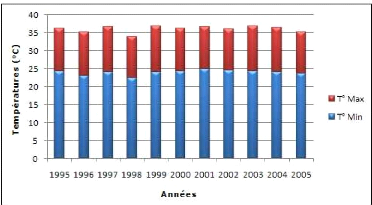
Figure 7 : Profil de variation des températures
moyennes de l'air.
4.5.2. Ensoleillement :
La région de Béni-Messous est
caractérisée par un été ensoleillé et un
hiver nuageux. La figure suivante révèle l'existence de trois
périodes où l'ensoleillement est :
· Fort entre Juin et Août atteignant son maximum, 329
h en Juillet ;
· Faible de Novembre à Février avec une
moyenne de 210 h ;
· Moyen réparti en deux phases, de Mars à Mai
et de Septembre à Octobre.
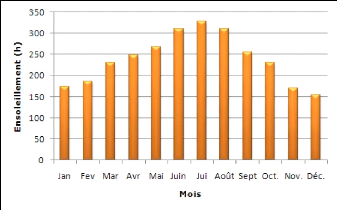
Figure 8 : Profil de l'ensoleillement mensuel moyen dans
la région de Béni-Messous.
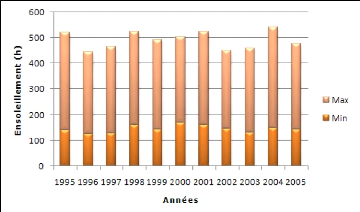
Figure 9 : Profil de variation de l'ensoleillement.
4.5.3. Vents :
Les vents soufflent environ 60 % du temps dans la région
de Béni-Messous. Cependant, les plus importants d'entre eux, de secteur
Sud-ouest, ne soufflent que 14 % du temps.

Tableau 6 : Répartition annuelle des vents sur
huit directions dans la région de Béni-Messous (ONM,
1960-2004).
Secteurs
|
N
|
NE
|
E
|
SE
|
S
|
SO
|
O
|
NO
|
Calme
|
Pourcentage
par direction
|
11,8
|
11,9
|
4
|
1,3
|
5,3
|
13,5
|
10,1
|
4,9
|
37,1
|
|
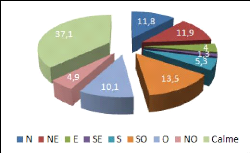
Figure 10 : Répartition annuelle des vents sur
huit directions
de la région de Béni-Messous (en %).
4.5.4. Pluviométrie :
À Béni-Messous, les pluies sont fréquentes
en automne et en hiver et diminuent dés la fin du printemps et
deviennent presque nulles en été.
Deux saisons humides se distinguent : l'une allant du mois de
Novembre au mois de Février où la moyenne mensuelle maximale
atteint 93 mm et l'autre plutôt sèche allant du mois de Juin au
mois d'Octobre avec un minimum de 1,95 mm. Il existe cependant, une
période transitoire entre Mars et Mai où les
précipitations moyennes varient entre 45 et 64 mm.
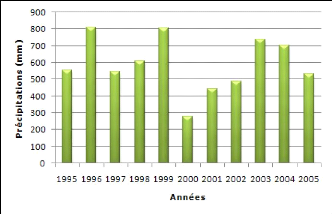
Figure 11 : Précipitations annuelles dans la
région de Béni-Messous.
4.5.5. Évaporation :
L'évaporation dans la région de
Béni-Messous atteint son maximum au mois d'Août avec une valeur de
141 mm ; tandis qu'au mois de Février, elle enregistre sa moyenne
mensuelle minimale avec une valeur de 52 mm. La moyenne annuelle est de 1104
mm.
La figure 12 indique qu'il existe trois périodes :
1
2
3
Une première, où l'évaporation est plus
importante que les précipitations correspondant ainsi à une
saison sèche de Mai à Octobre ;
Une deuxième, où les précipitations sont
plus importantes de Novembre à Février ;
Une troisième, de transition, où
l'évaporation est légèrement supérieure aux
précipitations et qui ne dure que deux mois, de Mars à Avril.
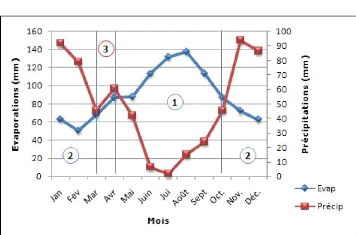
Figure 12 : Profil
évaporations-précipitations de la région de
Béni-Messous. Conclusion :
La lagune de Béni-Messous s'implante dans une
région caractérisée par un climat
méditerranéen ; avec un hiver plutôt humide et doux et un
été relativement chaud et aride. En effet, la région de
Béni-Messous connaît une saison humide de sept mois et une saison
sèche de cinq mois correspondant à la période estivale.
Contrairement à l'Hiver où l'activité
biologique dans les lagunes est ralentie, en été, elle atteint
sont optimum par les températures modérées
enregistrées dans la zone, ainsi que par un fort ensoleillement, une
grande évaporation et une pluviométrie presque nulle.



Introduction :
Dans toute station d'épuration des eaux usées
il est nécessaire d'effectuer des analyses de l'eau brute et de l'eau
traitée afin de déterminer les différents
paramètres physicochimique et bactériologiques permettant
d'évaluer le niveau de pollution dans chaque phase de traitement. Les
analyses ne sont valides que si le prélèvement et
l'échantillonnage ont été entourées de soins
suffisants ; la séquence
prélèvementéchantillonnage-conservation-analyse constitue
alors une chaine cohérente pour la quelle on aura conscience de ne
négliger aucun maillon.
5.1. Prélèvement et échantillonnage :
Le prélèvement est l'opération qui
consiste à prendre une partie aliquote du milieu à étudier
; alors que l'échantillonnage consiste à retenir une fraction du
prélèvement sur laquelle sera effectuée l'analyse.
L'échantillonnage peut se faire sans
prélèvement intermédiaire, l'eau est prise directement
dans des flacons sans transiter par une bouteille de prélèvement,
c'est l'étape la plus délicate dans la chaine de mesure de la
qualité des eaux, car elle conditionne les résultats analytiques
et l'interprétation qui en sera donnée. Il conviendra donc que
:
· d'une part, toutes les précautions soient prises
pour que l'eau prélevée subisse
le minimum de modification
entre l'instant du prélèvement et celui de l'analyse.
· d'autre part, les échantillons soient
homogène et aussi représentatif que possible du milieu.
On distingue deux types d'échantillons :
A- L'échantillon ponctuel :
L'échantillon ponctuel est celui où l'ensemble
du volume constituant l'échantillon est prélevé en une
seule fois. Ce type d'échantillons est utile pour déterminer la
composition d'une eau résiduaire à un instant donnée. Ce
type d'échantillon est généralement prélevé
manuellement en utilisant des récipients ou flacons, mais l'emploi
d'équipement automatique est également possible.
B- L'échantillon composite :
Ce sont des échantillons préparés par
mélange de plusieurs échantillons ponctuels. Il existe deux types
d'échantillons composites :
· échantillons dépendant du temps ;
· échantillons dépendant du débit.
5.2. Conditionnement des échantillons :
Lors de l'échantillonnage, il est nécessaire de
respecter un certain nombre de règles qui visent à faire un
flaconnage correct et un étiquetage précis afin d'assurer une
conservation et traçabilité des échantillons. Le
matériel d'échantillonnage doit être, de
préférence, constitué d'un matériau inerte non
susceptible de perturber les analyses effectuées sur
l'échantillon, la pratique courante consiste à employer des
récipients en polyéthylène ou en verre
borosilicaté.
Le tableau en annexe 4 récapitule le type de
récipients appropriés aux différents paramètres
à étudier.
Avant de commencer le prélèvement, il convient
de nettoyer le matériel avec de l'eau et du détergent puis le
rincer à l'eau (voir annexe 5). On peut avant utilisation, rincer le
matériel d'échantillonnage dans l'eau dans laquelle sera
effectué le prélèvement, afin de réduire au minimum
le risque de contamination.
La désignation des échantillons se traduit dans
la pratique par l'étiquetage ou le marquage de chaque flacon
d'échantillon d'eau. Il est indispensable de repérer l'ensemble
des récipients contenant les échantillons de façon claire
et durable afin de permettre leur identification sans ambigüités en
laboratoire. La solution la plus judicieuse consiste à opérer par
une des deux désignations possibles suivantes (voir annexe 6) :
· soit les flacons sont désignés par une
étiquette où sont indiquées l'origine de
l'échantillon et les conditions dans lesquelles il a été
prélevé ;
· soit il est possible de simplifier cette opération
en utilisant un système d'étiquettes numérotées ou
codées.
5.3. Conservation des échantillons :
Pour avoir des résultats analytiques significatifs, il
est très important de connaitre le devenir de l'échantillon entre
le prélèvement et l'analyse. Le moyen le plus courant de
conservation des échantillons d'eaux résiduaire consiste à
les garder dans une mallette isotherme de température comprise entre 0
et 4°C jusqu'à leur arrivée au laboratoire dans
un temps ne dépassant pas les 24 heures.
Pour stabiliser un échantillon ou du moins, ralentir
toutes réactions éventuelles, il n'existe pas de panacée.
On recommande de prendre pour chaque analyse des précautions
particulières et parfois, d'ajouter des agents chimiques (conservateurs)
(voir annexe 4) afin d'éviter certaines transformation lors du transport
ou certaines interférences au moment de l'analyse en laboratoire.
5.4. Application au lagunage de Béni-Messous :
En application aux recommandations de
prélèvement, d'échantillonnage et de conservation
cités précédemment et en rapport avec notre objectif de
déterminer la pollution résiduelle et qui nécessite qu'un
seul prélèvement, nous avons procédé à un
échantillonnage ponctuel et ce, à partir d'un
prélèvement manuel effectué le : 06 Juin 2007 dans chaque
bassin de la lagune de Béni-Messous, comme suit :
· aux entrées E1, E2, E3, E4 relatives aux bassins
B1, B2, B3, B4 respectivement ;
· à la sortie S du dernier bassin (B4).
Il est à noté que la journée du
prélèvement à été choisi de façon
à ce que l'accès aux digues et donc aux points de
prélèvement, soit plus facile.
Nous avons employé un flaconnage (soigneusement
étiqueté) correspondant à chaque paramètre de
pollution à mesurer (voir annexe 4) dont la méthode d'analyse est
passée en revu ci-après.
5.5. Analyses et modes opératoires :
Les analyses doivent être faites le plus tôt
possible après le prélèvement pour permettre d'avoir des
résultats représentatifs. Elles regroupent la mesure de
paramètres insitu ainsi que de paramètres au laboratoire :
5.5.1. Paramètres insitu :
Un certain nombre de paramètre physicochimique de l'eau
ne peuvent être mesurés que sur terrain car les valeurs peuvent
évoluer très rapidement dans les échantillons
prélevés. Ce sont principalement : la température de l'eau
et son pH.
5.5.1.1. La température de l'eau :
La température de l'eau est l'exemple même du
paramètre qui évolue très vite après le
prélèvement, en particulier quand l'écart avec celle de
l'air est important. Par ailleurs, la nécessité de transporter
les échantillons à basse température rend obligatoire la
mesure sur site.
A- Appareillage :
La mesure de la température de l'eau est aujourd'hui
réalisée à l'aide d'un appareil
électrométrique, une thermosonde. Cependant, il est toujours
possible d'utiliser un thermomètre.
B- Mode opératoire :
La température de l'eau sera prise en même temps
que le prélèvement de l'échantillon. L'immersion dans le
milieu à étudier devra être d'une durée suffisante
pour que la valeur affichée soit stabilisée. En cas
d'impossibilité de mesure au sein même des lagunes, on
prélèvera l'eau dans un seau de 5 à 10 litres de
capacité et on y plongera immédiatement l'appareil de mesure
soigneusement étalonné. On procédera à la lecture
de la température, dès que la stabilisation est observée,
en laissant la sonde dans l'eau.
C- Expression des résultats :
La précision recherchée pour ce paramètre
est habituellement de l'ordre de 0,5°C. Avec les appareils
électrométriques, la précision sur la mesure proprement
dite peut atteindre #177; 0,1°C.
5.5.1.2. Le potentiel d'Hydrogène (pH) :
Parmi tous les paramètres physico-chimiques
analysés sur le terrain, c'est un des plus délicats à
mesurer correctement.
Il est recommandé de déterminer le pH des eaux
in situ de façon à ne pas modifier les équilibres ioniques
par suite d'un transport ou d'un séjour plus ou moins prolongé
des échantillons d'eau dans des flacons. Le pH est mesuré avec un
appareil électrométrique avec électrode de verre, le
pH-mètre.
A- Appareillage :
Un pH-mètre est composé d'une électrode
de verre, d'une électrode de référence au calomel-KCl
saturé et d'un dispositif potentiométrique. Indépendamment
du dispositif potentiométrique dont les caractéristiques
techniques peuvent varier, il existe un très grand nombre
d'électrodes dont les spécificités sont propres à
chaque constructeur et à chaque domaine d'utilisation.
Le préleveur se rapportera donc aux recommandations
établies par le fabricant (domaine et gamme d'utilisation,
fréquence d'étalonnage, solution tampon, durée de vie de
la sonde...).
B- Mode opératoire :
L'étalonnage étant réalisé et
l'appareil ayant acquis son régime de marche, l'électrode est
plongée dans la solution à mesurer. La lecture est
effectuée après stabilisation du pH-mètre ce qui peut
prendre plusieurs minutes. Veiller à ce que la température de
l'échantillon ne varie pas pendant la mesure.
C- Expression des résultats :
Le plus souvent la précision recherchée est de
l'ordre de #177; 0,05 unité pH. Une manipulation rigoureuse, avec des
contrôles d'étalonnage fréquents, permet d'atteindre une
précision de #177; 0,02 unité pH. Les résultats sont
exprimés en unités de pH, à la température de
mesure qui doit être indiquée, sous la forme :
pH à XX°C = XX,XX
5.5.2. Paramètres mesurés au laboratoire :
Aussi tôt arrivés au laboratoire, les
échantillons sont soumis à une série d'analyses qui
permettent d'apprécier la qualité de l'eau brute et
traitée, de mesurer leur degré de pollution et de contrôler
l'efficacité du traitement qu'elles ont subi.
Nous nous intéressons principalement dans le lagunage
de Béni-Messous à la détermination de la pollution
résiduelle qui permet d'évaluer la pollution due à la
présence des micro-algues par l'estimation des paramètres :
matière en suspension (MES), demande chimique en oxygène (DCO) et
demande biologique en oxygène pendant 5 jours (DBO5) dont le mode
opératoire est décrit ci-après.
5.5.2.1. Matières en Suspension (MES) :
Selon le domaine d'application, la quantité d'eau
à analysé et la qualité présumée des
matières suspendues dans l'eau, Le protocole de détermination des
matières en suspension (MES) se basera sur l'une des méthodes
expérimentales suivantes :
· La néphélométrie ;
· La centrifugation ;
· La filtration.
Dans le cas de l'analyse des eaux usées, il est
recommandé de procéder par filtration sur couche d'amiante ou sur
filtre en fibre de verre pour les échantillons d'eaux traitées et
par centrifugation pour les échantillons d'eaux brutes et
chargées afin d'éviter le colmatage des filtres.
Le choix de la filtration sous vide avec membrane filtrante en
fibre de verre s'est imposé, dans notre cas, d'une part, en raison de sa
rapidité et de sa simplicité à mettre en oeuvre, et
d'autre part, de la possibilité de récupérer le filtrat
(fraction dissoute) nécessaire pour la détermination de la
pollution résiduelle.
A- Principe de la filtration :
Cette méthode se base sur le passage d'un
échantillon d'eau de volume V à travers un filtre en fibre de
verre de 0,47 um. le poids de matière retenue par le filtre, noté
P, est déterminé par pesée différentielle (avant et
après filtration). La concentration des matières en suspension
(MES) ne sera donc que le rapport de ce poids sur le volume d'eau
analysé.
B- Matériel utilisé :
- Dispositif de filtration ;
- Balance ;
- Capsules ;
- Filtres en fibre de verre porosité de 0,47 um ; -
Étuve.
C- Mode opératoire :
- Rincer le filtre à l'eau distillée et le
sécher à l'étuve à 105 °C environ
30 à 60 min ; - Laisser refroidir puis peser le filtre sec et noter son
poids P1 ;
- Homogénéiser l'échantillon à
analyser ;
- Filtrer sous vide un volume V de l'échantillon
mesuré à l'aide d'une éprouvette graduée ;
- Sécher, refroidir et peser une seconde fois le filtre.
Son poids est noté P2.
Note : Ne mettre l'eau que petit à petit, toujours en
homogénéisant bien pour ne pas avoir à filtrer de trop
grands volumes sur un filtre colmaté.
C- Expression des résultats :
La concentration de la matière en suspension en mg/l dans
l'échantillon analysé est obtenue par la relation suivante :
[MES] = ((P2 - P1)/V) . 103
Où :
P1 : Poids du filtre sec avant filtration (en mg) ;
P2 : Poids du filtre sec après filtration (en mg) ;
P2 - P1: Poids de la matière retenue par le filtre sec ; V
: Volume de la prise d'eau (en ml).
5.5.2.2. Demande Chimique en Oxygène (DCO) :
La détermination de la DCO se fait essentiellement par
oxydation avec le dichromate de potassium, K2Cr2O7 dans une solution
portée à ébullition à reflux pendant 2 heures en
présence d'ions Ag+ comme catalyseurs d'oxydation et d'ions
Hg2+ permettant de complexer les ions chlorures (Norme NF T 90-10,
équivalente ISO 6060). D'une manière simplifiée, on peut
décrire cela par la réaction :
|
Composés organiques
|
Catalyseur
+ Cr2O72- CO2 + H2O + Cr3+ (BLIEFERT et
PERRAUD, 2001)
H+
|
Plus il y a de substances oxydables dans un échantillon
d'eau, plus on utilise de dichromate. La DCO est déterminée par
le dosage de l'excès de dichromate titré avec du sulfate de fer
et d'ammonium (sel de Mohr) car la quantité de matière oxydable
est proportionnelle à la quantité de dichromate réduit.
A- Matériel nécessaire :
- DCO-mètre ;
- Granules : pierres ponces ou billes de verre.
B- Réactifs à utiliser (voir annexe 7 pour leur
préparation) :
- Solution d'acide sulfurique et sulfate d'argent ;
- Solution sulfate de fer (II) et d'ammonium (sel de Mohr)
[(NH4)2 Fe(SO4)2 6H2O] à 0,12 mol/l ;
- Solution de dichromate de potassium (K2Cr2O7)
à 0,04 mol/l et contenant du sulfate de mercure (II) ;
- Hydrophtalate de potassium (KC8H5O4) à
2,0824 mmol/l ;
- Ferroïne.
C- Mode opératoire :
- Transvaser 10 ml de l'échantillon pour l'analyse
(diluer si nécessaire) dans le tube de l'appareil, ajouter 5 ml de
solution de dichromate de potassium et quelques régulateurs
d'ébullition (granules : billes de verre) ;
- Ajouter avec précaution 15 ml d'acide sulfurique et
sulfate d'argent et raccorder immédiatement le tube au
réfrigérant ;
- Répéter les deux étapes
précédentes pour tous les échantillons à analyser
mais aussi pour deux échantillons à blanc (10 ml d'eau
distillée) et un essai témoin (10 ml d'hydrogénophtalate
de potassium) ;
- Amener le mélange réactionnel à
l'ébullition pendant 120 minutes à 150°C ; -
Rincer les réfrigérants à l'eau distillée et
refroidir les tubes ;
- Enlever le réfrigérant et diluer à 75 ml
et laisser refroidir ;
- Titrer l'excès de dichromate avec la solution de sel de
Mohr en présence d'une ou de deux gouttes de l'indicateur coloré
Ferroïne.
D- Expression des résultats : La DCO exprimée en
mg d'O2/l est donnée par la formule :
DCO = 8000 × CFe(VT - VE) / E
Où :
CFe : Concentration de la solution de sel Mohr
déterminée par étalonnage, soit dans le cas présent
0,12 mol/l ;
E : Volume de la prise d'essai en ml ;
VT : Volume en ml de la solution de sulfate de fer (II) et
d'ammonium titré pour l'essai à blanc ;
VE : Volume en ml de la solution de sulfate de fer (II) et
d'ammonium titré pour l'échantillon ;
8000 : Masse molaire en mg/l de 1/2 O2.
Note : On doit vérifier la validité de la
méthode en calculant la DCO de l'essai témoin, qui doit
être de 500 mg d'O2/l, en remplaçant dans l'équation VE par
VR.
Où :
VR : Volume en ml de la solution de sulfate de fer (II) et
d'ammonium titré pour l'essai témoin ;
Avec la valeur de la DCO, contrairement à la valeur de la
DBO5, les composés difficilement dégradables ou non
dégradables biologiquement sont également mesurés.
Tableau 7 : Valeurs typiques de DCO (BLIEFERT et
PERRAUD, 2001)
|
DCO (en mg/l)
|
Type d'eaux usées/substrat
|
|
5 ...
|
20
|
|
eaux courantes
|
|
20 ...
|
100
|
eaux usées communales après épuration
biologique
|
|
300
|
...
|
1000
|
eaux usées communales non épurées
|
|
22 000
|
|
eaux d'infiltration de décharges
|
5.5.2.3. Demande Biologique en Oxygène (DBO5) :
On dispose pour la détermination de la DBO5 de deux
catégories de méthodes :
· par dilution : ces méthodes ont pour
principe d'établir une dilution de l'eau riche en matières
organiques par une eau apportant l'oxygène dissous dont on mesure la
quantité résiduelle dans des conditions opératoires bien
déterminées.
· par un système de mesure OxiTop :
utilisation d'un appareillage pour la mesure de la DBO5.
Nous opterons pour l'utilisation d'un système de mesure
OxiTop pour la raison que ce système est plus pratique, rapide et donne
des résultats représentatifs.
A- Instruments et produits nécessaires :
- Système de mesure OxiTop ;
- Système d'agitation à induction ;
- Armoire thermostatique (T° à 20
°C) ;
- Flacons bruns et fiole jaugée ;
- Godets en caoutchouc ;
- Extracteur magnétiques et barreaux aimantés ; -
Pastilles de soude (NaOH).
B- Sélection du volume d'échantillon :
- Estimer la valeur de la DBO5 à 80 % de la valeur de la
DCO ;
- Déterminer la plage de mesure correspondante dans le
tableau en annexe 8.
D- Mode opératoire :
- Introduire le volume V correspondant à la gamme
d'estimation de la DBO5 par rapport à la DCO du même
échantillon dans un flacon brun en verre contenant un barreau
magnétique ;
- Placer un godet en caoutchouc contenant deux pastilles de
soude (NaOH) servant à absorber le CO2 produit lors de la consommation
de l'oxygène (les pastilles ne doivent jamais être en contact avec
l'échantillon) ;
- Visser l'OxiTop directement sur le flacon ;
- Lancer la mesure en appuyant sur S et M simultanément
(deux secondes) jusqu'à ce que l'afficheur indique 00 ;
- Maintenir, dans une armoire thermostatique, le flacon de
mesure avec l'OxiTop à 20 °C pendant 5 jours.
Après que la température de mesure soit atteinte (au maximum
après 1H), l'OxiTop lance automatiquement la mesure de la consommation
de l'oxygène ;
- l'échantillon est agité en continu pendant 5
jours. L'OxiTop mémorise automatiquement une valeur toutes les 24 heures
sur 5 jours. Pour connaitre la valeur courante, il faut appuyer sur la touche
M.
D- Expression des résultats :
La DBO5 s'exprime en mg d'O2/l et s'obtient par la
multiplication de la valeur affiché par l'OxiTop après 5 jours
d'incubation à 20°C par le facteur correspondant au
volume échantillonné qui est donné par la gamme
d'estimation (voir annexe 8).
La différence entre la DCO et la DBO5 vient des
substances présentes dans l'eau qui ne peuvent pas être
décomposées microbiologiquement. Parce que tous les polluants ne
sont pas totalement décomposables, la valeur de la DBO5 se situe en
dessous de celle de la DCO.
Tableau 8 : Valeurs typiques de DBO5 (BLIEFERT et
PERRAUD, 2001).
DBO5 (en mg/l)
|
Type d'eaux usées/substrat
|
6
|
cours d'eaux courantes modérément
pollués
|
20
|
eaux communales après traitement biologique
|
250
|
eaux communales non épurées
|
> 5000
|
eaux usées de l'industrie alimentaire
|
13 000
|
eaux de ruissellement sous les décharges
|
|
5.6. Classes de qualité des eaux :
On considère qu'une eau est polluée lorsque, la
concentration en oxygène dissous est située au-dessous d'une
certaine valeur limite ; car la consommation d'oxygène dans l'eau est
principalement due à des substances polluantes qui sont biologiquement
dégradables. Quelques substances inorganiques appartiennent à
cette catégorie, mais la plupart des composés qui utilisent
l'oxygène sont de nature organique.
On dispose de plusieurs possibilités pour
caractériser une eau avec des indicateurs. Dans le tableau suivant,
à coté de la teneur en oxygène sont données entre
autre la valeur de la DCO et de la DBO5 correspondantes.
Tableau 9 : Classement des eaux de surfaces stagnantes
et courantes d'après leur qualité
(BLIEFERT et PERRAUD,
2001).
Classe
de qualité
|
Taux de saturation
en O2 (en %)
|
Oxygène dissous
(en mg/l)
|
DBO5
(en mg/l)
|
DCO
(en mg/l)
|
Qualité
de l'eau
|
1A
|
=
|
90
|
=
|
7
|
=
|
3
|
=
|
20
|
excellente
|
1B
|
70
|
... 90
|
5 ...
|
7
|
3 ...
|
5
|
20
|
... 25
|
bonne
|
2
|
50
|
... 70
|
3 ...
|
5
|
5 ...
|
10
|
25
|
... 40
|
moyenne
|
3
|
<
|
50
|
<
|
3
|
10 ...
|
25
|
40
|
... 80
|
médiocre
|
4
|
|
-
|
-
|
|
>
|
25
|
>
|
80
|
Hors classe
|
|
1A : Qualité excellente - absence de pollution :
qualité d'eau normale ;
1B : Qualité d'eau bonne - pollution
modérée : eau possédant des propriétés
requises pour la vie et la production des poissons, ainsi que pour la
production d'eau destinée à l'alimentation humaine après
traitement simple ou normal ;
2 : Qualité moyenne - pollution nette : eau
possédant des propriétés requises pour la vie piscicole
mais où la reproduction du poisson est aléatoire, et permettant
la production d'eau destinée à l'alimentation humaine
après traitement poussé (affinage et stérilisation) ;
3 : Qualité mauvaise - pollution importante : eau dans la
quelle la vie piscicole est aléatoire et impropre à la production
d'eau destinée à l'alimentation humaine ;
4 : Hors classe - pollution très importante :
dégradation du milieu, possibilité de mort biotique ou
azoïque.
Conclusion :
Un certain nombre de mesures seront effectuées
obligatoirement sur le terrain, de préférence dans les lagunes
même, sinon dans un récipient de grande capacité :
température et pH par exemple. Ces mesures sont réalisées
à l'aide de sondes spécifiques et effectuées selon les
normes en vigueur, en se conformant aux instructions du fabricant. Les
appareillages doivent avoir fait l'objet, auparavant, d'un étalonnage ou
calibrage en laboratoire ou sur site. La lecture de la mesure se fait
après stabilisation de la valeur. Les résultats seront
consignés dans une fiche de terrain.
Le préleveur utilisera obligatoirement les flacons
appropriés aux analyses. Il vérifiera leur conformité et
leur propreté avant de partir sur terrain. Le repérage des
flacons sera fait à l'aide d'une étiquette stable sur laquelle
seront portés les éléments permettant d'identifier
facilement l'échantillon : soit une étiquette codée, soit
une étiquette comportant au minimum l'identification de la station et la
date du prélèvement.
Les échantillons seront transportés au
laboratoire à l'obscurité dans une enceinte
réfrigérée à une température entre 0 et
4°C. Ils seront livrés dans un délai maximum de
24 heures. Au laboratoire, l'analyste identifie les échantillons et
applique rigoureusement le protocole de chaque paramètre à
mesurer et dresse ensuite les résultats sur une fiche
récapitulative.
Les analyses appliquées (selon les normes en vigueur)
aux échantillons prélevés du lagunage naturel de
Béni-Messous durant la journée du : 06 Juin 2007 se sont
correctement déroulées pour donner les résultats
présentés avec leur interprétations dans le chapitre
suivant.


Introduction :
L'analyse des échantillons terminée, il
convient de présenter les résultats de telle façon qu'ils
soient facilement exploitables pour déterminer la pollution
résiduelle de la station d'épuration par lagunage naturel de
Béni-Messous. Il est également présenté, dans ce
qui suit, l'interprétation des résultats obtenus pour chaque
paramètre analysé.
6.1. La température :
Obtenue par la moyenne de l'entrée et de la sortie de
chaque bassin, la température dans les lagunes augmente
significativement de 21,4°C dans le bassin de tête à
23,2°C dans le bassin de sortie. Cette augmentation est due à la
fois, à la profondeur décroissante des bassins mais
également, à leur surface de contact avec l'air qui diminue
aussi. En effet, plus la profondeur et la surface de contact eau-air d'un
bassin sont moins importants, plus celui-ci s'échauffe.
Tableau 10 : Températures, profondeurs et
surface de contact air-eau des quatre bassins
du lagunage de
Béni-Messous.
Bassin
|
B1
|
B2
|
B3
|
B4
|
Température (°C)
|
21,4
|
21,9
|
22,8
|
23,2
|
Profondeur (m)
|
3
|
2
|
1,5
|
1,5
|
Surface de contact eau-air (m2)
|
18000
|
7000
|
3800
|
3040
|
|
La température moyenne de l'eau des lagunes est de
22,25°C.
Avec uniquement 23,2°C et comme illustré sur la
figure 13, la température de l'eau en sortie respecte largement la norme
fixée à 30°C (voir tableau 1).
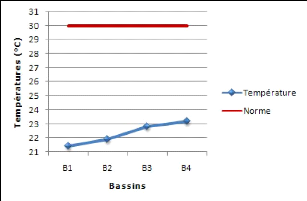
Figure 13 : Températures des bassins de la
station d'épuration
par lagunage naturel de Béni-Messous.
6.2. Le potentiel d'hydrogène (pH) :
Avec un minimum de 7,4 dans le premier bassin et un maximum
de 8,7 dans le troisième bassin (calculés par la moyenne de
l'entrée et de la sortie de chaque bassin), selon GAUJOUS (1995), le pH
reste compris entre 6 et 9, ce qui n'as pas d'incidence écologique forte
sur les organismes aquatiques.
D'après SEVRIN REYSSAC et al (1995), dans le cas de
très fortes densités algales, le pH reste très
élevé, généralement supérieur à 8,3.
Ceci explique la valeur maximale atteinte dans le troisième bassin qui
comme on peut le voir sur la figure 14, dépasse même la norme
limitée à 8,5. Ceci dit, ce pH élevé favorise la
volatilisation de l'azote ammoniacal dans l'atmosphère. En effet, ce
phénomène appelé « Stripping » permet
d'éliminer par entrainement gazeux des quantités d'autant plus
importantes d'azote ammoniacal que le pH est élevé (SEVRIN
REYSSAC et al, 1995).
Le pH alcalin et la température modérée
des bassins constituent des conditions de milieu idéales pour la
prolifération des algues et des bactéries qui établissent
un parfait équilibre biologique permettant la dégradation de la
matière organique et la décontamination de l'eau.
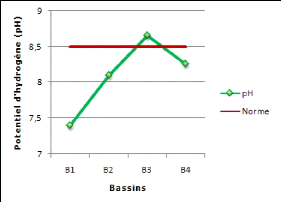
Figure 14 : Potentiel d'hydrogène (pH) des
bassins de la station d'épuration
par lagunage naturel de
Béni-Messous.
Les valeurs de pH généralement observées
en milieu naturel vont de 6 à 8,5 (SEVRIN REYSSAC et al, 1995). Le pH de
l'eau en sortie est de 8,2. Respectant la norme de rejet
délimitée entre 6,5 et 8,5 (voir tableau 1), cette valeur
coïncide, d'après GAUJOUS, 1995, avec le pH normal de l'eau de mer
et des eaux douces en zones calmes.
6.3. Les matières en suspension (MES) :
Les résultats obtenus pour les MES montrent qu'il y a
une élimination très importante de ces derniers entre
l'entrée et la sortie de la station. En effet, avec une teneur de 114
mg/l à l'entrée contre uniquement 8 mg/l au niveau de la sortie,
le rendement global de l'épuration pour ce paramètre atteint 93
%.
Sur la figure 15, on peut clairement voir l'écart
qu'accuse la faible teneur en MES de l'eau en sortie avec celle de
l'entrée ainsi qu'avec la norme de rejet, limitée à 35
mg/l (voir tableau 1).
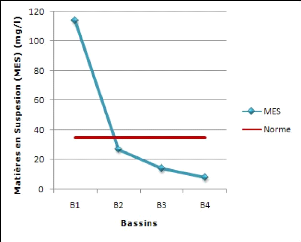
Figure 15 : Teneur en matières en suspension
(MES) dans les bassins de la station
d'épuration du lagunage de
Béni-Messous.
Au regard de la figure 16 ci-dessous, l'abattement des MES
est majoritaire dans le premier bassin avec un rendement de 81,6 % ; ce qui
confirme que celui-ci représente le bassin de décantation. Le
rendement des trois autres bassins est approximativement le même (environ
45 %) ; ce qui indique une épuration uniforme des matières en
suspension.
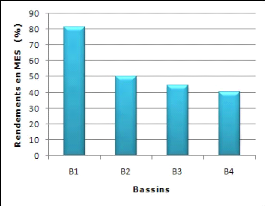
Figure 16 : Rendements d'épuration en MES des
quatre bassins de la station d'épuration
par lagunage naturel de
Béni-Messous.
6.4. Détermination de la pollution résiduelle
:
On estime souvent, dans une station d'épuration, la
pollution de l'eau de façon directe par la mesure des paramètres
globaux DCO et DBO5 qui offrent une représentation plus ou moins
complète (certains hydrocarbures ne sont, par exemple, pas oxydables)
des matières oxydables et biodégradables présentes dans un
échantillon.
Cependant, dans le cas d'une station d'épuration par
lagunage naturel, cette mesure directe constitue une surestimation de la
pollution en incluant en termes de DCO ou de DBO5 une part importante de
matière organique sous forme de biomasse algale qui ne devrait pas
être considérée comme étant une pollution. En effet
les micro-algues dans ce type de traitement des eaux usées sont non
seulement nécessaires à l'épuration mais présentent
aussi la possibilité d'être récupérées pour
divers usages bénéfiques (en agriculture par exemple).
De ce fait, cette pollution additionnelle due à la
présence des micro-algues que l'on définit comme pollution
résiduelle doit être déterminée et soustraite pour
estimer avec plus d'exactitude la véritable pollution de l'eau.
Il est nécessaire de mesurer la DCO et de la DBO5 des
échantillons, avant et après leur filtration pour
déterminer la pollution résiduelle qui se traduira alors par les
deux relations suivantes :
ADCO = DCOAvF - DCOApF
ADBO5 = DBO5AvF - DBO5ApF
Où :
ADCO : la pollution résiduelle
exprimée en termes de DCO ; DCOAvF : DCO de l'échantillon
analysé avant filtration ; DCOApF : DCO de l'échantillon
analysé après filtration ; ÄDBO5 : la pollution
résiduelle exprimée en termes de DBO5 ; DBO5AvF : DBO5 de
l'échantillon analysé avant filtration ; DBO5ApF : DBO5 de
l'échantillon analysé après filtration ;
L'analyse de la DCO et de la DBO5 des échantillons
prélevés aux entrées des bassins et à la sortie de
la station étudiée ont donné les moyennes
regroupées en annexe 9. Leur traitement a permis de déterminer la
pollution résiduelle dans chaque bassin dont le résultat et
l'interprétation sont présentés ci-après.
6.5. La demande chimique en oxygène (DCO) :
En se référant uniquement aux valeurs de DCO
des échantillons avant leur filtration, représentés sur la
figure 17 par la série DCOAvF, nous remarquerons alors l'abattement
important de la charge polluante globale (matières organiques et
inorganiques) des eaux interceptés par la lagune de Béni-Messous,
de 763 mg/l à 60,2 mg/l.
Cependant, la filtration des échantillons
révèle par la série DCOApF, que cet abattement est, en
réalité, de 456 à 27 mg/l et que la différence
entre les deux séries, représentée par la série
DCOR, n'est autre que la pollution résiduelle.
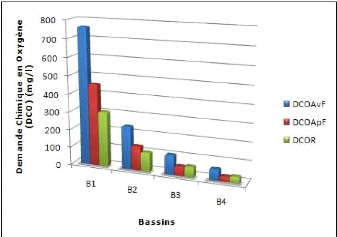
Figure 17 : DCO des bassins de la station
d'épuration par lagunage naturel de Béni-Messous.
Nous pouvons, également, constater à travers la
figure 17, l'importance de la pollution résiduelle sensiblement
grandissante jusqu'à même dépasser, dans les deux derniers
bassins, la véritable pollution en confirmant ainsi sa surestimation.
Le rendement global en DCO est de 94 %. Ceci témoigne
du traitement très efficace de l'épuration vis-à-vis des
matières oxydables. Avec une DCO de 27 mg/l, l'eau en sortie, est bien
inférieur à la norme de rejet fixée à 120 mg/l et
corresponds, effectivement, selon BLIEFERT et PERRAUD (2001) à la DCO
typique des eaux communales après épuration biologique.
La figure 18 illustre le rendement en DCO de chacun des quatre
bassins de la lagune de Béni-Messous.
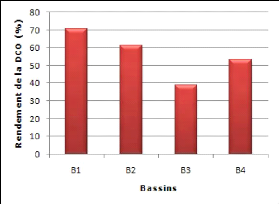
Figure 18 : Rendement en DCO des bassins de la station
d'épuration
par lagunage naturel de Béni-Messous.
6.6. La demande biologique en oxygène (DBO5) :

De façon analogue à la figure 17, la figure 18
illustre en termes de DBO5, l'importance de la pollution résiduelle
à travers les séries, DBO5Avf, DBO5ApF, et DBO5R.
Par rapport à la pollution globale sans filtration,
nous remarquons, avec les valeurs de la DBO5, de façon plus nette, la
part considérable que tient la pollution résiduelle ; avec plus
du double dans les bassins B3 et B4. Puisque la DBO5 donne uniquement la
représentation des matières biodégradables
présentes dans l'eau ; entre autre le phytoplancton en majorité
dans le cas du lagunage naturel, la mise en évidence de la pollution
résiduelle est meilleure qu'avec la DCO.
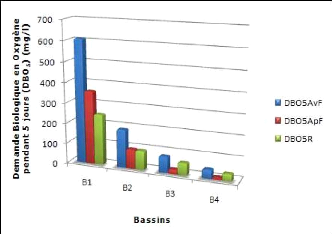
Figure 19 : DBO5 des bassins de la station
d'épuration par lagunage naturel de Béni-Messous.
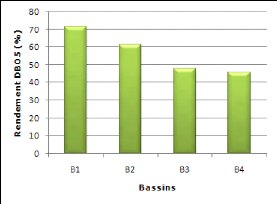
Figure 20 : Rendement en DBO5 des bassins de la station
d'épuration
par lagunage naturel de Béni-Messous.
En considérant la DBO5 après filtration, la
réduction des matières biodégradables est de 360 mg/l
à 9 mg/l ; ce qui représente un rendement global en DBO5 de 97,5
%. Tout comme les MES et la DCO, le rendement en DBO5 (voir figure 20), est
particulièrement important dans le premier (plus profond : 3m) bassin
où la majeur partie de la matière organique décante.
Bien en dessous de la valeur limite de rejet, 35 mg/l, l'eau
en sortie à une DBO5 de 9 mg/l ; ce qui se situe, d'après
BLIEFERT ET PERRAUD (2001), entre la DBO5 typique des cours d'eaux courantes,
modérément polluées, et celle des eaux communales
après traitement biologique.
6.7. La qualité de l'eau rejetée par la lagune
de Béni-Messous :
En tenant compte du classement de qualité des eaux
cité dans la section 5.6 du chapitre précédent et en se
basant sur les indicateurs DCO et DBO5 après filtration des
échantillons, l'eau rejetée par la lagune de Béni-Messous
sera du type 2 donc de qualité moyenne ; puisque l'eau en sortie est
caractérisée par une DCO de 27 mg/l et une DBO5 de 9 mg/l. Une
eau de cette catégorie est dite de pollution nette, c'est-à-dire,
une eau possédant des propriétés requises pour la vie
piscicole, mais où la reproduction du poisson est aléatoire, et
la production d'eau destinée à l'alimentation humaine
après traitement poussé (affinage et désinfection).
La DCO et la BDO5 de l'eau rejetée par la station son
respectivement compris entre 20 et 200 mg/l et entre 5 et 45 mg/l. Ce qui
encourage, selon VALENTINA LAZAROA et AKIÇA BAHRI (2005), sa
réutilisation pour l'irrigation. Cependant, il est nécessaire,
dans ce cas, pour évaluer davantage sa qualité, d'étudier
d'autres paramètres n'ayant pas fait l'objet de notre étude,
à savoir : la salinité, le rapport d'absorption du sodium (RAS),
les éléments traces (cadmium, aluminium, etc.), les ions
toxiques, les nutriments (N-P-K), ...
Conclusion :
Afin d'estimer de façon correcte la pollution, il faut
prendre le soin de déterminer, la pollution résiduelle
qu'engendre la présence des micro-algues, particulièrement
remarquable dans le cas d'une station d'épuration par lagunage naturel.
En effet, cette pollution, non négligeable peut être très
importante et influence donc l'appréciation de la véritable
charge polluante de l'eau épurée et de ce fait
l'interprétation des résultats.
L'état délaissé dans lequel la station
d'épuration par lagunage naturel de BéniMessous a
été trouvée n'a vraisemblablement pas influencé le
traitement. En effet, les résultats de l'analyse des paramètres
globaux de la pollution organique montrent que celle-ci rejette une eau
épurée de qualité satisfaisante ; sachant qu'une eau
épurée n'est considérée comme telle que lorsqu'elle
respecte les normes de rejets, ce qui est le cas pour tous les
paramètres étudiés.
L'efficacité du traitement durant notre étude a
été favorisée par l'absence d'écoulement des eaux
usées entre les bassins. Ce qui a permis, effectivement, aux eaux
usées de séjourner plus longtemps dans les bassins et donc de
s'épurer davantage.
L'eau du quatrième bassin est propice à la vie
piscicole mais son utilisation pour l'alimentation humaine requière des
traitements plus avancés, et sa réutilisation pour l'irrigation
nécessite l'analyse de paramètres spécifiques.



[on~~u~ion EiniriEIII

Nous avons tenté à travers ce travail de
déterminer la pollution résiduelle d'une station
d'épuration par lagunage naturel par l'analyse des paramètres
globaux d'estimation de la pollution organique des eaux usées.
Pour ce faire, nous avons tout d'abord choisi de regrouper
les informations pertinentes sur les eaux usées et leurs traitements
pour maitriser les principaux paramètres pouvant les
caractériser.
Nous avons aussi essayé d'établir un
état général de l'assainissement en Algérie pour
avoir une idée sur les différents procédés
utilisés dans notre pays. On retiendra, essentiellement, qu'au cours de
ces dernières années, le Ministère des Ressources en Eau
(MRE) à entrepris la mise en oeuvre d'un important programme
d'investissement concernant la réalisation, la réhabilitation ou
l'étude de réhabilitation de plusieurs stations
d'épuration ce qui permettra d'atteindre un parc de 194 STEP à
l'horizon 2010 dont 36 % seront représentés par le lagunage
naturel (DAPE, 2006).
Nous nous sommes ensuite penchés sur l'étude du
lagunage naturel en décrivant son principe de fonctionnement mais
également ses avantages, ses inconvénients et les
paramètres pouvant influencer son bon fonctionnement.
Après la description de la région de
Béni-Messous où est implantée la station
d'épuration par lagunage naturel sur la quelle nous avons choisi de
travailler, nous avons abordé les méthodes de
prélèvement, d'échantillonnage et de conservation des
échantillons d'eaux usées pour détailler ensuite les
méthodes d'analyses des paramètres étudiés à
savoir : la température, le pH, les MES, la DCO et la DBO5 ce qui a donc
permis de rassembler leurs protocoles d'analyse.
À l'issue du dernier chapitre qui présente les
résultats obtenus pour les échantillons prélevés de
la station étudiée, nous espérons avoir atteint l'objectif
qui vise l'appréciation de l'importance de la pollution
résiduelle d'une station d'épuration par lagunage naturel et la
qualité de l'eau qu'elle rejette. Cette dernière s'avère
dans le cas de la lagune de BéniMessous être satisfaisante,
confortant sa réutilisation surtout dans le cas ou l'eau potable se
raréfie de plus en plus.
Il nous semble utile, Cependant, de revenir sur quelques
points pouvant approfondir notre étude, à savoir :
· L'analyse de la chlorophylle pour quantifier la part de
la biomasse algale
dans la matière retenue par les filtres,
considérée dans notre cas majoritaire ;
· Suivre l'évolution de la pollution
résiduelle à l'issue de plusieurs prélèvements
répartis sur toute une saison par exemple ;
· Étudier la possibilité de
réutilisation de l'eau épurée de la station dans
l'irrigation des terres agricoles avoisinantes par l'étude davantage de
paramètres physicochimiques mais aussi microbiologiques.
· Faire des essais de grossissement d'espèces
piscicoles dans le bassin de sortie qui profiteront du phytoplancton
abondant.






Agence Nationale des Ressources Hydrauliques., 1996. Étude
de faisabilité du lagunage sur les hauts plateaux. 13p.
AMINOT A., CHAUSSEPIED M., 1983. Manuel des analyses chimiques en
milieu marin. CNEXO, 395p.
BADIA-GONDARD F., 2003. L'assainissement des eaux usées.
Edition techni.cités, 231p. BEAUDRY J.P., 1984. Traitement des eaux.
Edition le Griffon d'Aigle Inc, 231p.
BECHAC J.P., BOUTIN P., MERCIER B., NUER P., 1987. Traitement des
eaux usées. Edition Eyrolles, 281p.
BERNE F., CORDONIER J., 1991. Traitement des eaux. Edition
Technip, 306p.
BLIEFERT C., PERRAUD R., 2001. Chimie de l'environnement : Air,
Eau, Sols, Déchets. Edition de boeck, 477p.
BONTOUX J., 1993. Introduction à l'étude des eaux
douces : eaux naturelles, eaux usées, eaux de boisson. Edition Technique
et Documentation Lavoisier, 166p.
CHAIB A., 2004. Bioépuration par lagunage naturel.
Bulletin du Centre de Développement des Énergies Renouvelables
(CDER), N°5 Juin 2004, pp21.
DEGREMONT, 1978. Mémento technique de l'eau :
8ème édition. Edition Technique et Documentation
Lavoisier, 1200p.
DEGREMONT, 1989. Mémento technique de l'eau : vol. 1,
9ème édition. Edition Technique et Documentation
Lavoisier, 592p.




Direction de l'Assainissement et de la Protection de
l'Environnement (DAPE), 2006. Étude de réutilisation des eaux
épurées à des fins agricoles ou autres sur tout le
territoire national, Mission 1 : Reconnaissance et collecte des données
de base, 120p.
GAUJOUS D., 1995. La pollution des milieux aquatiques :
aide-mémoire. Edition Technique et Documentation Lavoisier, 220p.
GAUTHIER M., PIETRI C., 1998. Devenir des bactéries et
virus entériques en mer, Microorganismes dans les
écosystèmes océaniques. Edition Masson, 447p.
GOMELLA C., GUERREE H., 1978. Le traitement des eaux publiques,
industrielles et privées. Edition Eyrolles Paris, 262p.
GROSCLAUDE G., 1999. L'eau : usage et polluants. Edition INRA,
210p.
JOLY B., REYNAUD A., 2003. Entérobactéries :
systématiques et méthodes d'analyses. Edition Technique et
documentation, Paris, 356p.
Journal Officiel de la République Algérienne
(JORA). N°46, Juillet 1993. Journal Officiel de la République
Algérienne (JORA). N°26, Avril 2006.
JOLY B., REYNAUD A., 2003. Entérobactéries :
systématiques et méthodes d'analyses. Edition Technique et
documentation, Paris, 356p.
KOLLER E., 2004. Traitement des pollutions industrielles : eau,
air, déchets, sols, boues. Edition DUNOD, 424p.




LECLERC H., GAILLARD J.L., SIMONET M., 1995. Microbiologie
générale : la bactérie et le monde bactérien.
Edition Doin, 535p.
MARTIN G., LAFFORT P., 1991. Odeurs et désodorisation dans
l'environnement. Edition Technique et Documentation Lavoisier, 452p.
PNUE / OMS., 1979. Recommandation pour la surveillance
sanitaire des zones côtières à usage
récréatif et des zones conchylicoles. Bureau régional de
l'OMS pour l'Europe, Copenhague, 168p.
PEARSON H., 2005. Microbiology of waste stabilisation ponds. In:
A. SHILTON (Ed.) : pp.14-48. Pond Treatment Technology. London : IWA
Publishing.
REJSEK F., 2002. Analyse des eaux : Aspects Réglementaires
et Techniques. Edition SCEREM, 360p.
RODIER J., BAZIN C., CHAMBON P., BROUTIN J.-P., CHAMPSAUD H.,
RODI L., 1996. Analyse de l'eau : eaux naturelles, eaux résiduaires, eau
de mer, 8ème édition. Edition DUNOD, Paris. 1983p.
SATIN M., SELMI B., 1999. Guide technique de l'assainissement,
2ème édition. Edition LE MONITEUR, Paris, 680p.
SEVRIN-REYSSAC J., DE LA NOÜE J., PROULX D., 1995. Le
recyclage du lisier de porc par lagunage. Edition Technique et Documentation
Lavoisier, 118p.
VALIRON F., 1983. La réutilisation des eaux usées.
Edition Technique et Documentation Lavoisier, 207p.


Ann x 1







DONNÉES MÉTOROLOGIQUES
Station : ALGER DAR-EL-BEIDA
Altitude : 25 m - Latitude : 36°41 N - Longitude :
03°13 E
Précipitations : Précipitations mensuelles
et annuelles exprimées en millimètres (mm).
|
Jan.
|
Fév.
|
Mars
|
Avr.
|
Mai
|
Juin
|
Juil.
|
Août
|
Sept.
|
Oct.
|
Nov.
|
Déc.
|
An
|
|
1995
|
171
|
40
|
107
|
29
|
00
|
24
|
00
|
49
|
18
|
19
|
58
|
39
|
554
|
|
1996
|
94
|
232
|
57
|
161
|
36
|
32
|
07
|
04
|
38
|
86
|
27
|
34
|
808
|
|
1997
|
38
|
24
|
09
|
95
|
22
|
10
|
09
|
33
|
37
|
45
|
130
|
93
|
545
|
|
1998
|
29
|
52
|
37
|
76
|
151
|
01
|
00
|
08
|
22
|
49
|
103
|
82
|
610
|
|
1999
|
121
|
133
|
86
|
47
|
01
|
2
|
00
|
04
|
19
|
22
|
170
|
202
|
807
|
|
2000
|
16
|
06
|
19
|
17
|
53
|
0
|
01
|
01
|
04
|
47
|
74
|
41
|
279
|
|
2001
|
126
|
73
|
0
|
34
|
14
|
01
|
00
|
03
|
45
|
39
|
49
|
57
|
441
|
|
2002
|
39
|
15
|
34
|
39
|
14
|
00
|
00
|
34
|
12
|
54
|
145
|
102
|
488
|
|
2003
|
200
|
133
|
22
|
87
|
20
|
00
|
00
|
28
|
40
|
38
|
58
|
110
|
736
|
|
2004
|
90
|
46
|
79
|
56
|
149
|
01
|
02
|
01
|
12
|
43
|
116
|
109
|
704
|
|
2005
|
85
|
115
|
50
|
26
|
01
|
00
|
00
|
00
|
15
|
57
|
102
|
81
|
532
|
Températures : Températures maximales
moyennes exprimées en degrés Celsius (°C).
|
Jan.
|
Fév.
|
Mars
|
Avr.
|
Mai
|
Juin
|
Juil.
|
Août
|
Sept.
|
Oct.
|
Nov.
|
Déc.
|
An
|
|
1995
|
162
|
194
|
187
|
210
|
260
|
272
|
312
|
329
|
282
|
269
|
232
|
197
|
242
|
|
1996
|
190
|
156
|
189
|
204
|
233
|
267
|
308
|
310
|
272
|
231
|
216
|
197
|
231
|
|
1997
|
182
|
190
|
197
|
221
|
247
|
283
|
289
|
315
|
298
|
268
|
210
|
185
|
240
|
|
1998
|
179
|
192
|
197
|
216
|
230
|
279
|
315
|
320
|
301
|
247
|
203
|
18
|
225
|
|
1999
|
167
|
154
|
194
|
218
|
266
|
290
|
318
|
333
|
303
|
280
|
188
|
170
|
240
|
|
2000
|
147
|
191
|
203
|
230
|
258
|
275
|
322
|
338
|
295
|
252
|
217
|
198
|
244
|
|
2001
|
184
|
178
|
241
|
228
|
247
|
322
|
323
|
332
|
297
|
290
|
194
|
165
|
250
|
|
2002
|
178
|
186
|
213
|
221
|
266
|
297
|
306
|
308
|
297
|
259
|
216
|
194
|
245
|
|
2003
|
155
|
157
|
198
|
216
|
246
|
312
|
340
|
348
|
299
|
257
|
216
|
170
|
243
|
|
2004
|
174
|
184
|
184
|
213
|
219
|
288
|
312
|
337
|
317
|
292
|
198
|
176
|
241
|
|
2005
|
149
|
141
|
185
|
215
|
260
|
301
|
325
|
322
|
294
|
271
|
200
|
167
|
236
|
Températures : Températures minimales
moyennes exprimées en degrés Celsius (°C).
|
Jan.
|
Fév.
|
Mars
|
Avr.
|
Mai
|
Juin
|
Juil.
|
Août
|
Sept.
|
Oct.
|
Nov.
|
Déc.
|
An
|
|
1995
|
56
|
65
|
65
|
63
|
127
|
168
|
187
|
199
|
162
|
140
|
110
|
96
|
120
|
|
1996
|
95
|
70
|
78
|
99
|
106
|
158
|
182
|
203
|
159
|
111
|
95
|
81
|
120
|
|
1997
|
85
|
52
|
40
|
89
|
145
|
168
|
188
|
200
|
188
|
156
|
116
|
81
|
126
|
|
1998
|
62
|
63
|
58
|
92
|
127
|
154
|
180
|
194
|
189
|
112
|
96
|
55
|
115
|
|
1999
|
64
|
49
|
82
|
79
|
151
|
176
|
188
|
224
|
189
|
169
|
92
|
74
|
128
|
|
2000
|
21
|
41
|
68
|
99
|
149
|
162
|
201
|
199
|
174
|
129
|
100
|
74
|
118
|
|
2001
|
58
|
43
|
94
|
75
|
115
|
156
|
184
|
202
|
176
|
159
|
92
|
38
|
116
|
|
2002
|
47
|
36
|
67
|
84
|
109
|
161
|
186
|
195
|
165
|
133
|
106
|
85
|
115
|
|
2003
|
61
|
54
|
72
|
96
|
122
|
185
|
216
|
223
|
184
|
157
|
70
|
69
|
126
|
|
2004
|
57
|
61
|
79
|
85
|
110
|
155
|
210
|
209
|
179
|
153
|
95
|
74
|
122
|
|
2005
|
78
|
33
|
76
|
94
|
127
|
169
|
193
|
183
|
153
|
141
|
87
|
61
|
116
|



DONNÉES MÉTOROLOGIQUES (suite)
Évaporation : Évaporation, totaux mensuels
et annuels exprimés en millimètre (mm), mesurés sous abri
avec un évaporomètre Piche.
|
Jan.
|
Fév.
|
Mars
|
Avr.
|
Mai
|
Juin
|
Juil.
|
Août
|
Sept.
|
Oct.
|
Nov.
|
Déc.
|
An
|
|
1995
|
53
|
56
|
68
|
87
|
118
|
106
|
134
|
147
|
131
|
89
|
138
|
81
|
1208
|
|
1996
|
111
|
68
|
77
|
97
|
103
|
113
|
139
|
136
|
133
|
87
|
109
|
87
|
1260
|
|
1997
|
122
|
56
|
90
|
107
|
102
|
121
|
164
|
168
|
169
|
132
|
95
|
74
|
1400
|
|
1998
|
78
|
50
|
69
|
111
|
76
|
106
|
152
|
152
|
143
|
96
|
62
|
63
|
1158
|
|
1999
|
60
|
57
|
79
|
88
|
113
|
137
|
177
|
167
|
126
|
123
|
58
|
68
|
1253
|
|
2000
|
48
|
75
|
87
|
132
|
92
|
127
|
137
|
181
|
110
|
75
|
85
|
90
|
1239
|
|
2001
|
63
|
39
|
80
|
85
|
84
|
151
|
125
|
105
|
80
|
72
|
48
|
34
|
966
|
|
2002
|
35
|
40
|
64
|
72
|
104
|
94
|
93
|
85
|
90
|
71
|
65
|
50
|
863
|
|
2003
|
48
|
44
|
49
|
53
|
51
|
110
|
121
|
132
|
81
|
50
|
47
|
58
|
844
|
|
2004
|
46
|
37
|
43
|
61
|
48
|
84
|
90
|
141
|
107
|
95
|
38
|
40
|
830
|
|
2005
|
29
|
38
|
43
|
65
|
77
|
95
|
115
|
97
|
82
|
65
|
52
|
45
|
803
|
Ensoleillement : Ensoleillement, totaux mensuels et
annuels exprimés en heures (h).
|
Jan.
|
Fév.
|
Mars
|
Avr.
|
Mai
|
Juin
|
Juil.
|
Août
|
Sept.
|
Oct.
|
Nov.
|
Déc.
|
An
|
|
1995
|
178
|
223
|
236
|
280
|
308
|
269
|
381
|
333
|
251
|
199
|
177
|
139
|
2974
|
|
1996
|
145
|
124
|
221
|
200
|
295
|
307
|
320
|
290
|
259
|
251
|
223
|
144
|
2779
|
|
1997
|
129
|
228
|
308
|
234
|
261
|
335
|
300
|
299
|
257
|
221
|
153
|
160
|
2885
|
|
1998
|
188
|
201
|
244
|
248
|
244
|
314
|
364
|
301
|
241
|
233
|
159
|
173
|
2910
|
|
1999
|
146
|
175
|
213
|
313
|
259
|
253
|
348
|
287
|
271
|
237
|
142
|
154
|
2798
|
|
2000
|
226
|
251
|
256
|
262
|
260
|
334
|
330
|
327
|
252
|
215
|
188
|
170
|
3071
|
|
2001
|
164
|
205
|
251
|
276
|
263
|
363
|
343
|
300
|
261
|
237
|
170
|
161
|
2994
|
|
2002
|
206
|
202
|
236
|
243
|
302
|
291
|
304
|
273
|
258
|
238
|
145
|
153
|
2851
|
|
2003
|
131
|
130
|
221
|
227
|
265
|
328
|
279
|
296
|
238
|
184
|
136
|
134
|
2569
|
|
2004
|
209
|
172
|
169
|
242
|
201
|
312
|
312
|
393
|
253
|
213
|
196
|
148
|
2820
|
|
2005
|
193
|
143
|
160
|
213
|
289
|
303
|
333
|
315
|
261
|
248
|
175
|
165
|
2798
|
Vents : Vitesse des vents, moyenne mensuelles et annuelles
en (m/s).
|
Jan.
|
Fév.
|
Mars
|
Avr.
|
Mai
|
Juin
|
Juil.
|
Août
|
Sept.
|
Oct.
|
Nov.
|
Déc.
|
An
|
|
1995
|
23
|
17
|
21
|
20
|
22
|
28
|
24
|
23
|
22
|
12
|
24
|
29
|
22
|
|
1996
|
29
|
36
|
28
|
28
|
24
|
24
|
22
|
20
|
22
|
13
|
24
|
20
|
24
|
|
1997
|
26
|
12
|
15
|
21
|
21
|
21
|
27
|
23
|
20
|
18
|
29
|
19
|
21
|
|
1998
|
22
|
12
|
14
|
26
|
21
|
21
|
21
|
21
|
25
|
17
|
18
|
13
|
19
|
|
1999
|
20
|
22
|
20
|
16
|
28
|
28
|
28
|
32
|
28
|
26
|
24
|
33
|
25
|
|
2000
|
12
|
19
|
21
|
43
|
25
|
25
|
32
|
32
|
28
|
28
|
33
|
32
|
28
|
|
2001
|
33
|
24
|
31
|
30
|
33
|
33
|
31
|
25
|
30
|
19
|
20
|
14
|
27
|
|
2002
|
15
|
20
|
28
|
27
|
31
|
31
|
31
|
24
|
29
|
24
|
30
|
28
|
27
|
|
2003
|
40
|
34
|
20
|
27
|
25
|
28
|
27
|
25
|
24
|
20
|
25
|
33
|
27
|
|
2004
|
24
|
20
|
23
|
32
|
31
|
24
|
24
|
24
|
20
|
16
|
16
|
32
|
24
|
|
2005
|
20
|
26
|
21
|
30
|
27
|
28
|
35
|
31
|
24
|
20
|
21
|
23
|
26
|



CONSERVATION DES PRÉLÈVEMENTS
|
Caractéristique
ou
élément
analysé
|
Réci-
pient
|
Conservateur
à
utiliser
|
Volume
minimum
du
prélèvement
(en mL)
|
Température
de conser-
vation (en
°C)
|
Effectuer
la mesure
avant ...
|
|
Acidité-alcalinité
|
P ou Vb
|
0
|
200
|
4
|
24h (obsc)
|
|
Ammonium
|
P ou V
|
0
Acide sulfurique
q.s.p. pH < 2
|
|
4
|
48h (obsc)
quelques jours
(obsc)
|
|
Anhydride carbonique
|
|
Mesure in situ
|
|
4
|
|
|
AOX
|
Vb
|
0
|
500
flacon rempli
complètement
et
bouché
|
4
|
|
|
Arsenic, Sélénium, Titane, Vanadium.
|
P ou V
|
Acide nitrique
q.s.p. pH < 2
|
-
|
-
|
2 mois
|
|
Azote kjeldahl
|
P ou V
|
0
|
1000
|
4
|
48h (obsc)
|
|
|
Acide sulfurique
q.s.p. pH < 2
|
|
4
|
plusieurs semaines
(obsc)
|
|
Bore
|
P
|
|
|
|
|
|
Carbone Organique Total
|
Vb
|
0
passé 1 h à 400°C
|
500
|
4
|
quelques jours
(obsc)
|
|
V
|
Acide sulfurique
q.s.p. pH < 2
|
100
|
4
|
24 h (obsc)
|
|
Chlorophylle
|
V brun
|
|
1000
|
4
|
(*)
|
|
Chlorures
|
P ou V
|
0
|
100
|
-
|
15 jours
|
|
Composés organiques non volatils :
|
|
|
|
|
|
|
- organo-halogénés
|
V
|
0
|
1000
|
4
|
(**)(obsc)
|
|
- organo-phosphorés
|
V
|
0
|
1000
|
4
|
48h (obsc)
|
|
- organo-azotés
|
V
|
0
|
1000
|
4
|
quelques jours
|
|
|
|
|
|
(obsc)
|
|
Composés organiques volatils
|
V bouchon
serti
|
|
|
4
|
quelques jours
(obsc)
|
|
Conductivité
|
P ou V
|
Mesure in situ
de préférence
|
100
|
4
|
48h (obsc)
|
|
Cyanures totaux
|
P
|
Hydroxyde de sodium
q.s.p. pH > 10
|
500
|
4
|
quelques semaines
(obsc)
|
|
Cyanures libres
|
P
|
Hydroxyde de sodium
q.s.p. pH > 10
|
500
|
4
|
48h (obsc)
|
|
DBO
|
P ou V
|
0
|
1000
|
4
|
24h
|
|
DCO
|
P ou V
|
Acide sulfurique
q.s.p. pH < 2
|
100
|
4
|
24h (obsc)
|
|
Dureté
|
P ou V
|
Acide nitrique
q.s.p. pH < 2
|
100
|
-
|
1 mois
|
|
Fer
|
P
|
(voir texte)
|
-
|
-
|
-
|
|
Fluorures, Bromures
|
P
|
0
|
300
|
-
|
7 jours
|
|
Iodures
|
V
|
|
|
4
|
48h (obsc)
|
|
Huiles et graisses
|
V
|
Acide chlorhydrique
q.s.p. pH < 2
|
1000
|
4
|
15 jours
|
|
Hydrocarbures (indice)
|
V
|
Tétrachlorure
de carbone (10 mL)
|
800
|
4
|
6 jours (obsc)
|
|
Hydrocarbures polycycliques
|
V
|
Hexane (10 mL)
|
1000
|
4
|
6 jours (obsc)
|
|
Lithium, Sodium, Potassium,
|
|
|
|
|
|
|
Calcium, Magnésium, Strontium, Baryum
|
V
|
Acide nitrique
|
800
|
-
|
Plusieurs mois
|



CONSERVATION DES PRÉLÈVEMENTS (suite)
|
Caractéristique
ou
élément
analysé
|
Réci-
pient
|
Conservateur
à
utiliser
|
Volume
minimum
du
prélèvement
(en mL)
|
Température
de conser-
vation
(en°C)
|
Effectuer
la mesure
avant ...
|
|
Aluminium, Argent, Cadmium,
|
|
|
|
|
|
|
Chrome, Cuivre, Manganèse, Plomb, Zinc, Cobalt, Nickel,
Étain
|
P ou V
|
Acide nitrique
q.s.p. pH < 1,5
|
-
|
-
|
2 mois
|
|
Mercure
|
Vb
|
Acide nitrique
q.s.p. pH < 1,5
|
-
|
-
|
1 mois
|
|
|
+ Permanganate
de potassium
|
|
|
|
|
Nitrates
|
P ou V
|
0
|
|
4
|
48h (obsc)
|
|
|
Acide sulfurique
|
|
4
|
plusieurs semaines
|
|
|
q.s.p. pH < 2
|
|
4
|
(obsc)
|
|
Nitrites
|
P ou V
|
0
|
|
4
|
48h (obsc)
|
|
Matières en suspension
|
P ou V
|
0
|
1000
|
4
|
6h (obsc)
|
|
Odeur, Couleur, Saveur
|
V
|
0
|
500
|
4
|
24h
|
|
Oxygène Dissous
|
Vb
|
Mesure in situ
de préférence
|
300
|
4
|
24h (obsc)
|
|
Pesticides
|
V
|
0
|
2000
|
4
|
7 jours (obsc)
|
|
pH
|
P ou V
|
Mesure in situ
de préférence
|
-
|
4
|
24h (obsc)
|
|
Phénol (indice)
|
P ou V
|
Soude pH = 12
|
500
|
4
|
quelques jours
|
|
|
|
|
|
(obsc)
|
|
|
1 g/L de sulfate de cuivre
|
|
4
|
7 jours
|
|
|
+ acide phosphorique
q.s.p. pH < 2
|
|
|
|
|
Phosphates (Ortho, Poly et P total)
|
P ou V
|
0
|
100
|
4
|
48h (obsc)
|
|
|
Acide sulfurique
q.s.p. pH < 2
|
100
|
4
|
1 semaine
|
|
Radioactivité
|
P
|
0
|
1000
|
-
|
15 jours
|
|
Résidu
|
P ou V
|
-
|
500
|
4
|
7 jours
|
|
S.E.C.
|
V
|
Chlorure mercurique
|
variable
|
4
|
48h
|
|
|
(40 mg/L) ou
chloroforme (1 mL/L)
|
|
|
|
|
Silice
|
P
|
-
|
50
|
4
|
7 jours (obsc)
|
|
Sulfates
|
P ou V
|
-
|
200
|
4
|
7 jours
|
|
Sulfites, Sulfures
|
P
|
Prélèvement avec
flacon spécial
acétate
de zinc (pH 12 + soude)
|
100
|
4
|
plusieurs semaines
|
|
|
(voir texte)
|
|
|
|
|
Surfactifs (détergents anioniques et non ioniques)
|
V
|
Chloroforme (1 mL/L)
|
200
|
4
|
24h (obsc)
|
|
TA-TAC, TH
|
P ou V
|
Mesure in situ
de préférence
|
200
|
4
|
24h (obsc)
|
|
Turbidité
|
P ou V
|
-
|
100
|
4
|
24h (obsc)
|
|
Coliformes totaux
|
P ou V
|
Flacons stériles (***) (en
présence d'une eau
traitée
par un oxydant, ajouter
|
250
|
4
|
24h (obsc)
|
|
Coliformes fécaux Streptocoques fécaux
|
P ou V
P ou V
|
avant stérilisation 5 gouttes d'une solution de tio-
sulfate de sodium à 10%)
|
250
250
|
4
4
|
24h (obsc)
24h (obsc)
|
|
|
P : Polyéthylène V : Verre Vb : Verre
borosilicaté généralement bouché émeri obsc
: obscurité
|
|
(*) Voir norme AFNOR T 90-116 et T 90-117. (**) Voir norme AFNOR
T 90-120 et T 90-125.
|
|
(***) Les flacons en verre peuvent être
stérilisés au Four Pasteur à 180°C pendant 1 h 30 ou
à l'autoclave à 120°C pendant 1 h. les flacons
|
|
en polyéthylène peuvent être
stérilisés par irradiation (25 kGy soit 2,5 Mrad).
|
SOURCE : RODIER J., BAZIN C., CHAMBON P., BROUTIN J.-P.,
CHAMPSAUD H., RODI L., 1996.
Analyse de l'eau : eaux naturelles, eaux résiduaires, eau
de mer, 8ème édition. Edition DUNOD, Paris, 1983p.



PROTOCOLE DE NETTOYAGE DE LA VAISSELLE DE LABORATOIRE
1- Domaine d'application :
Ce protocole concerne toute la vaisselle utilisée au
laboratoire mais aussi le matériel nécessitant un
prétraitement avant utilisation.
2- Nettoyage de la vaisselle :
Toute la vaisselle utilisée au laboratoire doit
être rincée après utilisation à l'eau courante, puis
à l'eau déminéralisée. Après passage
à l'eau déminéralisée la vaisselle est
placée à l'étuve à 60°C, pendant au minimum
une nuit, puis rangée.
Dans le cas où la vaisselle est très sale, il
est nécessaire de la laisser tremper une nuit dans un bac de
détergent, de la rincer à l'eau courante et de la laisser tremper
une autre nuit dans des bacs d'acide (H2SO4 1%). La suite du rinçage
avant séchage se fait comme énoncé
précédemment.
De même pour les tubes ayant servi à un dosage,
il est nécessaire de les rincer à l'eau courante et de les
laisser tremper 24h dans des bacs à acide avant de les rincer à
l'eau et de les faire sécher à l'étuve.
Remarque : toutes les indications portées sur la
verrerie ou les éventuelles étiquettes doivent être
supprimées lors du nettoyage.
VERRERIE USUELLE
Burette Pipette Éprouvette Becher Erlenmeyer Fiole
graduée graduée jaugée

Ann x 5

ÉTIQUETAGE DES ÉCHANTILLONS
Les échantillons destinés au laboratoire doivent
être désignés de façon claire et durable afin de
permettre leur identification sans ambigüités. On distingue de
types de désignations possibles :
· soit les flacons sont désignés par une
étiquette où sont indiquées l'origine de
l'échantillon et les conditions dans lesquelles il a été
prélevé ;
· soit il est possible de simplifier cette opération
en utilisant un système d'étiquettes numérotées ou
codées.
Afin d'éviter les oublis lors du remplissage de
l'étiquette, l'ensemble de ses champs doit être renseigné
comme suit :
- La désignation de la station et du site
échantillonné est indispensable ;
- La date et l'heure sont très importants car ils
constituent une clé d'entrée pour retrouver l'échantillon
;
- L'origine de l'eau présente d'une part le type d'eau
prélevée (eau de surface, rejet, ...), et le milieu
consterné (rivière, canal, ...) d'autre part ;
- Le nom du préleveur ;
- Les analyses à effectuer ou le nombre de
paramètres à analyser ;
- Si un produit (conservateur) a été introduit,
cela doit être mentionné.
Station : N° de code :
Site : N° de code :
Date : Heure :
Origine de l'eau :
Nom du préleveur :
Analyses à effectuer :
Conservateur :
Il est recommandé, par souci de simplicité,
d'utiliser un système d'étiquettes codées. Le code du
flacon est reporté sur une fiche comme sur l'exemple
représenté dans la figure suivante :




PRÉPARATION DES RÉACTIFS NÉCESSAIRES
POUR
LA DÉTERMINATION DE LA DCO
1- Solution de dichromate de potassium (K2Cr2O7)
à 0,040 mol/l contenant du sulfate de mercure (II) :
· Dissoudre 80 g de sulfate de mercure dans 800 ml d'eau
déminéralisée ;
· Ajouter avec précaution 100 ml d'acide sulfurique
(H2SO2) concentré (ñ = 1,84) ;
· Laisser refroidir et ajouter 11,767 g de dichromate de
potassium préalablement séché à 105 °C pendant
2 h ;
· Transvaser dans une fiole jaugée d'un litre et
compléter au volume avec de l'eau distillée.
o Cette solution reste stable pendant 1 mois.
2- Solution d'acide sulfurique et sulfate d'argent :
· Ajouter 10 g de sulfate d'argent (Ag2SO4) à 40 ml
d'eau distillée ;
· Mélanger avec 960 ml d'acide sulfurique (H2SO2)
concentré (ñ = 1,84) ;
· Agiter et laisser refroidir.
o Laisser reposer 1 à 2 jours.
3- Solution de sulfate de fer (II) et d'ammonium (sel de Mohr)
[(NH4)2Fe(SO4)2 6H2O)] 0,12 mol/l :
· Dissoudre 47 g de sulfate de fer (II) et d'ammonium dans
de l'eau déminéralisée ;
· Ajouter 20 ml d'acide sulfurique (H2SO2) concentré
(ñ = 1,84) ;
· Laisser refroidir et diluer à 1000 ml.
o Cette solution doit être étalonnée
journellement.
4- Solution d'indicateur coloré (Ferroïne) :
· Dissoudre 0,7 g de sulfate de fer (II) dans de l'eau
distillée ;
· Ajouter 1,50 g de phénanthroline-1,10
monohydraté ;
· Diluer à 100 ml.
5- Solution d'hydrogénophtalate de potassium
(KC8H5O4) à 2,0824 mmol/l :
· Dissoudre 0,4253 g d'hydrogénophtalate de
potassium, préalablement séché à 105°C dans de
l'eau distillée et diluer jusqu'à 1000 ml dans une fiole
jaugée.
o Cette solution à une DCO théorique de 500 mg/l
et est stable au moins une semaine à 4°C.
6- Granules :
· Ce sont des régulateurs d'ébullition :
pierres ponce ou billes de verre.
SOURCE : REJSEK F., 2002. Analyse des eaux : Aspects
Réglementaires et Techniques. Edition SCEREM, 360p.



FICHE D'ANALYSE DE LA DBO5
Nom : Date :
Gammes d'estimation :
|
DBO (mg/l)
|
Prise d'essai (ml)
|
Facteur
|
|
0 ... 40
|
432
|
1
|
|
0 ... 80
|
365
|
2
|
|
0 ... 200
|
250
|
5
|
|
0 ... 400
|
164
|
10
|
|
0 ... 800
|
97
|
20
|
|
0 ... 2000
|
43,5
|
50
|
|
0 ... 4000
|
22,7
|
100
|
Mesure :
|
Échantillon
|
1
|
2
|
3
|
4
|
5
|
|
Station
|
|
|
|
|
|
|
Gamme de mesure
|
|
|
|
|
|
|
Prise d'essai
|
|
|
|
|
|
|
Dilution
|
|
|
|
|
|
|
Facteur
|
|
|
|
|
|
|
Lecture (chiffre)
|
|
|
|
|
|
|
Valeur de la DBO5
|
|
|
|
|
|
|
DBO5 si dilution
|
|
|
|
|
|
|
Remarques :
|



RÉSULTATS DES ANALYSES
Date de prélèvement et de début d'analyse :
06 Juin 2007
|
Station
|
E1
|
E2
|
E3
|
E4
|
S
|
|
Température (°C)
|
21,5
|
21,3
|
22,5
|
23,1
|
23,3
|
|
pH
|
7,3
|
7,5
|
8,7
|
8,65
|
7,75
|
|
MES (mg/l)
|
192
|
36
|
18
|
10
|
6
|
|
DCO
(mg/l)
|
Avant filtration
|
1180,4
|
345,6
|
134,4
|
82
|
38,4
|
|
Après filtration
|
710,4
|
201,6
|
68
|
34
|
20
|
|
DBO5
(mg/l)
|
Avant filtration
|
950
|
270
|
105
|
55
|
30
|
|
Après filtration
|
560
|
160
|
30
|
12
|
6
|
|
Bassins
|
-
|
B1
|
B2
|
B3
|
B4
|
-
|
|
Température (°C)
|
-
|
21,4
|
21,9
|
22,8
|
23,2
|
-
|
|
pH
|
-
|
7,4
|
8,1
|
8,7
|
8,2
|
-
|
|
MES (mg/l)
|
-
|
114
|
27
|
14
|
8
|
-
|
|
Rendements MES (%)
|
-
|
81,25
|
50
|
44,45
|
40
|
-
|
|
DCO
(mg/l)
|
Avant filtration
|
-
|
763
|
240
|
108,2
|
60,2
|
-
|
|
Après filtration
|
-
|
456
|
134,8
|
51
|
27
|
-
|
|
ÄDCO (mg/l)
|
-
|
307
|
105,2
|
57,2
|
33,2
|
-
|
|
Rendements DCO (%)
|
-
|
70,7
|
61,1
|
39
|
53,2
|
-
|
|
DBO5
(mg/l)
|
Avant filtration
|
-
|
610
|
187,5
|
80
|
42,5
|
-
|
|
Après filtration
|
-
|
360
|
95
|
21
|
9
|
-
|
|
ÄDBO5 (mg/l)
|
-
|
250
|
92,5
|
59
|
33,5
|
-
|
|
Rendements DBO5 (%)
|
-
|
71,6
|
61,1
|
47,6
|
45,5
|
-
|
| 


