I.2.B.1. Détermination de la courbe
d'étalonnage :
Afin de caractériser la libération du PA
encapsulé, nous avons appliqué la spectrophotomètrie
UV-Visible, à cause de l'absorption de l'oxacilline sodique dans le
domaine de l'UV ; ceci nécessite la détermination de la courbe
d'étalonnage et de connaître la longueur d'onde pour l'absorption
maximale de l'oxacilline sodique.
Principe :
L'absorption moléculaire dans le spectre ultraviolet
(UV) et visible dépend de la structure électronique de la
molécule. L'absorption d'énergie est quantifiée et
résulte du passage des électrons d'orbitales de l'état
fondamental vers des orbitales d'un état excité d'énergie
supérieur.
Une expression plus adéquate de l'intensité
d'absorption est celle dérivée de la loi de Beer-Lambert, qui
établit la relation entre l'absorbance, l'épaisseur de
l'échantillon et la concentration des espèces absorbantes.
Cette relation s'écrit :
A= log (I0/I) = å bC
Avec :
A : Absorbance ou densité optique ;
I0 : Intensité de l'énergie d'irradiation arrivant
sur l'échantillon ;
I : Intensité de la radiation qui a traversée
l'échantillon ;
å : Constante caractéristique du
soluté (coefficient d'absorption moléculaire ou d'extinction
molaire : mol-1.l. cm-1) ;
b : Longueur du chemin optique à travers
l'échantillon (cm) ;
C: Concentration du soluté (mol.l-1).
Ou bien :
A= log (I0/I) = abC
Avec :
a: Absorptivité (g-1.l.
cm-1) ;
C: Concentration du soluté (g.l-1).
Mode opératoire :
- Préparer quatre solutions de l'oxacilline sodique de
concentrations suivantes : 0.01 mg/ml, 0.005 mg/ml, 0.00125 mg/ml, 0.000625
mg/ml ;
- Remplir la cuvette en quartz avec la solution ;
- Utiliser la même cuvette pour l'échantillon et
pour le blanc ;
- Mesurer l'absorbance de chaque solution ainsi pour le blanc, en
utilisant la longueur d'onde d'absorption maximale (ë max de
l'oxacilline sodique égale à 235 nm) (Anonyme 7)
;
-Tracer la courbe d'étalonnage
à partir de la moyenne des lectures obtenues avec les différentes
solutions ;
- Déterminer la concentration de l'oxacilline sodique dans
la solution à examiner à l'aide de la courbe obtenue.
I.2.B.2. Préparation des sphères de
l'oxacilline sodique :
Principe :
Le principe de la microencapsulation consiste à former
une mince paroi polymérique au tour des gouttelettes ou des particules
du produit en suspension de microcapsule dont la taille varie entre un et
plusieurs centaines de microns. Le polymère utilisé peut
être naturelle ou synthétique.
Le procédé utilisé pour la
préparation des microsphères est le procédé de
gélification des gouttes, le choix de ce procédé est
basé sur la simplicité et sur disponibilité du
matériel nécessaire à ce niveau.
Mode opératoire :
A/ Préparation de la solution d'acide alginique :
Mélanger 3 g d'acide alginique dans 25 ml d'eau
distillé, faire l'agitation à laide d'un barreau
magnétique.
B/ Préparation de la solution d'hydroxyde de sodium :
Dissoudre 1.66 g d'hydroxyde de sodium dans 25 ml d'eau
distillé.
C/ Préparation de la solution d'alginate de sodium et
d'oxacilline sodique :
- Mélanger les solutions préparées en (A) et
(B) sous agitation magnétique ;
- Mélanger 50 mg d'oxacilline sodique (PA) avec la
solution précédente (alginate de sodium), agiter jusqu'à
ce que la solution devienne homogène.
D/ Préparation de la solution du chlorure de calcium :
Dissoudre 0.325 g de chlorure de calcium (CaCl2) dans 25 ml d'eau
distillée.
E/ À l'aide d'une seringue goutter 2 ml de la solution
préparée en (C) dans une boitte de pétrie remplie
préalablement par la solution de chlorure de calcium.
F/ Laisser la préparation quelques minutes pour que les
sphères se solidifient, filtrer à l'aide des papiers filtres,
rincer les sphères par quelques ml d'eau distillé, pour
éliminer l'excès de CaCl2, mesurer l'absorbance de filtrat pour
calculer le rendement d'encapsulation.
Les étapes du procédé de formulation des
sphères sont schématisées dans la figure 28.
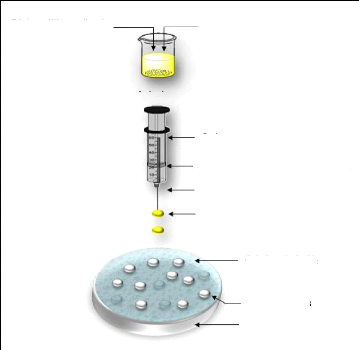
PA (oxacilline sodique) Alginate de sodium
Agitation
Seringue
Mélange d'alginate de sodium
et le PA
Aiguille de la seringue Gouttelettes de mélange
Solution de CaCl2
Sphères formés Boite de Pétri
Figure (28) : Etapes de préparation
des sphères.
| 


