0. INTRODUCTION
Les syndromes hypertensifs gravidiques forment un groupe
hétérogène d'états pathologiques dont le
dénominateur commun est une augmentation de la pression
artérielle (PA) pendant la grossesse. Ces états pathologiques
concernent 10 à 15% des grossesses et sont encore
responsables de 30% des décès maternels et de
20% de la mortalité foetale et néonatale (1).
Toute HTA survenant sur une grossesse, multiplie par trois le
risque de RCIU et de MFIU et ce risque est multiplié par 20
en cas de Pré-éclampsie surajoutée ou pas (2).
L'HTA retentit aussi bien sur la santé de la mère, que sur celle
du foetus. Il y a donc un double objectif à gérer : La survie de
l'enfant souvent prématuré et si possible sans séquelles
cérébrales et la survie maternelle, en évitant autant que
faire se peut, la survenue des complications souvent mortelles.
Pour réaliser ce double objectif, il faut une
équipe pluridisciplinaire comprenant obstétriciens,
anesthésiste-réanimateurs et pédiatres. Cette
équipe n'est pas toujours facile à réunir, surtout dans
les pays sous-développés dont fait partie le Burundi, en raison
de la pénurie du personnel médical et du sous équipement
en infrastructures sanitaires.
La réduction de la morbi-mortalité materno-foetale
due à l'association HTA et grossesse, observée dans les pays
développés n'est pas uniquement due à des progrès
thérapeutiques, mais elle est en grande partie due à une
surveillance bien planifiée
permettant une détection précoce des signes
avant-coureurs de complications potentiellement dangereuses et d'intervenir
avant que la situation ne dégénère.
Nos objectifs sont :
1. Analyser les aspects épidémiologique, clinique,
biologique et thérapeutique de l'association HTA et grossesse au CHU de
Kamenge,
2. Proposer des recommandations afin d'améliorer le
pronostic materno-foetale.
1. Généralités.
1.1 .définition.
L'HTA au cours de la grossesse est définie par une TA
systolique =140mm Hg et/ou une TA diastolique = 90 mm
Hg à au moins deux reprises mesurée au repos en position
de décubitus latéral gauche ou en position assise (1, 2, 3, 4,
5,6).
Physiologiquement, la pression artérielle baisse au cours
du 1er et du 2ème trimestre de la grossesse, du fait d'une
vasodilatation artérielle plus marquée que
l'élévation du débit cardiaque. Elle remonte à la
fin du 2ème trimestre pour atteindre les valeurs d'avant la
grossesse au 3ème trimestre. Ainsi une HTA chronique
méconnue peut passer inaperçue lors des prises de TA durant les 2
premiers trimestres de la grossesse. L'HTA gestationnelle pourrait aussi
être définie par une augmentation de la tension systolique de 30
mm Hg ou de la tension diastolique de 15mmHg par comparaison aux valeurs
obtenues avant 20 SA (6).
1.2. Classification.
On distingue 4 types selon le moment où l'HTA ou la
protéinurie surviennent (5,6).
|
Terme
|
HTA <20 SA
|
HTA >20 SA
|
|
Pas de protéinurie
|
HTA chronique
|
HTA gravidique
|
|
Protéinurie >0,3g/24H
|
Pré-éclampsie surajoutée
|
Pré-éclampsie
|
- HTA chronique : Elle est préexistante à
la grossesse, mais parfois peut être méconnue. Il faut alors
l'évoquer si l'HTA apparait avant 20SA ou si elle persiste 12 semaines
après l'accouchement. Elle touche souvent les femmes d'âge
mûr et son pronostic est bon en l'absence de Pré-éclampsie
surajoutée
- Pré-éclampsie surajoutée : elle
est définie par une HTA chronique compliquée par une
protéinurie (>300mg/24heures) apparue après la
20ème SA. Le pronostic materno-foetal est mauvais.
-HTA gravidique : elle est définie par une HTA
isolée apparue à partir de la 20éme SA, sans
protéinurie. Elle a tendance à apparaître en fin de
grossesse et à récidiver. Le pronostic foetal est bon, mais
évolue à long terme vers une HTA chronique
-Pré-éclampsie : Elle associe une HTA et
une protéinurie à partir de la 20ème SA. Dans
certains cas, une protéinurie peut manquer initialement, mais il est
licite de suspecter une Prééclampsie devant une HTA apparue de
novo associée à l'un ou l'autre des signes suivant (7) :
4 OEdèmes d'apparition brutale ou rapidement
aggravés.
4 uricémie > 350umol/L.
4 une élévation des transaminases au
delà des normes du laboratoire.
4 une thrombopénie (< 150.000 /ml)
4 un retard de croissance in utero (RCIU).
La pré-éclampsie sévère se
définit soit (7,8) :
*par la gravité de la tension artérielle (PAS
= 160 mm Hg et/ou PAD =110 mm Hg) ou
*par l'existence de un ou plusieurs des signes suivants
quelque soit le degré de la tension artérielle :
* douleurs épigastriques, nausées,
vomissements ; * céphalées persistantes,
*hyper-réflectivité
ostéo-tendineuse,
*Troubles visuels (scotomes scintillants, amaurose) et/ou
auditifs (acouphènes) *oligurie < 20 ml/h,
*Protéinurie > 3,5 g/24H,

*Créatinémie > 100 mol/L ;
*hémolyse (présence de schizocytes à
la GE, LDH > 600UI/l *Thrombopénie (< 100
000/mm-3);
*ASAT > à trois fois la norme du
laboratoire
1.3. Epidémiologie et facteurs de risque.
Les données permettant de préciser l'incidence et
les facteurs de risque sont relativement difficiles à analyser en raison
de l'inhomogénéité des données de la
littérature. Principale complication de la grossesse, l'HTA touche
10 à 15% des femmes enceintes (7). Elle fait partie du
tableau clinique d'un groupe d'affections comprenant la
prééclampsie, l'éclampsie, l'HTA chronique et l'HTA
gravidique transitoire. La pré-éclampsie est la plus dangereuse
de ces affections et se déclare chez environ 3 à 7%
des primigestes et chez 1 à 3 % chez les
multipares (6,7). Aucun élément ne permet actuellement de
prédire, en début de grossesse, la survenue de la
pré-éclampsie. Un certain nombre de facteurs de risque sont
classiquement reconnus (7,8) :
4 génétiques : des
antécédents de pré-éclampsie chez la mère ou
la soeur font augmenter l'incidence d'un facteur de 3 à 5 ;
4 Immunologiques : la primiparité, le
changement de géniteur ou l'insémination avec le sperme d'un
donneur. La brève exposition aux spermes du père apparaît
comme un facteur de risque important.
4 physiologiques : âge < 18 ans ou
> 40 ans
4 environnementaux : vie en altitude, stress
physique et psychologique ;
4 liées aux pathologies maternelles :
antécédent de pré-éclampsie,
l'obésité, le diabète, les thrombophilies, l'HTA, les
affections auto-immunes et les néphropathies chroniques ;
4 liées à la grossesse : un
intervalle long entre les grossesses, une grossesse multiple, anomalies
congénitales ou chromosomiques du foetus, anasarque foetale et
l'infection urinaire.
1.4. Physiopathologie de l'HTA gravidique.
Il faut d'emblée distinguer deux formes cliniques dont
la physiopathologie est
différente:
?L'HTA chronique : c'est-à-dire
préexistante à la grossesse ou découverte avant la 20eme
SA. Essentielle ou secondaire à une pathologie vasculo-rénale ou
à une endocrinopathie, elle nécessite un bilan simple et un
traitement en fonction des chiffres tensionnels. La seule hantise reste la
survenue d'une pré-éclampsie surajoutée, qu'il faut
rechercher tout au long de la grossesse et qu'il faut surveiller comme de
l'huile sur le feu.
?L'HTA est liée spécifiquement à la
grossesse. Elle apparaît dès la 20ème SA et
disparaît en général avant le 42ème jour
post-partum. L'HTA est ici un élément d'une maladie
multi systémique qui évolue à bas bruits
depuis plusieurs mois, lorsque l'hypertension apparaît. La survenue
d'une protéinurie annonce une
pré-éclampsie, qui peut être immédiatement
grave pour la mère et/ou le foetus. Sa physiopathologie demeure
aujourd'hui mal connue. Des progrès récents axés sur une
pathologie précoce de l'endothélium, liée à un
trouble de la placentation, ont permis une avancée significative des
connaissances.
1.4. 1. Anomalies de la placentation et ischémie
placentaire.
L'anomalie initiale menant à l'hypertension
artérielle et ses complications est un trouble précoce
de l'invasion trophoblastique endovasculaire (9). En effet, dans
l'utérus non gravide, les artères spiralées qui
perfuseront le placenta pendant la grossesse sont de petites artères
musculaires typiques. Pendant la grossesse normale, ces vaisseaux sont
considérablement modifiés entre la 2ème et
22ème semaine de gestation. Le diamètre luminal
est multiplié par 4 et le muscle lisse de la paroi vasculaire
disparaît.
En effet, durant le développement placentaire normal, le
cytotrophoblaste envahit les artérioles spiralées maternelles,
les remodèle complètement pour former des vaisseaux à
grande capacitance avec une faible résistance. Cette invasion
endovasculaire du cytotrophoblaste implique le remplacement non seulement de
l'endothélium mais aussi de la tunique musculaire "média" (10).
Cela entraîne outre la perte des récepteurs aux substances
vaso-actives, une dilatation passive considérable, qui permet
l'accroissement de débit nécessaire au bon déroulement de
la grossesse.
En cas de pré-éclampsie les modifications
physiologiques vasculaires sont incomplètes, inconstantes voir absentes.
Certains vaisseaux sont remodelés mais jamais au delà de la
limite muqueuse de l'utérus, alors que dans la grossesse normale ces
modifications s'étendent au tiers interne du myomètre. Nombreux
sont les vaisseaux qui ne sont pas remodelés (11).
En effet, au cours de la pré-éclampsie, la vague
d'invasion vasculaire trophoblastique du début du second
trimestre est habituellement réduite ou absente. Les
artères utéro-placentaires sont plus fines que normalement et ont
conservé une média avec de ce fait un certain degré de
contractilité (7). L'effet net est une distension insuffisante de la
paroi vasculaire artérielle, notamment à la phase tardive de la
grossesse lorsque la demande est plus importante. Il en résulte un
débit insuffisant et une ischémie placentaire. En cas de
pré-éclampsie, l'analyse anatomopathologique du placenta montre
des lésions de nature ischémique : infarctus placentaires de
taille variable ou nécrose focale villositaire avec dépôt
de fibrine. On admet qu'une nécrose excédant 30 à
40% du volume placentaire peut provoquer une ischémie
significative (7).
1.4.2 .Les conséquences pour le foetus de
l'ischémie placentaire.
La placentation anormale entraîne une réduction
de la perfusion utero- placentaire, une réduction de
l'oxygénation et de nutrition du foetus entraînant retard de
croissance intra-utérin et hypoplacentose (12).
1.4.3. Les conséquences pour la mère de
l'ischémie placentaire.
La réduction de la perfusion placentaire a trois effets
primordiaux :
4 production de radicaux d'oxygène et de peroxydes
toxiques en particulier pour les cellules endothéliales ;
4 Accroissement possible de l'apoptose, point de départ
de libération des fragments du syncytiotrophoblaste dans la circulation
maternelle ;
4 Production des facteurs directement incriminés dans la
physiopathologie du syndrome (facteurs anti-angiogéniques).
Deux protéines endogènes
anti-angiogènes d'origine placentaire ont été
impliquées dans la pathogenèse de la pré-éclampsie
: la tyrosine kinase fms-like soluble1 (sFlt-1) et l'Endogline
soluble (sEng) (13,14). La sFlt-1 circulant est une variante du
récepteur sFlt-1 au VEGF (vascular endothelial
growth factor) auquel il manque le domaine transmembranaire et
cytoplasmique du sFlt-1 intact, mais qui garde un domaine de liaison
au ligand VEGF. Circulant dans le sang, il agit comme un puissant
antagoniste à la fois du VEGF et du PlGF (placenta growth
factor) (10). La sFlt-1 se lie au PlGF et au
VEGF et inhibe leur interaction avec le récepteur
spécifique endothélial et déclencherai une
endothéliose généralisée.
Maynard et coll. (13) ont montré que les niveaux
plasmatiques de sFlt-1 sont, en moyenne, 5fois plus
élevés chez les femmes ayant des antécédents de
pré-éclampsie, avec une diminution correspondante du VEGF
et du PlGF libres (non liés circulant). L'effet
antiangiogeniques du SFlt-1 semble disparaître dans les 48
premières heures post-partum, puisque aucun effet n'a été
observé en ajoutant le sérum de femmes atteintes à une
culture de cellules endothéliales.
Quand un vecteur adénoviral exprimant le sFlt-1
était injecté à des rattes gravides, les rattes
développaient une hypertension, une protéinurie et une
endothéliose ressemblant à la pré-éclampsie
humaine. Cet effet passe par la neutralisation du VEGF et du
PlGF et par l'induction d'une dysfonction endothéliale (10).
Venkatesha et al cités par Hladunewich (15) ont montré, sur le
même modèle de ratte gravide, que l'endogline "sEng" exacerbe les
lésions endothéliales médiées par le
SFlt-1, entraînant une maladie sévère de type
pré-éclamptique, incluant le développement d'une
endothéliose glomérulaire sévère, un infarctus
placentaire, un retard de croissance foetale, une ischémie
hépatique, une hémolyse et une augmentation de la
perméabilité vasculaire pulmonaire, rénale et
hépatique.
Outre leur rôle dans la pathogenèse de la
pré-éclampsie, les concentrations de sFlt-1, de
PlGF et de sEng circulants peuvent avoir des implications
diagnostiques et thérapeutiques importantes. La concentration de
PlGF" libre" est inversement proportionnelle à la concentration
de sFlt-1. Les concentrations de sFlt-1 et de sEng augmentent 4 à 5
semaines avant l'apparition des manifestations cliniques de
pré-éclampsie et leur élévation est
corrélée à la sévérité de la maladie
(14,16).
Graphique n°1: Circulating
angiogenic factors and the risk of preeclampsia (16).
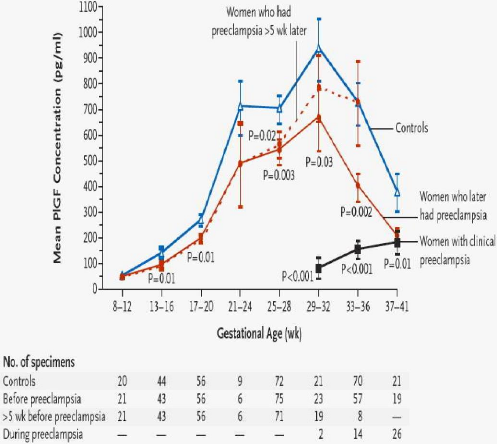
Ce graphique montre que lors d'une grossesse normale, les
concentrations du PlGF croît progressivement dès
12ème SA avec une petite stagnation entre
la 22ème et 26ème SA, pour
atteindre le maximum à 30SA et décroître
ensuite. En comparant les patientes qui plus tard ont développé
une pré-éclampsie, on constate que les concentrations du
PlGF est significativement inférieure par rapport aux
témoins (patientes sans pré-éclampsie) dès la
12ème SA et qu'à partir de
30SA plus la concentration est basse, plus précoce sera
la prééclampsie. En cas de pré-éclampsie clinique
les concentrations du PlGF sont très basses.
Graphique n°2: Circulating angiogenic factors and
the risk of preeclampsia (16).
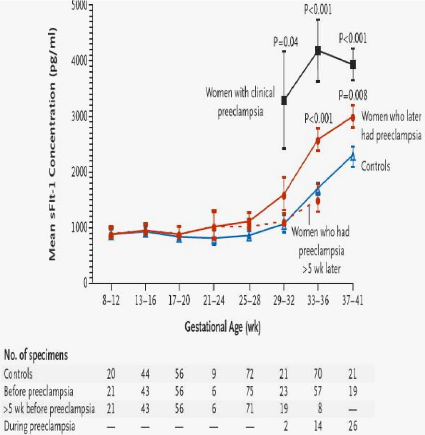
Ce graphique montre que par rapport à un groupe
témoins (sans pré-éclampsie), les patientes qui plus tard
développeront une pré-éclampsie ont des concentrations
plus élevées de sFlt-1 dès la 18ème SA
et qu'à partir de la 30ème SA plus la concentration de
sFlt-1est élevée, plus les manifestations cliniques de la
pré-éclampsie seront précoces. Les concentrations
supérieures à 3000Pg /ml se rencontrent qu'au stade clinique de
la pré-éclampsie.
terme (< à 37 SA), en comparaison à celles qui
ont développé la pré-éclampsie à terme. En
outre, les taux élevés d' sEng furent souvent
accompagnés d'un ratio augmenté de sFlt1/PlGF. Le risque
de pré-éclampsie le plus élevé se rencontre chez
les femmes qui ont à la
fois des taux élevés d'endogline et de
sFlt-1. Bien que chaque biomarqeur soit associé à un
risque de pré-éclampsie, une mesure combinée incorporant
sEng, sFlt-1 et PlGF est plus fortement prédictive d'une
pré-éclampsie (16).
En conclusion, la sécrétion par le placenta en
ischémie, de médiateurs actifs sur l'endothélium
vasculaire maternel, est responsable des manifestations cliniques de
la pré-éclampsie. Cependant, des zones d'ombres
persistent, si non, comment expliquer l'existence de réduction de
perfusion placentaire sans syndrome maternel, comme c'est le cas dans
les RCIU isolés ? Ou le syndrome maternel sans RCIU ?
Cela implique qu'ils existent des facteurs de susceptibilité
génétiques, immunologiques et environnementaux qui moduleraient
la réponse maternelle.
L'extrême variabilité des manifestations de la
pré-éclampsie, dont le spectre s'étend des femmes dont
l'atteinte est minimale, satisfaisant juste pour le diagnostic et qui donnent
naissance à un enfant de poids normal, aux femmes dont la maladie
comporte un risque pour elles et pour leurs foetus, suggère une
contribution diverse de l'hypo perfusion placentaire et des facteurs d'origine
maternelle. Dans certains cas, une réduction significative de la
perfusion placentaire coïnciderait avec une participation maternelle
minimale alors que dans d'autres cas une femme pourrait être très
extrêmement sensible à l'hypo perfusion placentaire et ne
requérir qu'une minime diminution du flux sanguin placentaire
(11).
1.5. Principes de prise en charge d'une grossesse
compliquée de HTA.
La découverte d'une HTA chez la femme enceinte, impose une
évaluation initiale qui a pour but :
?de classifier la condition de la patiente :
HTA préexistante à la grossesse ;
HTA gestationnelle sans protéinurie ;
HTA gestationnelle avec protéinurie ;
HTA gestationnelle avec protéinurie et conditions
défavorables ;
HTA gestationnelle avec protéinurie sans conditions
défavorables ?d'apprécier la gravité de l'HTA et si
possible d'en préciser la cause
?d'évaluer le retentissement foetal
L'interrogatoire va étudier les antécédents
personnels (médicaux et obstétricaux) de la patiente ainsi que
ses antécédents familiaux (antécédent de
pré-éclampsie, d'hypertension artérielle, de
diabète) chez des ascendants ou dans la fratrie.
Outre les éléments généraux tels que
le poids, la taille et les habitudes alimentaires, l'étude
détaillée des antécédents
obstétricaux est déterminante pour évaluer le
risque de complications: antécédents d'HRP,
pré-éclampsie, RCIU, MFIU ou d'éclampsie. En moyenne,
un incident de ce type aboutit dans 15 à 20% des cas
à un risque de récidive.
Un suivi personnalisé et adapté doit être
planifié, permettant de détecter le plus précocement
possible les signes avant coureurs de complications potentiellement dangereuses
pour la mère et le foetus, afin d'intervenir rapidement.
1.5.1. L'HTA préexistante à la grossesse.
1.5.1. 1.HTA chronique :
Dans le meilleur des cas, la grossesse doit être
programmée et les antihypertenseurs contre-indiqués au cours de
la grossesse doivent être écartés. Trois classes
thérapeutiques sont contre-indiquées : les
diurétiques car ils réduisent l'expansion
volémique nécessaire à la perfusion utérine ou
aggrave l'hypo volémie dans le syndrome prééclamptique,
les inhibiteurs de l'enzyme de conversion (IEC) et les
antagonistes de l'angiotensine 2,
responsables d'oligoamnios, persistance du canal artériel, insuffisance
rénale et anurie néonatale, difficultés respiratoires et
mortalité foetale (6). Si l'HTA est bien contrôlée, il faut
poursuivre le traitement en adaptant les doses en raison de la baisse
physiologique de la pression artérielle lors des deux premiers
trimestres de la grossesse.
Il convient de ne pas baisser la PA en dessous de 14 /9 mm Hg car
on augmente le risque de RCIU. Il faut s'efforcer de maintenir la diastolique
en dessous de 9,5mm jusqu'au 2ème trimestre et de 10mm Hg au
troisième trimestre (3).
1.5.1. 2. HTA non connue, découverte avant la
20ème SA :
Une HTA retrouvée à deux reprises
au repos justifie une prise charge. Il s'agit généralement d'une
HTA méconnue découverte à l'occasion
d'une grossesse. Il est important de prévoir une brève
hospitalisation où plusieurs cycles tensionnels sont mesurés si
possible en continu sur quelques heures (Dynamap) ou sur 24 heures en
utilisant un holter tensionnel, ce qui peut permettre de
mettre en évidence une inversion du rythme nycthéméral.
Comme dans l'HTA chronique, le risque principal est celui de
la survenue d'une prééclampsie surajoutée. La surveillance
de la pression artérielle et la recherche de la protéinurie
durant la grossesse, doit être fréquente spécialement en
cas de facteurs de risque associés, dont l'interrogatoire doit
s'attacher à rechercher.
1.5.2. HTA découverte après 20 SA :
L'élévation de la TA constitue
généralement la manifestation clinique la plus précoce du
syndrome pré-éclamptique. La recherche des autres signes du
syndrome doit être une préoccupation du médecin, notamment
la recherche d'une protéinurie par bandelettes. Si la protéinurie
est négative, il s'agit d'une HTA gestationnelle
transitoire qui est en général de bon pronostic, mais
qui doit être surveillée étroitement, car une
protéinurie peut être absente et réapparaitre
secondairement. Si la protéinurie est positive, c'est une
pré-éclampsie. Une hospitalisation est de règle pour une
bonne surveillance materno-foetale. La surveillance porte à la fois sur
des paramètres maternels et foetaux. La décision d'interrompre la
grossesse étant prise devant l'aggravation des signes maternels et /ou
foetaux.
1.5.2. 1. Surveillance maternelle :
Elle est à la fois clinique et biologique. Sur le plan
clinique, la surveillance de la TA doit être pluriquotidienne et
rapprochée. La TA est sévère si la
systole est = 160 et /ou la diastole =110mm
Hg. Il faut rechercher les autres signes de gravité :
-signes fonctionnels neurologiques (céphalées,
somnolence, ROT vifs), visuels (amaurose, phosphènes), auditives
(acouphènes), digestifs (douleur épigastrique en barre,
nausées,
vomissements), une prise de poids excessive avec apparition des
oedèmes du visage et des mains.
Les conditions obstétricales doivent être
précisées, éventuellement pour une terminaison rapide de
la grossesse en cas de risque maternel ou foetal : l'âge de la grossesse,
présentation foetale, les conditions locales : utérus cicatriciel
? Contractions utérines ? Modifications cervicales ?
Sur le plan biologique ; diurèse horaire,
Protéinurie de 24 heures (Normale <0,3g/24H),
NFS-Plaquettes, uricémie (Normale = 360umol/L),
Créatininémie, Transaminases, LDH, haptoglobine, bilirubine
direct et conjugué, bilan de coagulation : TP, TCK, Fibrinogène,
un ionogramme sanguin et urinaire et #177; ECBU, ECG avec un fond d'oeil
à la recherche d'un retentissement viscéral signant une
hypertension ancienne. L'uricémie, la protéinurie, le taux des
plaquettes ont une valeur pronostic.
1.5.2. 2. Surveillance foetale.
Sur le plan clinique, une petite hauteur utérine
par rapport à l'âge théorique de la grossesse peut
alerter sur un éventuel RCIU. Le comptage des MAF par
la mère peut aider à suspecter une aggravation de l'état
foetal en cas de diminution. Mais c'est surtout la surveillance para
clinique qui a toute son importance. Cette surveillance para clinique comprend
:
L'échographie foetale : Elle permet
d'apprécier la croissance et le bien être foetal : Les
biométries (BIP, circonférence abdominale et céphalique,
longueur du fémur, poids foetal estimé) doivent être
rapportées aux courbes de croissance foetale de référence
pour rechercher un RCIU et d'en apprécier l'importance (une cassure de
la courbe de croissance ou un arrêt de croissance). Elle étudie
également les annexes (vieillissement placentaire selon le stade de
Grannum, quantité de LA) et la morphologie foetale à la recherche
d'éventuelles malformations associées.
Le bien être foetal est apprécié par
l'étude du score biophysique de Manning qui comprend 5
éléments et coté sur 10 points :
4 le tonus foetal / 2pts
4 les mouvements actifs du foetus / 2pts
Les mouvements respiratoires / 2pts
4 Quantité de LA (index du LA) / 2pts
4 Aspect du rythme cardiaque foetal (RCF) sur un
tracé obtenu sur un cardiotocographe /2pts.
Un score = 4 impose une extraction foetale
immédiate.
L'enregistrement du RCF : est l'examen de
référence pour suspecter une souffrance
foetale et décider une extraction foetale quel que soit le
terme de la grossesse. Les anomalies recherchées sont :
4 une diminution de la réactivité (absence
d'accélérations)
4 une diminution de la variabilité (tracé
réduit ou plat)
4 présence de
décélérations
4 une bradycardie.
?L'analyse informatisée du RCF
(Oxford) permet d'analyser les paramètres du RCF
invisibles à l'oeil nu, comme la variation à court
terme (VCT) et évite les variations
d'interprétation individuelle.
Une VCT < 3 ms impose une extraction rapide
Une VCT comprise entre 3 et 5ms impose une surveillance active
Une VCT >5 ms impose une surveillance classique
Les examens Doppler : permettent la mesure
d'index, dont le plus connu est l'index de résistance
(IR) ou indice de Pourcelot
IR=(S- D) /S (S = pic systolique; D = pic
diastolique).
Plusieurs sites de mesure sont étudiés en routine
obstétricale.
4 Le Doppler utérin : explore les
artères utérines droite et gauche et recherche soit un IR
élevé, soit incisure protodiastolique (notch)
après la 24ème SA. Leur
présence est témoin d'un trouble de la circulation
placentaire.
4 Doppler ombilical : un index ombilical
pathologique constitue un facteur de risque notable de retard de croissance
intra-utérin. Lorsqu'il est extrêmement pathologique (flux
diastolique nul, ou flux diastolique inversé" reverse-flow"),
sa valeur prédictive dans la survenue d'une souffrance foetale est
très forte.
4 Doppler cérébral : les
anomalies du Doppler cérébral traduisent une
redistribution du flux sanguin en réponse à une hypoxie. Ce signe
marque une aggravation de l'état foetal et impose une extraction du
foetus.
4 Le doppler veineux (ombilical ou canal
d'Arantius). Leurs anomalies précèdent de quelques heures les
troubles sévères du RCF ou la mort in
utero.
1.6. Les complications.
Elles sont redoutables et surviennent essentiellement en cas
de pré-éclampsie et conduisent souvent à la
délivrance quel que soit le terme de la grossesse, car elle constitue le
seul traitement efficace de la pré-éclampsie
1.6.1. Complications maternelles :
1.6.1.1. Poussée hypertensive
sévère.
Elle est définie par une TA systolique =
160mmHg et diastolique = 110mmHg. Elle peut
être révélatrice de la pré-éclampsie ou
résistée au traitement médical. Non
contrôlée, elle évolue vers une crise d'éclampsie ou
un accident vasculaire aigue.
1.6.1.2. L'éclampsie.
Elle se manifeste par des crises convulsives
généralisées tonico-cloniques suivies d'un
état post critique chez une patiente présentant une
pré-éclampsie. C'est une grande urgence
thérapeutique afin d'éviter qu'un état de mal
convulsif ne s'installe. Elle peut être révélatrice de
la pré-éclampsie ou être précédée par
des prodromes qui doivent être surveillés :
céphalées, troubles visuels (phosphènes, diplopie,
amaurose), troubles auditifs (acouphènes), douleurs épigastriques
ou de l'hypochondre droit associées ou non à des
nausées et/ou vomissements et des ROT vifs. Elle survient dans
30% des cas dans le postpartum et dans 50%
des cas elle survient avant 37 SA (7).
1.6.1.3. Hématome rétro placentaire
(HRP)
Il complique 3 à 5% des
pré-éclampsies sévères (7). C'est un
décollement prématuré d'un placenta normalement
inséré. L'hématome qui se constitue va non seulement
supprimer une partie de la surface d'échange entre la mère et le
foetus, de taille plus ou moins importante selon les dimensions de
l'hématome, mais également responsable d'une coagulopathie de
consommation (CIVD). C'est une urgence obstétricale
maternofoetale. Sa survenue est imprévisible, brutale et sa
symptomatologie clinique trompeuse : métrorragies de faible
abondance, souffrance foetale et/ou une hypertonie-hypercinésie
utérine. Le diagnostic est échographique. La
césarienne en cas de foetus vivant permet de
réduire la mortalité foetale. En cas de MFIU, l'accouchement
par voie basse peut être tenté par un déclenchement,
mais sous surveillance stricte de la coagulation
1.6.1.4. HELLP syndrome. = "Hemolysis, Elevated Liver
enzymes, Low Platelets".
Décrit en 1982 par Weinstein, c'est un
syndrome de définition purement biologique (17). Il est
constitué de trois phénomènes biologiques (17, 18) :
Une hémolyse (~LDH,\ l'haptoglobine,
présence de schizocytes dans le sang périphérique),
Une cytolyse (~TGO, ~TGP) et Une
thrombopénie (plaquettes (< 150.000/ mm3). Il
peut apparaître en post-partum dans 30%
des cas ou en l'absence d'HTA dans 10
à 20% des cas (17). Il témoigne d'une
micro-angiopathie thrombotique et peut se compliquer d'un
hématome sous capsulaire du foie. La complication maternelle la
plus redoutée est la rupture hépatique. Cliniquement, le
signe le plus fréquent est une douleur abdominale, maximale au
niveau de l'hypochondre droit associée ou non aux nausées et/ou
vomissements.
1.6.1.5. L'insuffisance rénale aiguë.
Elle est liée en général à une
nécrose corticale. C'est la complication à craindre surtout
en cas de diagnostic tardif et qu'il existe une oligo-anurie
prolongée. La surveillance de la diurèse doit être
faite particulièrement en cas de pré-éclampsie
sévère.
1.6.1.6. L'oedème aigue du poumon (OAP).
Il est souvent favorisé par des apports
hydro-sodés excessifs ou le traitement par les
corticoïdes pour accélérer la maturation pulmonaire
foetale. Il survient dans 70% des cas dans le
post-partum (7).
1.6.1.7. La CIVD aiguë hémorragique.
Elle complique, un HRP un Hellp syndrome, une
éclampsie et certaines CIVD asymptomatiques à l'occasion d'une
hémorragie. Elle se caractérise par un effondrement des
facteurs de coagulation (20 à 80%), du
fibrinogène (<1g/l), des plaquettes (<
50.000/mm3), et de l'antithrombine (<70%), ainsi
que l'apparition des complexes solubles, des produits de dégradation du
fibrinogène (PDF) et des D-dimères, avec
parfois un raccourcissement du temps de lyse des euglobines (8). Leur
évolution peut être très rapide et leur surveillance
biologique doit être répétée parfois à
l'échelle horaire.
1.6.2. Complications foetales.
Elles sont particulièment fréquentes dans les
pré-éclampsies précoces (survenant avant 34 SA).
1.6.2.1. Le retard de croissance intra utérin
(RCIU).
IL touche 7 à 20% des grossesses compliquées de
HTA (18,19). Il est souvent tarif (apparaissant au 3ème
trimestre) et de type disharmonieux (prédominant sur les
biométries abdominales alors que le diamètre bipariétal
est normal ou peu diminué).
1.6.2.2. La Mort Foetale In Utero(MFIU).
Elle complique 2 à 5% des femmes
enceintes atteintes d'HTA, au terme d'une souffrance foetale chronique
sévère ou à l'occasion d'un accident aigu
(éclampsie, HRP) (19).
1.6.2.3. La prématurité.
Elle est souvent induite pour sauvetage foetal et/ou
maternel. La morbidité foetale associe celle de la
prématurité et de l'hypotrophie. Le pronostic est
particulièment mauvais avant 32SA en raison de la fréquence de la
maladie des membranes hyalines.
1.6.2.4. La mort néonatale précoce.
Elle est souvent la conséquence de la
prématurité, soit spontanée, soit iatrogène
(extraction dans un but thérapeutique), ou dans un tableau de
souffrance foetale aigue au cours du travail, souvent sur un foetus
avec RCIU.
1.7. Le traitement.
Dans l' HTA induite par la grossesse, le seul
véritable traitement est l'accouchement, mais qui ne se justifie que
dans les formes sévères ou proches du terme. Le traitement
médical antihypertenseur n'est qu'un traitement adjuvant
d'intérêt limité. En principe il fait partie d'une prise en
charge, permettant d'allonger la durée de la grossesse pour atteindre
une maturité pulmonaire dans les termes précoces. Son seul
objectif est d'éviter les à-coups hypertensifs chez la
mère (20). Un traitement antihypertenseur trop énergique est
même néfaste pour le foetus car il réduit la perfusion
utéro-placentaire et peut aggraver ou être à l'origine
d'une souffrance foetale (7, 19,20).
1.7.1 .Traitement des formes légères ou
modérées
En cas de HTA légère ou
modéré et en l'absence d'autres complications :
une surveillance renforcée peut se faire en ambulatoire (consultation
tous les dix jours, bilan biologique régulier, échographie
mensuelle et doppler ombilical et utérin) associée à un
repos en décubitus latéral gauche (20). Si avec le repos la TA
est = 14 /9, pas de traitement (19). Si l'HTA est modérée et que
la diastolique =10mm Hg, un traitement antihypertenseur doit
être institué (19). En première intention, on peut utiliser
:
les antihypertenseurs centraux qui sont
intéressants par leur action progressive et par leur innocuité
sur le développement foetal. L'alpha-méthyl dopa (Aldomet®))
dispose d'une large expérience dans ce domaine. Les doses iront
croissant de 500 à 2000 mg /24 heures de façon à obtenir
une tension artérielle entre 13/8 et 15/10 mm Hg (19).
?En seconde intention : les ß
bloquants cardiosélectifs (Acébutolol = Sectral®,
Atenolol = Tenormine® etc. .....). Souvent prescrits dans l'HTA chronique
ils peuvent être poursuivis. Le Labétalol (Trandate®) occupe
une place à part, en raison de ses propriétés alpha
bloquantes associées. Il possède en plus d'une forme orale, une
forme injectable et peut être utilisé en cas de HTA
sévère. Tous les ß-bloquants traversent la
barrière placentaire et sont susceptibles de provoquer des
manifestations néonatales à type de bradycardie, de
bronchospasme ou d'hypoglycémie. Par ailleurs, des RCIU
ont été observés chez des foetus
lorsque la mère a été soumise à un
traitement aux bêtabloquants. Le RCIU ne serait pas
düaux propriétés intrinsèques des
bêtabloquants, mais au traitement antihypertenseur énergique
abaissant trop la tension systolique (19).
Les inhibiteurs calciques doivent être
théoriquement évité avant 20 SA en raison des
malformations osseuses observées chez l'animal. Ils sont utilisés
au 2ème et 3ème trimestre de la grossesse. Ils sont
utilisés aussi dans le traitement de la menace d'accouchement
prématurée. Les deux produits les plus utilisés sont
la nifédipine (Adalate®) et la nicardipine
(Loxen®). Les formes à libération prolongée ont une
action lente et sont plus intéressantes car mieux tolérées
par le foetus. Les formes à action rapide (Adalate sublinguale)
sont utilisées dans les à-coups hypertensifs même
si elles ont la fâcheuse conséquence de baisser la TA de
façon trop brutale aggravant ainsi la baisse du flux sanguin
utéroplacentaire avec risque de SFA. Sont prohibés :
-le régime sans sel et diurétiques
(aggravent l'hypo volémie), -les inhibiteurs de l'enzyme de conversion
(foeto-toxiques), et -les inhibiteurs de l'angiotensine.
1.7.2 Traitement des formes sévères de la
pré-éclampsie.
En cas de HTA sévère (= 16/10 mm
Hg) ou de pré-éclampsie, L'hospitalisation s'impose pour
juger de la gravité et envisager une extraction foetale, seul
véritable traitement de la PE. Il faut faire en urgence un bilan
pré-opératoire, une consultation pré-anesthésique,
mettre une voie veineuse de bon calibre et administré un corticoïde
(à visée de maturation pulmonaire foetale) si terme de la
grossesse est comprise entre 27 et 34SA révolues. Un traitement
intraveineuse antihypertenseur (Loxen®, Trandate®, Nepressol®,
Catapressan®) doit être instauré en attendant une
évaluation rapide de l'état materno-foetal, permettant de
temporiser en l'absence de signes de gravité, et au cas contraire, une
terminaison immédiate
de la grossesse. Les signes de gravité suivants plaident
en faveur d'une délivrance immédiate :
4 HTA instable et non contrôlable par le traitement
médical,
4 Crise d'éclampsie,
4 Signes fonctionnels francs et permanents
(céphalées violentes, douleurs épigastriques en barre,
troubles visuels....)
4 Hématome rétro placentaire,
4 Perturbations biologiques sévères et/ou
évolutives (HELLP syndrome, insuffisance rénale franche,
uricémie > à 600 umol/l),
4 Altérations sévères du rythme
cardiaque foetal, alors que le foetus est vivant et
présuméviable.
En l'absence de ces signes de gravité, la prise en charge
obstétricale dépend du terme de la grossesse :
Entre 28 SA et 34 SA : une expectative
"armée" et administration de corticoïdes pour
accélérer la maturation pulmonaire foetale, 48 heures suffisent
pour que la corticothérapie produise ses effets.
Entre 34-36SA, un signe de gravité,
même isolé n'est pas acceptable, il faut provoquer la naissance,
par déclenchement du travail ou césarienne en fonction des
conditions obstétricales et de l'état foetal.
Terme = 37 SA il faut déclencher
l'accouchement si les conditions obstétricales le permettent, si non il
faut césariser.
En cas de crise d'éclampsie, le traitement,
outre celui de l' HTA menaçante, fait appel à une dose de
diazépam à la phase aiguë ou au sulfate de
magnésium qui est le traitement de choix dans la prévention
de la récidive (7, 19).
1.7.3. Le traitement préventif.
Malgré des progrès très
importants dans la connaissance des mécanismes physiopathologiques
impliqués dans l'installation de l'HTA induite par la
grossesse associée ou non à la protéinurie, la
prévention primaire n'est pas possible, car la véritable
cause reste inconnue. La prévention secondaire fait appel
à des méthodes de détection précoce des patientes
qui vont développer une HTA gestationnelle ; cependant aucun des tests
décrits (évolution des chiffres tensionnels, le Roll over test de
Gant, le taux sérique de HCG ou de l'alpha-foetoprotéine (sans
anomalies de fermeture du tube neural), les molécules d'adhésion
solubles, le Doppler des artères utérines, etc.) n'a de valeurs
prédictives positives suffisantes pour être utilisé en
pratique courante, quoi que ces tests soient utiles dans la surveillance des
patientes à haut risque .
Une place à part doit être réservée
aux antécédents obstétricaux de pathologie
vasculaire placentaire ( pré-éclampsie," MFIU, RCIU, HRP dans un
contexte vasculaire"). Le risque est d'autant plus important que
l'antécédent aura été sévère et
précoce. Dans ce contexte un traitement préventif par
l'aspirine à la dose de 100mg dès le début de la grossesse
jusqu'à la 35ème SA révolues est indiqué
(19). De même des antécédents personnels de maladies
auto-immunes (lupus, syndrome des anti-phospholipides), de
maladies thromboemboliques secondaires à une thrombophilie
et de pathologies vasculo-rénales (HTA chronique,
néphropathies) constitue une population à risque pour la
pré-éclampsie. Ces patientes à risque doivent avoir
une surveillance rapprochée.
La prévention tertiaire consiste à
éviter l'apparition des complications maternelles et foetales lorsque
l'HTA gestationnelle est déjà installée. Une prise en
charge obstétricale individuelle adaptée, un traitement
conservateur sous surveillance afin de faire naître un enfant au moment
et à l'endroit les plus adaptés représentent les moyens
thérapeutiques les plus efficaces (11).
2. MATERIEL ET METHODES.
2.1. Matériel.
Notre étude est rétrospective descriptive
et mono centrique. Elle a été réalisée au
Centre Hospitalo-universitaire de Kamenge et couvre une
période de 24 mois allant du 1er Janvier 2006 au 31
Décembre 2007.
Ont été incluses :
- toutes les gestantes, parturientes et femmes en suites de
couches hospitalisées, répondant aux critères d'HTA tels
que définis par l'OMS (TA = 140 /90 mm Hg).
Ont été exclues :
4 les patientes présentant une protéinurie
sans HTA,
4 les patientes hypertendues non enceintes.
Pour chacune des patientes incluses, nous avons
étudié les données suivantes :
4 les données générales :
l'âge, gestité, parité, les antécédents
médicaux et obstétricaux personnels et familiaux
4 les données cliniques : le motif
d'hospitalisation, les chiffres tensionnels lors de l'admission, les signes
d'accompagnement, et la fréquence de la surveillance clinique, le terme
à l'admission de l'HTA, les complications materno-foetales.
4 les données para cliniques : les
examens biologiques réalisés, échographie et Doppler
foetal, l'enregistrement du rythme cardiaque foetal et leur
fréquence.
4 les données thérapeutiques :
traitement en hospitalisation (médicaments, voies).
4 les données pédiatriques :
terme à l'accouchement, voie d'accouchement, poids à la
naissance, durée de séjour en néonatologie pour ceux qui y
ont étés admis.
2.2. Méthodes
Une fiche préétablie a permis de
recueillir les données pour chaque patiente (voir en annexe)
Nos sources de données ont
étés les fiches des malades, les
registres de mouvements des services de Gynécologie
Obstétrique et de Néonatologie.
Le traitement des données a été fait par
les logiciels Excel et EPI-info version 3.3.2.
3. Résultats.
3.1. Données épidémiologiques.
3.1. 1.La fréquence de l'HTA associée
à la grossesse.
Durant la période de notre étude, 5933
accouchements ont eu lieu dont 1836
césariennes (32,3% des accouchements). Nous avons
colligé pour la même période 109 cas
d'hypertensions gravidiques soit une fréquence de 1,83%.
Le tableau n°É montre la répartition des cas
d' HTA associé la grossesse selon l'année.
Tableau n° É : Répartition des cas selon
l'année
|
Année
|
2006
|
2007
|
2006-2007
|
|
Accouchements
|
2582
|
3351
|
5933
|
|
HTA
|
59
|
50
|
109
|
|
%
|
2,28%
|
1,49%
|
1,83%
|
3.1.2. L'âge.
L'âge moyen est de 29,97 ans avec
des extrêmes de 18ans pour la plus jeune et de
43ans pour la plus âgée. 47,7%
ont un âge compris entre 26ans et 31ans.
Tableau n°ÉÉ: Répartition des
cas par tranches d'âges.
|
Tranche d'âges
|
N cas
|
%
|
% cumulé
|
|
<20ans
|
3
|
2.8%
|
2.8%
|
|
20-25 ans
|
14
|
12.8%
|
15.6%
|
|
26-31 ans
|
52
|
47.7%
|
63.3%
|
|
32-37 ans
|
27
|
24.8%
|
88.1%
|
|
38-43 ans
|
13
|
11.9%
|
100.0%
|
|
Total
|
109
|
100.0%
|
100.0%
|
3.1.3 L'origine des patientes.
Le tableau n°ÉÉ montre que
78% des cas sont originaires de Bujumbura Mairie. Les autres
proviennent des provinces de l'intérieur du Burundi et sont souvent
transférées par d'autres structures de soins vers le CHU de
Kamenge qui est un Hôpital de référence au niveau
national.
Tableau n°ÉÉÉ :
répartition des cas selon la province d'origine.
|
PROVINCE D'ORIGINE
|
N cas
|
%
|
Cum Percent
|
|
Bujumbura Mairie
|
85
|
78.0%
|
78.0%
|
|
Bujumbura Rural
|
3
|
2.8%
|
80.7%
|
|
Bubanza
|
4
|
3.7%
|
84.4%
|
|
Bururi
|
2
|
1.8%
|
86.2%
|
|
Gitega
|
4
|
3.7%
|
89.9%
|
|
Muramvya
|
3
|
2.8%
|
92.7%
|
|
Cankunzo
|
1
|
0.9%
|
93.6%
|
|
Rutana
|
1
|
0.9%
|
94.5%
|
|
Cibitoke
|
3
|
2.8%
|
97.2%
|
|
Mwaro
|
2
|
1.8%
|
99.1%
|
|
Ngozi
|
1
|
0.9%
|
100.0%
|
|
Total
|
109
|
100.0%
|
100.0%
|
Si on considère la mairie de Bujumbura, le tableau
n°ÉV montre que beaucoup de nos parturientes viennent des
communes urbaines très peuplées (Musaga, Cibitoke, Ngagara,
Nyakabiga, Kamenge, Bwiza, Buyenzi).
Tableau n°ÉV : répartition des cas
selon la commune d'origine.
|
COMMUNE D'ORIGINE
|
Ncas
|
%
|
% CUMULES
|
|
Musaga
|
16
|
14.7%
|
14.7%
|
|
Kinindo
|
1
|
0.9%
|
15.6%
|
|
Gihosha
|
4
|
3.7%
|
19.3%
|
|
Bwiza
|
7
|
6.4%
|
25.7%
|
|
Cibitoke
|
14
|
12.8%
|
38.5%
|
|
Nyakabiga
|
8
|
7.3%
|
45.9%
|
|
Ngagara
|
9
|
8.3%
|
54.1%
|
|
Rohero
|
1
|
0.9%
|
55.0%
|
|
Kamenge
|
8
|
7.3%
|
62.4%
|
|
Kanyosha
|
3
|
2.8%
|
65.1%
|
|
Buyenzi
|
7
|
6.4%
|
71.6%
|
|
Kinindo
|
6
|
5.5%
|
77.1%
|
|
Autres Communes
|
25
|
22.9%
|
100.0%
|
|
Total
|
109
|
100.0%
|
100.0%
|
3.1.4. La Profession.
Plus de la moitié de nos patientes sont des
fonctionnaires. Ces dernières représentent 53,2%
des cas (58/109), suivies par les
ménagères et les cultivatrices qui représentent
37,4% des cas (43/109). Les autres fonctions
représentées sont, les commerçantes, les
étudiantes, et élèves avec respectivement 3,7%,
2,8%, et 0,9%.
Tableau n° V : Répartition des cas selon leur
profession.
|
PROFESSION
|
N cas
|
%
|
% cumulé
|
|
Fonctionnaires
|
58
|
53,2%
|
53,2%
|
|
Cultivatrices et ménagères
|
43
|
39,4%
|
92,6%
|
|
Commerçantes
|
4
|
3,7%
|
96,3%
|
|
Etudiantes
|
3
|
2,8%
|
99,1%
|
|
Elève
|
1
|
0,9%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.1.5. La parité et gestité.
3.1.5. A. La parité.
La parité moyenne est de
1,73. Le tableau n°VI montre que les nullipares
sont les plus nombreuses avec 42,2%. Les multipares (5 et
plus) représentent 10,1%. La moyenne d'enfants
vivants par femme est de 1,34.
Tableau n° VÉ: répartition des cas
selon la parité.
|
PARITE
|
N cas
|
%
|
% cumulé
|
|
0
|
46
|
42,2%
|
42,2%
|
|
1
|
11
|
10,1%
|
52,3%
|
|
2
|
18
|
16,5%
|
68,8%
|
|
3
|
14
|
12,8%
|
81,7%
|
|
4
|
9
|
8,3%
|
89,9%
|
|
5 et plus
|
11
|
10,1%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.1.5. B. La Gestité.
La gestité moyenne est de 2,8
grossesses/femme. Plus d'un tiers des cas (36%) sont
des primigestes. On remarque sur le graphique n°3 que le nombre
des cas diminue avec l'augmentation de la gestité avec une petite
ré-ascension à la 4ème grossesse.
Graphique n°3: Répartition des cas selon la
gestité.
|
Légende :
1 : Primigestes
2 :2ème gestes
3 :3ème gestes
4 :4ème gestes
5 :5ème gestes
6 :=6gestes
|
3.1.6. Antécédents familiaux.
Il faut souligner d'emblée qu'ils ne figuraient que
très rarement sur le dossier d'hospitalisation. Aucun
antécédent familial de diabète, de
pré-éclampsie ni de néphropathie n'a été
signalé. Un seul cas (0,92%) avait un
antécédent de HTA chronique dans sa fratrie.
3.1.7. Antécédents médicaux et
obstétricaux personnels.
Nous n'avons trouvé aucun
antécédent dans 67,89% (74/109) des cas.
Dans 32,11% (35/109) des cas nous avons trouvé au moins
un antécédent :
18,3% (20/109) ont un antécédent
de fausse couche,
17,4%(19/109) d'hypotrophie,
13,8%(15/109) de MFIU,
12,8%(14/109) de
pré-éclampsie,
11,9%(13/109) d'infection urinaire,
8,3%(9/109) d'hypertension artérielle
chronique.
3.1.8. Type de grossesse.
La majorité avait une grossesse mono foetale soit 95,41%
des cas. La gémellité représente 4,59% des cas.
Tableau n°VÉÉ : répartition des
cas selon le type de grossesse.
|
Type de grossesse
|
Ncas
|
%
|
|
Gémellaire
|
5
|
4,59
|
|
Mono-foetale
|
104
|
95,41
|
|
Total
|
109
|
100
|
3.1.9. Délais entre le début des
manifestations cliniques d'HTA et la consultation.
La durée moyenne entre les manifestations cliniques
(céphalées, troubles auditifs, troubles visuels etc..) et la
consultation est de 4,8 jours avec des extrêmes
de 0 à 90 jours. Le tableau
n°VÉÉÉ montre que 78,9%
seulement ont consultés dans la semaine depuis le début
des manifestations cliniques. 21,1% ont consulté
tardivement (malgré des signes cliniques déjà
présents : céphalées, oedèmes du visage....) et ont
mis au moins une semaine pour consulter une structure sanitaire.
Tableau n° VÉÉÉ : Délais
entre le début des manifestations cliniques d'HTA et la
consultation
|
Délais en jrs
|
N de cas
|
%
|
%Cumules
|
|
=1
|
35
|
32,1%
|
32,1%
|
|
2 à 7
|
51
|
46,8%
|
78,9%
|
|
8 à 14
|
16
|
14,7%
|
93,6%
|
|
15 à 34
|
6
|
5,5%
|
99,1%
|
|
= 35
|
1
|
0,9%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.1.10. Les consultations prénatales.
La grossesse n'était pas suivie dans 38
cas soit 34,9%. On peut dire que dans plus d'un cas sur deux, la
grossesse est mal et/ou non suivie puisque dans 51,4% des cas
on compte au plus 2 consultations prénatales alors que le terme moyen
à l'admission est de 35 SA.
Tableau n°ÉX: Répartition des cas
selon Nombre de consultations prénatales.
|
Nombre de CPN
|
Ncas
|
%
|
%Cumulés
|
|
0
|
38
|
34,9%
|
34,9%
|
|
1
|
5
|
4,6%
|
39,5%
|
|
2
|
13
|
11,9%
|
51,4%
|
|
3
|
23
|
21,1%
|
72,3%
|
|
4
|
16
|
14,7%
|
87,2%
|
|
=5
|
14
|
12,8%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.1.11. Type de HTA.
La pré-éclampsie prédomine avec
79,8% des cas. L'HTA chronique représente 3,7%
des cas. Dans 6cas, la classification n'a pas été possible par
manque d'éléments permettant leur classification. Il s'agit des
cas de HTA découverte de novo, après la 20ème
SA, mais dont on ne connaît pas la protéinurie car non
recherchée.
Tableau n° X : Répartition des cas selon le
type de HTA.
|
Type HTA
|
N cas
|
%
|
% Cumulés
|
|
Pré-éclampsie
|
87
|
79,8%
|
79,8%
|
|
HTA chronique
|
4
|
3,7%
|
83,5%
|
|
Pré-éclampsie surajoutée
|
5
|
4,6%
|
88,1%
|
|
HTA gravidique
|
7
|
6,4%
|
94,5%
|
|
Non classée
|
6
|
5,5%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.2. Les données cliniques.
3.2.1 Le terme de la grossesse à l'admission.
Le terme de la grossesse a été
déterminé à partir de la date des dernières
règles ou à partir d'une échographie si la date des
dernières règles est inconnue. En cas d'admission en post-partum,
nous avons considéré le terme à l'accouchement.
33% n'ont pas d'échographie déjà faite avant leur
admission. Le terme est inconnu dans 12,8% des cas (DDR
inconnue, pas d'échographie faite). Pour celles qui, le terme est connu,
la moyenne est de 35SA à leur admission.
Le tableau n° XÉ montre la
répartition des cas, selon l'âge de la grossesse à l`
admission.
41 patientes (35,8%) ont
été admises avant 34SA dont 18,3%
entre la 32ème et 34ème
SA.
Tableau n° XÉ : Terme de la grossesse
à l'admission.
|
TERME THEORIQUE
|
Ncas
|
%
|
% Cumulés
|
|
20-22SA
|
1
|
0,9%
|
0,9%
|
|
23-25SA
|
2
|
1,8%
|
2,8%
|
|
26-28SA
|
4
|
3,7%
|
6,4%
|
|
29-31SA
|
12
|
11,0%
|
17,4%
|
|
32-34SA
|
20
|
18,3%
|
35,8%
|
|
35-37SA
|
24
|
22,0%
|
57,8%
|
|
> 37SA
|
32
|
29,4%
|
87,2%
|
|
Inconnu
|
14
|
12,8%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.2.2 Principaux signes cliniques observés à
l'admission.
3.2.2.1. La tension artérielle systolique.
La tension systolique moyenne est de 16,97Cm
Hg. Le tableau n° X montre que 95 patientes
(87,2%) avaient une HTA sévère
(Systolique =16Cm Hg).
Tableau n°XÉÉ : répartition
selon la TA systolique.
|
TA Systolique (Cm Hg)
|
Ncas
|
%
|
%Cum
|
|
>20
|
8
|
7,3%
|
7,3%
|
|
18-20
|
37
|
33,9%
|
41,3%
|
|
17-16
|
50
|
45,9%
|
87,2%
|
|
15-14
|
14
|
12,8%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.2.2.2. La tension artérielle diastolique.
La tension diastolique moyenne est de 10,99Cm
Hg. Le tableau n° XÉ montre que dans
52,3% des cas, la diastolique est comprise entre
10 et 11Cm Hg et que dans 33,9% des cas, la
situation est préoccupante puisque la diastolique =
12Cm Hg.
Tableau n°XÉÉÉ :
Répartition des cas selon la TA diastolique.
|
TA diastolique (Cm Hg)
|
Ncas
|
%
|
%Cumulés
|
|
>13
|
9
|
8,3%
|
8,3%
|
|
12-13
|
28
|
25,7%
|
33,9%
|
|
10-11
|
57
|
52,3%
|
86,2%
|
|
9
|
15
|
13,8%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.2.2.3. Les signes cliniques associés.
Les manifestations cliniques sont dominées par les signes
neurosensoriels (céphalées, flou visuel ou scotomes scintillants,
bourdonnements d'oreilles) comme le montre le tableau n°
XÉV. Les convulsions témoins d'une
encéphalopathie hypertensive grave ont été
observées dans 21,1%. D'autres signes témoins
d'une situation inquiétante ne sont pas rares tels des oedèmes
généralisés particulièrement prédominant au
niveau du visage et des membres supérieurs (23,9%) et
des douleurs épigastriques (13,8%). Une patiente
pouvait présenter un ou plusieurs signes cliniques à la fois.
Fautes de données sur le poids, nous n'avons pas pu évaluer le
gain pondéral.
34 Tableau n°XÉV : les signes associés
à l'HTA.
|
Signe clinique
|
Ncas
|
%
|
|
céphalées
|
57
|
52,3%
|
|
Troubles visuels
|
36
|
33%
|
|
Troubles auditives
|
30
|
27,5%
|
|
OEdèmes
généralisés
|
26
|
23,9%
|
|
convulsions
|
23
|
21,1%
|
|
Douleurs épigastriques
|
15
|
13,8%
|
3.2.3. Délais entre la consultation et
l'hospitalisation.
L'hospitalisation immédiate est la pratique la plus
courante puisque 91 patientes (83,5%) ont
été admises le jour même de la consultation et parmi elles
26(23,9%) étaient des transferts. 15 patientes
(13,7%) ont été admises le lendemain et 3cas
(2,8%) seulement ont été admis après le
3ème jour de la consultation. Pour ces derniers cas, l' HTA
était modérée, permettant la prescription des examens para
cliniques en ambulatoire.
Tableau n° XV : Délais entre consultation et
l'hospitalisation
|
délais
|
Ncas
|
%
|
% cumulés
|
|
Même jour
|
91
|
83,5%
|
83,5%
|
|
2jours
|
15
|
13,7%
|
97,2%
|
|
3jours et plus
|
3
|
2,8%
|
100%
|
|
Total
|
109
|
100%
|
100%
|
3.2.4. Motif de transfert.
Quatre patientes on été
transférées pour un motif autre qu'une HTA : un cas de
tétanos qui en réalité était une crise
d'éclampsie, 2cas de dystocie mécanique et un cas de dystocie
dynamique, preuve que la prise de la tension artérielle n'est pas
systématique dans toutes les structures de soins. Pour les 22
autres patientes dont le diagnostic est déjà
posé, le motif de transfert est soit l'incapacité d'assurer une
prise en charge (Centre de Santé) ou soit l'absence d'un
service de néonatologie pouvant prendre en charge les
bébés prématurés (cliniques privées ou
autres hôpitaux publiques ne disposant pas de service de
néonatologie).
Tableau n° XVÉ : Motif de
transfert.
|
Motif de transfert
|
N cas
|
%
|
%Cumulés
|
|
Eclampsie
|
9
|
8,3%
|
8,3%
|
|
Pré-éclampsie
sévère
|
12
|
11,0%
|
19,3%
|
|
HTA sévère
|
1
|
0,9%
|
20,2%
|
|
Autres causes
|
4
|
3,7%
|
23,9%
|
|
Non transférées
|
83
|
76,1%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.3. Examens paracliniques.
Soulignons d'amblée que chez 20
patientes, aucun examen paraclinique n'a été
réalisé ni avant leur admission ni en hospitalisation. 22
patientes avaient un bilan biologique à leur admission.
63 patientes ont eu leur bilan le jour même ou le
lendemain de leur admission. 24 patientes ont passé
plus de 48H à l'hôpital sans aucun bilan
biologique. Le bilan est assez souvent incomplet. Le tableau
n°XVII montre que même les examens qui ont une valeur
pronostique tels : numération des plaquettes, acide urique,
transaminases, et la protéinurie des 24H sont loin d'être
systématiquement réalisés.
Tableau n° XVÉÉ : Répartition
des cas selon les examens réalisés.
|
examen
|
N de cas
|
%
|
|
fait
|
Non fait
|
fait
|
Non fait
|
|
Albuminurie
|
89
|
20
|
81,7%
|
18,3%
|
|
NFS-plaquettes
|
76
|
33
|
69,7%
|
30,3%
|
|
Acide urique
|
72
|
37
|
66,1%
|
33,9%
|
|
Créatinémie
|
69
|
40
|
63,3%
|
36,7%
|
|
Transaminases
|
68
|
41
|
62,7%
|
37,3%
|
|
Protéinurie des 24H
|
23
|
86
|
21,1%
|
78,9%
|
|
TP, TCK
|
20
|
89
|
18,3%
|
81,7%
|
|
ECBU
|
12
|
97
|
11%
|
89%
|
|
LDH
|
3
|
106
|
2,8%
|
97,2%
|
3.3.1. Albuminurie en croix.
Comme c'est souligné plus haut, l'albuminurie n'a pas
été faite chez 20 patientes. Dix
patientes ont une albuminurie négative. Sur 89
patientes dont l'albuminurie a été recherchée, a
peu près 2/3 (53/89 patientes) ont une albuminurie = 3
croix.
Tableau n° XVÉÉÉ :
Répartition des cas selon le nombre de croix de
l'albuminurie.
|
Albuminurie en Croix
|
N de cas
|
%
|
%Cumulés
|
|
inconnue
|
20
|
18,3%
|
18,3%
|
|
négative
|
10
|
9,2%
|
27,5%
|
|
1 à 2
|
26
|
23,9%
|
51,4%
|
|
3 à 4
|
53
|
48,6%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.3.2 : les plaquettes.
Le nombre de plaquettes est connu dans 76 cas,
dont 55 cas ont un nombre de plaquettes normal. On note une
thrombopénie sévère (=50.000/mm3) dans
deux cas dont un cas d'évolution fatale dans
un tableau de mal convulsif et biologiquement un HELLP syndrome et une IRA,
et l'autre a fait une crise d'éclampsie et un HELLP syndrome
heureusement d'évolution favorable.
Tableau n° XÉX : Répartition des cas
selon le nombre de plaquettes.
|
Plaquettes
|
N de cas
|
%
|
%Cumulés
|
|
Pas fait
|
33
|
30,3%
|
30,3%
|
|
= 50.000/mm3
|
2
|
1,8%
|
32,1%
|
|
50.001-100.000/mm3
|
8
|
7,3%
|
39,4%
|
|
100.001-149.999/mm3
|
11
|
10,1%
|
49,5%
|
|
= 150.000/mm3
|
55
|
50,5%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.3.3. Uricémie.
Le dosage de l'acide urique n'a pas été fait dans
33,9% des cas. 11% des cas ont une
uricémie > 560umol/L, dont
6,4%(7cas) ont une uricémie qui
dépasse 661umol/L. Tableau n° XX : Répartition des
cas selon l'uricémie en umol/l.
|
Uricémie en umol/l
|
N de cas
|
%
|
%Cumulés
|
|
Pas fait
|
37
|
33,9%
|
33,9%
|
|
< 360
|
32
|
29,4%
|
63,3%
|
|
360-460
|
22
|
20,2%
|
83,5%
|
|
461-560
|
6
|
5,5%
|
89,0%
|
|
561-660
|
5
|
4,6%
|
93,6%
|
|
=661
|
7
|
6,4%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.3.4 : Protéinurie des 24 heures en g/l.
Elle a été réalisée uniquement chez
23 patientes soit 21,1% des cas.
7patientes sur les 23 ont une protéinurie majeur
(>4g/l). Un seul cas avait une protéinurie non significative
(< 0,3g/l).
Tableau n° XXÉ : Répartition des cas
selon la protéinurie des 24 heures.
|
Protéinurie des 24H
|
N de cas
|
%
|
%Cumulés
|
|
Pas fait
|
86
|
78,9%
|
78,9%
|
|
< 0,3
|
1
|
0,9%
|
79,8%
|
|
0,3-1,50
|
10
|
9,1%
|
88,9%
|
|
1,151-2,80
|
1
|
0,9%
|
89,8%
|
|
2,81-4,00
|
4
|
3,7%
|
93,5%
|
|
4,01-5,49
|
3
|
2,8%
|
96,3%
|
|
=5,5
|
4
|
3,7%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.4. Surveillance materno-foetale.
3.4.1. Surveillance maternelle.
Nous évaluons la surveillance maternelle par le nombre de
prise de la TA par 24 Heures, par le nombre de fois qu'on a recherché
les signes cliniques de gravité par jour et par la pesée. Le
nombre moyen de visites médicales est de 4,2 par 24
h soit une visite médicale toutes les
6 heures. Le tableau n° XX montre que dans
55% des cas, la TA a été prise au plus
une fois toutes les 6 heures. Dans 68,9% des
cas, une recherche des signes cliniques de gravité au plus
toutes les 6 heures. Notons une surveillance largement insuffisante
(une fois en 24 heures) de la TA et des signes cliniques de
gravité chez respectivement 7patientes et 30 patientes.
La pesée est rarement fait et semble
ne pas faire partie des paramètres à surveiller puisque deux cas
seulement ont été pesés à leur admission. Il n'y a
pas eu de surveillance de la diurèse.
Tableau n° XXÉÉ : surveillance de la
TA et des signes cliniques de gravité
|
Nombre de Visites/24 heures
|
Contrôle de la TA
|
signes cliniques de gravité
|
|
N de cas
|
%
|
N de cas
|
%
|
|
1 fois
|
7
|
6,4%
|
30
|
27,5
|
|
2-4 fois
|
53
|
48,6%
|
45
|
41,4
|
|
5-7 fois
|
25
|
22,9%
|
20
|
18,3
|
|
8- 10fois
|
11
|
10,1%
|
7
|
6,4
|
|
>10 fois
|
13
|
11,9%
|
7
|
6,4
|
|
total
|
109
|
100%
|
109
|
100
|
3.4.2. Surveillance foetale.
Elle est à la fois clinique et paraclinique.
3.4.2.1 surveillances cliniques.
La surveillance des BCF n'avait pas d'indication
dans 29 cas (26,6%) soit parce qu'ils ont été
admis après l'accouchement ou la MFIU déjà
confirmée par une échographie, soit que l'urgence
(éclampsie) ne laissait pas de place à la surveillance.
Le nombre moyen des visites pour la surveillance des BCF
est de 6,4 fois/24 heures soit environ une visite
toutes les 4 heures .on note chez 8 patientes
au moins une visites toutes les 2 heures.
Tableau n° XXÉÉÉ : surveillance
des BCF.
|
Comptage des BCF par 24H
|
N de cas
|
%
|
%Cumulés
|
|
Pas d'indication
|
29
|
26,6%
|
26,6%
|
|
1-4 fois
|
38
|
34,9%
|
61,5%
|
|
5-9 fois
|
30
|
27,5%
|
89,0%
|
|
10-13 fois
|
4
|
3,7%
|
92,7%
|
|
>13 fois
|
8
|
7,3%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.4.2.2. Surveillance foetale paraclinique.
La surveillance foetale paraclinique a fait appel à
l'échographie, au Doppler ombilical et
l'enregistrement du rythme cardiaque foetal. Chez 13 patientes
(11,9%) ces examens n'avaient pas d'indication parce qu'elles ont
été admises en postpartum. 58 patientes (53,2%)
ont eu au moins une échographie obstétricale, 24
patientes (22%) un Doppler ombilical et 16 patientes
(14, 7%) un monitoring foetale. 34,9%, 66,1% et 73,4%
des cas n'ont pas bénéficiés respectivement
d'échographie foetale, de Doppler ombilical et de monitoring
foetal.
3.5. Le traitement.
3.5.1 Le traitement Médical.
Trois antihypertenseurs ont été couramment
utilisés : l'alpha-méthyledopa (Aldomet®), la
nifédipine rapide (Adalate®) per os et la clonidine
(catapressan®) en intraveineuse. L'Aldomet® est
prescrit en première intention, et en cas de pic hypertensif on ajout
l'Adalate® rapide. En cas de HTA sévère
(>16/10 Cm Hg) ou d'HTA résistant à ces deux
premiers antihypertenseurs, on administrait le Catapressan® en
intraveineuse. 35 patientes soit 32,1% ont eu
un traitement intraveineux. 31 patientes sont sorties
encore
sous traitement antihypertenseur. Sur les 36 patientes
admises entre 26 et 34 SA révolues, 31patientes soit 86,11%
ont eu du déxaméthasone pour accélérer la
maturation pulmonaire. En cas de crise d'éclampsie le
traitement a fait appel au diazépam (Valium ®). Le
sulfate de magnésium n'a pas été
utilisé.
3.5. 2. Le traitement Obstétrical.
Le traitement obstétrical consiste en l'évacuation
utérine. 3patientes ont eu une interruption
thérapeutique de grossesse respectivement à 20SA et1jrs,
à 22SA et 26 SA. L'expulsion a été obtenue par voie basse
après déclenchement au Misoprostol (cytotec®).
3.5.2. 1. Le terme avant l'accouchement.
Le terme moyen avant l'accouchement est de 35SA
4jours. 49 patientes (45%) ont accouché
prématurément (terme = 36SA 6/7) dont 31
(28,4%) à un terme = 33SA.
54 patientes (49,5%) ont accouché à
terme. Le terme n'est pas connu chez 6 patientes (5,5%) et n'a pas
été estimé après la naissance, en particulier
après l'expulsion d'un mort foetal in utero. Le tableau
n°XXV montre la répartition des cas selon le terme à
l'accouchement.
Tableau n° XXV : Terme avant
l'accouchement.
|
Termes à l'ACC en SA
|
N cas
|
%
|
%Cumulés
|
|
<28SA
|
5
|
4,6%
|
4,6%
|
|
28-30SA
|
6
|
5,5%
|
10,1%
|
|
31-33SA
|
20
|
18,3%
|
28,4%
|
|
34-36SA
|
18
|
16,5%
|
45,0%
|
|
=37SA
|
54
|
49,5%
|
94,5%
|
|
inconnu
|
6
|
5,5%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.5. 2.2. Modes d'accouchement.
36 patientes soit 33% ont accouché par
voie basse dont 17 (15,6%) accouchements
par voies basses spontanés et 19(17,4%)
après déclenchement artificiel du
travail. 72 patientes ont
accouché par césarienne dont 56 (51,4%) en
urgence, 12 (11%) programmées et
4 (3,7%) après échec de déclenchement
du travail. Le mode d'accouchement n'est pas connu chez une patiente
présentant une pré-éclampsie sévère qui a
été transférée vers un autre hôpital, par
manque d'O2 au CHU de Kamenge.
Tableau n° XXÉV : Modes
d'accouchement.
|
Mode d'accouchement
|
N cas
|
%
|
% cumulés
|
|
AV B
|
36
|
33%
|
33%
|
|
Césarienne
|
72
|
66,1%
|
99,1%
|
|
inconnu
|
1
|
0,9%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.6. Les complications.
Elles sont fréquentes et touchent aussi bien la
mère que le foetus. Le terme de la grossesse est facteur pronostic
important et plus le terme est précoce, plus le risque maternofoetal
est élevé.
3.6.1. Les complications maternelles.
3.6.1.1. La mortalité maternelle.
On a déploré cinq décès
maternels soit un taux de mortalité de 4,6%.
Durant la période de l'étude il y a eu 7 décès
au total soit 1,2 décès pour 1000
accouchements. Les désordres hypertensifs de la grossesse sont
donc responsables de 71, 43% des causes de décès
maternels.
3.6.1.2 La morbidité.
Les complications sont fréquentes. Elles peuvent
être isolées ou associées. Elles sont dominées par
l'éclampsie, l'insuffisance rénale aiguë,
l'hématome rétro placentaire, l'ascite, le HELLP syndrome et la
rétinopathie hypertensive observé respectivement dans
21,1% (23 cas), 9,2% (10 cas), 7,3% (8 cas), 5,5% (6cas), 4,6% (5 cas)
et 4,6% (5 cas). D'autres complications sont moins fréquentes,
comme l'OAP (2cas) et la CIVD
(2cas).
Certaines de ses complications peuvent être
sous-estimés car elles ne sont pas systématiquement
recherchées (fond d'oeil rarement fait, bilan biologique non fait ou
incomplet).
Tableau n°XXVÉ : Les complications
maternelles.
|
Complications
|
N cas
|
%
|
|
Eclampsie
|
23
|
21,1%
|
|
IRA
|
10
|
9,2%
|
|
HRP
|
8
|
7,3%
|
|
Ascite
|
6
|
5,5%
|
|
HELLP syndrome
|
5
|
4,6%
|
|
Rétinopathie
|
5
|
4,6%
|
|
OAP
|
2
|
1,8%
|
|
CIVD
|
2
|
1,8%
|
3.6.2. Les complications foetales.
3.6.2.1. La mortalité foetale et
néonatale.
Sur 114 bébés attendus des
104 grossesses mono foetales et 5 grossesses
gémellaires, 38 soit 33,33% sont décédés
dont :
-3 (2,63%) interruptions thérapeutiques
de grossesse pour sauvetage maternel,
-17 (14,91%) MFIU,
-18 (15,79%) décès
périnataux.
On ne connaît pas le devenir d'un bébé
hypotrophe transféré in utero vers la clinique prince Louis
Rwagasore, par manque d'O2 au centre hospitalo-universitaire de Kamenge.
3.6.2 .2. La morbidité
La mortalité foetale et néonatale
élevée est dû à deux complications qui sont
extrêmement fréquentes, la prématurité et
l'hypotrophie observée dans respectivement dans 45%(51
bébés) et 52,6% (60
bébés) des naissances. Le poids moyen à la
naissance est de 2221,2grs
avec des extrêmes de 1050 et 4700grs.
31 (28,4%) sont des grands prématurés
(nés avant 33SA).
3.6. Durée d'hospitalisation.
3.6.1. Durée entre hospitalisation et
accouchement.
Quatre vingt dix neuf patientes soit 90,8% ont
accouché dans les dix jours suivant leur admission dont
56 (51,4%) dans les 24heures. Le tableau n°
XXVÉÉ montre que l'hospitalisation n'a permis de gagner tout
au plus que 2semaines dans 8,2% des cas. Deux
patientes seulement ont dépassées 3 semaines
d'hospitalisation avant l'accouchement. La durée moyenne entre
l'admission et l'accouchement est de 3,62 jours.
Tableau n°XXVÉÉ : durée entre
hospitalisation et accouchement.
|
Durée entre Hospitalisation
&Accouchement
|
N de Cas
|
%
|
% Cumulés
|
|
= 1 jr
|
56
|
51,4%
|
51,4%
|
|
2-10 jrs
|
43
|
39,4%
|
90,8%
|
|
11-19 jrs
|
7
|
6,4%
|
97,2%
|
|
20-28 jrs
|
1
|
0,9%
|
98,2%
|
|
= 28 jrs
|
1
|
0,9%
|
99,1%
|
|
inconnue
|
1
|
0,9%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0
|
3.6.2. Durée entre accouchement et sortie.
La durée moyenne est de 8,12 jours avec
des extrêmes de 1 à 40 jours. Le tableau
n°XXVII montre que (15 cas) 13,8% sont sortis
précocement de la maternité et (82 cas) 75,2%
sont sortis dans les 9 jours suivants leur
accouchement. 14 patientes (12,8%) sont sorties tardivement de la
maternité (durée d'hospitalisation = 2
semaines).
Tableau n°XXVÉÉÉ : durée
entre accouchement et sortie de la maternité.
|
durée entre accouchement et sortie
|
|
N de cas
|
%Cumulés
|
|
=1 jr
|
15
|
13,8%
|
13,8%
|
|
2-5 jrs
|
11
|
10,1%
|
23,9%
|
|
6-9 jrs
|
56
|
51,4%
|
75,2%
|
|
10-13 jrs
|
12
|
11,0%
|
86,2%
|
|
14-17 jrs
|
7
|
6,4%
|
92,7%
|
|
=18jrs
|
7
|
6,4%
|
99,1%
|
|
inconnue
|
1
|
0,9%
|
100,0%
|
|
Total
|
109
|
100,0%
|
100,0%
|
3.6.3. Durée totale d'Hospitalisation.
La durée totale moyenne d'hospitalisation est de
11,74 jours avec des extrêmes de 1 à
40jours.
4. Discussion et revue de la littérature.
4.1. Données Epidémiologiques.
4.1.1. La fréquence.
La fréquence de l'association HTA et grossesse est
diversement appréciée dans la littérature. Elle est
estimée entre 5et 10 % aux Etats-Unis (5),
10 à 15% en France (7, 19), 9%
en Chine (21). En Afrique sub-saharienne, Bah et coll. (22)
rapportent une fréquence de 17, 05% en
Guinée Conakry, Touré et coll. (23) trouve une
fréquence de 8,9% au Niger et Attolou et coll.
(24) trouvent une fréquence de 7,65% au
Bénin. Deux études effectuées au Burundi,
une en 1988, sur les maladies hypertensives et grossesse par Sindayirwanya et
Coll. (25), l'autre en 1991 par Nakintije (26), relèvent une
fréquence de 2,38%. Dans notre étude
nous avons une fréquence de 1,83%. Même si notre
fréquence est proche de celle rapportée au Burundi, elle est
largement inférieure à celle rapportée par les
différents auteurs ci hauts cités. Nous pensons que notre
étude qui est rétrospective sous-estime la fréquence
réelle pour différentes raisons. Premièrement le
classement et l'archivage des différents registres et dossiers
médicaux accusent beaucoup d'imperfections et certains cas passent
probablement inaperçus. Secundo, une notification et une
recherche non systématique de tous les cas. En effet, en l'absence d'une
prise systématique de la TA, certains cas
d'hypertension gestationnelle modérée, sans autres manifestations
cliniques, restent méconnus.
Nous pensons qu'une étude prospective à large
échelle incluant les services de consultations prénatales et
services d'hospitalisations recherchant systématiquement les cas de HTA,
pourrait apporter la lumière sur la fréquence réelle de
l'association HTA et grossesse dans notre pays.
4.1.2 Facteurs de risques.
4.1.2.1. L'âge.
Dans notre étude, l'âge varie de 18 ans
à 43 ans et la moyenne est de 29,97ans. La
tranche d'âge la plus touchée est celle de
26-31ans qui représente 47,7% des
patientes. Ces données sont semblables à ceux rapportées
par d'autres auteurs. Bah et coll. (22), rapportent un âge qui varie
entre 15ans et 44ans avec une moyenne de 25ans #177;
7ans. Xu xiong et coll. (21) en Chine trouvent un âge moyen de
25,7ans #177; 2,7ans. Au Burundi,
Nakintije (26) a trouvé en 1991, un âge moyen de
27,5ans avec des extrêmes de 17 ans et
38 ans. L'HTA induite par la grossesse
(hypertension gestationnelle, pré-éclampsie, éclampsie)
touche avec prédilection la femme jeune, surtout en
début de leur activité génitale. Par contre, l'HTA
chronique touche la femme d'âge mûr. Pour
Sibaï (27) la fréquence de l'HTA
chronique chez la femme enceinte croît de
0,6 à 2% entre 18 ans et 29 ans, mais
passe de 4,6 à 22,3% entre 30ans et
39ans.
4.1.2.2. Origine et profession.
La majorité de nos patientes sont originaires de Bujumbura
Mairie (78%) et sont dans plus de la moitié des cas,
des fonctionnaires (53,2%) suivis par des
ménagères et cultivatrices qui représentent
39,4%. Cela s'explique par le fait que le Centre
HospitaloUniversitaire se trouve dans la ville de Bujumbura et est
majoritairement fréquenté par les habitants de Bujumbura qui
sont, pour la plupart des fonctionnaires du secteur privé ou public.
Dans la littérature, seul le fait d'être originaire d'une
région située en haute altitude (atmosphère
pauvre en O2) a été signalé comme étant un
facteur de risque de la prééclampsie (7). L'étude
de Bah et coll. (22) montre une prédominance des patientes non
scolarisées (73,47%) et celle de Touré
et coll. (23) montre une prédominance des
ménagères (88%). Cela trouve une
explication dans le fait que ces études se sont déroulées
dans des communautés où les non scolarisées et les
ménagères sont les plus nombreuses par rapport aux
scolarisées et aux fonctionnaires.
4.1.2.3. Gestité et Parité.
Dans notre étude, les primigestes et les
nullipares sont les plus touchées avec respectivement 37%
et 42,2%, ce qui en accord avec les données de la
littérature (6, 7, 8, 19, 21, 22, 23, 26). Cela est d'autant plus vrai
qu'il s'agit d'une HTA induite par la grossesse, en particulier la
pré-éclampsie. Aux Etats Unis, Hauth et coll. (28), estiment que
l'HTA gestationnelle touche entre 6% et 17% des
nullipares en bonne santé contre 2% à 4%
des multipares. Ceci suggérerait l'implication d'un
facteur immunologique. Il est possible que la tolérance des
antigènes foeto-placentaires par l'organisme maternel soit
facilitée par l'exposition préalable aux antigènes
paternels. Ainsi la pré-éclampsie est plus fréquente en
cas de brève exposition préalable aux spermes du géniteur,
de changement de géniteur quelque soit le rang de la gestité et
d'insémination avec les spermes d'un donneur (7).
4.1.2.4. Les antécédents familiaux.
L'existence des antécédents de
pré-éclampsie chez la mère ou la soeur augmente
l'incidence de pré-éclampsie d'un facteur 3 à
5(7). Ness et coll. (29) ont montré que le fait d'avoir 2
ou plusieurs membres de la famille hypertendus augmente de deux
fois, le risque de développer une
pré-éclampsie ou une HTA transitoire de la grossesse. De
même, des antécédents familiaux de maladies
cardio-vasculaires, de néphropathies, de diabète augmente le
risque de faire une Pré-éclampsie (29). Bah et coll. (22) ont
trouvé que dans leur série de 226 cas d' HTA
gestationnelle, 32,74% avaient un antécédent
familial de HTA. Dans notre étude nous ne pouvons pas conclure,
car les antécédents familiaux n'ont pas étaient
recherchés. Dans l'étude prospective de Nakintije en 1991,
18% avaient des antécédents familiaux de
HTA et 5% avaient des antécédents
familiaux de diabète (26). Ces antécédents doivent
être recherchés systématiquement pour épingler ceux
qui ont un risque de développer une HTA gestationnelle et instaurer une
bonne surveillance.
4.1.2.5. Les antécédents personnels.
Des études prospectives ont montré que des
patientes qui soufrent d' HTA, du diabète, d'une
néphropathie, de thrombophilie ou de collagénoses ont un
risque accru de développer une pré-éclampsie ou une
hypertension gestationnelle (11,29). Par rapport à une
femme qui n'est pas hypertendue, l'HTA chronique multiplie le
risque de développer une prééclampsie par un facteur
de 2 à 7(3). 8,3% de nos patientes
avaient une HTA chronique. 67,67% des patientes n'ont
aucun antécédent médical ou obstétrical
connu. Cela peut être dû au fait que, plus d'un tiers de nos
cas sont des primigestes pour qui, la grossesse a été la
première occasion de contact avec les structures de soins et que l'HTA
gestationnelle constitue probablement la première manifestation d'une
pathologie sous-jacente. Dans notre série, les antécédents
obstétricaux personnels sont dominés par des
antécédents de fausses couches, de RCIU, de MFIU et de
pré-éclampsie. En effet, après un épisode de
prééclampsie, de RCIU ou d'une MFIU d'origine vasculaire le
risque de récidive n'est pas négligeable. Ce risque
dépend de la sévérité de l'épisode
précédente et de sa date d'apparition. Il est
inférieur à 10% dans les formes peu
sévères et d'apparition tardive, mais peut atteindre 50%
dans les formes sévères survenant avant 30 semaines de
grossesse (3).
4.1.2.6. Type de grossesse.
Par rapport à une grossesse mono foetale, une grossesse
multiple comporte un risque accru de développer une
pré-éclampsie (30). Ce risque serait du à une
sur-distension utérine comprimant les artères utérines,
réduisant ainsi le flux sanguin utérin, à la quelle
s'ajoute un gros volume placentaire à perfuser, source d'une mauvaise
perfusion placentaire, responsable de la pré-éclampsie. Ce
dernier mécanisme est aussi invoqué en cas d'hydramnios ou de
grossesse molaire(7,19). La gémellité représente
5% des grossesses dans notre série, 11%
dans celle de Nakintije, alors que le taux de grossesses multiples est
de 2,12% de tous les accouchements (2 6). Pour Bah et coll.
(22), en cas de grossesse gémellaire chez la primigeste, l'incidence de
la toxémie gravidique est 2,5fois plus
élevée.
4.2. Prise en charge.
4.2.1. Délai entre la symptomatologie et la
consultation.
La découverte d'une hypertension artérielle est
parfois fortuite au cours d'une consultation prénatale de routine, mais
peut être aussi découverte à l'occasion des signes
cliniques (céphalées, troubles visuels, douleur
épigastrique en barre, des oedèmes modelant le faciès
etc..) qui amènent la patiente à consulter après un
délai variable selon les patientes. Ce délai devrait être
le plus court possible, car il permet une prise en charge précoce. Cela
suppose que les patientes soient éduquées à
reconnaître les signes précoces de la maladie et à
consulter rapidement. Malheureusement, dans notre étude, ce
délaie est relativement long puisque il est en moyenne de 4,8
jours avec 21,1% qui ont consulté
après une semaine. Nous n'avons pas trouvé d'autres
études qui ont pris ce critère en considération pour
pouvoir comparer avec notre étude, mais nous pensons que le mauvais
pronostic observé dans notre est en partie lié à ce retard
de consultation.
4.2.2. Consultations prénatales.
Nous dégageons de notre étude que les
consultations prénatales ne sont pas régulièrement
suivies, ce qui fait que le diagnostic est souvent fait au stade clinique ou
des complications de la maladie. Seulement 12,8% des cas ont
suivi régulièrement les consultations prénatales
(= 5 CPN au moment de leur admission) comme c'est
recommandé. Xiong (21) et coll. dans leur étude en Chine sur
l'hypertension gestationnelle en Chine trouvent un nombre moyen de
consultations prénatales de 9#177;3 et
l'âge de la grossesse à la
première consultation se situait à
12#177;6,9 SA. Dans notre étude, 34,9%
n'ont fait aucune consultation prénatale avant leur admission.
Des études faites dans les pays en voie de développement montrent
des résultats semblables aux nôtres. 42% des
patientes n'ont pas eu de consultations prénatales dans l'étude
de Pambou et coll. (31) réalisée au CHU de Brazzaville à
propos de 100 cas d'éclampsie. Des consultations
prénatales de qualité ont permis dans les pays
développés, de réduire considérablement le taux
morbi-mortalité due aux grossesses à risques (11,20). Dans notre
pays, des efforts doivent être portés sur la sensibilisation des
gestantes à suivre les consultations prénatales et à
l'amélioration de leur qualité.
4.2.3. Types de HTA.
Plusieurs types de classifications existent, mais celle qui est
plus utilisée est celle de la société internationale
pour l'étude de l'hypertension gravidique [ISSHP] (32). Quatre
types de troubles hypertensifs de la grossesse sont individualisés :
la pré-éclampsie, l'HTA chronique, la
pré-éclampsie surajoutée et l'hypertension gestationnelle
transitoire ou isolée (sans protéinurie). La
pré-éclampsie est celle qui a le mauvais pronostic et c'est
elle qui prédomine dans notre étude avec 79,8%
des cas.
Tableau n° XXÉX : types de HTA et revue de la
littérature.
|
Auteur(s),
|
Pré- éclampsie
|
HTA chronique
|
Pré-
éclampsie
surajoutée
|
HTA gestationnelle transitoire
|
Non classée
|
|
Attolou et coll. (24),
|
26,41%
|
41,51%
|
18,87%
|
13,21%
|
0%
|
|
Touré et coll. (23)
|
27,1%
|
7,2%
|
0%
|
55,7%
|
10%
|
|
Nakintije (26)
|
48,2%
|
0%
|
1,79%
|
41,07%
|
8,93%
|
|
Bah et coll. (22)
|
66,37%
|
8,41%
|
6,19%
|
19,03
|
0%
|
|
Notre étude
|
79,8%
|
3,7%
|
4,6%
|
6,4%
|
5,5%
|
Le tableau n° XXÉX montre que, même si
toutes ces études citées ont été effectuées
dans les pays en voie de développement (Bénin, Niger, Burundi,
Guinée), la proportion de chaque type de HTA gestationnelle varie d'une
étude à l'autre. Dans notre étude comme dans celle de Bah
et coll. (22), la pré-éclampsie prédomine. Le taux de
HTA chronique est inférieur à 10%, sauf
dans l'étude d'Attolou et coll. (24) où il est de 41,51%
sans qu'aucune explication ne soit fournie. Cette classification est
imparfaite car implique une idée de pronostic materno-foetal constamment
démenti par les faits. Une classification proposée par la
conférence de consensus de la société
canadienne d'hypertension en 1997, tente de parier à cette
insuffisance en rajoutant à chaque type de HTA, l'existence ou non
des facteurs défavorables (6). Les facteurs
défavorables étant des symptômes, des signes et/ou des
anomalies des testes biologiques dont la présence annonce que le risque
de complication est élevé. De plus ces classifications ne
considèrent pas le terme de la grossesse au moment du diagnostic de
l'HTA, alors que c'est un élément qui a une grande influence sur
le pronostic, en particulier le pronostic foetal. Une HTA
gestationnelle découverte près du terme, ne pose
pas les mêmes problèmes de surveillance ou de prise en charge
qu'une HTA gestationnelle découverte avant 34SA.
4.2.4 : Etude clinique.
4.2.4. 1 : Le terme à l'admission.
Il est en moyenne de 35SA confirmant, comme les
autres l'ont déjà constaté, que le diagnostic de l'HTA
gestationnelle se fait souvent au 3ème trimestre de la
grossesse (22,23). 7cas (6,4%) seulement ont été
diagnostiqué et admis au 2ème
trimestre (= 28SA) et leur pronostic foetal est sombre,
avec 3 abandons foetaux pour sauvetage maternelle (ITG),
3 MIU, et un décès
périnatal. Dans l'étude sur l' hypertension
gestationnelle au CHUK de Nakintije (26), 92,59 % des cas ont
été diagnostiqué au 3ème
trimestre, dont 53,9% à terme. Ces
résultats sont semblables aux nôtres puisque nous avons
93,6% des cas diagnostiqués au troisième
trimestre avec 29,5% diagnostiqués au
delà de 37SA.
4.2.4. 2 : les signes cliniques.
La majorité de nos cas ont été admises
immédiatement en hospitalisation et souvent dans un tableau de HTA
sévère. La TA moyenne à l'admission est de
16,98/10,99cm Hg avec 87,3% qui ont une
tension systolique sévère (=16cm Hg) et
33,9% ont une tension diastolique = 12cm Hg.
A cette HTA sévère s'ajoutent d'autres signes de
gravité, tels que des céphalées (plus d'un
cas sur deux), des troubles visuels et/ou auditifs, des oedèmes
importants d'installation brutale, modelant les traits du visage (faciès
lunaire) et au niveau des extrémités (membres supérieurs
et inférieurs), une douleur de l'hypochondre droit etc. Dans
l'étude de Nakintije (26) en 1991, même si la TA moyenne
(17,07/10,50 cm Hg) est presque égale à la
notre, les signes cliniques de gravités étaient
moins fréquents ; 10,7% avaient des
céphalées et un cas avait une douleur
épigastrique. La prédominance des formes
sévères dans notre étude expliquerait le mauvais pronostic
materno-foetal que nous avons noté dans notre étude. Des
études cas-témoins ont montré que le taux de complications
dans les formes modérées (HTA chronique, hypertension
gestationnelle isolée, pré-éclampsie) est
légèrement différent par rapport aux gestantes
normo-tendues, mais qu'il est plus élevé chez celles qui ont une
forme sévère (21, 27, 28,30). La prédominance des formes
sévères, s'explique par le fait que, le Centre
Hospitalo-Universitaire de Kamenge est un hôpital de
référence au niveau national, et pratiquement le seul à
disposer d'un service de néonatologie et reçoit souvent des cas
compliqués ou sévères (cfr tableau n°XVI)
transférés des autres formations sanitaires. Quatre cas de faux
diagnostic au moment du transfert, appellent de toute urgence une formation
à l'endroit des prestataires de soins, surtout dans les centres de
santé d'où proviennent ces cas, pour les sensibiliser sur le
diagnostic et la prise en charge de la pré-éclampsie.
4.2.5. Examens paracliniques.
Les examens paracliniques permettent d'apprécier la
gravité de l'affection, d'établir un pronostic et de suivre
l'évolution des différents paramètres biologiques.
Certains examens (NFS-plaquettes, uricémie, albuminurie,
transaminases, créatinémie, ionogramme sanguin et urinaire etc.)
doivent être faits systématiquement dès le diagnostic
de l'HTA au cours de la grossesse, d'autres doivent être demandés
en fonction des résultats de ces premiers (ECBU et
protéinurie de 24 h si albuminurie positif, LDH, PDF, haptoglobine,
bilirubinémie en cas de thrombopénie). Les résultats
de notre étude montrent que le suivi biologique des patientes est loin
d'être optimal, car dans 18,3% des cas, aucun examen n'a
été réalisé, même
pas l'albuminurie par bandelette, permettant de
différencier une hypertension gestationnelle isolée d'une
pré-éclampsie, ou une HTA chronique évoluant vers une
pré-éclampsie surajoutée. Des difficultés
financières de la part des patientes et un laboratoire
non fonctionnel 24/24h et 7/7 jours expliquent le mauvais suivi
biologique. Un effort particulier doit être fait afin que l'albuminurie
soit dépistée à chaque consultation prénatale.
Même si l'albuminurie a une corrélation médiocre avec la
quantité de protéines excrétées dans les urines,
elle a le mérite de sélectionner les patientes chez les quelles,
il est nécessaire de réaliser une protéinurie de 24heures.
Une ECBU doit être faite pour éliminer une infection urinaire.
4.2.5. 1. La protéinurie de 24 heures
La protéinurie de 24 heures a une valeur pronostique,
puisque une protéinurie = 3,5grs/24 h définit
une forme sévère de pré-éclampsie avec risque
accrue de complications (7,28). Mais il n'y pas d'unanimité sur cette
valeur seuil qui définisse une forme sévère de
pré-éclampsie, puisque certaines auteurs considèrent une
protéinurie plus basse = 1g /24 h (18) alors que
d'autres considèrent une protéinurie =5grs/24 h
(19,30). Dans notre étude, la protéinurie a été
faite chez 23 patientes (21,1%), et parmi elles,
7 patientes avaient une protéinurie =4grs/24
h. Parmi ces 7 patientes, 5 patientes ont
été césarisées en urgence pour
pré-éclampsie sévère dont 3patientes
avant 34SA. Une parmi ces dernières est
décédée en post opératoire dans un tableau
d'oedème aigue du poumon et d'insuffisance rénale.
4.2.5. 2. uricémie.
De tous les paramètres biologiques,
l'uricémie est celle qui est corrélée au
pronostic foetal. Elle est le reflet de la réduction de
la volémie donc de la réduction de la perfusion placentaire.
Le taux normal pendant la grossesse se situe entre 180
et 250pLmol/L. Son degré a une valeur pronostic. Une
uricémie =360~mol est péjorative, puisqu'elle
est retrouvée chez 90% des enfants hypotrophes
et chez 96% des morts foetale in utero (33).
Audelà de 600pLmol/L, le foetus doit être extrait
s'il est encore vivant. Dans notre étude 36,7% des cas
avaient une uricémie supérieure à 360jtmol/L, dont
8,3% (7cas) dépassaient 660ptmol/L.
Des 17 MFIU enregistrées dans notre
série, l'uricémie n'a pas été
précisée dans 9 cas et dans 3
cas, elle était supérieure à
360ptmol/L. Parmi les 7 cas dont
l'uricémie était supérieure à 660pmol/L,
6 ont accouché d'un enfant hypotrophe et
4 enfants sont décédés en période
périnatale.
4.2.5. 3. NFS-plaquettes.
L'anémie (Hgb < 11g/dl) est
fréquente au cours de la grossesse mais s'accompagne souvent d'une chute
de l'hématocrite (< 33%). Au cours d'une
pré-éclampsie l'élévation de
l'hématocrite au-delà de 40% traduit une
hémoconcentration, donc une baisse de la volémie responsable
d'une diminution de la perfusion utéro-placentaire, source d'un retard
de croissance intra-utérin. Une thrombopénie
(<100.000/mm3) est facteur de mauvais pronostic
car elle constitue un indice d'une CIVD et est un des
éléments de la triade biologique du HELLP
syndrome (18, 19,33). Les résultats de notre étude
montrent que le pronostic est mauvais si les plaquettes sont = à
100.000/mm3. Chacune des dix patientes dont les plaquettes
sont = 100.000/mm3 a fait au moins une ou deux
voire trois complications majeures. Nous avons noté dans ce groupe,
6 cas d'éclampsie dont un cas de décès
dans un tableau de mal convulsif, 3 cas de HELLP syndrome,
3 cas d'insuffisance rénale aigue, 7 cas de MFIU
et un cas d'OAP. La découverte d'une
thrombopénie doit pousser à rechercher les autres
paramètres du HELLP syndrome, notamment la recherche
d'une cytolyse hépatique par le dosage des
transaminases et une hémolyse qui se traduit par
une chute de l'hémoglobine associée à une
présence de schizocytes dans le sang périphérique
(GE).L'hémolyse peut aussi être traduite par une
élévation des LDH, une élévation de la
bilirubinémie ou une chute de l'haptoglobine (34,35). Un bilan de
coagulation (TP, TCK, fibrinogène, PDF et des
D-dimères) doit être fait pour confirmer ou infirmer une
CIVD. Dans notre étude nous avons noté 5
cas de Hellp syndrome et 2 cas de CIVD. Les deux cas
de CIVD ont été constatés en per opératoire devant
les difficultés à faire l'hémostase.
4.2.6 : La surveillance.
Elle est à la fois clinique et paraclinique. Une
surveillance bien faite, permet de suivre l'évolution des chiffres de la
TA et l'apparition des complications maternelles et/ou foetales afin
d'intervenir rapidement avant que la situation ne
dégénère.
4.2.6.1 : La surveillance maternelle.
Dans notre étude, La surveillance clinique est
extrêmement variable d'une patiente à l'autre. Elle varie d'une
visite médicale à plus de 10 visites médicales par
24 heures. En l'absence de protocole validé et affiché
dans le service sur la prise en charge de l'HTA gestationnelle, il est
difficile d'évaluer la qualité de la surveillance clinique.
Chez celles qui sont bien suivies, on retrouve un tableau de
surveillance de la TA et des signes cliniques de gravité qui est repris
chaque jour alors que chez d'autres, ce tableau est inexistant durant toute la
durée de leur hospitalisation. La surveillance du poids et de la
diurèse n'est pas faite, même pas chez les patientes qui ont des
oedèmes.
La surveillance paraclinique est elle aussi très
variable. A coté de celles qui n'ont aucun bilan biologique, on trouve
celles qui ont un bilan biologique tous les 2jours et d'autres qui ne l'ont que
toutes les 2 semaines. Cette mauvaise surveillance clinique et para clinique
retarde le diagnostic des complications et par conséquent leur prise en
charge. Une fiche de surveillance clinique et para clinique doit être
établie et utilisée pour chaque patiente en fonctions de son
état à son admission. Sibaï (30) recommande si le bilan
initial est normal et qu'il n'y pas de signes cliniques de
gravité un bilan biologique par semaine comprenant
protéinurie de 24 h, NFS-plaquettes, ionogramme sanguin,
créatinémie et dosage des transaminases. S'il y a des
signes cliniques ou biologiques de gravité, ce bilan doit
être fait chaque jour jusqu'à l'accouchement. Le bilan de
coagulation n'est pas nécessaire si les plaquettes et les transaminases
sont normales.
4.2.6.2 : La surveillance foetale.
L'élément principal de la surveillance clinique
foetale a été le compte des BCF au
stéthoscope de Pinard. On a enregistré en moyenne un
compte des BCF toutes les 4 heures. Nous n'avons pas pu évaluer
le compte des mouvements foetaux par la mère car c'est un
élément d'interrogatoire qu'on n'a pas trouvé sur la fiche
de la patiente. La hauteur utérine a été prise
systématiquement à l'admission. Si la surveillance clinique
aide à tirer une sonnette d'alarme, c'est avec les examens
paracliniques qu'on peut évaluer l'état foetal.
L'échographie constitue un outil irremplaçable,
car elle permet d'apprécier la croissance foetale par les
biométries, d'évaluer la quantité de liquide amniotique et
d'apprécier le bien être foetal (score de Manning).
Couplée au Doppler pulsé ombilical et
cérébral, elle permet surtout en cas de RCIU,
d'étudier le retentissement de la réduction de la perfusion
utéroplacentaire sur le foetus. Une diastole ombilicale nulle ou
négative (reverse flow) et une diastole cérébrale
élevée précède de peu la MFIU
et leur présence est un critère d'extraction foetale en
urgence. Il est recommandé de faire une échographie au
moment du diagnostic et en fonction des résultats de cette
première échographie et du tableau clinique maternel, une
échographie toutes 2 à 4 semaines (18, 19,30). En cas de
diminution des mouvements actifs du foetus, l'échographie et
l'étude du rythme cardiaque foetal permettent l'appréciation
du
bien être foetal par le score de Manning
(33). L'autre examen indispensable est l'enregistrement du rythme
cardiaque foetal, car ces altérations sont tardives et
précèdent de peu les lésions cérébrales de
l'hypoxie. Les altérations du RCF même en apparence
modérées sont témoins d'une souffrance foetale
sévère et constituent un bon critère d'extraction
foetale. On recommande de le faire une fois par semaine
dans les HTA modérées sans RCIU, et de le faire
tous les jours dans les formes
sévères (18,30). Malheureusement les résultats de
notre étude montrent que ces examens ne sont pas facilement accessibles
pour toutes les patientes puisque un bon nombre n'en ont pas
bénéficié. 34,9% n'ont pas eu
d'échographie foetale, 66,1% n'ont pas eu
de Doppler et 73,4% n'ont pas eu d'enregistrement
du rythme cardiaque foetal. Pour améliorer la surveillance foetale,
la maternité du CHU de Kamenge devra se doter d'un échographe et
d'un appareil de monitoring foetal, sans oublier un personnel utilisateur
qualifié, afin de rendre ces examens accessibles 24/24 heures et 7/7
jours.
4.2.7 : La prise en charge thérapeutique
Une des mesures thérapeutiques les plus anciennes est
le repos absolu au lit en décubitus latéral gauche. Il
est sensé réduire les chiffres tensionnels et améliorer la
perfusion utéro-placentaire en libérant la compression de l'aorte
et de la veine cave inférieure due à la dextrorotation droite de
l'utérus. Son utilité tend à être contestée
et certains auteurs le trouvent même délétère car il
augmente le risque thromboembolique, sans que son effet bénéfique
soit clairement établi (19,30). Dans notre étude, il a
été systématique chez toutes les patientes, mais nous
n'avons pas noté de complications thromboemboliques.
A ce repos au lit, on y adjoint un traitement
hypotenseur. L'alpha-méthyldopa est largement
utilisé en cas d'hypertension modérée (= 16/10 cm
Hg) à dose progressive de 500mg à 1500mg/24
heures. En cas de pic hypertensif on y associe une
gélule d'Adalate® rapide 10mg. En cas de HTA
sévère ou en cas d'échec des antihypertenseurs
précédents, la clonidine (catapressan®) est
utilisée par voie intraveineuse en perfusion continue à dose
progressive. Le choix du catapressan® nous semble être
dicté par sa disponibilité. Le Nepressol® (Hydralazine)
ou la Trandate® (Labétalol) autre fois utilisé en cas
d'éclampsie n'est plus disponible au CHUK (36). En France, la
Loxen® (nicardipine) est le médicament de première
intension en cas d'hypertension gestationnelle ou de
pré-éclampsie sévère (7). Elle a une action
vasodilatatrice puissante et une action rapide, mais son inconvénient
est qu'elle est contre indiquée en cas d'usage du sulfate de
magnésium
qui constitue le meilleur traitement en cas de crise
d'éclampsie (30). Aux Etats-Unis, Sibaï (30) utilise en
première intension la Labétalol (Trandate®)
jusqu'à la dose maximale de 220 mg et si
inefficace, il ajoute la nifédipine rapide par voie orale. Le
traitement antihypertenseur influence peu le pronostic de la grossesse, son
seul objectif est d'éviter les à-coups hypertensifs responsables
des accidents vasculaires cérébraux chez la mère. A
l'opposé un traitement hypotenseur trop énergique aggrave la
souffrance foetale car il réduit la perfusion utéro-placentaire
(18, 19,33). Il est recommandé de ne pas abaisser les chiffres
tensionnels en dessous de 14/9 cm Hg. Les
études comparant l'abstention thérapeutique ou placebo au
traitement antihypertenseur jusqu'à l'accouchement en cas de HTA
modérée ne montrent aucun bénéfice sur le pronostic
foetal, sauf une petite réduction du risque d'évolution vers une
HTA sévère (37). Pour Sibaï (30), le traitement de HTA
modérée peut retarder le diagnostic de l'HTA sévère
et recommande une bonne surveillance sans traitement antihypertenseur.
L'abstention thérapeutique est légitime devant une hypertension
légère à modérée (systolique
<16cm Hg et/diastolique <10 cm Hg).
En cas de prématurité précoce
(<34SA) l'administration d'un
corticoïde permet de réduire les conséquences
liées à la prématurité. Dans notre
étude 86,11% des patientes admises entre 26 et
34SA ont reçu du déxaméthasone (12mg en IM
renouvelé 24h après). Une étude prospective
randomisée en double aveugle d'une série de 218 patientes
ayant une pré-éclampsie sévère et
un âge gestationnel compris entre 26 et 34 SA, certaines
recevant de la bétaméthasone (n =110),
d'autres un placebo (n=108) a montrée une
réduction de 53% du syndrome de détresse respiratoire chez celles
qui ont reçu du bétaméthasone. La
corticothérapie était également associée
à une réduction du risque d'hémorragie intra
ventriculaire du nouveau-né (RR : 0,35), du risque d'infection
néonatale (RR : 0,39) et du risque de décès
néonatal (RR : 0,5). Si on considère les complications
maternelles, il n'y pas de différance entre les deux groupes (38).
En cas d'éclampsie ou d'existence de signes
annonciateurs d'une crise d'éclampsie, le traitement de choix
est le sulfate de magnésium (4g en 15 minutes suivies d'une dose
d'entretien de 1 à 2 g/h à la pousse seringue électrique,
jusqu'à 24h post-partum (18,19). En effet, une étude
multicentrique randomisée menée dans 33
pays, incluant 10141 femmes (571 recevant du
sulfate de magnésium, 570 recevant un placebo) a montrée et
sans risque pour le foetus, une réduction du risque
d'éclampsie et de la mortalité maternelle de 50% dans le
groupe traité par sulfate de magnésium par rapport au groupe
recevant un
placebo (39). L'usage du sulfate de magnésium
exige une surveillance spéciale (fréquence respiratoire,
diurèse, réflexes ostéo-tendineux). En cas de surdosage
(dépression respiratoire, abolition des ROT), il faut arrêter le
traitement et administrer une ampoule de gluconate de calcium qui est
son antidote. Les benzodiazépines (diazépam,
clonazépam, midazolam) sont une alternative, mais sont
responsables d'une intoxication chez le nouveau-né de
sévérité et de durée variable (jusqu'à 15
jours) avec dépression respiratoire, troubles de
thermorégulation, troubles de la succion, hypo réactivité,
hypotonie, pouvant être suivie d'un syndrome de sevrage
(hyperexcitabilité, trémulations, et troubles digestifs à
type de diarrhées et de vomissements (7). Dans notre étude
le traitement de la crise d'éclampsie a fait appel au
Diazépam (Valium®). Le sulfate de magnésium n'a pas
été utilisé car indisponible au CHU de
Kamenge. Son usage doit être promu et sa disponibilité garantie
car son intérêt par rapport aux autres anticonvulsivants a
été démontré.
4.2.8 : La prise en charge obstétricale.
Le seul véritable traitement de l'HTA
induite par la grossesse est la délivrance. Si la
décision est aisée à prendre à l'approche du terme,
la survenue précoce de la maladie impose la recherche d'un moins mauvais
compromis entre la naissance d'un enfant avec un minimum de séquelles et
le risque de complications maternelles potentiellement mortelles. Dans
l'hypertension gestationnelle ou pré-éclampsie
légères à modérées, sans signes de
souffrance foetale, l'expectative jusqu'à 37SA est de règle
puis déclenchement ou césarienne. Après 37SA, Caughey
et coll. (40) ont montré que le risque de complications maternelles
(HRP, éclampsie, etc.) s'accroît, alors que
l'expectative n'améliore pas le pronostic foetal. Dans
l'hypertension gestationnelle ou pré-éclampsie
sévère, en raison du risque élevé de
morbi-mortalité materno-foetale, il est universellement admis qu'il faut
provoquer l'accouchement si la maladie se développe après 34
SA (7,30). L'accouchement immédiat souvent par césarienne
est clairement indiqué quelque soit le terme en cas de :
4 Hypertension incontrôlable malgré un
traitement intraveineux bien conduit,
4 Éclampsie ou menace d'éclampsie (signes
cliniques persistants),
4 Défaillance multi-viscérale (HELLP syndrome,
IR, OAP),
4 RCIU sévère (=5ème
percentile),
Hématome rétro placentaire,
Existence de signes de souffrance foetale.
Bien que l'accouchement quelque soit le terme permet de
réduire la morbi-mortalité maternelle, c'est au prix d'une
augmentation de la prématurité iatrogène dont les
conséquences néonatales dépendent de l'âge de la
grossesse au moment de l'accouchement. Ainsi avant 34 SA,
certains auteurs proposent une prolongation de la grossesse
à condition que sous traitement, l'état maternelle soit
stable, les tests foetaux rassurants et que le centre
qui suit la patiente dispose d'un personnel et d'un équipement
médical, permettant une bonne surveillance materno-foetale. Le centre
doit être capable d'assurer une réanimation materno-foetale en cas
de détérioration de l'état maternel et/ou foetal (7, 19,
30,41). Pour Sibaï (30), aux Etats-Unis, entre 33 et 34
SA, les patientes reçoivent une
corticothérapie et l'accouchement (souvent par
césarienne) est réalisé 48 h après.
Si le terme est <23 SA, une interruption
thérapeutique de grossesse est proposée en concertation avec
les parents, puisqu'à cette âge le taux de survie
néonatale ne dépasse pas 10% et pour
les survivants le taux d'infirmité est de
90%. Entre 23-32 SA, les patientes reçoivent
un traitement individualisé basé sur la réponse clinique
au traitement durant les 24 premiers heures. Si la TA est bien
contrôlée et les tests foetaux (échographie- Doppler,
score de Manning, enregistrement du rythme cardiaque foetal) rassurant,
elles sont surveillées en unité de soins intensive
jusqu'à 34 SA ou jusqu'à ce qu'il y est une
indication maternelle et/ou foetale pour provoquer l'accouchement. Dans notre
étude 28,4% ont accouché avant 33
SA et parmi eux 3 patientes dont le terme de la
grossesse est =26 SA ont eu une ITG.
L'expectative n'a permis de gagner en moyenne que moins de 4jours (3,62
jours). Dans plus d'un cas sur deux (51,4%)
l'accouchement a eu lieu dans les 24 h suivant leur admission.
L'expectative n'est généralement envisageable que dans
certains cas bien choisis, dont l'état maternel et foetal est rassurant,
mais dans les autres cas, nous pensons que l'accouchement est la bonne
attitude, surtout dans nos pays où l'équipement médical et
le personnel sont insuffisants pour assurer une bonne surveillance
materno-foetale.
4.2.9. Voie d'accouchement.
En raison du risque encouru par la mère et/ou le foetus,
l'accouchement a souvent lieu par césarienne. En cas de grossesse
compliquée de HTA, le risque d'accoucher
par césarienne est multiplié par 2
par rapport aux autres parturientes. Nous avons noté dans notre
étude que le taux de césarienne est de 32,3 % de
tous les accouchements alors qu'il est de 66,1% chez
celles dont la grossesse était compliquée de HTA. Ce
taux de césarienne est plus élevé comparativement à
celui trouvé dans des études publiées
antérieurement. Il est de 19% dans l'étude de
Nakintije (26), et 39,1% dans celle de Sindayirwanya et Coll.
(25). Le taux de césarienne est influencé par la
sévérité de la maladie et atteint 75%
dans les formes sévères (21) et 85%
si le terme est précoce (<27SA) (42). Le
déclenchement artificiel du travail se solde souvent par un échec
en raison de l'immaturité du col.
4.3. Les complications.
Elles sont fréquentes et souvent l'apanage de la
pré-éclampsie. D'apparition et d'évolution souvent rapide,
elles imposent l'arrêt de la grossesse qui est à l'heure actuelle
le seul véritable traitement, quelque soit le terme de la grossesse.
4.3. Les complications maternelles.
L'évolution a été fatale dans cinq cas soit
un taux de mortalité de 4,6% (5 sur 109 cas). Les
désordres hypertensifs de la grossesse représentent
71,43% des causes de la mortalité maternelle
(5décès / 7décès au total) sur toute la
période de l'étude. 4/5 des patientes ont
développé une pré-éclampsie sévère
avant 32 SA et aucun nouveau-né n'a survécu. Une seule
patiente a fait une éclampsie du post-partum, qui a été
mal prise en charge dans un centre de santé (traitement par
antibiothérapie), car non reconnue et transférée au
8ème jour post-partum dans un tableau de coma profond et est
décédée une heure après son admission.
L'âge de la grossesse au moment du diagnostic et la
sévérité du tableau clinique ont une grande valeur
pronostic. Le développement sanitaire et la prise en charge
multidisciplinaire (obstétriciens, pédiatres et
réanimateurs) ont permis de réduire la morbimortalité
maternelle dans les pays développés. Elle reste
élevée dans les pays en voie de développement. En
France l'éclampsie est responsable de 2% des
décès maternelles (7,19). Aux Etats-Unis, la
mortalité maternelle est de 0,2% et le taux de
morbidité de 5% en cas de pré-éclampsie
sévère (30). Pambou et coll. (32) rapportent au CHU de
Brazzaville une mortalité de 6% en cas
d'éclampsie. Bukuru (36) au Burundi a trouvé en 1998 une
mortalité de 12% en cas d'éclampsie. Bah et
coll. (43) ont trouvé une mortalité de 5,3%
en Guinée en cas de grossesse compliquée de
HTA. Pour Touré et coll. (23) au Niger, cette mortalité
est estimée à 2,8%. Dans les pays en voie de
développement, la réduction de la mortalité
maternelle passera par l'application des soins dont
l'utilité est déjà établie, et
l'amélioration des infrastructures sanitaires.
4.3.2. Les complications foetales.
Deux complications sont extrêmement fréquentes
: l'hypotrophie secondaire à l'insuffisance placentaire et
la prématurité souvent iatrogène. Ces deux
complications conditionnent le pronostic foetal et néonatal. Le taux de
mortalité foetal et néonatale précoce est de
33,33% dans notre étude, dont 2,63%
d'abandon foetal pour sauvetage maternelle, 14,91%
de MFIU, 15,79% de mortalité
périnatale précoce. Sindayirwanya et coll. (25) ont
montré que la mortalité périnatale est
multipliée par 5 en cas de maladie hypertensive gravidique puisqu'elle
est de 20% contre 4% dans la population générale. Une
étude cas témoin réalisée à Niamey (Niger) a
montré une mortalité foetale quatre fois plus
élevée chez le groupe des gestantes hypertendues par rapport
à celui des normo tendues (23). En Guinée Conakry, Bah
et coll. (43), ont trouvé une mortalité périnatale
de 28,88% au cours des désordres hypertensifs de la
grossesse dont 55 cas de MFIU et 12 cas de
décès néonataux. Même dans les pays
développés, la mortalité foetale reste
élevée en cas de grossesse compliqué d' HTA
particulièment en cas d'éclampsie. En France le taux de
mortalité néonatale est de 12,5% en cas
d'éclampsie (44).
5. CONCLUSION ET RECOMMANDATIONS
5. 1. CONCLUSION.
Les désordres hypertensifs de la grossesse
représentent la première cause de décès maternel au
centre hospitalo-universitaire de Kamenge. La
pré-éclampsie surajoutée ou non prédomine avec
84,4% des cas. Le pronostic foetal et néonatal est
particulièrement sévère avec 33,33% de
décès foetal et néonatal. La morbidité
maternelle est également importante car dans plus d'un cas
sur cinq l'évolution s'est faite vers une crise
d'éclampsie.
La prise en charge reste difficile dans un contexte de sous
équipement (impossibilité de monitorer la TA (pas de Dynamap
ou une holter tensionnel), une gamme d'antihypertenseurs peu
diversifiée (un seul utilisable par voie intraveineuse le
Catapressan®) et absence de seringues auto pousseuses permettant
d'administrer correctement les doses prescrites. A cela s'ajoute un
problème de suivi paraclinique (laboratoire non fonctionnel 24 / 24
H et 7j/7j, absence d'échographe dans le service,
appareil de monitoring en panne pendant plusieurs mois et
s'il est fonctionnel absence de papier pour imprimer).
Afin d'améliorer le pronostic materno-foetal, un effort
particulier doit être fourni pour corriger toutes ces insuffisances. Les
prestataires des consultations prénatales doivent veuillez à ce
que la tension artérielle soit prise systématiquement et demander
aux futures mères de suivre correctement le calendrier des CPN.
5. 2. RECOMMANDATIONS.
Afin de réduire la morbi-mortalité
materno-foetale, nous recommandons ce qui suit :
1. Aux pouvoirs publics :
4 de promouvoir les consultations prénatales par une
information, éducation et communication à toutes les futures
mères.
4 d'assurer une formation de tous ceux qui sont chargé de
faire les consultations prénatales afin d'améliorer leur
qualité, pour qu'ils puissent détecter les futurs mères
à risque, afin d'intensifier la surveillance, de détecter
précocement les cas qui risquent de dégénérer et de
les référer le plus rapidement possible vers une structure
sanitaire capable de les prendre en charge correctement.
4 développer un système de référence
contre référence performant et fonctionnel 24/24 heures.
2. Au Centre Hospitalo-universitaire de Kamenge :
4 de promouvoir une prise en charge multidisciplinaire
(obstétriciens, pédiatres, réanimateurs) des cas graves de
pré-éclampsie.
4 d'élaborer un protocole de prise en charge des cas
d'hypertension gestationnelle et l'afficher ou le rendre disponible dans le
service de maternité afin de standardiser la conduite à tenir en
fonction du tableau clinique de chaque patiente.
4 d'élargir la liste d'antihypertenseurs,
particulièment ceux utilisables par voie intraveineuse (Nicardipine
[LOXEN®], Trandate® etc..) pour permettre une prise en charge des cas
de HTA sévère.
4 de disponibiliser des seringues auto-pousseuses, des Dynamap,
et holter tensionnels pour une meilleure dispensation des doses
d'antihypertenseurs et une bonne surveillance de la tension
artérielle
4 de disponibiliser et promouvoir l'usage du Sulfate de
Magnésium en cas d'éclampsie ou de pré-éclampsie
sévère avec des signes de menace d'éclampsie.
4 de doter le service de maternité d'un échographe
avec Doppler et d'un appareil de monitoring foetal et leurs accessoires (gel,
papiers).
4 doter la maternité d'un personnel suffisant,
compétant et motivé.
Bibliographie
1. Mounier-Vehier C, Equine O, Valat-Rigot A.S, et
al. Syndromes hypertensifs de la femme enceinte : physiologie,
définition et complications évolutives materno-foetales. La
Presse médicale 1999, 28(16) :880-885
2. Thiam M, Goumbala M, Gning S.B, et al.
Pronostic maternel et foetal de l'association HTA et grossesse en
Afrique
Sub-saharienne.
J.Gynecol-Obstet. et Biol. de la Reprod. 2003, 32(1) :
35-38
3. De Plaen J.F. Hypertension artérielle
et grossesse. Louvain Med, 2000, 119:S2-S5
4. Mounier-Vehier C. Guidelines for management
of arterial hypertension. J. Hypertension, 2007; 25:1105-87.
5. Report of the National High Blood Pressure Education Program
Working Group on high blood pressure in pregnancy. Am. J. Obst. Gynecol.
2000; 183:S1-S22.
6. Couture G., Milot A. Hypertension
artérielle et grossesse. In société
Québécoise d'hypertension artérielle. Guide
thérapeutique. 2ème édition Janvier 2002,
97-120.
7. CONFERENCE D'EXPERTS. Réanimation des
formes graves de pré-éclampsie (texte court).
Société française d'anesthésie
réanimation (SFAR). (c)Elsevier, Paris, 2000, 260 pages.
8. Edouard D. Pré-éclampsie,
éclampsie. Encycl. Méd. Chir. Anesthésie
Réanimation. Paris. Editions Scientifiques et Médicales Elsevier
2003 ; 36980 A10
9. Bronsens Jan J., Pijnenborg R., Bronsens Ivo A.
The myometrial junctional zone spiral arteries in normal en abnormal
pregnancies. Am. J. Obstetr. Gynecol. 2002; 187:1416-1423.
10. karamuchi S.A, Lam C. Mécanismes
impliqués dans la pré-éclampsie, progrès
récents. Actualités Néphrologiques. (c) Flammarion
Médecine Science.2004 : 167-176.
11. Roberts J-M. Pré-éclampsie :
entre connaissances et incertitudes. Actualités
Néphrologiques. (c) Flammarion, Médecine Sciences. 2002 :
73-88
12. Moignet C., diemunsch P., Pottecher T.
Principes de la réanimation des femmes atteintes de
pré-éclampsie sévère. Conférence
d'actualisation. (c) Elsevier 2003 : 387-406.
13. Maynard SE, Min J, Merchan J. et al.
Excessive placental soluble fms-like tyrosine kinase1 (sFlt-1), may contribute
to endothelial dysfunction, hypertension and proteinuria in preeclampsia.
J. Clin. Invest. 2003; 111: 649-658.
14. Levine R-J., Lam C., Qian C. et al. Soluble
endogline and other circulating antiangiogenic factors in preeclampsia. N.
Eng. J. Med. 2006; 355:992-1005.
15. Hladunewich M. nouveaux aspects dans la
pré-éclampsie: mise au point sur une patiente enceinte ayant une
maladie rénale chronique. Néphrologie "Conférences
Scientifiques". Mars 2007, Volume 8, N°3.
16. Levine RJ, Maynard SE, Qian C, et al.
Circulating angiogenic factors and the risk of preeclampsia. N. Eng. J.
Med. 2004; 350: 672-683.
17. Weinstein L. Syndrome of hemolysis,
elevated liver enzyme and low platelet count: a severe consequence of
hypertension in pregnancy. Am. J. Obstetr. Gynecol., 1982, 142 : 159-
167.
18. Conférence Nationale des professeurs des
Universités. Les principales complications de la grossesse:
HTA. J. Gynecol. Obstétr. Biol. Reprod. (c)Masson, Paris, 2002 ;
31:3S28- 3S32.
19. Sentilhes L., Gillard P. Biquard F., Deschamps
P. Hypertension et grossesse. In Obstétrique pour le
praticien. 5ème Edition, (c) Masson, Paris 2008:
161-171.
20. Pourrat O. Pré-éclampsie et
éclampsie : progrès thérapeutiques. Actualités
néphrologiques. (c) Flammarion Médecine Sciences 2004 :
177-189.
21. Xu Xiong, Damon Mayes, Nestor Demianczuk et
al. Impact of pregnancy induced hypertension on foetal growth. Am.
J. Obstet. Gynecol 1999; 180:207-213.
22. Bah A.O., Diallo M.H., Diallo A.A.S., Keïta N.,
Diallo M.S. Hypertension artérielle et grossesse : aspects
épidémiologiques et facteurs de risques. Médecine
d'Afrique Noire : 2000, 47(10) :422-425.
23. Touré I.A., Brah F., Prual A.
Hypertension artérielle et grossesse au Niger : Etude cas
/témoins à propos de 70 cas. Médecine d'Afrique Noire
: 1997, 44 (4) :205-208.
24. Attolou V., Takpara I., Akvavit J. et all.
Les différents types d'hypertension artérielle chez les femmes
enceintes Béninoises admises au CNHU de Cotonou. Cahiers
d'études et de recherches francophones/ Santé. Octobre- Novembre
1998 : 8 (5) : 353-356.
25. Sindayirwanya J.B, Ninteretse G, Rufyikiri TH,
Molard D, Mention J.E. Maladies hypertensives et grossesse. A propos
de 25 cas, Rev. Méd. De Bujumbura 1988, 4, 36.
26. Nakintije M-R. Etude prospective de l'HTA
gravidique au C.H.U de Kamenge (à propos de 56 cas), Thèse de
Doctorat en Médecine 1991, Bujumbura, 108 pages.
27. Sibai BM. Chronic hypertension in
pregnancy. Obstetric & Gynecol 2002; 100(2): 369- 377.
28. Hauth JC, Ewell MG, Levine RL, Esterlitz JR, Sibai
BM, Curet LB. Pregnancy outcomes in health nulliparas women who
subsequently developed hypertension. Obstetric & Gynecol 2000;
95(1):24-28
29. Roberta B. Ness, Nina Markovic, Debra Bass, Gail
Harger, James M. Roberts. Family history of hypertension, heart
disease, and stroke among women who develop hypertension in pregnancy.
Obstetric & Gynecol 2003; 102(6): 1366-1371.
30. Sibai BM. Diagnosis and management of
gestational hypertension and preeclampsia. Obstetr. & Gynecol. 2003;
102(1): 181-192.
31. Pambou O, Ekoundzola JR, Malanda JP, Buambo
S. Prise en charge et pronostic de l'éclampsie au CHU de
Brazzaville. A propos d'une étude prospective de 100 cas.
Médecine d'Afrique noire : 1999, 46(11) : 508-512.
32. Brown MA, Lindheimer MD, De Swiet M, Van Assche A,
Moutquin JM. The classification and diagnosis of the hypertensive
disorders of pregnancy: a statement from the international society for the
study of hypertension in pregnancy [ISSHP]. Hypertens pregnancy
2001; 20: 9-14.
33. HTA et grossesse in "Lansac J, Berger C, Magnin G.
Obstétrique pour le praticien". 4ème édition, (c)Masson,
Paris 2003 : 149-159.
34. Ellart D, Guévart E, Forzy G. et
coll. Le Hellp syndrome. A propos d'une série de 9 observations
sans coagulation intra-vasculaire disséminée. Rev. Fr.
Gynécol. Obstetric. 1990, 85, 4: 220-226.
35. Kuhn W, Rath W, Loos W, Graeff H. Le
syndrome Hellp. Résultats cliniques et d'analyses en laboratoire.
Rev. Fr. Gynécol. Obstét.1992, 87,6 : 323-328.
36. Bukuru H. Contribution à
l'étude de l'éclampsie au CHUK ; Etude rétrospective
à propos de 30 cas, Thèse de doctorat en Médecine,
1998, Bujumbura.
37. Magee LA, Ornstein MP, Von Daderlszen P.
Fortnightly review: Management of hypertension in pregnancy. BMJ
1999; 318: 1332-1336.
38. Amorim MMR, Santas LC, Faundes A.
Corticosteroid therapy for prevention of respiratory distress syndrome in
severe preeclampsia. Am. J. Obstetric. & Gynaecology. 1999; 180:
1283-1288
39. The Magpie trial collaborative group. Do
women with pre-eclampsia, and their babies, benefit from magnesium sulphate?
The Magpie trial: a randomised placebo-controlled trial. Lancet 2002;
359: 1877-1890.
4O. Caughey AB, Stotland NE, Escobar GJ. What is
the best measure of maternal complications of term pregnancy? Ongoing
pregnancies or pregnancies delivered. Am. J. Obstetric. Gynaecology. 2003;
189: 1047-1052.
41. Gansevoort W, Rep A, De Vries JIP, Bonsel GJ, Wolf
H. prediction of maternal complications and adverse infant outcome at
admission for temporizing management of early-onset severe hypertensive
disorders of pregnancy. Am. J. Obstetrics & Gynaecology. 2006; 195:
495-503.
42. Bombrys AE, Barton JR, Nowacki EA et al.
Expectant management of severe preeclampsia at less than 27 weeks' gestation:
maternal and perinatal outcomes according to gestational age by week at onset
of expectant management. Am. J. Obstetric & Gynaecology. 2008, 199:
e247-e6.
43. Bah A.O, Diallo M.H, Condé A.M, Keita N.
Hypertension artérielle et grossesse : mortalité
maternelle et périnatale. Médecine d'Afrique Noire 2001, 48,
461-464.
44. Ducarme G, Heernberger S, Pharisien I, Carbillon L,
Uzan M. Eclampsie : étude rétrospective de 16
cas. Gynécol.
Obstétr. et Fertilité 2009, 37 : 11-17
|
|



