3-Les types de nitrification
Deux types de nitrification doivent être
distingués:


La nitrification Autotrophe :
caractérisée par l'utilisation de substrats inorganiques
comme source d'énergie (donneurs d'électrons) pour
la croissance et comme source
d'azote, le dioxyde de carbone comme source de carbone et
l'oxygène comme
accepteur final d'électrons (Bock et al.,
1989).
La nitrification hétérotrophe :
les micro-organismes nitrifiants hétérotrophes utilisent le
carbone organique comme source d'énergie et oxydent des composés
azotés organiques ou inorganiques à une vitesse beaucoup plus
faible que celle observée chez les autotrophes. Certains
micro-organismes peuvent utiliser deux accepteurs d'électrons,
l'oxygène et le nitrate, et atteignent, alors une croissance plus rapide
qu'en utilisant l'oxygène seul. (Kester et al.,
1997).



4- Type de micro-organismes
Deux groupes des bactéries sont spécialisées
dans la fonction de la nitrification :


Un groupe oxyde l'ammonium en nitrite: ce sont les
bactéries nitritantes (ou
nitrosantes, ou nitreuses, ou ammonio-oxydantes), dont les noms
de genre portent
le préfixe nitroso (
Nitrosomonas, ,
Nitrosococcus ,...), (Bock et
al., 1989).
Nitrosospira
Un groupe oxyde le nitrite en nitrate : ce sont les
bactéries nitratantes (ou nitriques,
ou nitrite- oxydantes), dont les noms de genre portent le
préfixe nitro(
Nitrobacter, Nitrococcus ,
Nitrospira...),(Watson et al.,
1989).
Cependant, de nombreux genres et espèces de
bactéries nitrifiantes ont été identifiés.
Elles peuvent soit oxyder l'ammonium en nitrite (nitritation),
soit oxyder le nitrite en nitrate
(nitratation). Il n'y a pas d'organisme connu qui puisse
directement oxyder l'ammonium en
nitrate. Dans les sols, la nitritation est
généralement attribuée à Nitrosomonas
europaea et la
nitratation à Nitrobacter agilis.
5-Facteurs du milieu influencant la croissance et
l'activité des bactéries Nitrifiantes
D'une manière générale, la croissance des
bactéries nitrifiantes est contrôlée par un
certain nombre de paramètres : disponibilité du
substrat, température, oxygène dissous,
pH, pour lesquels il existe une limite de tolérance et un
optimum. Une cinétique de
nitrification réalisée dans des conditions
favorables aux micro-organismes nitrifiants est
schématisée sur la Figure suivante.
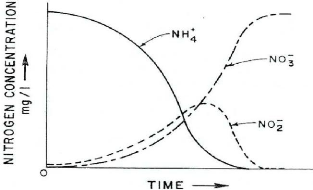



Figure 2 : Schématisation des transformation
de l'azote durant la nitrification en absence d'inhibiteur
(Anthonisen et al
., 1976)
fi. ~~mperature
La gamme des températures favorables à la
nitrification est très large. La limite inférieure
serait 5°C (Jones and Hood, 1980), alors
que la limite supérieure se situerait entre 40°C et 45°C
(Henze et al., 1997) . Dans cette large gamme,
les micro-organismes nitrifiants présentent une
température optimale qui se situe entre 25 et 36°C.
Les constantes de croissance (umax et KS)
dépendent fortement de la température. Les deux
espèces nitrifiantes sont influencées par
la température : la vitesse maximale de croissance et
l'affinité augmentent avec la
température (figure 3).
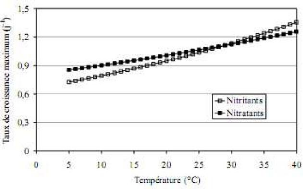
Figure 3 : Evolution des taux de croissance maximum
en fonction de la température (Knowles 1965)



Cependant, à forte température (supérieure
à 30°C), la vitesse maximale de croissance
de Nitrosomonas devienne supérieure à celle de
Nitrobacter, alors que l'inverse est observé à
moins de 30°C.
B. Le pgf
L'activité des microorganismes nitrifiants est
très sensible au pH. Dans la nature, ces bactéries peuvent
croître dans une large plage de pH. Cependant, leurs
croissances et leurs activités optimales se situent aux environs d'un pH
compris entre 7.5 et 8.5 (Josserand, 1983; Bock et al., 1989).
La vitesse de nitrification diminue avec la diminution du pH. D'après
Anthonisen et al., 1976, le pH agit via l'ammoniac (NH3) et
l'acide nitreux (HNO2) toxiques pour les micro-organismes nitrifiants et dont
les concentrations sous forme libre sont dépendantes du pH.
Ainsi à un pH élevé, la teneur en NH3 est
relativement importante du fait du déplacement
de l'équilibre NH3 par NH4+, inversement à pH
faible, c'est la teneur en HNO2 qui est forte du fait
du déplacement de l'équilibre NO2- par
HNO2. Anthonisen et al., 1976.
C. Teneur en oxyane dissous
L'oxygène dissous est utilisé comme accepteur final
d'électrons par les bactéries
nitrifiantes pour réaliser les réactions de la
nitrification. De ce fait, une carence en oxygène
dissous peut induire un ralentissement et même un
arrêt de la réaction.
Plusieurs auteurs (Henze et al., 1997), ont
établi que le taux de nitrification se maintient
à 100% pour des concentrations en oxygène dissous
supérieures ou égales à 3 mg O2.L-1. Le
Tableau suivant présente différentes valeurs des
constantes d'affinité pour l'oxygène
données dans la littérature pour chacune des deux
populations Nitritantes et Nitratantes.



Tableau 1 : Différentes valeurs de KO2
publiée dans la littérature
|
Constantes d'affinité pour l'oxygène K02 ( mg
021-1)
|
Auteurs
|
|
Nitritantes
|
0,25 - 0,3
|
Loveless (1968)
|
|
0,25 - 0,3
|
Peeters et al., (1969)
|
|
0,5 a 30°C
|
Bal melle et al (1991)
|
|
0,5 - 1
|
Henze et al (1997)
|
|
Nitratantes
|
0,3 - 0,7
|
Stenstro m (1980)
|
|
0,8 - 2,5
|
Peeters et al., (1969)
|
|
1 A 30°C
|
Bal melle et al (1991)
|
|
1 a 30°C
|
Henze et al (1997)
|
Les bactéries nitratantes sont donc plus sensibles aux
faibles concentrations en
oxygène dissous, que les bactéries nitritantes.
Cette tendance est confirmée par les
travaux d'Hanaki et al., 1990 qui ont
observé une accumulation de nitrites et une
augmentation du taux de croissance des nitritantes pour des
concentrations en oxygène
dissous d'environ 0,5 mg O2.L-1. Dans ces
conditions, la vitesse d'oxydation du nitrite décroît
plus rapidement que celle de l'ammonium.
Par ailleurs, autres chercheurs (Zhao et al.,
2006) ont montré qu'à faible concentration
en oxygène il peut y avoir une dérive
métabolique plus importante vers la production de
protoxyde d'azote (N2O), qui est un gaz totalement
indésirable (gaz à effet de serre donc
indésirable compte-tenu du réchauffement
atmosphérique).
0- Composes Toxiques
La nitrification est inhibée par une large
variété de composés. On peut citer notamment
les métaux lourds (comme le cuivre, le nickel, le
cobalt, le zinc et le chrome), les amines, les
phénols, les composés sulfurés,
chlorés et les composés cycliques azotés. Cependant, tous
ces
composés ne sont pas inhibiteurs aux mêmes
concentrations et il faut noter que les micro-
organismes nitrifiants possèdent une forte capacité
d'adaptation (Martin, 1979).




| 


