2.1 Revue de la littérature
Notre revue de la littérature s'articulera autour des
points suivants: la définition de quelques concepts et les
généralités sur la schistosomiase.
2.1.1 Définition des concepts
a )Surveillance
épidémiologique:
Selon A.D Langmuir c'est un processus de collecte, de
compilation et d'analyse des données, ainsi que leur diffusion à
l'ensemble de ceux qui ont besoin d'être informés. Cette
définition appelle trois commentaires:
- La surveillance épidémiologique est un
processus continu et systématique; elle
peut être opposée aux enquêtes, plus
ponctuelles.
- La rapidité du traitement de l'information et de la
diffusion des résultats est
indispensable au bon fonctionnement d'un système de
surveillance épidémiologique moderne.
- La finalité du système de surveillance est de
fournir des informations servant
plus au moins directement à la prise de mesures de
prévention ou de contrôle d'un problème de santé
publique.
Pour le Docteur JEAN Kostrzewski,
épidémiologiste Polonais, "la surveillance, c'est de
l'information appelant l'action". [2]
b) Proportion:
C'est un rapport dont le numérateur fait
partie du dénominateur. Tous deux étant mesurés
simultanément. Une proportion est de la forme: [2]
x
* 100
x + y
c) Incidence:
C'est un indicateur dynamique de morbidité. C'est un
taux qui prend en compte la vitesse de survenue de la maladie dans une
population. Au numérateur de l'incidence figurent le nombre de
nouveaux cas d'une maladie apparus pendant une période
de temps donné. Selon la période de temps
considérée, on distingue plusieurs façons de calculer
l'incidence.
· Incidence cumulée
L'incidence cumulée est le rapport du nombre de
nouveaux cas d'une maladie survenue pendant une période de temps
déterminée divisée par la population à risque de
développer la maladie pendant cette période. Certains utilisent
simplement le terme d'incidence pour l'incidence cumulée.
- L'incidence cumulée s'exprime sous forme d'un chiffre
compris entre 0 et 1ou
Pourcentage : x cas pour cent (ou pour 1000, 10000, etc.)
personnes pendant la période.
- La période d'étude est en
général une période de temps systématique. Le
choix
de la période dépend de la dynamique
générale de la maladie. On calcule des incidences cumulées
annuelles, mensuelles, hebdomadaires, ou même journalières dans
certains cas.
- L'incidence cumulée de la maladie, est
calculée sur une population. Elle est
équivalente au risque moyen de contracter la maladie
pendant la période étudiée pour un individu quelconque de
cette population.
L'incidence cumulée est le taux d'attaque en
période d'épidémie.
· Taux d'incidence ou densité
d'incidence
Lorsque la population est très instable (nombreuses
arrivées et départs) ou lorsqu'il existe de nombreux perdus de
vue pendant la période d'étude, le dénominateur
utilisé pour l'incidence cumulé est impropre. Il est
nécessaire de tenir compte des variations intermédiaires de ce
dénominateur. On utilise alors le concept de personnes - temps. On
divise la période d'étude en sous périodes pour lesquelles
on dispose de données démographiques sur la population
suivie.[5]
d) Fréquence
C'est le nombre de fois qu'un phénomène a
été ou est observable pendant une unité de temps. Un
phénomène est périodique si les caractéristiques
observées se reproduisent à l'identique pendant des durées
égales consécutives.[21]
2.1.2 Généralités sur la
schistosomiase
2.1.2.1 Historique[9]
Des oeufs de Schistosoma haematobium ont
été retrouvés dans une momie
égyptienne de la 20è dynastie (plus
de 1000 ans avant JESUS - Christ).
En 1851, THEODOR BILHARZ découvre le parasite à
l'école de médecine du CAIRE, fait part à SIEBOLD en
Allemagne de la découverte de Distoma haematobia dans les veines
mésentériques d'un malade de la région du Caire. Quelque
temps après, il démontre que ces vers dont les oeufs
possèdent un éperon terminal sont à l'origine de
l'hématurie d'un paysan. Par ailleurs, il considère que les oeufs
à éperon latéral mis en évidence dans les selles de
malade sont issus d'une autre forme de même parasite nommé plus
tard Bilharzia heamatobia par COBBOLD en 1859. A la même époque,
HARLEY et COBBOLD émettent l'hypothèse qu'un mollusque est
l'hôte intermédiaire et que la peau en est la porte
d'entrée.
LOOS conteste la phase de développement malacologique.
En 1893 MANSON pense qu'il existe deux espèces de schistosome :
· L'une dont les oeufs sont à éperon
latéral
· L'autre dont les oeufs sont à éperon
terminal.
En 1902 il repose la même hypothèse. En 1907,
SABON pense comme MANSON qu'il existe deux espèces et désigne la
deuxième sous le nom de Schistosoma mansoni. Cette thèse est une
fois de plus contestée par LOOS, car selon lui, les oeufs à
éperon latéral ne sont que des oeufs pathologiques de
Schistosoma haematobium.
Il faudra attendre les travaux de TURNER et NAYSALAND pour
confirmer les conclusions de SAMBON. Ils trouvent que les femelles porteuses
d'oeufs à éperon latéral sont exclusivement situées
dans le canal juguécophore comme chez Schistosoma
haematobium.
Les travaux de LEIPER entre 1915 et 1918 donneront la preuve
définitive de l'existence de ces deux espèces. Cet auteur montre
:
· Que les deux espèces sont morphologiquement
distinctes
· Que l'infection se fait par voie transcutanée
· Enfin, que chaque espèce évolue chez un
hôte intermédiaire.
Les travaux les plus nombreux sont ceux qui ont
été conduits en Egypte, en Extrême Orient et en
Amérique Centrale et principalement au Mexique. Ceux menés en
Afrique de l'Ouest sont bien moins nombreux.
2.1.2.2 Définition
Selon le professeur Pierre Aubry, les schistosomiases sont des
maladies parasitaires dues à des vers plats (schistosomes ou
bilharzies). La transmission est essentiellement urinaire ou fécale,
faisant intervenir des hôtes intermédiaires qui sont des
mollusques d'eau douce. La symptomatologie de ces pathologies est le reflet des
lésions provoquées par la migration ou l'embolisation des oeufs.
Elles sont en extension directement liées au développement
agricole et à l'augmentation des réseaux d'irrigation.
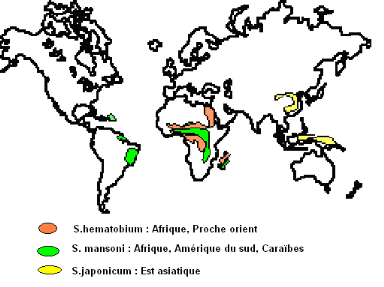
Carte N° 1 : Répartition
géographique de la schistosomiase au niveau mondial (zones hyper
endémiques) [22]
2.1.2.3 Epidémiologie
a) Agents pathogènes :
Schistosomes ou Bilharzies
Le professeur Pierre Aubry soutient qu'il existe trois groupes
:
· Le groupe mansoni qui comprend : Schistosoma
mansoni, agent de la
bilharziose intestinale;
· Le groupe haematobium composé de :
Schistosoma haematobium, agent de la
schistosomiase urinaire et schistosoma intercalatum,
agent de la bilharziose rectosigmoïdienne;
· Le groupe japonicum regroupe : Schistosoma
japonicum, agent de la bilharziose
artério-veineuse et Schistosoma mekongi.
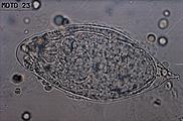
Image N° 1 : Oeuf de Schistosome
haematobium [22]
On le distingue de celui du Schistosoma mansoni par son
éperon terminal (et non latéral).
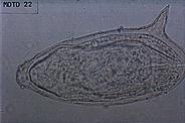
Image N° 2 : Oeuf de Schistosome
mansoni [22]
On le reconnaît par sa localisation (selles) et son
éperon latéral. Les autres schistosomes intestinaux (intercalatum
et japonicum) ont par contre un éperon terminal comme le
S.hæmatobium
Selon l'OMS, sur les dix-neuf espèces
de schistosome actuellement connues , cinq sont principalement des parasites de
l'homme, à savoir Schistosoma mansoni, Schistosoma haematobium,
Schistosoma intercalatum, Schistosoma japonicum et
Schistosoma mekongi. D'autres espèces ne parasitent l'homme que
de façon occasionnelle. Les 19 espèces identifiées peuvent
être subdivisées en quatre groupes, ceux de S.
haematobium, de S. mansoni, de S. indicum et de S.
japonicum. [6]
b) Cycle parasitaire
Il y a deux phases de multiplication des parasites.
[6]
· La phase sexuée chez l'hôte
définitif : l'homme parasité
Après avoir pénétré par voie
transcutanée, les furcocercaires migrent par voie circulatoire, gagnent
le territoire mésentérique inférieur et deviennent des
adultes (mâles et femelles). Les femelles pondent des oeufs (des milliers
d'oeufs par jour) dans les veinules des organes profonds, les oeufs migrent
à travers la paroi d'un organe creux (vessie, intestin) pour être
éliminés avec les excréta.
Certains oeufs sont bloqués et ne peuvent pas
être expulsés : cette migration inachevée entraîne la
bilharziose urinaire et ou intestinale.
Les oeufs peuvent migrer à contre courant et rester
séquestrés dans les différents viscères dont le
foie. Cette migration aberrante rend compte de la bilharziose hépatique.
· La phase asexuée chez l'hôte
intermédiaire : les mollusques d'eau douce.
Les oeufs éliminés ne peuvent poursuivre leur
évolution que dans l'eau douce. Ils libèrent les embryons ou
miracidiums qui pénètrent les mollusques, hôtes
intermédiaires. Les miracidiums survivent dix-huit heures dans l'eau
douce. Trois semaines à deux mois après la
pénétration des miracidiums, les larves quittent les mollusques,
nagent à la surface des eaux à la recherche des hôtes
définitifs (hommes ou animaux) qu'elles pénètrent par voie
transcutanée.
c) Réservoir de virus
Schistosoma haematobium est un parasite strictement
humain. Les autres espèces sont des zoonoses. Schistosoma
mansoni a été retrouvé chez les mammifères que
sont les primates les bétails et les rongeurs. En pratique, l'homme est
le réservoir de virus essentiel.
d) Hôtes intermédiaires
Les hôtes intermédiaires des Schistosomes sont
des gastéropodes d'eau douce, aquatiques ou amphibies. Les
espèces aquatiques du genre Bulinus transmettent
Schistosoma haematobium et celles du genre Biomphalaria,
Schistosoma mansoni; les espèces amphibiennes du genre
Oncomelania transmettent les Schistosomes du groupe S.
japonicum, tandis que les gastéropodes du genre Neotricula
(famille des hydrobiidés) transmettent S.mekongi.
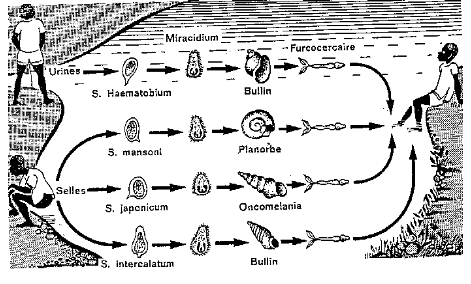 Image N°3 : Schéma du cycle évolutif
de la schistosomiase [22] Image N°3 : Schéma du cycle évolutif
de la schistosomiase [22]
2.1.2.4 Clinique[6]
L'étude clinique concernera Schistosoma haematobium
et schistosoma mansoni. Trois phases correspondent aux
différents stades évolutifs des parasites chez l'homme.
a) Phase initiale de contamination ou d'infection
cercarienne
Elle est essentiellement cutanée,
caractérisée par un prurit, une réaction urticarienne
localisée. Cette réaction est le plus souvent inapparente pour
S. haematobium ou fugace (un à deux jours) pour
S. mansoni.
b) Phase d'invasion ou de dissémination
larvaire
Après une période muette de deux à dix
semaines suivant la contamination surviennent des manifestations
immuno-allergiques :
· Fièvre (supérieure à 38°C)
· Signes cutanés à type de prurit,
urticaire, oedèmes.
· Douleurs (myalgies, arthralgies)
· Toux, parfois dyspnée asthmatiforme
· Douleurs abdominales, diarrhée
· Céphalées.
c) Phase d'état ou de focalisation
viscérale
Elle survient plusieurs mois après le bain infectant,
les signes cliniques sont en rapport avec le schistosome en cause.
· Bilharziose urinaire ( S.
haematobium )
Elle se manifeste par :
ü Une hématurie d'origine vésicale :
terminale, capricieuse, spontanée, répétée,
indolore.
ü Une dysurie
ü Une infection urinaire
ü Une crise de colique néphrétique
· Bilharziose intestinale (S.
mansoni)
Elle se traduit par des douleurs abdominales et un
syndrome diarrhéique ou dysentérique avec parfois
rectorragies.
d) Techniques de diagnostic
A des fins de santé publique, le diagnostic doit faire
appel à une technique simple, n'exigeant aucune manipulation
délicate et praticable avec des fournitures et du matériel
faciles à se procurer.[7] Le diagnostic de la
schistosomiase peut se faire par des techniques immunologiques
(détection d'anti-corps), des techniques parasitologiques :
· Recherche d'oeufs dans les urines par filtration pour
la bilharziose urinaire
· Recherche d'oeufs dans les selles pour la bilharziose
intestinale.
Des techniques indirectes, à savoir l'observation d'une
hématurie macroscopique est une technique simple et fiable pour affirmer
une infestation à Schistosoma haematobium. Il y a
également la mise en évidence d'une hématurie
microscopique, au moyen de bandelettes réactives.
e) Le traitement
Les médicaments recommandés par l'OMS
dans le cadre du traitement de la bilharziose sont au nombre de
trois : le praziquantel, l'oxaminiquine et le métrifonate. Le
praziquantel est efficace contre toutes les formes de schistosomiase et ne
présente que peu d'effets secondaires passagers. C'est le
médicament retenu dans le cadre de la lutte contre la schistosomiase par
le PNLSc.
f) Les complications
Des complications surviennent au stade tardif de la maladie
après plusieurs années d'évolution. Elles concernent
principalement :
· La vessie : cystites, surinfections
bactériennes, risque de cancérisation mais sans
métastase.
· L'uretère : calcifications,
surinfections
· Les organes génitaux :
hémospermie, épididymite, éjaculation douloureuse chez
l'homme ; ulcérations du col utérin et du vagin,
métrorragies, avortements, stérilité.
· Le foie : hépatomégalie,
hypertension portale.
Une étude réalisée en milieu hospitalier
à Kara en république du Togo a révélé 11.35%
de complications liées à la schistosomiase chez les
hospitalisés. Ces complications sont essentiellement :
l'anémie, l'ictère, l'encéphalite, l'hypertension portale,
des crises convulsives et le syndrome néphrotique. [18]
g) La prophylaxie
· Générale se traduit
par :
ü la lutte antimollusque, hôte intermédiaire
de la schistosomiase.
ü Le dépistage et le traitement des populations
atteintes en zones d'endémie.
ü La lutte contre le péril fécal
ü L'éducation sanitaire
· Individuelle : éviter les
bains en eau douce en région d'endémie.
2.1.3 La schistosomiase au Burkina Faso
2.1.3.1 Situation épidémiologique
Les premiers travaux sur la schistosomiase ont
été entrepris dans les régions de Ouagadougou et de
Bobo-Dioulasso dans les années 1955 à 1960. A partir de 1960, les
équipes de l'OCCGE, du Ministère de la santé, de
l'université de Ouagadougou, du Centre National de la recherche
Scientifique et Technique, de l'Ecole Inter-Etats des Ingénieurs de
l'Equipement Rural ont mené des travaux souvent en rapport avec les
aménagements hydrauliques.
Une revue de la littérature réalisée par
PODA et collaborateurs (1997) permet de noter les
prévalences de la schistosomiase selon les trois zones climatiques du
pays: [15]
a) Zone sahélienne,
située au nord du 14eme parallèle avec une
pluviométrie inférieure à 650 mm couvre la région
de Dori
· Bilharziose urinaire : 5 à 85%
· Bilharziose intestinale : 0%
b) Zone nord - soudanienne ou soudano -
sahélienne, située entre les parallèles 14°
et 11° 30 à pluviométrie comprise entre 650 mm et 1000
mm.
· Bilharziose urinaire : 5 à 85 %
· Bilharziose intestinale : 0 à 8%
c) Zone sud - soudanienne située au
sud du parallèle 11°30'.
· Bilharziose urinaire : 1 à 86 %
· Bilharziose intestinale : 0 à 79%
De cette étude PODA et collaborateurs
notent un certain nombre de points quant à la distribution de la
schistosomiase au Burkina Faso:
1. Une forte prévalence de la bilharziose urinaire
autour des mares du nord du
pays (B. truncatus étant le principal
hôte intermédiaire)
2. Une multiplicité des hôtes
intermédiaires dans la zone nord soudanienne avec
l'apparition de Biomphalaria pfeifferi, hôte
intermédiaire de la schistosomiase intestinale.
3. Un renforcement de la bilharziose urinaire dans la zone
nord soudanienne lié à
la multiplicité des mares temporaires avec B
senegalensis.
4. Une prédominance de Schistosoma mansoni
sur Schistosoma haematobium à
certains endroits de la zone sud - soudanienne due à
une présence très importante de B pfeifferi qui infeste
30% des mares de cette zone.
5. Un accroissement important des cultures de contre saison et
des cultures
irriguées qui pourraient favoriser l'augmentation de la
prévalence déjà constatée.
Tableau N° I: Situation de la
schistosomiase au Burkina Faso selon les zones climatiques et les
localités.
|
Zone climatique
|
Localité
|
S.hematobium
|
S. mansoni
|
Année de l'étude
|
|
Prévalence
|
Méthode
|
Prévalence
|
Méthode
|
|
|
Sahélienne
|
Dori
Arbinba
Sebba
|
80%
93%
58%
|
Centrifu-
gation
|
-
|
-
|
1952
|
|
Dori
Gorom
Djibo
Markoye
Tassamakat
|
57%
84%
90%
95%
100%
|
Filtra-
tion
|
-
|
-
|
1979
|
|
Bogandé
Mani
Thion
|
62%
82%
100%
|
Filtra-
tion
|
-
|
-
|
1980
|
|
Yatenga
|
43.5%
|
Filtra-
tion
|
-
|
-
|
1985
|
|
Bam
|
34.3%
|
Filtra-
tion
|
-
|
-
|
1985
|
|
Naoka
Damesma
Louda
|
32.75%
13.5%
10%
|
Filtra-
tion
|
-
|
-
|
1983
|
|
Sahélo- soudanienne
|
Ouagadougou
|
9.5- 36.5%
|
Filtra-
tion
|
-
|
-
|
|
|
Kombissiri
|
1978
|
|
Daguilma
Ziniaré
Tanguiga
|
85%
9.5-36.6%
55.4
|
Filtra-
tion
|
-
|
-
|
1990
1978
1990
|
|
Bagré
|
35%
36.7
|
Filtra-
tion
|
-
|
-
|
1978
1992
|
|
Dédougou
Tougan
Souma
|
51%
7%
29%
|
Centrifu-
gation
|
-
|
-
|
1960
|
|
Vallée du Sourou
|
19%
32%
52.9%
|
Filtra-
tion
|
3 cas
3.22%
|
Kato-Katz
|
1980
1980
1999
|
|
Fada
Mahadaga
Namounou
Tambaga
Diapaga
|
52%
98%
52%
34%
70%
|
Filtra-
tion
|
0.6%
|
Kato-Katz
|
1973
1973
1973
1973
1981
|
|
yayo
|
55.3%
|
Filtra-
tion
|
69.3%
|
Richtie
|
1999
|
|
Soudanienne
|
Yaran
|
80%
68%
|
Filtra-
tion
|
40%
0.94%
|
Kato-katz
|
1974
1999
|
|
Bobo- Dioulasso
|
1 à 98%
|
Filtra-
tion
|
1 à 51%
|
Kato-katz
|
1977
|
|
Dafiguisso
Dafinso
|
-
|
|
64.4%
44.7%
|
Kato-katz
|
1982
|
|
Kampti
|
70%
|
Filtra-
tion
|
19%
|
Kato-katz
|
1974
|
Source: Programme national de schistosomiase 2003
Une enquête réalisée en 1984 par les
chercheurs du département "Santé et Développement" de
l'université de Bordeaux II, du CEGET - CNRST (France) et du CNRST
(Burkina Faso) montre que dans la région de Kongoussi il semble exister
un gradient d'infestation dont l'intensité croit en fonction de
l'éloignement du lac Bam. Il apparaît aussi que l'infestation se
diffuse d'autant plus vite au sein de la population que celle-ci n'a pas de
puits pérennes à margelle à sa disposition. D'une
façon générale, les éleveurs sont plus
touchés que les cultivateurs.[10]
Une étude réalisée dans deux villages de
la province de l'Oubritenga en 1987 a estimé la prévalence de la
bilharziose urinaire à 55.4% à Tanguiga et 85% à
Dalguilma, chez les enfants de cinq à dix-sept ans.
[8]
En 1962, Mac Mullen et Francotte estimaient q'au Burkina Faso,
1.5 millions de personnes auraient contracté la bilharziose.
[20]
De la synthèse des études déjà
réalisées, on note qu'au Burkina Faso il existe deux formes de
schistosomiase : la bilharziose urinaire à Schistosoma
hematobium et la bilharziose intestinale due à Schistosoma
mansoni.
2.1.3.2 Le Programme National de Lutte contre la
Schistosomiase
Afin de mieux combattre la bilharziose, les autorités
sanitaires du Burkina Faso ont mis sur place un Programme National de Lutte,
dont la mise en oeuvre proprement dite est intervenue courant 2004.
a) Objectif général du
Programme
Réduire de façon significative la
morbidité due aux schistosomoses dans l'ensemble du pays ainsi que leurs
conséquences socio-économiques, en particulier chez les enfants
de moins de 15 ans.
Cet objectif visera aussi à réduire le
développement des complications additionnelles de la morbidité
chez les adultes.
b) Objectifs spécifiques
· Réaliser une cartographie nationale des
bilharzioses urinaire et intestinale d'ici
début 2004 en utilisant les données du
système de santé et celles des organismes de recherche.
· Amener 80% des structures sanitaires de base à
améliorer leurs capacités de
dépistage et de traitement de la bilharziose urinaire
et intestinale en quatre ans.
· Augmenter les taux de prise en charge de la bilharziose
urinaire et intestinale
d'au moins 75% en quatre ans.
· Améliorer à moyen terme les
connaissances, attitudes et pratiques des
populations envers la schistosomiase.
· Réduire la transmission de la schistosomiase au
bout des quatre années du
projet.
· Développer l'aptitude des responsables des
formations sanitaires à la gestion
Autonome.
· Développer le réseau d'information et
d'échanges en utilisant les techniques
modernes de télécommunication (Internet).
c) Stratégies du Programme
Pour atteindre ses objectifs, le PNLSc a inscrit au nombre de
ses stratégies:
· L'évaluation du degré
d'endémicité au niveau d'une zone.
· Le traitement et le choix de la distribution
communautaire du praziquantel.
· L'éducation pour la santé.
· Les stratégies complémentaires
composées essentiellement de l'assainissement
du milieu et de la promotion de l'approvisionnement en eau
potable.
· La supervision et l'évaluation.
· L'intégration du programme dans les
activités de routine des services de santé
et garantie de durabilité.
2.1.4 Les directives relatives à la
schistosomiase. [4]
Selon le guide technique de la surveillance
intégrée de la maladie et la riposte au Burkina Faso, les
directives relatives à la schistosomiase se présentent comme
suit:
2.1.4.1 Présentation
Infection parasitaire très répandue dans le
monde surtout dans les zones tropicales, la bilharziose ou schistosomose ou
encore schistosomiase constitue aujourd'hui la deuxième affection
liée à l'eau après le paludisme de par leur ampleur. C'est
une maladie chronique insidieuse, peu reconnue à ses stades
précoces qui touche les systèmes urinaire et
hépato-digestif. Ses répercussions sanitaires et
socio-économiques sont importantes car touchant les hommes et les femmes
pendant leurs années les plus productives. Elles exposent à une
morbidité grave qu'induisent les oeufs des vers adultes qui restent
séquestrés dans les tissus de leurs hôtes. Les
complications de la bilharziose constituent toute la gravité de cette
affection. Parmi ces complications, on peut noter le cancer de la vessie.
Au Burkina Faso la morbidité de la schistosomiase est
voilée par d'autres problèmes de santé. La multiplication
des aménagements hydroagricoles constitue un facteur de risque. Le
Burkina Faso a mis en place de nouvelles stratégies de lutte contre
cette affection à travers la création d'un programme.
2.1.4.2. But de la surveillance
a) Détecter et répondre aux flambées
épidémiques
b) Identifier les zones à haut risque
2.1.4.3 Définition de cas
recommandée
a) Cas suspects
Bilharziose urinaire: Tout
individu présentant une hématurie macroscopique, en tenant compte
de la prévalence de la schistosomiase dans la zone. En absence
d'hématurie macroscopique, tout individu se plaignant de signes
urinaires (dysurie, brûlure mictionnelle, douleurs sus-pubiennes) chez
qui la recherche d'une hématurie microscopique avec des bandelettes
Hématix ®est positive
Bilharziose intestinale : Tout individu
présentant des symptômes intestinaux chronique ou
récurrents (sang dans les selles, diarrhée sanglante,
diarrhée, douleurs abdominales) ou à un stade ultérieur,
une hépatosplénomégalie.
b) Cas confirmés
Bilharziose urinaire: cas suspect avec
présence d'oeuf de Schistosoma haematobium dans le culot
urinaire
Bilharziose intestinale : cas suspect avec
présence des oeufs de schistosoma mansoni ou schistosoma Japonicum,
schistosoma mekongi, schistosoma intercalatum dans les selles.
2.1.4.4 Répondre à une flambée
suspecte
S'il y a augmentation du nombre au cours d'une période
donnée:
· Notifier les cas au niveau supérieur
· Mener des investigations pour identifier les risques de
transmission
· Prendre en charge le cas, conformément aux
directives en vigueur du programme.
2.1.4.5 Répondre à une flambée
confirmée
S'il y a augmentation de cas confirmé par le
laboratoire
· Continuer la prise en charge de tous les cas selon la
directive du programme.
· Organiser des séances d'IEC à l'endroit
de la population.
· Améliorer l'assainissement du milieu.
· Promouvoir la construction et l'utilisation des
latrines.
· Promouvoir l'utilisation d'eau potable.
2.1.4.6 Analyser et interpréter les
données
a) Temps : tracer périodiquement un
graphique de cas
b) Lieu : Faire la cartographie des cas
c) Personne: Faire le décompte
périodique des cas selon l'âge, le sexe, la profession.
2.2 Cadre conceptuel
L'étude vise la description de la situation de la
bilharziose dans le district sanitaire de Tougan sur une période de cinq
ans, à savoir de 1999 à 2003. Elle s'inscrit autour des concepts
suivants:
2.2.1 La distribution de la maladie
a) Selon le sexe :
a) Par tranches d'âges
b) Selon le type de bilharziose
c) Par formation sanitaire
2.2.2 Evolution temporo-spatiale de la
maladie
a) Incidence de la maladie par formation sanitaire et par an
de 1999 à 2003 dans le district.
b) Incidence de la maladie par zone et par an de 1999 à
2003.
SCHEMA DU CADRE CONCEPTUEL
EVOLUTION TEMPORO-SPATIALE DE
LA MALADIE
· Incidence de la maladie par formation sanitaire et par an
de 1999 à 2003
· Incidence de la maladie par zone et par an de 1999
à 2003
DISTRIBUTION DE LA MALADIE
· Selon le sexe
· Par tranche d'âge
· Selon le type de schistosomiase
· Selon le laboratoire
EVOLUTION DE LA SCHISTOSOMIASE DE 1999 à 2003
DANS LE DISTRICT SANITAIRE DE TOUGAN

| 


