2.1.1 Phénomène de
l'hystérésis
L'hystérésis entre l'adsorption et la
désorption de la datte est importante à la
température 25 °C (Fig. 16).
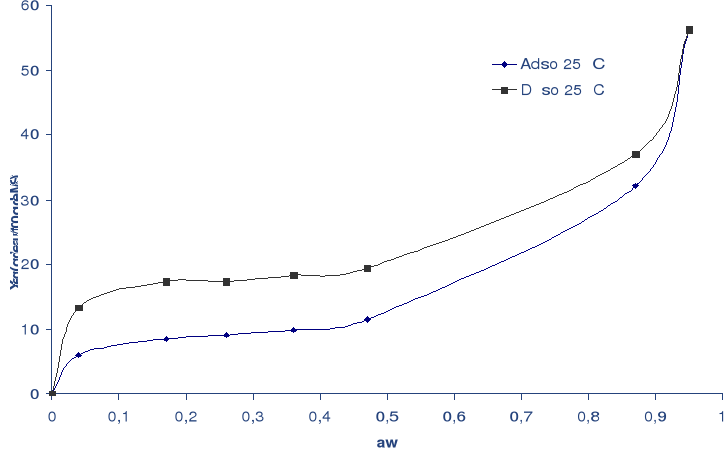
Fig. 16 : Courbe d'isotherme de désorption et
d'adsorption de la datte à 25 °C.
2.1.2 Effet de la température sur les isothermes
d'adsorption et de désorption
2.1.2.1 Effet de la température sur l'isotherme
de désorption
La figure 17 montre que lorsque la température augmente
la teneur en eau à l'équilibre diminue. Cette
figure montre qu'aux environs de l'activité de l'eau 0.8 on
n'observe aucun croisement et qu'aux valeurs de l'aw supérieures
à 0.8 l'augmentation de la température entraîne une
diminution de la teneur en eau à l'équilibre. Ces
résultats comparables à ceux de Kechaou et al.
(1996).
0
10
20
30
40
50
60
0
0,1
0,2
0,3
0,4
0,5
0,6
0,7
0,8
0,9
1
aw
Xeq (g d'eau / 100g de MS)
à 25°C
à 40°C
![]()
Fig. 17 : Courbe d'isotherme de désorption de la
datte à 25 et 40 °C.
2.1.2.2 Effet de la température sur l'isotherme
d'adsorption
La figure 18 présente les courbes des isothermes
d'adsorption déterminées à 25 et 40 °C. On
remarque que la teneur en eau à l'équilibre diminue lorsque la
température augmente pour une même valeur de l'activité de
l'eau. Ceci est observé pour les activités de l'eau
inférieure à 0.8 (Fig. 18).
Cependant, pour les valeurs supérieures à
l'activité de l'eau 0.8 l'effet opposé est observé
à savoir que la teneur en eau à l'équilibre augmente
lorsque la température augmente. Le croisement des deux courbes des
isothermes est observé aux environs des activités de
l'eau 0.8 (Fig. 18).
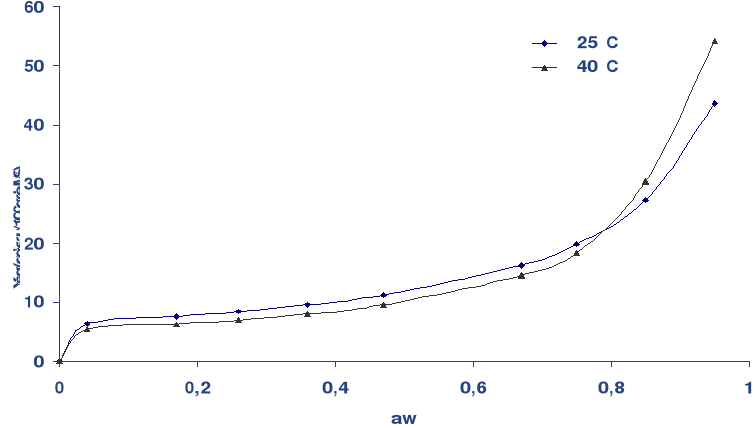
Fig. 18 : Courbe d'isotherme d'adsorption de la datte
à 25 et 40 °C.
2.2 Ajustement des valeurs
expérimentales aux modèles mathématiques
de sorption (GAB - BET).
Les résultats de l'analyse de la régression non
linéaire de l'ajustement de l'équation de GAB et de BET
aux valeurs expérimentales sont présentés
respectivement sur les tableaux 16 et 17. Les valeurs de la
moyenne relative du pourcentage de déviation P (%) sont
données par le tableau 15. Les valeurs du pourcentage
P(%) sont comprises entre 3.6 et 6.32 pour les cinq isothermes
de désorption et d'adsorption (Tableau 15). Les valeurs de
P(%) sont donc inférieures à 10 % et cela nous
permets de conclure que les équations de GAB et de BET peuvent
être utilisées pour prédire la valeur de la
teneur en eau à l'équilibre et d'autres paramètres
tels que la teneur en eau de la couche mono-moléculaire
et les enthalpies de liaison de la monocouche et la
multicouche.
Les figures 19, 20, 21, 22 et 23 représentant les
isothermes de désorption et d'adsorption des dattes de la
variété Deglet-Nour, montrent que les courbes des
points expérimentaux et calculés sont presque confondues et
ceci est confirmé par les faibles valeurs de P(%) .(Tableau
15).
Tableau 15 : La valeur de P (%) des
différentes isothermes.
|
Isotherme
|
P (%)
|
|
Désorption à 25 °C
|
6.32
|
|
Adsorption à 25 °C
|
5.86
|
|
Adsorption à 30 °C
|
4.41
|
|
Désorption à 40 °C
|
4.68
|
|
Adsorption à 40 °C
|
3.6
|
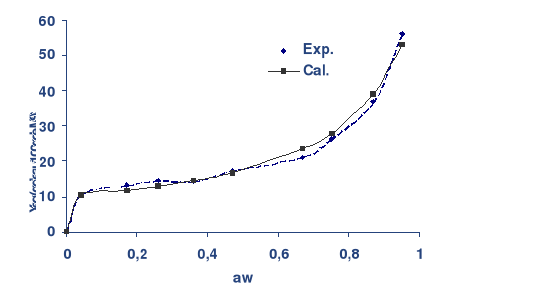
Fig. 19 : Isotherme de
désorption de la datte à 25 °C représentée par
les points expérimentaux et calculés.
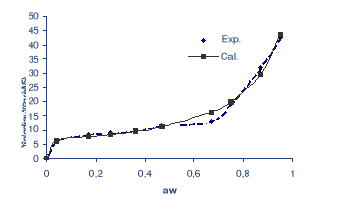
Fig. 20 : Isotherme d'adsorption de la
datte à 25 °C représentée par les points
expérimentaux et calculés.
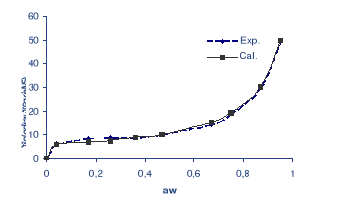
Fig. 21 : Isotherme d'adsorption de la datte
à 30 °C représentée par les points
expérimentaux et calculés.
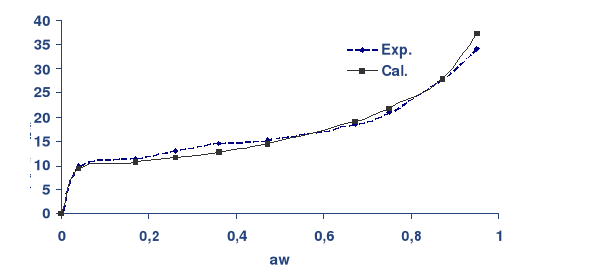
Fig. 22 : Isotherme de désorption de la datte
à 40 °C représentée par les points
expérimentaux et calculés.
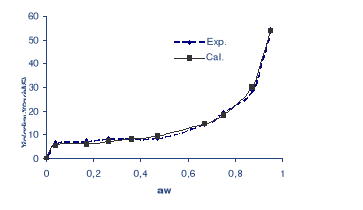
Fig. 23 : Isotherme d'adsorption de la
datte à 40 °C représentée par les
points expérimentaux et calculés.
2.2.1 Estimation des paramètres
Les paramètres de l'équation de GAB (Xm, C, K)
et BET (Xm, C) sont déterminés à partir des
résultats expérimentaux en utilisant la régression non
linéaire.
Les valeurs de la teneur en eau de la couche
mono-moléculaire Xm déterminées par les
équations de GAB et de BET sont présentées
respectivement sur les tableaux 16 et 17.
Les valeurs de Xm déterminées par
l'équation de BET sont légèrement supérieures
à celles déterminées par l'équation de GAB.
Cette observation est similaire à celle rapportée par
Labuza et al. (1985).
Tableau 16 : Valeurs des
paramètres de l'équation de GAB.
|
Paramètre
Isotherme
|
Xm
|
C
|
K
|
R2
|
|
Adsorption à 25 °C
|
6.525
|
377.655
|
1.207
|
99.363
|
|
Désorption à 25 °C
|
10.071
|
1228.635
|
1.665
|
95.510
|
|
Adsorption à 40 °C
|
5.290
|
1854.669
|
1.625
|
99.827
|
|
Désorption à 40 °C
|
9.388
|
2680.387
|
1.662
|
94.382
|
|
Adsorption à 30 °C
|
5.779
|
1796.135
|
1.263
|
99.896
|
Tableau 17 : Valeurs des paramètres de
l'équation de BET.
|
Paramètre
Isotherme
|
Xm
|
C
|
R2
|
|
Adsorption à 25 °C
|
6.451
|
342.942
|
96.01
|
|
Désorption à 25 °C
|
11.921
|
790.382
|
99.17
|
|
Adsorption à 40 °C
|
5.343
|
376.592
|
94.08
|
|
Désorption à 40 °C
|
9.673
|
362.725
|
95.92
|
|
Adsorption à 30 °C
|
5.857
|
885.202
|
97.77
|
La valeur de la teneur en eau de la
couche mono-moléculaire (Xm) estimée
par l'équation de GAB à 25 °C est de 10.07 % .
Cette valeur est supérieure à celle rapportée par
Belarbi et al.
(2000) (Tableau 18).
Tableau 18 : Comparaison des valeurs du
Xm de la datte avec d'autres fruits secs.
|
Produit
|
Datte
|
Abricot
|
Pomme
|
Pomme de terre
|
Raisin
Sec
|
|
Echantillon
|
D'après Belarbi et al. (2000)
|
|
Xm (%MS)
|
10.07
|
8.73
|
9.5
|
7.6
|
6.7
|
11.5
|
2.2.2 Valeurs thermodynamiques déterminées
par l'équation de GAB à 5 paramètres
Le paramètre H1 de l'équation de GAB
représente la différence entre l'enthalpie de la couche
mono-moléculaire et celle de la multicouche. Dans cette
étude la valeur H1 est estimée à 39.70 kJ/mole
(Tableau 19). Cette valeur indique qu'il existe une forte liaison entre
les sites hydrophiles primaires du solide et la première couche des
molécules d'eau. H2 qui représente la différence entre
la chaleur latente de condensation de l'eau pure et la chaleur de sorption
de la multicouche est estimée à - 0.74 kJ/mole (Tableau 19).
Cette valeur négative montre que la chaleur de sorption de
multicouche est supérieure à celle de la chaleur
latente de condensation de l'eau pure.
Tableau 19 : Les valeurs des cinq
paramètres de GAB d'ajustement aux isothermes de
désorption et d'adsorption des dattes.
|
Paramètre
Isotherme
|
Xm
|
C'
|
K'
|
ÄH1 (kJ/mole)
|
ÄH2
(kJ/mole)
|
R2
|
|
Adsorption à 25 °C
|
6.525
|
377.655
|
1.207
|
39.760
|
- 0.740
|
99.363
|
|
Désorption à 25 °C
|
10.07
|
1228.635
|
1.665
|
67.401
|
- 1.657
|
95.510
|
|
Adsorption à 40 °C
|
5.290
|
1854.669
|
1.175
|
31.734
|
- 0.554
|
99.827
|
|
Désorption à 40 °C
|
9.388
|
2680.387
|
1.662
|
52.213
|
- 2.028
|
94.382
|
|
Adsorption à 30 °C
|
5.779
|
1796.135
|
1.263
|
23.413
|
- 0.770
|
99.896
|
2.2.3 Calcul de la chaleur de sorption de la couche
monomoléculaire et la multicouche
La chaleur de désorption de la couche
monomoléculaire (Hm) et de la multicouche (Hq) a
été obtenue à l'aide de l'équation de GAB. La
résolution de cette équation par la régression non
linéaire donne la valeur de ?H2 (Tableau 19).
1.2.3.1 Chaleur de désorption de la multicouche
(Hq)
?H2 = HL - Hq
HL : Chaleur latente de
vaporisation de l'eau pure = 43.980 kJ /mole (10500 cal/mole)
D'où :
Hq = 45.637 kJ/mole
Le poids d'une mole d'eau égale à la masse
molaire d'une molécule d'eau (18 gr).
Hq = 2535.38 kJ / kg d'eau
Soit :
1.2.3.2 Chaleur de désorption de couche
mono-moléculaire (Hm)
Hm = 113.03 k J/mole
?H1 = (Hm - H q)
d'où :
Hm = 6279.88 k J / kg d'eau
Soit :
On remarque d'après ces résultats que la chaleur
de désorption de la couche mono-moléculaire
(Hm = 113.03 kJ/mole) est plus importante que celle de la
multicouche (Hq = 45.637 kJ/mole). Cette
supériorité est probablement due à une forte fixation des
molécules d'eau. Dans la monocouche, les molécules d'eau sont
fortement fixées aux sites polaires par des liaisons hydrogènes
de fortes énergies (Annexe II). Alors que les molécules d'eau
dans la multicouche sont retenues par des liaisons hydrogènes dont les
énergies sont de moins en moins fortes (Multon, 1982).
Cela explique que l'eau de cette couche
monomoléculaire est relativement difficile à enlever. Ces
résultats sont comparables à ceux trouvés par
Kaymak-Ertekin et Gedik (2004).
La chaleur de désorption de la multicouche Hq
est estimée à 2535.38 kJ / kg d'eau, permet de calculer
la quantité de chaleur nécessaire pour diminuer la teneur en eau
de la datte comme suit :
L'énergie nécessaire pour évaporer l'eau
des dattes est :
Q = Hq . me
On a :
Hq : La chaleur de
désorption de la multicouche : Hq = 2535.38 kJ / kg
d'eau.
me : Quantité d'eau à
évaporer qui se calcule selon cette formule :
me = mi (mci - mcf) / (100-mcf)
D'où :
mi : Quantité du produit à
sécher =1 Kg.
mci : Taux d'humidité initial = 29.56 %.
mcf : Taux d'humidité final = 16.21 %.
me = 0.159 kg d'eau à évaporer
Soit :
Q = 403.12 kJ
D'où:
Puisque on a 1 Kwh = 3,6. 10 3 kJ, on aura
alors :
Q = 0.111 Kwh
L'énergie nécessaire pour diminuer la teneur en
eau initiale (29.56 %) des dattes en une teneur en eau de 16.21%, est
égale à 0.111 Kwh.
2.3 Calcul de chaleur de sorption
Les valeurs de ÄHb
calculées sont inversement proportionnelles
aux valeurs des teneurs en eau. La variation de la chaleur de
sorption en fonction de la teneur en eau est
représentée dans la figure 24. Ces résultats sont
comparables à ceux trouvé par Do Amaral Sobral
et al. (1999).
L'étude de la variation de la chaleur de sorption d'eau
en fonction de la teneur en eau, a montré que ÄHb
augmente lorsque la teneur en eau diminue, et ceci s'explique par la
forte interaction qui existe entre l'eau et les composants adsorbants de la
datte. A des teneurs en eau élevées, les sites de
sorption diminuent et ceci conduit à une diminution de la valeur du
ÄHb.
Aux faibles teneurs en eau ( 0,15) l'énergie de liaison
(ÄHb) est négative et cela montre que l'interaction est
exothermique. La valeur maximale de cette énergie (-ÄHb)
étant égale à 32 kJ/mole.
Aux teneurs en eau élevées, la valeur de
l'énergie de liaison tend vers zéro, cela signifie que la
chaleur de sorption isostérique est égale à la chaleur de
condensation de l'eau (Qst = Ho).
Sur la figure 24 on constate que dans la zone des teneurs en
eau élevées la chaleur de sorption (ÄHb) est positive et
ceci indique que l'interaction entre l'eau et le substrat est endothermique
correspondant à une dissolution des sucres. La chaleur de sorption
initiale est très élevée aux faibles teneurs en eau.
Les valeurs élevées des chaleurs de sorption à faible
teneur en eau indiquent que l'interaction entre les composants de l'aliment
et l'eau est importante. Lorsque la teneur en eau augmente les sites de
sorption disponibles diminuent et conduisant ainsi à une diminution
des valeurs des chaleurs de sorption.
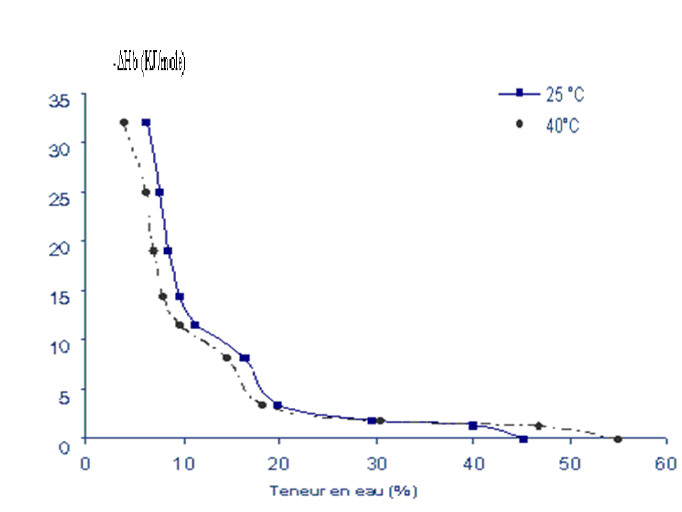
Fig. 24 : Relation entre l'énergie de sorption de
la datte variété
Deglet-Nour et la teneur en eau.
3. CINETIQUE DE SECHAGE
D'après les résultats obtenus on peut dire que
deux variables influencent la cinétique de séchage :
§ La température (Figure 25 et 26).
§ La vitesse de l'air (Figure 27 et 28).
Ces mêmes résultats sont trouvés par Kechaou
et al. (1996).
3.1 L'effet de la température et de la vitesse de l'air
sur la perte en eau
3.1.1 Effet de la température de l'air
Les figures 25 et 26 montrent que la teneur en eau au cours
du séchage diminue avec l'augmentation de la température de l'air
et par conséquent la diminution du temps de séchage. Ces
observations peuvent facilement s'explique par l'augmentation de l'apport en
chaleur du produit.
Les figures 25 et 26 confirment cet effet où pour
une vitesse d'air constante, la perte en eau est affecté par la
température.
Ces travaux sont comparables à ceux trouvé par
Newman et al. (1996) pour le séchage des prunes.
Ces résultats corroborent ceux trouvés par
Kechaou et al. (1996).
3.1.2 Effet de la vitesse de l'air
Les figures 27 et 28 montrent l'effet de la vitesse de l'air
de séchage sur la perte en eau. En effet, la vitesse
de l'air la plus élevée donne une perte d'eau plus grande pour
une température constante de séchage. Ceci est bien
illustré par les valeurs des pertes en eau. En effet, pour une
température constante de 40 °C et une vitesse de l'air variable
entre 0.5 et 1.5 m/s la perte en eau augmente de 27.72 % à 46.42 %.
Ces travaux sont comparables à ceux trouvé par
Bimbenet (1978) et similaires à ceux trouvé par
Kechaou et al. (1996).
En fin, pour mieux voir l'effet de ces variables
(température et vitesse de l'air) nous donnons ci-dessous un
résumé des résultats obtenus (Tableau 20).
Tableau 20 : Effet de la température et de la
vitesse de l'air sur la cinétique de séchage.
|
T (°C)
|
30
|
40
|
|
Vitesse de l'air (m/s)
|
0.5
|
1
|
1.5
|
0.5
|
1
|
1.5
|
|
Perte en eau (%)
|
27.57
|
32.41
|
39.28
|
27.72
|
35.71
|
46.42
|
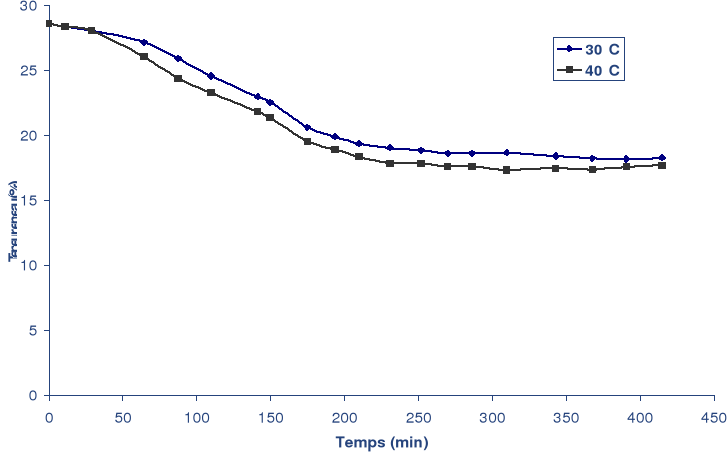
Fig. 25 : Effet de la température sur la perte en
eau (Vair = 0.5 m/s).
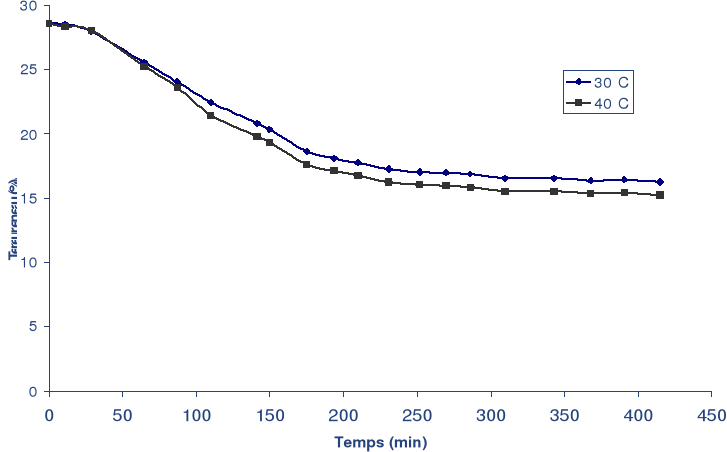
Fig. 26 : Effet de la température sur la perte en eau
(Vair = 1.5 m/s).
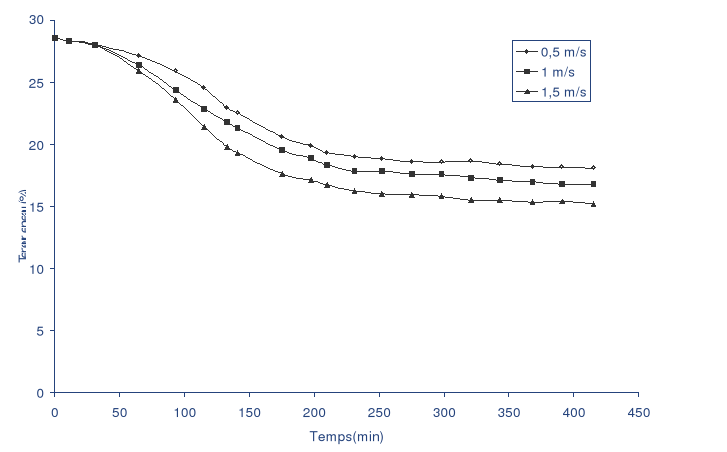
Fig. 27 : Effet de la vitesse de l'air sur la perte en eau
à une température de 40 °C.
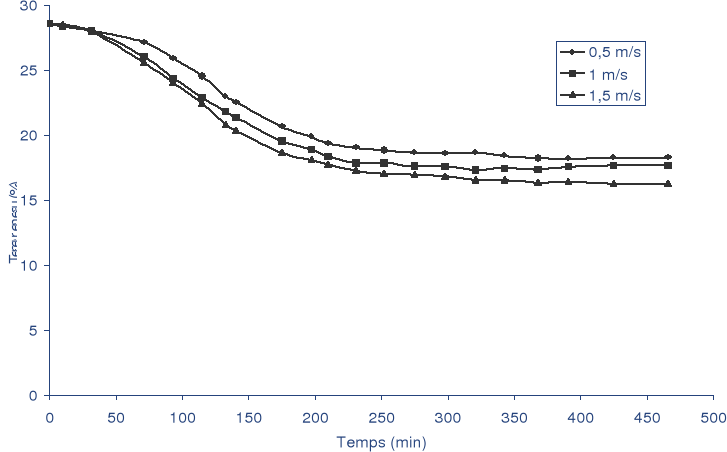
Fig. 28 : Effet de la vitesse de l'air sur la perte en eau
à une température de 30 °C.
3.2 Allure de séchage
L'allure de séchage des dattes Deglet-Nour
présente deux phases (figure 29). La première phase de
séchage à vitesse décroissante, appelée souvent
« deuxième phase de séchage »
pendant laquelle le facteur limitant est la migration interne de l'eau. D'autre
part nous remarquons l'influence de la température et la vitesse de
l'air sur la cinétique de séchage. Ces
observations peuvent facilement s'expliquer d'une part par l'augmentation de
l'apport de chaleur au produit et, d'autre part, par l'augmentation
de la vitesse de l'air, c'est-à-dire par la diminution de la force
motrice globale de transfert (X-Xeq) à l'intérieure de ce
solide. La deuxième phase de séchage appelée
« troisième phase de séchage » : la
vitesse de séchage décroît moins rapidement pour s'annuler
au point Xeq, correspondant à l'équilibre du produit avec les
conditions extérieures constantes.
Aux teneurs en eau comprises entre 15 % et 20 % la vitesse de
séchage n'est pas influencée par la variation de la
température. Ceci est expliqué par le fait que l'eau est
fortement liée.
Cependant lorsque la teneur en eau est élevée
(> 27%), la vitesse de séchage est sensiblement
influencée par la température. Cette augmentation de la vitesse
de séchage est due à l'eau se trouvant à
l'état libre. Lorsque la température augmente de
30 à 40 °C la vitesse de séchage s'élève de
0.40 g d'eau / 100 g de MS/ h 0.45 g d'eau/ 100g de MS/h.
Ces résultats sont en accord à ceux trouvés
par Kechaou et al. (1996).
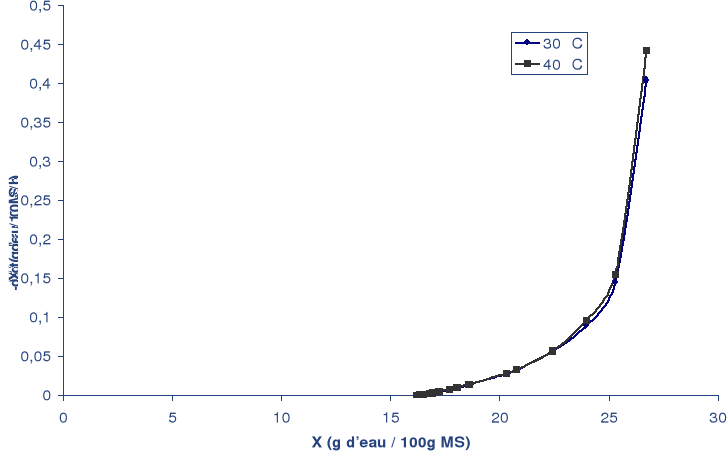
Fig. 29 : Cinétiques de séchage d'une datte
isolée.
| 

