2.3.3.2. Détermination
des formes moléculaires de An. gambiae s.s.
Ø 5' ... GCG C ... 3'
3' ... C GCG ... 5'
Principe :
L'endonucléase Hhal (Haemophilus haemoliticus),enzyme
de restriction, digèreles moléculesd'ADN et entraine leur rupture
au niveau des sitesderestriction présentéecomme suit :
Protocole : Les produits de
l'amplification sont distribués (10ul) dans des microtubes de 0,2ml
contenant 15ul du "Master MIX" préalablement préparé sur
glace (Tableau C, Annexe 1). Cet ensemble est placé à
l'étuve (37°C) pendant au moins 3h ou toute une nuit.
Après digestion, on fait migrer le produit sur un gel
d'agarose à 2% avec des témoins positifs (An. gambiae M
et S) et le marqueur de tailles. L'ensemble sera photographié
sous UV. Les tailles attendues sont 727 pb pour la forme M et 475 pb pour la
forme S.
2.4. DETERMINATION DE
L'INFESTATION DES ANOPHELES
La mise en évidence de l'infestation des
anophèles femelles par Plasmodium a été faite par
la technique ELISA (Enzyme Linked ImmunoSorbent Assay) qui permet
de détecter la protéine circumsporozoïte de
Plasmodium (CSP) dans l'organisme des anophèles. La technique
utilisée est celle de Burkot et al., (1984)
améliorée par Wirtz et al., (1987).
Principe : Elle consiste
à coupler la protéine CSP à un anticorps monoclonal de
capture (ACm) anti-circumsporozoïte(anti-CSP) préalablement
fixé sur la paroi des puits d'une plaque. Le complexe
antigène-anticorps formé est ensuite révélé
par un anticorps monoclonal anti-CSP couplé à la peroxydase
(marqué). L'adjonction d'un substrat qui sera dégradé sous
l'action de l'enzyme induit une réaction colorée visible et dont
la densité optique sera mesurée par spectrophotométrie
(figure 7).
Puits de la plaque
fixation
Ac
Ac : anticorps
Ag : antigène
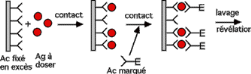
Figure 8 :Schéma du principe de
la technique "ELISA sandwich"
Protocole ELISA-CSP
monospécifique : La tête et le thorax de chaque
moustique sont coupés et placés dans des tubes
numérotés. On y ajoute 20ul de Np40 (détergent qui
facilite la destruction des tissuspar hydrolyse des protéines
membranaires) et le tampon de broyage "Blocking Buffer" (BB) à raison de
2x190ul par tubes et on les broie. Ces broyats sont conservés pendant
1hà -20°C.
Chaque plaque ELISA (Plaque de Nunc à 96
puits) est sensibilisée à raison de 50ul d'ACm de capture par
puits et laissée une nuità +4°C, ce qui permet l'adsorption
de l'ACm sur les parois de la plaque. Le lendemain, les plaques sont
vidées, puis sans les laver, 200ul de tampon BB sont mis dans chaque
puits pour saturer les sites de fixation libres des ACm. Après 1h
d'incubation à température ambiante, les plaques sont
vidées de nouveau et 50ul du broyat de moustique sont ajoutésdans
chaque puits. La colonne de négatifsne reçoit que du BB et pour
les puits des témoins positifs, 50ul de protéine
circumsporozoïtique de l'espèce (P. falciparum) sont
utilisés (annexe 3).
Après 2h d'incubation les plaques sont vidées et
lavées 2 fois au PBS/Tween20. Ensuite on ajoute une solution d'ACm
conjugué à la peroxydase (50ul/puits) préparée 10
min à l'avance. Après 1h d'incubation à température
ambiante, les plaques sont de nouveau vidées et lavées 4 fois au
PBS/Tween 20. Le substrat préparé 5 min avant la fin de
l'incubation est distribué à raison de 100ul/puits. Les plaques
sont alors conservées 30 minutes à l'obscurité. La
dégradation du substrat sous l'action de la peroxydase se traduit par
une coloration bleue.
Cette réaction est stoppée en ajoutant 50ul
d'acide sulfurique 4N par puits, ce qui change la coloration bleue en une
coloration jaune. La lecture s'effectue au moyen d'un spectrophotomètre
à 450 et 650 nm. L'intensité seuil des positifs est fixée
à deux fois la moyenne des témoins négatifs. La
composition des réactifs et les quantités utilisées sont
présentées en annexe 4.
| 


