LA CHLAMYDIOSE AVIAIRE
1. INTRODUCTION
La chlamydiose aviaire est une zoonose infectieuse,
contagieuse provoquée par une bactérie Chlamydia psittaci,
très répondue dans l'avifaune sauvage et domestique. Elle se
définie chez les psittacidés (perroquet) par un syndrome
entérotyphique souvent mortel qui est la psittacose et chez tous les
autres oiseaux par un syndrome respiratoire le plus souvent inapparent qui est
l'ornithose.
La maladie est transmissible à l'homme, elle se traduit
par une pneumonie atypique primitive (PAP) aiguë ou subaiguë. Fort
heureusement, les thérapeutiques actuelles ont considérablement
modifié les données du problème et réduit la
portée de cette maladie chez l'homme. Chez les oiseaux le traitement de
choix sera fait avec les tétracyclines, il a l'inconvénient de
créer des porteurs sains inapparents, excréteurs de
chlamydies (ANDRE, 1994; VILLATE, 2001).
2. ETIOLOGIE
L'agent causal, fait partie de l'ordre des Chlamydiales, famille
des Chlamydiaceae, qui comprend 2 genres et 9 espèces.
- Le genre
Chlamydia comprend 3 espèces dont une seule
rencontrée chez l'homme, C. trachomatis.
- Le genre Chlamydophila regroupe 6
espèces. Deux sont rencontrées chez l'homme, C. pneumoniae et C.
psittaci
. C. pneumoniae spécifiquement humain.
. C. psittaci
comprend des souches variées isolées chez les oiseaux sauvages
(perroquets) ou domestiques (perruches) et les volailles (canards, poulets).
Les chlamydies sont des bactéries parasites
intracellulaires obligatoires, parfois désignées sous le nom" des
parasites d'énergies", très petites (0.25 micron de large, par
0.35 micron de long) ce sont des bactéries Gram négatif. Elle
contient du DNA, du RNA, ainsi que de nombreux ribosomes. Il s'agit d'un
organisme ubiquiste, fortement infectieux remarquable par sa capacité
à esquiver les défenses immunitaires de la cellules hôte.
La chlamydie se présente sous deux formes:
- Corps élémentaires (CE) : il s'agit de la forme
infectieuse, pouvant se trouver dans le milieu extérieur, elle est
incapable de se multiplier. Le CE est sphérique (0.2 à 0.4 um de
diamètre) immobile, sans flagelles et métaboliquement inerte.
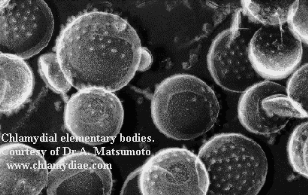
Figure 1 Chlamydies sous forme (CE) (Anonyme2,
2004)
Figure 2 Corps
élémentaires( Anonyme8, 2004).
- Corps réticulé (CR) : Il
représente la forme non infectieuse, intracellulaire
métaboliquement active (division binaire) de la chlamydie. Son
diamètre est de 0.6 à 0.8 um.
Les chlamydies sont très résistantes dans le
milieu extérieur et peuvent garder leur pouvoir infectieux plusieurs
mois, dans les selles et les secrétions. Par contre elles sont
très sensibles à l'action de la chaleur et du formol
(André, 1994;
Anonyme5, 2004).

Figure 4 Vues en microscopie
électronique, Dr Mortemousque, Pr Gendre, Laboratoire de Microscopie
électronique, Université de Bordeaux I
(Anonyme5).
3. PATHOGENIE
3.1 ATTACHEMENT ET ENTREE DU CE DANS LA CELLULE HOTE
Le CE présente un tropisme
préférentiel pour les cellules à épithélium
cylindrique, essentiellement celles des muqueuses respiratoires et digestives.
Il s'attache aux microvillosités de la surface apicale de ces cellules.
La cellule hôte génère des invaginations de sa membrane
plasmatique. Ces genres de vésicules abritent alors les CE et par la
suite, s'accumulent dans la zone de Golgi. Les CE restent partiellement
protégés vis-à-vis du système immunitaire de le
l'hôte par leur situation intracellulaire.
3.2 DIFFERENCIATION DU CE EN CR
Les CE, métaboliquement inerte, vont
se transformer en CR métaboliquement actifs. On assiste à une
modification au niveau des membranes du CE : les ponts disulfures
interprotéiques disparaissent. Se réalise ensuite une
synthèse de DNA, de RNA et de protéines conduisant la formation
de CR.
3.3 CROISSANCE DU CR
Le CR plaque son endosome contre les
mitochondries de la cellule hôte et grâce à
l'intermédiaire d'une ATPase spécifique (translocase), il
parasite son ATP. Des carences en éléments nutritifs chez la
cellule hôte pourraient faire en sorte que la chlamydie se mette
temporairement en sommeil, restant alors à l'état latent chez
l'hôte porteur. Par la suite grâce à une scission binaire,
se forme alors un groupe de un à plusieurs centaines (100 à 500)
CR, ce groupe prenant le nom d'inclusion (ou "corps de Levinthal-Cole-Lillie").
Lors de la division de la cellule hôte, il y a possibilité de
transmission de l'inclusion.
3.4 MATURATION DES CR
Ils sont considérés comme
matures, lorsque les éléments nutritifs de la cellule hôte
sont épuisés.
3.5 CONDENSATION DES CR EN CI (CORPS
INTERMEDIAIRE)
Cette mutation se déroule à
l'intérieur de l'inclusion. On peut considérer les chlamydies
comme des agents mise en sommeil, pouvant persister plus ou moins longtemps,
sans activité, dans les cellules hôtes. Après cette
étape les CI vont se transformer en CE.
3.6 RELARGAGE DES CE
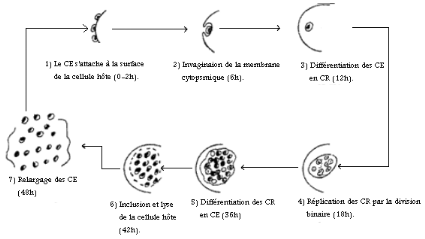 Figure 4 Cycle de développement de la chlamydie
(48h) (Anonyme2; 2004).
Figure 4 Cycle de développement de la chlamydie
(48h) (Anonyme2; 2004).
Il se produit à la suite de la lyse de la cellule
hôte (sous l'action d'enzymes produits par la chlamydie), les CE
envahissant alors de nouvelles cellules hôtes ou étant
disséminés à l'extérieur (André,
1994; Anonyme5; 2004).
4. EPIDEMIOLOGIE
4.1 ESPECES RECEPTIVES
4.1.1 Les psittacidés
Perroquets et perruches semblent
relativement résistants mais, mais comme les pigeons,
représentent des réservoirs naturels.
4.1.2 Les passériformes
Canari, pinson, gould, padda cardinal sont sensibles.
4.1.3 Les columbidés
Colombes, tourterelles, pigeons (véritables
réservoirs).
4.1.4 Les palmipèdes Les canards, les
oies.
4.1.5 Les gallinacés
Poules, faisans, dindes (principales sources d'infection
humaine aux Etats-Unis), dindons, pintades.
- Il ne faut pas oublier de citer, parmi les espèces
réceptives, la classe des mammifères au premier rang desquels on
trouve l'homme.
4.2 TRANSMISSION
La dissémination du germe se fait par les fientes, les
sécrétions nasales des oiseaux infectés, on peut trouver
les germes dans le matériel, la poussière de plume, au niveau
des pondoirs et les couveuses, les marchés d'oiseau, et les stations de
quarantaine qui sont également des secteurs de gros risque.
Habituellement la transmission est due à l'inhalation
de poussière de selles (voie respiratoire), à l'absorption de
graines, de plantes souillées par les excréments (voie
digestive). Elle peut se produire chez les jeunes au nids, lors du gavage par
les parents (par l'intermédiaire du lait du jabot), par la souillure
provoquée par les excréments des parents. La présence
d'arthropodes pourrait jouer un rôle. Sont également virulents,
les sécrétion nasales, et oculaires, le sang.
4.3 FACTEURS FAVORISANTS
4.3.1 Age Les jeunes oiseaux étant
les plus sensibles.
4.3.2 Espèce
4.3.3 Stress le froid, le transport, la
surpopulation, les mauvaises conditions sanitaire et alimentaire, les
parasitoses (André, 1994; Anonyme8,
2004; Anonyme4, 2001).
5. SYMPTOMATOLOGIE
Il faut préciser que, dans la majorité des cas,
l'infection reste inapparente. Ces symptômes présentent une
diversité en fonction de l'état immunitaire de l'oiseau, la
charge bactérienne infectante et la présence concomitante
d'autres maladies. L'incubation est de 3 à 10 jours, parfois plus.
5.1 FORME SURAIGUE
Elle est plus particulièrement observée chez
les jeunes oiseaux et les petits exotiques. La mort survient en quelques
heures, sans signes particuliers préalables.
5.2 FORME AIGUE
C'est la forme la plus classique. La maladie prend, en
général, une forme septicémique;
- L'oiseau est abattu, se tient en " boule", présente
une forte hyperthermie.
- Les paupières mi-closes, il souffre de
conjonctivo-blépharite, voire de kérato-conjonctivite.
- Il tient les ailes plus ou moins pendantes.
- Des troubles respiratoires : dyspnée,
polypnée, jetage nasal séro-muqueux, éternuements.
- Des troubles digestifs : gastro-entérite,
diarrhée de couleur citron-vert, souillant les plumes
péri-cloacales.
- Une polyurie, urines verdâtre ou jaunâtre.
- Enfin, des troubles nerveux (paralysies, convulsions),
traduisant une atteinte du système nerveux central,
précédent parfois la mort.
- La mort peut survenir dans les 4 à 15 jours qui
suivent le déclanchement de la maladie.
5.3 FORME SUBAIGUE OU CHRONIQUE
On n'observe aucun des symptômes
précédemment décrits ou alors essentiellement des troubles
respiratoires (dyspnée, toux, râles, éternuements, jetage
nasal), souvent accompagnés d'un écoulement oculaire, un manque
d'appétit, des plumes hérissées ou un oiseau dormant la
plupart du temps (léthargie), peut laisser suspecter la présence
de la maladie. Chez nombreux oiseaux, le seul signe extérieur reste une
conjonctivite (chez le pigeon).
5.4 FORME INAPPARENTE
Pas de symptômes extérieurs
caractéristiques de la maladie. Chez les psittacidés, le taux de
porteurs chroniques inapparents est estimé comme étant de 10
à 40 %, voir dans quelques cas de 100 % (André, 1994;
Anonyme1, 2004).
6 LESIONS
6.1 MACROSCOPIQUE
A l'autopsie on note également
- Un amaigrissement.
- Un dépôt fibrineux blanchâtre sur les
séreuses péritonéale et cardiaque, ainsi que sur les sacs
aériens (dépôts très riches en chlamydies).
- Un oedème pulmonaire, une pneumonie secondaire, de
l'aérosacculite.
- Un foie hypertrophié, à bords arrondis de
couleurs ocracée et une splénomégalie
- Une nécrose multifocale dans le foie et la rate.
- Une dégénérescence hépatique
graisseuse et, parfois la présence de petits foyers nécrotique
(psittacomes).
- La rate présente une pulpe rouge sombre, molle, avec
parfois, présence de psittacomes. (Lors de l'infection inapparente, la
splénomégalie est souvent la seule lésion visible).
- Des reins sont parfois hypertrophiés, friable, de
couleur grisâtre.
- Une entérite catarrhale et un épanchement
péritonéal dans certains cas.

Figure 5 Lésions du foie
(Anonyme8, 2004)
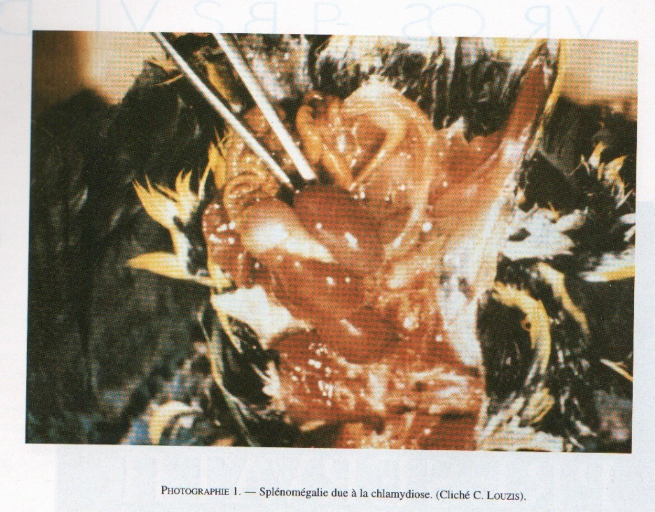
Figure 6 Splénomégalie due
à la chlamydiose (André, 1994).
6.2 MICROSCOPIQUE
Les meilleurs prélèvements sont
représentés par les exsudats inflammatoires contenant des
mononucléaires (macrophage) ; le jetage, contient pour l'essentiel des
cellules épithéliales squameuses, la conjonctive, liquide
péritonéal...
Après la coloration (Giemsa ou de Stamp), les lames,
sont observées au microscope (immersion x 1000), à la recherche
d'éventuelles inclusions intra-cytoplasmiques. (André, 1994;
Anonyme2, 2004; Anonyme8, 2004).
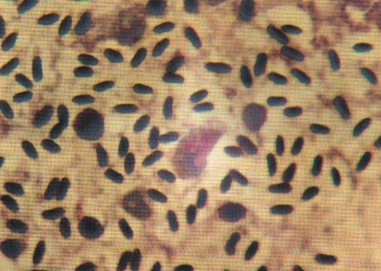
Figure 7 Inclusion Chlamydienne, coloration du
Stamp, foie du perroquet (André, 1994).
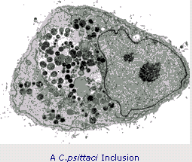
Figure 8 Inclusions intracytoplasmiques
(Anonyme6, 2004).

Figure 9 Les corps réticulés
(Anonyme2, 2004)
7. DIAGNOSTIC
7.1 CLINIQUE
Le diagnostic d'un oiseau soupçonné d'avoir la
psittacose peut être difficile. Il convient de
procéder à une collecte de l'anamnèse la plus objective
possible :
espèce - lieu et période d'acquisition,
provenance de l'oiseau - traitement antérieurs connus - conditions
d'hébergement - antécédents pathologiques...
Dans bien de cas, l'observation attentive de l'oiseau permet
la découverte des symptômes préalablement
décrits.
7.2 COMPLEMENTAIRES
7.2.1 Radiographie
- Une augmentation de densités des sacs
aériens.
- Une hépatomégalie, une
splénomégalie entraînant un déplacement des
viscères abdominaux vers le bas.
7.2.2 Hématologie
- Une leucocytose (augmentation de nombre de globule blanc)
- Une hétérophilie.
7.2.2 Biochimie
- Une augmentation des protéines
totales, LDH, SGOT, CPK, des acides biliaires.
7.3 EXPERIMENTAL
7.3.1 Sérologique
- Deux sérologies sont généralement
nécessaires à 3 ou 4 semaines d'intervalle.
- Une augmentation des anticorps lors du deuxième
prélèvement sanguin.
7.3.2 Test de fixation du complément
(FC)
- Il détecte seulement les IgG.
- Un taux positif identique qu'une infection chlamydienne a
bien eu lieu, infection peut-être disparue au moment où est
réalisée l'analyse.
7.3.3 Méthode BELISA (Bloking Enzyme Linked
Immunosorbent Assay)
- Permet de détection des globulines IgM dans le
sérum. Il est associé avec le test ELISA.
7.3.4 Méthode ELISA (Enzyme Linked
Immunisorbent Assay)
- Les anticorps sont associés à une peroxydase
ou à des marqueurs fluorescents.
- Détecter l'antigène lipopolysaccharides de la
membrane externe de CE.
7.4 DIFFERENTIEL
Les lésions et les symptômes
n'étant pas pathognomoniques, il faudra éliminer l'action
d'autres agents infectieux, qui par ailleurs peuvent agir concomitamment avec
la chlamydie : Pasteurella, Salmonella, Escherichia coli, Mycoplasmes,
virus,... (André, 1994).
8. TRAITEMENT
8.1 TETRACYCLINES
Il est nécessaire de poursuivre le traitement
pendant au moins 15 jours. Ces antibiotiques ont fait leurs preuves. Les
tétracyclines n'ont aucun intérêt, distribués dans
l'eau de boisson, car leur concentration est insuffisante. Il est donc
nécessaire de les distribuer dans un aliment
supplémenté.
8.2 QUINOLONES
À action bactéricide, agissent sur une plus
courte durée d'administration et sont également actifs
vis-à-vis de nombreuses maladies bactériennes.
- Enrofloxacin (Baytryl).
- Ciproflaxicine.
8.3.1 TRAITEMENT D'APPOINT
Distribuer aux oiseaux sous traitement, du
yaourt, des lactobacilles (Océdiar), un détoxifiant
hépatique, tel que le lactulose (Duphalac) (André,
1994).
9. PROPHYLAXIE
9.1 PROPHYLAXIE MEDICALE
Un vaccin efficace sera certainement difficile à
réaliser, en raison des variations antigéniques
dépendantes des différentes souches chlamydiennes. Il sera
nécessaire d'associer les diverses classes d'anticorps (IgA-IgM-IgG).
9.2 PROPHYLAXIE SANITAIRE
Il faut choisir les agents chimiques capables d'attaquer la
fraction lipidique de leur membrane cellulaire. le chlorure de benzalkonium [22
bis]. Sont également utilisables, l'alcool iodé, l'éthanol
à70°, l'eau oxygénée (André,
1994).
10. LA LEGISLATION
CODE SANITAIRE POUR LES ANIMAUX TERRESTRES
2003
PARTIE
2
TITRE 2.7.
CHAPITRE 2.7.4.
CHLAMYDIOSE AVIAIRE
Article 2.7.4.1.
Les normes pour les épreuves diagnostiques sont
fixées dans le Manuel terrestre.
Article
2.7.4.2.
Les Administrations vétérinaires des
pays indemnes de chlamydiose aviaire peuvent interdire l'importation ou le
transit sur leur territoire, en provenance de pays considérés
comme infectés de chlamydiose aviaire, de tout oiseau de la famille des
Psittacidés.
Article 2.7.4.3.
Les Administrations vétérinaires des
pays importateurs tiennent compte :
pour les oiseaux de
la famille des Psittacidés :
De la présentation d'un certificat
vétérinaire international attestant que les
oiseaux :
1. Ne présentaient aucun signe clinique de chlamydiose
aviaire le jour de leur chargement ;
2. Ont été placés, durant les
45 jours ayant précédé leur chargement, sous
surveillance vétérinaire, et ont été traités
contre la chlamydiose aviaire avec de la chlortétracycline.
(Anonyme3, 2004).
LA BIBLIOGRAPHIE
1. ANDRE J.P., 1994.
La chlamydiose aviaire à Chlamydia psittaci chez les
oiseaux de cage : revue bibliographique.
In : Revue de médecine vétérinaire.
Décembre 1994, n°145, p 915-929.
2. VILLATE D., 2001.
Les chlamydioses : Ornithose-Psittacose.
In : Maladies des volailles. 3eme Ed.
éd : France agricole., p 282.
3. ANONYME1 :
www.calopsitte.com 2004
4. ANONYME2:
www.chlamydie.com. 2004
5. ANONYME3 :
www.oie.int. 2004
6. ANONYME4 : Epidémies
d'ornithose dans un abattoir de volailles.
In : Document pour le médecin du travail, N°85
1èr trimestre 2001.
7 ANONYME5 :
www.microbe-edu.org/etudiant/ chlamydia.html. 2004
8. ANONYME6 :
www.ocbs-nt-server.umaryland.edu/ bavoil/turni. 2004
9. ANONYME8: Avian Biotech International.
2004



