|

Cancer du poumon non à petites cellules chez la
femme
Expérience du Service d'Oncologie
Médicale du CHU de Tanger
Etude rétrospective
MEMOIRE PRESENTE PAR
Docteur ABRINI HOUDA
Née le 08/07/1991 à Ottignies-Louvain-La
neuve
POUR L'OBTENTION DU DIPLOME DE SPECIALITE EN
MEDECINE
OPTION : ONCOLOGIE MEDICALE
Sous la Direction de
PROFESSEUR FATIMA ZAHRA EL M'RABET
Session Juin 2024

Remerciements

1

A notre maître
Madame le PROFESSEUR FATIMA ZAHRA EL M'RABET
Professeur
Agrégée en Oncologie Médicale
Nous avons eu un grand
plaisir de travailler sous votre direction et de
bénéficier de
votre guidance et de vos conseils remarquables tout au long
de notre
formation.
Vos compétences professionnelles et vos
qualités humaines exemplaires ont
conquis notre admiration et notre respect.
Chère maître, nous tenons à vous rendre
un grand hommage et à vous
exprimer notre gratitude la plus profonde.
Nous vous sommes très reconnaissantes et nous vous
adressons nos
marques de respect les plus sincères.
2

A notre maître
Madame le PROFESSEUR MOUNIA AMZERIN
Professeur
Assistante en Oncologie Médicale
Votre expertise, votre modestie et
vos qualités humaine et professionnelle
ont été pour
nous une source d'admiration.
Elles représentent des modèles à suivre.
Nous désirons, être à la hauteur
de votre confiance.
Nous vous adressons ces mots en toute humilité pour
exprimer notre
sincère reconnaissance.
3

A notre maître
Madame le PROFESSEUR KHADIJA DARIF
Professeur Assistante
en Oncologie Médicale
Votre élan remarquable, votre rigueur
professionnelle et votre humanisme
sont des qualités qui nous ont
profondément marqués et que nous
admirons
sincèrement.
Veuillez recevoir ces mots comme un témoignage de
notre gratitude et de
notre respect.
4

Dédicaces

5

A ma très chère famille
À mes très chers parents Jamal ABRINI et
Nadia SKALI, dont le soutien
indéfectible et l'amour inconditionnel
ont été mes piliers tout au long de
ma formation. Votre
bienveillance et votre encouragement ont toujours
été pour moi
la plus grande motivation pour mener à terme mes projets.
Que Dieu tout puissant vous protège et vous octroie
une longue vie.
À ma petite soeur Aya, dont la présence
joyeuse et les mots
d'encouragement ont illuminé même les jours
les plus sombres que j'ai dû
traverser. Ta force et ta bienveillance
ont été pour moi une source
d'inspiration constante.
À mes chers frères Oussama et Mouad, sachez
que vous avez été des
mentors précieux. Votre
perspicacité et votre soutien m'ont guidé à
travers les
défis de ce parcours endurant.
À vous tous, ma famille bien-aimée, je
dédie ce travail.
Avec tout mon amour et ma gratitude infinis
Houda
6

7
Résumé
Introduction : Le cancer du poumon est
actuellement un grand problème de santé publique. Son incidence
ne cesse d'augmenter chez les femmes et l'écart de l'incidence entre les
deux sexes diminue au niveau mondial. L'objectif de cette étude est
d'évaluer le profil épidémiologique, clinique,
histologique, moléculaire, thérapeutique et le pronostic du
cancer du poumon non à petites cellules (CPNPC) chez la femme.
Méthodes : C'est une étude
rétrospective incluant des patientes atteintes du CPNPC confirmé
et suivies au service d'Oncologie Médicale du Centre Hospitalier
Universitaire Mohammed VI de Tanger entre mai 2018 et décembre 2023.
Résultats : 77 patientes ont
été incluses dans l'étude. Leur âge moyen
était de 60.5 ans. Toutes les patientes étaient non fumeuses. Le
délai moyen du diagnostic était de 5.1 mois. Le suivi
médian était de 5 mois. Les signes cliniques majeurs
étaient la dyspnée (42.8%), la toux (31.1%) et la douleur
thoracique (25.9%). La majorité des patientes étaient
diagnostiquées au stade IV (90.9%). L'adénocarcinome était
le type histologique le plus fréquemment diagnostiqué (87%). Les
localisations métastatiques les plus fréquemment
retrouvées étaient la plèvre (55.7 %), les os (44.3 %) et
le poumon (30%). Le test de mutations du gène de l'EGFR
réalisé chez 27 patientes était positif chez 13 patientes
(48.1%). Les mutations retrouvées étaient exclusivement celles au
niveau de l'exon 19 et la mutation ponctuelle L858R dans l'exon 21 qui sont
couramment associées à la sensibilité aux inhibiteurs de
la tyrosine kinase (ITK) de l'EGFR. La mutation ALK qui a été
recherchée chez 8 patientes était positive dans 12.5% des cas. La
chimiothérapie palliative de première ligne a été
indiquée chez 54 patientes dont 46 avaient reçu une
chimiothérapie à base de sels de platine (5 d'entre elles
étaient EGFR muté) et 8 EGFR muté avaient
bénéficié d'une thérapie par les ITK de l'EGFR
(erlotinib ou gefitinib). La survie globale (SG) médiane des patientes
mutées pour l'EGFR traitées en première ligne par les ITK
de l'EGFR était significativement plus longue par rapport à celle
des patientes EGFR muté traitées par chimiothérapie
à base de sels de platine (20 mois contre 9 mois, p=0.05) et la survie
sans progression (SSP) médiane chez ces patientes était
également significativement plus longue par rapport à celle des
patientes traitées par chimiothérapie à base de sels de
platine (19 mois contre 5 mois, p=0.028).
Conclusion : La population des femmes
atteintes de CPNPC étudiée était
caractérisée par l'absence de tabagisme, la dominance du type
histologique adénocarcinome et par un pourcentage élevé de
mutations de l'EGFR. La SSP et la SG médianes des patientes
traitées par les ITK de l'EGFR étaient significativement plus
longues que la SSP et la SG des patientes qui avaient reçu une
chimiothérapie à base de sels de platine. Ces résultats
nous incitent à la réalisation des tests de mutations de l'EGFR
chez l'ensemble des patientes diagnostiquées avec un
adénocarcinome afin qu'elles puissent recevoir une thérapie
ciblée par les ITK de l'EGFR.
Mots-clés : CPNPC, Femmes,
Adénocarcinome, Non-fumeuses, Métastases, Mutations de l'EGFR,
Chimiothérapie aux sels de platine, Mutation ALK, ITK de l'EGFR

8
Abstract
Introduction: Lung cancer is currently a
major public health problem. Its incidence continues to increase in women, and
the gap in incidence between the two sexes is decreasing worldwide. The aim of
this study was to assess the epidemiological, clinical, histological,
molecular, therapeutic and prognostic profile of non-small cell lung cancer
(NSCLC) in women.
Methods: This is a retrospective study
including patients with confirmed NSCLC followed at the Medical Oncology
Department of the Mohammed VI University Hospital Centre in Tangier between May
2018 and December 2023.
Results: 77 female patients were included in
the study. Their mean age was 60.5 years. All patients were non-smokers. The
average time to diagnosis was 5.1 months. The median follow-up was 5 months.
The major clinical signs were dyspnoea (42.8%), cough (31.1%) and chest pain
(25.9%). The majority of patients were diagnosed at stage IV (90.9%).
Adenocarcinoma was the most frequently diagnosed histological type (87%). The
most common metastatic sites were the pleura (55.7%), bones (44.3%) and lungs
(30%). EGFR gene mutation testing was performed in 27 patients and was positive
in 13 (48.1%). The mutations found were exclusively those in exon 19 and the
L858R point mutation in exon 21, which are commonly associated with sensitivity
to EGFR TKIs. The ALK mutation, which was detected in 8 patients, was positive
in 12.5% of cases. First-line palliative chemotherapy was indicated in 54
patients, 46 of whom had received platinum-salt-based chemotherapy (5 of whom
were EGFR mutated) and 8 EGFR mutated patients had received therapy with EGFR
tyrosine kinase inhibitors (TKIs) (erlotinib or gefitinib). The median overall
survival (OS) of EGFR-mutated patients treated as first-line therapy with EGFR
TKIs was significantly longer than that of EGFR-mutated patients treated with
platinum-based chemotherapy (20 months versus 9 months, p=0.05) and the median
progression-free survival (PFS) of these patients was also significantly longer
than that of patients treated with platinum-based chemotherapy (19 months
versus 5 months, p=0.028).
Conclusion: The population of women with
NSCLC studied was characterized by the absence of smoking, the dominance of the
adenocarcinoma histological type and a high percentage of EGFR mutations. The
median PFS and OS of patients treated with EGFR TKIs were significantly longer
than the PFS and OS of patients who had received platinum-based chemotherapy.
These results encourage us to carry out EGFR mutations testing in all patients
diagnosed with adenocarcinoma so that they can receive targeted therapy with
EGFR TKIs.
Key words: NSCLC, Females, Adenocarcinoma,
Non-smokers, Metastases, EGFR mutations, Platinum chemotherapy, ALK mutation,
EGFR-TKI.

9
Sommaire
Résumé 7
Abstract 8
Liste des abréviations 11
Liste des tableaux 12
Liste des figures 13
I. Introduction 15
II. Matériel et méthodes 18
1. Matériel d'étude 18
1.1. Type d'étude 18
1.2. Population d'étude 18
1.2.1. Critères d'inclusion 18
1.2.2. Critères d'exclusion 18
2. Méthodes d'études 18
2.1. Recueil des données 18
2.2. Fiche d'exploitation 18
2.3. Analyses statistiques 19
2.4. Considérations éthiques 19
III. Résultats 21
1. Données démographiques cliniques et
histologiques 21
1.1. Caractéristiques démographiques 21
1.2. Caractéristiques cliniques 21
2.3. Caractéristiques histologiques 23
2. Données radiologiques 23
3. Profil moléculaire 25
4. Prise en charge thérapeutique 26
5. Survie 28
IV. Discussion 33
1. Données épidémiologiques 33
2. Données cliniques 35
3. Aspects anatomopathologiques 36
4. Stade radiologique 36
5. Profil moléculaire 36
6. Prise en charge thérapeutique et survie 38
V. Conclusion 43
VI.

10
Références Bibliographiques 45
VII. Annexes 54
Annexe 1 54
Annexe 2 55
Annexe 3 57
Liste des abréviations

11
ADK : Adénocarcinome
ALK : Anaplastic Lymphoma Kinase
BPCO : Bronchopneumopathie Chronique Obstructive
BSC : Best supportive care (soins de support palliatifs
exclusifs)
CHU : Centre Hospitalier Universitaire
TNM : Tumeur (Tumor)-ganglion (node)-métastase
(metastasis)
CPC : Carcinome à petites cellules
CPNPC : Cancer du poumon non à petites cellules
EGFR: Epithelial Growth Factor Receptor
HTIC: Hypertension intracrânienne
IC : Intervalle de confiance
IMC : Indice de masse corporelle
ITK : Inhibiteurs de la tyrosine kinase
PD-L1: Programmed Death-Ligand 1
PS : Performance Status (Indice de performance)
RCC : Radio-chimiothérapie concomitante
ROS: Reactive Oxygen Species
SG: Survie globale
SSP : Survie sans progression
TDM TAP : Tomodensitométrie
Thoraco-Abdomino-Pelvienne
Liste des tableaux

12
Tableau 1: Caractéristiques
démographiques, cliniques et histologiques des patientes 22
Tableau 2: Méthodes de confirmation
histologique des CPNPC 23
Tableau 3: Répartition des tumeurs
selon les classifications TNM 24
Tableau 4: Stades radiologiques 24
Tableau 5: Répartition des
différentes localisations métastatiques 25
Tableau 6: Statut des mutations EGFR, ALK et
ROS1 25
Tableau 7: Protocoles utilisés chez
les patientes en 2ème ligne 27
Tableau 8: Comparaison des séries de
la littérature rapportant la fréquence des femmes atteintes du
cancer du poumon par rapport à la totalité des
patients atteints de la maladie 33
Tableau 9: Comparaison
des séries de la littérature rapportant la fréquence des
patientes atteintes de
CPNPC par rapport à l'ensemble des CPNPC
34
Tableau 10: Variation des taux de mutations de l'EGFR
chez les patientes atteintes de CPNPC au
Maroc et dans différents pays 37
Tableau 11:
Caractéristiques cliniques et localisations des mutations de
l'EGFR chez les patientes
EGFR muté de notre étude et de celles de
séries de la littérature 38
Tableau 12:
Comparaison de séries de la littérature rapportant la
SSP médiane et la SG médiane chez
les femmes atteintes de CPNPC EGFR muté traitées
en première ligne par les ITK de l'EGFR 41
Tableau 13: 8ème classification TNM du
cancer du poumon 55
Tableau 14: Classification par stade
(8ème classification TNM du cancer du poumon) 56

13
Liste des figures
Figure 1: Schéma des thérapies
utilisées pour le traitement des patientes 26
Figure 2: Protocoles utilisés chez les
patientes en 1ère ligne 27
Figure 3: Courbe de Kaplan-Meier
représentant la survie globale des patientes 29
Figure 4: Courbe de Kaplan-Meier
représentant la survie sans progression des patientes 29
Figure 5: Courbe de Kaplan-Meier
représentant la survie globale des patientes EGFR muté
traitées par anti EGFR et par chimiothérapie
à base de sels de platine 31
Figure 6: Courbe de
Kaplan-Meier représentant la survie sans progression des patientes
EGFR
muté traitées par anti EGFR et par
chimiothérapie à base de sels de platine 31

14
Introduction

15
I. Introduction
Le cancer du poumon constitue un grave problème de
santé publique dans le monde et représente la première
cause de décès par cancer [1]. En 2020, approximativement 2.2
millions de nouveaux cas et 1.8 millions de décès ont
été enregistrés à travers le monde [2]. Le
pronostic de la maladie reste actuellement dépréciatif avec un
taux de survie globale à cinq ans qui varie de 6% à 14% chez les
hommes et de 7% à 18% chez les femmes [3]. Néanmoins nous
assistons dans les dernières années à des
rémissions prolongées voire des guérisons après
l'introduction de l'immunothérapie.
Au Maroc, le taux d'incidence du cancer du poumon demeure
généralement élevé (31.9/100 000) en comparaison
avec d'autres pays du continent Africain [4]. Cette maladie continuera à
occuper les premières places parmi les cancers en 2040 avec un taux de
mortalité de 16/100 000 [5].
Les cancers du poumon sont classés histologiquement en
cancers du poumon non à petites cellules (CPNPC) et les carcinomes
à petites cellules (CPC). Environ 85 % des cas sont des cancers du
poumon non à petites cellules [6].
Après l'apparition des symptômes, la
majorité des cancers du poumon sont à un stade avancé
(stade IV) lorsqu'ils sont diagnostiqués et ne peuvent pas faire l'objet
d'une résection chirurgicale qui reste l'élément
fondamental du traitement. C'est pourquoi le cancer du poumon doit être
diagnostiqué à un stade précoce (stade I) par le biais du
dépistage. En effet, l'introduction du dépistage de ce cancer
devrait favoriser un changement de stade vers un stade précoce au moment
du diagnostic, avec une amélioration de la survie.
Au cours des dix dernières décennies, le cancer
du poumon était considéré comme une maladie masculine
essentiellement. Actuellement, bien que le cancer du poumon reste plus
fréquent chez les hommes que chez les femmes, l'écart entre les
deux sexes tend à s'estomper dans plusieurs régions du monde du
fait de la progression constante de la maladie chez les femmes [7].
Le principal facteur de risque du cancer du poumon est le
tabagisme avec une corrélation exposition - effet [8]. Dans la
population féminine, alors que l'impact du tabagisme était
évalué comme la cause principale du cancer du poumon dans la
plupart des pays développés, des recherches
épidémiologiques ont mis le point sur la présence d'autres
contributeurs épidémiologiques et facteurs hormonaux,
génétiques et moléculaires agissant comme des

16
facteurs de risque indépendants ou interagissant avec
l'effet du tabagisme [9]. L'affirmation potentielle selon laquelle les femmes
ont une sensibilité accrue aux substances cancérigènes du
tabac reste controversée [10]. Par ailleurs, l'importance relative et la
contribution des facteurs liés à l'environnement et au mode de
vie au risque de ce cancer peuvent varier en fonction de la zone
géographique et des conditions socio-économiques. Il en
résulte que le cancer du poumon chez la femme est une affection
distincte et spécifique qui nécessite plusieurs études
pour définir ses caractéristiques épidémiologiques,
cliniques, moléculaires et thérapeutiques.
Au Maroc, très peu d'études ont abordé le
cancer du poumon chez la femme. Ces études avaient concerné les
régions de Rabat, Casablanca, Fès et Marrakech.
Dans le présent travail nous présentons une
étude rétrospective d'une série de cas de cancer du poumon
non à petites cellules chez les femmes traitées au service
d'Oncologie Médicale du Centre Hospitalier Universitaire Mohamed VI de
Tanger. Cette étude est la première réalisée au
Nord du Maroc, elle a eu pour but d'évaluer les caractéristiques
épidémiologiques, diagnostiques, moléculaires,
thérapeutiques et pronostiques du CPNPC chez la femme.

17
Matériel et Méthodes

18
II. Matériel et méthodes
1. Matériel d'étude 1.1. Type
d'étude
Cette étude entreprend une analyse
rétrospective descriptive d'une série de cas menée au sein
du Service d'Oncologie Médicale du Centre Hospitalier Universitaire de
Tanger, couvrant une période de six ans, de mai 2018 à
décembre 2023.
1.2. Population d'étude 1.2.1. Critères
d'inclusion
Les sujets inclus dans notre analyse sont des patients de
sexe féminin, ayant été traitées pour un cancer du
poumon non à petites cellules, confirmé par histologie.
1.2.2. Critères d'exclusion
Nous avons exclu de notre étude les patients de sexe
masculin, les patientes diagnostiquées avec un cancer pulmonaire
à petites cellules, ainsi que tous les dossiers incomplets jugés
non exploitables.
2. Méthodes d'études 2.1. Recueil des
données
Pour cette étude, les dossiers médicaux des
patientes du service d'Oncologie Médicale du Centre Hospitalier
Universitaire de Tanger ont été examinés, et les
données ont été extraites et consignées dans des
feuilles de calcul Microsoft Excel (Microsoft Corp. Redmond, WA,
États-Unis, 2013).
2.2. Fiche d'exploitation
Les dossiers ont été examinés en
utilisant une fiche d'exploitation prédéfinie, remplie de
manière rétrospective. Cette fiche nous a permis une exploration
approfondie des données épidémiologiques, cliniques,
paracliniques, thérapeutiques et évolutives.

19
2.3. Analyses statistiques
Les données recueillies ont subi une analyse via le
logiciel IBM SPSS Statistics 29 (SPSS Inc., Chicago, IL, USA). Les moyennes,
écarts-types et pourcentages, relatifs à l'âge des
patientes, aux données démographiques, aux
caractéristiques cliniques et histologiques, ainsi qu'aux aspects
thérapeutiques, ont été calculés et
détaillés dans cette étude. La survie globale (SG)
médiane et la survie sans progression (SSP) médiane ont
été déterminées en utilisant la méthode de
Kaplan-Meier. La valeur de p a été obtenue par le biais du test
Log-Rank non stratifié, servant à comparer la survie globale
médiane (SG) et la survie sans progression médiane (SSP) entre
deux groupes de patientes. Par exemple, cela inclut la comparaison entre le
groupe traité avec Anti-EGFR et celui recevant une chimiothérapie
à base de sels de platine. Une valeur de p inférieure à
0.05 a été considérée comme statistiquement
significative.
2.4. Considérations éthiques
Étant une analyse rétrospective de dossiers,
notre étude n'a pas requis le consentement des patientes ni une
soumission formelle à la commission d'éthique. Cependant, afin de
préserver le secret medical, l'anonymat a été
rigoureusement préservé dans les fiches d'exploitation.

20
Résultats

21
III. Résultats
1. Données démographiques cliniques et
histologiques 1.1. Caractéristiques démographiques
Durant une période de 6 ans (2018-2023), un total de
596 patients (86 femmes et 510 hommes) atteints du cancer du poumon ont
été traités au sein du service d'Oncologie Médicale
du CHU de Tanger. La fréquence des patients de sexe féminin
était de 14.4%. Parmi les 596 patients, 315 (77 femmes et 238 hommes)
ont été traités pour un cancer du poumon non à
petites cellules (CPNPC). Notre étude a porté sur les 77 femmes
atteintes de CPNPC. La proportion de ces patientes par rapport à la
totalité des patients atteints de CPNPC était de 24.4 % et la
proportion des femmes avec CPNPC par rapport à la totalité des
femmes atteintes du cancer du poumon était de 89.5 %.
Le nombre moyen de patientes colligées par an
était de 12.8. La moyenne d'âge des 77 patientes de notre cohorte
était de 60.5 #177;13.2 ans avec des extrêmes allant de 32
à 94 ans. On note que les 2 tranches d'âge <55 ans et 55-64 ans
étaient majoritaires avec un taux de 29.8% et 31.2% respectivement,
suivies de la tranche d'âge 65-74 ans (24.7%) alors que la tranche
d'âge=75 ans était minoritaire (14.3%). (Tableau 1).
L'analyse des dossiers des patientes a montré que 93.5%
étaient non tabagiques et 6.5% étaient exposées au
tabagisme passif. 7.8% des patientes étaient traitées pour
tuberculose pulmonaire et 3.9% avaient la Bronchopneumopathie Chronique
Obstructive (BPCO). L'antécédent de cancer du poumon était
présent dans 2.6% des cas (Tableau 1).
1.2. Caractéristiques cliniques
Le délai du diagnostic entre le début des
symptômes et la confirmation histologique était variable entre 1
et 36 mois avec une moyenne de 5.1 mois. Le symptôme le plus
fréquemment rapporté était la dyspnée (42.8% des
patientes), suivi par la toux (31.1% des cas) et enfin la douleur thoracique
(25.9% des cas) (Tableau 1).
Par ailleurs, nous avons observé que la plupart des
patientes (64.9%) présentaient un état général
conservé (PS=1). 28.6% avaient un PS 2 et 6.5% un PS 3. (L'Indice de
Performance PS est présenté en Annexe 1). L'indice de masse
corporelle (IMC) moyen était de 24.7 kg/m2 (extrêmes :
13.9-37 kg/m2) et la majorité des patientes (72.7%) avaient
un IMC = à 18.5 kg/m2

22
Tableau 1: Caractéristiques
démographiques, cliniques et histologiques des patientes
|
Caractéristiques
|
n
|
%
|
|
Cas durant 6 ans
|
|
|
|
2018
|
1
|
1.3
|
|
2019
|
19
|
24.6
|
|
2020
|
10
|
13
|
|
2021
|
18
|
23.4
|
|
2022
|
16
|
20.8
|
|
2023
|
13
|
16.9
|
|
Moyenne des cas /ans
|
12.8
|
|
|
Age (ans)
|
|
|
|
<55
|
23
|
29.8
|
|
55-64
|
24
|
31.2
|
|
65-74
|
19
|
24.7
|
|
=75
|
11
|
14.3
|
|
Age moyen : 60.5
|
|
|
|
Tabagisme
|
|
|
|
Tabagisme actif
|
0
|
0
|
|
Tabagisme passif
|
5
|
6.5
|
|
Absence de tabagisme
|
72
|
93.5
|
|
Signes cliniques
|
|
|
|
Dyspnée
|
33
|
42.8
|
|
Toux
|
24
|
31.1
|
|
Douleur thoracique
|
20
|
25.9
|
|
Hémoptysie
|
9
|
11.6
|
|
Amaigrissement
|
21
|
27.2
|
|
Douleur osseuse
|
16
|
20.7
|
|
HTIC
|
6
|
7.8
|
|
Syndrome cave supérieure
|
1
|
1.3
|
|
Performance Status au diagnostic
|
|
|
|
PS0
|
5
|
6.5
|
|
PS1
|
45
|
58.4
|
|
PS2
|
22
|
28.6
|
|
PS3
|
5
|
6.5
|
|
Types histologiques
|
|
|
|
Adénocarcinome
|
67
|
87
|
|
Carcinome épidermoïde
|
10
|
13
|

23
2.3. Caractéristiques histologiques
Le type histologique le plus fréquemment
diagnostiqué chez les patientes était l'adénocarcinome
(87%), suivi du carcinome épidermoïde (13%) (Tableau 1).
La confirmation histologique a été
réalisée par biopsie scannoguidée chez 61% des cas, par
bronchoscopique chez 18.2% des cas, par biopsie osseuse chez 14.2% des cas, par
biopsie ganglionnaire sus-claviculaire chez 3% des cas et chez 1.2% des cas,
elle a été réalisée par
|
biopsies cérébrale, hépatique et
péricardique (Tableau 2). Tableau 2: Méthodes de
confirmation histologique des CPNPC
|
|
|
|
Méthodes utilisées
|
n=77
|
%
|
|
Biopsie scannoguidée
|
47
|
61
|
|
Bronchoscopie
|
14
|
18.2
|
|
Biopsie osseuse
|
11
|
14.2
|
|
Biopsie ganglionnaire sus-claviculaire
|
2
|
3
|
|
Biopsie cérébrale
|
1
|
1.2
|
|
Biopsie hépatique
|
1
|
1.2
|
|
Biopsie péricardique
|
1
|
1.2
|
2. Données radiologiques
Sur base de la Tomodensitométrie
Thoraco-Abdomino-Pelvienne (TDM TAP), les tumeurs étaient localement
avancées dans la majorité des cas. Ainsi, les tumeurs T4
représentaient 40.4% et l'envahissement ganglionnaire N2 était
retrouvé dans 41.4% des tumeurs (Tableau 3).
En se basant sur la 8ème édition de la
classification TNM (Annexe 2), le stade radiologique le plus fréquent
était le stade IV chez 90.9% des patientes. Le stade III était
présent chez 7.8% des patientes et une seule patiente a
été diagnostiquée au stade I (1.3%) (Tableau 4).
70% de nos patientes avaient plus d'un site
métastatique. Les localisations métastatiques les plus
fréquentes étaient celles au niveau pleural, osseux, pulmonaire,
hépatique et cérébral (Tableau 5).
Tableau 3: Répartition des tumeurs selon
les classifications TNM
|
Classification
|
n
|
%
|
|
T
|
|
|
|
T1
|
10
|
19.2
|
|
T2
|
10
|
19.2
|
|
T3
|
11
|
21.2
|
|
T4
|
21
|
40.4
|
|
N
|
|
|
|
N0
|
18
|
31
|
|
N1
|
7
|
21.1
|
|
N2
|
24
|
41.4
|
|
N3
|
9
|
15.5
|
|
M
|
|
|
|
M0
|
7
|
9.1
|
|
M1
|
70
|
90.9
|
|
M1a
|
48
|
68.57
|
|
M1c
|
22
|
31.43
|
Tableau 4: Stades radiologiques
Stadesa n Pourcentage
(%)
1.3
1 1.3
7.8
2 2.6
4 5.2
Stade I IA-2
Stade III
IIIA IIIB

24
Stade IV IVA
a. 8ème classification TNM.

25
Tableau 5: Répartition des
différentes localisations métastatiques
Localisations métastatiques n
Pourcentage (%)
Pleurale 39 55.7
Osseuse 31 44.3
Pulmonaire 21 30
Hépatique 12 17.1
Cérébrale 10 14.3
Surrénalienne 6 8.6
Péricardique 5 7.1
3. Profil moléculaire
Le test de mutation de l'EGFR (Epithelial Growth Factor
Receptor) a été réalisé chez 27 patientes (35% des
cas), revenant positif chez 13 patientes (48.1%) et négatif chez 14
patientes (51.9%). Les mutations étaient prédominantes sur l'exon
19 (9 patientes soit 69.2%), suivies par la mutation L858 sur l'exon 21 (4
patientes soit 30.8%) (Tableau 6).
La mutation ALK (Anaplastic Lymphoma
Kinase) qui a été recherchée chez 8 patientes
(soit 29.6% des cas), a été positive chez une patiente, celle qui
était au stade IA-2 (soit 12.5%). La recherche de la mutation ROS1
(Reactive Oxygen Species) a été réalisée chez 2
patientes (7.4%) et était négative dans les deux cas (Tableau
6).
La recherche de l'expression du PD-L1 (Programmed Death-Ligand
1) a été effectuée chez 6 patientes. Une faible
positivité (<50%) a été retrouvée chez 5
patientes représentant 83.3% des cas et une forte positivité
à 60% a été noté chez une seule patiente
(16.7%).
Tableau 6: Statut des mutations EGFR, ALK et
ROS1
|
n
|
Pourcentage %
|
|
Mutation de l'EGFR
|
|
|
|
Réalisée
|
27
|
35
|
|
Positive
|
13
|
48.1
|
|
Mutation sur :
|
|
|
|
Exon 19
|
9
|
69.2
|
|
L858 sur l'exon 21
|
4
|
30.8
|
|
Mutation ALK
|
|
|
|
Réalisée
|
8
|
29.6
|
|
Positive
|
1
|
12.5
|
|
Mutation ROS1
|
|
|
|
Réalisées
|
2
|
7.4
|
|
Positive
|
0
|
0
|

26
4. Prise en charge thérapeutique
Le délai entre la confirmation histologique et le
début du traitement des patientes dans notre étude était
de 2.1 mois en moyenne, il était variable entre 6 jours et 13.8 mois.
Parmi les 77 patientes, 13 ont été perdues de
vue (16.8%) et 6 patientes (7.8%) avaient reçu des soins de support
palliatifs exclusifs (BSC : Best Supportive Care). 1 seule patiente (stade
IA-2) a été adressée pour chirurgie (1.3%) puis perdue de
vue, 3 patientes stade IIIB (4%) avaient reçu une chimiothérapie
néoadjuvante suivie d'une radiochimiothérapie concomitante (RCC)
puis mise sous surveillance et 54 patientes stade IV (70.1%) avaient
reçu un traitement systémique palliatif en première ligne.
Parmi celles-ci, 46 avaient reçu une chimiothérapie à base
de sels de platine (dont 5 EGFR muté) (85.2%) et 8 EGFR muté
(14.8%) un traitement par anti-EGFR (Figure 1).
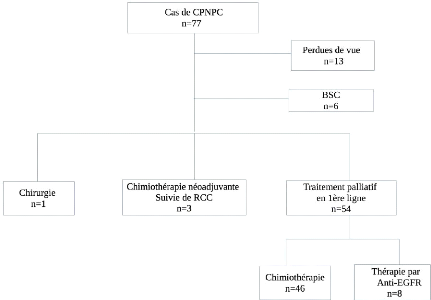
Figure 1: Schéma des traitements
utilisés chez les patientes atteintes de CPNPC
La figure 2 présente les protocoles utilisés en
première ligne chez les patientes au stade IV. L'acide zoledronique a
été associé au traitement systémique palliatif chez
13 patientes (16.9%

27
Protocoles de 2ème ligne
Docétaxel
Gemcitabine monothérapie Navelbine monothérapie
Etoposide monothérapie Carbo-Paclitaxel Carbo-Navelbine
Paclitaxel Pemetrexed Erlotinib
|
n=20
|
Pourcentage (%)
|
|
6
|
30
|
|
3
|
15
|
|
2
|
10
|
|
2
|
10
|
|
1
|
5
|
|
1
|
5
|
|
1
|
5
|
|
1
|
5
|
|
3
|
15
|
des cas) et le bevacizumab chez 3 patientes (4% des cas). Le
nombre moyen de cycles de chimiothérapie reçu était de 3.8
[extrêmes : 1 - 7]. Pour la thérapie par anti-EGFR, le nombre
moyen de cycles était de 15.9 [extrêmes :6 - 40]. Parmi les 46
patientes ayant reçu une chimiothérapie, 16 patientes n'ont pas
pu être évaluées pour la réponse au traitement car
perdues de vue au cours du suivi. L'évaluation de la maladie a
été basée sur les critères RECIST
présentés en annexe 3. Parmi les 30 patientes ayant une maladie
évaluable, 1 patiente (3.3%) a eu une réponse partielle, 6
patientes (20%) ont eu une stabilité et 23 patientes (76.6%) avaient une
progression. Concernant le traitement par anti-EGFR (n=8), 1 patiente a
été perdue de vue (12.5%), 1 patiente avait une réponse
partielle (12.5%), 5 patientes présentaient une stabilité (62.5%)
et 1 patiente avait une progression (12.5%).
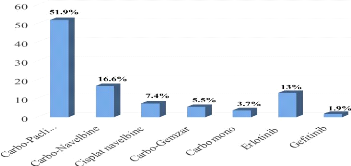
Figure 2: Protocoles utilisés chez les
patientes en 1ère ligne
Après progression, 20 patientes ont reçu un
traitement systémique de 2ème ligne. 17 patientes, (soit 85%) ont
reçu la chimiothérapie et 3 patientes (15%) ont reçu
l'anti EGFR (Tableau 7).
Tableau 7: Protocoles utilisés chez les
patientes en 2ème ligne

28
La radiothérapie palliative a été
réalisée chez 23 patientes, décompressive sur le rachis
chez 10 patientes, cérébrale chez 9 patientes, de consolidation
et antalgique sur le col du fémur chez 2 patientes et sur
l'humérus chez 1 patiente et enfin une radiothérapie palliative
pulmonaire a été réalisée chez 1 patiente.
5. Survie
Dans notre série, le suivi médian était
de 5 mois [extrêmes : 0-56], la survie globale (SG) médiane
était de 5 mois IC 95% [2.2-7.7]. La survie sans progression (SSP)
médiane était de 5 mois IC 95% [3.6-6.4]. Par ailleurs, les taux
de survie globale à 6 et 12 mois étaient de 44.4% et 28.7%
respectivement et les taux de survie sans progression (SSP) à 6 et 12
mois étaient de 38.5% et 7.7% respectivement (Figures 3 et 4).
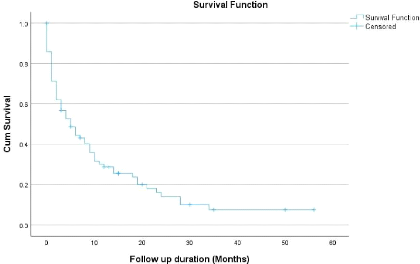

29
Figure 3: Courbe de Kaplan-Meier
représentant la survie globale des patientes
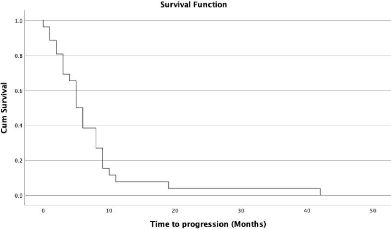
Figure 4: Courbe de Kaplan-Meier
représentant la survie sans progression des patientes

30
La survie globale (SG) médiane dans le groupe des
patientes EGFR muté traitées par anti EGFR était de 20
mois IC 95% [12.6-27.4] et dans le groupe EGFR muté traité par
chimiothérapie à base de sels de platine, elle était de 9
mois IC 95% [4.7-13.3]. Cette SG médiane chez le groupe thérapie
anti EGFR était significativement plus longue que celle dans le groupe
chimiothérapie à base de sels de platine avec une valeur de
p=0.05 (Figure 5).
De même, la survie sans progression (SSP) médiane
dans le groupe des patientes EGFR muté traitées par anti EGFR
était de 19 mois IC 95% [8.3-29.7] alors que dans le groupe des
patientes mutées pour l'EGFR traité par chimiothérapie
à base de sels de platine, celle-ci était de 5 mois IC 95%
[0.7-9.3]. La SSP médiane chez le groupe thérapie anti EGFR
était aussi significativement plus longue que celle chez le groupe
chimiothérapie aux sels de platine avec une valeur de p=0.028. On a
noté également que les courbes de la survie globale et celle de
la survie sans progression du traitement par chimiothérapie ont
chuté plus rapidement par rapport à celles du traitement par anti
EGFR signifiant que le décès des patientes s'est produit
très rapidement sous chimiothérapie (Figure 6).
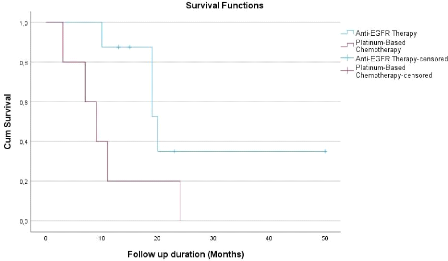

31
Figure 5: Courbe de Kaplan-Meier
représentant la survie globale des patientes EGFR muté
traitées par anti EGFR et par chimiothérapie à base de
sels de platine
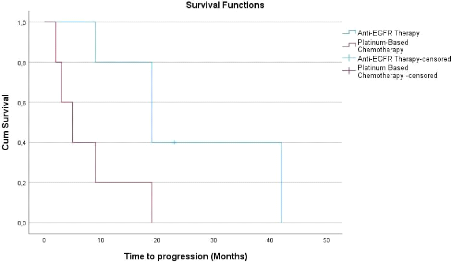
Figure 6: Courbe de Kaplan-Meier
représentant la survie sans progression des patientes
EGFR
mutées traitées par anti EGFR et par chimiothérapie
à base de sels de platine

32
Discussion

33
IV. Discussion
1. Données
épidémiologiques
Le cancer du poumon est l'une des principales causes de
cancers dans le monde, il constitue 11,4% des cas de cancers [11]. Il est l'une
des principales causes de décès liés au cancer chez les
hommes et chez les femmes et cela aussi bien dans les pays
développés que dans ceux en voie de développement [2].
Cependant, les femmes dans les pays développés souffrent d'un
taux de mortalité par cancer du poumon plus élevé. En
effet, chez ces dernières les décès dus au cancer du
poumon sont classées deuxièmes après le cancer du sein
[12].
Dans notre cohorte, la fréquence des femmes atteintes
du cancer du poumon était de 14.4%, ce qui corrobore parfaitement avec
les fréquences des femmes atteintes de ce cancer rapportées
à l'échelle nationale dans deux séries de cas à
Rabat entre 2005 et 2015 (14.5%) et entre 2014 et 2017 (14%) et sont
également en accord avec celles obtenues à Rabat entre 2005 et
2008 (10.5%), celles obtenues dans deux séries de cas à Marrakech
entre 2003 et 2009 (9%) et entre 2015 et 2021 (10.9%) et celles
rapportées à Oujda entre 2005 et 2014 (9%). Cependant, cette
fréquence reste nettement inférieure à celles des femmes
avec cancer du poumon rapportées en Guadeloupe entre 2008 et 2009
(27.4%), au Brésil entre 2006 et 2014 (39.5%) et aux USA entre 2001 et
2019 (46.7%) (Tableau 8), confirmant ainsi la plus grande fréquence de
la maladie chez les femmes dans les pays développés.
Tableau 8: Comparaison des séries de
la littérature rapportant la fréquence des femmes atteintes du
cancer du poumon par rapport à la totalité des patients atteints
de la maladie
|
Pays
|
Périodes
|
Fréquences (%)
|
Années
|
Références
|
|
Maroc- Tanger
|
2018-2023
|
14.4
|
2024
|
Cette étude
|
|
Maroc-Rabat
|
2005-2015
|
14.5
|
2019
|
[13]
|
Maroc-Rabat
|
2014- 2017
|
14
|
2022
|
[14]
|
Maroc-Rabat
|
2005-2008
|
10.5
|
2016
|
[15]
|
Maroc-Marrakech
|
2015-2021
|
10.9
|
2023
|
[16]
|
Maroc-Marrakech
|
2003-2009
|
9
|
2013
|
[10]
|
Maroc-Oujda
|
2005-2014
|
9
|
2019
|
[17]
|
France-Guadeloupe
|
2008-2009
|
27.4
|
2013
|
[18]
|
Brésil
|
2006-2014
|
39.5
|
2020
|
[19]
|
USA
|
2001-2019
|
46.7
|
2023
|
[20]
|
|

34
Concernant les patientes atteintes du cancer du poumon non
à petites cellules qui ont fait l'objet de notre étude, le
pourcentage des femmes atteintes de CPNPC était de 24.4%. Cette
fréquence est similaire à celles obtenues à Rabat entre
2014 et 2017 (23.3%) et entre 2010 et 2017 (27.5%), s'approche de celles
obtenues en Turquie (20.6%), en Guadeloupe (26.9%) et en Indonésie (28%)
mais elle est bien inférieure à celles rapportées dans la
Réunion (35%), en Malaisie (42.3%) et aux USA (45.9%) (Tableau 9),
marquant ainsi une importante variabilité de la fréquence du
carcinome non à petites cellules chez les femmes entre les pays.
Tableau 9: Comparaison des séries de la
littérature rapportant la fréquence des patientes atteintes de
CPNPC par rapport à l'ensemble des CPNPC
|
Pays
|
Années
|
Fréquences (%)
|
Années
|
Références
|
|
Maroc-Tanger
|
2018-2023
|
24.4
|
2024
|
Cette étude
|
|
Maroc-Rabat
|
2014-2017
|
23.3
|
2020
|
[21]
|
Maroc-Rabat
|
2010-2017
|
27.5
|
2020
|
[22]
|
Maroc-Fès
|
2008- 2018
|
13.8
|
2021
|
[23]
|
Maroc-Fès
|
2007-2012
|
13.4
|
2015
|
[24]
|
Turquie
|
2011-2014
|
20.6
|
2018
|
[25]
|
France-Guadeloupe
|
2008-2009
|
26.9
|
2013
|
[18]
|
France-Réunion
|
2017-2018
|
35
|
2020
|
[26]
|
Indonésie
|
2005-2015
|
28
|
2018
|
[27]
|
Malaisie
|
2010-2011
|
42.3
|
2014
|
[28]
|
|
|
USA
|
2001-2019
|
45.9
|
2023
|
[20]
|
Dans notre série, l'âge moyen des patientes
était de 60.5 ans. Cette moyenne est similaire à celle
rapportée en Italie (60 ans) [29]. Elle est légèrement
supérieure à celle rapporté au Maroc (58.3 ans) [24] et en
Indonésie (56.9 ans) [27] et légèrement inférieur
à celle observée en Suisse (62 ans) [30] chez les femmes
atteintes du cancer du poumon non à petites cellules. Par ailleurs, dans
notre étude les extrêmes d'âge se situaient entre 32 et 94
ans indiquant que le CPNPC affecte aussi bien les femmes jeunes que les femmes
âgées. Cependant, les tranches d'âge majoritaires
étaient <55 ans et entre 55 et 64 ans,
La majorité des patientes (93.5%) étaient non
fumeuses et 6.5% étaient exposées au tabagisme passif. Ces
résultats vont dans le même sens que ceux de Zakkouri el al [31]
qui ont rapporté que le tabagisme n'explique pas tous les cas de cancer
du poumon chez les femmes, car 75 % des patientes n'ont jamais fumé et
14 % ont été exposées au tabagisme passif. Le tabagisme

35

36

37
passif est un facteur de risque du cancer du poumon chez la
femme assez évoquée dans la littérature. Selon Sisti et
Boffetta [32], le tabagisme passif est mis en cause chez les femmes dans 14.2 %
des cas. Cependant le risque relatif diffère selon le type d'exposition
: familiale, professionnelle ou sociale [33], et selon l'intensité et la
durée du tabagisme passif subi [34].
7.8% des patientes de notre étude étaient
traitées pour tuberculose pulmonaire. La tuberculose et d'autres
infections pulmonaires augmentent le risque de cancer du poumon en raison d'une
inflammation prolongée, de la fibrose pulmonaire et des lésions
tissulaires pulmonaires [35, 36].
L'antécédent de cancer du poumon était
présent dans 2.6% des cas dans notre étude. Une étude de
l'International Lung Cancer Consortium [37] a montré qu'il y a 1.5 fois
plus de risque de cancer du poumon chez les personnes dont un parent de premier
degré (mère, père, frère ou soeur) souffre d'un
cancer du poumon, ce qui relèverait le caractère
héréditaire de la maladie.
2. Données cliniques
Les patients diagnostiqués à un stade
précoce bénéficient d'un taux de guérison
élevé. Cependant, le cancer du poumon est souvent
diagnostiqué tardivement à cause de l'apparition tardive des
symptômes, du caractère inexpressif de la maladie et du manque
d'un programme précoce de dépistage.
Le délai du diagnostic entre le début des
symptômes et la confirmation histologique de la maladie chez les
patientes de notre étude était de 5.1 mois en moyenne. Ce
délai dans notre contexte, soulève la problématique du
retard du dépistage du cancer bronchique chez la femme.
Le symptôme le plus fréquemment observé
dans notre étude était la dyspnée (42.8 %), suivie de la
toux (31.1%), puis la douleur thoracique (25.9%), ce qui concorde avec une
étude réalisée à Marrakech [38].
L'amaigrissement a été retrouvé chez
27.2% des patientes ce qui est en accord avec les résultats de
l'étude réalisée au Mali [39] qui rapporte une perte de
poids chez 30% des cas. Une étude américaine a
évalué l'évolution du poids chez 78 hommes et 74 femmes
ayant un CPNPC, il en ressort que les femmes perdent moins de poids par rapport
aux hommes [40]. L'état général peut être
quantifié par l'indice de Performance (PS). Dans notre étude,
seules 35.5% des patientes avaient un PS altéré ce qui concorde
avec les résultats obtenus à Meknès [41].
3. Aspects anatomopathologiques
L'adénocarcinome est le type histologique le plus
prédominant chez les femmes atteintes d'un cancer du poumon non à
petites cellules [42, 43, 44]. Dans notre série, l'adénocarcinome
(87 %) était aussi le type histologique le plus fréquemment
diagnostiqué chez les patientes atteintes de CPNPC par rapport au
carcinome épidermoïde. Ces résultats sont similaires
à ceux rapportés dans une étude aux USA qui a
montré que 71 % des cancers du poumon chez les femmes étaient des
adénocarcinomes [45]. De même, une méta-analyse de 17
études avait révélé que l'incidence de
l'adénocarcinome était 3.4 fois plus importante que le carcinome
épidermoïde chez les patientes non-fumeuses, et que jusqu'à
60 % des cancers du poumon chez les femmes étaient classés comme
adénocarcinomes [46].
La confirmation histologique a été
réalisée par biopsie scannoguidée chez la majorité
des cas, ce qui concorde avec les résultats de l'étude
menée à l'Hôpital Militaire d'Instruction Mohamed V de
Rabat [47]. Par contre, dans d'autres études [48, 49, 38] le principal
moyen de confirmation diagnostique était la biopsie bronchique suivie de
la biopsie scannoguidée.
4. Stade radiologique
Dans notre série, le stade radiologique le plus
fréquent était le stade IV (90.9%). Ces résultats
rejoignent ceux des autres séries dans lesquelles la majorité des
cancers bronchiques étaient diagnostiqués à un stade
localement avancé ou métastatique [49, 38, 41]. Dans les
séries Européennes et Américaines, la plupart des cas de
cancer du poumon non à petites cellules ont été
diagnostiqués à un stade relativement avancé [50]. De
même, dans l'étude de Zakkouri el al [31], la proportion des
cancers du poumon non à petites cellules diagnostiqué au stade IV
était plus élevée (82 %) par rapport à celles au
stade III (16 %) et au stade II (2 %). Le pourcentage élevé des
CPNPC au stade IV chez nos patientes peut s'expliquer par un retard du
diagnostic.
5. Profil moléculaire
La fréquence de mutation de l'EGFR varie en fonction
des zones géographiques et de l'origine ethnique. Dans notre
étude, la fréquence de mutation de l'EGFR était
élevée (48.1%). Cette fréquence est similaire à
celles obtenues dans d'autres études chez les femmes atteintes de CPNPC
au niveau national et en Turquie et au Liban. Cependant la fréquence de
l'EGFR mutée obtenue dans une étude réalisée
à Casablanca était nettement inférieure, ce qui
s'expliquerait
par la proportion élevée des patientes fumeuses
(Tableau 10). En Europe et en Amérique, cette fréquence est
généralement plus basse. Cependant chez les femmes asiatiques
atteintes de CPNPC, la fréquence de mutation de l'EGFR est très
élevée (Tableau 10).
Tableau 10: Variation des taux de mutations
de l'EGFR chez les patientes atteintes de CPNPC au Maroc et dans
différents pays
|
Pays
|
Mutations de l'EGFR
% (n patientes positives de N patientes
testées)
|
Année
|
Références
|
|
Maroc-Tanger
|
48.1 (13 de 27)
|
2024
|
Cette étude
|
|
Maroc-Rabat
|
47.8 (22 de 46)
|
2013
|
[51]
|
Maroc-Rabat
|
41.3 (38 de 92)
|
2020
|
[22]
|
Maroc-Rabat
|
38.4 (38 de 99)
|
2023
|
[52]
|
Maroc-Casablanca
|
24.3 (17 de 70)
|
2019
|
[53]
|
Turquie
|
48.4 (30 de 62)
|
2018
|
[25]
|
Liban
|
44.4 (7 de 34)
|
2014
|
[54]
|
Portugal
|
37.8 (31 de 82)
|
2012
|
[55]
|
Italie
|
30 (9 de 30)
|
2007
|
[29]
|
Pays -bas
|
13.4 (48 de 357)
|
2012
|
[56]
|
Brésille
|
33.3 (40 de 120)
|
2012
|
[57]
|
USA (Afro-Américaines)
|
15.7 (16 de 102)
|
2011
|
[58]
|
Chine
|
70.5 (74 de 105))
|
2018
|
[59]
|
Malaisie
|
62.3 (40 de 64)
|
2014
|
[28]
|
Taiwan
|
55.5 (20 de 36)
|
2004
|
[60]
|
|
Les patientes de notre étude présentant une
mutation EGFR étaient caractérisées par une moyenne
d'âge de 58 ans avec la présence de patientes jeunes, par le
sous-groupe histologique adénocarcinome et étaient non fumeuses.
D'autres études (Tableau 11) rapportent également que les femmes
EGFR muté étaient majoritairement non fumeuses et que leur type
histologique était également dominé par
l'adénocarcinome. En outre on note aussi dans ces études la
présence de patientes jeunes (Tableau 11). Il ressort de toutes ces
études que le type histologique adénocarcinome, le taux
élevé de mutation de l'EGFR et le non tabagisme sont liés
au cancer du poumon non à petites cellules chez la femme.
Par ailleurs, dans notre étude, la mutation EGFR la
plus fréquente était dans l'exon 19 (69.2%). Cette distribution
est similaire à celle obtenue dans d'autre séries (Casablanca :
64.7%, Italie : 55.5%, Malaisie : 58.8%) (Tableau 11). Les mutations les plus
courantes associées à la

38
sensibilité aux ITK de l'EGFR comprennent la mutation
de l'exon 19 et la mutation ponctuelle L858R dans l'exon 21 [51]. Dans notre
étude, ces deux mutations représentaient 100% de toutes les
mutations de l'EGFR vue que les mutations de l'exon 18 et 20 étaient
absentes.
Tableau 11: Caractéristiques cliniques
et localisations des mutations de l'EGFR chez les patientes EGFR muté de
notre étude et de celles de séries de la littérature
|
Pays
|
n
|
Age moyen (extrêmes)
|
N F
(%)
|
ADK
(%)
|
Exon19 n (%)
|
Exon21 n (%)
|
Année
|
Références
|
|
Maroc-Tanger
|
13
|
58 (36-72)
|
100
|
100
|
9 (69.2)
|
4 (30.8)
|
2024
|
Cette étude
|
|
Maroc-Casablanca
|
17
|
55.8 (33-69)
|
88.2
|
100
|
11 (64.7)
|
4 (23.5)
|
2019
|
[53]
|
|
Jordanie
|
12
|
56.6 (47-78)
|
83.3
|
100
|
4 (33.3)
|
7 (58.3)
|
2016
|
[61]
|
|
Italie
|
9
|
|
|
|
5 (55.5)
|
2 (22.2)
|
2007
|
[29]
|
|
Portugal
|
25
|
|
88
|
80
|
11 (44)
|
7 (28)
|
2013
|
[62]
|
|
Malaisie
|
211
|
|
|
100
|
124 (58.8)
|
77 (36.5)
|
2013
|
[28]
|
|
Taiwan
|
20
|
62. (40-82)
|
95.2
|
100
|
4 (20)
|
14 (70)
|
2004
|
[60]
|
NF: Non fumeuses ADK: Adénocarcinome
La mutation ALK qui a été recherchée chez
8 patientes était positive chez une patiente (12.5%). La
fréquence de la mutation ALK est peu étudiée à
l'échelle nationale. Dans une étude réalisée
à Rabat [21] cette mutation a été recherchée chez
28 femmes et était négative chez toutes ces dernières.
L'utilisation d'inhibiteurs de l'ALK chez les patients atteints de CPNPC
présentant une mutation de l'ALK a démontré un taux de
réponse et une survie sans progression impressionnants par rapport
à la chimiothérapie [63]. Dans notre série, le pourcentage
des femmes testées pour la recherche de la mutation ALK était
faible (10,4%), hors il est recommandé d'élargir cette recherche
étant donné que la détermination de la mutation ALK est un
facteur décisif dans la démarche thérapeutique dans le cas
du CPNPC [21]. Par ailleurs dans notre étude, la mutation ALK
était présente chez une patiente (stade IA-2) qui était
EGFR négative indiquant l'absence de la concomitance des mutations EGFR
et ALK dans notre cas.
6. Prise en charge thérapeutique et survie
Le traitement du cancer du poumon non à petites
cellules comprend diverses approches, telles que la chirurgie, la
chimiothérapie, la radiothérapie, les thérapies
ciblées et l'immunothérapie.

39

40
Ces traitements sont déterminés en fonction de
la stadification du cancer et de l'état général des
patients. Dans notre étude, les stades observés incluaient le
stade IA-2, les stades IIIA et IIIB, ainsi que les stades IVA et IVB.
Pour les patients au stade I, la chirurgie est le traitement
de base. Après une résection chirurgicale, le taux de survie sans
maladie à 5 ans est d'environ 60 % et le taux de survie globale à
5 ans atteint environ 80 % [64]. Dans notre série, une seule patiente
était au stade IA-2 et a été adressée à la
chirurgie.
Les patients au stade IIIA et IIIB non éligibles
à la chirurgie reçoivent habituellement une
radiochimiothérapie concomitante (RCC) qui est considérée
comme le traitement de référence [65]. Dans notre étude,
trois patientes au stade IIIB avaient reçu une chimiothérapie
néoadjuvante suivie d'une RCC vu qu'elles étaient non
résécables malgré un PS 1.
Pour les stades IV, la chimiothérapie de
première ligne consiste en une combinaison de sels de platine et d'une
drogue de troisième génération (gemcitabine, paclitaxel,
docetaxel, irinotécan, vinorelbine) pour les patients PS 0-1. Pour ceux
avec un PS 2, une monothérapie ou une combinaison sans platine est
recommandée, tandis que les patients avec un PS 3 nécessitent des
soins palliatifs [66]. Dans notre série, 54 patientes au stade IV
avaient reçu un traitement systémique de première ligne,
dont 46 une chimiothérapie à base de sels de platine (5 EGFR
muté, 10 non mutées pour l'EGFR et 31 non diagnostiquées
pour la mutation de l'EGFR) et 8 EGFR muté étaient
traitées par des ITK de l'EGFR (erlotinib ou gefitinib). Parmi les 46
patientes ayant reçu la chimiothérapie par les sels de platine,
28 avaient un PS 0-1, 14 un PS 2 et 4 un PS 3. Parmi les 8 patientes
traitées par les ITK de l'EGFR, 7 avaient reçu de l'erlotinib
(dont 6 avaient un PS 1 et 1 un PS 2) et 1 patiente (PS 0) était
traitée par le gefitinib.
La radiothérapie palliative vise à
atténuer la douleur ou à soulager les symptômes de la
maladie. Dans notre série, 29,9 % des patientes ont
bénéficié de cette modalité thérapeutique,
comparativement à 17,7 % dans la série de Debieuvre [67] et 22 %
dans celle de Radzikowska [68].
La survie globale (SG) médiane et la survie sans
progression (SSP) médiane des patientes de notre série
étaient de 5 mois. Le taux de survie globale à 12 mois
était de 28.7%. Ce taux est légèrement inférieur
à ceux obtenus dans les études réalisées à
Rabat (32.3%) [15] et au Brésil (34.5%) [69].
Pour évaluer les différences de réponse
à la chimiothérapie, Albain et al. [70] avaient constaté
que les femmes traitées avec des sels de platine survivaient plus
longtemps, avec un risque de décès réduit de 14 %,
différence notable chez les femmes de 60 ans et plus. De même
Wakelee et al. [71] avaient comparé des patients de sexes féminin
et masculin dans l'essai de l'Eastern Cooperative Oncology Group et avaient
constaté que la survie médiane globale était
significativement plus longue chez les femmes (9.2 mois contre 7.3 mois).
Wheatley-Price et al. [72] avaient regroupé cinq essais cliniques de
phase III et avaient rapporté que les femmes répondaient mieux
à la chimiothérapie à base de sels de platine avec une
survie plus longue que les hommes (9.6 mois contre 8.6 mois), cette observation
était spécifique aux patientes présentant un
adénocarcinome.
En deuxième ligne, une monothérapie (docetaxel,
pemetrexed) ou des inhibiteurs de tyrosine kinase (erlotinib) sont
utilisés [66]. Dans notre série, 20 patientes avaient reçu
un traitement systémique de deuxième ligne. 85 % avaient
reçu la chimiothérapie (dont la majorité une
monothérapie) et 15 % de l'erlotinib. Plusieurs études ont
montré que le sexe féminin était prédictif d'une
meilleure réponse aux ITK de l'EGFR (gefitinib ou erlotinib), notamment
chez les patientes atteintes de CPNPC. Les études IDEAL 1 et IDEAL 2 ont
démontré que le sexe féminin, l'adénocarcinome et
le non tabagisme étaient des prédicteurs de meilleures
réponses [73, 74].
Les inhibiteurs de la tyrosine kinase de l'EGFR ont
montré une plus grande efficacité par rapport à la
chimiothérapie, de ce fait ces derniers sont devenus le traitement de
première ligne pour les cancers du poumon non à petites cellules
avec mutation de l'EGFR, améliorant notablement la prise en charge des
patients.
Dans l'étude ENSURE ayant examiné 217 patients
dont de 61% de femmes avec CPNPC EGFR muté au stade IIIB/IV, comparant
l'erlotinib à un doublet de cisplatine, la SSP médiane
était de 11 mois dans le groupe erlotinib contre 5.5 mois dans le groupe
chimiothérapie [75].
L'essai EURTAC [76] en Europe consacré aux patients
atteints de CPNPC EGFR muté dont 72.4% de sexe féminin, a
comparé l'erlotinib à une chimiothérapie à base de
platine en première ligne métastatique. Les résultats ont
révélé une SSP de 5.2 mois dans le bras
chimiothérapie à base de platine contre 9.7 mois dans le bras
erlotinib. Le taux de réponse était de 10.5 % sous
chimiothérapie contre 54.5 % sous erlotinib, et la médiane de
survie globale était de 18.8 mois pour la chimiothérapie
comparée à 22.9 mois pour l'erlotinib.

41
Dans notre étude, la SSP médiane était
significativement plus longue dans le groupe des patientes EGFR muté
ayant reçu une thérapie anti-EGFR (19 mois) par rapport au groupe
des patientes EGFR muté recevant la chimiothérapie à base
de sels de platine (5 mois). Cette SSP s'approche de celles obtenues en chine
et en Corée dans lesquels les SSP médianes des patients femmes
traitées par les ITK de l'EGFR étaient de 17.8 et 15.8 mois
respectivement mais elle est supérieure à celles obtenues en
Asie, Hongrie, Turquie et Lettonie et en Italie (14, 13.2 et 11.4 mois
respectivement) (Tableau 12) et cela malgré la taille restreinte de
notre série de patientes. De même, la SG médiane
était significativement plus longue pour les patientes EGFR muté
traitées avec une thérapie anti-EGFR (erlotinib ou gefitinib) (20
mois) comparativement à celles des patientes mutées pour l'EGFR
ayant reçu une chimiothérapie à base de sels de platine (9
mois). Cette SG médiane est inférieure à celle obtenue en
Coré (30.3 mois) mais bien supérieure à celles
rapportées en Asie (12 mois) et dans les pays bas (12.4 mois) (Tableau
12).
Tableau 12: Comparaison de séries de
la littérature rapportant la SSP médiane et la SG médiane
chez les femmes atteintes de CPNPC EGFR muté traitées en
première ligne par les ITK de l'EGFR
|
Pays
|
Stades
|
Patientes
|
SSP m
|
SG m
|
Références
|
|
|
(n)
|
(mois)
|
(mois)
|
|
|
Maroc-Tanger
|
IV
|
8
|
19
|
20
|
Cette étude
|
|
Italie
|
IIIB-IV
|
39
|
11.4
|
NR
|
[77]
|
Corée
|
IV
|
2572
|
15.8
|
30.3
|
[78]
|
Pays bas
|
IV
|
9885
|
NR
|
12.4
|
[79]
|
Chine
|
IIIB-IV
|
79
|
17.8
|
NR
|
[80]
|
Asie
|
IV
|
3029
|
14
|
12
|
[81]
|
Hongrie, Turquie,
|
IV
|
49
|
13.2
|
NR
|
[82]
|
|
|
Lettonie
|
|
|
|
|
|
SSP m : Survie sans progression médiane. SG m: Survie
globale médiane. N R : Non rapporté

42
Conclusion

43
V. Conclusion
Le cancer du poumon chez la femme est un complexe
hétérogène, constituant une affection à part
entière. C'est une pathologie peu comprise et peu connue par la
population qui ne cesse de croitre durant ces dernières
années.
Dans notre étude, le cancer du poumon non à
petites cellules a été diagnostiqué chez un nombre non
négligeable de femmes. Il représentait 24,4% des CPNPC totaux et
89,5% des cancers du poumon chez la femme.
Le tabagisme ne constituait pas un facteur de risque chez nos
patientes, en effet celles-ci étaient toutes non fumeuses. D'autres
facteurs d'ordre hormonal, génétique et moléculaires
seraient responsables du CPNPC chez les patientes de notre étude.
L'adénocarcinome était le type histologique
majoritaire (87%) et près de 91 % des CPNPC chez les femmes de notre
série étaient diagnostiqués à un stade
avancé (stade IV) non éligible à la chirurgie justifiant
la nécessité d'instaurer un programme efficace de
prévention contre ce cancer incluant les femmes et de faciliter à
ces dernières l'accès aux moyens de dépistage
précoce.
Seul un tiers des patientes de notre série avaient
réalisé des tests moléculaires. Chez celles-ci une
fréquence élevée de mutations de l'EGFR (48,1%) a
été enregistrée. Les patientes EGFR muté
étaient toutes non fumeuses et avaient toutes un adénocarcinome
non à petites cellules révélant ainsi que le non tabagisme
et le type histologique adénocarcinome sont de bons prédicteurs
des mutations de l'EGFR chez ces patientes.
La thérapie ciblée par les Inhibiteurs de la
Tyrosine Kinase de l'EGFR avait bien démontré chez les patientes
EGFR muté étudiées, sa grande efficacité sur la
survie sans progression médiane et avait également
confirmé son important bénéfice pour la survie globale
médiane de ces patientes indiquant un gain de survie de 11 mois par
rapport à la chimiothérapie par sels de platine.
Ainsi les résultats de notre étude nous incitent
fortement à réaliser les tests de mutations de l'EGFR chez la
totalité des femmes diagnostiquées pour un adénocarcinome
pulmonaire non à petites cellules pour détecter ces mutations et
faire bénéficier ces patientes d'un protocole
thérapeutique adéquat par les ITK de l'EGFR afin
d'améliorer leur survie.

44
Références Bibliographiques

45
VI. Références Bibliographiques
1. Ferlay, J., Soerjomataram, I., Dikshit, R., Eser, S.,
Mathers, C., Rebelo, M., Parkin, D.M., Forman, D., Bray, F. (2015). Cancer
incidence and mortality worldwide: sources, methods and major patterns in
GLOBOCAN 2012. International journal of cancer. 136(5): E359-86. doi:
10.1002/ijc.29210.
2. Sung, H., Ferlay, J., Siegel, R.L, Laversanne, M.,
Soerjomataram, I., Jemal, A., Bray, F. (2021). Global Cancer Statistics 2020:
GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185
Countries. CA Cancer J Clin. 71(3):209-249. doi: 10.3322/caac.21660.
3. Youlden, D.R., Cramb, S.M., Baade, P.D. (2008). The
International Epidemiology of Lung Cancer: geographical distribution and
secular trends. Journal of thoracic oncology. 3(8) :819- 31.
doi:10.1097/JTO.0b013e31818020eb
4. Bray, F., Ferlay, J., Soerjomataram, I., Siegel, R. L.,
Torre, L. A., & Jemal, A. (2018). Global Cancer Statistics 2018: GLOBOCAN
Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries.
CA: A Cancer Journal for Clinicians. 68:394-424. doi:10.3322/caac.21492
5. Ben Abdelaziz, A., Melki, S., Nouira, S., Ben Abdelaziz,
A., Khelil, M., Azzaza, M., Mokni, M. (2019). Cancers in the Central Maghreb:
epidemiology from 1990 to 2017 and trends in 2040. Tunis Med. 97(6)
:739-770.
6. Travis, W.D., Brambilla, E., Noguchi, M., Nicholson, A.G.,
Geisinger, K., Yatabe, Y., Ishikawa, Y., Wistuba, I., Flieder, D.B., Franklin,
W., Gazdar, A., Hasleton, P.S., Henderson, D.W., Kerr, K.M., Petersen, I.,
Roggli, V., Thunnissen, E., Tsao, M. (2013). Diagnosis of lung cancer in small
biopsies and cytology: implications of the 2011 International Association for
the Study of Lung Cancer/American Thoracic Society/European Respiratory Society
classification. Archives of Pathology and Laboratory Medicine.137(5) :668-84.
doi: 10.5858/arpa.2012-0263-RA.
7. Kamangar, F., Dores, G.M., Anderson, W.F. (2006). Patterns
of Cancer Incidence, Mortality, and Prevalence Across Five Continents: Defining
Priorities to Reduce Cancer Disparities in Different Geographic Regions of the
World. Journal of Clinical Oncology, 24(14): 2137-2150.
doi:10.1200/jco.2005.05.2308
8. Quoix, E., Lemarié, E. (2011).
Épidémiologie du cancer bronchique primitif: aspects classiques
et nouveautés. 28(8) : 1048-1058. doi:10.1016/j.rmr.2010.12.015
9. Barrera-Rodriguez, R., Morales-Fuentes, J. (2012). Lung
cancer in women. Lung Cancer: Targets and Therapy. 3: 79-89.
doi:10.2147/LCTT.S37319
10.Khouchani, M., Selmaji, I., Elmorabit, B.,
Ismaili, N., Elomrani, A., Belbaraka, R., Tahri, A. (2013). Female lung cancer
in Marrakech. Clinical Cancer Investigation Journal, 2(2): 128131.
https://doi.org/10.4103/2278-0513.113635
11. Chhikara, B. S., Parang, K. (2023). Global
Cancer Statistics 2022: The Trends Projection Analysis. Chemical Biology
Letters. 10(1): 451.
https://pubs.thesciencein.org/journal/index.php/cbl/article/view/451
12. Barta, J.A., Powell, C.A., Wisnivesky, J.P. (2019) Global
Epidemiology of Lung Cancer. Annals of Global Health. 85(1): 1-16. DOI:
https://doi.org/10.5334/aogh.2419
13.

46
Haimer, A., Belamalem, S., Habib, F., Mokhtari, A.,
Soulaymani, A., Hami, H. (2019). Epidemiology and Risk Factor of Lung Cancer in
Morocco. Biosciences Biotechnology Research Asia. 16(1): 55-59.
http://dx.doi.org/10.13005/bbra/2720
14. Erefai, O., Soulaymani, A., Mokhtari, A., Hami, H.
(2022). Clinical and histopathological pattern of lung cancer in Morocco. Pan
Afr Med J. 42:283. doi: 10.11604/pamj.2022.42.283.35593.
15. Lachgar, A., Tazi, M.A., Afif, M., Er-Raki, A., Kebdani,
T., Benjaafar, N. (2016). Lung cancer: Incidence and survival in Rabat,
Morocco. Rev Epidemiol Sante Publique. 64(6) :391395. doi:
10.1016/j.respe.2016.02.012.
16. Tafenzi, H.A., Choulli, F., Baladi, A., Essaadi, I.,
Belbaraka, R. (2023). Lung cancer in middle and southern Morocco.
Ecancermedicalscience. 17:1518. doi: 10.3332/ecancer.2023.1518.
17. Belmokhtar, K.Y., Tajir, M., Boulouiz, R., Bennani, A.,
Brahmi, S.A., Alloubi, I., Kouismi, H., Kamaoui, I., Skiker, I., Afqir, S.,
Abda, N., Bellaoui, M., Mezouar, L. (2019). Cancer du poumon au Maroc Oriental
: où en sommes-nous ? [Lung cancer in Eastern Morocco: where do we
stand?]. Pan Afr Med J. 34:177. doi: 10.11604/pamj.2019.34.177.19934.
18. Cadelis, G., Kaddah, S., Bhakkan, B., Quellery, M.,
Deloumeaux, J. (2013). Épidémiologie et incidence du cancer
bronchique primitif dans une région à faible consommation
tabagique : la Guadeloupe. Données 2008-2009 du registre des cancers.
Revue Des Maladies Respiratoires. 30(7) : 537-548.
doi:10.1016/j.rmr.2013.01.010
19. Costa, G. J., Telles da Silva, G., Ferreira, C. G.,
Gonçalves de Mello, M. J., Bergmann, A., & Santos Thuler, L. C.
(2020). Brazilian women with lung cancer have a higher overall survival than
their male equivalents: a cohort study. Clinical Lung Cancer. 22(3): e313-e319.
doi:10.1016/j.cllc.2020.05.022
20. Fu, Y., Liu, J., Chen, Y., Liu, Z., Xia, H., Xu H. 2023).
Gender disparities in lung cancer
incidence in the United States during 2001-2019. Sci Rep
13, 12581.
https://doi.org/10.1038/s41598-023-39440-8
21. El yacoubi, H., Sow, M. L., Kettani, F., Gamra, L.,
Mestari, A., Jabri, L., Elghissassi, I., Errihani, H. (2020). Frequency of
anaplastic lymphoma kinase rearrangements in Moroccan patients with non-small
cell lung cancer: a multi-institutional national retrospective study. BMC
Cancer. 20(1): 479-. doi :10.1186/s12885-020-06973-4
22. Lemine Sow, M., El Yacoubi, H., Moukafih, B., Balde, S.,
Akimana, G., Najem, S., El Khoyaali, S., Abahssain, H., Chaibi, A., Zeb Khan,
S., Trapani, D., Benzekri, A., Ghaouti, M., Gamra, L., Mestari, A., Kettani,
F., Rahali, Y., Mrabti, H., Elghissassi, I., Errihani, H. (2020). Frequency and
types of EGFR mutations in Moroccan patients with non-small cell lung cancer.
Tumori.107(4):335-340. doi: 10.1177/0300891620964571.
23. Nouiakh, L., Oualla, K., Atassi, M., Ouafki, I., Berrad,
S., Erraichi, H., Amaadour, L., Benbrahim, Z., Arifi, S., El Fakir, S. and
Mellas, N. (2021). Prognostic Factors Influencing the Survival of Patients with
Metastatic Non-Small Cell Lung Cancer in the Moroccan Population: Retrospective
Study of 405 Cases. Advances in Lung Cancer. 10: 1-10.
https://doi.org/10.4236/alc.2021.101001
24. Amaadour, L., Boudahna, L., Benbrahim, Z., Arifi, S.,
Mellas, N. (2015). SEX differences in presentation, management and prognosis of
moroccan patients with non-small cell lung

47
carcinoma: a retrospective analysis of 224 cases. Annals of
Oncology. 26 (Supplement 1): i6- i9. doi:10.1093/annonc/mdv044.8
25. Demiray, A., Yaren, A., Karagenç, N., Bir, F.,
Demiray, Ag., Karagür, Er., Tokgün, O., Elmas, L., Akça, H.
(2018). The Frequency of EGFR and KRAS Mutations in the Turkish Population with
Non-small Cell Lung Cancer and their Response to Erlotinib Therapy. Balkan J
Med Genet. 21(2) : 21-26. doi: 10.2478/bjmg-2018-0022.
26. Moreau, D., Huchot, E., Allou, N., Gazaille, V., Chirpaz,
E., Saint Paul, A., André, M. (2020). Profils moléculaires des
cancers bronchiques non à petites cellules à la Réunion.
Revue Des Maladies Respiratoires Actualités, 12(1) : 116-117. doi:
10.1016/j.rmra.2019.11.245.
27. Sutandyo N, Suratman E. (2018). Non-Small Cell Lung
Carcinoma in Women: A Retrospective Cohort Study in Indonesia. Acta Med
Indones. 50(4) :291-298.
28. Liam, C.K., Leow, H.R., How, S.H., Pang, Y.K., Chua,
K.T., Lim, B.K., Lai, N.L., Kuan, Y.C., Pailoor, J., Rajadurai, P. (2014).
Epidermal growth factor receptor mutations in non-small cell lung cancers in a
multiethnic malaysian patient population. Asian Pac J Cancer Prev. 15(1):321-6.
doi: 10.7314/apjcp.2014.15.1.321.
29. Baldini, E., Melfi, F., Boldrini, L., Doria, S.,
Pennucci, C., Tibaldi, C., Gisfredi, S., Ursino S., Orlandini, C., Fontanini,
G. (2007). Non-small-cell lung cancer in women: clinical and molecular aspects.
Journal of Thoracic Oncology. 2(8): S743. doi:
10.1097/01.jto.0000284124.89325.a6.
30. de Perrot, M., Licker, M., Bouchardy, C., Usel, M.,
Robert, J., Spiliopoulos, A. (2000). Sex differences in presentation,
management, and prognosis of patients with non-small cell lung carcinoma. The
Journal of Thoracic and Cardiovascular Surgery. 119(1):21-26.
doi:10.1016/s0022-5223(00)70213-3.
31. Zakkouri, F. A., Saloua, O., Halima, A., Rachid, R.,
Hind, M., Hassan, E. (2015). Smoking, passive smoking and lung cancer cell
types among women in Morocco: analysis of epidemiological profiling of 101
cases. BMC Research Notes. 8:530. doi:10.1186/s13104-015-1503-3.
32. Sisti, J., Boffetta, P. (2012). What proportion of lung
cancer in never-smokers can be attributed to known risk factors? International
Journal of Cancer. 131(2): 265- 275. doi:10.1002/ijc.27477.
33. Charloux, A., Quoix, E., Pauli, G. (1996). Tabagisme
passif et cancer bronchique: un lien difficile à établir [Passive
smoking and bronchial cancer: a difficult relation to establish]. Rev Pneumol
Clin. 52(4):227-34.
34. Brownson, R. C., Alavanja, M. C., Hock, E. T., Loy, T. S.
(1992). Passive smoking and lung cancer in nonsmoking women. American Journal
of Public Health. 82(11):1525-1530. doi:10.2105/ajph.82.11.1525.
35. Shiels, M. S., Albanes, D., Virtamo, J., Engels, E. A.
(2011). Increased Risk of Lung Cancer in Men with Tuberculosis in the
Alpha-Tocopherol, Beta-Carotene Cancer Prevention Study. Cancer Epidemiology
Biomarkers & Prevention. 20(4): 672-678.
doi:10.1158/1055-9965.epi-10-1166.
36. Tsai, L.L., Chu, N.Q., Blessing, W.A., Moonsamy, P.,
Colson, Y.L. (2022). Lung Cancer in Women. Ann Thorac Surg. 14(5):1965-1973.
doi: 10.1016/j.athoracsur.2021.09.060.
37.

48
Coté, M.L., Liu, M., Bonassi, S., Neri, M., Schwartz,
A.G., Christiani, D.C., Spitz, M.R., Muscat JE, Rennert G, Aben KK, Andrew AS,
Bencko V, Bickeböller H, Boffetta P, Brennan P, Brenner H, Duell EJ,
Fabianova E, Field JK, Foretova L, Friis S, Harris CC, Holcatova I, Hong YC,
Isla D, Janout V, Kiemeney LA, Kiyohara C, Lan Q, Lazarus P, Lissowska J, Le
Marchand L, Mates D, Matsuo K, Mayordomo JI, McLaughlin JR, Morgenstern H,
Müeller H, Orlow I, Park BJ, Pinchev M, Raji OY, Rennert HS, Rudnai P,
Seow A, Stucker I, Szeszenia-Dabrowska N, Dawn Teare M, Tjønnelan A,
Ugolini D, van der Heijden HF, Wichmann E, Wiencke JK, Woll PJ, Yang P, Zaridze
D, Zhang ZF, Etzel CJ, Hung RJ. (2012). Increased risk of lung cancer in
individuals with a family history of the disease: a pooled analysis from the
International Lung Cancer Consortium. Eur J Cancer. 48(13):1957-68. doi:
10.1016/j.ejca.2012.01.038
38. Amro, L. (2018). Cancer bronchique primitif : à
propos de 173 cas. Thèse pour obtention de doctorat en médecine,
Faculté de médecine et de pharmacie- Marrakech. Université
Kadi Ayyad, N°077/18.
39. Eolyn, K. Y. (2005). Problématique du cancer
broncho-pulmonaire primitif dans le service de pneumologie de l'hôpital
du point G. Thèse de médecine. Faculté de médecine
de Bamako. Mali.
40. Palomares, M. R., Sayre, J. W., Shekar, K. C.,
Lillington, L. M., Chlebowski, R. T. (1996). Gender influence on weight-loss
pattern and survival of non-small cell lung carcinoma patients.
Cancer.78(10):2119-2126.
https://doi.org/10.1002/(sici)10970142(19961115)78:
10%3119::aid-
cncr12%3E3.0.co;2-1
41. Ouarssani, A. (2016). Le cancer bronchique primitif :
à propos d 228 cas, Expérience du service de pneumologie de
l'hôpital militaire Molay Ismail de Meknès. Thèse de
doctorat en médecine, Faculté de médecine de et de
pharmacie. Fès, 2016, N°135/16.
42. Collisson, E. A., Campbell, J. D., Brooks, A. N., Berger,
A. H., Lee, W., Chmielecki, J., Danilova, L. (2014). Cancer Genome Atlas
Research Network. Comprehensive molecular profiling of lung adenocarcinoma.
Nature. 511(7511):543-550.doi:10.1038/nature13385
43. Belani, C. P., Marts, S., Schiller, J., Socinski, M. A.
(2007). Women and lung cancer: Epidemiology, tumor biology, and emerging trends
in clinical research. Lung Cancer. 55(1):15-23.
doi:10.1016/j.lungcan.2006.09.00
44. Liu, N. S., Spitz, M. R., Kemp, B. L., Cooksley, C.,
Fossella, F. V., Lee, J. S., Hong WK, Khuri, F. R. (2000). Adenocarcinoma of
the lung in young patients. Cancer. 88(8):1837- 1841.
doi:10.1002/(sici)1097-0142(20000415)88:8<1837::aid-cncr12>3.0.co;2-e
45. Bennett, W. P., Alavanja, M. C. R., Blomeke, B.,
Vahakangas, K. H., Castren, K., Welsh, J. A., Bowman, E.D., Khan, M.A.,
Flieder, D.B., Harris, C. C. (1999). Environmental Tobacco Smoke, Genetic
Susceptibility, and Risk of Lung Cancer in Never-Smoking Women. JNCI Journal of
the National Cancer Institute. 91(23):2009-2014. doi:101093/jnci/91.23.2009
46. Sun, S., Schiller, J. H., Gazdar, A. F. (2007). Lung
cancer in never smokers -- a different disease. Nature Reviews Cancer.
7(10):778-790. doi:10.1038/nrc2190
47. Defaa, L. (2021). Aspects épidémiologiques,
diagnostiques, thérapeutiques et évolutifs du cancer bronchique
non à petites cellules Thèse de médecine et de pharmacie
de Rabat. Université Mohamed V.
48. Alaoui-Yazidi, A., Amro, L. Sajiai, H. (2013). Profil
épidémiologique, clinique,

49
anatomopathologique et thérapeutique du cancer
bronchique au Maroc (expérience Marrakech). J Afr Cancer. 5:88-93.
https://doi.org/10.1007/s12558-013-0255-z
49. Moussoki, P.G. (2014). Etude descriptive et comparative
des 63 patients de l'année 2010 et des 45 patients de l'année
2000 atteints de cancer bronchique primitif au centre hospitalier de
Périgueux. Thèse de médecine 2014. Université de
Bordeaux. ffdumas-01096562f
50. Grivaux, M., Breton, J. L., Bombaron, P., Kuntz, P.,
Lebas, F. X., Mehdaoui, A., Herman, D., David, P., Berruchon, J., Delclaux, B.,
Zureik, M., Blanchon, F. (2004). Lung cancer among women in France. Lung
Cancer. 45(3): 279-287.doi:10.1016/j.lungcan.2004.02.01
51. Errihani, H., Inrhaoun, H., Boukir, A., Kettani, F.,
Gamra, L., Mestari, A., Jabri, L., Bensouda, Y., Mrabti, H. Elghissassi, I.
(2013). Frequency and Type of Epidermal Growth Factor Receptor Mutations in
Moroccan Patients with Lung Adenocarcinoma. Journal of Thoracic Oncology.
8(9):1212-1214. doi:10.1097/jto.0b013e31829f6b4a
52. Boustany, Y., Laraqui, A., El Zaitouni, S., Ghaouti, M.,
Benzekri, A., Kettani, F., Oukabli, M., Ennibi, K., Belkadi, B., Sekhsokh, Y.
(2023). Advanced Non-small Cell Lung Cancer: EGFR Mutation Analysis Using
Pyrosequencing and the Fully Automated qPCR-Based IdyllaTM System.
Cancer Control. 30:1-8. doi: 10.1177/10732748231177538
53. Kaanane, H., El Attar, H., Louahabbi, A., Berradi, H.,
Idrissi, H. H., Khyatti, M., Nadifi, S. (2019). Targeted methods for molecular
characterization of EGFR mutational profile in lung cancer Moroccan cohort.
Gene. 705:36-43. doi: 10.1016/j.gene.2019.04.044
54. Fakhruddin, N., Mahfouz, R., Farhat, F., Tfayli, A.,
Abdelkhalik, R., Jabbour, M., Yehia, L., Mahfoud, Z., Zaatari, G. (2014).
Epidermal growth factor receptor and KRAS mutations in lung adenocarcinoma: a
retrospective study of the Lebanese population. Oncol Rep. 32(5):2223-9. doi:
10.3892/or.2014.3406
55. De Mello, R. A., Pires, F. S., Marques, D. S., Oliveira,
J., Rodrigues, A., Soares, M., Azevedo, I., Peixoto, A., Santos, C., Pinto, C.,
Hespanhol, V., Teixeira, M.R., Amaro, T., Queiroga, H., Araújo, A.
(2012). EGFR exon mutation distribution and outcome in non-small-cell lung
cancer: a Portuguese retrospective study. Tumor Biology. 33(6):2061-2068.
doi:10.1007/s13277-012-0465-5
56. Smits, A. J. J., Kummer, J. A., Hinrichs, J. W. J.,
Herder, G. J. M., Scheidel-Jacobse, K. C., Jiwa, N. M., Ruijter, T.E., Nooijen,
P.T., Looijen-Salamon, M.G., Ligtenberg, M.J., Thunnissen, F.B., Heideman,
D.A., de Weger, R.A., Vink, A. (2012). EGFR and KRAS mutations in lung
carcinomas in the Dutch population: increased EGFR mutation frequency in
malignant pleural effusion of lung adenocarcinoma. Cellular Oncology.
35(3):189-196. doi:10.1007/s13402-012-0078-4
57. Bacchi, C.E., Ciol, H., Queiroga, E.M., Benine, L.C.,
Silva, L.H., Ojopi, E.B. (2012). Epidermal growth factor receptor and KRAS
mutations in Brazilian lung cancer patients.. Clinics (Sao Paulo).67(5):419-24.
doi: 10.6061/clinics/2012(05)03
58. Cote, M. L., Haddad, R., Edwards, D. J., Atikukke, G.,
Gadgeel, S., Soubani, A. O., Lonardo, F., Bepler, G., Schwartz, A.G., Ethier,
S. P. (2011). Frequency and Type of Epidermal Growth Factor Receptor Mutations
in African Americans with Non-small Cell Lung Cancer. Journal of Thoracic
Oncology. 6(3):627-630. doi:10.1097/jto.0b013e31820a0ec0
59.

50

51
Zhou, X., Cai, L., Liu, J., Hua, X., Zhang, Y., Zhao, H.,
Wang, B., Li, B., Gai, P. (2018). Analyzing EGFR mutations and their
association with clinicopathological characteristics and prognosis of patients
with lung adenocarcinoma. Oncol Lett. 16(1):362-370. doi:
10.3892/ol.2018.8681
60. Huang, S.-F. (2004). High Frequency of Epidermal Growth
Factor Receptor Mutations with Complex Patterns in Non-Small Cell Lung Cancers
Related to Gefitinib Responsiveness in Taiwan. Clinical Cancer Research.
10(24): 8195-8203. doi:10.1158/1078-0432.ccr-04-1245
61. Obeidat, N., Awidi, A., Ababneh, N., Shomaf, M.,
Al-Adaily, T., Jaber, M., Al-Khateeb, M., Abbasi, S. (2016). Frequency of
epidermal growth factor receptor mutations in Jordanian lung adenocarcinoma
patients at diagnosis. J Cancer Res Ther. 12(2):616-9. doi:
10.4103/09731482.147711.
62. Castro, A. S., Parente, B., Gonçalves, I.,
Antunes, A., Barroso, A., Conde, S., Neves S, J. C. (2013). Estudo da
mutação do recetor do fator de crescimento epidérmico,
durante 5 anos, numa população de doentes com cancro do
pulmão de não pequenas células. Revista Portuguesa de
Pneumologia. 19(1): 7-12. doi:10.1016/j.rppneu.2012.08.002
63. Solomon, B.J, Kim, D.W., Wu, Y.L., Nakagawa, K., Mekhail,
T., Felip, E., Cappuzzo, F., Paolini, J., Usari, T., Tang, Y., Wilner, K.D.,
Blackhall, F., Mok, T.S. (2018). Final Overall Survival Analysis From a Study
Comparing First-Line Crizotinib Versus Chemotherapy in ALK-Mutation-Positive
Non-Small-Cell Lung Cancer. J Clin Oncol. 36(22):2251-2258. doi:
10.1200/JCO.2017.77.4794
64. Altorki N, Wang X, Kozono D, Watt C, Landrenau R, Wigle
D, Port J, Jones DR, Conti M, Ashrafi AS, Liberman M, Yasufuku K, Yang S,
Mitchell JD, Pass H, Keenan R, Bauer T, Miller D, Kohman LJ, Stinchcombe TE,
Vokes E. (2023). Lobar or Sublobar Resection for Peripheral Stage IA
Non-Small-Cell Lung Cancer. N Engl J Med. 9; 388(6):489-498. doi:
10.1056/NEJMoa2212083.
65. Postmus, P. E., Kerr, K. M., Oudkerk, M., Senan, S.,
Waller, D. A., Vansteenkiste, J. Escriu C, Peters S; (2017). Early and locally
advanced non-small-cell lung cancer (NSCLC): ESMO Clinical Practice Guidelines
for diagnosis, treatment and follow-up†. Annals of Oncology, 28(suppl_4),
iv1-iv21. doi:10.1093/annonc/mdx222
66. Bosquée, L., Frusch, N., Louis, R. (2007). Prise
en charge du cancer pulmonaire non à petites cellules. Rev Med Suisse.3:
1890-5. DOI: 10.53738/REVMED.2007.3.122.1890
67. Debieuvre, D., Locher, C., Neidhardt, A.-C., Goupil, F.,
Lemaire, B., Blanchet-Legens, A.-S., Renaultf, D., Tavernier, J.Y., Tagu, P.,
Mahmoudi, H., Figueredoj, M., Grivaux, M. (2014).Évolution en 10ans du
cancer bronchique non à petites cellules en fonction du sexe.
Résultats de l'étude KBP-2010-CPHG du Collège des
pneumologues des hôpitaux généraux. Revue Des Maladies
Respiratoires. 31(9): 805-816. doi:10.1016/j.rmr.2013.10.644
68. Radzikowska, E., Glaz, P., Roszkowski, K. (2002). Lung
cancer in women: age, smoking, histology, performance status, stage, initial
treatment and survival. Population-based study of 20 561 cases. Annals of
Oncology. 13(7): 1087-1093. doi:10.1093/annonc/mdf187
69. Duarte, R., Monteiro, A., Zamboni, M. (2013). Lung Cancer
in Nonsmoker Women: Clinical and Survival Patterns. Chest. 144(4): 653A.
doi:10.1378/chest.1703770
70. Albain, K.S., Unger, J., Gotay, C.C., Davies, A. M.,
Edelman, M., Herbst, R. S., Kelly, K., Williamson, S., Wozniak, A. J., Gandara,
D. R. (2007). Toxicity and survival by sex in patients
with advanced non-small cell lung carcinoma (NSCLC) on modern
Southwest Oncology Group (SWOG) trials.; Journal of Clinical Oncology. 25 (18
Suppl):7549-7549.
https://doi.org/10.1200/jco.2007.25.18_suppl.7549
71. Wakelee, H. A., Wang, W., Schiller, J.
H., Langer, C. J., Sandler, A. B., Belani, C. P., Johnson, D. H. (2006).
Survival Differences by Sex for Patients with Advanced Non-small Cell Lung
Cancer on Eastern Cooperative Oncology Group Trial 1594. Journal of Thoracic
Oncology. 1(5): 441-446. doi:10.1016/s1556-0864(15)31609-9
72.Wheatley-Price, P., Blackhall, F., Lee,
S.-M., Ma, C., Ashcroft, L., Jitlal, M., Qian W. Hackshaw A, Rudd R., Booton
R., Danson S., Lorigan P, Thatcher N. Shepherd, F. A. (2010). The influence of
sex and histology on outcomes in non-small-cell lung cancer: a pooled analysis
of five randomized trials. Annals of Oncolog., 21(10): 2023-2028.
doi:10.1093/annonc/mdq067
73. Fukuoka, M., Yano, S., Giaccone, G., Tamura, T.,
Nakagawa, K., Douillard, J.-Y., Nishiwaki, Y., Vansteenkiste, J., Kudoh, S.,
Rischin, D., Eek, R., Horai, T., Noda, K., Takata, I., Smit, E., Averbuch, S.,
Macleod, A., Feyereislova, A., Dong, R.P., Baselga, J. (2003).
Multi-Institutional Randomized Phase II Trial of Gefitinib for Previously
Treated Patients With Advanced Non-Small-Cell Lung Cancer. Journal of Clinical
Oncology. 21(12): 2237- 2246. doi:10.1200/jco.2003.10.038 . Erratum in: J Clin
Oncol. 2004 Dec 1;22(23):4863. Corrected and republished in: J Clin Oncol. 2023
Feb 20;41(6):1162-1171.
74. Kris, M. G., Natale, R. B., Herbst, R. S., Lynch, Jr, T.
J., Prager, D., Belani, C. P., Schiller, J.H., Kelly, K., Spiridonidis, H.,
Sandler, A., Albain, K.S., Cella, D., Wolf, M.K., Averbuch, S.D., Ochs, J.J.,
Kay, A. C. (2003). Efficacy of Gefitinib, an Inhibitor of the Epidermal Growth
Factor Receptor Tyrosine Kinase, in Symptomatic Patients With Non-Small Cell
Lung Cancer. JAMA. 290(16): 2149-2158. doi:10.1001/jama.290.16.2149
75. Wu, Y.-L., Zhou, C., Liam, C.-K., Wu, G., Liu, X., Zhong,
Z., Lu S., Cheng Y., Han B., Chen, L.., Huang, C.., Qin, S., Zhu Y., Pan H.,
Liang H., Li E., Jiang G., How, S. H., Fernando, M. C. L., Zhang, Y,. Xia F.,
Zuo, Y. (2015). First-line erlotinib versus gemcitabine/cisplatin in patients
with advanced EGFR mutation-positive non-small-cell lung cancer: analyses from
the phase III, randomized, open-label, ENSURE study. Annals of Oncology. 26(9):
1883-1889. doi:10.1093/annonc/mdv270
76. Rosell, R., Carcereny, E., Gervais, R., Vergnenegre, A.,
Massuti, B., Felip, E., Palmero, R., Garcia-Gomez, R., Pallares, C., Sanchez,
J.M., Porta, R., Cobo, M., Garrido, P., Longo, F., Moran, T., Insa, A., De
Marinis, F., Corre, R., Bover, I., Illiano, A., Dansin, E., de Castro, J.,
Milella, M., Reguart, N., Altavilla, G., Jimenez, U., Provencio, M., Moreno,
MA., Terrasa, J., Muñoz-Langa, J., Valdivia J, Isla D, Domine M,
Molinier O, Mazieres J, Baize N, Garcia-Campelo R, Robinet G, Rodriguez-Abreu
D, Lopez-Vivanco G, Gebbia V, Ferrera-Delgado L, Bombaron P, Bernabe R, Bearz
A, Artal A, Cortesi E, Rolfo C, Sanchez-Ronco M, Drozdowskyj A, Queralt C, de
Aguirre I, Ramirez JL, Sanchez JJ, Molina MA, Taron M, Paz-Ares L (2012).
Erlotinib versus standard chemotherapy as first-line treatment for European
patients with advanced EGFR mutation-positive non-small-cell lung cancer
(EURTAC): a doi:10.1016/s1470-2045(11)70393-x
77.Rotella, V., Fornaro, L., Vasile, E.,
Tibaldi, C., Boldrini, L., Chella, A., D'Incecco, A., Cirigliano, G., Chioni,
A., Lupi, C., Sensi, E., Ginocchi, L., Giovannelli, S., Pennucci, M.C.,
Fontanini, G., Baldini, E. (2014). EGFR and K-Ras mutations in women with lung
adenocarcinoma: implications for treatment strategy definition. J Exp Clin
Cancer Res. 33(1):77. doi: 10.1186/s13046-014-0077-6.
78.

52
Kwon, B.S., Park, J.H., Kim, S., Park, S., Ji, W., Kim, W.S.,
Lee, J.C., Park, Y.R., Choi, C.M. (2019). Survival benefit of first-generation
epidermal growth factor receptor-tyrosine kinase inhibitors in female with
advanced lung cancer. Tumori. 105(3):216-224. doi: 10.1177/0300891619839292.
79. Ten Berge, D.M.H.J., Aarts, M.J., Groen, H.J.M., Aerts,
J.G.J.V., Kloover, J.S. (2022). A population-based study describing
characteristics, survival and the effect of TKI treatment on patients with EGFR
mutated stage IV NSCLC in the Netherlands. Eur J Cancer. 165:195-204. doi:
10.1016/j.ejca.2022.01.038.
80. Cui, S., Xiong, L., Lou, Y., Shi, H., Gu, A., Zhao, Y.,
Chu, T., Wang, H., Zhang, W., Dong, L., Jiang, L. (2016). Clinical model to
predict progression-free survival in EGFR-mutant lung adenocarcinoma patients
treated with first-generation EGFR-TKIs. Transl Cancer Res. 5(4):476-485.
10.21037/ tcr.2016.07.08
81. Becker, D.J., Wisnivesky, J.P., Grossbard, M.L.,
Chachoua, A., Camidge, D.R., Levy, B.P. (2017). Survival of Asian Females With
Advanced Lung Cancer in the Era of Tyrosine Kinase Inhibitor Therapy. Clin Lung
Cancer. 18(1):e35-e40. doi: 10.1016/j.cllc.2016.08.008.
82. Markóczy, Z., Sárosi, V., Kudaba, I.,
Gálffy, G., Turay, Ü.Y., Demirkazik, A., Purkalne, G., Somfay, A.,
Pápai-Székely, Z., Rásó, E., Ostoros, G. (2018).
Erlotinib as single agent first line treatment in locally advanced or
metastatic activating EGFR mutation-positive lung adenocarcinoma (CEETAC): an
open-label, non-randomized, multicenter, phase IV clinical trial. BMC
Cancer.18(1):598. doi: 10.1186/s12885-018-4283-z.
83. Anonyme ; (2024). AURA-Référentiels en
oncologie thoracique. Cancer Bronchique non à petites cellules.
https://referentiels-aristot.com/129-cancer-bronchique-non-petites-cellules/texte-integral-sur-le-referentiel/.
Consulté le 15/05/2024.
84. Eisenhauer, E.A., Therasse, P., Bogaerts, J., Schwartz,
L.H., Sargent, D., Ford, R., et al.(2009). New response evaluation criteria in
solid tumours: Revised RECIST guideline (version 1.1). European Journal of
Cancer. 45(2):228-47.

53
Annexes
VII. Annexes

54
Annexe 1
Performance status (PS)
0 : Capable d'une activité identique
à celle précédant la maladie.
1 : Activité physique diminuée
mais malade ambulatoire et capable de mener un travail
2 : Malade ambulatoire et capable de prendre
soins de lui-même mais incapable de travailler. Alité ou en chaise
moins de 50% de son temps de veille.
3 : Capable seulement de quelques soins,
alité ou en chaise de plus de 50% de son temps de veille.
4 : Incapable de prendre soins de
lui-même, alité ou en chaise en permanence

55
Annexe 2
1. 8ème classification TNM du cancer du poumon
Tableau 13: 8ème classification TNM du
cancer du poumon [83]
|
T - Tumeur (plus grande dimension)
|
|
Tx
|
Tumeur primitive non connue ou tumeur prouvée par la
présence de cellules malignes dans les sécrétions
broncho-pulmonaires mais non visible aux examens radiologiques et
endoscopiques.
|
|
T0
|
Absence de tumeur identifiable.
|
|
Tis
|
Carcinome in situ.
|
|
T1
|
Tumeur de 3 cm ou moins dans ses plus grandes dimensions,
entourée par du poumon ou de la plèvre viscérale, sans
évidence d'invasion plus proximale que les bronches lobaires à la
bronchoscopie (c'est-à-dire pas dans les bronches souches).
|
|
T1a(mi)
|
Adénocarcinome à invasion minime
|
|
T1a
|
= 1cm
|
|
T1b
|
> 1 cm et = 2 cm
|
|
T1c
|
> 2 cm et = 3 cm
|
|
T2
|
Tumeur de plus de 3 cm, mais de moins de 5 cm OU avec un
quelconque des éléments suivants -envahissement d'une bronche
souche quelle que soit sa distance par rapport à la carène mais
sans envahissement de la carène, -envahissement de la plèvre
viscérale, - existence d'une atélectasie ou pneumonie
obstructive
|
|
T2a
|
> 3 cm mais = 4 cm
|
|
T2b
|
> 4 cm mais = 5 cm
|
|
T3
|
Tumeur de plus de 5 cm et de moins de 7 cm, OU associée
à un(des) nodule(s) tumoral(aux) distinct(s) dans le même lobe, OU
envahissant directement : -la paroi thoracique (incluant les tumeurs du
sommet), -le nerf phrénique, -la plèvre pariétale ou le
péricarde pariétal.
|
|
T4
|
Tumeur de plus de 7 cm ou associée à des nodules
tumoraux séparés dans deux lobes différents du même
poumon, ou envahissant directement : -le médiastin, -le coeur ou les
gros vaisseaux, -la trachée, ou la carène -le diaphragme, -le
nerf récurrent, -l'oesophage, - un(des) corps vertébral(ux).
|
|
N - Adénopathies
|
|
Nx
|
Envahissement locorégional inconnu.
|
|
N0
|
Absence de métastase dans les ganglions lymphatiques
régionaux.
|
|
N1
|
Métastases ganglionnaires péri-bronchiques
homolatérales et/ou hilaires homolatérales incluant une extension
directe.
|
|
N2
|
Métastases dans les ganglions médiastinaux
homolatéraux ou dans les ganglions sous-carénaires
|
|
N3
|
Métastases ganglionnaires médiastinales
controlatérales ou hilaires controlatérales ou
scaléniques, susclaviculaires homo- ou controlatérales.
|
|
Métastases
|
|
M0
|
Pas de métastase à distance.
|
|
M1
|
Existence de métastases :
|
|
M1a
|
Nodule(s) tumoral(ux) séparés dans un lobe
controlatéral, ou nodules pleuraux ou pleurésie maligne ou
péricardite maligne
|
|
M1b
|
Une seule métastase extra-thoracique dans un seul
organe
|
|
M1c
|
Plusieurs métastases extra-thoraciques dans un seul ou
plusieurs organes
|

56
2. Classification par stade
Tableau 14: Classification par stade
(8ème classification TNM du cancer du poumon) [83]
|
Carcinome occulte
|
Tx N0 M0
|
|
|
|
Stade 0
|
Tis N0 M0
|
Stade IIB
|
T1,2 N1 M0 T3 N0 M0
|
|
Stade IA-1
|
T1a(mi) N0 M0 T1a N0 M0
|
Stade IIIA
|
T1,2 N2, M0
T3 N1 M0
T4 N0,1 M0
|
|
Stade IA-2
|
T1b N0 M0
|
Stade IIIB
|
T1,2 N3 M0 T3,4 N2 M0
|
|
Stade IA-3
|
T1c N0 M0
|
Stade IIIC
|
T3,4 N 3 M0
|
|
Stade IB
|
T2a N0 M0
|
Stade IV-A
|
Tout M1a Tout M1b
|
|
Stade IIA
|
T2b N0 M0
|
Stade IV-B
|
Tout M1c
|
Annexe 3
CRITERES RECIST [84]
1. Définitions
· Maladie mesurable :
o =10mm au scanner pour une lésion
non-ganglionnaire mesuré dans sa plus longue dimension (grand axe).
o =15 mm au scanner pour un ganglion
lymphatique mesuré dans son petit axe (perpendiculaire au à la
plus grande dimension).
· Maladie non mesurable :
o Conditions ci-dessus non réunies.
o Lésions réellement non-mesurables : maladie
lepto-méningée, ascite, pleurésie, péricardite,
lymphangites carcinomateuses pulmonaires, lésions kystiques.
o Les lésions osseuses de type lytique ou qui
contiennent une composante identifiable de tissus mous, peuvent être
considérés comme mesurables, si elles sont mesurables, par
scanner ou IRM.
o Les lésions situées dans une région
préalablement irradiée ou ayant reçu une autre
thérapie loco-régionale ne sont en général pas
considérées comme étant mesurables, sauf si elles ont
progressé depuis le traitement local.
· Lésions cibles : Ce sont les lésions
sélectionnées parmi les lésions mesurables.
o Elles ne doivent pas excéder 5 lésions en
tout, dont un maximum de deux par organe.
o Le choix doit être représentatif de la maladie
et de tous les sites envahis en choisissant les lésions plus grandes
dans chaque organe.
o C'est la somme des diamètres des lésions
cibles (plus petit axe pour les adénopathies et plus grand axe pour les
autres) qui est ensuite suivi.
o Les autres lésions, sont relevées, sans
être mesurée, et considérées comme lésions
non-cibles.
|
· Réponse complète (Complete response,
CR) : Disparition de toutes les lésions, les ganglions lymphatiques
devant désormais être tous <10mm dans leur plus petit axe.
· Réponse partielle (Partial response, PR)
: Diminution d'au moins 30% de la somme des diamètres
des lésions cibles par rapport à la somme initiale des
diamètres (baseline).
· Progression (Progressive disease, PD) :
o Augmentation d'au moins =20% (et =0,5cm)
de la somme des diamètres des lésions cibles par rapport
à la plus petite somme des diamètres observées (NADIR), y
compris la mesure initiale.
o OU, apparition d'une ou plusieurs nouvelles
lésions.
· Stabilisation (Stable disease, SD) : Ni PR, ni CR, ni
PD. La somme des diamètres des lésions cibles n'est ni
inférieur à 30% par rapport à l'imagerie initiale
(baseline), ni =20% par rapport au NADIR, et il n'y a pas de nouvelle(s)
lésion(s).
· Pour les lésions non-cibles, les
critères sont un peu différents :
o Réponse complète : Disparition de toutes les
lésions non-cibles. Tous les ganglions lymphatiques doivent avoir
atteint un petit diamètre < 10mm
o Réponse incomplète - Stabilisation :
Persistance d'au moins une lésion non-cible.
o Progression : Augmentation indiscutable de
la taille des lésions non-cibles ou apparition d'une nouvelle
lésion.

57
2. Critères de réponse
|
|



