|
_
L'inflammation est un processus homéostatique dont le
but est de limiter les destructions tissulaires, détruire l'agent causal
et activer le processus de réparation tissulaire. La réaction
inflammatoire peut se manifester de manière aigue ou chronique ;
cette dernière, caractérisée notamment par sa grande
durée peut toutefois survenir spontanément (Ferguson,
2010).
Les maladies inflammatoires chroniques comme les maladies
cardiovasculaires, les cancers, les maladies respiratoires, les
diabètes, les maladies digestives et les affections cutanées
ainsi que les pathologies infectieuses sont en nette recrudescences dans notre
pays. Selon les projections de l'OMS, les décès dus à ces
maladies augmentent dans l'ensemble du monde avec un accroissement plus
marqué dans les régions africaines et méditerranées
orientale (OMS, 2008). En effet, selon l'OMS 2008 l'incidence dans le cas par
exemple du pseudo polyarthrite rhizomélique est de 10 à 50 pour
100000/an tandis que la prévalence du lupus érythémateux
disséminé est de 12 à 40 pour 100000/an. Ceci Constitue
alors de plus en plus un problème mondial de santé publique. Ces
pathologies s'accompagnent généralement de processus
inflammatoire qui est souvent l'un des signes d'alerte vers les complications.
Qu'elles soient d'origine inflammatoire ou autre, elles s'accompagnent de
désordres dans l'organisme surtout sur le plan protéique ;
en effet, l'inflammation fait intervenir des cellules, des vaisseaux, des
modifications de la matrice extracellulaire et de nombreux médiateurs
chimiques qui peuvent être pro ou anti- inflammatoires et qui peuvent
modifier ou entretenir la réaction inflammatoire. Ainsi, les maladies
chroniques sont responsables de 60% des décès dans le monde selon
l' (OMS, 2007) et représentent de ce fait la première cause de
mortalité. Toujours selon les données de l'OMS 2007, 80% de
décès dus à ces maladies surviennent dans les pays
à revenu faible ou intermédiaire.
La réaction inflammatoire
généralisée d'origine infectieuse ou non peut entrainer
un état de choc avec défaillance multi-viscérale qui
engage le pronostic vital (décès dans 50% des cas). Ces
situations requièrent un diagnostic et un traitement en urgence. Le
diagnostic de maladie inflammatoire chez l'adulte peut avoir des
conséquences dans la prise en charge ; une prise en charge
« intelligente » implique une connaissance
« intégrée » de la physiopathologie, dont des
méthodes de diagnostic fiables et adaptées. Les progrès
dans la connaissance des mécanismes physiopathologique impliqués
dans la réponse inflammatoire ont été à l'origine
du développement de méthodes d'exploration nouvelles et
variées. Devant ce foisonnement de méthodes, il importe de faire
la part entre les examens qui apportent une information réellement
utile pour le diagnostic ou la prise de décision. C'est ainsi que
devant le foisonnement de méthodes d'explorations du processus
inflammatoire il importe de faire la part entre les examens qui apportent une
information réellement utile pour le diagnostic ou la prise de
décision comme l'hémogramme, la VS ,
l'électrophorèse des protéines sériques, le profil
protéique et les examens en cours de validation à l'instar du
dosage des cytokines et chemokines, des formes solubles de molécules
d'adhésion, des médiateurs lipidiques dont l'indication doit
encore être réservée aux protocoles de recherche clinique.
Dès lors la vitesse de sédimentation qui est un
élément d'orientation diagnostic, non spécifique mais
simple à réaliser devient un outil précieux ; il
s'agit de la vitesse nécessaire aux cellules sanguines pour
sédimenter et se déposer au fond d'un tube à essai. Le
sang rendu incoagulable est placé dans un tube à essai et l'on
observe la vitesse à laquelle les globules rouges tombent et se
déposent dans le fond du tube. C'est ainsi qu'on l'utilise
régulièrement dans le suivi de certaines maladies inflammatoires,
les rhumatismes par exemple. La VS est élevée dans la plupart des
maladies infectieuses et inflammatoires, en raison de l'augmentation dans le
sang des protéines de la réaction inflammatoire comme le
fibrinogène ou l'alpha 2 globulines. Ces molécules vont
précipiter la chute des globules au fond du tube. Ainsi la VS est d'une
aide précieuse dans le diagnostic des inflammations. Cependant sa technique de réalisation d'un
centre de santé à l'autre n'est pas toujours identique ;
en effet, lors de nos stages académiques, nous avons constaté
que les procédures standard de la VS telles que décrite par
l'OMS( les points auxquels il convient de veiller lors de la réalisation
d'une vitesse de sédimentation comprennent un bon mélange de
l'échantillon de 1,6ml de sang complet avec 0,4 ml de solution de
citrate de sodium ( 3,8%), le positionnement vertical du tube de verre ou de
matière synthétique, le début de la mesure au plus tard
deux heures après le prélèvement sanguin et le maintien
d'une température ambiante( entre 18 et 22°c). tout non respect de
ces conditions standard peut fausser les résultats.) ne sont pas
toujours appliquées dans nos structures sanitaires.
En Afrique et au Cameroun en particulier le non respect de
ces procédures dans la réalisation de la VS entraine non
seulement un fardeau économique considérable à la
société mais aussi une mauvaise prise en charge du patient ;
le coût annuel des dépenses des patients pour le dépistage
des maladies liées à l'inflammation est énorme.
Ce constat nous amène à poser la question
suivante : quelles sont les variabilités dans les résultats
de la VS par l'utilisation de ces méthodes ? C'est ce qui nous a
motivé à proposer un thème de recherche portant
sur : l'étude évaluative des techniques de
détermination de la vitesse de sédimentation observé en
clinique ; d'ou la question de recherche :
1. question de recherche
Qu'elle est l'appréciation faite des techniques
d'estimation de la vitesse de sédimentation utilisée en
clinique ?
2. objectifs d'étude
2.1 objectif générale
Établir la corrélation qui existe entre la
méthode standard de la vitesse de sédimentation et anticoagulants
avec les techniques utilisées.
2.2. Objectifs spécifiques
Plus spécifiquement il s'agit :
- de réaliser la VS selon le protocole standard de
l'OMS ;
- de réaliser la VS avec la variante de l'inclinaison
influençant le temps de lecture ;
- de réaliser la VS avec le variant anticoagulant
- corréler les deux techniques.
3. intérêt
Ce travail présente un intérêt double
à savoir :
- sur le plan théorique : décrire la
corrélation existant entre les deux méthodes dans notre
localité ;
- sur le plan pratique : permettre une bonne prise en charge
du patient par un diagnostique de qualité réduisant le cout
attribuer au mauvais diagnostic.
CHAPITRE I : REVUE DE LA
LITTERATURE
I. Définition de l'inflammation
L'inflammation est un processus physiologique de
défense de l'organisme contre une agression. La fonction première
de la réponse inflammatoire est :
· De détecter l'agent agresseur ;
· Puis de l'éliminer ou de l'isoler du reste de
l'organisme ;
· Et de permettre, le plus rapidement possible, la
réparation des tissus lésés (Lawrence T ; et
al ; nature reviews Immunology 2,787-795, octobre 2002).
L'inflammation est un mécanisme de défense par
les organismes vivants en réponse à une agression
étrangère. Ce mécanisme de défense a pour but de
maintenir l'intégrité des tissus agressés
(Russo-Marie et coll ; 1998).
La réaction inflammatoire permet à certaines
cellules du système immunitaire (leucocytes ou globules blancs) ainsi
qu'aux substances produites (anticorps, cytokines, complément...)
d'accéder rapidement au foyer infectieux.
La réaction inflammatoire est la réponse
à une agression d'origine exogène (cause infectieuse,
traumatique) ou endogène (cause immunologique, par exemple une
réaction d'hypersensibilité ou une autre cause, par exemple le
syndrome d'ischémie-reperfusion).
La réaction inflammatoire est une composante de la
réponse immune. Elle est impliquée dans l'immunité
naturelle en réponse à un signal de danger. Elle favorise ainsi
l'induction de la réponse immune spécifique. C'est, par exemple
le rôle des adjuvants dans les vaccins qui, en créant une
réaction inflammatoire, favorisent les réponses
spécifiques.
La réaction inflammatoire est, le plus souvent, une
réponse adaptée strictement contrôlée par de
multiples systèmes régulateurs. Elle est
généralement protectrice en participant aux processus de
défense naturelle et à la réparation des tissus
lésés. Si la réponse inflammatoire est inadaptée ou
mal contrôlée ; elle peut devenir agressive. Ainsi, les
syndromes inflammatoires sont fréquemment rencontrés en pratique
clinique courante (25% à 30% des patients consultants ou
hospitalisés) et le médecin doit évaluer leur importance
et en faire un diagnostic étiologique car la réaction
inflammatoire peut être associée à une très grande
variété de situation pathologique (infections, maladies de
système, cancers, pathologies thromboemboliques...).
La réaction inflammatoire peut être aigue,
voire suraigüe (quelques minutes à quelques jours). On peut citer
comme exemple de syndrome inflammatoire aigu systémique : (choc
septique, syndrome de défaillance multi viscérale, syndrome de
détresse respiratoire de l'adulte, pancréatites aigues, syndrome
d'écrasement, brûlures, formes graves
d'ischémie-reperfusion). (B. DEVULDER, PY.
HATRON, E. HACHULLA, 2002)
La réaction inflammatoire peut être chronique
(semaines, années). Les maladies inflammatoires chroniques sont la 3eme
cause de mortalité après les affections cardiovasculaires et les
cancers ; et une des première causes de morbidité dans les
« pays développés » (morbidité
fonctionnelle des maladies inflammatoires chroniques au niveau des tissus
cibles : articulations, tissus nerveux, muqueuse digestive,
respiratoire...).
La réaction inflammatoire peut être locale
(vasodilatation locale, exsudation plasmatique et afflux local de cellules
inflammatoires au niveau cutané à la suite d'une plaie ou au
niveau de la muqueuse bronchique dans l'asthme allergique par exemple) ou
générale (signes généraux comme la fièvre,
production hépatique des protéines de la phase aigue ;
exemple du syndrome inflammatoire aigu systémique). (B.
DEVULDER, PY. HATRON, E. HACHULLA, 2002).
II. Physiopathologie de la réaction
inflammatoire
Les facteurs qui déclenchent une
réponse inflammatoire sont très variés :
ï Infection par des micro-organismes (ex :
bactéries, virus, parasites, champignons) ;
ï Agents physiques : traumatisme( ex : plaie)
ou nécrose tissulaire( ex : infarctus), chaleur( ex :
brûlure) ou froid( ex : gelure), radiations par des UV :
ultra-violets( ex : coup de soleil) ou des rayons X, corps
étranger( ex : prothèse, poussières de
silice,...) ;
ï Agents chimiques (ex : caustiques, toxiques,
venins).


251655680
Figure 1 : Exemple de facteurs
déclenchant l'inflammation
Source : (Ketty Schwartz, 2011)
Quelle que soit la nature du stimulus, les manifestations de
la réponse inflammatoire se ressemblent. Néanmoins, la nature des
cytokines produites, l'intensité et la durée de ces
manifestations pourront changer en fonction du stimulus (Ketty
Schwartz, 2011) p 16.
Trois séquences d'événements
complexes et intriqués composent la réponse
inflammatoire :
1. Une phase d'initiation (phase vasculaire) qui fait suite
à un signal de danger d'origine soit extérieur (exogène)
soit intérieure (endogène) et qui met en jeu une première
série d'acteurs. Cette première phase varie en fonction du type
d'agression (endogène, exogène) qu'a subi l'organisme ;
2. Une phase d'amplification avec la mobilisation et
l'activation d'autres acteurs ;
3. Une phase de résolution et de réparation qui
tend à restaurer l'intégrité du tissu agressé. Pour
mieux comprendre ces différences séquences, nous prendrons
l'exemple d'une plaie avec coupure (brèche vasculaire). Ceci va
entrainer une réaction locale qui vise dans un premier temps à
stopper l'hémorragie puis à recruter les cellules inflammatoires
au niveau du tissu lésé, pour finir par réparer le
tissu. (Ketty Schwartz, 2011) p 16.
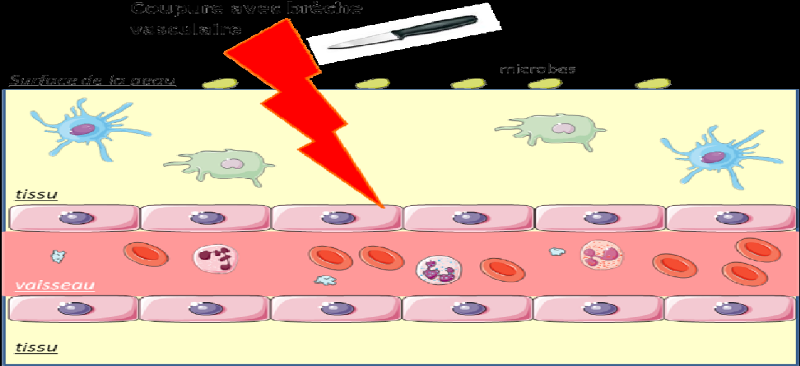
Figure 2 : Cas d'une plaie
avec coupure
Légende :

Ø La phase d'initiation : phase vasculaire
et activation des cellules résidentes
Source : (Ketty Schwartz,
2011)
Activation des plaquettes et des premiers
médiateurs
Les plaquettes sont activées très
rapidement : elles interviennent, avec l'aide de facteurs pro-coagulants
présents dans le plasma, pour colmater la brèche et limiter
l'accès des pathogènes à l'organisme. Les plaquettes
activées libèrent aussi des protéines aux
propriétés agrégantes et vasoconstrictrices (=
rétrécissement du diamètre des vaisseaux) puissantes.
L'activité de vasoconstriction est extrêmement brève et
sert à limiter les « fuites » de sang.
(Ketty Schwartz, 2011) p 17.
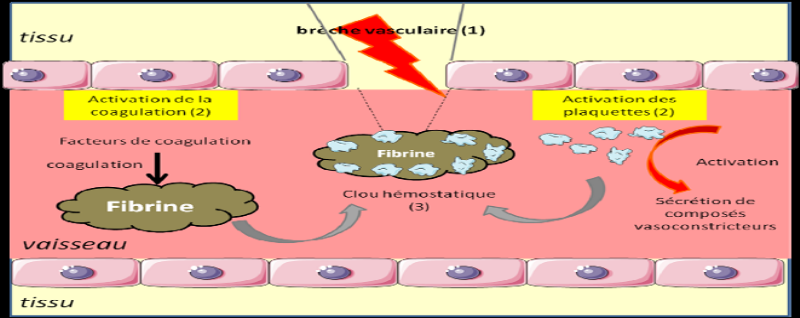
Figure 3 : Activation plaquettaire au
cours des premières étapes de la phase vasculaire
Source : (Ketty Schwartz,
2011)
Très rapidement, un grand nombre de
médiateurs solubles présents dans le sang sont activés
(système du complément, système des kinines,...). Leur but
est de « donner l'alerte » rapidement et de recruter les
cellules de l'immunité innée sur le lieu de l'inflammation.
Le système du complément joue un rôle
important dans :
ï La vasodilatation ;
ï L'augmentation de la perméabilité
vasculaire ;
ï L'attraction des cellules circulantes vers le site
lésé (chimiotactisme). Le système des kinines est
responsable entre autre :
ï De la perméabilité des vaisseaux ce qui
va permettre aux cellules de l'immunité d'arriver au niveau du
tissu ;
ï Mais aussi de la sensation de douleur grâce
à leur interaction avec les neurones sensoriels qui sont des cellules
jouant le rôle de « capteur de douleur ».
En somme :
L'inflammation se déroule dans les tissus
vascularisés, préférentiellement dans le tissu conjonctif.
Les tissus dépourvus de vaisseaux, comme le cartilage ou la
cornée, sont incapables de développer une réaction
inflammatoire complète.
Activation des cellules résidentes au niveau du tissu
lésé pour recruter des patrouilles circulantes.
Il existe un peu partout dans les tissus, des cellules du
système immunitaire inné
appelées « cellules résidentes ». Il
s'agit des macrophages et des cellules dendritiques. Ces cellules proviennent
de la moelle osseuse et ont colonisé ensuite les différents
tissus de l'organisme. Au niveau du tissu, elles sont les première
à être activées suite à la reconnaissance du microbe
(voir encarta sur « comment les cellules résidentes
reconnaissent-elles le microbe ? ») et à donner
l'alerte. Suite à leur activation, les cellules résidentes
sécrètent des messagers solubles (chimiokines, cytokines
pro-inflammatoires comme le TNF-á, l'IL-1 et l'IL-6) qui vont avoir
plusieurs effets, notamment en local :
ï Attirer des cellules du système immunitaire
inné circulant dans le sang, en particulier les neutrophiles ;
Perméabiliser les vaisseaux, ce qui permet le passage
des cellules circulantes (neutrophiles, monocytes) du sang vers le tissu
lésé. (Ketty Schwartz, 2011) p 18.
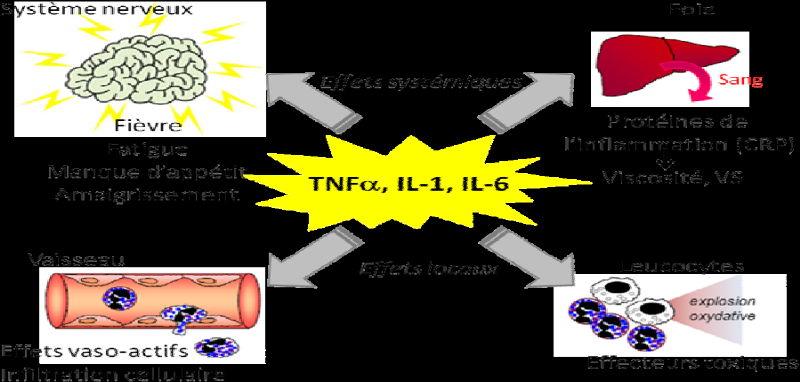
Figure 4 : Effets
locaux et systémiques des cytokines par les macrophages (CRP :
protéine C-réactive)
Source : (Ketty Schwartz, 2011)
Un autre type cellulaire joue un rôle important dans
la phase d'initiation : les mastocytes. Ils sont souvent situés
près des vaisseaux sanguins et, certains de leurs médiateurs,
l'histamine notamment, agissent sur les cellules des parois vasculaires. Il en
résulte une vasodilatation et la formation d'un oedème local.
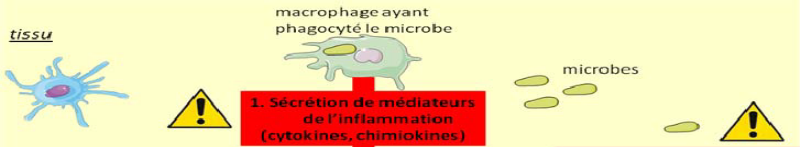




Figure 5 : Vasodilatation et
chimiotactisme induit par les messagers sécrétés par le
mastocyte et macrophage activé
Source : (Ketty Schwartz,
2011)
Schématiquement les signes de l'inflammation sont
agencés selon Schwartz, 2011comme
suit :
ü Perméabilisation et dilatation des
vaisseaux ROUGEUR/ CHALEUR
Exsudation plasmatique oedème par distension des
tissus GONFLEMENT forte pression sur les terminaisons nerveuses locales
DOULEUR activation du système des kinines DOULEUR.
(Ketty Schwartz ; 2011) p 19.
La reconnaissance de l'agent
pathogène :
Les cellules phagocytaires reconnaissent
des « motifs » très conservés,
appelés PAMP (pour Pathogen-associated Molecular Pattern, en bleu sur le
schéma ci-après) chez bon nombre de microbes (bactéries,
champignons, virus) mais qui sont absents des cellules de l'hôte. Cette
reconnaissance se fait via des récepteurs(en marron sur le
schéma) appelés PRR (pour Pathogen Recognition Receptors),
présents à la surface des cellules phagocytaires.
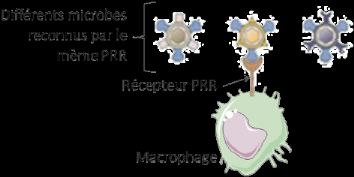
Figure 6 : Reconnaissance des
pathogènes par les cellules phagocytaires
Source :(Ketty Schwartz, 2011)
Les macrophages et les cellules dendritiques expriment des
récepteurs reconnaissant des motifs présents à la surface
de nombreuses bactéries mais absents des cellules de
mammifères.
Il existe de nombreux récepteurs PRR à la
surface d'une même cellule et chaque récepteur est capable de
fixer de nombreux microbes porteurs d'un même motif (exemples :
motif spécifique des parasites ou motif spécifique des virus).
Ainsi avec un nombre restreint de récepteurs de
spécificité large, chacun capable de reconnaître une classe
de pathogènes, ces cellules peuvent reconnaître le monde microbien
très varié.

Figure 7 : Diversité des
récepteurs des cellules du système immunitaire
inné
Source : (Ketty
Schwartz, 2011)
Légende : récepteurs de l'immunité
innée multiples mais invariants :

Ø La phase d'amplification :
arrivée des patrouilles circulantes et activation des cellules au niveau
du tissu lésé
Les neutrophiles sont les premières cellules
circulantes à arriver au niveau du tissu lésé. Si les
neutrophiles ne suffisent pas pour détruire les microbes, des
monocytes/macrophages circulants, attirés par les chimiokines, vont
venir en renfort sur le site lésé pour phagocyter les microbes et
les débris cellulaires. Dès leur arrivée sur le site
lésé, les cellules du système inné sont
activées soit par contact direct avec le pathogène, soit par la
présence des cytokines sécrétées par les cellules
résidentes. La reconnaissance des motifs microbiens par les neutrophiles
et les macrophages conduit à la destruction d'une partie des
microbes.
Les neutrophiles, après ingestion du microbe,
produisent et déversent, au niveau du tissu lésé, des
composés hautement réactifs (un peu comme de l'eau
oxygénée !), contenus dans leurs granules : il s'agit
de formes réactives de l'oxygène, de monoxyde d'azote et de
peptides antimicrobiens.

Figure 8 : Contenu des granules
libérés par le neutrophile
Source :(Ketty Schwartz, 2011)
Pour
Ketty Schwartz, 2011 les composés n'ont pas la
capacité de discriminer entre le microbe et les propres cellules de
l'individu. Des dégâts collatéraux au niveau du tissu de
l'individu sont donc, lors de cette étape, inévitables. Ces
tissus lésés, ainsi que des bactéries, des neutrophiles et
des macrophages ayant phagocyté les bactéries, composent le pus
qui signe une réaction inflammatoire efficace. Les macrophages
sécrètent aussi des facteurs de croissance et d'autres
protéines à remodeler le tissu lésé.
Parallèlement, des macrophages ayant phagocyté
des microbes migrent vers les ganglions lymphatiques ou ils présenteront
ultérieurement des fragments de ces microbes aux lymphocytes T (et
notamment aux lymphocytes T4), pour initier une réponse plus
ciblée et spécifique contre ce microbe. Cette réponse
adaptative, qui s'installe en 2 à 5 jours, prendra la suite de la
réponse innée si nécessaire. (Ketty Schwartz,
2011) p 21.
Ø La phase de réparation
tissulaire
La réaction inflammatoire doit être
limitée dans le temps. Cette dernière phase de réparation
dépend du degré de lésion au niveau du tissu et peut
prendre 10 à 15 jours.
Dans le meilleur des cas, les microbes ont été
éliminés par les neutrophiles, et éventuellement les
macrophages. Les produits de dégradation et les débris
cellulaires sont phagocytés par les macrophages qui vont
sécréter des cytokines induisant la phase de cicatrisation et de
régénération tissulaire. Le retour à l'état
normal nécessite une réparation des tissus lésés
qui peut se faire :
ï Par les cellules endothéliales elles-mêmes
(production de collagène, laminine,...) en cas de faibles
dégâts ;
ï Par d'autres cellules, si l'atteinte est plus grave et
des tissus détruits : les macrophages vont participer à la
réparation des vaisseaux (angiogénèse) et les fibroblastes
vont produire les protéines de la matrice extracellulaire
(collagène, fibronectine, laminine) pour permettre la reconstruction du
tissu. Cette réparation tissulaire met l'angiogénèse au
repos.
Après une blessure, l'angiogénèse
(création de nouveaux vaisseaux sanguins) permet de restaurer le flux
sanguin après réparation des tissus lésés. Cette
néo-vascularisation normale est strictement régulée par
des facteurs qui stimulent (tels que le VEGF) ou inhibent (par exemple
l'angiostatine) l'angiogénèse en fonction de l'état des
vaisseaux.
La production de nouveaux vaisseaux sanguins constitue un
processus essentiel durant le développement d'un embryon et pendant le
renouvellement de tissu lors de la grossesse ou de la cicatrisation d'une
blessure. Une angiogénèse anormale peut être mise en
rapport avec bon nombre de maladies : une angiogénèse
insuffisante entraîne une adduction sanguine réduite vers les
tissus (sclérose) alors qu'une angiogénèse
exagérée peut faciliter une infection, ou la progression de
tumeurs. (Ketty Schwartz, 2011) p 22.
Ces trois phases mettent en action différents
systèmes d'adaptations et impliquant de multiples médiateurs. La
nature des différents effecteurs et le développement de chacune
de ces trois phases conditionnent le profil d'expression clinique et biologique
de la réponse inflammatoire (aigue ou chronique, local ou
systémique) (MIOSSEC, 2003)
En somme, l'inflammation fait intervenir des cellules, des
vaisseaux, des modifications de la matrice extracellulaire et de nombreux
médiateurs chimiques qui peuvent être pro ou anti-inflammatoires
et qui peuvent modifier ou entretenir la réponse inflammatoire. Quelle
que soit son siège et la nature de l'agent pathogène, le
déroulement d'une réaction inflammatoire présente des
caractères morphologiques généraux et des
mécanismes communs. Néanmoins, les différentes
étapes présentent des variations liées à la nature
de l'agent pathogène, l'organe ou se déroule la réaction,
le terrain physiologique de l'hôte : tous ces éléments
conditionnent l'intensité, la durée de la réaction
inflammatoire et l'aspect lésionnel. Notons qu'une inflammation trop
importante ou trop prolongée peut avoir des conséquences
préjudiciables (Galanaud, 2001).
III. Signes clinique
III.1- signes locaux
Quatre signes cliniques cardinaux caractérisent la
réaction inflammatoire :
- La chaleur
Au cours d'une réaction inflammatoire, la chaleur est
due exclusivement à une augmentation du flux sanguin (Galanaud,
2001).
- La rougeur
La rougeur encore appelée érythème est
à la vasodilatation. Alors que ce sont les vaisseaux qui conditionnent
la résistance au flux sanguin et en conséquence la
température des tissus périphériques, ce sont les
capillaires et veinules des couches superficielles qui déterminent la
couleur des tissus. Dans le cas de l'inflammation, l'érythème est
toujours associé à une augmentation de la chaleur locale
(Galanaud, 2001).
- Tuméfaction
La tuméfaction (oedème) des tissus
inflammatoires est également due aux phénomènes
vasculaires. Il consiste en une augmentation du volume du compartiment
interstitiel extravasculaire local (Galanaud, 2001).
- Douleur
Certains médiateurs qui conditionnent la
vasodilatation sont à l'origine de la douleur quand ils sont
appliqués dans les tissus normaux. L'élévation de la
pression sanguine vasculaire et la transsudation peuvent contribuer par effet
mécanique à la production des sensations douloureuses
(Galanaud, 2001).
III-2- signes généraux
En cas d'inflammation aigue, les signes
généraux tels que l'anorexie, l'asthénie l'amaigrissement
et la fièvre peuvent être observés. La fièvre est
liée à l'action de l'interleukine au niveau du centre de la
thermorégulation. En cas d'inflammation chronique elle peut
s'accompagner de l'altération de l'état général
liée en particulier à la sécrétion de TNF
(Galanaud, 2001).
IV- Diagnostic de l'inflammation : les
différents tests de diagnostic de l'inflammation
Les progrès dans la connaissance des
mécanismes physiopathologiques impliqués dans la réponse
inflammatoire ont été à l'origine du développement
de méthodes d'explorations nouvelles et variées. Devant ce
foisonnement, il importe de faire la part entre les examens qui apportent une
information réellement utile pour le diagnostic ou la prise de
décision et les examens en cours de validation dont l'indication doit
encore être réservée aux protocoles de recherche
clinique.
1. La vitesse de sédimentation
La vitesse de sédimentation correspond au
dépôt de globules au fond d'un tube de sang laissé au
repos. Elle mesure le degré d'inflammation de l'organisme et est
fonction de la viscosité sanguine qui est en partie liée aux
anticorps. Chez un sujet normal, elle est à la première heure
inférieure à 5mm et à la deuxième inférieure
à 10mm, mais ces normes augmentent avec l'âge (Godeau et
al ; 2000).
2. Les protéines de la phase aigue de
l'inflammation
Les protéines de la phase aigue sont non seulement
d'excellents témoins de l'existence d'une réaction inflammatoire
avec des conséquences systématiques, mais sont aussi des acteurs
de la réaction inflammatoire par l'intermédiaire de leurs
propriétés biologiques respectives (GODEAU et
al ; 2000).
3. Les anomalies de l'hémogramme évoquant un
syndrome inflammatoire
· Anémie : taux
d'hémoglobine modérée > 8g/dl normo chrome normocytaire
puis microcytaire qui apparaît vers la S61*6 semaine. La ferritine est
haute et la transferrine basse même s'il existe une carence martiale
associée ;
· Polynucléose neutrophile>
7000/mm3 mais inconstante (par exemple au cours du lupus, de la leishmaniose
etc.) ;
· Thrombocytes> 400000/mm3 pouvant
atteindre 1000000/mm3. Evoquer un syndrome myéloprolifératif au
dessus de 1000000/mm3 (Willemin, 2000).
4. L'électrophorèse et l'immuno
électrophorèse des protéines.
Ces deux examens sont aussi utiles car perturbés
en cas d'inflammation. Ils permettent d'analyser la qualité et la
quantité des différentes protéines de l'organisme. Ces
protéines sont modifiées en cas de cirrhose de foie. Ils
permettent également de dépister la présence de
protéines anormales, protéines que l'on recherche en particulier
dans les gammapathies (Galanaud, 2001).
Lorsqu'il y a une agression dans l'organisme, il
apparaît une réponse immunitaire non spécifique
immédiate liée à la production de médiateurs
semblés pro-inflammatoires par les macrophages. Elle induit une
modification de la perméabilité vasculaire, une migration des
leucocytes vers le site de l'inflammation, leur activation et la production
essentiellement hépatique de protéines plasmatiques
appelées protéines de la phase aigue de l'inflammation
(Galanaud, 2001).
V- Diagnostic de l'inflammation en pratique
courante
En clinique, la vitesse de sédimentation est
couramment utilisée dans nos centres de santé pour le diagnostic
des inflammations ou des maladies inflammatoires ; cependant la technique
de réalisation de cet examen n'est pas la même suivant les centres
de santé. En effet, la technique de réalisation de la VS telle
que décrit par Westergreen et adopté par l'International
Committee for Standardization in Hematology( ICSH) en 1977(
bon mélange de l'échantillon de 1,6mg de sang complet avec 0,4ml
de solution de citrate de sodium(3,8%) comme anticoagulant, la position
vertical du tube de verre ou de matière synthétique, le
début de la mesure au plus tard deux heures après le
prélèvement sanguin et le maintien d'une température
ambiante ( entre 18° et 22°C) ; cependant ces différentes
conditions ne sont pas toujours respectées dans nos centres de
santé ; en effet la technique de réalisation de cet test
d'un centre à l'autre connaît des variabilités. Dans
certains centres, le sang destiné à la réalisation de la
VS est prélève dans le tube EDTA ; d'autres centres encore
préfèrent incliner le tube de westergreen à un angle de
45° puis lire le résultat 7min après ; cette valeur
est rendu avec les valeurs normales comme si elle était
réalisée par la méthode standard de Westergreen et
comparable à celle lu en 1heure lorsque le tube est laissé
perpendiculairement ; dans certaines structures sanitaires encore, le sang
prélevé dans la seringue est laissé perpendiculairement et
la lecture se fait une heure après ; la seringue étant
graduée, le niveau de graduation est comparé à celui de
Westergreen pour donner le résultat. Cependant, les résultats
obtenus sont- ils comparables à ceux donnés par la
méthode de Westergreen ?
CHAPITRE II : Matériel et
méthodes
II.1- Présentation du site de collecte des
données
II.1.1- Critère de choix et justification du lieu
d'étude
Notre étude s'est déroulée dans
les services d'hématologie de l'hôpital protestant de MBOUO
BANDJOUN ; l'hôpital protestant de MBOUO(HPM) est situé dans
la région de l'ouest, délégation de la santé de
l'ouest, district de santé du KOUNG-KHI, aire de santé de MBOUO
I ; l'unité de laboratoire de l'HPM a un plateau technique unique
en son genre à l'ouest ; emploie à temps plein 10
professionnels de laboratoire. Elle a à sa tête un technicien
principal d'analyse médicale, assisté d'une technicienne
d'analyse médicale. Le nombre moyen de patients reçu par jour
dans cette unité est d'environ 30, avec une moyenne par patient de 3
examens. Le poste d'hématologie exécute en moyenne 5 VS par jour
(moyenne calculée à partir des chiffres de l'année 2013).
Il s'agit de l'un des plus grands et des plus fréquentés des
hôpitaux de la région de l'ouest, c'est également un
idéal lieu où nous pouvions mener nos enquêtes avec
sérénité. Nous dépensions aussi moins d'argent
pour le déplacement.
II.1.2- Dessin ou type d'étude
Il s'agit d'une étude transversale descriptive car
elle vise à décrire les performances des techniques de la VS
utilisant l'EDTA et l'inclinaison.
II.1.3- Durée de l'étude
Nous avons mené une étude de Mars 2014 à
Mars 2015 soit environ un an et la collecte des données c'est faite du
15 juillet au 19 septembre 2014.
II.2- Méthode d'échantillonnage
II.2.1- Population de l'étude, population source et
population cible
Notre population source était
constituée des patients venus en consultation à l'hôpital
protestant de MBOUO BANDJOUN du 15 juillet au 19 septembre 2014.
La population cible était constitué de
ceux dès deux sexes à qui une vitesse de sédimentation
était demandée.
II.2.2- Critères
II.2.2.1- Critères d'inclusion
Etait considéré dans notre
étude :
- les sujets de sexe masculin ou féminin venus en
consultation pendant la période d'étude et à qui une VS
était demandée ;
- les sujets ayant donné leur consentement
éclairé par écrit avant participation.
II.2.2.2- Critères d'exclusion
N'ont pas été inclus dans la présente
partie de cette étude :
- les sujets non consentant ;
- les sujets à qui la VS n'était pas
demandé ;
- les sujets qui ne respectaient pas les conditions pour la
réalisation de la vitesse de sédimentation même si la VS
leur était demandé.
II.2.3- Echantillonnage
II.2.3.1- Taille de l'échantillon
La taille de l'échantillon n'était pas
définie à l'avance ; nous avons sollicité
définir la taille de l'échantillon selon la technique
d'échantillonnage de durant la période de collette soit une
taille de 73.
II.2.3.2- Technique d'échantillonnage
Nous avons procédé à un
échantillonnage par convenance. En effet, nous avons
systématiquement recruté tous les patients qui remplissaient les
critères d'inclusion pendant la durée de collecte. Soit au total
73 personnes des deux sexes.
Les patients reçus en consultation par un
médecin ou in infirmier et envoyés au laboratoire ;
après avoir pris connaissance de la demande d'examen formulée par
un consultant de l'hôpital protestant de Mbouo Bandjoun (carnet de
consultation ou bulletin d'examen), nous nous chargions d'expliquer à
chaque patient (ou accompagnateur) les buts et les objectifs de l'étude,
il lui a été ensuite remis un formulaire de consentement
éclairé (pour les mineurs, leur ayant droit était
sollicité). Après accord de celui-ci manifesté par la
signature du formulaire de consentement, si le patient remplissait alors les
conditions requises, un numéro d'identification lui était alors
attribué et le cas échéant et la fiche de collette
était remplie suivi du recueil au niveau du pli du coude de 9ml de sang
sous tubes EDTA et citrate tri sodique. Le respect strict des règles de
bonnes pratiques des prélèvements sanguin (OMS, 1994)
était de rigueur.
II.2.3.3- considération éthique de la
recherche
Pour réaliser la présente étude,
nous avons au préalable sollicité et obtenu auprès de
Monsieur le Directeur de l'HPM (Annexe 1), l'autorisation de
réaliser nos travaux de recherche au laboratoire de l'hôpital
Protestant de Mbouo Bandjoun, notamment le recrutement des patients et la
réalisation des différentes analyses. Nous avons aussi
sollicité et obtenu par signature, le consentement éclairé
de chaque participant ou mandataire qui, par ailleurs était libre de
participer à l'étude. Les analyses ont été
exécutées selon les règles de bonnes pratiques de
laboratoire (OMS, 1994).
Notre étude a obéi ainsi au respect des
principes de l'éthique et de la déontologie du travail, à
la démarche administrative.
II.3- collecte des données
II.3.1- méthode de collecte
Pour la collecte de nos données, nous
avons prévu la fiche de consentement accompagnée de la fiche de
collecte dans le but de recenser les informations orientant
l'étude.
II.3.1.1-phase pré
analytique
il est question ici de prendre contact avec le
patient ; les patients reçus en consultation par un médecin
ou in infirmier sont envoyés au laboratoire ; après avoir
pris connaissance de la demande d'examen formulée par un consultant de
l'hôpital protestant de Mbouo Bandjoun (carnet de consultation ou
bulletin d'examen),nous nous chargions d'expliquer à chaque patient ( ou
accompagnateur) les buts et les objectifs de l'étude, il lui a
été ensuite remis un formulaire de consentement
éclairé ( pour les mineurs, leur ayant droit était
sollicité). Après accord de celui-ci manifesté par la
signature du formulaire de consentement, si le patient remplissait alors les
conditions requises, un numéro d'identification lui était alors
attribué et le cas échéant et la fiche de collette
était remplie suivi du recueil au niveau du pli du coude de 9ml de sang
sous tubes EDTA et citrate tri sodique. Le respect strict des règles de
bonnes pratiques des prélèvements sanguin (OMS, 1994)
était de rigueur.
Chaque acte commence par la préparation du
matériel :
- Portoirs de tubes
- Aiguilles et/ou seringues à usage unique
- Tampon d'alcool
- Tampon sec
- Gants
- Garrot
- Tubes avec EDTA
- Tubes avec citrate tri sodique
- Marqueurs + crayons
- Sparadrap
- Dispositif d'élimination des déchets
contaminés
Le malade étant confortablement installé,
nous portons nos gants de sécurité, prenons notre garrot qu'on
attache au pli du coude, repérons la veine la plus accessible,
badigeonnons la zone à l'aide d'un coton imbibé d'alcool à
70°, puis à l'aide de notre aiguille bien fixé au corps
d'une seringue de 10cc, nous prélevons 9ml du sang par ponction veineuse
et enfin, nous introduisons 4cc dans le tube avec citrate tri sodique et 4cc
dans le tube avec EDTA ; les deux tubes possédant le code du
patient préalablement inscrit.
II.3.1.2- phase analytique
L'analyse débute par la préparation
du matériel qui dans notre cas consistait à placer le portoir de
Westergreen ainsi que les tubes, de vérifier le bon fonctionnement de la
minuterie.
Le montage de ce test se faisait de différentes
manières lors de nos stages académiques ; mais dans le cadre
de notre étude, nous avons confronté ces méthodes à
la méthode standard, c'est-à-dire celle de Westergreen.
v Technique de Westergreen
Le sang veineux est recueilli dans un tube contenant du
citrate de sodium (un volume de citrate pour quatre volumes de sang).
Matériel :
Ø Tube de Westergreen de dimensions suivantes :
§ Longueur : 300 #177; 1,5mm gradué de 0
à 200mm ;
§ Diamètre intérieur : 2,55 mm #177;
0,15 mm;
Ø Support de tubes permettant leur maintien en position
verticale stricte ;
Ø Seringue et tuyau(ou aide pipette) adaptés aux
tubes pour aspirer le sang.
Méthode :
Ø Après homogénéisation soigneuse
du sang, on plonge le tube de Westergreen dans le tube de sang,
Ø Au moyen de la seringue, on aspire le sang jusqu'au
repère 0,
Ø On place le tube de Westergreen sur le support, et on
note le temps,
Ø Au bout d'une heure, on lit la hauteur de plasma en
millimètres, depuis le ménisque supérieur jusqu'au sommet
de la colonne d'hématies.
Ce travail est fait aussi bien avec le tube citrate tri
sodique que le tube avec l'anticoagulant EDTA ; en effet, après
avoir bien homogénéisé le sang dans les tubes citrate tri
sodique et EDTA, on y plonge le tube de Westergreen dans celui du sang que l'on
aspire à l'aide d'une seringue avec tuyau adapté aux tubes
jusqu'au repère 0. le tube de Westergreen est ensuite placé sur
son portoir en position verticale ; respectivement avec citrate et EDTA
qui sont placés cote à cote sur le portoir.

Figure 9 :
Sédimentation du sang anti coagulé (lors de la collette des
données)
Source : (HPM)

Figure 10 :
réalisation de la VS.
Source : (HPM)
II.3.1.3- phase post analytique
Après avoir obtenu les résultats, nous les
enregistrons dans le registre de la paillasse d'hématologie, inscrivons
sur la fiche du malade ainsi que sur la fiche de collecte de données de
ce dernier puis rendons le résultat au patient.
Etaient considéré comme non malades des
hommes dont la VS était inférieur à 6mm à la
première heure, des femmes dont la VS était inférieur
à 8mm à la première heure ; ces
références étaient également respecté pour
le cas de 7min.
Etaient considéré comme malades tous les
hommes dont la valeur à la première heure et à 7min
était supérieure à 6mm et les femmes dont la valeur
était supérieure à 8mm. (Pierrick Hordé
2014)
II.4- méthode d'analyse des résultats
II.4.1- définition des variables et indicateurs
d'analyse
Nous avons analysés nos données en fonction des
anticoagulants (citrate tri sodique, EDTA), du sexe, de l'âge, et du
temps ; la méthode de Westergreen expliquée plus haut a
été strictement respectée.
Variables statistique :
- la moyenne(M) : est la somme des
valeurs de VS des individus(S) sur la proportion
(N) des patients ayant participés à
l'étude.
· M=S/N
- Ecart-type(ET) : c'est le plus
significatif de tous les paramètres de dispersion ; il mesure la
variabilité autour de la moyenne, c'est-à-dire de combien les
observations individuelles sont éloignées de la moyenne.
· ET=vv
Avec V= variance
II.4.2- saisie informatique
Nos données ont été saisies dans
une feuille de calcul du logiciel Excel 2007 de la suite bureautique
Microsoft ; les analyses ont été réalisées
avec le logiciel statistique R version 3.0.2.
II.4.3- traitement et analyse des données
Nos données ont été
traitées et analysées par le logiciel statistique R version
3.0.2.
Nous avons mis en évidence l'influence de
l'anticoagulant et de la méthode par le calcul de la moyenne des
valeurs, de la déviation standard et du test de student à
intervalle de confiance 95%.
Le seuil de significativité pour comparer deux
proportions a été fixé à une valeur P <0,05.
Les résultats ont été
présentés sous formes de tableaux.
Notons bien que ces différentes valeurs ont
été calculées et trouvées automatiquement par le
logiciel.
Chapitre III : résultats et
interprétations
Les résultats ont été
présentés sous forme de tableau comme suit :
Tableau1 : valeurs moyenne de la
VS chez les hommes et les femmes par utilisation du citrate tri sodique et
l'anticoagulant EDTA.
|
citrate tri sodique
|
EDTA
|
|
|
7min
|
1h
|
7min
|
1h
|
|
hommes
|
24,21#177;21,89
|
18,93#177;23,54
|
37,42#177;29,54
|
21,24#177;22,64
|
|
femmes
|
38,65#177;33,44
|
26,35#177;23,67
|
38,90#177;26,81
|
32,42#177;25,51
|
.
Sur les 73 patients testés, 33 étaient des
hommes soit un pourcentage de 45%( 33/73) tandis que 40 représentait les
femmes pour un pourcentage de 45% soit un sex-ratio (F/M) de 1,2. Les
moyenne#177; ET des valeurs de la VS chez les hommes à 7min par
utilisation du citrate tri sodique et de l'EDTA étaient 24,21#177;21,89
et 37,42#177;29,54 respectivement. Cependant chez les femmes elle était
38,65#177;33,44 et 38,90#177;26,81 respectivement. Apres 1heure, les moyennes
des valeurs de la VS chez les hommes étaient pour le citrate tri sodique
18,93#177;23,54 et pour l'EDTA 21,24#177;22,64mm/hr
Tableau 2: valeur moyenne#177; ET de
la VS dans la population globale selon les tranches d'âges
|
|
0 à 50ans
|
51ans et plus
|
|
moyenne
|
21,86#177;26,17
|
24,22 #177;21,10
|
|
P-value
|
0,67
|
0,67
|
La moyenne#177; ET de la VS dans la population en 1heure par
tranche d'âge pour 0 à 50ans est de 21,86#177;26,17 et de 51ans
et plus une moyenne de 24,22 #177;21,10.
Tableau 3 : comparaison des
moyennes#177; ET des valeurs de citrate et d'EDTA dans la population globale
à la première heure
|
|
citrate tri sodique
|
EDTA
|
|
moyenne
|
23#177;23
|
27,36#177;24,73
|
|
p-value
|
0,27
|
0,27
|
La comparaison de la moyenne#177; ET de la VS dans la population
globale par utilisation du citrate tri sodique et de l'EDTA à la
première heure .cette comparaison n'est pas significative car
(p>0.05).
Tableau 4 : comparaison des
moyennes#177; ET des valeurs de la VS de l'EDTA 7min et du citrate 7min
|
EDTA
|
citrate tri sodique
|
|
moyenne
|
38,23#177;27,89
|
32,12#177;29,51
|
|
p-value
|
0,2
|
0,2
|
La comparaison entre la moyenne#177; ET de la VS en 7min en
utilisant d'une part le citrate tri sodique et d'autre part l'EDTA ; la
différence n'est pas significative car (p>0.05).
Tableau 5 : comparaison des
moyennes#177; ET des valeurs de la VS du citrate en7 min et en 1heure
|
|
7min
|
1heure
|
|
moyenne
|
32,12#177;29,51
|
23#177;23
|
|
p-value
|
0,04
|
0,04
|
La comparaison entre la moyenne#177; ET obtenu par le
citrate tri sodique en 7min et en 1heure ; la différence est
significative car (p<0.05).
Tableau 6 : comparaison des
moyennes#177; ET des valeurs de la VS de l'EDTA en 7min et en 1heure
|
7min
|
1heure
|
|
moyenne
|
38,23#177;27,89
|
27,36#177;24,73
|
|
p-value
|
0,01
|
0,01
|
Une comparaison entre la moyenne de la VS donné par l'EDTA
après 7min et après 1heure ; comparaison significative car
(p< 0.05).
Chapitre IV :
discussion

Sur un échantillon de 73 spécimens sanguin
notre étude destiné à analyser la relation qui existe
entre la VS réalisée avec le citrate tri sodique et l'EDTA d'une
part et l'influence de l'inclinaison d'autre part, ceci afin d'évaluer
les méthodes utilisées en clinique et d'établir une
méthode acceptable pouvant aider pour avoir de bons résultats.
Une comparaison de moyennes des résultats de la VS obtenus en
utilisant le diluent conventionnel, citrate tri sodique selon les
recommandations de OMS a été pris pour référence
avec ceux obtenus avec l'EDTA comme diluent. De cette méthodes il en
découle pour résultats à p-value = 0.278 qu'il n'existe
pas de différence significative entre ces deux diluent lorsque la
technique standard est respecté, Cette observation ne rejoins pas les
observations de (Emeribe et Ukonu, 1992) pour qui la différence
était significative entre les résultats de la VS obtenus par le
citrate tri sodique et l'EDTA.les raisons de cette observation ne sont
probablement pas attribuées au climat influençant la VS. En effet
la température ambiante du laboratoire lors de notre étude
était entre 24°c -28°c comparé à celle de
18°c- 25°c à laquelle les valeurs Caucasiens étaient
obtenues. La VS varie directement avec la température (Hall et Malia,
1984). Cependant pour le même auteur le citrate tri sodique
réduirait la formation en rouleaux du sang alors que l'EDTA qui
favoriserait ceci conduirait a une différence de viscosité,
où l'EDTA peut être plus visqueux que le citrate tri sodique ce
qui expliquerait les résultats un peu élevés. De
même le sexe n'exerçant aucune influence statistiquement
significative. En effet les valeurs de la VS chez les hommes et les femmes
consultés à l'hôpital de Mbouo lors de notre période
de collecte étaient 18,93#177;23,54mm et 26,35#177;23,67mm
respectivement à la première heure. Les femmes ont des valeurs de
VS élevées par rapport aux hommes qui est soutenu par le rapport
par (Saadeh, 1998). La raison de cela peut être du à plusieurs
changements physiologiques qui arrivent chez la femme comme les menstruations.
La confrontation de la méthode de la VS faisant
intervenir inclinaison rencontrer en clinique (VS en 7min ) et la technique
standard tels décrit par OMS présente une différence
significative ; Quelque soit l'anticoagulant utilisé (le citrate ou
l'EDTA), le raccourcissement du temps d'exécution de l'analyses par
l'action de l' inclinaison permet l'obtention des résultats errones.ces
valeurs étaient bien rencontre dans les étude de Emeribe et Ukonu
en 1992 pour qui la différence était significatives. Cette
étude confirme et renforce le fait que le temps conventionnel de
lecture de ce test est de 60min. la presque disparition de la
réalisation des VS par la méthode conventionnelle observée
dans nos structures interpelle les professionnels sur la qualité de la
prise en charge, les statistiques et le diagnostique des syndromes
l'inflammation.
Conclusion et suggestions
1. Conclusion
Au terme de notre étude ou il était
question d'évaluer les procédures opératoires de la VS en
clinique à l'hôpital protestant de Mbouo Bandjoun du 15 juillet
au 19 septembre 2014. Nous pouvons conclure que le citrate tri sodique est le
meilleur anticoagulant que l'on doit utiliser dans nos laboratoires ;
cependant, l'EDTA peut être utilisé en l'absence du citrate tri
sodique car les deux diluants donnent des valeurs de VS relativement
rapprochés dans le cas de la technique standard de l'OMS. Cette
étude a également montré que la valeur de
référence chez les individus venus à l'hôpital
pendant la période de collecte est 18,93#177;23,54mm et
26,35#177;23,67mm respectivement chez les hommes et chez les femmes. Il en
découle de cette étude que la confrontation de la méthode
de la VS faisant intervenir une inclinaison rencontrée en clinique (VS
en 7min) permet l'obtention des résultats erronés en effet la
différence est significative car p=0,04 ; valeur inférieur
à 0,05.
2. Suggestions
Vu l'importance de la VS dans la surveillance de
l'évolution du processus inflammatoire, de l'efficacité du
traitement, sa réalisation doit être rigoureuse. L'utilité
de la VS n'étant plus à démontrer, pour les pays en voie
de développement tel que le notre, nous suggérons :
· Aux autorités en charge de la
santé
- De financer les projets de recherche dans le domaine des
maladies inflammatoire.
- D'instaurer de façon systématique et en
première intension la VS chez tous les patients présentant des
signes de maladie inflammatoire.
- d'interdire la commercialisation des portoirs à
inclinaison
· Aux biologistes
- de respecter la méthode de Westergreen dans la
réalisation de la VS tel que prescrite par le comité de
standardisation des normes ;
- De respecter le temps qui est d'1e heure avant la
lecture ;
- D'utiliser l'anticoagulant le plus recommandé qui est le
citrate tri sodique et de n'utiliser l'EDTA qu'en car d'absence quasi-totale du
citrate tri sodique.
· Aux médecins responsables
d'hôpitaux
- de ne part inclure la VS dans la liste des examens à
réalisation rapide ;
- de permettre aux biologistes l'acquisition du matériel
adéquat ;
- de recommander aux biologistes la réalisation de la VS
par la méthode de Westergreen.
En perspective une étude similaire pourrait
être faite pour comparer la VS en utilisant le citrate tri sodique et
l'eau physiologique.
REFERENCES
Ø B. Willemin (2000). Exploration de la réaction
inflammatoire. Ann.med interne, 141, n°4 pp 333-39.
Ø
Docteur Pierrick HORDÉ : https://
plus.google.com/u/o/115238239615758137667/ ?rel=author.
Ø Emeribe, A.O. and Ukonu, G.O. (1992):Comparative study
of erythrocyte sedimentation rate using three diluents. J Med Lab Sci,
2:41 -44
Ø Hall, R; Malia, R. (1998): Function of Blood In:
Médical laboratory Haematology, Butherworth, London. Pp. 16-17.
Ø International Council for Standardization in
Haematology (ICSH). (Expert Panel on Blood Rheology) (1993): ICSH
recommendations for measurement of erythrocyte sedimentation rate. J. Clin.
Pathol, 46: 198-203
Ø Lawrence T ; et al ; nature reviews
Immunology 2,787-795, octobre 2002.
Ø MEDECINE INTERNE, Abrégé Masson, 2002
B. DEVULDER, PY. HATRON, E. HACHULLA
Ø OMS (1994) Manuel des Techniques de
Base pour laboratoires tropicaux, Bibliothèque de l'OMS,
Genève, 488 P.
Ø OMS(2009). Relevé
épidémiologique des maladies inflammatoires
Ø OMS(2010). Le point sur les maladies inflammatoires,
rapport spécial sur la prévention des maladies
cardiovasculaires.
Ø P. GALANAUD, D. Éntilie(2001). Physiologie et
physiopathologie de
l'inflammation J Gynecol Obstet Biol Reprod / Volume 30,
supplément au
n°l.
Ø P. GODEAU, S. HERSON, J.C. PIETTE(2000). Traité
de Médecine, Paris
3eir ' Ed Flammarion,
Médecine Sciences.
Ø Pierre MIOSSEC, (2003). Physiopathologie de
l'inflammation, Rev Prat, p53
Ø Saadeh, C. (1998): The erythrocyte sedimentation rate:
old and new clinical applications. South Med J 3: 220-225.
Ø Séminaire Ketty
Schwartz « inflammation et maladies : clés de
compréhension 2011-2012. Pp 16-22.
Annexes
1- demande d'une autorisation de recherche en vue des
travaux de recherche en Analyses médicales
2-budgétisation
|
activités
|
Description et justification
|
quantité
|
Cout unitaire
|
montant
|
|
documentation
|
Il sera utile de faire la recherche sur internet
|
------------
|
-------------
|
5000fcfa
|
|
réactifs
|
|
|
|
200fcfa
|
|
Matériel de prélèvement
|
Seringues
Coton
Alcool
Tube EDTA
Tube citrate tri sodique
Portoir de Westergreen
Tube de Westergreen
|
100
50g
1l
100
100
2
4
|
50fcfa
-------
------
100fcfa
100fcfa
|
5000fcfa
800fcfa
1500fcfa
10000fcfa
10000fcfa
5000fcfa
5000fcfa
|
|
Frais de communication et de transport
|
Rencontre de l'encadreur et déplacement pour le lieu de
collecte des données
|
------------
|
----------
|
10000fcfa
|
|
Saisie et impression
|
Le protocole et le mémoire devront être saisie et
imprimés
|
------------
|
----------
|
30000fcfa
|
|
total
|
-----------
|
-----------
|
------------
|
82500fcfa
|
3-chronogramme
|
Activités
|
Année 2014
|
Année 2015
|
|
mars
|
Avril
|
Mai
|
juillet
|
aout
|
octobre
|
nov.
|
déc.
|
jan
|
Fr
|
mars
|
avril
|
mai
|
|
Elaboration du protocole
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ü ü ü Collecte et analyse des
échantillons
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ü ü ü Traitement des données
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ü ü Rédaction du mémoire
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ü ü Correction du mémoire
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ü Pré-soutenance
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ü Soutenance
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ü 4-Fiche de collecte des données
Code:
....................................................................sexe :..........
Date :
..................................................................âge :
............
Résidence :
..............................................................................
Résultats :
VS première heure avec EDTA :
...............................................
VS première heure avec citrate tri sodique :
...........................
VS deuxième heure avec EDTA :
...............................................
VS deuxième heure avec citrate de sodium :
.........................
VS inclinée avec
EDTA :...............................................................
VS inclinée avec Citrate tri
sodique :...........................
5- Fiche de consentement
Consentement de participation
Je
soussigne :..............................................................................
Certifie avoir lu et compris le document d'information qui m'a
été remis et avoir la possibilité de poser toutes les
questions que je souhaite à :
...................................... Je comprends les objectifs, les
contraintes, les risques et les bénéfices potentiels lies
à ma participation à cette étude.
J'accepte que les produits biologiques soient utilisés
dans l'étude. Ces échantillons seront utilisés pour
vérifier éventuellement certaines données de
l'étude et effectuer si cela est souhaitable des recherches biologiques
complémentaires.
J'accepte que les données anonymes enregistrées
à l'occasion de cette étude puissent faire l'objet d'un
traitement informatisé.
J'ai bien noté que je pourrai avoir accès à
ces données à tout moment en m'adressant à (au) :
..........................................................................................
J'accepte que tout médecin ou tout scientifique
impliqué dans le déroulement de cette recherche, ainsi que les
représentants des autorités de sante aient accès à
l'information dans le respect le plus stricte de la confidentialité.
J'accepte librement de participer à cette étude
dans les conditions précisées dans la notice d'information. Je
pourrais à tout moment si je le désire interrompre ma
participation sans avoir à me justifier ; mais je ferais mon
possible pour en
informer...................................................................................................................
Cette interruption ne remettra pas en cause la qualité des
soins ultérieurs.
Fait à
..................................................le
....................................
Noms et
prénoms.................................................................
Signature :
Je
soussigne..........................................................................certifie
avoir communiqué toute informations utiles concernant cette
étude. Je m'engage à faire respecter les termes de cette note de
consentement, conciliant le respect des droits et de liberté
individuelle et les exigences d'un travail scientifique.
Fait
à................................................le.......................................
Nom et prénom de
l'enquêteur............................................................
| 


