|
UNIVERSITE DE
LIKASI
FACULTE DE MEDECINE

PROFIL SÉRIQUE DU BILAN LIPIDIQUE DE JUILLET
2023 AU JUIN 2025 À LIKASI
« Cas du laboratoire international Medical
Service »
Mémoire présenté en vue de
l'obtention du grade de baccalauréat en Médecine.
Par : KASONGO MATEMBO Phinées
Directeur : Docteur KAZADI LUBOBO Claude
Professeur
Demandé par Prof. KAIJ
EPIGRAPHE
« Que ta nutrition soit ta seule
médecine ».
Hippocrate
IN MEMORIAM
A ma grand-mère MWAPE
partie trop tôt, ton amour, ta tendresse, ta
générosité resteront gravés dans nos
mémoires.
DEDICACE
A vous les artisans de ce chemin parcouru, qui avaient
sacrifié votre vie pour nous, merci pour l'amour, le soutien et tous les
efforts fournis à notre égard, qui nous ont permis d'aller plus
loin.
Mes très chers parents, COSTATIN MUSONDA et LEONTINE
KISHA, que Dieu vous bénisse.
A mon frère CHADRACK SALIYA, ton encouragement, ton
assistance nous a aidé d'aller en avant.
A Dieu le tout puissant, pour le souffle de vie, la force,
l'assistance et pour nous avoir guidé de mener à bien ce
travail.
KASONGO MATEMBO Phinées
REMERCIEMENTS
A la fin de notre premier cycle, il nous a été
demandé de produire un travail à caractère
scientifique.
Elaborer ce travail n'a pas été chose facile pour
nous, tout travail cette grandeur comporte des tâchesingrates mais, pour
les avoir réalisé avec attention,nous tenons à exprimer
nos profonds remerciements à :
Notre directeur, le Professeur KAZADI LUBOBO Claude qui, non
seulement a accepté de diriger ce travail, mais aussi et surtout, a
guidé avec soin dans son élaboration couronnant notre premier
cycle. Nous espérons que vous trouverez dans ce travail l'expression de
notre plus grand respect. Prospérez à tous égards.
A notre Co-directeur, Mr le CT. TSHIBUMBU KABEYA Edouard pour
votre disponibilité, votre sacrifice qui nous a servi pour mener
à bien ce travail, votre générosité nous a
marqué tout au long de la rédaction de ce modeste travail.
Prospérez à tous égards
A mes parents, votre rigueur nous a servi aujourd'hui, votre
sacrifice et votre assistance a fait de nous ce que nous sommes.
A toute ma famille, JOSUE MUSONDA, CHADRACK SALIYA ; sa
femme et ses enfants, REBECCA MUSHIYA, PHILIPPE KAZADI, DORCAS MWAPE, JEREMIE
SALIYA, ELISE SELEMANI, restons unis.
A vous grand-père ; KAZADI Philippe, notre
dictionnaire vivant, que tu vives longtemps.
A vous frère JOSEPH ASUMANI, merci pour l'assistance.
A vous mes collègues carabines et carabins ; MILOLO
Zacharie, MUSAU Marlène, MWENZE Jemima, MANDA Chris, MUSUL Prince,
KALALA Taylor, NURU Aurore, SAKA Patrick. La liste n'est pas exhaustive ;
Pour les bons moments passés ensemble, l'entraide et le partage de
l'expertise.
Tous nos remerciements à Dieu le tout puissant qui nous a
donné la force, le courage, la sagesse, l'intelligence et qui pourvu des
moyens durant toutes les années passées à
l'université de Likasi
A tous ceux dont leurs noms ne sont pas cités sur cette
page, qu'ils ne se sentent pas lésés, car vous êtes
gravés dans le coeur.
KASONGO MATEMBO Phinées
LISTE DES
ABRÉVIATIONS
AG : Acides Gras.
Apo : Apolipoprotéines.
CT : Cholestérol total.
HDL : High Density Lipoprotein.
HDL-c : High Density Lipoprotein
Cholesterol.
HTA : Hypertension artérielle.
IDL : Intermediate Density Lipoprotein.
LDL : Low Density Lipoprotein.
LDL-c : High Density Lipoprotein
Cholesterol.
Lp : Lipoprotéines.
LPL : Lipoprotéine Lipase.
MCV : Maladies Cardiovasculaires.
PL : Phospholipides.
PLTP : Protéine de Transfert de
Phospholipides (Phospholipid Transfer Protein).
TG : Triglycérides.
VLDL : Very Low Density Lipoprotein .
LISTE DES FIGURES
|
Figure
|
Titre
|
page
|
|
1
|
Classification des lipides.
|
6
|
|
2
|
Acide gras.
|
7
|
|
3
|
Glycérophospholipide.
|
15
|
|
4
|
Phosphatidylcholine.
|
15
|
|
5
|
Sphingophospholipide.
|
16
|
|
6
|
Glycolipide(cérébroside).
|
16
|
|
7
|
Représentation du caractère amphiphile.
|
17
|
|
8
|
Monocouche .
|
18
|
|
9
|
Micelle .
|
18
|
|
10
|
Répartition des patients selon le sexe.
|
37
|
LISTE DES TABLEAUX
|
Tableau
|
Titre
|
Page
|
|
1
|
Composition en pourcentage des lipoprotéines en lipides et
en Apo lipoprotéines.
|
21
|
|
2
|
Répartition des patients en fonction de sexe.
|
37
|
|
3
|
Répartition des patients en fonction de la valeur du CT et
du sexe.
|
38
|
|
4
|
Répartition des patients en fonction de la valeur du CT et
de la tranche d'âge.
|
38
|
|
5
|
Répartition des patients en fonction de la valeur de
HDL-cholestérol et du sexe.
|
39
|
|
6
|
Répartition des patients en fonction de la valeur de
HDL-cholestérol et de la tranche d'âge.
|
39
|
|
7
|
Répartition des patients en fonction de la valeur de
LDL-cholestérol et du sexe.
|
40
|
|
8
|
Répartition des patients en fonction de la valeur de
LDL-cholestérol et de la tranche d'âge.
|
40
|
|
9
|
Répartition des patients en fonction de la valeur de TG et
du sexe.
|
41
|
|
10
|
Répartition des patients en fonction de la valeur de TG et
de la tranche d'âge.
|
41
|
INTRODUCTION
1.ETAT DE LA QUESTION
Le bilan lipidique correspond à un ensemble d'analyse
permettent demettre en évidence des anomalies du métabolisme des
lipides et d'optimiser la prise en charge, le suivi, la surveillance et
l'évolution du risque athérogène. [1]
Ce bilan inclut le cholestérol total, le
LDL-cholestérol, souvent qualifié de « mauvais
cholestérol » le HDL- cholestérol, connu comme « bon
cholestérol », ainsi que les triglycérides. Ces trois
derniers composants sont reconnus comme indicateurs clés du risque de
développer une MCV. [3]
Le calcul du LDL- cholestérol se fait habituellement
par la formulede friedewald pour des valeurs de triglycérides inferieurs
à 3,4g/l. Au-delà de ce seuil, une méthode directe est
utilisée pour mesurer le LDL-cholestérol, car la formule de
friedewald n'est plus applicable. [4]
Il est largement prouvé que la diminution du
LDL-cholestérol estefficace pour diminuer l'incidence des MCV. De
même, la baisse des triglycérides et l'augmentation du
LDL-cholestérol contribuent à réduire le risque. [5]
Le bilan lipidique est une analyse du sang,
réalisé suite à ladécouverte d'une augmentation du
taux de cholestérol total, pour contrôler une maladie
déjà connue. En fonction des résultats, il convient de
mettre en place des mesures hygiéno-diététiques
(régime, activités physiques, ...) ou des traitements
médicamenteux. [28]
Une étude descriptive a été
réalisée de janvier jusqu'au mois de mars 2016 sur 108 sujets, au
laboratoire de biochimie de l'établissement public hospitalier de la
région de blida. Les résultats présentés
correspondent donc à une prévalence fréquente de la
dyslipidémie (72,2%) ainsi que différentes dyslipidémies
de sujets sains dont la plupart des individus sont affectés par une Hypo
HDLemie (50,9%), suivi des hyper HDLemie (35,7%), une
hypercholestérolémie (26,9%) et une
hypertriglycéridémie (17,6%).
L'analyse de ces résultats avec des facteurs de risque
cardio-vasculaire ont montrés une relation significative (P<0,05) du
cholestérol total avec l'âge (51-65 ans). [6]
La présence de dyslipidémie chez une population
apparemment enBonne santé souligne l'exigence du dépistage
précoce de l'hyperlipidémie et ses facteurs de risque
associé à la protection primaire contre la progression de la
maladie coronarienne.) [1]
Le bilanlipidique permet de surveiller le taux de lipide dans
le sang, en particulier le cholestérol. Ce dernier comprend le LDL
cholestérol et le HDH cholestérol.
L'intérêt du bilan lipidique ne réside pas
seulement dans le diagnostic de la dyslipidémie, mais aussi dans la
stratification du risque cardio vasculaire permettant ainsi une
prévention proactive des maladies cardiaques.
En effet, la dyslipidémie ou trouble lipidique ne
présente souvent aucun symptôme, apparent ce qui rend les examens
de laboratoire essentiels. [7]
2.CHOIX ET INTERETS DU SUJET
La plupart des dyslipidémies accroissent le risque de
complications cardio-vasculaires ischémiques. Leur traitement
réduit la morbimortalité cardio-vasculaire. La réalisation
d'un bilan lipidique (exploration d'une anomalie lipidique : EAL) est
nécessaire lors de l'évaluation initiale du risque
cardio-vasculaire (RCV), pour disposer d'une appréciation du niveau de
risque individuel et lors du suivi pour estimer l'efficacité du
traitement, s'assurer de l'observance, motiver les patients à propos des
règles hygiéno-diététiques et guider
l'intensification éventuelle du traitement
Nous avons choisi ce sujet parce que nous avons
constaté que le profil lipidique à Likasi est décrit de
façon parcellaire et il n'existe pas de données
actualisées du profil lipidique à Likasi
2.1. Intérêt
personnel
Ce sujet va renforcer ma motivation à approfondir mes
connaissancesdans ce domaine.
2.2.Intérêt
social
Mieux comprendre le bilan lipidique contribue à la
sensibilisation età l'amélioration des stratégies
préventives.
2.3. Intérêt
scientifique
Les résultats de cette étude pourraient
être un outil de référence àd'autres chercheurs qui
viendront après nous.
3.PROBLEMATIQUE
La dyslipidémie demeure encore aujourd'hui un
problème majeur dans les pays développés comme dans les
pays en voie de développement. Tout au long de cette étude, cette
question mérite d'être posée :
Comment se présenterait le bilan lipidique à
Likasi ?
4.OBJECTIFS DU TRAVAIL
Le but de ce travail est d'évaluer le bilan lipidique
sérique à Likasi.
Pour y parvenir nos objectifs sont les suivants :
ü Doser les marqueurs lipidiques à Likasi
ü Faire les statistiques descriptives du bilan lipidique
à Likasi
5.DELIMITATION DU SUJET
Notre étude s'est effectuée au centre para
clinique INTERNATIONAL MEDICAL SERVICE (IMS) sur une période allant du
juillet 2023 au juin 2025.
6.DIVISION DU TRAVAIL
En plus de l'introduction et la conclusion, ce présent
travail comprend deux parties :
- Une partie théorique : qui traite l'aspect
général et les généralités sur les lipides
et les lipoprotéines ;
- Une seconde partie qui parle de matériel et
méthodes, résultats et de la discussion.
PREMIERE PARTIE :
APPROCHE THEORIQUE
CHAPITRE I : GENERALITES SUR LES LIPIDES
1.1.Définition
On regroupe sous le nom de lipides des substances naturelles
insolubles dans l'eau mais solubles dans certains solvants organiques tels que
le méthanol, le chloroforme, l'acétone, l'alcool, etc. les
lipides ont des structures et des fonctions très diverses). [8]
On classe les lipides en fonction de leur nature chimique et
du rôlequ'ils tiennent dans la structure et le fonctionnement des
organismes.
Les lipides de réserve, c'est-à-dire les huiles
et les graisses, sont destriacylglycerols qui représentent une
importante réserve d'énergie sous forme concentrée chez la
plupart des êtres vivants ; de plus, lorsqu'ils sont localisés
sous la peau, ils apportent une protection efficace contre le froid). [9]
Les lipides de structures sont des phospholipides et
dessphingolipides qui s'associent pour former une double couche lipidique ;
cette dernière constitue, avec le cholestérol, les membranes
biologiques qui délimitent les cellules ou les organites
intracellulaires tels que le noyau, les mitochondries, les chloroplastes, le
réticulum endoplasmique, les peroxysomes ou les lysosomes ; pour cette
raison, les phospholipides et sphingolipides sont appelés habituellement
lipides membranaires. [9]
Tous ces lipides contiennent dans leur structure des acides
gras oùces derniers apparaissent comme les constituants
élémentaires clés.
Par ailleurs, d'autres lipides, bien que présents en
quantité moindre,jouent des rôles fonctionnels d'une grande
importance. Ainsi, appartiennent au groupe des lipides les sels biliaires qui
participent à la digestion et l'assimilation des lipides de
l'alimentation, les hormones stéroïdes, les hormones
eicosanoïdes, les vitamines liposolubles A, D,E et K qui interviennent
dans la régulation de nombreux processus biologiques fondamentaux, des
pigments susceptibles d'absorber la lumière, des cofacteurs
enzymatiques, des transporteurs d'électrons et des messages intra
cellulaires.
Ils sont caractérisés par la présence
dans la molécule d'au-moins unacide gras ou chaîne grasse.
Ils sont rattachés aux lipides en raison de leur
insolubilité dans l'eaule cholestérol, les stéroïdes,
la vitamine D). [10]
1.2.Rôles
Les lipides ont de nombreuses fonctions qui sont importantes
pour tous les organismes vivants :
A.Stockage de
l'énergie
Les lipides servent de source d'énergie. Lorsque les
lipides sont décomposés, ils libèrent de l'énergie
et de l'eau, deux éléments précieux pour les processus
cellulaires.). [11]
B.Composants structurels des
cellules
Les lipides se trouvent à la fois dans les membranes de
la surface descellules (également appelés membranes plasmiques)
et dans les membranes entourant les organelles. Ils aident les membranes
à rester flexibles et permettent aux molécules liposolubles de
passer à travers ces membranes.
C.Reconnaissance cellulaire
Les lipides auxquels un glucide est attaché sont
appelés glycolipides. Leur rôle est de faciliter la reconnaissance
cellulaire, ce qui est crucial lorsque les cellules forment des tissus et des
organes.[11]
D.Isolation
Les lipides qui sont stockés sous la surface du corps
isolent leshumains de l'environnement, ils gardent notre corps au chaud.
Cela se produit aussi chez les animaux : les animaux
aquatiquesconservent la chaleur grâce à une épaisse couche
de graisse sous leur peau.
E.Protection
Les lipides servent de bouclier protecteur autour des organes
vitaux. Les lipides protègent également notre plus grand organe :
la peau.
Les lipides épidermiques ou les lipides qui forment nos
cellulescutanées, empêchent la perte d'eau et
d'électrolytes, préviennent les dommages causés par le
soleil et servent de barrière contre divers micro-organismes.
F.Précurseurs pour les
hormones (hormones stérides comme les oestrogènes) ;
G.Dissolvent également
les vitamines liposolubles (A, D,E et K)
H.Facilite la digestion des
vitamines liposolubles. [12]
1.2.1.Rôles
biologiques
Les lipides ont un rôle biologique important, qui peut
être résumé en :
- Stockage de l'énergie : les graisses et les huiles
(1g lipides?9kcal) ;
- Messager intracellulaire ;
- Pigments qui absorbent la lumière ;
- Les lipides représentent environ 20% du poids du
corps ;
- Deux acides gras polyinsaturés sont des facteurs
essentiels car ils ne sont pas synthétisés par l'organisme et
doivent lui être apportés par l'alimentation. Ces sont des acides
gras indispensables : acides linoléiques et acides linoléiques ;
- Les plaques d'athérome constituées de
dépôt lipidique entraînent le durcissement desartères
(athérosclérose). [10]
1.3.Classification
On classe les lipides en deux grandes catégories :
ï Les lipides à base d'A.G
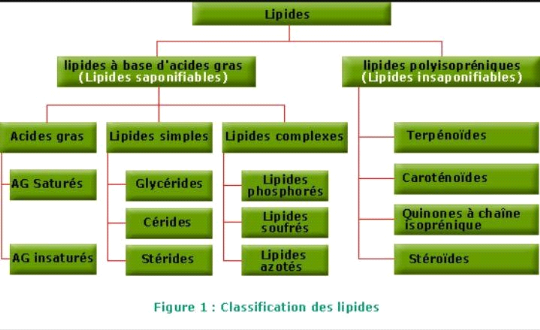
ï Les lipides à base d'isoprène (lipides
polyisopréniques) [12]
Dans la catégorie des lipides à base d'acides
gras, on retrouve lesacides gras eux-mêmes, ainsi que deux familles
nommées :
- Lipides simples ;
- Lipides complexes.
Les lipides simples regroupent les glycérides, les
cérides et lesstérides.
Les lipides complexes désignent les lipides
phosphorés, lipidesazotés et lipides soufrés. Chacune de
ces familles lipidiques est elle-même divisée en plusieurs
catégories de composés lipidiques regroupés par leur
homologie de structure.
Les lipides à base d'acides gras sont également
appelés « lipidessaponifiables » (lipides qui, traités
avec NaOH ou KOH, donnent du savon).
En revanche, les lipides n'aboutissant pas à la
formation du savonpar traitement alcalin sont appelés « lipides
insaponifiables ».
Ce dernier groupe renferme les lipides polyisopréniques
qui sontdivisés en trois catégories :
- Les terpénoïdes ;
- Les caroténoïdes ;
- Les quinones à chaîne isoprénique et les
stéroïdes. [9]
1.3.1.Acides gras
Les acides gras sont des acides carboxyliques aliphatiques
à chaînecarbonée plus ou moins longue dérivant de/ou
contenu dans les graisses animales et végétales. Par extension,
le terme est parfois utilisé pour désigner tous les acides
carboxyliques à chaîne carbonée non cyclique.
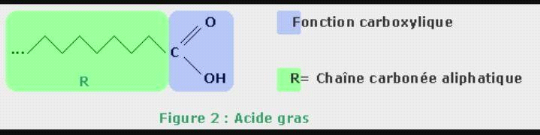
Les AG ont généralement un goût aigre et
une odeur prononcée. Ilssont insolubles dans l'eau, mais solubles entre
eux et dans les solvants organiques comme l'éther). [13]
Malgré leur importance quantitative comme constituants
des lipides,ils se trouvent en très faible quantité à
l'état libre. Dans le corps humain, l'essentiel des acides gras provient
de la dégradation enzymatique (moyennant les enzymes lipases) des
lipides au niveau du système digestif.
On connait une quarantaine d'acides gras naturels, dont les
plusimportants sont l'acide butyrique que l'on trouve dans le beurre, l'acide
palmitique (huile de palme), l'acide stéarique (suif), l'acide
linoléique (huile d'arachide) duquel est dérivé l'acide
arachidonique et l'acide linoléique (huile de bourrache).
Les acides linoléiques et lenoléique sont des
acides gras dit essentiels: les animaux sont incapables de les
synthétiser et doivent donc obligatoirement les trouver dans leur
alimentation.
Dans les industries, les acides gras sont fabriqués par
l'hydrolyse desliaisons ester de triglycérides (lipides
constitués de glycérol et de trois acides gras. [13]
I. Acides gras
saturés
Un acide gras saturé est un acide gras totalement
saturé enhydrogène: toutes les liaisons entre les carbones sont
simples (pas de liaisons doubles). Les acides gras saturés sont
généralement solides à T° ambiante (sous forme de
graisse) à l'exception des acides butyriques
(C4H8O2) et caproïque
(C6H12O2). On les trouve dans les aliments
d'origine animale comme le beurre, le lait et le fromage.
Les acides gras saturés ont pour formule chimique
générale :
H3C - [CH2]n - COOH où
n est un nombre entier égal ou supérieur à 2.
II. Acides gras
insaturés
Un acide gras insaturé est un acide gras contenant une
ou plusieursinsaturations (présence de doubles liaisons
carbone=carbone). Il est mono insaturé s'il contient une seule double
liaison carbone=carbone et polyinsaturé s'il contient deux ou plusieurs
doubles liaisons carbone=carbone. La présence d'une double liaison dans
un acide gras entraîne une Isomérie cis-Trans.
Double liaison cis
Une double liaison Trans :
C =
C = C
H H COOH
H C3 COOH CH3 H
Les 2 hydrogènes sont du même côté.
Les 2 hydrogènes sont opposés.
A température ordinaire, les acides gras
insaturés sont liquides (huiles) qu'on trouve généralement
dans les aliments d'origine végétale. Il est possible de
transformer des huiles en graisses par hydrogénation de leurs doubles
liaisons (ajout d'atomes d'hydrogène). Ce qui correspond à une
saturation des doubles liaisons. Cette opération est utilisée par
exemple pour obtenir les margarines à partir des huiles
végétales. [13]
III. Acides gras essentiels et
acides gras indispensables
En nutrition, les nutritionnistes appellent les acides gras
indispensables, les acides gras que le corps est incapable de les
synthétiser lui-même.
Ces acides gras doivent donc être apportés
obligatoirement parl'alimentation. A partir d'eux, l'organisme est ensuite
capable de synthétiser les autres acides gras, dont le corps en a besoin
pour fonctionner. Ces derniers acides gras pouvant être
synthétisé prennent le nom d'acides gras essentiels.
Pour les chimistes, en revanche, les acides gras sont dits
essentiels sil'organisme en a besoin pour vivre et s'il n'est capable de les
synthétiser lui-même. C'est en fait ceux que les nutritionnistes
appellent acides gras indispensables. Les autres sont tout simplement
appelés acides gras par les chimistes alors que les nutritionnistes les
appellent acides gras essentiels.
Ainsi, il faudra toujours faire attention dans l'appellation
des acidesgras, c'est-à-dire si l'on se place d'un point de vue chimiste
ou nutritionniste.
La définition la plus courante et la plus
utilisée est celle deschimistes : un acide est dit essentiel
lorsque l'organisme ne peut fabriquer qu'en petite quantité voire pas du
tout, ils doivent par conséquent, être apportés par la
nourriture. [12]
A.1.1. La nomenclature
Des dénominations parallèles existent : la
nomenclaturesystématique s'efface souvent devant les noms d'usage. Deux
nomenclatures coexistent, l'une systématique et l'autre utilisée
en dialectique qui permet de regrouper les acides gras insaturés en
série.
A.1.2. Propriétés
physiques
Le point de fusion
- L'état physique des acides gras en fonction de la
température peutavoir des conséquences vitales pour les
organismes vivants. De manière générale:
- La longueur de la chaîne des acides gras
saturés élève la température de fusion (passage
à l'état liquide) ;
- La méthylation diminue la température du point
de fusion, par exemple dans la série des C18, la différence de
température du point de vue entre un acide gras saturé et un
acide gras insaturé avec une seule double liaison en configuration cis
est de 50°C.
Ce sont les acides gras qui imposent leur état à
la majorité des lipides, ce qui impliquera des variations dans la nature
de ces derniers selon leur fonction dans les organismes vivants. Par exemple :
le tissu adipeux profond d'emballage et de protection des organes, les couches
d'isolation thermique de certains mammifères, les parois de
mycobactéries...
La solubilité des
acides gras
La tête des acides gras qui porte la fonction
carboxylique est polairedans l'eau à un PH > 5,5, par contre la
chaîne carbonée est apolaire (queue hydrophobe).
Ceci impliquera que la solubilité dans l'eau des acides
gras diminuera lors de l'augmentation du nombre de carbones : en dessus de
C4 et C5, les acides gras sont insolubles et s'organisent
:
- Soit en film moléculaire (mono ou bicouche ou
multicouche) à l'interface eau-air.
- Soit en micelles (Emulsion). [2]
C
Tête polaire
Queuehydrophobe
AIR
Bicouche
Ou multicouches
Emprisonnant de
l'eau.
Bulle de
savon
Eau
Bicouche
Monocouche
A.1.3. Propriétés
chimiques
Le groupe carboxyle
Dans les lipides, ce groupement est rarement libre, le pka du
groupeest d'environ 4,75 à 25°C. L'acide libre des lipides est
dosable : elle sert de marqueur de la dégradation des corps gras en
contrôle alimentaire.
Les sels
Les sels de sodium et de potassium des acides gras sont des
savons. On les obtient par traitement alcalin des lipides : la saponification.
v L'addition d'halogène (double liaison)
C'est un procédé de routine d'évaluation
de l'insaturation d'un acidegras par addition d'iodes dans les conditions
particulières qui évitent les substitutions (catalyseur,
obscurité).
?L'hydrogénation
(double liaison)
Ce procédé est utilisé pour transformer
des huiles comestiblesd'acides gras insaturés en margarines qui est
composée d'acides gras saturés qui sont solides à la
température ambiante et qui de plus ne s'oxydent pas.
?L'oxydation chimique
Les oxydants puissants (ozone, ion permanganate en milieu
alcalin) provoquent la scission de la molécule d'un acide gras
insaturé en mono et en diacides :
H2C - (CH2)n - CH = CH -
(CH2)n - COOH
Acide gras monoénique (mono insaturé)
H2 C - (CH2)n - COOH + HOOC -
(CH2)n - COOH
Monoacide diacide
L'auto oxydation des huiles et des graisses à l'air
libre a pourrésultat :
- Le rancissement qui produit des peroxydes puis par nature de
la chaîne, des aldéhydes responsables de l'odeur et des acides
(tous toxiques).
- La siccativité : des huiles polyinsaturées
comme l'huile de lin, par fixation du dioxygène, se polymérisent
en vernis et solides imperméables.
L'oxydation biologique
- Les lipides insaturés des membranes subissent une
dégradation lors d'agression oxydative (irradiation ultra-violette,
espèce réactives de l'oxygène comme les peroxydes ou les
radicaux libres). La vit. E, composé terpénique à un effet
protecteur contre cette dégradation.
- Les oxygénations enzymatiques, par différentes
oxygénases du précurseur acide arachidonique conduisent aux
médiateurs des familles prostaglandines, Leucotriènes et
tromboxanes.[2]
1.3.1. Les lipides simples
Les lipides simples, encore appelés les homolipides
sont des corpsternaires (C, H, O). Ils sont des esters d'AG que l'on classe en
fonction de l'alcool:
- Acylglycérols (ou glycérides) sont des esters
du glycérol ;
- Cérides : sont des esters d'alcools à longue
chaîne (alcool gras) ; -Stérides sont des esters de stérols
(alcool polycyclique).
I.Les acylglycérols
Le glycérol est un triol, il pourra donc par
estérification avec desacides gras donner des mono esters (mono
acylglycérols ou mono glycéride), des diester (di
glycéride) et des triesters (triglycérides).
Lorsque les molécules d'AG constituant le di ou tri
ester sontidentiques, on parlera de diacylglycérol ou triacylglycerol
homogènes, dans le cas contraire le diacylglycérol ou
triacylglycérol mixtes. Les triacylglycérols sont des lipides
neutres. [9]
La nomenclature doit permettre d'écrire la formule
développée d'une glycéride sans ambiguïté:
1. á CH2OH CH2 - O - CO -
R CH2OH CH2 -O-CO-R1
2. â CHOH CHOH CH-O-CO-R
CH OH
3. áCH2OH CH2OH
CH2-O-CO-R2 CH2-O-CO-R2
Glycérolá mono glycéride â
monoglycérideádi glycéride (Mixte).
CH2-O-CO-R CH2
-O-CO-R CH2-O-CO-R1
CH-O-CO-R CH-O-CO-R
CH-O-CO-R2
C H2 O H C
H2 - O - CO - R C H2 - O - CO -
R3
áâ diglycéride
triglycéride triglycéride
(Homogène) (Homogène)(Mixte)
A.Propriétés
physiques
La propriété physique dominante est le
caractère complètementapolaire des acylglycérols naturels,
essentiellement de triglycérides. Les groupes polaires (hydroxyle ou
carboxyle)disparaissent dans les liaisons esters.
- Ils sont insolubles dans l'eau et très solubles dans
les solvants les plus apolaires comme l'acétone ;
- Agités dans l'eau, ils forment des émulsions
très instables qui se transforment en système bi phasique. Les
tensioactifs, comme les savons, les dispersent et stabilisent ces
émulsions où les TAG se mettent en suspension sous forme de
micelles.
B.Propriétés chimiques
Elles sont celles des chaînes d'AG et celles des esters
:
-L'hydrolyse enzymatique
Des lipides hydrolysent les TAG avec différentes
spécificités. Parexemple, la lipase pancréatique, les
hydrolyses par étapes et c'est en émulsion (sels biliaires
présents dans l'intestin) et en présence d'un facteur
protéique, la Co lipase ; un TAG est hydrolysé en
diglycérides avec libération d'un acide gras et le di
glycéride en 2 - mono acylglycérol et un acide gras qui sont
absorbés par l'intestin.
-La saponification
Les bases en solution alcoolique (hydroxyde de sodium ou
depotassium) et à chaud coupent les liaisons esters des
glycérides en libérant les acides gras sous leurs formes de sels
de sodium (savons durs) ou de potassium (savons mous).
Cette réaction peut aussi servir à :
- Doser la fraction non saponifiable d'un extrait lipidique
qui contient les lipides non acides et non esters (hydrocarbures,
isoprénoides...)
- Détruire un indice de saponification défini
comme la masse de KOH (en mg) nécessaire pour saponifier 1g de corps
gras. [12]
C.Rôle biologique
-Réserve énergétique
La plupart des eucaryotes stockent ces lipides neutres dans
desinclusions huileuses du cytosol : tissu adipeux des mammifères,
graines des plantes oléagineuses. Cette réserve
énergétique offre des avantages par rapport aux glucides :
- Leur catabolisme par oxydation s'accompagne d'une production
d'énergie 2 fois plus grande, alors que les glycogènes sont une
source rapide de glucose épuisable en une journée, les
acylglycérols sont une réserve à long terme de quelques
mois.
-Isolant thermique
Le tissu adipeux sous cutané est un isolant thermique
très efficace.[14]
II.Les cérides
Ils tirent leur nom générique au fruit qu'ils
sont les principaux constituants des cires Animales, végétales et
bactériennes.
Les cérides sont des mono esters d'acides gras et
d'alcools aliphatiques à longue chaîne qui sont en
général d'alcools primaires, à nombre pair de carbones,
saturés et non ramifiés.
OH
OH H3C - (CH2) - C + HO -
CH2 - (CH2)n - CH3
Aide gras O alcool gras
H3C - (CH2)n - C - O -
CH2 - (CH2)n - CH3
Céride liaison ester.
Propriété
La structure à deux longues chaînes
carbonées saturées fait descérides des composés :
- A température de fusion élevée
(60-100°c) et solides à température ordinaire;
- A très forte insolubilité dans l'eau
(très apolaires) : ils sont seulement solubles à chaud dans le
solvant organique ;
- Inertes chimiquement : ils résistent aux acides et
à la plupart des réactifs et sont difficilement saponifiables.
III.Les stérides
Ils résultent de l'estérification d'AG par les
stérols.
Les stérols
Ces alcools dérivent du noyau stéroïde,
produit de la condensation de 4 cycles dont l'hydroxyle est une fonction alcool
secondaire toujours à la même position. Le plus
représentatif est lecholestérol.
Les stérides sont principalement des esters d'AG + le
stérol.
C
C C C
C C C C C C C
C C
C
Noyau cholestérol.
CH
2
HO
CH
2
CH
2
CH
2
CH
2
CH
2
CH
CH
2
CH
2
CH
2

Cholestérol
Le cholestérol, malgré sa mauvaise
réputation, est essentiel à notresanté :
Il s'associe aux phospholipides pour former les membranes
descellules animales (il n'y a pas de cholestérol chez les animaux) et
sert aussi à former différentes molécules essentielles
comme les hormones stéroïdes, la vitamine D ou les sels biliaires
(ces derniers sont contenus dans la bile, ils aident à la digestion des
lipides dans l'intestin).
La plupart de nos cellules fabriquent du cholestérol.
Près de 80% ducholestérol de l'organisme est ainsi
synthétisé. Le reste provient de l'alimentation.
La consommation d'aliments riches en cholestérol et en
gras saturéstend à faire augmenter le taux de cholestérol
sanguin.
N.B : toutes les études démontrent qu'il y a une
corrélation élevée entre un taux de cholestérol
sanguin élevé et les risques de maladies cardiaques,
particulièrement l'athérosclérose.
Le cholestérol est présent sous deux formes dans
l'organisme : le boncholestérol et le mauvais cholestérol. Le bon
cholestérol (HDL : High Density Lipoproteins) est celui qui, uni aux
acides gras essentiels des huiles vierges, est assimilable par l'organisme. Le
mauvais cholestérol (LDL : Low Density Lipoproteins) est celui qui ne
faisant qu'accompagner les graisses et se dépose n'importe où.
[9]
1.3.2.Lipides complexes
Les lipides complexes sont des lipides qui contiennent en plus
ducarbone, hydrogène et O2, un ou plusieurs
hétéroatomes (azote, phosphore, soufre).
Suivant la nature de l'hétéro atome, on
distingue :
- Les lipides phosphorés ;
- Les lipides azotés ;
- Et les lipides soufrés.
I. Les lipides
phosphorés
On appelle phospholipides (ou lipides phosphorés) les
composéslipidiques contenant du phosphore. Ces sont les constituants
principaux des membranes biologiques.
On désigne sous le terme « phospholipides »,
l'ensemble des glycérophospholipides et des sphingophospholipides.
I.1. Les
glycérophospholipides
Sont des esters de glycérol, 2 acides gras, un
phosphate et un alcool.
Selon le type d'alcool, on distingue :
- Le phosphatidylcholine (Alcool = choline)
- Le phosphatidyléthanolamine (alcool = ethanolamine)
- Le phosphatidylsérine (alcool = serine)
- Le phosphatidylinositol (alcool = inositol)
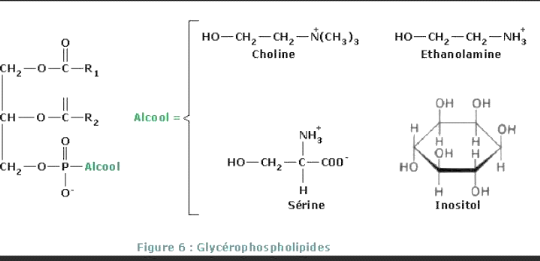
Figure3 glycérophospholipides
Le phosphatidylcholine sont connus sous le nom de «
lécithine ». Cecomposé est présent dans tous les
tissus vivants, en particulier dans les tissus nerveux et dans les globules
rouges du sang. On trouve également des lécithines dans les
végétaux et le jaune d'oeuf.
La lécithine est utilisée comme
émulsifiant dans la margarine et dans d'autrespréparations
alimentaires. Les lécithines commerciales sont produites principalement
à partir de soja.
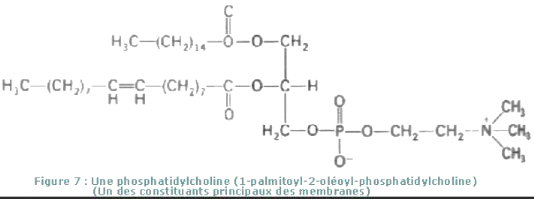 Figure4 phosphatidylcholine Figure4 phosphatidylcholine
Les sphingophospholipides sont des lipides membranaires ne
contenant pas de glycérol. Ils sont composés d'un acide gras
à longue chaîne, un alcool gras aminé comme la sphingosine
ou un de ses dérivés et un phosphate.
La sphingosine est un composé de 18 atomes de carbone,
un doubleliaison Trans, un groupement aminé et 2 hydroxydes. [12]
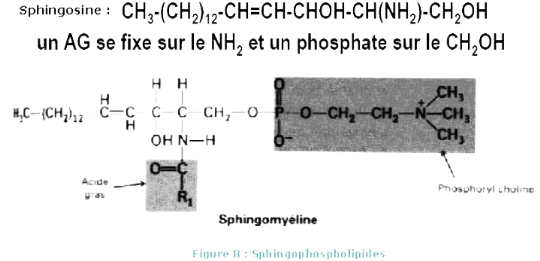
Figure5 Sphingophospholipides
II.Lipides azotés
On appelle les lipides azotés, les composés
lipidiques contenant de l'azote. Ce sont des constituants des membranes
biologiques. On distingue dans ce groupe :
- Les acyles sphingosine ou céramides d'une part
- Et les sphingosidolipidiques ou glycolipides
(cérébrosides) d'autre part.
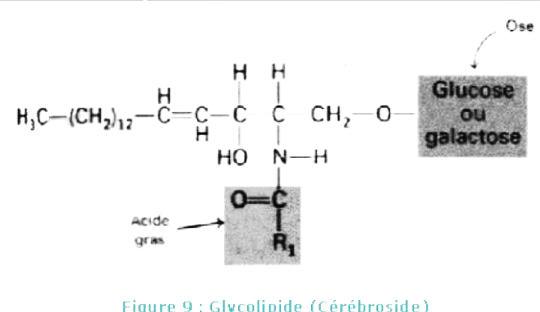
Figure6 : Glycolipide
(cérébroside)
Les lipides soufrés
Les lipides soufrés sont aussi appelés
sulfolipides ou sulfatides. Il s'agit d'esters sulfuriques des cerebrosides
(glycolipides).
1.3.3.Lipides
polyisopréniques
Les lipides polyisopréniques sont des lipides à
base d'isoprène.
Ce groupe des lipides est aussi appelés LIPIDES
INSAPONIFIABLES et jouent un rôlebiologique fondamental (hormones et
vitamines).
Ils sont divisés en quatre catégories :
- Les terpénoïdes ;
- Les caroténoïdes ;
- Les quinones à chaîne isoprénique ;
- Les stéroïdes.
Les carotènes (pigment rouge-orangé), les
xanthophylles (pigment jaune) et la vitamine A font partie des
caroténoïdes.
La vitamine E, K, les ubiquinones et les plastoquinones font
partie des quinones à chaîne isoprénique. Les
stéroïdes regroupent les stérols, les acides biliaires, les
hormones stéroïdes et la vitamine D. Ces trois derniers sont des
dérivés des stérols.
Les huiles essentielles des végétaux
(géraniol, limonène, menthol pinène, camphre) qui
contribuent à l'odeur et à la saveur de certaines espèces
sont aussi des lipides polyisopréniques.
Comportement des lipides dans l'eau
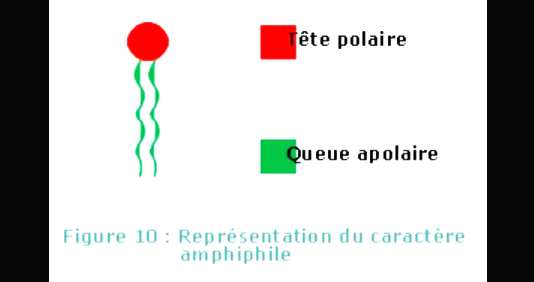
Les lipides sont des molécules amphiphiles : ils ont
une tête polaire (hydrophile) qui aime l'eau et une queue apolaire
(hydrophobe) qui pousse l'eau. Le caractère amphiphile est très
accentué chez les phospholipides, lesacides gras dans les savons et les
sphingolipides. C'est ce caractère amphiphile qui conditionne
l'organisation des lipides dans l'eau en : monocouche, bicouche (liposomes) ou
micelles.
Figure7 : Représentation du
caractère amphiphile
En déposant une petite quantité d'huile à
la surface de l'eau, lesmolécules de lipides forment une couche
mono-moléculaire (monocouche) l'interface eau-air et les parties
hydrophiles du lipide se dirigent vers l'eau et les parties hydrophobes se
dirigent vers l'air.
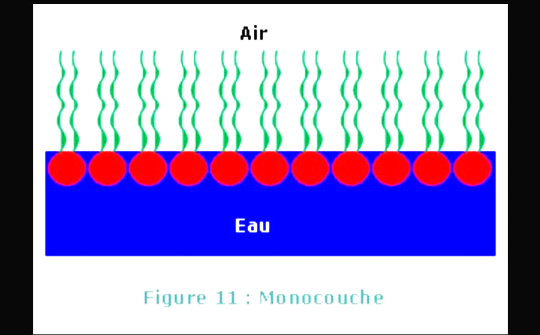
Figure8 : Monocouche
En présence de savons, certains lipides sont apparemment
solubles dans l'eau, en réalité, il s'agit d'un regroupement des
lipides sous forme de micelles les parties polaires (hydrophiles) se dirigent
vers l'extérieur (en contact avec l'eau) et les parties apolaires
(hydrophobes) se dirigent vers l'intérieur (en contact avec les autres
parties hydrophobes).

Figure9 : Micelle
CHAPITRE II : GENERALITES
SUR LES LIPOPROTEINES
II.1. Définition
Les lipoprotéines sont des complexes
macromoléculaires sphérique hydrosolubles composés des
protéines et des lipides qui transportent massivement les graisses dans
tout le corps. De nombreuses enzymes, antigènes et toxines sont des
lipoprotéines. [15]
II.2. Structure
Les lipides plasmatiques insolubles en milieux aqueux
circulent dans les plasmas liés à des protéines
spécifiques les Apo lipoprotéines est forment des complexes
macromoléculaires : les lipoprotéines.
Les lipides polaires constituent la zone
périphérique : cholestérollibre (CL), phospholipides (PL)
et Apo lipoprotéines ; le noyau est formé de lipides hydrophobes
: triglycérides et esters de cholestérol. [16]
C E
TG
C E : cholestérol estérifié
T G : triglycérides
II.3. Classification des
lipoprotéines
Les lipoprotéines sont classées en fonction de
leur densité selon leurcomportement en ultracentrifugation en 5 groupes.
Ce sont des moins denses aux plus denses :
II.3.1. Selon la
densité
En dehors des chylomicrons, qui sont eux-mêmes des
très grosseslipoprotéines, il existe quatre autres classes
majeures de lipoprotéines, classées suivant la densité
mesurée par ultracentrifugation :
1. Les lipoprotéines de très basse
densité, qui contiennent des hautes concentrations en
triglycérides et des concentrations modérées en
cholestérol et phospholipides ; ou VLDL (Very Low Density Lipoproteins)
;
2. Les lipoprotéines intermédiaires, qui sont
des lipoprotéines des très basses densités auxquelles une
large part des triglycérides a été enlevée, de
sorte que les concentrations en cholestérol et en phospholipides soient
augmentées (IDL : Intermedate Density Lipoproteins) ;
3. Les lipoprotéines de faible densité, qui sont
des lipoprotéines de densité intermédiaires auxquelles a
été enlevée la presque totalité des
triglycérides, laissant donc particulièrement une haute
concentration en cholestérol et une concentration modérée
en phospholipides (LDL : Low Density Lipoproteins) ;
4. Les lipoprotéines de haute densité, qui
contiennent une très grande concentration de protéines, environ
50%, mais des concentrations plus faibles en cholestérol et en
phospholipides.
Densité
- Les chylomicrons : constitués à 90% des
triglycérides d'origine alimentaire d'apoprotéines.
- Le VLDL : constitués à 60% des
triglycérides d'origine endogène, d'apoprotéines B100, E ;
- IDL : riches en cholestérol, triglycérides,
ApoE ;
- LDL : constitués à 45% de cholestérol,
d'Apo B100 essentiellement CI, CII, CIII et E.
- HDL : sont des composés pour moitié dans
protéines dont les Apo AI et AII essentiellement.
II.3.2. Selon la
mobilité électrophorétique
A.Chylomicron ;
B. VLDL ;
C. LDL ;
D. HDL
Mobilité
Chylomicrons : ne migrent pas et restent au dépôt ;
sont absents chez un sujet sain ;
- VLDL : migrant en position pré-bêta
(pré-â Lipoprotéines) ;
- LDL : migrent en position Bêta (â
Lipoprotéines) ;
- HDL : migrent en position á (á
Lipoprotéines).
II.4. Origine des lipides et
des lipoprotéines
Les lipoprotéines sont synthétisées avec
des lipides d'origineexogène ou endogène.
1.Apports lipidiques
endogènes
La synthèse endogène de triglycérides est
effectuée dans le foie àpartir du glucose et des acides gras
libres libérée par l'adipocyte puis transportés par la
sérumalbumine jusqu'au foie. Le cholestérol peut être
synthétisé à partir de l'acétyle CoA. [17]
2.Apports lipidiques
exogènes
Les lipides alimentaires sont d'origine animale et
végétale. Ils sonthydrolysés dans le duodénum par
les enzymes pancréatiques : lipase, phospholipase, cholestérol
estérase.
L'hydrolyse des lipides nécessite une
émulsifiassions en gouttelettesgrâce aux sels biliaires qui sont
indispensables à l'action de la lipase pancréatique ainsi qu'un
cofacteur protéique, la colipase.
Le produit de la digestion des lipides sont des mono
glycérides, desacides gras du cholestérol, des
lysophospholipides. [16]
II.5. Les Apo
lipoprotéines
Les apoprotéines représentent la partie la plus
externe deslipoprotéines, elles sont constituées d'au moins 5
classes majeures : A, B, C,D et E. Il existe plusieurs sous-classes : (A3, AII,
AIV). (B100, B48). (CI, CII, CIII). (E2, E3 et E4).
Outre leur rôle structural, les apoprotéines
jouent des rôlesimportants dans le métabolisme lipidique :
- Rôle dans la synthèse et la
sécrétion des lipoprotéines ;
- Reconnaissance des récepteurs spécifiques aux
lipoprotéines ;
- Régulateurs des enzymes du métabolisme des
lipoprotéines (activateurs et inhibiteurs).
Selon les lipoprotéines, les apoprotéines ne
sont pas les mêmescertains sont transférables d'une
lipoprotéine à une autre, comme les apoprotéines E (Apo E)
et C (Apo C).
On distingue :
- L'apoprotéine A (Apo A) présente à la
surface des HDL, dont l'apoprotéine A1 ;
- L'apoprotéine B avec deux iso formes :
ï Apoprotéine B-48, à la surface des
chylomicrons ;
ï Apoprotéine B-100, à la surface des VLDL,
des IDL et LDL.
- L'apoprotéine C (Apo C) à la surface des
chylomicrons, des HDL, des VLDL, qui se subdivisent en apoprotéine C-I,
C-II, C-III, et C-IV ;
- L'apoprotéine D (Apo D) à la surface des HDL ;
- L'apoprotéine E (Apo E) à la surface des
chylomicrons, des HDL, des IDL et des VLDL ;
- L'apoprotéine L, dont l'apoprotéine LI ;
- L'apoprotéine M et l'apoprotéine O.
Ainsi, en fonction des apoprotéines présentes
à leur surface, leslipoprotéines seront capturées par des
cellules différentes (possédant des récepteurs aux Apo
lipoprotéines différents). Le tableau résume les
différents composants des lipoprotéines. [16]
Tableau 1 : composition en pourcentage des
lipoprotéines en lipides et en Apolipoprotéines.
|
Triglycérides
|
Cholestérols libres
|
Cholestérols estérifiés
|
Phospholipides
|
Apo
lipoprotéines
|
|
Chylomicrons
|
85
|
1
|
2
|
8
|
B-48 (C,E) 2
|
|
VLDL
|
55
|
7
|
10
|
20
|
B-100 (C,E) 9
|
|
IDL
|
26
|
8
|
30
|
23
|
B-100 E 11
|
|
LDL
|
10
|
10
|
35
|
20
|
B-100 20
|
|
HDL
|
8
|
5
|
15
|
25
|
AI
(A,C,E,F,G,H)
45
|
II.6. Métabolisme de
lipoprotéines
II.6.1. Métabolisme des
lipoprotéines riches en triglycérides
1.Origines des chylomicrons et
des VLDL
Les lipoprotéines riches en triglycérides sont
synthétisées parl'intestin pour leschylomicrons et une faible
partie des VLDL (20%) avec des lipides d'origine exogène.
Ces lipoprotéines d'origine intestinale sont
libérées dans la lymphe puis circulent dans le sang. Les VLDL
sont principalement synthétisées par le foie avec des
triglycérides d'origine endogène.
Les chylomicrons et le VLDL vont subir l'action de la
lipoprotéinelipase (LPL) de l'endothélium des capillaires qui
dégradera leurs triglycérides en acide gras et glycérol.
La lipoprotéine lipase est activée par l'Apo C
cédée préalablement par les HDL, véritables
réservoirs d'Apo C. les AG libérés peuvent subir la (3
oxydations et libérer de l'énergie pour différents tissus,
soit être stockés par les adipocytes tous sous forme de
triglycérides). [18]
2.Devenir des chylomicrons et
VLDL
Après l'action de la lipoprotéine lipase sur les
deux lipoprotéines, leschylomicrons sont transformés en
particules résiduelles ou « remuants » et le VLDL en
lipoprotéines intermédiaires, les IDL. Les remuants sont reconnus
par les récepteurs à Apo B/E du foie et sont
dégradés. Plusieurs types de récepteurs ont
été décrits proches du récepteur-LDL en particulier
le « LDL receptor related protein » ou LRP qui permet aussi
l'épuration des remuants avec reconnaissance de l'Apo E.
De même les lipoprotéines intermédiaires
IDL, tout en continuant àsubir l'action de la LPL, viendront
également se fixer sur les récepteurs hépatiques. Ces Apo
E3 et E4 sont reconnus par ces récepteurs mais pas l'Apo E2 ce qui
pourra provoquer une hyperlipoprotéinemie avec accumulation d'IDL. Les
IDL subissent alors l'action probable du triglycéride lipase
hépatique pour être transformées en LDL. [16]
3.Devenir des LDL
Les LDL ainsi formées se composent d'Apo B, de
cholestérol libreet estérifié. Elles circulent dans le
sang vers les tissus périphériques et le foie. Elles sont
reconnus par les récepteurs à Apo B/E une anomalie quantitative
ou qualitative du récepteur Apo B/E ou une modification de la LDL pourra
entraîner une dyslipoprotéinemie.
Après fixation sur le site récepteur, la LDL est
internalisée etdégradée en cholestérol libre, acide
gras et acides aminés de l'Apo B.
Le cholestérol libre pourra :
- Etre utiliser pour la structure des membranes ;
- Etre stocké sous forme de cholestérol
estérifié. Une enzyme, l'Acyle cholestérol acetyle
transferase (ACAT) permet en effet d'estérifier le cholestérol
intracellulaire avec de l'acyle coenzymes A ;
-Inhiber la synthèse des récepteurs à
l'Apo B/E.
Certaines LDL ne sont pas captées par les
récepteurs à Apo B/E carelles sont modifiées, surtout par
peroxydation ou acétylation. Elles sont alors catabolisées par la
voie du récepteur « scavenger » des macrophages. Ce
récepteur n'est pas régulé par le taux de
cholestérol et le macrophage pourra absorber un excès de LDL et
se transformer en cellule spumeuse. Ce mécanisme peut être une des
causes de l'installation de la lésion athérosclérose. Ce
cholestérol libre cellulaire en excès pourra être pris en
charge par les HDL (« efflux » du cholestérol) pour être
ramené au foie et y être dégradé. [21]
4.Métabolisme des
HDL
Les HDL plasmatiques ont plusieurs origines :
- Sécrétion par l'intestin et par le foie ;
- Formation à partir des chylomicrons et des VLDL.
Au cours de la lipolyse, il y a en effet des échanges
permanents delipides et d'Apo lipoprotéines entre les différentes
classes de lipoprotéines. Phospholipides et Apo A sont
détachés de la surface des lipoprotéines riches en
triglycérides lors de la lipolyse et contribuent à la
synthèse des HDL.
Les HDL ont été divisées en quatre sous
classes : HDL1, HDL2, HDL3 et les lipoprotéines de très haute
densité (VHDL). HDL2 et HDL3 sont les plus importantes et correspondent
aux principales étapes métaboliques.
Les premières HDL libérées dans la
circulation sanguine ou HDLnaissantes secrétées par les
hépatocytes ne contiennent pas de cholestérol
estérifié. Elles ont une forme de disque. Au fur et à
mesure, la particule s'enrichit en cholestérol et phospholipides.
Après l'estérification du cholestérol par la LCAT, le
cholestérol estérifié hydrophobe se localisera au centre
et transformera le disque en sphère : les HDL3
Les HDL ont plusieurs fonctions :
- Intervenir dans la lipolyse des chylomicrons et VLDL en leur
transférant l'Apo CIL activateur de la LPL et récupérer,
après la lipolyse, des particules de phospholipides, cholestérol
libre et apoprotéines.
- Récupérer l'excès de cholestérol
libre des tissus périphériques à l'intervention d'un
récepteur spécifique à HDL. Il s'agit alors de la
sous-classe : HDL3 ;
- Echanger ce stéride ainsi formé contre des
triglycérides des LDL grâce à une protéine
permettant cet échange, la CETP (Cholesteryl Ester Transfert Protein) ;
- Ramener au foie le cholestérol des tissus non
échangé avec les triglycérides des LDL. HDL2 est donc la
vraie lipoprotéine anti cholestérol (20-30% des HDL totales).
Au niveau du foie, le cholestérol libre peut alors
être éliminé dans labile ou servir à la
synthèse des acides biliaires. La lipase hépatique, en
hydrolysant les triglycérides et les phospholipides des HDL2, permettant
leur retour dans la circulation sous forme de HDL3. [19]
DEUXIEME PARTIE : APPROCHE PRATIQUE
CHAPITRE III. CADRE
D'ÉTUDE ET APPROCHE MÉTHODOLOGIE
III.1. CADRE D'ÉTUDE
L'étude s'est déroulée au Centre
diagnostique international médical service (IMS).
Le choix de ce centre s'explique par :
- La disponibilité des données biologiques
fiables,
- L'accessibilité aux dossiers médicaux
archivés,
- Et la fréquence des demandes de bilans lipidiques dans
cette structure qui nous a permis d'avoir une proportion acceptable pour une
étude.
III.1.1. HISTORIQUE DU CENTRE
DIAGNOSTIQUE IMS
Le centre diagnostique IMS a été
créé en juillet 2023 par un arrêté
ministériel sous l'approbation et l'autorisation des autorités
tant provinciales qu'urbaines de la ville de Likasi.
Ainsi naissant, l'IMS est une structure médicale
privée d'appartenance indienne ayant une mission d'assurer un diagnostic
médical d'une multitude des maladies avec des examens
spécialisés ; entre autres des laboratoires, de
radiographies, d'échographie et des scanner numérisé.
Comme service organisés dans le domaine médical.
Grâce à sa mission, ses objectifs et ses
activités bien définies, des examens spécialisés,
d'installation du tout 1er scanner numérisé dans la
ville, du personnel mieux placé avec un savoir-faire
apprécié, l'IMS est devenu actuellement une de plus grandes
structures médicales de référence en ce qui concerne le
diagnostic des maladies et le contrôle de qualité des analyses
venant d'autres hôpitaux et centres hospitaliers de la ville de Likasi et
ses environs (soit Kambove, Lwambo, Fungurume, Kapolowe, Kakanda, et même
de Kolwezi, ...).
III.1.2. Services
organisés
III.1.2.1. Service de
pathologie
- La biochimie
- La microbiologie
- La sérologie
- L'immunologie
- La pathologie clinique
- La pathologie modulaire
- La cytogénétique.
III.2.1.2. Service de
radiologie
- Échographie
- ECG
- Doppler couleur
- Examens spéciaux
- Radiologie numérique
- Scanner.
III.1.3. Situation
géographique
Le centre diagnostique international médical service
(IS) est en République Démocratique du Congo, Province du
Haut-Katanga, dans la ville de Likasi, dans un bâtiment privé, au
N° 13 sur l'avenue du Parc prolongée, au quartier Zout dans la
commune de Likasi.
Ainsi, nous pouvons le limiter comme ceci :
Il est à côté du domicile du
général (militaire) d'Afridex.
- À son côté Es se situe l'abattoir du
quartier (Zout)
- Et du côté Ouest, le bassin de la ville de Likasi
III.1.4. Organigramme
Manager
Médecin en chef
Réception
Administrateur gestionnaire
Chef de labo
Autres service
Chef d'écho
Chef de scanner
Chef de radio
,
PRELEVEMENT
Immuno-serol
Og
i
Hematologie
Microbiologie
Parasitologie
Biochimie
Entretien
Security society
Service de menage
Transport
III.2. Population et
méthode
III.2.1. Type
d'étude
Il s'agit d'une étude rétrospective, descriptive
et transversale, basée sur l'exploitation des fiches de résultats
des patients ayant effectué un bilan lipidique.
III.2.2. Population
d'étude
Notre population d'étude est constituée des
toutes les personnes ayant réalisées un bilan lipidique
sérique au centre diagnostique international médical service
entre juillet 2023 et juin 2025 indépendamment de leur sexe ou
âge.
III.2.3.
Échantillonnage
· Technique d'échantillonnage
La technique d'échantillonnage que nous avons
utilisé est l'échantillonnage probabiliste exhaustif.
Toutes les fiches répondant aux critères
d'inclusion ont été prises en compte.
· Critère d'inclusion
- Toute personne ayant réalisé un bilan lipidique
complet durant la période d'étude au centre IMS ;
- Fiches contenant les résultats de quatre
paramètres lipidiques principaux (cholestérol Total,
HDC-cholestérol, LDL-cholestérol, triglycérides).
· Critères d'exclusion
- Fiches incomplètes ou illisibles
- Bilan lipidique partiel ou interrompu
- Bilan lipidique hors de la période d'étude.
· Taille de l'échantillon
La taille de notre échantillon est de 232 patients.
III.2.4. Collecte des
données
* Technique
Les données ont été
récoltées manuellement à partir des anciennes fiches
d'archives du laboratoire. Une fiche de collecte structurée a
été conçue pour noter les informations suivantes :
- Sexe
- Âge
- Résultats des paramètres lipides
(cholestérol total, LDL-cholestérol, HDC-cholestérol,
triglycérides).
· Matériels
- Fiche de collecte
- Le stylo
- Les papiers
- Le téléphone
III.2.5. Variables
étudiées
· Variables sociodémographiques
- Sexe
- Âge
· Variable biologique (résultats du
bilan lipidique) :
- Cholestérol total (en mg/dl)
- LDL cholestérol.
- HDC cholestérol.
- Triglycéride
III.2.8. Considérations
éthiques
- L'étude a respecté l'anonymat des patients. Aucun
nom ou information personnelle identifiable n'a été
enregistré.
- L'autorisation du centre IMS a été obtenue avant
l'exploitation des données
2.6. Analyses de
laboratoire
2.6.1 CHOLESTEROL
TOTAL
2.6.1.1 Principe de la
méthode
Le cholestérol et ses esters sont libérés
des lipoprotéines par des détergents. L'estérase de
cholestérol hydrolyse les esters et H2O2 est
formé dans l'oxydation enzymatique suivante du cholestérol par le
cholestérol oxydase selon les équations suivantes. Dans la
dernière réaction un colorant rouge de quinoneimine est
formé dont l'intensité est proportionnelle à la
concentration du cholestérol dans l'échantillon.
CHE
CHOD
Cholestérol esters + H2O
Cholestérol + acides gras
POD
Cholestérol + O
Choles-4-en-3-one + H2O
H2O2 +4-AAP + Phénol
Colorant de Quinoneimine + 2 H2O
2.6.1.2 Composition des
réactifs
|
Réactif
|
Pipes pH7,0
Phénol
2,4 dichlorophénol
Cholestérol estérase (CHE)
Cholestérol oxydase (CHOD)
Peroxydase
4 - Aminoantipyrine (4 - AAP)
|
70 mmol/l
6 mmol/l
0,5 mmol/l
400 U/l
400 U/l
1000 U/l
0,5 mmol/l
|
|
Standard
|
Cholestérol sol
|
200 /dl
|
2.6.1.3 Echantillon
Sérum ou plasma
Le cholestérol est stable 7 jours entre 2-8°C ou 3
mois à 20°c.
2.6.1.4 Procédure
1. Longueur d'onde 510 nm (500-550) ; Température
37°C/15-25°c ; cuvette trajet optique 1 cm ;
2. Ajuster le zéro de l'instrument avec de l'eau
distillée ;
3. Pipeter dans une cuvette.
|
Blanc
|
Standard
|
Echantillon
|
|
Standard
Echantillon
Réactif
|
--
--
1 ml
|
10ul
--
1 ml
|
--
10ul
1 ml
|
|
Mélanger et incuber 10 min à 37°c ou 15 min
à 15-25°c
Mesurer les absorbances (Abs) de l'échantillon et du
standard contre le tube blanc. La couleur est stable au moins 45 minutes.
|
2.6.1.5 Calcul
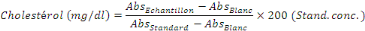
Facteur de conversion : 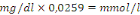 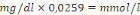
2.6.1.6 Valeur de
référence
Evaluation du risque (adultes) :
|
Moins de 200mg/dl
|
Désirables
|
|
200 - 239 mg/dl
|
Suspectes hautes
|
|
240 mg/dl et au-delà
|
Élevées
|
Ces valeurs sont données à titre indicatif.
Chaque laboratoire doit élaborer sa propre plage de
référence.
2.6.3. CHOLESTEROL HDL DIRECT
(Dosage enzymatique colorimétrique)
2.6.3.1.
Principe
Le test HDL cholestérol ne nécessite pas de
prétraitement de l'échantillon ou d'étape de
fractionnement et mesure les taux de HDLC directement en utilisant des
substances tensioactives spécialement formulés.
Le LDL, les lipoprotéines de très basse
densité (VLDL) et les chylomicrons (CM) se lient avec le polyacide
vinyle sulfonique (PVS) et le polyéthylène-glycol méthyle
ester (PEGME), qui les rendent inaccessibles à la réaction avec
le cholestérol oxydase (CHOD) et le cholestérol lestérase
(CHE). Le HDL réagit avec les enzymes pour produire du
H2O2 quantifié par la réaction de Trinder.
L'intensité de la couleur est proportionnelle à la concentration
du cholestérol HDL présent dans l'échantillon.
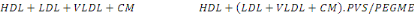
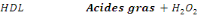

POD
CHOD/CHE
PVS/PEGME
2.6.3.2. Composition des
réactifs
|
Réactif 1
Détergent
|
Tampon MES pH 6,5 ..................................
TODB .................................................
Polyacide vinyle sulfonique (PVS) ...............
Polyéthylène glycol méthyle ester (PEGME)
...
MgCl2
.................................................
EDTA
..........................................................
Détergent
.....................................................
|
< 500 mmol/l
< 50 mmol/l
<50 g/l
< 50 g/l
< 50 mmol/l
< 10 mmol/l
< 2 %
|
|
Réactif 2
Enzymes
|
Tampon MES pH 6,5 ...............................
Cholestérol estérase (CHE)
........................
Cholestérol oxidase (POD) ........................
Peroxydase (POD) ..................................
4 - Aminoantipyrine ...............................
Détergent
.............................................
|
< 500 mmol
< 100 U/l
< 100 U/l
< 100 U/l
< 50 mmol/l
< 2 %
|
|
Réactifs additionnel (non inclus) :
|
|
Calibreur
HDL/LDL Direct
|
HVC11................................................
|
1  1 ml 1 ml
|
2.6.3.3.
Echantillons
Sérum or plasma (EDTA, citrate, Li Héparine).
Des échantillons à jeun et des échantillons pas
à jeun peuvent être utilisés.
2.6.3.4. Procédure
1. Longueur d'onde 600 nm (560 - 600) ;
Température 37°C ; Cuvette trajet optique 1 Cm
2. Ajuster le zéro de l'instrument avec de l'eau
distillée
3. Pipeter dans une cuvette :
|
Blanc
|
Standard
|
Echantillon
|
|
Standard
Echantillon
Eau Distillée
Réactif 1
|
--
--
10ul
750ul
|
10ul
--
--
750ul
|
--
10ul
--
750ul
|
|
Mélanger et incuber 5 min à 37°C
Mesurer l'absorbance (Abs 1) du calibrateur et des
échantillons par rapport au blanc.
Ajouter :
|
|
Réactif 2
|
250ul
|
250ul
|
250ul
|
|
Mélanger et mettre à incuber pendant 5 min
à 37°C
Mesurer l'absorbance (Abs 2) par rapport au blanc
|
2.6.3.5. Calcul
Calculer 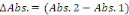 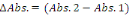
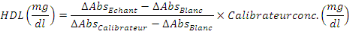
2.6.5.6. Valeurs de référence
Niveau de risque :
|
Moins de 400mg/dl
|
Elevé
|
|
40 - 59 mg/dl
|
Modérément élevé
|
|
= 60 mg/dl
|
Pas de risque
|
2.7. CHOLESTEROL LDL
(dosage enzymatique colorimétrique)
2.7.1.
Principe
Le test LDL ne nécessite pas de prétraitement de
l'échantillon ou d'étape de fractionnement et mesure les taux de
LDL-C directement en utilisant des substances tensioactives spécialement
formulées. Le dosage comprend deux étapes ; au cours de la
1ère étape, les chylomicrons, les VLDL et les HDL
sont éliminés dans les conditions spécifiques de ces
lipoprotéines. Le cholestérol dérivé de ces
lipoprotéines, mais non pas des LDL. Au cours de la
2ème étape, le LDL-C restant peut être
dosé spécifiquement comme formation de couleur (pigment quinone)
après une série de réductions enzymatiques.
2.7.2. Composition des
réactifs
|
Réactif 1
Enzymes
|
PIPES pH 7,0
Cholestérol estérase (CHE)
Cholestérol oxydase (CHOD)
Catalase
TOOS
|
50 mmol/l
= 600 U/l
= 500 U/l
= 600 KU/l
2 mmol/l
|
|
Réactif 2
Enzymes
|
PIPES Ph 7,0
4-AA
Peroxydase (POD)
|
50 mmol/l
4 mmol/l
= 4 KU/l
|
|
Calibrateur HDL/LDL
|
Sérum lyophilisé
|
Conc. Sur l'étiquette
|
2.7.3.
Echantillon
Utiliser du sérum, du plasma héparinisé
ou du plasma EDTA comme échantillon. Si un échantillon a des
précipités, centrifuger avant de son utilisation.
Stabilité : 6 jours entre 2 et 8°C. Ne pas
congeler les échantillons.
2.7.4.
Procédure
1. Longueur d'onde 600 nm (590-700) ; Température
37°C ; cuvette trajet optique 1 cm ;
2. Ajuster le zéro de l'instrument avec de l'eau
distillée ;
3. Pipeter dans une cuvette.
|
Blanc
|
Standard
|
Echantillon
|
|
Calibrateur
Echantillon
Réactif 1
|
--
--
750 ul
|
10 ul
--
750 ul
|
--
10 ul
750 ul
|
|
Mélanger et mettre à incuber pendant 5 min
à 37°C
Ajouter
|
|
Réactif 2
|
250 ul
|
250 ul
|
250 ul
|
|
Mélanger et mettre à incuber 5 min à
37°C. Mesurer l'absorbance (Abs) par rapport à un réactif
à blanc.
|
2.7.5. Calcul
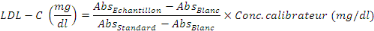
2.7.5. Valeur de
référence
Niveaux de risque :
|
Moins que 100 mg/dl
|
Normal
|
|
130 - 160 mg/dl
|
Modéré
|
|
160 mg/dl and above
|
Elevé
|
Ces valeurs sont données à titre indicatifs.
Chaque laboratoire doit élaborer sa propre plage de
référence.
2.8. Triglycéride
2.8.1. Principe de la
méthode
LPL
les triglycérides dans l'échantillon sont
hydrolysés de manière enzymatique en glycérol et acides
gras libres. Le glycérol libéré est d'abord
phosphorylé par le glycérol kinase et est ensuite oxydé
par glycérol - 3 - phosphate oxydase, libérant d'une
quantité équivalente de l'eau oxygénée
(H2O2). Le H2O2 participe à
une réaction de Trinder modifiée, qui entraîne la formation
d'un colorant quinoneimine rouge. L'intensité de la couleur
formée est proportionnelle à la concentration de
triglycérides de l'échantillon.
GK
Triglycérides + 3H2O
Glycérol + 3 acides gras
GPO
Glycérol + ATP
Glycéroles-3-phosphate + ADP
POD
Glycérol - 3 - phosphate + O2
Dihydroxyacétone - P + H2O
H2O2 + 4 - AAP + DHBS
Colorant de Quinoneimine + 2 H2O
2.8.2. Composition des
réactifs
|
Réactif
|
Pipes pH7,0
DHBS
Lipoprotein lipase (LPL)
Glycérol kinase (GK)
Glycérol - 3 - phosphate oxidase (GPO)
Peroxidase (POD)
4 - Aminoantyrine (4 - AAP)
ATP
|
50 mmol/l
1 mmol/l
1500 U/l
700 U/l
1500 U/l
2000 U/l
0,8 mmol/l
1,5 mmol/l
|
|
Standard
|
Triglycérides aqueux (en glycérol)
|
200 /dl
|
2.8.3.
Echantillon
Sérum ou plasma. Le Triglycéride est stable 5
jours entre 2-8°C.
2.8.4.
Procédure
1. Longueur d'onde 510 nm (500-550) ; Température
37°C/15-25°C ; cuvette trajet optique 1 cm ;
2. Ajuster le zéro de l'instrument avec de l'eau
distillée ;
3. Pipeter dans une cuvette.
|
Blanc
|
Standard
|
Echantillon
|
|
Standard
Echantillon
Réactif
|
--
--
1 ml
|
10ul
--
1 ml
|
--
10ul
1 ml
|
|
Mélanger et incuber 5 min à 37°C ou 10 min
à 15-25°C
Mesurer les absorbances (Abs) de l'échantillon et du
standard contre le tube blanc. La couleur est stable au moins 30 minutes.
|
2.8.4.1. Calcul
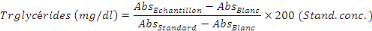
Facteur de conversion : 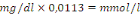 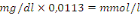
2.8.4.2. Valeur de
référence
Evaluation du risque (adultes) :
|
< 150 mg/dl
|
Normal
|
|
150 - 199 mg/dl
|
Elevé
|
|
200 - 499 mg/dl et au-delà
|
Hyperglycéridémique
|
|
> 499 mg/dl
|
Très élevé
|
Ces valeurs sont données à titre indicatif.
Chaque laboratoire doit élaborer sa propre plage de
référence.
III.2.9. Traitement et analyse
des données
Les données ont été saisie sur
l'ordinateur à l'aide du logiciel Word 2016, les résultats ont
été présentés sous forme des tableaux, puis sous
forme des graphiques grâce au logiciel Excel.
III.2.10. Difficultés
rencontrées
1. Manque de matériel technologique : l'absence d'un
téléphone ou d'un outil numérique personnel a ralenti
l'accès à l'internet, et la rédaction du travail.
2. Accès limité aux ouvrages physiques :
l'indisponibilité des ouvrages spécialisés à la
bibliothèque universitaire de Likasi (principalement des ouvrages de
biochimie biologie et physiologie) a contraint l'auteur à recourir
à des sources en ligne pour la documentation théorique.
CHAP IV : RESULTATS ET
DISCUSSION
III.1 Caractéristique
démographiques
Tableau I. Répartition des patients selon le sexe

Dans notre étude, le sexe masculin était plus
représenté avec 57% contre 43% pour le sexe féminin.
Tableau II : Répartition des patients en fonction
de l'âge.
|
Age /an
|
Fréquence
|
Pourcentage
|
|
8-28
|
20
|
8,62 %
|
|
29-48
|
95
|
41%
|
|
49-68
|
100
|
43,10%
|
|
69 et plus
|
17
|
7,33%
|
|
Total
|
232
|
100%
|
Dans notre étude, les patients de la tranche
d'âge de 49-68 sont les plus représentés.
Tableau III. Répartition des patients en fonction de la
valeur de cholestérol total et du sexe
|
Sexe
|
Normal
|
Elevé
|
Total
|
|
Masculin
|
102
|
14
|
116
|
|
Féminin
|
98
|
18
|
116
|
|
Total
|
200
|
32
|
232
|
Dans notre étude environ, 17% des patients du sexe
féminin avaient un taux de cholestérol total élevé.
TableauIV : Répartition des patients en fonction
de la valeur du cholestérol total et de la tranche d'âge
|
Tranche d'âge
|
Normal
|
Elevé
|
Total
|
|
8-28
|
20
|
5
|
25
|
|
29-48
|
90
|
11
|
101
|
|
49-68
|
77
|
13
|
90
|
|
68 et plus
|
14
|
2
|
16
|
|
Total
|
201
|
31
|
232
|
Dans notre étude, 5% des patients de la tranche
d'âge de 49-68 ans ont un taux de cholestérol total
élevé.
Tableau V. Répartition des patients en fonction de la
valeur du HDL -cholestérol et de la tranche d'âge
|
Tranche d'âge
|
HDL - cholestérol
|
|
Normal
|
Faible
|
Elevé
|
Total
|
|
8-28
|
3
|
13
|
6
|
22
|
|
29-48
|
37
|
46
|
12
|
95
|
|
49-68
|
50
|
46
|
6
|
102
|
|
69-85
|
9
|
4
|
0
|
13
|
|
Total
|
99
|
109
|
24
|
232
|
Dans notre étude, environ 21,5% des patients
âgés de 49-68 ans avaient un taux de HDL cholestérol
faible.
Tableau VI : Répartition des patients en fonction
de valeur du HDL-cholestérol et du sexe
|
Sexe
|
HDL - cholestérol
|
|
Faible
|
Normal
|
Elevé
|
Total
|
|
Masculin
|
78
|
42
|
4
|
124
|
|
Féminin
|
17
|
74
|
17
|
108
|
|
Total
|
95
|
116
|
21
|
232
|
Dans notre étude, environ 33 des patients du sexe
masculin avaient un taux de HDC cholestérol faible.
Tableau VII. Répartition des patients en fonction de la
valeur de LDL-cholestérol et du sexe
|
Sexe
|
LDL - cholestérol
|
|
Normal
|
Faible
|
Elevé
|
Total
|
|
Masculin
|
50
|
92
|
4
|
146
|
|
Féminin
|
46
|
31
|
9
|
86
|
|
Total
|
96
|
123
|
13
|
232
|
Dans notre étude, environ 9% des patients du sexe
féminin avaient un taux de LDL cholestérol élevé
(soit 92 patients /232).
Tableau VIII. Répartition des patients en fonction de
la valeur de LDL cholestérol et de la tranche d'âge.
|
Tranche d'âge
|
LDL - cholestérol
|
|
Normal
|
Faible
|
Elevé
|
Total
|
|
8-28
|
20
|
4
|
0
|
24
|
|
29-48
|
73
|
16
|
4
|
93
|
|
49-68
|
64
|
20
|
7
|
91
|
|
69-85
|
21
|
3
|
0
|
24
|
|
Total
|
178
|
43
|
11
|
232
|
Dans notre étude, environ 1,7% des patients
âgés de 20-48 ans avaient un taux de LDL cholestérol
élevé.
Tableau IX : Répartition des patients en fonction
de la valeur des triglycérides et de la tranche d'âge.
|
Tranche d'âge
|
Triglycérides
|
|
Faible
|
Normal
|
Elevé
|
Total
|
|
8-28
|
0
|
20
|
4
|
24
|
|
29-48
|
0
|
88
|
9
|
97
|
|
49-68
|
0
|
84
|
12
|
96
|
|
69-85
|
0
|
12
|
3
|
15
|
|
Total
|
0
|
204
|
28
|
232
|
Dans notre étude, environ 5% des patients de la tranche
d'âge de 49-68 ans avaient un taux de triglycérides
élevé.
Tableau X. Répartition des patients en fonction de la
valeur des triglycérides et du sexe.
|
Tranche d'âge
|
Triglycérides
|
|
Faible
|
Normal
|
Elevé
|
Total
|
|
Masculin
|
0
|
124
|
8
|
132
|
|
Féminin
|
0
|
83
|
17
|
100
|
|
Total
|
0
|
207
|
25
|
232
|
Dans notre étude, environ 34% des patients du sexe
masculin avaient un taux de triglycérides élevés.
CHAPITRE : DISCUSSION
Nous avons étudié les paramètres
lipidiques : cholestérol total, le HDL cholestérol, le LDL
cholestérol et les triglycérides chez 232 patients ayant
effectués le bilan lipide indépendamment de leur âge et
sexe sur une période qui s'étend de juillet 2023 - juin 2025.
Sur les 232 patients inclus dans l'étude, 132
étaient du sexe masculin et 100 du sexe féminin.
I. Caractéristiques
démographiques
I.1. Âge
Dans notre étude, les patients de la tranche
d'âge 49-68 ans sont les plus représentés, suivent ensuite
ceux de 29-48 ans.
I.2. Sexe
Dans notre étude, le sexe masculin était plus
représenté avec 57% contre 43% pour le sexe féminin.
Nous ne sommes pas loin de la même proportion pour le
sexe masculin que l'étude faite à l'INRSP en 1988 où les
patients du sexe masculin représentaient 61% contre 39% pour le sexe
féminin.
Et de l'étude faite à INRSP en 2015 où
les patients du sexe masculin représentaient 67% contre 33% pour le sexe
féminin. [22]
II. Les paramètres
lipidiques
II.1. Cholestérol
total
Dans notre étude, le cholestérol total est
élevé chez les patients du sexe féminin (soit 17%) contre
10,6% pour le sexe masculin.
9% des patients dont l'âge est compris entre 49-68 ans
ont un taux du cholestérol total élevé ; alors que
4,7% de patients dont l'âge est compris entre 29-48 ans ont un taux du
cholestérol total élevé.
Dans l'étude de Erem et al., le CT, LDL-C et TG
augmentent avec l'âge et plus spécifiquement dans la tranche
d'âge 60-69 ans.[23]
Au Mali, Mohamed Aly FOTANA a trouvé que 50% des
patients dont l'âge est compris entre 50-59 ans ont un taux de
cholestérol total élevé ; alors que 10% des patients
qui ont 60 ans et plus ont un cholestérol total
élevé.[24]
Nos résultats concordent avec ceux de Bensudoum et al.,
qui ont trouvés que les patients du sexe féminin ont un taux de
cholestérol supérieur à celui des patients du sexe
masculin en Côte d'Ivoire.[25]
A l'Université de Blida, Ayem Soumia et al., ont
trouvésdes résultats contraires au nôtre.[6]. Dans notre
étude, 26,9% des patients avaient un taux de cholestérol total
élevé contre 73,1% des patients qui avaient un taux de
cholestérol total normal.
Nous ne pouvons pas donner une explication scientifique
à ce phénomène, mais les facteurs environnementaux, et le
mode de vie occupe une part importante.
Dans une étude faite à l'INRSP par Dr Sanogo, le
cholestérol total augmente avec l'âge, mais chez le sexe
féminin, il est légèrement supérieur à celui
du sexe masculin. Le taux moyen de cholestérol total est de 4,23 mmol/l
pour le sexe masculin contre 4,36mmol/l pour le sexe féminin.[6]
II.2. HDL
cholestérol
Dans notre étude, le taux de HDL-cholestérol bas
est nettement plus fréquent chez les patients du sexe masculin (78/132
soit 59 ,09%) que chez les patients du sexe féminin (17/100 soit
17%). A l'analyse par tranche d'âge, la baisse de HDL cholestérol
prédomine chez les patients dont l'âge est compris entre 29-48 ans
(37 patients, soit 15,9%).
Cette distribution met en évidence l'effet cumulatif de
l'âge et du mode de vie sur le métabolisme lipidique.
Dans notre étude 40,9% des patients du sexe masculin et
féminin ont un faible taux de HDL - cholestérol.
AYEB et al., ont constatés que 50,9% des patients
avaient un faible taux de cholestérol HDL.[6]
Au mali, Mohamed. A., a trouvé des résultats
contraires au nôtre. Et dans son étude, le taux moyen de HDL
cholestérol chez le sexe masculin était plus élevé
que celui des femmes.[24]
II.3. LDL
cholestérol
La majorité des patients présente un
LDL-cholestérol inférieur aux seuils (masculin 97/
, soit /, soit 31%) des patients.
Les élévations de LDL cholestérol restent
rares (4 patients du sexe masculin, soit 3% et 9 patients du sexe
féminin soit 9%). Ce qui est encourageant mais appelle à
maintenir la surveillance.
L'évolution avec l'âge montre un pic de LDL
élevé chez les 29-48 ans (4/93, soit 4,3%) et chez les 49-68 ans
(7/91, soit 7,7%) traduisant possiblement un relâchement des mesures
diététiques.
Laforest et al., ont trouvé des résultats
contraires aux nôtres. Dans son étude, 28% des patients avaient un
taux de LDL cholestérol élevé.[27]
A l'Université de Blida, Ayeb et al., ont
trouvés que 35,2% des patients ont un taux de cholestérol
élevé. [6]
II. Les
triglycérides
Les triglycérides élevés concernent peu
la population (masculin : 8/132, soit 6% et féminin 17/100, soit
17%). L'incidence reste stable quel que soit l'âge, avec un Legé
accroissement après 49 ans (12/96, soit 12,5% chez les patients dont
l'âge est compris entre 49-68 ans.
Ayeb et al., ont trouvés 17,6% de patients qui avaient
un taux des triglycérides élevés [6].
CONCLUSION
L'étude que nous avons menée sur le bilan
lipidique de 232 patients à l'IMS sur une période allant de
juillet 2023 - juin 2025 ; a permis d'identifier plusieurs tendances
significatives concernant la santé publique de la population
examinée en tenant compte des variables de sexe et d'âge.
Nos résultats mettent en lumière des
différences importantes entre les sexes, ainsi que des variations selon
les tranches d'âges, soulignant ainsi l'importance de personnaliser les
approches préventives et thérapeutiques en matière de la
santé. Nous avons observé une surreprésentation du sexe
masculin dans notre échantillon, ce qui pourrait refléter des
comportements de santé et des facteurs de risque variés ente les
sexes. Le taux de cholestérol total était plus
élevé chez le sexe féminin, en particulier dans la tranche
d'âge de 49-68 ans. Cela soulève des préoccupations quant
à l'impact des niveaux élevés de cholestérol sur la
santé à long terme et la nécessité d'un suivi
régulier, surtout chez le sexe féminin de cette tranche
d'âge.
En ce qui concerne les lipoprotéines, notre
étude révèle une prévalence alarmante de faibles
taux de HDL-C chez les patients du sexe masculin. Ce qui accentue le risque
cardiovasculaire de cette population. A l'inverse, bien que les niveaux de la
LDL-C restent généralement en dessous des seuils
préoccupants, il est essentiel de maintenir une surveillance active, en
particulier en raison des caractéristiques démographiques
spécifiques de notre échantillon. Le fait que la majorité
des patients aient des LDL-C inférieurs aux seuils indique possiblement
une prise de conscience croissante des risques associés aux lipides
élevés, mais cela doit être accompagné d'efforts
continus en matière de sensibilisation et de prévention.
Quant aux triglycérides, bien que leur
prévalence reste relativement faible, un léger accroissement a
été noté chez les patients de plus de 49 ans. Ce qui
pourrait indiquer une tendance à surveiller.
Enfin, notre étude souligne la nécessité
d'une meilleure connaissance des déséquilibres lipides et des
facteurs de risque associés dans notre population. Les résultats
mettent en exergue l'importance de la mise en place de stratégies de
santé publique adaptées qui tiennent compte des
spécificités démographiques et biomédicales. Il est
essentiel d'encourager des comportements de vie sains, de promouvoir des
examens réguliers du bilan lipide et de sensibiliser la population aux
risques associés.
Ces mesures pourraient contribuer à une meilleure
santé lipidique et, par conséquent, à une réduction
de l'incidence des maladies cardiovasculaires dans les futures
générations.
Cette étude ouvre également la voie à des
recherches futures pour explorer en profondeur les facteurs de risque et les
impacts psychosociaux associés aux anomalies lipides, tout en soulignant
l'importance d'une approche multidisciplinaire en santé publique et en
médecine préventive.
RECOMMANDATIONS
Au terme de cette étude, nous formulons des
recommandations suivantes à l'endroit de :
a. Gouvernement :
- Faciliter l'accès aux bilans lipidiques en augmentant le
nombre des structures sanitaires pouvant réaliser ces examens.
b. La direction de l'IMS :
- Assurer la formation continue et la motivation du personnel de
l'unité biochimique pour une fiabilité des résultats des
bilans lipidiques.
c. Aux prescripteurs de ces bilans lipidiques
- Promouvoir les examens du bilan lipidique
- Encourager les patients à la pratique de l'exercice
physique surtout pour les personnes âgées.
d. A la population
- Éviter de manger trop gras, trop salé et trop
sucré ;
- Pratiquer l'activité physique à tout âge au
moins 30 minutes par jour et 3 fois par semaine ;
- S'informer au prêt des spécialistes de la
santé sur les conséquences de l'hyperlipidémie et comme
l'éviter.
e. Aux autorités universitaires
- Faciliter la recherche scientifique des étudiants en
médecine, en mettant en place des ouvrages de la médecine et
particulièrement de la biochimie et physiologie.
- Favoriser les partenariats avec d'autres institutions pour des
projets de recherches plus larges et de partage d'expertise.
BIBLIOGRAPHIE
1.Guelma [En ligne]
https://www.asace.univ-guelma.dz(jspui/bitstrem/123456789/10732/1/Nezli-ines-science,
1945.
2.« Les lipides »[en ligne]
https://www.yupu.com/fr/document/ead/21956127/les-lipides.
Page consultée le 23 avril 2025.
3. « Interpréter un bilan lipidique complet
au sein de check up » [en ligne]
https://montaigne-sante.fr/bilan-de-santé/check-up-bilan-lipidique/
4. « UnenouvellemethodepourestimerleLDLcholesterol »[Enligne]
https://www.lequotidiendumedecin.fr/specialistes/cardiologie/une-nouvelle-methode-pour-estimer-le-ldl-cholesterol/
5.« Comment faire baisser le taux du
cholestérol rapidement »[en ligne]
https://www.medecindirect.fr/maladies/cholesterol/
6. Ayem et al., « La prévalence de la
dyslipidémie et les facteurs de risque cardio vasculaire associé
chez les sujets sains obeses et non obeses » université de
blida,2015-2016.
7.« Bilan lipidique : qu'est-ce que
c'est ? »[en ligne]
https://www.futura-sciences.co/sante/definition/medecin-bilan-lipidique-14299/
8. Pr pierre Méhul, « cours de
biochimie » faculté de médicine de l'université
saint Antoine de paris
9.Dr Demmak R.G. « cours de biochimie,Structure et
métabolisme des lipoprotéines » univ salah boubnider,
constantine 3 faculté de médecine 2020-2021
10.Pr. Y.Touitou « Biochimie, structure des glucides
et des lipides » Université Pierre et Marie Curie ;
2005-2006 ; Paris
11.« lipides : définition,
rôle » [en ligne]
https://www.studysmaster.fr/resumes/biologique/corps-humain/lipides/.
12.Dr Zerriouh merien « cours de
biochimie » Université Belhadj, Bouchai bain temouchent.
Faculté de sciences, département de science de la nature et de la
vie,2019-2020.
13.« Lipide : Acide gras, lipides simples et
lipides complexes » [en ligne]
https://sientecal.com.lipides-acides-gras-ipides-simples-et-lipides-complexe.
Page consultée le 17 mars 2025.
14. Pr Lubobo C. « cours de biochimie »
université de Likasi, faculté de médecine,
2023-2024.
15.« leslipoprotéines »[en
ligne]
https://www.aquaportail.com/dictionnaire/definition/1137/lipoprteine.
16. Valdequie ; P. Biochimie clinique, Toulouse,
2ème édition, SD.
17. Pr Wele ; M. « lipide et
lipoprotéines plasmatique » 2019-2020 usTTB Bamako, mali
18. Pr Nachi M « cours de biochimie »
université salah boubnider,Constantine 2019-2020.
19. Horton, H. et al., principles of biochemistry, Bruxelles,
1ère édition, 2000
20.«Bilanlipidique :analyse,interprétationdesrésultats »[enligne]https:wwwdoctessimo.fr/html/sante/analyse/analipidique0-.htm-davidBêne.
Consulté le 17/07/2025, 20 :35.
21.Bilan lipidique : « à jeun,
valeurs normales, quand faire ? » [en ligne]
https://sante.journal-des-femmes.fr/fches-anatomie-et-examens/2837611-bilan-lipidique-indication-a-jeun-valeurs-normales.complet-interpretation/.
22.Mohamed A,«Contribution à l'étude du
bilan lipidique chez les sujets âgés de 30 ans et plus à
l'Institut National de recherche de santé publique » INRSP.
23.Erem, C., Hacihasanoglu, A., Deger, O et al. Prevalence of
dyslipidemia and associated risk
factors among Turkish adults: Trabzon lipid study. Endocr [en
ligne]. 2008.
24. Mohamed ;
A.« Contributionàl'étude du bilan lipidique chez les
sujets âgés de 30 ans et plus » ; INRSP
2015-2016
25. BENSADOUM et al., « Bilan lipidique, valeurs
moyennes, implication cardio-vasculaire » Département de
biologie clinique, service de chimie.
26. SANOGO.A et al., « contribution
àl'étude du bilan lipidique en milieu hospitalier,
INRSP » 1988
26. Laforesta.L, Souchetb.T, Moulinc.F. et al Prevalence of
low high-density lipoprotein
cholesterol and hypertriglyceridaemia in patients treated with
hypolipidaemic drugs. Archives
of Cardiovascular Disease. 2009.
TABLE DES MATIÈRES
EPIGRAPHE
i
IN MEMORIAM
ii
DEDICACE
iii
REMERCIEMENTS
iv
LISTE DES ABRÉVIATIONS
v
LISTE DES FIGURES
vi
LISTE DES TABLEAUX
vii
INTRODUCTION
1
1.ETAT DE LA QUESTION
1
2.CHOIX ET INTERETS DU SUJET
2
2.1. Intérêt personnel
2
2.2.Intérêt social
2
2.3. Intérêt scientifique
2
3.PROBLEMATIQUE
2
4.OBJECTIFS DU TRAVAIL
2
4.1. Objectif général
2
5.DELIMITATION DU SUJET
3
6.DIVISION DU TRAVAIL
3
CHAPITRE I : GENERALITES SUR LES LIPIDES
4
1.1.Définition
4
1.2.Rôles
4
A.Stockage de l'énergie
5
B.Composants structurels des cellules
5
C.Reconnaissance cellulaire
5
D.Isolation
5
E.Protection
5
F.Précurseurs pour les hormones (hormones
stérides comme les oestrogènes) ;
5
G.Dissolvent également les vitamines
liposolubles (A, D, E et K)
5
H.Facilite la digestion des vitamines liposolubles.
[12]
5
1.2.1.Rôles biologiques
5
1.3.Classification
6
1.3.1.Acides gras
7
I. Acides gras saturés
8
II. Acides gras insaturés
8
III. Acides gras essentiels et acides gras
indispensables
8
A.1.1. La nomenclature
9
A.1.2. Propriétés physiques
9
Le point de fusion
9
La solubilité des acides gras
9
A.1.3. Propriétés chimiques
10
Le groupe carboxyle
10
Les sels
11
v L'addition d'halogène (double liaison)
11
?L'hydrogénation (double liaison)
11
?L'oxydation chimique
11
L'oxydation biologique
11
1.3.1. Les lipides simples
12
I.Les acylglycérols
12
A.Propriétés physiques
13
C.Rôle biologique
13
II.Les cérides
14
Propriété
14
III.Les stérides
14
Les stérols
14
1.3.2.Lipides complexes
16
I. Les lipides phosphorés
16
I.1. Les glycérophospholipides
16
1.3.3.Lipides polyisopréniques
18
CHAPITRE II : GENERALITES SUR LES LIPOPROTEINES
21
II.1. Définition
21
II.2. Structure
21
II.3. Classification des lipoprotéines
21
II.3.1. Selon la densité
21
II.3.2. Selon la mobilité
électrophorétique
22
A.Chylomicron ;
22
II.4. Origine des lipides et des lipoprotéines
23
1.Apports lipidiques endogènes
23
2. Apports lipidiques exogènes
23
II.5. Les Apo lipoprotéines
23
II.6. Métabolisme de lipoprotéines
24
II.6.1. Métabolisme des lipoprotéines
riches en triglycérides
24
1.Origines des chylomicrons et des VLDL
24
2.Devenir des chylomicrons et VLDL
25
3.Devenir des LDL
25
4.Métabolisme des HDL
26
2.6. Analyses de laboratoire
27
2.6.1 CHOLESTEROL TOTAL
27
2.6.1.1 Principe de la méthode
27
2.6.1.2 Composition des réactifs
27
2.6.1.3 Echantillon
27
2.6.1.4 Procédure
27
2.6.1.5 Calcul
28
2.6.1.6 Valeur de référence
28
2.6.3. CHOLESTEROL HDL DIRECT (Dosage enzymatique
colorimétrique)
28
2.6.3.1. Principe
28
2.6.3.2. Composition des réactifs
29
2.6.3.3. Echantillons
29
2.7. CHOLESTEROL LDL (dosage enzymatique
colorimétrique)
30
2.7.1. Principe
30
2.7.2. Composition des réactifs
31
2.7.3. Echantillon
31
2.7.4. Procédure
31
2.7.5. Calcul
31
2.7.5. Valeur de référence
32
2.8.1. Principe de la méthode
32
2.8.2. Composition des réactifs
32
2.8.3. Echantillon
32
2.8.4. Procédure
33
2.8.4.1. Calcul
33
2.8.4.2. Valeur de référence
33
CHAPITRE III. CADRE D'ÉTUDE ET APPROCHE
MÉTHODOLOGIE
34
III.1. CADRE D'ÉTUDE
34
III.1.1. HISTORIQUE DU CENTRE DIAGNOSTIQUE IMS
34
III.1.2. Services organisés
34
III.1.2.1. Service de pathologie
34
III.2.1.2. Service de radiologie
35
III.1.3. Situation géographique
35
III.1.4. Organigramme
36
III.2. Population et méthode
37
III.2.1. Type d'étude
37
III.2.2. Population d'étude
37
III.2.3. Échantillonnage
37
III.2.4. Collecte des données
37
III.2.5. Variables étudiées
38
III.2.8. Considérations éthiques
38
III.2.9. Traitement et analyse des données
38
III.2.10. Difficultés rencontrées
38
CHAP III : RESULTATS ET DISCUSSION
39
III.1 Caractéristique démographiques
39
DISCUSSION ET COMMENTAIRES
44
I. Caractéristiques démographiques
44
I.1. Âge
44
I.2. Sexe
44
II. Les paramètres lipidiques
44
II.1. Cholestérol total
44
II.2. HDL cholestérol
45
II.3. LDL cholestérol
45
II. Les triglycérides
46
CONCLUSION
47
RECOMMANDATIONS
49
BIBLIOGRAPHIE
50
| 


