2.6.1.3 Echantillon
Sérum ou plasma
Le cholestérol est stable 7 jours entre 2-8°C ou 3
mois à 20°c.
2.6.1.4 Procédure
1. Longueur d'onde 510 nm (500-550) ; Température
37°C/15-25°c ; cuvette trajet optique 1 cm ;
2. Ajuster le zéro de l'instrument avec de l'eau
distillée ;
3. Pipeter dans une cuvette.
|
Blanc
|
Standard
|
Echantillon
|
|
Standard
Echantillon
Réactif
|
--
--
1 ml
|
10ul
--
1 ml
|
--
10ul
1 ml
|
|
Mélanger et incuber 10 min à 37°c ou 15 min
à 15-25°c
Mesurer les absorbances (Abs) de l'échantillon et du
standard contre le tube blanc. La couleur est stable au moins 45 minutes.
|
2.6.1.5 Calcul
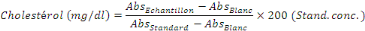
Facteur de conversion : 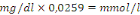 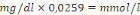
2.6.1.6 Valeur de
référence
Evaluation du risque (adultes) :
|
Moins de 200mg/dl
|
Désirables
|
|
200 - 239 mg/dl
|
Suspectes hautes
|
|
240 mg/dl et au-delà
|
Élevées
|
Ces valeurs sont données à titre indicatif.
Chaque laboratoire doit élaborer sa propre plage de
référence.
2.6.3. CHOLESTEROL HDL DIRECT
(Dosage enzymatique colorimétrique)
2.6.3.1.
Principe
Le test HDL cholestérol ne nécessite pas de
prétraitement de l'échantillon ou d'étape de
fractionnement et mesure les taux de HDLC directement en utilisant des
substances tensioactives spécialement formulés.
Le LDL, les lipoprotéines de très basse
densité (VLDL) et les chylomicrons (CM) se lient avec le polyacide
vinyle sulfonique (PVS) et le polyéthylène-glycol méthyle
ester (PEGME), qui les rendent inaccessibles à la réaction avec
le cholestérol oxydase (CHOD) et le cholestérol lestérase
(CHE). Le HDL réagit avec les enzymes pour produire du
H2O2 quantifié par la réaction de Trinder.
L'intensité de la couleur est proportionnelle à la concentration
du cholestérol HDL présent dans l'échantillon.
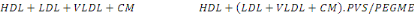
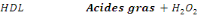

POD
CHOD/CHE
PVS/PEGME
2.6.3.2. Composition des
réactifs
|
Réactif 1
Détergent
|
Tampon MES pH 6,5 ..................................
TODB .................................................
Polyacide vinyle sulfonique (PVS) ...............
Polyéthylène glycol méthyle ester (PEGME)
...
MgCl2
.................................................
EDTA
..........................................................
Détergent
.....................................................
|
< 500 mmol/l
< 50 mmol/l
<50 g/l
< 50 g/l
< 50 mmol/l
< 10 mmol/l
< 2 %
|
|
Réactif 2
Enzymes
|
Tampon MES pH 6,5 ...............................
Cholestérol estérase (CHE)
........................
Cholestérol oxidase (POD) ........................
Peroxydase (POD) ..................................
4 - Aminoantipyrine ...............................
Détergent
.............................................
|
< 500 mmol
< 100 U/l
< 100 U/l
< 100 U/l
< 50 mmol/l
< 2 %
|
|
Réactifs additionnel (non inclus) :
|
|
Calibreur
HDL/LDL Direct
|
HVC11................................................
|
1  1 ml 1 ml
|
2.6.3.3.
Echantillons
Sérum or plasma (EDTA, citrate, Li Héparine).
Des échantillons à jeun et des échantillons pas
à jeun peuvent être utilisés.
2.6.3.4. Procédure
1. Longueur d'onde 600 nm (560 - 600) ;
Température 37°C ; Cuvette trajet optique 1 Cm
2. Ajuster le zéro de l'instrument avec de l'eau
distillée
3. Pipeter dans une cuvette :
|
Blanc
|
Standard
|
Echantillon
|
|
Standard
Echantillon
Eau Distillée
Réactif 1
|
--
--
10ul
750ul
|
10ul
--
--
750ul
|
--
10ul
--
750ul
|
|
Mélanger et incuber 5 min à 37°C
Mesurer l'absorbance (Abs 1) du calibrateur et des
échantillons par rapport au blanc.
Ajouter :
|
|
Réactif 2
|
250ul
|
250ul
|
250ul
|
|
Mélanger et mettre à incuber pendant 5 min
à 37°C
Mesurer l'absorbance (Abs 2) par rapport au blanc
|
2.6.3.5. Calcul
Calculer 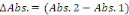 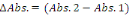
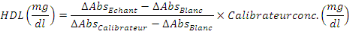
2.6.5.6. Valeurs de référence
Niveau de risque :
|
Moins de 400mg/dl
|
Elevé
|
|
40 - 59 mg/dl
|
Modérément élevé
|
|
= 60 mg/dl
|
Pas de risque
|
2.7. CHOLESTEROL LDL
(dosage enzymatique colorimétrique)
2.7.1.
Principe
Le test LDL ne nécessite pas de prétraitement de
l'échantillon ou d'étape de fractionnement et mesure les taux de
LDL-C directement en utilisant des substances tensioactives spécialement
formulées. Le dosage comprend deux étapes ; au cours de la
1ère étape, les chylomicrons, les VLDL et les HDL
sont éliminés dans les conditions spécifiques de ces
lipoprotéines. Le cholestérol dérivé de ces
lipoprotéines, mais non pas des LDL. Au cours de la
2ème étape, le LDL-C restant peut être
dosé spécifiquement comme formation de couleur (pigment quinone)
après une série de réductions enzymatiques.
2.7.2. Composition des
réactifs
|
Réactif 1
Enzymes
|
PIPES pH 7,0
Cholestérol estérase (CHE)
Cholestérol oxydase (CHOD)
Catalase
TOOS
|
50 mmol/l
= 600 U/l
= 500 U/l
= 600 KU/l
2 mmol/l
|
|
Réactif 2
Enzymes
|
PIPES Ph 7,0
4-AA
Peroxydase (POD)
|
50 mmol/l
4 mmol/l
= 4 KU/l
|
|
Calibrateur HDL/LDL
|
Sérum lyophilisé
|
Conc. Sur l'étiquette
|
2.7.3.
Echantillon
Utiliser du sérum, du plasma héparinisé
ou du plasma EDTA comme échantillon. Si un échantillon a des
précipités, centrifuger avant de son utilisation.
Stabilité : 6 jours entre 2 et 8°C. Ne pas
congeler les échantillons.
2.7.4.
Procédure
1. Longueur d'onde 600 nm (590-700) ; Température
37°C ; cuvette trajet optique 1 cm ;
2. Ajuster le zéro de l'instrument avec de l'eau
distillée ;
3. Pipeter dans une cuvette.
|
Blanc
|
Standard
|
Echantillon
|
|
Calibrateur
Echantillon
Réactif 1
|
--
--
750 ul
|
10 ul
--
750 ul
|
--
10 ul
750 ul
|
|
Mélanger et mettre à incuber pendant 5 min
à 37°C
Ajouter
|
|
Réactif 2
|
250 ul
|
250 ul
|
250 ul
|
|
Mélanger et mettre à incuber 5 min à
37°C. Mesurer l'absorbance (Abs) par rapport à un réactif
à blanc.
|
2.7.5. Calcul
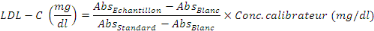
2.7.5. Valeur de
référence
Niveaux de risque :
|
Moins que 100 mg/dl
|
Normal
|
|
130 - 160 mg/dl
|
Modéré
|
|
160 mg/dl and above
|
Elevé
|
Ces valeurs sont données à titre indicatifs.
Chaque laboratoire doit élaborer sa propre plage de
référence.
2.8. Triglycéride
2.8.1. Principe de la
méthode
LPL
les triglycérides dans l'échantillon sont
hydrolysés de manière enzymatique en glycérol et acides
gras libres. Le glycérol libéré est d'abord
phosphorylé par le glycérol kinase et est ensuite oxydé
par glycérol - 3 - phosphate oxydase, libérant d'une
quantité équivalente de l'eau oxygénée
(H2O2). Le H2O2 participe à
une réaction de Trinder modifiée, qui entraîne la formation
d'un colorant quinoneimine rouge. L'intensité de la couleur
formée est proportionnelle à la concentration de
triglycérides de l'échantillon.
GK
Triglycérides + 3H2O
Glycérol + 3 acides gras
GPO
Glycérol + ATP
Glycéroles-3-phosphate + ADP
POD
Glycérol - 3 - phosphate + O2
Dihydroxyacétone - P + H2O
H2O2 + 4 - AAP + DHBS
Colorant de Quinoneimine + 2 H2O
2.8.2. Composition des
réactifs
|
Réactif
|
Pipes pH7,0
DHBS
Lipoprotein lipase (LPL)
Glycérol kinase (GK)
Glycérol - 3 - phosphate oxidase (GPO)
Peroxidase (POD)
4 - Aminoantyrine (4 - AAP)
ATP
|
50 mmol/l
1 mmol/l
1500 U/l
700 U/l
1500 U/l
2000 U/l
0,8 mmol/l
1,5 mmol/l
|
|
Standard
|
Triglycérides aqueux (en glycérol)
|
200 /dl
|
2.8.3.
Echantillon
Sérum ou plasma. Le Triglycéride est stable 5
jours entre 2-8°C.
2.8.4.
Procédure
1. Longueur d'onde 510 nm (500-550) ; Température
37°C/15-25°C ; cuvette trajet optique 1 cm ;
2. Ajuster le zéro de l'instrument avec de l'eau
distillée ;
3. Pipeter dans une cuvette.
|
Blanc
|
Standard
|
Echantillon
|
|
Standard
Echantillon
Réactif
|
--
--
1 ml
|
10ul
--
1 ml
|
--
10ul
1 ml
|
|
Mélanger et incuber 5 min à 37°C ou 10 min
à 15-25°C
Mesurer les absorbances (Abs) de l'échantillon et du
standard contre le tube blanc. La couleur est stable au moins 30 minutes.
|
2.8.4.1. Calcul
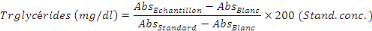
Facteur de conversion : 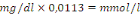 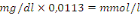
2.8.4.2. Valeur de
référence
Evaluation du risque (adultes) :
|
< 150 mg/dl
|
Normal
|
|
150 - 199 mg/dl
|
Elevé
|
|
200 - 499 mg/dl et au-delà
|
Hyperglycéridémique
|
|
> 499 mg/dl
|
Très élevé
|
Ces valeurs sont données à titre indicatif.
Chaque laboratoire doit élaborer sa propre plage de
référence.
| 


