|

REPUBLIQUE DEMOCRATIQUE DU CONGO
ENSEIGNEMENT SUPERIEUR ET UNIVERSITAIRE
UNI 50 / Lwiro
D.S. BUKAVU, PROVINCE DU SUD KIVU, RDC
(Université Publique des Sciences, Technologies et
Innovations pour le Développement)
FACULTE DES SCIENCES
Département de ZOOLOGIE


Etude de la biodiversité des insectes pollinisateurs :
cas de la région de Lwiro, Sud-Kivu, RD Congo
Mémoire présenté et défendu en vue de
l'obtention du diplôme de Bachelier en Ecologie et Gestion des Ressources
Animales
Par : TAYI KARUME Irénée
Directeur : KUSAMBA Chifundera Zacharie, Professeur
Associé
Co-Directeur : Ir RUBABURA Kituta Jean Augustin, Chef de
Travaux
ANNEE ACADEMIQUE 2021-2022

EPIGRAPHES
Un pays est à l'image de ses animaux. De la protection
qu'on leurs accorde. Si les gens ont un comportement bestial envers les
animaux, aucune démocratie ne pourra leur venir en aide. Pas plus
qu'autre chose d'ailleurs.
OLGA TOKARCZUK
Sans abeilles, en quatre ans, plus d'herbe, plus de fruits, plus
d'hommes sur terre
EINSTEIN
II
DÉDICACE
A mes Parents KARUME SHABUYANGE Zacharie et CHIKWANINE
Jeannette,
A mes Soeurs, Frères et Amis : ANDEMA IRAGI Destin, BONANE
NDATABAYI David et autres,
TAYI KARUME Irénée
III
REMERCIEMENTS
Nos remerciements s'adressent au Professeur Associé
CHIFUNDERA Kusamba Zacharie qui en dépit de ses multiples occupations a
approuvé de diriger ce présent travail, pour ses multiples
conseils et pour toutes les heures qu'il a consacrées pour nous. Nous
avons été extrêmement sensible à ses qualités
humaines d'écoute et de compréhension tout au long de ce
travail.
Au Chef de Travaux RUBABURA Kituta Jean Augustin, co-Directeur
de ce présent travail, merci de m'avoir partagé votre talent sur
la taxonomie des insectes, ainsi que pour votre soutien affectif sans
faille.
Nos remerciements s'adressent à mon père KARUME
Shabuyange Zacharie et Ma mère CHIKWANINE Migabo Jeannette pour la
volonté de nous avoir payé les frais scolaires et
académiques.
Nos gratitudes s'orientent vers nos Camarades et Compagnons de
lutte. Nous pensons à LUKOLOLA MIGEZI Claude, ISHARA MIHALI Petit
Jésus, NGALYA KYATOKEKWA Sarah et WITANDAYI LWATOMWA Crépin.
En fin nos sincères remerciements s'adressent à
nos Frères Juvénal MWIKIZANGABO, Dr MUSOLE Robert, CIRHUZA Didier
et nos Soeurs NABINTU Esther, NSHOBOLE Jémima, ZAWADI Divine et SHUKURU
Dorcas.
IV
SIGLES ET ABRÉVIATIONS
% : pourcentage
CRSN : Centre de Recherche en Sciences
Naturelles
Fam : famille
Ind : individus
MTES : Ministère de la Transition
Ecologique et Solidaire
Pi : abondance relative
PNKB : Parc National de Kahuzi-Biega RDC
: République Démocratique du Congo sp :
espèce
Uni-50 : Université du
Cinquantenaire
V
LISTE DES TABLEAUX
Tableau 1. Inventaire taxonomique et abondance relative de
l'entomofaune pollinisatrice dans la
région de Lwiro 15
Tableau 2. Richesse spécifique (S) par ordre
taxonomique au sein des trois biotopes. 18
VI
LISTE DES FIGURES
Figure 1. Appareil buccal d'une abeille à langue longue
( Eardley et al., 2010). 8
Figure 2. Localisation de sites d'échantillonnage 12
Figure 3. Proportions des ordres de l'entomofaune de Lwiro
16
Figure 4. Structure de la communauté et distribution
des abondances 17
Figure 5. Indices de Shannon, de Pielou et de Simpson dans
chaque biotope 19
Figure 6. Pourcentage de similarité entre les biotopes
20
VII
TABLE DE MATIERE
EPIGRAPHES I
DÉDICACE II
REMERCIEMENTS III
SIGLES ET ABRÉVIATIONS IV
LISTE DES TABLEAUX V
LISTE DES FIGURES VI
RESUME X
ABSTRACT XI
CHAPITRE I. INTRODUCTION 1
1.1. Aperçu général 1
1.2. La problématique 2
1.3. Questions de recherche 2
1.4. Hypothèses 3
1.5. Objectifs de la recherche 3
1.6. Choix du sujet 3
1.7. Intérêt du sujet 4
1.8. Période d'étude 4
1.9. Subdivision du travail 4
CHAPITRE II. REVUE DE LITTERATURE 5
2.1. La pollinisation 5
2.1.1. Définition de la pollinisation 5
2.1.2. Les modes de pollinisation 5
2.1.3. Importance agro-économique et écologique de
la pollinisation 6
2.2. Les différents ordres des insectes pollinisateurs
6
2.2.1. Aperçu général 6
2.2.2. Les coléoptères 6
2.2.3. Les diptères 7
2.2.4. Les lépidoptères 7
2.2.5. Les hyménoptères 7
2.3. Relation plantes-pollinisateurs 8
2.3.1. Coévolution et adaptations morphologiques 8
2.3.2. Les syndromes de pollinisation 9
VIII
2.3.3. Signaux visuels et guides nectarifères 9
CHAPITRE III. MATÉRIELS ET MÉTHODES 10
3.1. Milieu d'étude 10
3.1.1. Localisation et cadre géographique 10
3.1.2. Climat, sol et végétation 10
3.1.3. Description des sites d'échantillonnage (Biotopes)
11
3.2. Méthodologie 12
3.2.1. Échantillonnage et collecte des données
12
3.2.2. Identification taxonomique 13
3.2.3. Analyse statistique des données 13
CHAPITRE IV. PRESENTATION DES RÉSULTATS 15
4.1. Etat des lieux et Structure de l'entomofaune 15
4.1.1 Composition taxonomique globale 15
4.1.2. Richesse spécifique et abondance 17
4.2. Ecologie comparative de biotopes 18
4.3. Analyse de la stabilité et de la similarité
écologique 18
4.3.1. Equilibre des milieux 19
4.3.2. Similarité et connectivité 20
CHAPITRE V. DISCUSSION DE RESULTATS 22
5.1. Structure taxonomique des pollinisateurs et dominance des
Hyménoptères 22
5.2. Organisation des abondances et hiérarchisation des
espèces 23
5.3. Rôle structurant des jachères dans la
conservation des pollinisateurs 23
5.4. Simplification écologique des champs cultivés
24
5.5. Particularité écologique du milieu
marécageux 24
5.6. Connectivité écologique et similarité
des habitats 25
5.7. Implications pour la gestion durable des paysages agricoles
du Sud-Kivu 25
CHAPITRE VI. CONCLUSION ET RECOMMENDATIONS 26
6.1. Conclusion 26
6.2. Recommandations 26
1. Conservation des habitats semi-naturels 26
2. Promotion d'une agriculture écologiquement
intégrée 27
3. Renforcement de la recherche scientifique locale 27
4. Sensibilisation et formation 27
6.3. Perspectives de recherche 27
IX
RÉFÉRENCES BIBLIOGRAPHIQUES 28
ANNEXES 36
X
RESUME
La diversité des insectes pollinisateurs constitue un
indicateur majeur du fonctionnement écologique des
agroécosystèmes tropicaux. Dans la région de Lwiro, au
Sud-Kivu (République Démocratique du Congo), les connaissances
sur la structuration des communautés de pollinisateurs restent
limitées malgré l'importance de l'agriculture locale.
La présente étude vise à analyser la
composition taxonomique, la diversité et la similarité des
communautés d'insectes pollinisateurs dans trois biotopes
contrastés de 1 hectare chacun : une jachère, un champ
cultivé et un milieu naturel marécageux. L'échantillonnage
a été effectué à l'aide d'un filet entomologique,
et les spécimens collectés ont été
identifiés au niveau spécifique ou morphospécifique.
L'analyse écologique s'est appuyée sur les indices de
Shannon-Weaver (H'), de Simpson (D), d'équitabilité de
Piélou (J) et de similarité de Sorensen (Cs).
Les résultats révèlent une dominance
nette des Hyménoptères dans l'ensemble des biotopes, confirmant
leur rôle structurant dans les réseaux de pollinisation tropicaux.
La distribution des abondances met en évidence une organisation
caractérisée par quelques espèces dominantes et un
ensemble d'espèces rares. La jachère présente les valeurs
les plus élevées de richesse spécifique et de
diversité (indices de Shannon et de Simpson), soulignant son rôle
de réservoir écologique. Le champ cultivé affiche une
diversité réduite, traduisant un effet de simplification
lié aux pratiques agricoles. Le milieu marécageux présente
également une diversité plus faible, probablement en raison de
contraintes écologiques spécifiques.
La similarité plus élevée entre la
jachère et le champ cultivé indique une connectivité
écologique fonctionnelle au sein du paysage étudié. Ces
résultats mettent en évidence l'importance des habitats
semi-naturels pour la conservation des pollinisateurs dans les
agroécosystèmes du Sud-Kivu.
Mots-clés : insectes pollinisateurs ;
diversité spécifique ; indice de Shannon ; indice de Simpson ;
biotopes ; jachère ; Lwiro ; Sud-Kivu ; République
Démocratique du Congo.
XI
ABSTRACT
Pollinator diversity is a key indicator of ecological
functioning in tropical agroecosystems. In Lwiro, South Kivu (Democratic
Republic of the Congo), information on the structure of insect pollinator
communities remains limited despite the importance of local agriculture.
This study aimed to assess the taxonomic composition,
diversity, and similarity of insect pollinator communities across three
contrasting one-hectare habitats: fallow land, cultivated field, and natural
marsh ecosystem. Sampling was conducted using sweep nets, and collected
specimens were identified to species or morphospecies level. Ecological
analyses were based on the Shannon-Weaver index (H'), Simpson's diversity index
(D), Pielou's evenness index (J), and Sorensen's similarity index (Cs).
Results show a clear dominance of Hymenoptera across all
habitats, confirming their structuring role in tropical pollination networks.
Species abundance distribution reveals a pattern characterized by a few
dominant species and numerous rare species. Fallow land exhibited the highest
species richness and diversity values (Shannon and Simpson indices),
highlighting its function as an ecological reservoir. The cultivated field
showed lower diversity, reflecting ecological simplification associated with
agricultural practices. The marsh ecosystem also displayed reduced diversity,
likely due to specific environmental constraints.
Higher similarity between fallow land and cultivated field
indicates functional ecological connectivity within the studied landscape.
These findings emphasize the importance of semi-natural habitats for pollinator
conservation in South Kivu agroecosystems.
Keywords: insect pollinators; species
diversity; Shannon index; Simpson index; habitats; fallow land; Lwiro; South
Kivu; Democratic Republic of the Congo.
1
CHAPITRE I. INTRODUCTION
1.1. Aperçu général
Les insectes constituent un groupe important de la
biodiversité du règne animal et jouent un rôle
écologique remarquable comme bio-indicateurs de l'état des
écosystèmes (Oudjiane et al. 2014). Ils interagissent
à de multiples niveaux au sein des écosystèmes. Ils sont
alors à l'origine de différents services (Loreau, 2000 ; Lavelle
et al., 2006). D'après Wratten et al. (2007), les
milieux naturels et les agrosystèmes renferment souvent une faune
entomologique typique et riche en espèces.
Plusieurs auteurs tels qu'Andersen et al. (2002),
Hites et al. (2004), Rohr et al. (2006) cité par
Groc(2007) montrent dans leurs études que la reconnaissance des insectes
dans les processus touchant les écosystèmes et comme composants
majeurs de la biodiversité a provoqué progressivement une
augmentation significative de leur représentation. Cependant, leur
incorporation dans les études en particulier pour les
écosystèmes terrestres est plutôt considérée
comme onéreuse (Andersen et al. .2002 ; New, 1996 ; Oliver
& Beattie, 1996 ; Schnell et al., 2003 cité par
Groc,2007).
Par ailleurs, la pollinisation est un facteur clé dans
la reproduction sexuée de nombreuses espèces
végétales. La symbiose entre les insectes et les plantes permet
le maintien de la biodiversité. Il se fait grâce à la
pollinisation croisée et la pérennisation de certains
écosystèmes. Cette activité de pollinisation par les
insectes a une contribution importante dans l'amélioration de la
qualité et de la quantité des fruits et de légumes
(Vaissière, 2005).
Ainsi, la connaissance des insectes pollinisateurs des
différentes plantes cultivées est très importante. La
protection des populations d'insectes pollinisateurs devient alors plus que
nécessaire pour préserver la sécurité alimentaire
et l'état des écosystèmes.
L'Indice Planète Vivante (2020) montre que la
population animale mondiale a diminué de 68 % en moyenne en moins d'un
siècle. Le rapport Global Risks (2020) du Forum Economique Mondial
montre que les cinq défis les plus urgents auxquels l'Afrique sera
confrontée au cours de la prochaine décennie sont tous
liés à l'environnement. Ils incluent la perte de
biodiversité (WWF, 2020). D'après Peter et al. (2012)
à peu près 1,3 million d'espèces des insectes sont
décrites alors qu'ils constituent 55 % de la biodiversité animale
(Mawdsley and Stork, 1995). Leur biomasse est estimée 300 fois
supérieure à celle des autres classes du règne animal.
Selon Wilson (2008), les insectes sont décrits comme « les petites
choses qui font tourner le monde».
2
En Afrique, le déclin des espèces insectes varie
selon les espèces et plusieurs chercheurs s'accordent à dire que
les causes sont presque toutes d'origine anthropique (MTES, 2019).
1.2. La problématique
Bien que la recherche sur la diversité entomologique en
République Démocratique du Congo (RDC) ait connu un essor
significatif depuis deux décennies (Lukoki, 2021), la connaissance de
l'entomofaune demeure fragmentaire et inégalement répartie sur le
territoire national (Milau et al., 2020). À ce jour, un
déséquilibre géographique subsiste : si l'ouest du pays,
notamment Kinshasa et le Kongo-Central, ainsi que la province de la Tshopo ont
bénéficié de nombreuses investigations (Kapiamba, 1980 ;
Badjedjea, 2006 ; Desclée, 2017 ; Bukaka et al., 2020 ; Lukoki et al.,
2021), l'Est du pays, malgré les travaux récents de Rubabura et
al. (2019, 2020, 2021), reste encore largement sous-exploré.
À cette disparité géographique s'ajoute
un biais taxonomique majeur. La majorité des études se sont
focalisées sur des groupes spécifiques tels que les moustiques,
les papillons, les mouches des fruits ou les abeilles, délaissant
d'autres taxons essentiels comme les coléoptères. Pourtant, selon
Biot, (2011) ce manque de données est d'autant plus préoccupant
que les populations d'insectes subissent un déclin mondial sans
précédent sous l'effet de pressions anthropiques multiples.
Dans la province du Sud-Kivu, et plus spécifiquement
dans la région de Lwiro, le déficit de connaissances est
frappant. Si les travaux de Paul et al. (2015) sur la rivière Kalango
ont révélé une abondance exceptionnelle d'insectes dans le
groupement de Bugorhe, leur étude s'est strictement limitée
à la faune aquatique. Or, les insectes pollinisateurs, véritables
piliers de la stabilité des écosystèmes et de la
sécurité alimentaire par leur rôle dans
l'amélioration de la production agricole (Vaissière, 2015), n'ont
fait l'objet d'aucune recherche systématique dans cette
région.
1.3. Questions de recherche
Quand à cette recherche, il nous a été
d'une grande importance d'orienter les questions de la manière suivante
:
· Quels sont les insectes pollinisateurs rencontrés
à Lwiro ?
· Quelle est la composition de la biodiversité des
insectes pollinisateurs de Lwiro ?
· Existe-t-il des biotopes qui soient plus
diversifiés en insectes pollinisateurs que les autres à Lwiro
?
3
1.4. Hypothèses
De ce fait, 3 hypothèses ont été
conçues de la manière suivante ;
· La région de Lwiro serait plus
diversifiée en termes des insectes pollinisateurs qui seraient
composés des hyménoptères, des lépidoptères,
des coléoptères et des diptères,
· Au sein de la population des insectes pollinisateurs
à Lwiro, certains groupes d'insectes seraient plus abondants que les
autres dans les différents les biotopes de Lwiro,
· Certains biotopes de Lwiro seraient plus
diversifiés en insectes pollinisateurs que les autres.
1.5. Objectifs de la recherche 1.5.1. Objectif
principal
L'objectif principal de cette étude est de
caractériser la biodiversité des insectes pollinisateurs dans la
région de Lwiro
1.5.2. Objectifs Spécifiques
? Faire la prospection des biotopes et la captures des
spécimens d'insectes pollinisateurs ? Déterminer les abondances
relatives, des insectes pollinisateurs de la région de Lwiro ainsi que
la richesse spécifique de cette région en insectes
pollinisateurs
? Comparer les différents biotopes (les
jachères, les champs des cultures et milieu naturel) par le biais des
indices de biodiversité tels que l'indice de Shannon-Weaver, l'indice de
Piélou, l'indice de Simpson et l'indice de Sorensen
1.6. Choix du sujet
Le thème a été orienté sur les
insectes pollinisateurs puisqu'ils jouent plusieurs rôles dans la nature.
En effet, ils sont des bio-indicateurs des états des
écosystèmes. Plus nombreux et les plus diversifiés du
règne animal, ils interviennent dans la pollinisation chez les
végétaux ainsi que dans la chaîne tropique. Certaines
espèces sont menacés d'extinction selon la liste rouge de l'UICN
comme le cas des plusieurs espèces d'abeilles sauvages.
4
1.7. Intérêt du sujet
L'intérêt de ce travail a un triple aspect :
1.7.1. Intérêt socio-économique
L'inventaire des insectes pollinisateurs permet leur
conservation puisqu'on ne conserve pas ce qu'on ne connaît pas. Les
insectes pollinisateurs garantissent la sécurité alimentaire par
leur fonction d'améliorer la productivité chez les
végétaux.
1.7.2. Intérêt scientifique
Ce travail met en exergue la richesse spécifique des
insectes pollinisateurs de Lwiro et la manière dont ils interagissent
avec leur environnement. Le taxon des insectes est le plus diversifié du
règne animal.
1.7.3. Intérêt personnel
Personnellement, cette étude va me permettre
d'améliorer mes capacités en zoologie animale
précisément en entomologie
1.8. Période d'étude
Notre période d'étude va d'Octobre 2022 jusqu'en
décembre 2022.
1.9. Subdivision du travail
Ce présent travail est structuré en six
chapitres principaux. Le premier chapitre présente l'introduction
générale, comprenant le contexte de l'étude, la
problématique, les hypothèses, les objectifs ainsi que
l'intérêt scientifique du travail. Le deuxième chapitre est
consacré à la revue de la littérature, dans laquelle sont
développés les fondements théoriques relatifs à la
pollinisation entomophile. Le troisième chapitre décrit le milieu
d'étude et la méthodologie adoptée. Il présente la
région de Lwiro, les caractéristiques des trois biotopes
étudiés (jachère, champ cultivé et milieu naturel),
les techniques d'échantillonnage ainsi que les méthodes d'analyse
des données. Le quatrième chapitre expose les résultats
obtenus, présentés de manière descriptive et analytique
à l'aide de tableaux et figures. Le cinquième chapitre est
consacré à la discussion des résultats, en les confrontant
aux données de la littérature scientifique.
Enfin, le sixième chapitre présente la
conclusion générale du travail ainsi que les recommandations
formulées à l'issue de l'étude.
5
CHAPITRE II. REVUE DE LITTERATURE 2.1. La
pollinisation
2.1.1. Définition de la
pollinisation
La pollinisation est un mode de reproduction des plantes
angiospermes et gymnospermes. Il s'agit du processus de transport d'un grain de
pollen depuis l'étamine (organe mâle) vers les stigmates (organe
femelle). Cela peut se faire soit par autofécondation (concerne une
minorité de plantes telles que les légumineuses ou les
graminées), soit par fécondation croisée
c'est-à-dire que le grain de pollen d'une fleur se dépose sur les
stigmates d'une autre fleur de la même espèce, faisant souvent
intervenir un insecte pollinisateur (Geneves, 1992 ; Pouvreau 2004).
2.1.2. Les modes de pollinisation
Il existe trois modes de pollinisation : l'anémogamie, la
zoogamie et l'hydrogamie
· L'anémogamie : correspond au
phénomène de transport par le vent. Ce dernier va pouvoir
transporter le pollen d'une plante à l'autre. Dans 1/5ème des
cas, la fécondation se fait par cette voie
· L'hydrogamie : correspond au transport du pollen par
l'eau. Ce phénomène reste très marginal et ne concerne que
quelques plantes dont le pollen est de forme très allongée
· La zoogamie : est le transport du pollen par les
animaux. C'est le phénomène le plus courant, il concerne
4/5ème de ce cas de pollinisation. Les insectes contribuent à la
reproduction de 90% des 250000 espèces angiospermes (espèces
à fleurs) recensées dans le monde (Pouvreau, 2004). La
pollinisation par les insectes (dite pollinisation entomophile) résulte
d'un processus de coévolution. Cela se manifeste notamment par une
spécialisation des pièces buccales en fonction du pistil des
plantes à polliniser (Vaissiere et al., 2005). Plus de 1000
espèces de vertébrés participent à la pollinisation
(Colibris, chauves-souris...), auxquels s'ajoutent de très nombreux
insectes. Parmi les insectes, plusieurs ordres sont particulièrement
impliqués, comme les lépidoptères, certains
coléoptères, les diptères (syrphes notamment) et les
hyménoptères (Chagnon, 2008).
6
2.1.3. Importance agro-économique et
écologique de la pollinisation
La pollinisation entomophile est le facteur clé de la
reproduction de la majorité des angiospermes. Ecologiquement, c'est
aussi un élément primordial pour le maintien de la
diversité et de la stabilité des écosystèmes. Elle
permet un meilleur brassage génétique. Celui-ci évite la
dégénérescence. Elle permet une grande diversité et
une résistance accrue des plantes. De ce fait, les insectes
pollinisateurs jouent un rôle très important et
irremplaçable dans l'évolution des plantes sauvages et
cultivées (Vaissiere ,2002).
Par addition près de 75% des plantes angiospermes
dépendent des insectes pollinisateurs pour leur reproduction
sexuée. Les insectes pollinisateurs constituent ainsi un chainon
essentiel dans l'agriculture et la sécurité alimentaire
puisqu'elle forme le vecteur indispensable pour la dissémination de
pollen des espèces végétale (Poureau, 1987 ; Vaissiere
,2002 ; Terzo & Ramont, 2007 ; Fourmier, 2008 ; Praz et al. 2008
cités par Djebli & Nekkeche, 2016).
En fin l'apport des insectes pollinisateurs aux principales
cultures mondiales en 2005 a été évalué à
153 milliards d'euros, ce qui représente 9,5 % de la valeur de la
production alimentaire mondiale (Gallai et al., 2009).
2.2. Les différents ordres des insectes
pollinisateurs
2.2.1. Aperçu général
On distingue quatre ordres d'insectes ayant une réelle
activité sur les fleurs. Le rôle dans la pollinisation des fleurs
est lié à leurs caractéristiques morphologiques, Notamment
leurs pièces buccales. En fonction de la morphologie de celles-ci, les
insectes sont plus ou moins spécialisés dans la pollinisation de
certaines fleurs (Pouvreau, 2004).
2.2.2. Les coléoptères
Bien que les coléoptères constituent 40% des
espèces d'insectes, ils sont les insectes les moins adaptés
à la pollinisation des fleurs, en raison notamment de leurs
pièces buccales courtes et de leur poids important. L'ordre des
Coléoptères regroupe un grand nombre d'espèces xylophages
et phytophages. Les adultes peuvent aussi être floricoles (Brown,
1991)
La pollinisation par les coléoptères est ainsi
assez brutale et peut causer des dommages aux fleurs (stigmates ou pistils
endommagés). Il arrive parfois que ces insectes aient un impact
négatif sur les cultures lorsqu'ils sont trop nombreux comme c'est le
cas des cétoines par exemple (Pouvreau, 2004).
7
Les coléoptères sont caractérisés
par :
· La présence d'élytres, qui sont leurs
ailes antérieures épaisses. Elles protègent effacement
leur abdomen des agressions extérieures.
· Les ailes postérieures, se replient au repos
afin de se détendre.
· Ils disposent de mâchoires puissantes, capables
de broyer de nombreux aliments.
· Ces insectes effectuent une métamorphose
complète. C'est -à-dire qu'ils naissent sous la forme d'un oeuf.
Ils deviennent ensuite une petite larve, puis une nymphe, avant d'atteindre
l'âge adulte. Ces quatre phases de leur vie sont très
régulières chez les coléoptères (Pouvreau,
2004).
2.2.3. Les diptères
Les diptères ont la particularité de ne
posséder qu'une paire d'ailes, la seconde est modifiée et
réduite pour constituer un balancier ou haltère. L'appareil
buccal est généralement de type suceur. On distingue les
Nématocères aux antennes filiformes (moustiques) et les
Brachycères aux antennes courtes et trapues (mouches). Les larves sont
terrestres ou aquatiques, très différentes des imagos dans tous
les cas (120000 espèces dans le monde). Les diptères
possédant un labium court visitent des fleurs aux nectaires accessibles.
Certains ont un labium long qui leur permet d'accéder aux nectars moins
accessibles chez certaines fleurs avec une corolle étroite. Parmi eux
les syrphes sont de bons pollinisateurs (Pouvreau, 2004)
2.2.4. Les lépidoptères
Les Lépidoptères sont un ordre d'insectes
holométaboles dont la forme adulte (ou imago) est communément
appelée papillon et dont la larve est appelée chenille, et la
nymphe chrysalide. Ils se caractérisent à l'état adulte
par trois paires de pattes (comme tous les insectes) et par deux paires d'ailes
recouvertes d'écailles de couleurs très variées selon les
espèces. En outre, Les lépidoptères possèdent une
trompe permettant d'atteindre le nectar de fleurs très étroites,
moins accessible aux autres pollinisateurs. Ils peuvent avoir une
activité nocturne, diurne ou les deux (Pouvreau, 2004)
2.2.5. Les hyménoptères
L'ordre des hyménoptères est celui qui a le plus
d'importance en termes de pollinisation. Le rôle principal est tenu par
la super-famille des Apoïdes (Pouvreau, 2004)). Les Apoïdes
Comprennent les bourdons et les abeilles, soit 20 000 à 30 000
espèces dans le monde. Les abeilles solitaires et sauvages
représentent 85% des Espèces d'Apoïdes. Leur activité
n'est donc pas négligeable et est même plus importante que Celle
des abeilles domestiques (Campbell,
8
1995 ; Pouvreau, 2004). Les abeilles possèdent une
langue (glosse) qui leur permet de récolter le nectar des fleurs.
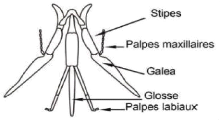
Figure 1. Appareil buccal d'une abeille à
langue longue ( Eardley et al., 2010).
2.3. Relation plantes-pollinisateurs
La relation entre les plantes et les pollinisateurs est l'un
des exemples les plus aboutis de mutualisme dans le monde vivant. Au cours de
l'évolution, les végétaux ont développé des
stratégies d'attraction sophistiquées (signaux visuels, olfactifs
et récompenses trophiques) pour assurer leur reproduction (Chittka et
Schürkens, 2001). On distingue généralement deux
stratégies adaptatives : la généralisation, où la
plante attire un large spectre de visiteurs, et la spécialisation,
où elle fidélise un groupe restreint de pollinisateurs,
augmentant ainsi l'efficacité du transfert de pollen. Dans les cas
d'hyper-spécialisation, comme le complexe figuiers-guêpes
Agaonidae, la survie des deux partenaires devient strictement
interdépendante (Cook et Rasplus, 2003).
2.3.1. Coévolution et adaptations
morphologiques
Les interactions plantes-pollinisateurs sont ancestrales. Des
découvertes de fossiles dans l'ambre suggèrent que ces relations
existaient déjà au Crétacé, il y a environ 100
millions d'années, impliquant initialement des thrips et des
gymnospermes (Peñalver et al., 2012). Cependant, c'est
l'émergence et la domination des angiospermes qui ont
accéléré la diversification des insectes.
Cette coévolution a façonné des
adaptations morphologiques remarquables. Les insectes ont
développé des pièces buccales spécialisées
(proboscis, langues allongées) et des structures de récolte comme
les corbeilles (corbiculae) ou les brosses à pollen sur les pattes
postérieures des Apidae (Michener, 2007). Ces outils permettent une
collecte optimale du nectar et du pollen tout en limitant les dommages aux
fleurs. Toutefois, cet équilibre millénaire est aujourd'hui
menacé. Le déclin rapide des populations d'insectes avec environ
40 % des espèces
9
documentées menacées d'extinction (Potts et al.,
2010) fait peser un risque systémique sur la stabilité des
écosystèmes mondiaux.
2.3.2. Les syndromes de pollinisation
L'ensemble des traits floraux (forme, taille,
accessibilité) constitue ce que les chercheurs appellent les syndromes
de pollinisation (Fenster et al., 2004). Ces traits permettent de
prédire le type de pollinisateurs associés à une plante
:
? Lépidoptères : Attirés par des fleurs
à corolle tubulaire profonde (éperons) nécessitant une
longue trompe.
? Hyménoptères et Diptères :
Préfèrent les inflorescences ouvertes et peu profondes (ex :
Asteraceae) facilitant l'accès au nectar avec une langue courte.
? Coléoptères : Souvent associés à
des fleurs robustes, aplaties et à ovaires protégés,
capables de résister à leurs pièces buccales de type
broyeur (Tautz, 2009).
2.3.3. Signaux visuels et guides
nectarifères
La communication visuelle repose sur une "signalétique"
colorée adaptée au spectre de vision des insectes. Chaque groupe
possède ses préférences : les papillons de jour
privilégient les tons vifs (bleu, rose, violet), tandis que les
papillons de nuit sont attirés par le blanc qui reflète la
luminosité nocturne. Les abeilles, quant à elles, sont sensibles
aux ultra-violets (UV) mais perçoivent le rouge comme du noir (Chittka,
1992).
Pour guider les insectes vers les zones de récolte, de
nombreuses fleurs arborent des guides nectarifères. Ces motifs, souvent
visibles uniquement dans le spectre UV, agissent comme des balises pointant
vers le centre de la fleur. Certaines plantes utilisent même des
changements chromatiques post-fécondation, comme le marronnier dont le
centre passe du jaune au rouge, signalant ainsi aux insectes que la fleur
n'offre plus de récompense (Gori, 1983).
10
CHAPITRE III. MATÉRIELS ET MÉTHODES 3.1.
Milieu d'étude
3.1.1. Localisation et cadre
géographique
La région de Lwiro tire son nom de la rivière
éponyme, un affluent du lac Kivu trouvant sa source dans le marais
Musisi, au sein du Parc National de Kahuzi-Biega (PNKB). Historiquement, cette
zone a été définie pour la première fois comme
entité écologique par Rahm et Dieterlen (1966) lors de leurs
travaux sur les muridés. Située dans le territoire de Kabare,
à environ 50 km au nord de Bukavu, la région englobe les
localités des groupements d'Irhambi et de Bugorhe. Elle est
drainée par un réseau hydrographique dense comprenant, outre la
Lwiro, des affluents tels que la Nyabachiwesa, la Kalengo et la Kamirihembe
(Beatra, 2002).
Géographiquement, elle s'étend entre 28°
45' et 28° 85' de longitude Est et 2° 15' et 2° 30' de latitude
Sud. Son altitude, marquée par un relief de collines et de
vallées, varie entre 1470 m et 2200 m à la lisière du
PNKB, sur une superficie totale de 41 km2. La population,
estimée à environ 152 000 habitants, est majoritairement
constituée d'autochtones (Rapports annuels Bugorhe et Irhambi, 2011).
3.1.2. Climat, sol et
végétation
Le milieu repose sur des sols d'origine volcanique
particulièrement fertiles. Le climat est de type tropical humide,
caractérisé par une alternance saisonnière marquée
: une longue saison des pluies de neuf mois (septembre à mai) et une
saison sèche de trois mois (juin à août). Avec une
température moyenne annuelle de 19,5 °C et une humidité
relative oscillant entre 68 % et 75 %, la région offre des conditions
optimales pour une grande diversité agricole. La
végétation originelle, aujourd'hui fragmentée, est
dominée par une savane herbeuse de montagne parsemée d'arbustes
et de graminées diversifiées (Beatra, 2002).
Sur le plan institutionnel, Lwiro est un pôle
scientifique historique abritant le Centre de Recherche en Sciences Naturelles
(CRSN, ex-IRSAC) et l'Institut National pour l'Étude et la Recherche
Agronomique (INERA) à Mulungu (Balagizi, 2010).
11
3.1.3. Description des sites d'échantillonnage
(Biotopes)
Pour cette étude, trois biotopes d'une superficie d'un
hectare chacun ont été sélectionnés afin de
comparer la diversité des pollinisateurs.
1. Le biotope de jachère
Situé dans le domaine de Muller à Bishibiru
(02° 14' 33,0" S ; 28° 48' 18,3" E), ce site se trouve à une
altitude de 1708 m. La végétation y est spontanée et
diversifiée, dominée par des espèces telles que
Viguiera dentata, Gymnanthemum coloratum, Bidens pilosa, Lantana camara,
Ocimum gratissimum, Pentas lanceolata, Kitaibelia vitifolia et Ipomoea
asarifolia.
2. Le biotope de culture
Ce site est localisé dans la zone dite «
Magnétisme » à 1687 m d'altitude (02° 15' 06,4» S
; 28° 48' 22,8» E). Contrairement au précédent, ce
milieu est anthropisé et caractérisé par une faible
diversité floristique, principalement représentée par les
cultures de haricot (Phaseolus vulgaris) et de maïs (Zea
mays).
3. Le biotope de milieu naturel
Le choix s'est porté sur le marais de Mbayo,
situé à une altitude plus élevée de 2122 m
(02° 15' 31,8" S ; 28° 45' 18,5" E). Ce milieu humide présente
une flore spécifique adaptée, comprenant notamment Carex
oshimensis, Solanum mauritianum, Canna indica, Zantedeschia aethiopica et
Bidens pilosa.
La Figure ci-dessous présente la localisation
cartographique de nos trois biotopes dans le territoire de Kabare, Province du
Sud-Kivu.
L'échantillonnage s'est déroulé sur une
période de deux mois, s'étendant du 10 octobre au 2
décembre 2022, couvrant ainsi une phase de floraison importante dans les
trois biotopes d'étude.
12
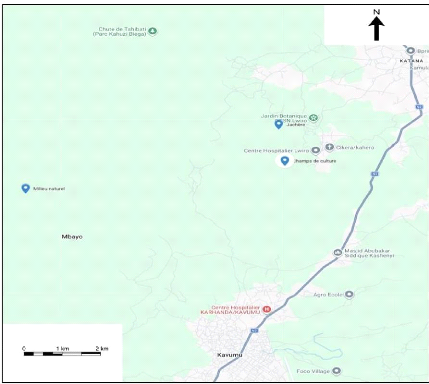
Figure 2. Localisation de sites
d'échantillonnage
Sur la figure 2, les trois points bleus avec un petit trou blanc
représentent nos trois biotopes étudiés
3.2. Méthodologie
3.2.1. Échantillonnage et collecte des
données
L'inventaire de l'entomofaune a été
réalisé par une méthode de capture active (Louis-Michel et
al., 2009). Cette technique consiste à prélever les insectes
directement sur la strate herbacée et arbustive à l'aide d'un
filet fauchoir. Ce choix méthodologique est justifié par le
caractère principalement ailé et la grande mobilité des
insectes pollinisateurs ciblés.
13
Les spécimens capturés ont été
traités selon leur groupe taxonomique :
? Insectes généraux : Conservés dans des
flacons contenant de l'éthanol à 96 % pour une conservation
optimale des caractères morphologiques.
? Lépidoptères : Placés individuellement
dans des enveloppes en papier cristal (papillotes) afin d'éviter la
dégradation de l'écaillage alaire, essentiel pour
l'identification.
3.2.2. Identification taxonomique
L'identification a été réalisée au
Laboratoire d'Entomologie Agricole du Centre de Recherche en Sciences
Naturelles (CRSN/Lwiro). Nous avons adopté l'approche Rapid Biodiversity
Assessment (RBA), qui permet de classer les spécimens par
morpho-espèces afin d'obtenir un relevé de biodiversité
complet, même en l'absence de révisions taxonomiques
récentes pour certains groupes complexes (Krell, 2004).
La détermination systématique s'est appuyée
sur :
? Des clés de détermination
spécialisées (Delvare et Aberlenc, 1989 ; Mike et al., 2004). ?
La comparaison avec les spécimens de référence
conservés dans l'insectarium du CRSN/Lwiro.
Pour l'identification de la flore associée, nous avons
combiné l'utilisation d'outils numériques de reconnaissance (Tela
Botanica, PlantNet) et la consultation des planches de l'Herbarium du CRSN.
3.2.3. Analyse statistique des données
Pour caractériser la structure et la diversité
des peuplements de pollinisateurs, les indices suivants ont été
mobilisés :
3.2.3.1. Abondance relative (Pi)
Elle exprime la proportion d'une espèce par rapport
à l'effectif total et permet de définir la composition de la
biodiversité de chaque biotope (Zaime et Gautier, 1989, cité par
Noudjoud, 2006) :
????.100
Pi=
N
Où ni représente l'effectif de l'espèce i et
N l'effectif total toutes espèces confondues.
14
3.2.3.2. Indice de diversité de Shannon-Weaver
(H')
Cet indice mesure la complexité et la diversité
spécifique du milieu en tenant compte à la fois de la richesse et
de l'équitabilité (Ramade, 2003) :
Où H' est l'indice de Shannon-Waever et Pi est la
fréquence relative de l'espèce i. La valeur maximale de cet
indice (H max) est atteinte lorsque toutes les espèces ont la même
abondance, soit Hmax = ln(S), où S est la richesse spécifique
(Marcon, 2010).
3.2.3.3. Équitabilité de Pielou
(J')
Elle permet d'évaluer la régularité de la
répartition des individus au sein des espèces d'un biotope
(Marcon, 2010).
Avec :
? J' : l'indice de Piélou
? H' : l'indice de Shannon-Weaver
? S : la richesse spécifique d'un point
L'indice J varie de 0 à 1 ; une valeur proche de 1 indique
que les espèces ont des abondances
équilibrées au sein du milieu.
3.2.3.4. Indice de similarité de Sorensen (S ou
IC)
Utilisé pour mesurer la diversité bêta, cet
indice compare la composition faunistique entre deux biotopes (Triplet, 2020)
:
2 A
K = ( 2 A + ?? + ?? ) * 100
Avec:
· A : le nombre d'espèces communes aux deux biotopes
comparés
· B : le nombre d'espèces présentes dans le
biotope B mais absentes dans le biotope C
· C : le nombre d'espèces présentes dans le
biotope C mais absentes dans le biotope B
15
CHAPITRE IV. PRESENTATION DES RÉSULTATS 4.1. Etat
des lieux et Structure de l'entomofaune
Ce premier axe d'analyse dresse le profil taxonomique global
de l'entomofaune pollinisatrice de Lwiro. Il s'agit de caractériser la
structure fondamentale du peuplement afin d'identifier les groupes biologiques
dominants de la région. Cet état des lieux constitue le socle
nécessaire à la compréhension des équilibres
écologiques avant toute analyse comparative des milieux.
4.1.1 Composition taxonomique globale
L'inventaire global réalisé dans la
région de Lwiro a permis de recenser une communauté
composée de 4 ordres, répartis en 10 familles pour un total de 34
espèces, totalisant un effectif de 554 individus (Tableau
1).
Tableau 1. Inventaire taxonomique et abondance
relative de l'entomofaune pollinisatrice dans la région de
Lwiro
Ordres Familles
|
Nombre d'espèces
|
Effectif Abondance relative (%)
|
Hymenoptera
Lepidoptera
Coleoptera Diptera
Total
|
Apidae
|
8
|
110
|
19,86
|
|
5
|
88
|
15,88
|
|
2
|
109
|
19,68
|
|
3
|
17
|
3,07
|
|
1
|
2
|
0,36
|
|
7
|
44
|
7,94
|
|
3
|
118
|
21,30
|
|
1
|
5
|
0,90
|
|
2
|
28
|
5,05
|
|
2
|
33
|
5,96
|
|
34
|
554
|
100,00
|
|
De plus, l'analyse de la structure de ce peuplement,
basée sur les abondances relatives des familles, met en évidence
une répartition inégale des abondances. La communauté est
numériquement dominée par quatre familles majeures qui
représentent, à elles seules, plus de 75 % de
l'échantillon total : les Pieridae (21,30 %), les Apidae (19,86 %), les
Formicidae (19,68 %) et les Vespidae (15,88 %). Ces groupes constituent le
socle de l'entomofaune pollinisatrice locale (Tableau 1).
16
À l'inverse, les autres familles identifiées
présentent une représentativité nettement plus faible. Les
Nymphalidae (5,96 %), les Syrphidae (5,96 %) et les Scarabaeidae (5,05 %)
apparaissent comme des composantes secondaires du système. Les familles
les moins fréquentes, telles que les Lycaenidae, noctuidae contribuent
que de manière marginale à l'abondance globale, chacune
représentant moins de 3 % de l'effectif total (Tableau
1).
Les proportions des ordres de l'entomofaune de Lwiro à
l'échelle globale sont représentées par la figure
ci-dessous :
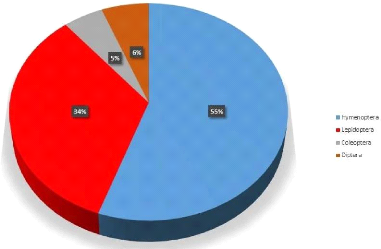
Figure 3. Proportions des ordres de l'entomofaune de
Lwiro
L'analyse du diagramme circulaire révèle une
prédominance marquée des Hyménoptères, qui
représentent à eux seuls 55 % de l'abondance totale du
peuplement. Les Lépidoptères constituent le second pôle
d'importance avec 34 % de l'effectif global. Enfin, les ordres des
Diptères (6 %) et des Coléoptères (5 %) complètent
la structure de la communauté (Figure 1).
.
17
4.1.2. Richesse spécifique et
abondance
L'analyse de la structure de la communauté,
illustrée par la courbe de rang-abondance de whitaker (Figure
4), permet d'appréhender l'organisation écologique du
peuplement au-delà de sa simple composition taxonomique. Cette courbe,
représentée sur une échelle logarithmique, offre une
vision précise du partage des ressources entre les 34 espèces
recensées.
Rang de dominance
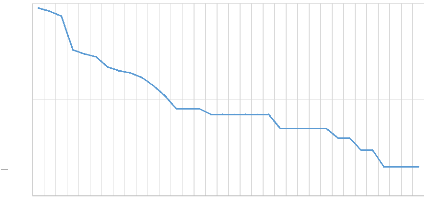
Nombre d'individus (log10)
100
10
1
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22
23 24 25 26 27 28 29 30 31 32 33 34
Figure 4. Structure de la communauté et
distribution des abondances
Le profil graphique met en évidence une structure
typique des écosystèmes tropicaux, caractérisée par
une forte disparité entre les taxons dominants et les taxons satellites.
La partie initiale de la courbe présente une pente abrupte,
révélant la présence de quelques espèces
ultra-dominantes qui concentrent l'essentiel de la biomasse numérique.
Ce phénomène de dominance est particulièrement
marqué pour les trois premiers rangs, correspondant aux espèces
Dorylus niarembensis (Formicidae), Leptidea sinapis
(Pieridae) et Apis mellifera (Apidae).
À l'opposé, la courbe s'étire en une
"longue traîne" horizontale à mesure que l'on progresse vers les
rangs supérieurs (du rang 22 au rang 34). Cette morphologie graphique
témoigne d'une proportion importante d'espèces rares,
représentées par un très faible nombre d'individus,
souvent des singletons. Les rangs des toutes les espèces sont repris en
annexe 9.
18
4.2. Ecologie comparative de biotopes
Pour mieux comprendre comment les insectes pollinisateurs se
répartissent dans le paysage de Lwiro, nous avons comparé la
richesse spécifique au sein de trois biotopes distincts : les
jachères, les champs de cultures et le milieu naturel. Cette approche
permet de mesurer l'attractivité de chaque milieu et d'identifier
précisément ceux qui abritent la plus grande diversité
d'espèces au moment de l'étude (Tableau 2).
Tableau 2. Richesse spécifique (S) par ordre
taxonomique au sein des trois biotopes.
Ordres Jachères (S)
|
Champs des cultures (S)
|
Milieu naturel S)
|
Hymenoptera Lepidoptera Coleoptera Diptera
Total (Richesse S)
|
14
|
3
|
2
|
|
4
|
5
|
|
1
|
0
|
|
1
|
0
|
|
9
|
7
|
|
Les données recueillies montrent une nette
prédominance de la jachère, qui concentre à elle seule 31
espèces, soit la grande majorité de la diversité totale
recensée. Les ordres des Hyménoptères et des
Lépidoptères y sont particulièrement bien
représentés avec respectivement 14 et 13 espèces
identifiées. En revanche, on observe un fléchissement
marqué de la richesse spécifique dans les deux autres milieux,
les champs de cultures ne comptant que 9 espèces et le milieu naturel
seulement 7. Il est également à noter que les Diptères et
les Coléoptères sont totalement absents du milieu naturel dans
nos relevés, tandis que les Hyménoptères restent le seul
groupe présent de manière constante dans l'ensemble des biotopes
étudiés, bien que leur nombre d'espèces diminue de
moitié en dehors des jachères (Tableau 2).
4.3. Analyse de la stabilité et de la
similarité écologique
L'analyse de la stabilité et de la similarité
écologique permet de passer d'un simple inventaire à une
compréhension réelle de la dynamique des milieux. L'objectif est
ici d'évaluer la santé interne de chaque biotope et de mesurer
les liens qui les unissent, afin de déterminer si
l'écosystème de Lwiro forme un ensemble cohérent et
résilient pour les insectes pollinisateurs.
19
4.3.1. Equilibre des milieux
Pour évaluer la structure interne de nos peuplements
d'insectes, il est nécessaire d'aller au-delà de la simple
présence d'espèces et d'analyser la manière dont les
individus se répartissent entre elles. L'utilisation conjointe des
indices de Shannon, de Simpson et de Pielou permet d'appréhender cet
équilibre sous trois angles complémentaires : la
complexité du milieu, la probabilité de dominance d'un groupe
précis et la régularité de la distribution globale. Cette
analyse structurelle est déterminante pour juger de la capacité
d'un biotope à maintenir une biodiversité fonctionnelle et
résiliente
3,13
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,85
|
|
|
|
|
|
0,95
|
0,91
|
|
|
|
1,3
|
|
|
|
|
|
0,81
|
0,84
|
|
0,67
|
0,67
|
|
|
|
|
|
|
|
JACHÈRES CHAMPS DE CULTURE MILIEU NATUREL
indice de shannon indice de simpson Indice de pielou
Figure 5. Indices de Shannon, de Pielou et de
Simpson dans chaque biotope
L'analyse de la figure 5 montre que la jachère est le
milieu le plus riche et le mieux structuré de notre zone d'étude.
Avec un indice de Shannon de 3,13 et une
équitabilité de Pielou de 0,91, on comprend que
les populations d'insectes y sont réparties de manière
très homogène. L'indice de Simpson vient confirmer ce constat :
il indique une faible dominance, ce qui signifie qu'aucune espèce ne
supplante les autres. La jachère offre donc un environnement stable
où la diversité peut s'exprimer pleinement.
20
À l'inverse, le milieu naturel apparaît comme le
plus fragile. Son indice de Shannon est bas (1,3) et son
équitabilité ne dépasse pas 0,67. Ici,
l'indice de Simpson suggère qu'un petit nombre d'espèces domine
largement le groupe, rendant l'écosystème moins diversifié
et plus instable. Enfin, les champs de cultures présentent un profil
intermédiaire. Bien que leur richesse soit modeste avec un Shannon de
1,85, l'indice de Pielou de 0,84 et l'indice
de Simpson de 0,81 montrent que les insectes présents y
vivent tout de même de façon assez équilibrée, sans
qu'une espèce ne devienne envahissante
4.3.2. Similarité et
connectivité
Après avoir étudié l'équilibre
interne de chaque milieu, il est crucial de comprendre comment ces biotopes
communiquent entre eux. L'indice de Sorensen nous permet ici de mesurer la
parenté faunistique, c'est-à-dire le degré de ressemblance
entre les communautés d'insectes de deux sites différents. En
identifiant la proportion d'espèces partagées, nous pouvons
évaluer la connectivité du paysage : plus l'indice est
élevé, plus les échanges d'espèces sont
facilités, ce qui témoigne d'une continuité
écologique entre les habitats.
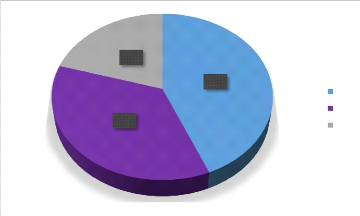
37%
21%
45%
J-C
J-M
C-M
Figure 6. Pourcentage de similarité entre les
biotopes
Les résultats de l'indice de Sorensen mettent en
évidence des niveaux d'affinité très variables selon les
milieux comparés. La similarité la plus forte est observée
entre les jachères et les champs de cultures, avec un taux de 45 %. Ce
chiffre indique que près de la moitié des espèces sont
communes à ces deux habitats, suggérant une circulation fluide
des pollinisateurs entre les zones en repos et les zones cultivées
(Figure 6).
21
À l'opposé, le lien entre les champs de
cultures et le milieu naturel est le plus faible, ne s'élevant
qu'à 21 %. Cette faible similarité montre que ces deux biotopes
abritent des communautés très différentes, avec peu
d'espèces capables de passer de l'un à l'autre. Enfin, la
comparaison entre la jachère et le milieu naturel révèle
une affinité intermédiaire de 37 % (Figure
6).
22
CHAPITRE V. DISCUSSION DE RESULTATS
5.1. Structure taxonomique des pollinisateurs et
dominance des Hyménoptères
L'inventaire réalisé dans la région de
Lwiro met en évidence une prédominance nette des
Hyménoptères au sein des communautés d'insectes
pollinisateurs échantillonnées. Cette configuration est conforme
aux observations faites dans plusieurs agroécosystèmes d'Afrique
centrale, où les Apoidea constituent le noyau fonctionnel des
réseaux de pollinisation.
En République Démocratique du Congo, les
travaux de Bukaka (2018) sur les insectes floricoles des systèmes
agricoles du Kongo Central montrent une forte représentation des
abeilles sauvages dans les milieux semi-naturels et cultivés. De
même, Lukoki et al. (2021), dans leurs analyses des interactions
plantes-pollinisateurs en RDC, soulignent que les Hyménoptères
occupent une position centrale dans les réseaux écologiques en
raison de leur efficacité de transport du pollen et de leur
fidélité florale.
La dominance observée dans la présente
étude peut s'expliquer par plusieurs facteurs écologiques dont la
plasticité trophique, la capacité de dispersion, l'organisation
sociale pour certaines espèces et aptitude à exploiter des
milieux perturbés. Milau et al. (2020), travaillant sur la
biodiversité entomologique associée aux cultures vivrières
en RDC, ont également mis en évidence que les
Hyménoptères résistent mieux aux perturbations agricoles
que d'autres ordres comme les Lépidoptères ou les
Coléoptères.
Ainsi, la structure taxonomique observée à
Lwiro s'inscrit dans une dynamique cohérente avec les tendances
décrites dans d'autres régions agroécologiques
congolaises.
Ainsi, les résultats confirment que les
jachères jouent un rôle de réservoir écologique et
de corridor biologique dans le paysage agricole de Lwiro.
23
5.2. Organisation des abondances et
hiérarchisation des espèces
La courbe rang-abondance révèle une
distribution caractérisée par quelques espèces dominantes
et un ensemble d'espèces faiblement représentées. Cette
organisation traduit une hiérarchisation écologique typique des
milieux soumis à des perturbations modérées.
Dans les agroécosystèmes tropicaux, Munyuli
(2013) a montré que la simplification du paysage favorise les
espèces généralistes, qui deviennent dominantes, tandis
que les espèces spécialistes déclinent. Les observations
faites dans la région de Lwiro corroborent cette tendance.
Bukaka (2018) note également que dans les zones
agricoles du Kongo Central, certaines espèces d'abeilles et de fourmis
présentent des abondances élevées, reflétant leur
capacité d'adaptation aux milieux anthropisés. Cette dominance
peut être interprétée comme un indicateur de
résilience écologique, mais aussi comme un signal
d'homogénéisation fonctionnelle progressive.
La présence d'espèces rares dans
l'échantillonnage peut traduire soit une spécialisation
écologique, soit une faible densité naturelle, soit une
limitation temporelle de l'étude. Lukoki et al. (2021) soulignent que
les réseaux tropicaux comportent souvent un cortège
d'espèces à faible fréquence, contribuant néanmoins
à la stabilité globale du système.
5.3. Rôle structurant des jachères dans la
conservation des pollinisateurs
Les jachères présentent les indices de
diversité les plus élevés. Ce résultat est
écologiquement significatif. Les habitats semi-naturels constituent des
zones refuges offrant une diversité floristique plus importante et une
continuité de ressources trophiques.
En RDC, Milau et al. (2020) ont montré que la
diversité entomologique est significativement plus élevée
dans les parcelles non intensifiées que dans les cultures
homogènes. De même, Munyuli (2013) a démontré que la
proximité d'habitats semi-naturels augmente la richesse et l'abondance
des pollinisateurs dans les paysages agricoles d'Afrique des Grands Lacs.
Les jachères offrent non seulement des ressources
nectarifères diversifiées, mais aussi des sites de nidification
pour les abeilles terricoles et cavicoles. Cette
hétérogénéité structurelle favorise une
meilleure équitabilité, comme le montrent les indices obtenus
dans cette étude.
24
5.4. Simplification écologique des champs
cultivés
Les champs cultivés présentent une richesse et
une diversité inférieures à celles des jachères.
Cette tendance correspond aux observations faites par Milau et al. (2020) dans
les systèmes agricoles congolais, où l'intensification
entraîne une réduction des niches écologiques
disponibles.
Bukaka (2018) souligne que les cultures à faible
diversité floristique limitent la présence des pollinisateurs
spécialistes et favorisent les espèces opportunistes. Cette
homogénéisation écologique peut réduire la
stabilité des services de pollinisation à long terme.
La dominance de quelques espèces dans les champs
étudiés suggère une sélection écologique
liée aux contraintes environnementales et aux pratiques agricoles
locales.
5.5. Particularité écologique du milieu
marécageux
Le milieu marécageux présente une
diversité plus faible que la jachère. Ce résultat peut
s'expliquer par la structure floristique spécifique des
écosystèmes hydromorphes.
Lukoki et al. (2021) indiquent que la diversité des
pollinisateurs dépend fortement de la composition végétale
et du type de syndromes de pollinisation dominants. Dans les zones humides,
certaines espèces végétales peuvent être moins
attractives pour les insectes floricoles généralistes, ce qui
limite la richesse spécifique.
Il est également possible que les conditions
microclimatiques propres aux marais influencent la distribution des
pollinisateurs, notamment en ce qui concerne la nidification des abeilles
terricoles.
25
5.6. Connectivité écologique et
similarité des habitats
La similarité plus élevée entre
jachères et champs traduit une connectivité fonctionnelle entre
ces deux milieux. Munyuli (2013) a montré que les habitats semi-naturels
agissent comme sources de recolonisation pour les parcelles cultivées
adjacentes.
Cette dynamique semble se confirmer dans le paysage
étudié. La faible similarité entre le marais et les champs
suggère une différenciation écologique liée aux
contraintes environnementales spécifiques de chaque biotope.
5.7. Implications pour la gestion durable des paysages
agricoles du Sud-Kivu
Les résultats confirment que la diversité des
pollinisateurs dépend fortement de
l'hétérogénéité paysagère. Dans le
contexte du Sud-Kivu, caractérisé par une pression
foncière croissante, la conservation des jachères apparaît
comme une stratégie prioritaire pour maintenir les services
écosystémiques.
Les travaux de Bukaka, Lukoki et Milau en RDC convergent vers
la même conclusion : la simplification des agroécosystèmes
entraîne une réduction de la diversité entomologique,
tandis que les habitats intermédiaires soutiennent la stabilité
écologique.
26
CHAPITRE VI. CONCLUSION ET RECOMMENDATIONS
6.1. Conclusion
La présente étude a permis de
caractériser la diversité et la structure des communautés
d'insectes pollinisateurs dans trois biotopes contrastés de 1 hectare
chacun situés à Lwiro, au Sud-Kivu. Les résultats mettent
en évidence une dominance marquée des Hyménoptères,
confirmant leur rôle central dans les réseaux de pollinisation
locaux. La structuration des abondances révèle une organisation
hiérarchisée, avec quelques espèces dominantes et un
cortège d'espèces rares.
La jachère apparaît comme le biotope le plus
riche et le plus diversifié, soulignant son importance écologique
comme réservoir de biodiversité et source potentielle de
recolonisation des milieux cultivés. À l'inverse, les champs
cultivés présentent une diversité réduite,
traduisant un effet de simplification associé aux pratiques agricoles.
Le milieu marécageux montre également une diversité plus
faible, probablement liée à des contraintes écologiques
spécifiques.
Dans l'ensemble, ces résultats confirment que
l'hétérogénéité paysagère constitue
un facteur déterminant du maintien des pollinisateurs dans les
agroécosystèmes du Sud-Kivu. La conservation des habitats
semi-naturels apparaît ainsi comme un levier essentiel pour
préserver les services de pollinisation.
6.2. Recommandations
Au regard des résultats obtenus, plusieurs
recommandations peuvent être formulées à l'intention des
gestionnaires, des agriculteurs et des décideurs locaux :
1. Conservation des habitats semi-naturels
? Maintenir et valoriser les jachères dans les
paysages agricoles, en évitant leur conversion systématique en
cultures permanentes.
? Encourager l'installation de bandes fleuries ou de haies
diversifiées en périphérie des parcelles
cultivées.
? Préserver les mosaïques paysagères
favorisant la connectivité écologique.
27
2. Promotion d'une agriculture écologiquement
intégrée
· Réduire l'usage non contrôlé des
pesticides susceptibles d'affecter les pollinisateurs.
· Encourager les pratiques agroécologiques
favorisant la diversification des cultures.
· Intégrer des cultures à floraison
étalée afin d'assurer une disponibilité continue des
ressources nectarifères et polliniques.
3. Renforcement de la recherche scientifique
locale
· Mettre en place un suivi pluriannuel des
communautés pollinisatrices afin d'évaluer leur dynamique
saisonnière et interannuelle.
· Diversifier les méthodes
d'échantillonnage (pièges colorés, pan traps, observation
directe) pour réduire les biais méthodologiques.
· Étudier les interactions spécifiques
plantes-pollinisateurs afin d'évaluer l'efficacité pollinisatrice
réelle des différents groupes.
4. Sensibilisation et formation
· Sensibiliser les agriculteurs à l'importance
des insectes pollinisateurs pour la productivité agricole.
· Intégrer l'éducation à la
biodiversité dans les programmes scolaires et universitaires locaux.
· Encourager la collaboration entre chercheurs,
communautés locales et autorités environnementales.
6.3. Perspectives de recherche
Des recherches futures devraient intégrer :
· Une approche fonctionnelle (taux de pollinisation,
rendement agricole associé),
· Une analyse paysagère à l'aide d'outils
de télédétection (ce qui pourrait être
particulièrement pertinent compte tenu de ton intérêt pour
la cartographie et la dynamique spatiale),
· Une évaluation de l'impact des changements
climatiques sur la phénologie des plantes et des pollinisateurs.
28
RÉFÉRENCES BIBLIOGRAPHIQUES A.
Ouvrages
1. Agosti & Johnson, N.F. Editors.2005. Antbase. World
Wide Web electronic AGOSTI Publication.
2. Bray, J.R. & Curtis, J.T.1957. An ordination of the
upland forest communities of southern Wisconsin. Ecological
Monographs, 27 : 325-349
3. Campbell, N.A.1995. Biologie. DeBoek Université.
1190p
4. Chagnon, M. (2008). Causes et effets du déclin
mondial des pollinisateurs et les moyens d'y remédier.
Fédération canadienne de la faune, Québec, 75p.
5. Delvare, G. & Aberlenc, H. (1999). Les insectes
d'Afrique et d'Amérique tropicale. Clés pour la recommandation
des familles. Clamecy : Imprimerie caballery.
6. Eardley, C., Kuhlmann, M. &Pauly, A., (2010), Les
genre et sous genre d'abeilles de l'Afrique subsaharienne. Abc taxa, Volume
9.144p
7. Jean- Prost, P. &Le Conte, Y.(2005).Apiculture,
connaitre l'abeille, conduire le Rucher. 7eme édition
Lavoisier, 698p
8. Krell, F.T. (2004). Parataxonomy vs. Taxonomy in
biodiversity studies--pitfalls and applicability of `morphospecies'
sorting, Biodiversity Conservator 13, 795- 812.
9. Laurent, C. (2013)., les fourmis : une biodiversité
méconnue. Rev. Sce. Bourgogne-Nature.18, 233-242
10. Louis -Michel, N., Christophe, B. & Philippe, B.
(2009). L'étude des insectes en forêt : Méthodes et
techniques, éléments essentiels pour standardisation. Paris.
144p.
11. Marcon, E. (2010).Mesure de la biodiversité,
écologie des forêts, 58p. CNRS, INRA.
12. Maurice, P. (1980). Initiation à la morphologie,
la systématique et la biologie des insectes. Paris. 258p
13. Michener, C.D. (2007), the hymenoptera of the world. 2eme
Ed. The Johns Hopkins UniversityPress Baltimore. 953p.
14. Mike P, Charles G & Alan W. (2004). Field Guide to
insects of South Africa. 2e édition. Stuik Nature. ISBN :
9781770070615
15. Ministère de l'Agriculture et l'Agroalimentaire au
Canada (2014). Les insectes indigènes et l'agriculture au canada,
AA121926. Version électronique disponible sur
www.agrgcca.com
16. Ndayikeza, L., Nzigidahera, B., Mpawenimana, A., Bernadette,
H.(2014). Abondance et distribution des abeilles du genre Xylocopa
Latreille, 1802 (Hymenoptera: Apoidea) du Burundi. Bull. sci. Inst.
natl. environ. conserv. nat. 11: 38-48
29
17. Pouvreau, A., 2004. Les insectes pollinisateurs. La
bibliothèque du naturaliste, 190p
18. Ramade ,F. (2003). Eléments d'écologie-
écologie fondamentale. 3e édition. Dunod. Paris
B. Articles
1. Badjedjea, B. (2006). Contribution à l'inventaire de
l'entomofaune de la réserve de la
biosphère de Yangambi (RDC). [Mémoire de
licence inédit]. Université de Kisangani. Belgique, de Suisse Et
du Grand-Duche de Luxembourg. Bull. Soc. Ent. France, 100 (H.S)
: 1-98
2. Briot, M. (2011). Menaces sur les insectes pollinisateurs.
Rapport d'information, Assemblée Nationale, France.
(Référence citée sous "Mathilde, 2011").
3. Bukaka, M. M. (2018). Diversité et abondance des
insectes floricoles dans les agroécosystèmes du Kongo Central
(République Démocratique du Congo). Revue Congolaise des Sciences
et Technologies, 4(2), 45-58.
4. Bukaka, P., Lukoki, L., & Baya, B. (2020).
Diversité et abondance des insectes associés aux cultures
maraîchères dans la zone de Kinshasa, RD Congo. Revue Marocaine
des Sciences Agronomiques et Vétérinaires, 8(2).
5. Bukaka, W., Belade, Z., Nsabatien, N. &Nagahuedi,
M.2020. Etude de la structure des communautés des abeilles sauvages
(Hymenoptera, Apoidea) de Kinshasa (R.D. Congo), cas de la Vallée de la
Funa, des Symphonies Naturelles et de Lutendele. International Journal of
Applied Research. 6(10) :941-951.
6. Chittka, L. (1992). The colour strategy of flies appearing
at flowers and various other targets. Journal of Comparative Physiology A,
170(6), 769-781.
7. Chittka, L., & Schürkens, S. (2001). Successful
invasion of North America by European bumblebees (Apis mellifera) and their
impact on native pollinators. Nature, 411, 684-687.
8. Cook, J. M., & Rasplus, J. Y. (2003). Mutualists with
attitudes: Coevolving fig wasps and figs. Trends in Ecology & Evolution,
18(5), 241-248.
9. Desclée, B. (2017). Inventaire et diversité
des insectes pollinisateurs en milieu urbain : Cas de la ville de Kinshasa.
[Thèse de doctorat].
10. Djebli, Z.E., Nekkeche, M. 2016.Inventaire des insectes
butineurs et comportement de butinage de l'abeille domestique
(Hyménoptère Apoïdea) sur deux rosacés fruitiers : le
pommier (Malus communis) et le cerisier (prumus cerasus) de la région de
Hama
30
Bouziane (Constantine). Mémoire de mastère,
Université Mentouri de Constantine. 53p
11. Fenster, C. B., Armbruster, W. S., Wilson, P., Dudash, M.
R., & Thomson, J. D. (2004). Pollination syndromes and floral
specialization. Annual Review of Ecology, Evolution, and Systematics, 35,
375-403.
12. Free, J. B., 1966. The pollination of the beans
Phaseolus multiflorus and Phaseolus vulgaris by Honeybees.
Journal of Apicultural Research, 5 : 87-91.
13. Gallai, N., Salles, J. M., Settele,J.& Vaissiere, B.
2009. Economic valuation of the vulnerability of world agriculture
confrontedwithpollinatordecline. Ecological Economics, 68 : 810-821
14. Geneves, L. 1992. Reproduction et développement
des végétaux. Bioscience Dunod, Paris. 233p
15. Gori, D. F. (1983). Post-pollination environmental and
developmental changes in flowers: Their effect on pollinator behavior. In B.
Bentley & T. Elias (Eds.), The Biology of Nectaries (pp. 31-49). Columbia
University Press.
16. Groc, S.2007. Structure taxonomique et application de la
notion de minimalisme taxonomique à la mymécofaune des Nouragues,
Guyane Française. Mémoire de Master 2 SEP (systématique,
Evolution et paléontologie, parcours systématique et
évolution). Université Pierre et Marie Curie-Paris VI, 32 p.
17. Innocent, K., Serge, N., Hermes,
M.,Trésor,M.,Alphonse ,B.,Bajope,B. et Mwapu, I. 2013. Perspectives de
gouvernance environnementale durable dans la région de Lwiro (Sud Kivu,
République Démocratique du Congo). Hors-série. Vers une
bonne gouvernance des ressources naturelles dans la région des Grands
Lacs africains
18. Jacob-Remacle, A., 1990, Abeilles sauvages et
pollinisation. Faculté des sciences Agronomiques de Gembloux.39p
19. Kapiamba, W. (1980). Étude des populations
d'insectes dans la région de Kisangani. [Mémoire de licence].
UNIKIS.
20. Kearns, C.A. 2001. North American Dipteran Pollinators:
Assessing Their Value and Conservation Status, Ecology and
Society,5
21. Lavelle, P., Decaëns, T., Aubert, M., Barot, S.,
Blouin, M., Bureau, F., Margerie, P., Mora, P. & Rossi, J.P. 2006. Soil
invertebrates and ecosystem services, European Journal of Soil Biology,
42, p 3-15.
31
22. Le Féon V. (2010). Insectes pollinisateurs dans
les paysages agricoles : approche pluri-échelle du rôle des
habitats semi-naturels, des pratiques agricoles et des cultures entomophiles.
Ecologie, Environnement.Université Rennes 1.
23. Longin, N., Benoît, N., Alexis, M. &
Habonimana,B. 2014. Abondance et distribution des abeilles du genre Xylocopa.
Latreille, 1802(hymenoptera : Apoidae) du Burundi. Bull, Sci, Nat. Environ.
Conserv. Nat. 11 :38-28
24. Loreau M. 2000. Biodiversity and ecosystem functioning:
recent theoretical advances, Oikos 91,
25. Louis, J. 1970. Etude sur les ailes des
hyménoptères. L'aile des hyménoptères
mellifères. Apidologie (4) :375-400
26. Lukoki, N., Kikufi, B. & Lukoki, L.2021. Etude des
choix floraux des pollinisateurs entomophiles. Etude des réseaux
d'interactions plantespollinisateurs : Cas du Jardin Botanique de Kisantu et de
la Vallée de la Funa. Editions Universitaires Européennes. ISBN:
978-620-2-54819-9. 2021, 111.
27. Lukoki., Joël I., Trésor B. &
Félicien L.2021. Preliminary study of the ecology and community wasps
(Hymenoptera) in the Luki Biosphere reserve (KongoCentral/Democratic Republic
of Congo). Journal of Entomology and Zoology Studies, 9(6) : 31-41
28. Mawdsley, N. &Stork, N.1995.Species extinctions in
insects: ecological and biogeographical consideration, in insects in a changing
environment, eds R. Harrington and N Stork. Academic Press,
321-369.
29. Michener, C. D. (2007). The Bees of the World (2nd ed.).
Johns Hopkins University Press.
30. Mike, P., Charles, G., & Alan, W. 2004. Insectes of
South Africa. Struck Nature. 444p
31. Milau, E., Aloni, K., Mahele, E., Lema, K.&Francis,
F. 2020.Contribution à l'étude de la biodiversité
entomologique associée à la culture de manioc (Manihot esculant
Crantz) dans le territoire de Mbanza Ngungu (RDC). Entomologie Faunistique-
Faunistic ;(73) :15-25.
32. Milau, M., Bakina, J., & Musanda, K. (2020).
Inventaire préliminaire de l'entomofaune du Kongo-Central :
Diversité et menaces. Revue Congolaise des Sciences de la Vie, 4(2).
33. Munyuli, B. T. (2011). Pollinator biodiversity in Uganda
and DR Congo agricultural landscapes: Habitat and landscape effects.
International Journal of Biodiversity and Conservation, 3(6), 217-228.
32
34. Munyuli, B. T. (2013). Drivers of pollinator biodiversity
in African agricultural systems. Journal of Insect Conservation, 17,
111-123.
of the Congo, and preliminary prospects for biological
control. Adv Plants Agric Res. 9(1):41?48.
35. Oudjiane, A., Doumandji, S., Daoudi-Hacini, S. &
Boussad, F. 2014. Biodiversity of entomological inventories in the Tigzirt
region.AFPP-Procedings of the Tenth International Conference on Agricultural
Pests, 22-23, Montoellier France, 1-7.
36. Paul, M., Arthur, M., Pascal, M.&François,
M.2015. Etude du macrofaune aquatique de la rivière Kalengo, Sud-Kivu,
République Démocratique du Congo.Vol. 13, International
Journal of Innovation and Scientific Research .388397
37. Peñalver, E., Labandeira, C. C., Barrón,
E., Delclòs, X., Nel, P., Nel, A., Tafforeau, P., & Miret, C. S.
(2012). Thrips pollination of Mesozoic gymnosperms. Proceedings of the National
Academy of Sciences (PNAS), 109(22), 8623-8628.
38. Peter, H., Linda, R. & David, M.2012.Environment.
John WileySon, l 326.
39. Potts, S. G., Biesmeijer, J. C., Kremen, C., Neumann, P.,
Schweiger, O., & Kunin, W. E. (2010). Global pollinator declines: Trends,
impacts and drivers. Trends in Ecology & Evolution, 25(6), 345-353.
40. Pouvreau, A. 2004. Les insectes pollinisateurs. Dela
chaux&Niestlé, 157 p
41. Praz, C., Carron, G. & Michez, D.2008 ;
Dasypodabraccata EVERSMANN (Hymenoptera, Dasypo-daidae), espèce nouvelle
pour la faune d'Italie. Osmia (2) :1620
42. Rahm, U. & Dieterlen, F. 1966. Les muridés de
la région de Lwiro. Bruxelles, Musée Royal de Tervuren, 41 p.
43. Rasmont, P., Ember, A.W., Benaszak, J. & Zanden, G.,
Van der. 1995. HymenopteraApoideaGallica.Liste taxonomique des abeilles de
France, de
44. Roche, M. 2014. Prévention et prise en charge des
piqûres d'hyménoptères en France Métropolitaine :
Rôle du pharmacien d'officine ; Thèse Doctorat ; Université
d`Angers France ; 18p.
45. Rubabura, J. A., Basengere, B., & Katuala, P. (2019).
Diversité des insectes dans les agro-écosystèmes du
Sud-Kivu : Cas de la région de Kabare. Revue de l'Environnement et de la
Biodiversité en RDC, 3(1).
46. Rubabura, K. JA, Munyuli, B.M.T., Bisimwa, B.E. &
Kazi, K.S. 2015. Invasive fruit fly, Ceratitis species (Diptera:
Tephritidae), pests in South Kivu region,eastern of
33
Democratic Republic of Congo, International Journal of
Innovation and Scientific Research, ISSN 2351-8014 Vol. 16 No. 2 ,
403-408
47. Rubabura, K. JA., Chihire, B.P. & Bisimwa, B.E.2019.
Diversity and abundance of fruit flies (family: Tephritidae) in the Albertine
rift zone, Democratic Republic
48. Rubabura, K.JA. & Muhigwa, B. JB. 2021. Current
status of the Solanum fruit fly Bactrocera latifrons (Hendel) in the eastern
part of Democratic Republic of Congo. Insect Environment. Vol. 24 (3),
370-380
49. Rubabura, K.JA. & Muhigwa, B. JB.2022. Infestation
Rate and Abundance of Fruit Fly Species (Diptera, Tephritidae) on Solanum
aethiopicum, Solonanum lycopersicum, and Capsicum spp in
Eastern of Democratic Republic of Congo. NASS Journal of Agricultural
Sciences. Vol.1, 21-32
50. Scheuchl,E., 1995 IllustrieteBestimmungstabellen der
WildbienenDeutschlands und Österreichs. Band I- Anthophoridae, 150p
51. Stephenw, P., Bohart, G. E. & Torchio ,P. F., 1969,
The Biology and ExternalMorphology of Bees. The Agricultural Experiment Station
and printed by the Department of Printing, Oregon State University, Corvallis,
Oregon, 140 p
52. Tautz, J. (2009). L'étonnant monde des abeilles.
Belin.
53. Vaissiere, B. 2002. Abeilles et pollinisation. Le
courrier de la Nature 196, Spécial Abeilles : 2427.
54. Vaissière, B. E. (2015). La pollinisation des
cultures par les insectes : Un service écosystémique essentiel.
Organisation des Nations Unies pour l'Alimentation et l'Agriculture (FAO).
55. Vaissiere, B., Morison, N. & Carre, G. 2005.
Abeilles, pollinisation et biodiversité. Abeilles et compagnie, 106,
5p.
56. Wilson, J., Grsiwold, T., Messinger, O.2008. Sampling Bee
Communities (Hymenoptera: Apiformes) in a desert Landscape: Are Pan Traps
Sufficient. Journal of the Kansas Entomological Society;
81(3):288-300.
57. Wratten, S.D., Gurr, G.M., Tylianakis J.M. &
Robinson, K.A. 2007. Cultural control. In van Emden, H.F. & Harrington R.
(éd.), Aphids as Crop Pests, p. 423445. CAB International, Cambridge,
Massachusetts.
34
C. Rapports
1. MTES (Ministère de la Transition Ecologique et
Solidaire), (2019). Rencontre avec les pollinisateurs, 17.
2. WWF (2020). Living Planet Report: Bending the curve of
biodiversity loss 2020.
D. TFC, Memoires; Theses
1. Armand, L. (2011). Biodiversité des abeilles de
Kinshasa : cas de l'université de Kinshasa. Mémoire de licence
2. Badjedjea, B. (2006). Contribution à l'étude
de la Biodiversité des Lépidoptères Rhopalocères de
la Réserve Forestière de MASAKO à Kisangani (R.D.Congo).
Mémoire inédit : Université de Kisangani (RDC) 2006,
31.
3. Chergui, L. (2011). Inventaire et efficacité
pollinisatrice des insectes butineurs de la courgette (Cucurbita pepo
L.) (Cucurbitaceae) et du piment (Capsicum annuum L.)
(Solanaceae. Mémoire master : faculté des sciences de la nature
et de la vie. Université des Frères Mentouri Constantine 53p.
4. Desclee, D. (2017). Vers l'intégration des
dynamiques humaines Et spatiales dans un processus systémique de
diagnostic Multidimensionnel du `Livelihoods' pour un Développement
durable : Cas d'étude de la Réserve de Biosphère de Luki
en RDC. Thèse de doctorat : Cotutelle, Université de
Kinshasa/Université catholique De Louvain (RDC).
5. Maghni, N. (2006). Contribution à la connaissance
des abeilles sauvages (Hymenoptera ; Apoidea) dans les milieux naturels et
cultivés de la région de Khenchela. Mémoire de Magister;
Université Mentouri Constantine.
6. Noudjoud, M. (2006). Contribution à la connaissance
des abeilles sauvages (Hyménoptère, Apoidea) dans les milieux
naturels et cultivés de la région de khenchela, Mémoire de
Master, Université de Constantine, 139p.
35
E. Webographie
1.
https://jardinage.lemonde.fr/dossier-1050-coleopteres-especes-insectes.html.
Consulté le 26 octobre 2022
2.
https://www.insectescomestibles.fr/content/12-les-coleopteres-qu-est-ce-qu-uncoleopteres.
Consulté le 26 octobre 2022
3.
https://www.pollinis.org/publications/plantes-et-pollinisateurs-une-histoiredamour-et-de-dependance-millenaire/.
Consulté le 07 novembre 2022
4.
https://www.pollinisateurs-nouvelle-aquitaine.fr/la-pollinisation/).Consulté
le 26 octobre 2022
5.
https://www.quelestcetanimal.com/dipteres/.
Consulté le 26 octobre 2022
6.
https://www.bonosworld.org/fr/glossaire/indice-de-sorensen.
Consulté le 03 décembre 2022
36
ANNEXES
ANNEXE 1. Calculs des indices de Shannon-Weaver et de
piélou pour les jachères
|
Espèce
|
N.ind
|
pi
|
Lnpi
|
piLnpi
|
|
Xylocopa caffra
|
3
|
0,01
|
-4,61
|
-0,05
|
|
Xylocopa nigrita
|
5
|
0,02
|
-3,91
|
-0,07
|
|
Xylocopa combusta
|
2
|
0,01
|
-4,61
|
-0,03
|
|
trigona spinepes
|
7
|
0,02
|
-3,91
|
-0,10
|
|
Apis mellifera
|
20
|
0,07
|
-2,66
|
-0,18
|
|
frieseomelitta nigra
|
5
|
0,02
|
-3,91
|
-0,07
|
|
Diadasia bituberculata
|
7
|
0,02
|
-3,91
|
-0,10
|
|
Polistes gigas
|
15
|
0,05
|
-3,00
|
-0,16
|
|
Polistes badius
|
10
|
0,03
|
-3,51
|
-0,12
|
|
Delta emarginatum
|
5
|
0,02
|
-3,91
|
-0,07
|
|
Delonogaster griseus
|
17
|
0,06
|
-2,81
|
-0,17
|
|
Delonogaster juncea
|
8
|
0,03
|
-3,51
|
-0,10
|
|
Dorylus niarembensis
|
40
|
0,14
|
-1,97
|
-0,27
|
|
Lasius niger
|
19
|
0,07
|
-2,66
|
-0,18
|
|
Asota speciosa
|
3
|
0,01
|
-4,61
|
-0,05
|
|
Paralacydes arborifera
|
7
|
0,02
|
-3,91
|
-0,10
|
|
Spilosoma lutescens
|
5
|
0,02
|
-3,91
|
-0,07
|
|
Cynthia cardui
|
6
|
0,02
|
-3,91
|
-0,08
|
|
Chalaxe jacius
|
4
|
0,01
|
-4,61
|
-0,06
|
|
Eurytela dryope
|
5
|
0,02
|
-3,91
|
-0,07
|
|
Phalantha phalantha
|
5
|
0,02
|
-3,91
|
-0,07
|
|
Acropetes turbaghia
|
2
|
0,01
|
-4,61
|
-0,03
|
|
Protogonimorpha parhassus
|
7
|
0,02
|
-3,91
|
-0,10
|
|
Melanitis leda
|
5
|
0,02
|
-3,91
|
-0,07
|
|
Belenois aurota
|
2
|
0,01
|
-4,61
|
-0,03
|
|
Leptidea sinapis
|
8
|
0,03
|
-3,51
|
-0,10
|
|
Anthene definita
|
5
|
0,02
|
-3,91
|
-0,07
|
|
Pochnoda interrupta
|
20
|
0,07
|
-2,66
|
-0,18
|
|
Taurhina splendens
|
8
|
0,03
|
-3,51
|
-0,10
|
37
|
Volucella inanis
|
22
|
0,08
|
-2,53
|
-0,19
|
|
Eristalinus taeniops
|
11
|
0,04
|
-3,22
|
-0,12
|
|
S =31
|
|
|
|
-3,13
|
|
indice de shannon-weaver
|
3,13
|
|
|
|
|
Hmax
|
3,43
|
|
|
|
|
Indice de piélou
|
0,91
|
|
|
|
ANNEXE 2. Les calculs des indices de Shannon-wear et
piélou dans les champs des cultures
|
Espèce
|
N.ind
|
pi
|
Lnpi
|
piLnpi
|
|
Apis mellifera
|
30
|
0,20
|
-1,62
|
-0,32
|
|
frieseomelitta nigra
|
3
|
0,02
|
-3,93
|
-0,08
|
|
polistes gigas
|
13
|
0,09
|
-2,46
|
-0,21
|
|
polistes badius
|
20
|
0,13
|
-2,03
|
-0,27
|
|
Dorylus niarembensis
|
50
|
0,33
|
-1,11
|
-0,37
|
|
Spilosoma lutescens
|
2
|
0,01
|
-4,33
|
-0,06
|
|
Cynthia cardui
|
8
|
0,05
|
-2,94
|
-0,15
|
|
Belenois aurota
|
7
|
0,05
|
-3,08
|
-0,14
|
|
Leptidea sinapis
|
19
|
0,13
|
-2,08
|
-0,26
|
|
S=9
|
|
|
|
-1,85
|
|
indice de shannon-weaver
|
1,85
|
|
|
|
|
Hmax
|
2,20
|
|
|
|
|
Indice de piélou
|
0,84
|
|
|
|
38
ANNEXE 3. Les calculs de l'indice de Simpson dans les
champs des cultures
|
Espèces
|
n.ind
|
(n-1)
|
n (n-1)
|
|
Apis mellifera
|
30
|
29
|
870
|
|
frieseomelitta nigra
|
3
|
2
|
6
|
|
polistes gigas
|
13
|
12
|
156
|
|
polistes badius
|
20
|
19
|
380
|
|
Dorylus niarembensis
|
50
|
49
|
2450
|
|
Spilosoma lutescens
|
2
|
1
|
2
|
|
Cynthia cardui
|
8
|
7
|
56
|
|
Belenois aurota
|
7
|
6
|
42
|
|
Leptidea sinapis
|
19
|
18
|
342
|
|
N=152
|
|
4304
|
|
N (N-1)
|
22952
|
|
|
|
? ??(??- 1)
|
0,19
|
|
|
|
N(N - 1)
|
|
Indice de simpson
|
0,81
|
|
|
ANNEXE 4. Calculs de l'indice de simpson dans les
jachères
|
Espèces
|
n.ind
|
(n-1)
|
n (n-1)
|
|
Xylocopa caffra
|
3
|
2
|
6
|
|
Xylocopa nigrita
|
5
|
4
|
20
|
|
Xylocopa combusta
|
2
|
1
|
2
|
|
trigona spinepes
|
7
|
6
|
42
|
|
Apis mellifera
|
20
|
19
|
380
|
|
frieseomelitta nigra
|
5
|
4
|
20
|
|
Diadasia bituberculata
|
7
|
6
|
42
|
|
polistes gigas
|
15
|
14
|
210
|
|
polistes badius
|
10
|
9
|
90
|
|
delta emarginatum
|
5
|
4
|
20
|
|
belonogaster griseus
|
17
|
16
|
272
|
39
|
belonogaster juncea
|
8
|
7
|
56
|
|
Dorylus niarembensis
|
40
|
39
|
1560
|
|
Lasius niger
|
19
|
18
|
342
|
|
asota speciosa
|
3
|
2
|
6
|
|
paralacydes arborifera
|
7
|
6
|
42
|
|
spilosoma lutescens
|
5
|
4
|
20
|
|
Cynthia cardui
|
6
|
5
|
30
|
|
Chalaxe jacius
|
4
|
3
|
12
|
|
Eurytela dryope
|
5
|
4
|
20
|
|
phalantha phalantha
|
5
|
4
|
20
|
|
acropetes turbaghia
|
2
|
1
|
2
|
|
Protogonimorpha parhassus
|
7
|
6
|
42
|
|
Melanitis leda
|
5
|
4
|
20
|
|
belenois aurota
|
2
|
1
|
2
|
|
leptidea sinapis
|
8
|
7
|
56
|
|
Anthene definita
|
5
|
4
|
20
|
|
Pachnoda interrupta
|
20
|
19
|
380
|
|
Taurhina splendens
|
8
|
7
|
56
|
|
Volucella inanis
|
22
|
21
|
462
|
|
Eristalinus taeniops
|
11
|
10
|
110
|
|
N=288
|
|
4362
|
|
N (N-1)
|
82656
|
|
|
|
? ??(?? - 1)
|
0,05
|
|
|
|
N(N - 1)
|
|
indice de simpson
|
0,95
|
|
|
40
ANNEXE 5. Calcul des indices de shannon et
piélou dans le milieu naturel
|
Espèce
|
N.ind
|
Pi
|
Lnpi
|
piLnpi
|
|
Xylocopa fenestrata
|
4
|
0,04
|
-3,35
|
-0,12
|
|
Apis mellifera
|
24
|
0,21
|
-1,56
|
-0,33
|
|
Grammodes exclusiva
|
2
|
0,02
|
-4,04
|
-0,07
|
|
Belenois aurota
|
24
|
0,21
|
-1,56
|
-0,33
|
|
Leptidea sinapis
|
56
|
0,49
|
-0,71
|
-0,35
|
|
Eurema hecabe
|
2
|
0,02
|
-4,04
|
-0,07
|
|
Melanitis leda
|
2
|
0,02
|
-4,04
|
-0,07
|
|
S=7
|
|
|
|
|
|
indice de shannon-weaver
|
1,3
|
|
|
|
|
Hmax
|
1,9
|
|
|
|
|
Indice de piélou
|
0,67
|
|
|
|
ANNEXE 6. Indice de Simpson milieu naturel
|
Espèces
|
n.ind
|
(n-1)
|
n (n-1)
|
|
Xylocopa fenestrata
|
4
|
3
|
12
|
|
Apis mellifera
|
24
|
23
|
552
|
|
Grammodes exclusiva
|
2
|
1
|
2
|
|
Belenois aurota
|
24
|
23
|
552
|
|
Leptidea sinapis
|
56
|
55
|
3080
|
|
Eurema hecabe
|
2
|
1
|
2
|
|
Melanitis leda
|
2
|
1
|
2
|
|
N=114
|
|
4202
|
|
N (N-1)
|
12882
|
|
|
|
? ??(??- 1)
|
0,33
|
|
|
|
N(N - 1)
|
|
Indice de simpson
|
0,67
|
|
|
41

1. Hyménoptères
Xylocopa fenestrata Xylocopa nigrita Xylocopa
caffra
Polistes gigas Apis mellifera
ANNEXE 7. Indice de Sorensen dans les différents
biotopes
|
Jachères
|
Champ des cultures
|
Milieu naturel
|
|
Jachères
|
-
|
45
|
21
|
|
Champ des cultures
|
45
|
-
|
37
|
|
Milieu naturel
|
21
|
37
|
-
|
ANNEXE 8. Quelques photos de spécimen d'insectes
capturé et identifiés.
42

2. Lépidoptères
Eurema hecabe Belenois aurota Grammodes
exclusiva
Protogonimorpha parhassus Cynthia
cardui

Leptidea sinapis Melanitis leda Phalantha
phalantha
43
3. Diptères

Volucella inanis Eristalinus
taeniops
4. Coléoptères

Taurhina splendens Pachnoda
interrupta
44
ANNEXE 9. Rangs de toutes les espèces
inventoriées
|
Rang
|
Espèces
|
Effectif
|
|
1
|
Dorylus niarembensis
|
90
|
|
2
|
Leptidea sinapis
|
83
|
|
3
|
Apis mellifera
|
74
|
|
4
|
Belenois aurota
|
33
|
|
5
|
Polistes badius
|
30
|
|
6
|
Polistes gigas
|
28
|
|
7
|
Volucella inanis
|
22
|
|
8
|
Pachnoda interrupta
|
20
|
|
9
|
Lasius niger
|
19
|
|
10
|
Belonogaster griseus
|
17
|
|
11
|
Cynthia cardui
|
14
|
|
12
|
Eristalinus taeniops
|
11
|
|
13
|
Frieseomelitta nigra
|
8
|
|
14
|
Belonogaster juncea
|
8
|
|
15
|
Taurhina splendens
|
8
|
|
16
|
Diadasia bituberculata
|
7
|
|
17
|
Trigona spinepes
|
7
|
|
18
|
Paralacydes arborifera
|
7
|
|
19
|
Spilosoma lutescens
|
7
|
|
20
|
Protogonimorpha parhassus
|
7
|
|
21
|
Melanitis leda
|
7
|
45
|
22
|
Xylocopa nigrita
|
5
|
|
23
|
Delta emarginatum
|
5
|
|
24
|
Eurytela dryope
|
5
|
|
25
|
Phalantha phalantha
|
5
|
|
26
|
Anthene definita
|
5
|
|
27
|
Xylocopa fenestrata
|
4
|
|
28
|
Chalaxe jacius
|
4
|
|
29
|
Xylocopa caffra
|
3
|
|
30
|
Asota speciosa
|
3
|
|
31
|
Xylocopa combusta
|
2
|
|
32
|
Grammodes exclusiva
|
2
|
|
33
|
Acropetes turbaghia
|
2
|
|
34
|
Eurema hecabe
|
2
|
46
ANNEXE 10. Systématique des ordres
inventoriées 1. Coléoptères et diptères
|
Ordres
|
Familles
|
Espèces
|
Jachère
|
Champs
|
Milieu naturel
|
Total
|
|
Coleoptera
|
Scarabaeidae
|
Pachnoda interrupta
|
20
|
0
|
0
|
20
|
|
Taurhina splendens
|
8
|
0
|
0
|
8
|
|
Diptera
|
Syrphidae
|
Volucella inanis
|
22
|
0
|
0
|
22
|
|
Eristalinus taeniops
|
11
|
0
|
0
|
11
|
|
Total
|
|
|
61
|
0
|
0
|
61
|
47
2. Hyménoptères
|
Ordre
|
Famille
|
Espèce
|
Jachère
|
Champs
|
Milieu naturel
|
Total
|
|
Hymenoptera
|
Apidae
|
Apis mellifera
|
20
|
30
|
24
|
74
|
|
Diadasia bituberculata
|
7
|
0
|
0
|
7
|
|
Trigona spinepes
|
7
|
0
|
0
|
7
|
|
Frieseomelitta nigra
|
5
|
3
|
0
|
8
|
|
Xylocopa nigrita
|
5
|
0
|
0
|
5
|
|
Xylocopa caffra
|
3
|
0
|
0
|
3
|
|
Xylocopa combusta
|
2
|
0
|
0
|
2
|
|
Vespidae
|
Xylocopa fenestrata
|
-
|
0
|
4
|
4
|
|
Belonogaster griseus
|
17
|
0
|
0
|
17
|
|
Polistes gigas
|
15
|
13
|
0
|
28
|
|
Polistes badius
|
10
|
20
|
0
|
30
|
|
Belonogaster juncea
|
8
|
0
|
0
|
8
|
48
|
|
Delta emarginatum
|
5
|
0
|
0
|
5
|
|
|
Dorylus niarembensis
|
40
|
50
|
0
|
90
|
|
Formicidae
|
|
|
|
|
|
|
|
Lasius niger
|
19
|
0
|
0
|
19
|
|
Total
|
|
|
163
|
116
|
28
|
307
|
3. Les lepidoptères
|
Ordres
|
Familles
|
Espèces
|
Jachère
|
Champs
|
Milieu naturel
|
Total
|
|
Lepidoptera
|
Erebidae
|
Paralacydes arborifera
|
7
|
0
|
0
|
7
|
|
Spilosoma lutescens
|
5
|
2
|
0
|
7
|
|
Asota speciosa
|
3
|
0
|
0
|
3
|
|
Noctuidae
|
Grammodes exclusiva
|
0
|
0
|
2
|
2
|
|
Nymphalidae
|
Protogonimorpha parhassus
|
7
|
0
|
0
|
7
|
|
Cynthia cardui
|
6
|
8
|
0
|
14
|
|
Eurytela dryope
|
5
|
0
|
0
|
5
|
|
Phalantha phalantha
|
5
|
0
|
0
|
5
|
|
Melanitis leda
|
5
|
0
|
2
|
7
|
|
Chalaxe jacius
|
4
|
0
|
0
|
4
|
|
Acropetes turbaghia
|
2
|
0
|
0
|
2
|
|
Pieridae
|
Leptidea sinapis
|
8
|
19
|
56
|
83
|
|
Belenois aurota
|
2
|
7
|
24
|
33
|
|
Eurema hecabe
|
0
|
0
|
2
|
2
|
|
Lycaenidae
|
Anthene definita
|
5
|
0
|
0
|
5
|
|
Total
|
|
|
64
|
36
|
86
|
186
|

49
ANNEXE 11. Les photos des plantes visitées par les
insectes pollinisateurs
Viguiera dentata Lantana camara
Ocimum gratissimum Pentas lenceolata
50

Gymnanthemum coloratum Kitaibelia
vitifolia

Bidens pilosa Ipomoea asarifolia
51

Zea mays Phaseolus vulgaris
|
|
|
Solanum mauritianum
|
|
Zantedeschia aethiopica
|

52
Canna indica
| 
