2. Principes physiques,
technologie et applications
des supercondensateurs
2. Principes physiques, technologie et applications
des supercondensateurs
2.1. Introduction
Les supercondensateurs offrent des performances en
densité de puissance supérieures à celles des batteries et
simultanément, des densités énergétiques plus
élevées que les condensateurs classiques. Leur structure
anode-cathode à base de charbon actif, permet de disposer d'une surface
active importante ce qui permet d'obtenir des valeurs de capacité
très élevées (plusieurs milliers de Farad) avec des
courants de fonctionnement pouvant être supérieurs aux centaines
d'Ampère et donc une puissance spécifique instantanée
importante. Ils peuvent être combinés avec un accumulateur
électrochimique classique et cette association offre alors l'ensemble
des propriétés des deux solutions individuelles : d'une part, une
puissance acceptable pour conserver la longévité des batteries et
d'autre part une puissance instantanée élevée pour des
demandes occasionnelles [1].
2.2. Principes physiques
Les supercondensateurs peuvent stocker l'énergie par
deux processus. Le premier est la séparation des charges positives et
négatives à l'interface entre l'électrode solide et
l'électrolyte liquide (stockage électrostatique). Ce
phénomène s'appelle la capacité de double couche. Le
deuxième emmagasine les charges par des réactions faradiques
réversibles (réactions de transfert d'électrons entre les
électrodes et l'électrolyte) (stockage électrochimique
comme dans les batteries) [2, 3].
2.2.1. Double couche électrique
Un supercondensateur est composé de deux
électrodes, d'un électrolyte et d'un séparateur (cf. fig.
2-1). Lorsqu'il chargé, la répartition des charges entre une
électrode (conducteur ou semi-conducteur) et un électrolyte
(liquide ou solide ) permet la création de deux couches : une
composée de charge positives dans l'électrode et des charges
négatives (anions) dans l'électrolyte, et une autre
composée des charges négatives (électrons) dans
l'électrode et des charges positives (cations) dans
l'électrolyte.
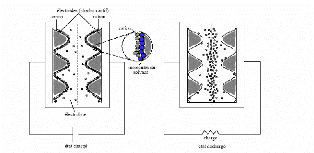
Fig. 2-1 : Structure interne des supercondensateurs
à double couche électrique [4]
Le principe de base des supercondensateurs repose sur les
propriétés capacitives de l'interface entre un conducteur
électronique solide et un conducteur ionique. Le stockage
d'énergie s'effectue par distribution des ions d'électrolyte au
voisinage de la surface de chaque électrode, sous l'influence
électrostatique de la tension appliquée. Il se crée ainsi
aux interfaces une zone de charge d'espace, appelée double couche
électrique, d'épaisseur limitée à quelques
nanomètres, et dans laquelle règne un champ électrique
relativement intense [4, 5].
Pour comprendre les processus électriques qui se
produisent dans une double couche électrique, plusieurs modèles
sont développés pour expliquer ce phénomène.
Le modèle de Helmholtz modélise la nature
capacitive de l'interface entre un condensateur électrique solide et un
conducteur ionique liquide et considère que les charges
accumulées à l'interface forment un plan parallèle
à celle-ci (cf. fig. 2-2-a) : nous parlons de plan de Helmholtz. Le
calcul de la capacité surfacique C de la double couche est
calculé par C=å/d avec å
la permittivité diélectrique du solvant et d
l'épaisseur de la double couche assimilable dans ce cas au
diamètre moléculaire du solvant. Cependant, ce modèle est
linaire et ne prend pas en compte la variation de capacité en fonction
de la tension appliquée, ce qui induit une valeur de C
supérieure d'un ordre à la valeur mesurée
réellement [5].
Avec le modèle de Gouy-Champman, la double couche ne se
limite pas au seul plan de Helmholtz, mais prend en compte une distribution
volumique de charges dans l'électrolyte connue aujourd'hui sous le nom
de couche diffusée (cf. fig. 2-2-b). Il est établi que dans le
cas d'un profil unidirectionnel de champ électrique, la capacité
surfacique de l'interface entre électrode et électrolyte est
donnée par la relation suivante [5] :

2 qn å ? Ø
z . 0 2-1
0
C z
= .
d
?
. ch ? ?
u T ? 2 . u T ?
avec, ø0 le potentiel de surface, z
la valence des ions, n0 la concentration en anions et cations à
l'équilibre thermodynamique, å la permittivité
diélectrique de l'électrolyte, q la charge
électrique élémentaire, k la constante de
Boltzmann, è la température et uT
l'unité de potentiel thermodynamique (uT =
k.è/q) [5] .
Le modèle le plus utilisé est celui de
Gouy-Chapman-Stern qui combine les deux modèles en faisant intervenir la
couche dense de Helmholtz (appelée alors couche de Stern) et la couche
diffusée de Gouy-Chapman (cf. fig. 2-2-c). La capacité surfacique
C de la couche double électrique est alors donnée par
:
1 1 1
= + 2-2
C C c Cd
Cc étant la capacité
associée à la couche compacte, de même nature que celle
préconisée par Helmholtz et Cd la capacité de la
couche diffusée de Gouy et Chapman. Ces deux couches forment la double
couche électrochimique.

(a)
(b) (c)
Fig. 2-2 : La double couche, modèles de Helmholtz
(a), Gouy-Champn (b) et Stern (c) [5]
| 


