|
LISTE DES ABREVIATIONS
Ø RPM : rupture prématurée
des membranes
Ø SA : semaine
d'aménorrhée
Ø ECBU : examen
cytobactériologique des urines
Ø NFS : numération formule
sanguine
Ø CRP : protéine C
réactive
Ø AINS : anti inflammatoire non
stéroïdien
Ø RCIU : retard de croissance intra
utérine
Ø HTA : hypertension
artérielle
Ø LA : liquide amniotique
Ø AFI : amniotique foetal
indice
Ø GEM : grossesse intra
membraneuse
Ø VS : vitesse de
sédimentation
Ø GB : globule blanc
Ø FL : formule leucocytaire
Ø IMG : interruption
médicale de la grossesse
Ø IM : intra musculaire
Ø RAPE : rupture artificielle de la
poche des eaux
Ø MIU : mort in utero
Ø CIVD : coagulation intra
vasculaire disséminée
Ø DC : décompensation
cardiaque
Ø RDC : République
démocratique du Congo
Ø CHRB 1er : centre
hospitalier roi Baudouin 1er
Ø CG : conseil de gestion
Ø DMO : dossiers médicaux
et obstétricaux
Ø ATB : antibiotique
Ø = : inférieur ou
égal
Ø < : supérieur
Ø % : un pourcentage, une façon
d'exprimer le rapport
(Ou valeur relative ou proportion) des
effectifs de deux
Ensembles au moyen d'une fraction cent.
Dans ce travail
% = Nbre de cas × 100/Total
Ø SFA : souffrance foetale
aigue
Ø SONU : soins obstétricaux
et néonataux d'urgence.
EPIGRAPHE
« La patience est une plante qui ne
pousse pas dans toutes les herbes »
Beverly LUTULA LUHALUfiston
DEDICACE
A l'Eternel Dieu tout puissant, le Dieu de Malachie 4, l'auteur
du visible et de l'invisible,
A mes très chers parents : LUHALU NDJEKA Joseph et
ETSHUMBA AKASA Marie Louise,
A tous les LUHALU,
A tous les EKASA,
A ma future épouse « Mlle. Jessica
MIPU »
A vous tous, je dédie ce travail.
REMERCIEMENT
Ce présent travail que nous avons l'honneur de
vousprésenter n'est rien d'autre qu'un mémoire sanctionnant la
fin de notre deuxième cycle d'étude à l'université
technologique BEL CAMPUS, Kinshasa ; R.D .Congo, spécialement
à la noble faculté de Médecine.
Ainsi, le désir majeur qui nous anime au terme de ce
second cycle, est celui de rendre hommage à notre alma mater et à
tout le corps professoral pour tous les enseignements, orientations et
directives que nous avons bénéficiés durant tout notre
parcours estudiantin.
Néanmoins, il convient de dire ici que la
matérialisation de ce travail n'est pas à comparer avec une veste
prêt- à- porter car non seulement qu'elle avait connu des
obstacles mais aussi d'ennuis liés à la nature en
général, et à la nature humaine en particulier, il fallait
un long souffle pour se maintenir en équilibre et percer sinon
l'échec se glorifierait.
Mais loin de nous toute pensée de vouloir faire croire
à l'humanité que ce travail est le fruit d'un effort personnel
car il a bénéficié de l'apport de plus d'une
personne ; matériel que financier, moral qu'intellectuel et des
orientations de plusieurs personnes que nous ne pouvons citer exhaustivement
ici.
Seulement, que toutes ces personnes trouvent par ici
l'expression de notre gratitude.
Cependant, une mention spéciale au Dr. KALONJI qui, en
dépit de ces multiples occupations, n'a pas épargné son
temps pour rendre réalisable ce manuel en acceptant la direction de
celui-ci ; qu'il trouve ici l'expression de notre profonde gratitude et
que le bon Dieu lui prête encore vie pour continuer à servir notre
alma mater.
Ces mêmes sentiments de reconnaissance
s'adressent également au Dr. Vincent KOBO, qui a aussi accepté en
fournissant le meilleur de lui-même pour le maintien de ce travail sur la
voie scientifique. Que Dieu du haut de cieux lui soit favorable.
A mon Pasteur Polydor KABEYA pour le soutient moral et
spirituel,
A mes chers maitres : Drs.
Mfumuseke ;Tossainmbula ; PitchouKanza ;Mamie Mbo ; Marthe
Nyalipoko ; Erick Zola doudou ; Serges Luwawu ;
TétuMbuze ; Rosada ;Guylain Ntangu ; PatyLebugue ;
Julie Ndaya ; Elisée Lumbala.
A vous mes amis(es) de lutte : Christian Kayembe ;
Dollar Matona ; Erick Eboma ; Jean Makinisi ;
Mi-joséBolenge ; GlorianneMbanzulu ; Josué
Baraka ; Lord Kebana ; Pascal yodi ; Philippe Diwoko ; JC
Otomba ; MerfetteMayala ; Rober Roy ; Mariame Tube; Dora Kabeya;
Patrick Kadongo ; Junior Makakala; Yves Yodi ; Albert Wato ;
Jessy Mukendi ;Jp.Ongala ,amis avec qui nous avons passé des
bons moments d'études ensemble et à tous les amis et membre de la
famille, qui d'une manière ou d'une autre nous ont donné un coup
de pousse dans la réalisation de notre travail.
Sans oublier le staff médical du CHRB
1er en particulier Dr. ANYSHAY M.J et toute la communauté
hospitalière pour ce qu'ils ont fait de nous dans l'encadrement pour
notre formation intégrale en médecine.
L'ingratitude nourrit le sot et laisse affamer le
sage dit-on, à vous tous qui vous reconnaissez les miens par crainte
d'oublier certains, trouvez à ce travail l'expression de ma grande
considération, pour tous les efforts individuels que vous avez dû
apporter dans l'élaboration de ce travail.
Que tous ceux qui, de loin ou de près avaient
posé leur pierre pour l'édification de ce travail, trouvent ici
l'expression de notre profonde gratitude.
Beverly LUTULA LUHALU Fiston
PLAN
0. INTRODUCTION
1.1. PROBLEMATIQUE
1.2. OBJECTIFS
§ Général
§ Spécifique
1.3. IMPORTENCE DE L'ETUDE
1.4. DELIMITATION DE L'ETUDE
1.5. SUBDIVISION DE L'ETUDE
CHAPITRE 1. GENERALITE
1.1. APERCU GENERAL SUR LA RUPTURE PREMATUREE DES MEMBRANES
1.1.1. Définition
1.1.2. Rappel anatomo physiologique de membrane
1.1.3. Anatomie pathologique
1.1.4. Etiologie de la rupture prématurée des
membranes
1.1.5. classification des RPM
1.1.6. Symptomatologie et diagnostic de la RPM
1.1.7. Diagnostic différentiel
1.1.8. Conduite à tenir
1.1.9. Complications
1.1.10. Pronostic
1.1.11. Eléments de surveillance
CHAPITRE 2. MATERIEL ET METHODES
2.1. MATERIEL
v Description du terrain d'étude
v Situation géographique
v Organisation de l'hôpital
v Aspect fondamentaux
v Capacité d'accueil
v Horaire de travail
2.2. METHODES
1. TYPE ET PERIODE D'ETUDE
- Etude descriptive documentaire
- Période d'étude
2. CADRE DE L'ETUDE
3. POPULATION D'ETUDE
4. CRITERE D'EXCLUSION
5. RECCEUIL DES DONNEES
6. LES VARIABLES RECCEUILLIES
CHAPITRE 3. RESULTATS
CHAPITRE 4. DISCUSSION
INTRODUCTION
La rupture prématurée des membranes de l'oeuf
constitue un problème en obstétrique car elle met en
communication la cavité amniotique qui est stérile et la
cavité vaginale où se trouve une flore, microbienne
variée. Ces microbes vaginaux peuvent même être la cause de
cette rupture des membranes.
Selon MERGER et COLL., la rupture prématurée des
membranes(RPM) peut compromettre le pronostic foetal et même maternel.
En effet, la possibilité de l'infection intra
amniotique ainsi que l'accouchement prématuré dont elle peut
être à l'origine conduisent souvent à la mort
périnatale ; l'infection accroît la morbidité
maternelle des suites des couches.
La RPM constitue par conséquent une grande
préoccupation pour l'obstétricien dans la prise en charge de la
gestante et du foetus.
En effet ; lorsqu'elle survient
précocement, elle pose le problème de prise en charge d'enfant
généralement prématuré d'une part, et d'autre part
elle augmente le risque infectieux pour le nouveau-né et pour la
mère.
Dans les pays développés les
progrès réalisés en périnatalogie ont permis de
prendre en charge des enfants nés trop tôt, l'accessibilité
aux antibiotiques les plus efficaces contre la plupart d'infection et ont
permis d'améliorer le pronostic de ces enfants.
Dans les pays en voie de développement par
contre, les enfants nés trop tôt sont confrontés à
des problèmes de survie liés à leur immaturité et
ceux qui sont nés à terme sont souvent confrontés à
des problèmes infectieux.
Très peu d'études ont
été réalisées dans ce domaine au sein de nos
centres. C'est pourquoi il nous a paru utile d'effectuer cette étude
dans l'un des plus grands hôpitaux de Kinshasa où nous avons une
prévalence élevée d'accouchement.
Les principaux mécanismes physiopathologiques que nous
allons évoquer mettent en jeu une fragilisation des membranes. Ils
demeurent encore précisément mal connus mais font intervenir
plusieurs hypothèses dont mécaniques (décollement
placentaire, contraction, hydramnios) et infectieuses ou carentielles,
oligoamnios, vitamines,).
0.1. PROBLEMATIQUE
La République Démocratique du Congo, RDC en
sigle, notre cher et beau pays, comme le reste des pays Africains est
confrontée à d'énormes problèmes de santé
publique. Le budget alloué à la santé n'a que pour
conséquence d'accroitre cette situation.
Les pathologies obstétricales ne font pas exception
à la règle, tous les experts s'accordent sur le fait que les
conditions de maternité sont loin d'être satisfaisantes en
Afrique. Parmi ces problèmes obstétricaux, nous épinglons
particulièrement la rupture prématurée des membranes.
Bien que de nombreux travaux aient récemment
apporté un nouvel éclairage sur les thérapeutiques
à mettre en oeuvre dans cette pathologie, des nombreuses inconnues, la
conduite thérapeutique médicale et obstétricale restent un
sujet de discussion qui jusque-là aucun consensus n'est
trouvé.
Par le biais de ce travail rétrospectif, nous nous
sommes proposé d'étudier les dossiers des parturientes
présentant une rupture prématurée des membranes et admises
au centre hospitalier Roi Baudouin 1er (MASINA) à Kinshasa, durant la
période de 2 ans soit (Du 01 Janvier 2011 au 31 Décembre
2013).
0.2. OBJECTIFS
· GENERAL
o Contribuer à l'amélioration de la prise en
charge de la R.P.M afin de réduire le taux de mortalité
périnatale et celui des accouchements prématurés dus
à la R.P.M
· SPECIFIQUES:
o Déterminer la fréquence de la R.P.M,
o Décrire le profil de gestantes victimes de la
R.P.M,
o Etudier le pronostic maternel des gestantes ayant
accouchée après R.P.M ainsi que leur produit de conception.
o Révéler les différents aspects de sa
prise en charges.
1.3. IMPORTANCE DE
L'ETUDE
Notre étude a pour but d'étudier le profil
clinique et para clinique de la rupture prématurée des
membranes ; avec comme objectif de contribuer à
l'amélioration de la prise en charge de la R.P.M afin de réduire
le taux de mortalité périnatale et celui des accouchements
prématurés dû à la R.P.M.
1.4. DELIMITATION DE
L'ETUDE
Ce travail a été mené au service de
gynécologique-obstétrique du centre hospitalier Roi Baudouin 1er
de MASINA du 1er janvier 2011 au 31 Décembre 2013. Elle se limite
à l'observation des gestantes avec rupture prématurée des
membranes. Les constatations dégagées dans cette étude ne
sont valables que pour cette institution sanitaire.
1.5. SUBDIVISION DE
L'ETUDE
Hormis l'introduction et la conclusion notre étude
comporte quatre chapitres à savoir :
- GENERALITE ;
- MATERIEL ET METHODES ;
- RESULTATS ;
- DISCUSSIONS
CHAPITRE I : GENERALITES
I.1. APERCU GENERAL SUR LA RUPTURE PREMATUREE DES
MEMBRANES
I.1.1. Définition
La rupture prématurée des membranes est
définie par la rupture franche (la solution de continuité) entre
l'amnios et le chorion survenant plus de douze heures avant le début de
travail et ce quelque soit le terme lors de la rupture. Le mot «
prématurée » s'applique au travail et non à
l'âge gestationnel. Cette définition inclut les fissurations de la
poche des eaux mais exclut les ruptures en cours de travail.
La RPM peut survenir :
- Avant le terme (avant 37SA) dans 0,5 à 7,2% des
grossesses selon les auteurs. Elle est alors responsable de 30% et 60% des
accouchements prématurés ;
- A terme (après 37 SA) dans 8 à 10% des
grossesses.
On définit la période de latence comme
étant le délai entre la rupture des membranes et la naissance.
I.1.2.Rappel théorique sur les membranes et le
liquide amniotique
a) LES MEMBRANES
· Les membranes ovulaires sont au nombre de trois au
début (amnios, chorion, caduque ovulaire), mais la caduque ovulaire est
peu refoulée par le développement de l'enfant et à terme,
il n'en reste plus que des vestiges, soudés à la caduque
utérine, membranes qui tapisse l'utérus.
De dehors en dedans, nous avons le chorion et
l'amnios :
2. Le chorion : c'est la membrane située
entre la caduque et l'amnios. Elle est fibreuse, transparente et
résistante. Dans le placenta, elle devient la plaque choriale
d'où émanent les villosités choriales.
Le chorion adhère à la caduque et se
sépare facilement en rapport avec le bouchon de mucus qui obstrue le
canal cervical. Sa structure est analogue à celle de la membrane
choriale du placenta. Le chorion est constitué de deux parties : la
zone sous amniotique et le trophoblaste chorial.
· La zone sous amniotique : elle comprend une couche
superficielle mince, faite de collagènes , riche en fibres et une couche
profonde, myxoide , celle-ci réalise un réseau alvéolaire
et contient deux types cellulaires : des fibroblastes allongés ou
étroites dont le noyau est volumineux et dont le mince cytoplasme
péri nucléaire est riche en organites , centrosome appareil de
Golgi , ergastoplasmes , mitochondrie et des cellules de nature histiocytaire (
cellules de HOF BAUER) dispensées dans le maille du réseau
fibrillaire. Cette zone sous amniotique ne contient pas de vaisseaux aussi bien
sanguins que lymphatiques.
· Le Trophoblaste chorial
Le trophoblaste chorial est parfaitement vivant. Il est
constitué des cellules parfois soutenues par une substance fibrinoide
dans laquelle on peut reconnaitre les axes conjonctifs hyalinisés ou
scléreux et vasculaires ; il s'agit de villosités choriales
digérées. La couché trophoblastique choriale est continue,
quoique, disloquées par place. Les cellules trophoblastiques sont
volumineuses, souvent binucléés.
Il n'est pas rare d'observer des figures de mitoses. La
surface des cellules trophoblastiques qui regarde le chorioamnios est
soulevée par de nombreuses protubérances en forme de
pédicelles. Ces protubérances en limitent parfois les embauches
des canaux intercellulaires qui sillonnent le trophoblaste primitif.
· Le trophoblaste (ou trophectoderme) est présent
dès le 5ème jour du développement embryonnaire,
autour de l'embryon. C'est lui qui va d'enzymes spécifiques, puis il se
différenciera pour former le placenta. Il a maintenant pour rôle
essentiel l'élaboration d'annexes embryonnaires adaptées à
la nutrition de l'embryon. Il est constitué de remplis creux de petite
taille : les villosités choriale, plus tard, le trophoblaste va se
différentier en deux couches : le cytotrophoblaste est la couche
cellulaire interne des villosités du chorion (rappel : c'est au
niveau de ces villosités choriales ou choriovilleux que s'opèrent
les échanges gazeux et nutritionnels entre le sang maternel et le sang
foetal) et le syncytiotrophoblaste externe (ou trophoblaste syncitial). C'est
l'ensemble de ces deux couches qui forme le chorion. A partir du
3ème mois, le trophoblaste prend le nom de placenta. Le
cytotrophoblaste est constitué de cellule épithéliales
polygonales appelées cellules de Langhans (à ne pas confondre
avec les cellules géantes de Langhans qui se forment, souvent par fusion
cellulaire, dans la tuberculose ou la sarcoïdose et qui se
caractérisent par la présence de nombreux noyaux souvent
rassemblés à la périphérie du cytoplasme). Pendant
le premier trimestre de la grossesse, le cytotrophoblaste et le
mésenchyme des villosités à la barrière
placentaire, c'est au cours du 4ème mois du
développement embryonnaire que le cytotrophoblaste disparait
partiellement de villosités choriales et évolue en ilots.
3. L'amnios : c'est une membrane mince,
transparente très résistante qui circonscrit en dedans la
cavité amniotique de 0, 3 à 0,5 mm d'épaisseur.
Membrane interne, l'amnios tapisse la face interne du placenta engaine le
cordon et rejoint à l'ombilic la peau du foetus. Surface externe est
accolée au chorion et s'en détache facilement. Il est
formé par un épithélium uni-stratifié,d'aspect
lisse et brillant, présentant, par place, des excroissances
irrégulières : les caroncules.Les cellules amniotiques, d'abord
cubiques,deviennent cylindriques en fin de grossesse. Auvoisinage du terme, le
revêtement amniotiquepeut subir une métaplasie
pavimenteused'intensité variable, localisée en foyer dequelques
millimètres, de préférence près del'insertion
funiculaire. Ces plages peuvent êtreapparentes à l'examen
macroscopique, sousforme de tâches blanchâtres
translucides.L'épithélium amniotique est composé
d'uneassise de cellules dont le pôle apical (correspond à sa
surface libre) est hérissé des nombreuses micros
villosités. Entre de cellulesadjacentes, on trouve un système de
canaux intercellulaires bordés d'expansions cytoplasmiques dessinant un
puzzle compliqué.Le pôle basal de la cellule, en rapport
avecl'assise conjonctive sous-jacente, s'appuie sur une basale fibrillaire
dense. On y note desexpansions cytoplasmiques en forme debotte, dont le grand
axe est perpendiculaire àl'axe de la cellule. On peut y observer des
hémidesmosomes.
Les cellules amniotiques sont uni nucléés.
Ellespossèdent les différents organites cellulaires : chondriome,
réticulum endoplasmique lisse, ergastoplasme, appareil de Golgi.
D'aprèsDUMINY (1974), à mesure que la grossesseapproche de son
terme, ces organites, enparticulier appareil de Golgi et l'ergastoplasme, se
raréfient tandis que les enclaves lipidiquesaugmentent.
La plupart des auteurs dont BOURNE, (1962) etDUMINY, (1974) ne
trouvent aucune structurepermettant d'évoquer un capillaire sanguin,
unlymphatique dans cette couche amniotique.
b) LE LIQUIDE AMNIOTIQUE
a) Définition.
Le liquide amniotique est un liquide clair au début de
la grossesse, opalescent et devient trouble à la fin dela grossesse. Son
odeur est fade, son poids spécifique est de 1.007g ; sa réaction
estfaiblement alcaline ; le pH est compris entre6,90 et 7,20 ; son poids
atteint celui du foetus vers le milieu de la grossesse. A terme, sonvolume
varie entre 500 et 1.000 ml enmoyenne. Une quantité supérieure
à 2.000 ml définit l'hydramnios.
§ S'il est rosâtre : penser aux
phlyctènes qui se développent sur le corps macéré,
un foetus mort depuis un certain temps.
§ S'il est purulent : ce qu'il contient un foetus
putréfié ;
§ Un liquide amniotique de couleur jaune : penser
à un ictère grave du foetus.
b) Origine.
Elle est essentiellement foetale. Mais le liquideamniotique
est aussi produit par deux autres voies : amniotique et maternelle.
1. Origine foetale. Au début de la grossesse, leliquide
amniotique n'est qu'une expansion duliquide extracellulaire du foetus
liée à la perméabilité de la peau qui
disparaît vers 20semaines. Plus tard, il provient des
sécrétionsrénales. Toutefois, sa composition est
différentede celle de l'urine. L'excrétion urinaire n'entreque
pour une part dans la composition duliquide amniotique. A terme 7 ml/Kg/h
sontexcrétés par le foetus. Viennent s'y ajouter au cours du
dernier trimestre des sécrétionspulmonaires (300 ml/24
heures).
2. Origine amniotique. Le liquide amniotique serait aussi
sécrété par l'amnios, que tout l'épithélium
participe à cette fonction ou que celle-ci soit réservée
à des cellules sécretentes spécialisées. Les
études microscopiques et histochimiques de l'épithélium
amniotiques ont montré des images de sécrétion cellulaire,
sans que la preuve formelle de la sécrétion ait encore
été faite. Un autre mécanisme a été
évoqué, la transsudation de liquide à partir du sang
foetal contenu dans les vaisseaux villositaires ; pour que cette transsudation
soit possible, il faut que la tension de la veine ombilicale soit très
supérieure à la normale ; aussi ce mécanisme ne
semble-t-il jouer un rôle que dans certains cas pathologiques.
3. Origine maternelle. La transsudation de liquide amniotique
d'origine maternelle à travers les membranes ovulaires serait possible.
L'injection de colorant dans la circulation maternelle montre son passage
à travers l'épithélium amniotique. Ce liquide amniotique
se vide lorsque les contractions de l'utérus percent le sac
amniotique : c'est la rupture de la poche des eaux.
c) Composition
Le liquide amniotique est constamment renouvelé. Il est
constitué d'eau, mais contient aussi des cellules foetales
(desquamation) et amniotiques, de l'urine foetale, le glucose,... .
Le glucose passe de 0,5 g/l au début de lagrossesse
à 0,20 g/l près du terme.
Le taux de l'urée passe de 0,22 g/l au début
dela grossesse à 0,33 g/l à la fin.Celui de la créatinine
varie beaucoup et passede 10 mg/l à la fin du 2ème trimestre
à 20 mg/là terme.
La bilirubine n'est contenue qu'en faiblequantité. Elle
apparaît dès la 12ème semaine, atteint sa
concentration maximum entre 16 et30 semaines et disparaît après 36
semaines. Ellepeut être mise en évidence
parspectrophotométrie.Les lipides sont de l'ordre de 50 mg par 100 ml.La
mesure par chromatographie de deuxd'entre eux, élaborés par le
poumon du foetus,les lécithines (L) et les Sphyngomyelines (S) à
une application pratique. Au terme de 36 semaines, les
lécithinesdeviennent proportionnellement plusimportantes que les
Sphyngomyelines. Durapport entre ces deux substances, on peutévaluer la
maturité pulmonaire foetale.Différentes hormones sont
également retrouvées dans le liquide amniotique.
Deux semblentparticulièrement intéressantes pour
lasurveillance du foetus : l'oestriol et l'hormonechorionique
somatomammotrophique ouhormone placentaire lactogénique(H.P.L.). Le taux
de certains de ces constituantsreprésente le degré de
maturité de diversorganes du foetus, le taux de bilirubine pour
lafonction hépatique, rapport L/S desphospholipides pour la
maturité pulmonaire.L'alphafoetoprotéine est une
glycoprotéineformée dans le foie foetal et la
vésiculeombilicale. Sa concentration dans le liquideamniotique diminue
graduellement à partir de la 14ème semaine jusqu'
à terme. Elle est trèsabondante en cas de mort `' in utero''
etsurtout lorsque le foetus a des malformations dusystème nerveux
central avec lésion ouverte etperte du liquide
céphalo-rachidien.
d) Cytologie.
Le liquide amniotique contient des
cellulesépidermiques, desquamées, des poils, de lanugoet des
fragments de matières sébacées quiforment des grumeaux
blanchâtres, égalementdes cellules épithéliales
provenant de l'arbreurinaire foetal, et du vagin lorsque le foetus estde sexe
féminin.
La culture des cellules foetales permet son
étudegénétique. On peut ainsi, dès le
troisième moisde la grossesse, établir le caryotype et faire
lediagnostic, non seulement du sexe, mais des éventuelles anomalies
chromosomiques.
e) réabsorption.
La résorption de liquide amniotique est
expliquée par deux mécanismes :
a. La déglutition du liquide amniotique par lefoetus.
Le liquide dégluti est absorbé parl'intestin parvenu dans le sang
foetal, il traversela barrière placentaire, emprunte la
circulationmaternelle et est éliminé par les reinsmaternels. On
estime à 500 ml la perte deliquide ainsi dégluti par le foetus en
vingt-quatre heures.
b. La réabsorption par l'épithélium
amniotique. Il s'agit d'un processus deréabsorption active pour
certaines substances : l'eau et les glucides. En somme, on admet
engénéral que le passage de la circulation maternelle dans le
liquide amniotique et, àl'inverse, le passage du liquide amniotique dans
l'organisme maternel est soit direct à traversles membranes, soit
indirect par l'intermédiairedu foetus.
Ainsi s'établit, entre la production et
larésorption du liquide, un équilibre qui maintientson volume
sensiblement constant. Son renouvellement s'effectue en 3 heures. Sacirculation
est contrôlée par un mécanismerégulateur encore mal
connu.
f) rôle physiologique.
Ce rôle est différent pendant la grossesse
etpendant l'accouchement.Pendant la grossesse, le liquide assurel'hydratation
du foetus et lui apportequotidiennement une certaine quantité d'eau et
de sels minéraux, Il permet le développementdu foetus et son
déplacement, Il facilitel'accommodation de la présentation, Il
réalisel'isolement thermique du foetus, Il le protège contre les
traumatismes extérieurs, contre lescompressions du cordon ombilical,
contrel'infection. La cavité amniotique étant close etl'amnios
imperméable aux germes exogènes. Pendant l'accouchement, il
continue àprotéger contre l'infection et le traumatisme.
Ilconcourt à la formation de la poche des eaux. Illubrifie la
filière génitale après la rupture desmembranes et facilite
les progrès de laprésentation.
g) Pathologies :
1. Définition
v OLIGOAMNIOS : il s'agit d'une
diminution pathologique de la quantité de liquide de liquide amniotique
dont le diagnostic est échographique : plus large citerne de
liquide amniotique inférieur à 2cm ou index amniotique des 4
quadrants inférieur ou égal à 5 cm. Quantité du L.A
inferieure à 500 ml entre 21e et 41e S.A, les
membranes étant intactes. Pathologie longtemps négligée
car les obstétriciens avaient du mal à poser le diagnostic
clinique.
§ Cause :
- Foetales : malformations (urinaires),
anomalies chromosomiques, RCIU, post maturité, rupture
prématurée des membranes ;
- Maternelles : insuffisance
utéro-placentaire (syndromes vasculo rénaux, hypo
volémie), iatrogènes (AINS et inhibiteurs de l'enzyme de
conversion) ;
- Placentaires : syndrome
transfuseur-transfusé.
§ Conduite à
tenir :
Les investigations révèlent de
techniques spécialisées de médecine foetale.
L'échographie est essentielle pour le diagnostic positif, la recherche
d'une malformation foetale (uropathie obstructive ou non) et du retentissement
sur la vitalité (RCIU). Elle doit être complétée
d'une vélocimétrie Doppler utérine et ombilicale. Une
amniocentèse et /ou cordocentèse permet de faire un caryotype
foetal (anomalie chromosomique de l'ordre de 5 %, surtout si RCIU
associé). L'amnio-infusion (injection intra amniotique de sérum
physiologique) facilite le diagnostic échographique et permet parfois
d'objectiver une rupture prématurée des membranes (injection
intra-amniotique de bleu EVANS ou de carmin indigo).
Au deuxième trimestre : dans les
cas graves (oligoamnios avant 20 SA, malformation), une interruption
médicale de la grossesse peut être discutée. Des
amnio-infusions hebdomadaires pour éviter l'hypoplasie pulmonaire et les
déformations articulaires du foetus ont été
proposées.
Au troisième trimestre : si la
cause est une souffrance foetale chronique (HTA, toxémie, terme
dépassé), le bilan de vitalité permettra d'adopter la
meilleure conduite à tenir (déclenchement du travail ou
césarienne).
v HYDRAMNIOS :
Définition :
Selon MERGER ; à la fin de la grossesse, on
distingue :
§ Excès de liquide c'est-à-dire entre 1 et
2 litres
§ Hydramnios si la quantité est supérieur
à 2 litres
Selon l'échographie ;
§ Chamberlin : l'hydramnios, quand une citerne de
liquide amniotique est supérieur à 8 mm.
§ Phelan : retient l'hydramnios si l'index
amniotique est supérieur à 25 mm, c'est-à-dire, on divise
l'abdomen en 4 quadrants par 2 droites perpendiculaires passant par
l'ombilic : la profondeur de 4 citernes est mesurée et
additionnée entre 18 - 25 mm : excès de liquide
amniotique.
§ Au-delà de 25 mm : excès anormal du
volume de liquide amniotique défini en échographie par une
citerne de liquide amniotique supérieure à 18 mm ou un index
amniotique supérieur à 25 mm.:
- Cause :
· Foetales : malformations,
grossesse gémellaire avec anastomose vasculaires (jumeau transfuseur),
infection congénitale, transfusion foeto-maternelle.
· Maternelles : diabète
· Placentaires : chorio-angiome
§ Conduite à tenir
Hydramnios aigu du deuxième trimestre :
malformation foetale et syndrome transfuseur-transfusé d'une grossesse
gémellaire :
le traitement repose sur des évacuations amniotiques
répétées, mais le pronostic est mauvais.
Hydramnios chronique du troisième
trimestre : recherche des causes, échographiques pour étude
de la morphologie, de la motricité et de la déglutition
foetales ;
- Traitement
Traiter la cause de l'hydramnios si elle est
connue, mettre en route un traitement symptomatique : amniocentèse
répétée, prescription d'indométacine (de 2 à
3 mg/kg/j) qui diminue la diurèse foetale, mais qui risque de provoquer
une fermeture prématurée du canal artériel et une
insuffisance rénale néonatale.
v L'ANAMNIOS : absence totale du L.A
2. Fréquence : entre 0,4 et 4%
des grossesses
3. Etiopathogénie :
· Grossesse prolongée
· Mort foetale in utéro
· Certaines malformations foetales touchant l'appareil
urinaire : Agénésie rénale bilatérale
(Syndrome de Potter) Reins poly kystiques congénitaux.
4. Causes iatrogènes : la
prescription des anti inflammatoires non stéroïdien
(indométacine et ibuprofène) ; responsables d'une
insuffisance rénale fonctionnelle par diminution de débit
utéro-placentaire (réversible).
5. Le diagnostic : examen essentiel est
l'échographie pour la quelle un échographiste entrainé
mesurera les citernes en calculant l'A.F.I.
6. Pronostic : découverte d'un
oligo amnios avant 6 mois de grossesse ; toujours très mauvais
pronostic. Le pronostic est d'autant plus grave que la survenue de l'oligo
amnios est précoce. En cas de retard de croissance isolé, l'oligo
amnios est un élément de gravité.
7. Conséquences foetales :
Hypoplasie pulmonaire :
- Complication redoutable suspectée par l'absence des
mouvements de la cage thoracique ;
- Peut aboutir à la mort dans les premiers jours de la
vie ou laisser des séquelles respiratoires définitives ;
- Déformation par compression mécanique :
pieds bots, dysplasie, luxation de la hanche.
8. Conséquences
obstétricales
Fréquences élevées :
- Des présentations de siège,
- Dystocie dynamique,
- Mortalité périnatale.
9. Conduite à tenir :
· Si malformation incompatible avec la vie :
interrompre la grossesse
· Autres situations :
- Laisser évoluer la grossesse
- Injection intra amniotique de liquide de remplacement (Nacl
à 9 gr % par voie trans-abdominale).
v EPIDEMIOLOGIE : entre 0,4 et un et ½ % dans les
grossesses uniques
v PHYSIOPATHOLOGIE : le rôle du foetus apparait
essentiel dans la régulation du volume du L.A.
4. Anomalie de résomption : toutes
anomalies anatomiques ou fonctionnelles empêchant la déglutition
ou le transit (atrésie oesophagienne, pathologie
neuromusculaire) ;
5. Anomalie de production : origine foetale. Toute
entrave à la circulation foeto-placentaire modifiant l'équilibre
hémodynamique.
I.1.3. Anatomie pathologique
La rupture classique franche, est celle qui ouvre le pole
inferieur de l'oeuf à son point le plus bas. C'est-à-dire ce qui
avait été la poche des eaux au moment du travail. Certains
auteurs ne croient guère à la fissuration. Selon eux si une telle
lésion existait, elle ne saurait être que tout à fait
éphémère. Elle ne tarderait pas à se transformer en
une rupture franche à la moindre contraction. En revanche, il faut
affirmer l'existence d'une rupture haute, siégeant à distance de
l'orifice interne du col. De même, il faut admettre la rupture de
certaines poches liquides constituées entre amnios et chorion (poche
amniochoriale).
I.1.4. Etiologie et pathologie
Nombreux sont les germes pouvant envahir la cavité
amniotique qu'il s'agisse d'une espèce microbienne particulière
ou de flores associées. Certains germes sont plus fréquents que
d'autres, mais leur fréquence respective est en perpétuel
changement.
La RPM peut être due soit à des causes
mécaniques, soit à l'altération des membres ; mais il
existe également certains autres facteurs étiologiques de cet
accident.
Les causes mécaniques sont celles qui
révèlent, soit d'une sur distension de l'oeuf, par hydramnios,
par grossesse gémellaire avec ou sans hydramnios, soit d'un
défaut d'accommodation (présentation vicieuse) le placenta bas
inséré, la béance cervicale ; qu'elle soit d'origine
traumatique ou fonctionnelle peuvent également favoriser la RPM.
Les causes importantes sont :
- Les infections génitales : l'infection vaginale
ascendante (le plus souvent bactérienne, par exemple E. coli,
Streptocoque B) fragilisent les membranes.
- L'insuffisance du col et les contractions
prématurées du col, les membranes sont libres aux pôles
inférieurs de l'oeuf et peuvent facilement se rompre.
- L'augmentation de la pression intra utérine l'or
d'une grossesse gémellaire, d'un hydramnios ou d'une macrosomie
foetale.
- L'anomalie de position (vice de position), position
transversale en particulier avec procidence d'un bras, présentation des
pieds.
L'altération des membranes est le fait
d'une amniotite infectieuse ; cette amniotite qui peut être mise en
évidence par l'histologie et la bactériologie (frottis des
membranes) fragilise les membranes et favorise leur rupture. L'infection
procède l'ouverture de l'oeuf son origine est souvent urinaire et
cervico-vaginale. Nombreux germes peuvent envahir la cavité
amniotique. C'était le streptocoque lui ont succédé les
entérobactéries, notamment Escherichia coli ; aujourd'hui
domine le streptocoque B et occasionnellement la Listéria.
Les facteurs personnels et constitutionnels : le bas
niveau socio-économique, la malnutrition, le déficit en vitamine
C, en cuivre et en zinc, la maladie de collagène, la
nulliparité ; sont là autant des facteurs favorisant la
R.P.M.
Les facteurs physiologiques :
Certains auteurs citent les contractions utérines post
coïtales.
- Causes mécaniques : traumatismes,
exemple : si coït avec quelqu'un qui pèse plus que
vous ;
- Béance cervicale : les membres
exposés deviennent fragiles
- Notion des grossesses multiples
- Notion de la grossesse cerclée : ces
microbes se filtre dans le file de cerclage ainsi, il faut des ovules vaginaux
pour désinfecter le milieu.
Les causes inconnues : soixante pour cent (60%) des RPM.
Ce qui a fait discuter la possibilité d'une fragilité
constitutionnelle de la poche amniotique de certaines gestantes, responsable de
RPM répétée lors des différentes grossesses.
I.1.5. Classification des RPM
On définit le moment de la rupture
prématurée des membranes par rapport aux phases de
l'accouchement.
- La Rupture prématurée des membranes :
avant le début des contractions utérines
régulières, c'est-à-dire avant la période de la
dilatation ;
- La Rupture précoce des membranes : (la plus
fréquente) durant la période de dilatation c'est-à-dire
avant la dilatation complète ;
- La Rupture tempestive des membranes :(rare), durant la
période d'expulsion ; c'est-à-dire après la
période complète, avant la naissance de l'enfant ;
- La Rupture retardée des membranes : rupture
après l'expulsion de la tête foetale ou à la fin de la
phase d'expulsion ;
- La Rupture haute des membranes : la rupture des
membranes dans la cavité utérine la poche des eaux avant la
tête foetale est encore intacte.
I.1.6. Symptomatologie et diagnostic de la rupture
prématurée des membranes
L'écoulement du liquide amniotique plus de 24 heures
avant le début du travail par une fissure ou une rupture franche de la
poche des eaux. Cet écoulement doit faire rechercher une autre anomalie
obstétricale et insister à une surveillance rigoureuse.
Les mesures suivantes permettent de confirmer la rupture des
membranes
· Examen ou speculum ; écoulement liquide
visible, prélever des sécrétions au niveau du cul-de-sac
vaginal postérieur et faire un frottis microbiologique.
· Test au papier tournesol : le liquide amniotique
est alcalin éventuellement compléter par un examen d'urines pour
le diagnostic différentiel.
· Test au bleu de Nil : test des flocons de
vernix ; peut-on voir des flocons de vernix.
· Amnioscopie : la poche des eaux est-elle
visible ?
· Echographie : pour vérifier ou
apprécier la quantité du liquide amniotique et la
présentation foetale.
· Si Tarnier positif, faire le FERN TEST (mot allemand
qui veut dire feuille de fougère), il y aura cristallisation en feuille
de fougère à cause des ions Na.
· On peut également mettre en évidence la
Di - amino-oxydase (enzyme contenue dans le liquide amniotique par
radio-isotope). Le test à la fluorescéine donne de bons
résultats, mais il s'agit d'injecter la solution fluorescente.
- Les méthodes calorimétriques testant le pH
vaginal ont les mêmes inconvénients que le test de cristallisation
et sont inefficace si la rupture est ancienne, s'il existe une infection
vaginale ou si la patiente a reçue des antibiotiques. La recherche
d'éléments graisseux provenant du foetus par le noir cerol ou par
le soudant, il n'est pratiquement plus utilisée ; l'étude
cytologique de l'écoulement après coloration de HARRISHOR ou au
bleu de méthylène est fiable lorsque la desquamation foetale est
insuffisante, par contre, perd sa précision lorsque la rupture est
ancienne.
N.B. : le test de cristallisation donne
d'excellents résultants lorsque l'écoulement est suffisamment
abondant et qu'il n'est pas souillé par le sang ; par contre, il
devient très infidèle lorsque l'écoulement est minime ou
souillé.
FORMES CLINIQUES INHABITUELLES
Quand les membranes se rompent au début de la
grossesse, l'avortement est de règle. Ce pendant dans certains cas
rares, la grossesse continuera à évoluer. Dans ce dernier cas,
l'écoulement est toujours prématuré, souvent par
siège, l'enfant est marqué par des déformations
inhabituelles aux grossesses évoluant sans liquide amniotique et le
pronostic maternel est bon à l'absence des complications
infectieuses.
Ces formes inhabituelles se présentent sous deux
variétés : la grossesse intra-amniotique et la grossesse
intra membraneuse.
La grossesse intra-amniotique est une variété
très rare de la rupture des membranes ; peut-être aussi son
diagnostic est difficile car dans la majorité des cas, l'avortement est
précoce. Elle serait la conséquence de la rupture isolée
de l'amnios avant son accolement au chorion ; l'amnios se
rétractant, le foetus se développe entre amnios et chorion.
L'examen du placenta permet le diagnostic.
L'amnios résiduel peu développé, entoure
le cordon ombilical en prenant souvent un aspect en carole. La majorité
de la plaque choriale est ainsi formée uniquement par le chorion. La
pathologie de brides amniotiques et de certaines anencéphalies serait
expliquée par ce mécanisme. Grossesse extra-membraneuse. La GEM
est bien comme depuis la fin du siècle dernier et représente une
forme clinique exceptionnelle de la rupture prématurée des
membranes ; pathogénie, étiologie. La GEM ne peut se
constituer que si la rupture des membranes a lieu aux alentours du
5ème mois de la grossesse, à un moment où
l'amnios et chorion sont soudés, mais où la caduque
réfléchie n'est pas encore accolée à la caduque
vrai. Dans les quelques cas exceptionnels à la vérité,
où l'avortement ne se produit pas le sac membraneux se colle laisse
sortie le foetus qui vient se loger et continue à se développer
de la cavité utérine au contact direct des caduques. La cause de
la rupture des membranes reste habituellement inconnue. Les signes cliniques
sont ceux d'une banale rupture des membranes avec hydrorrhée amniotique
persistante ; l'évolution de la grossesse peut être
relativement longue après rupture des membranes mais les complications
sont exceptionnelles.
L'enfant à la naissance a un aspect
caractéristique traduisant les conditions de logement anormal
(déformation du crâne et des membres, secondaire à la
compression par l'utérus). Le pronostic foetal et néonatal est
sombre, car l'accouchement est habituellement prématuré et se
fait fréquemment par siège. Seul l'examen du placenta permet le
diagnostic.
Anatomie pathologique : le
placenta présente des modifications caractéristiques ; le
sac membraneux est aplatit et possède un orifice ovulaire et
régulier par le quel fait issu le cordon ombilical. La taille de la
cavité amniotique résiduelle et son orifice montrent à
l'évidence qu'ils ne pouvaient contenir ni laisser passer le foetus au
moment de l'expulsion. Au niveau de l'orifice, les membranes sont
réguliers, un peu épaissies, cicatricielles, à caduque
pariétale nécrotique. L'écoulement persistant de liquide
amniotique a pour conséquence un oligoamnios chronique. Ce dernier
entraine un amnios nodusum, à nodules relativement grêles, peut
étoffés en raison, sans doute du nombre réduit de
cellules provenant de la cavité amniotique résiduelle. En
même temps, le placenta est margine, extra chorial, sans doute par
croissance marginale des cotylédons à défaut d'extension
de la plaque choriale, sous l'effet du précédent sommaire
suivant.
I.1.7. Diagnostic différentiel
Il pourrait s'agir de :
- Fissuration haute
- Incontinence urinaire
- Rupture précoce des membranes
- Rupture de la poche amnios-choriale
- Expulsion du bouchon muqueux
- Leucorrhée fluide
I.1.8. CONDUITE A TENIR
Les complications néonatales sont liées, d'une
par à la prématurité et d'autre part à la
durée de temps de latence qui conditionne aussi bien l'infection
néonatale que maternelle. Près du terme, le seul problème
à considérer est le risque infectieux lorsque l'accouchement ne
survient pas spontanément dans un délai rapide, il faut alors
mettre en balance les risques de la thérapeutique destinés
à hâter l'accouchement avec ceux de l'expectative. La conduite
à tenir sera envisagée suivant un ordre chronologique en
étudiant successivement pendant la grossesse et au cour de
l'accouchement et sera envisagée enfin la conduite à tenir chez
le nouveaux né.
1. Conduite à tenir pendant la
grossesse
Deux problèmes doivent
être discutés en premier lieu :
Ø L'hospitalisation de la patiente et
l'antibiothérapie.
- L'hospitalisation : l'osque le diagnostic de RPM est
certain, la plupart des auteurs sont d'accord pour hospitaliser la patiente
jusqu'à l'accouchement à la cour de celle-ci, seront
effectuées régulièrement des investigations maternelles
(le dosage de la CRP, l'hémoculture, l'examen bactériologique du
L.A, la VS et le globule blanc) et foetales (la surveillance du rythme
cardiaque).
- L'antibiothérapie : il faut distinguer deux
types d'antibiothérapies : l'antibiothérapie
préventive et curative, en cas d'infection amniotique.
a) Antibiothérapie préventive : elle est
généralement systématique si quelques auteurs avaient
proposés l'antibiothérapie préventive systématique
par voie générale dès la survenue d'une RPM (ROUVILLOIS
J.L), d'autres actuellement, la proscrivent (CREPING, GUNNG).cette
dernière attitude est logique en raison de l'activité anti
bactérienne du liquide amniotique d'autre par, étant donné
la richesse de la flore génitale, une antibiothérapie
systématique risquerait de sélectionner des souches
résistantes.
b) L'antibiothérapie curative en cas d'infection
amniotique. L'hospitalisation de la patiente permet une
surveillance clinique et biologique minutieuse ; prise de la
température plusieurs fois par jour, examen bactériologique de
l'écoulement cervical et des urines en cas de fièvre au moins une
fois par semaine à titre systématique, l'hémoculture.
Ces différents examens permettent d'identifier les
germes en cause et d'effectuer un antibiogramme. Les germes les plus souvent
rencontrés sont :
- les antéro bactéries (klebsiella, Escherichia
coli) :
- les streptocoques : surtout du groupe B :
- Les staphylocoques ;
- Certaines aérobies.
En entendant le retour de l'examen
bactériologique, on mettra en route un traitement en large spectre
suivant la gravite de l'état infecté. Par contre, les germes
anaérobiques sont plus difficiles en mettre en culture et à
isoler, en plus le délai pour obtenir l'antibiogramme est assez long.
En cas d'infection générale grave cliniquement
exprimée, un traitement doit être entrepris dès que les
prélèvements sont effectués en utilisant un produit actif
sur les anaérobies avec une posologie suffisante ;
Parmi ceux-ci on peut citer :
§ La pénicilline G (perfusion de 20 a 40 millions
d'unités par jour) ;
§ La clindamycine (dalacin IV 300mg toutes les 6
heures) ;
§ Le métronidasole per os, 250mg à 750mg
toutes les 8 heures. Ces produits peuvent également être
administrés par perfusion 3x 500mg.
Conduite à tenir en fonction de l'âge
gestationnel.
On distingue trois périodes :
v Avant 34 semaines,
v Entre 34 et 37 semaines
v Apres 37 semaines
A. Prise en charge des RPM avant 34
S.A.
Les prises en charge dépendent surtout
de l'âge gestationnel au moment de la rupture des membranes.
1. Prise en charge des RPM avant 24 SA
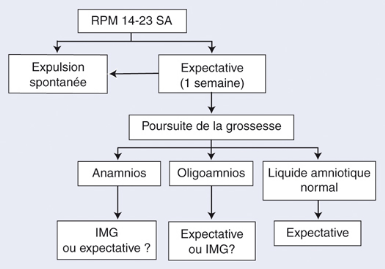
Figure : arbre décisionnel RPM avant 24S.A
d'après P.Audra
Les chances de survie sont très faibles si la naissance
a lieu pendant cette période.Deux attitudes sont discutées en
fonction des données cliniques et échographiques ; l'interruption
de grossesse : si une chorioamniotite survient pendant cette période ou
si l'on diagnostique à l'échographie foetale un oligoamnios voire
un anamnios, un retard de croissance intra-utérin ou une malformation,
cette option est discutée. On privilégie avant tout la
santé maternelle. L'attitude expectative en espérant atteindre le
seuil de viabilité mais avec les risques liés à la grande
prématurité. On recherche des signes cliniques et biologiques
infectieux. Un bilan infectieux est prélevé
régulièrement.
Il comprend un prélèvement vaginal, un examen
cytobactériologique des urines (ECBU), une numération formule
sanguine (NFS) et un dosage de la protéine C réactive (CRP). On
surveille régulièrement à l'échographie la
croissance foetale ainsi que la quantité de liquide amniotique.
Une antibiothérapie est débutée et
adaptée en fonction du prélèvement vaginal maison
n'effectue ni tocolyse, ni corticothérapie.
2. Entre 24 et 34 SA :
· La tocolyse : le risque de morbidique et de
mortalité néonatale lié à la
prématurité est élevé et impose la tocolyse en
contraction utérine. Ce traitement comporte néanmoins certains
contres indications :
ü l'infection amniotique ;
ü la souffrance ;
ü les contre-indications maternelles aux substances
bêtamimétiques (cardiopathies, hyper thyroïdien, etc.). Dans
ce dernier cas, cependant le recours aux inhibiteurs de la synthèse en
prostaglandines, (indométacine par exemple) peut être utile.
La corticothérapie
préventive : l'emploi des corticoïdes pour prévenir le
risque des maladies des membranes hyalines chez le nouveau-né est
discutable en raison du risque infectieux.
Il semble toutefois justifié car si la RPM semble
diminuer, pour certains, ce risque de maladie des membranes hyalines, elle ne
le fait pas disparaitre, surtout dans le cas de grande
prématurité.
Avant de prescrire une
corticothérapie, il est bien impératif d'en respecter les
contre-indications : infection patent, toxémie surajoutée,
et la posologie de la corticothérapie tient compte de la dose et de la
durée du travail.
Dose : 4 injections IM de 5mg de
Bétaméthasone, sous forme de Betnesol Dépôt.
NB : En l'absence de signes infectieux
ou de signe de toxémie, la prévention de la maladie des membranes
hyalines par l'administration de Bétaméthasone sous couverture
antibiotique semble logique.
B : Entre 34 et 37 semaines :
Certains auteurs proposent le
déclenchement systématique du travail après 34 semaines ou
dès que le poids foetal est estimé supérieur à 2000
grammes. Malheureusement à cette période les conditions
physiologiques ne sont pas toujours favorables au déclenchement du
travail d'accouchement et l'enfant est fragile. On n'entreprend ni tocolyse ni
corticothérapie à cette période où le risque
infectieux deviendrait alors plus important que le risque de
prématurité. Il est donc proposé une attitude
d'expectative en laissant débuter spontanément le travail
d'accouchement. Il faut bien sûr, surveiller la patiente à
l'hôpital pour pouvoir intervenir rapidement en cas de complication.
C : Après 37 semaines
Le déclenchement artificiel du travail doit être
réalisé dans les 24 heures si les conditions cervicales sont
favorables (score de BISHOP supérieur à 6). Si non, il faut
attendre que les conditions cervicales de déclenchement soient
améliorées. Toutefois, il faut éviter que le temps de
latence se prolonge au-delà de 48 heures.
Conduire à tenir dans certains cas particuliers
Certaines circonstances
particulières peuvent obliger à modifier le schéma
chronologique ci-dessus ; ces circonstances sont détaillées
ci-dessous.
Ø Présentation de siège : il faut
appliquer le schéma chronologique ; tocolyse avant 34 semaines,
expectative ensuite. Mais la tendance actuelle est de pratiquer une
césarienne en cas d'accouchement par présentation de siège
35 semaines, sauf en cas d'infection amniotique. Après 35 semaines, si
le bassin est normal, il faut attendre le déclenchement spontané
du travail et de pratiquer l'accouchement par voie basse.
En cas de rétrécissement pelvien, une
césarienne sera pratiquée immédiatement.
Ø Grossesse gémellaire : il faut appliquer
le schéma habituel : Tocolyse et corticothérapie avant 34
semaines, expectative ensuite. Par contre, après 37 semaines, il semble
préférable de poursuivre l'expectative plutôt que de
vouloir déclencher artificiellement le travail après 48 heures de
latence. Si le premier jumeau est en présentation du siège, on
rapporte à la conduite à tenir dans le cas
précédent.
Ø Utérus cicatriciel : le schéma
chronologique s'applique très bien pour les deux premières
périodes. Par contre, si l'on a choisi l'accouchent par voie basse
après épreuve utérine, l'expectative jusqu'au début
spontané du travail est préférable au
déclenchement, même si le temps après 37 semaines
dépasse 48 heures.
Ø Mort du foetus in utéro : le risque
infectieux revient au premier plan puis que le risque de
prématurité ne compte plus. Dans ce cas, le déclenchement
du travail est à envisager le plus rapidement possible.
Conduite à tenir pendant le
travail
La RPM, outre le déclenchement du travail entraine deux
conséquences qui sont :
- Le risque de dystocie supplémentaire au cours du
travail ;
- La fragilisation foetale (infection, suppression du
rôle amortisseur du L.A) qui est d'autant plus marquée que
l'enfant est plus prématurée.
Ceci impose une surveillance étroite d'accouchement
avec un respect très strict de délai de l'accouchement normal.
CAS PARTICULIERS
o Grossesse avec cerclage du col ; enlever le fil
o Si grossesse gémellaire ; tocolyse avant 34
SA ;
o Si mort foetal in utéro ; déclencher le
travail rapidement.
Les indications de la voie haute
Elles résultent en premier lieu de
certaines circonstances obstétricales ; présentation
transversale, procidence du cordon, procidence d'un membre, placenta
prævia.
En ce qui concerne la présentation du
siège, la conduite à tenir a été envisagée
ci-dessus. En fin, la RPM fait souvent accélérer la
décision obstétricale, car le travail prolongé augmente le
risque infectieux.
Précautions particulières pendant
le travail : il faut insister sur les précautions d'asepsie
vaginale en cas d'examen vaginal et pour la mise en place de système de
monitorage interne. Ce dernier n'est pas contre-indiqué en l'absence
d'infection amniotique et permet de diriger le travail plus efficacement par un
contrôle plus fiable de l'activité utérine
Conduite à tenir chez le
nouveau-né
A sa naissance, l'enfant sera
traité pour sa prématurité et pour une éventuelle
infection.
Des prélèvements pour les
examens bactériologiques seront toujours faits aux divers
orifices : nez, oreilles, anus. Dans le même temps seront
prélevés pour les examens histologiques et
bactériologiques, les différents constituants ovulaires :
placenta, cordon membranes, frottis extemporané, pour donner des
renseignements immédiats en particuliers en cas de listériose.
I.1.9. Les complications
Chaque rupture prématurée des membranes est un
risque de procidence et avant tout de procidence du cordon. Pour cette raison,
la patiente devrait aussitôt s'allonger, se faire transporter allonger
à la clinique et rester allonger jusqu'à ce qu'on soit sur que la
tête foetale se colmate bien le col. En dehors de la procidence des
parties (bras, pied) en raison de la communication directe entre le vagin et
l'espace intra-utérin suite à la rupture des membranes, il y a un
risque survenue qui souvent apparait quelques heures après la rupture
des membranes et va augmenter le risque d'un accouchement
prématuré (selon l'âge de la grossesse).
ü CHORIO AMNIOTITE : c'est une
infection de la cavité amniotique, le plus souvent secondaire à
une rupture prématurée des membranes.
Clinique : fièvre, contractions
utérines régulières et douloureuse, liquide amniotique
teinté, fétide voir purulent ; tachycardie foetale ;
Conduite à tenir : urgence
obstétricale, hospitalisation, antibiothérapies ; la
conduite obstétricale dépend du terme et de la gravité de
l'infection, de l'existence ou non d'une souffrance foetale. En l'absence de
grande prématurité, l'accouchement doit avoir lieu sans
délais.
ü EMBOLIE PULMONAIRE (maternelle) :
- circonstance de survenue (RPM, RAPE, MIU, liquide
méconial) : le passage du liquide amniotique ou du méconium
dans les vaisseaux sanguin jusqu'au niveau pulmonaire entrainant l'obstruction
des artérioles et une activation de processus de la coagulation (action
de la thromboplastine tissulaire) aboutissant à la CIVD, hypertension
pulmonaire et même décompensation cardiaque (DC).
I.1.10. Le pronostic
Ø Le pronostic maternel : hormis les cas
exceptionnels l'infection amniotique, le pronostic maternel est bon. La
morbidité des suites de couches est plus élevée que
normalement à cause de la relative fréquence des
endométrites (environ 2,5% de cas).
Ø Le pronostic foetal : la morbidité
périnatale liée à la prématurité,
essentiellement et à l'infection est augmentée en cas de RPM
atteignant même 3%. La morbidité infectieuse reste une
préoccupation sur la prise en charge. Nous vous rappelons que
l'ouverture des membranes accélère, au bout d'un certain laps de
temps, la maturation pulmonaire du foetus prématuré.
I.1.11. LES ELEMENTS DE SURVEILLANCE
ü Surveiller des signes vitaux (t° et pouls)
ü Surveiller les signes inflammatoires (VS, GB,
amnioculture, PCR, FL)
ü Surveiller les contractions utérines, BCF, et
l'odeur du L.A.
NB : la grossesse sera interrompue au
moindre signe infectieux si la maturation pulmonaire est acquise.
Sphyngomyeline ; mais si le foetus n'est pas viable, c'est-à-dire
moins de 28 S.A, on évacuera la grasse sans tarder.
CHAPITRE II. MATERIEL ET METHODES
II.1. MATERIEL
a) DESCRIPTION DU TERRAIN D'ETUDE
Notre étude a été
réalisée au département de
Gynéco-obstétrique du Centre Hospitalier Roi Baudouin
1er, de Janvier 2011 au Décembre 2013.
b) SITUATION GEOGRAPHIQUE
Le CHRB 1er se trouve dans la commune patriotique
de MASINA, il est borné :
Ø A l'Est par le marché de la
liberté ;
Ø A l'Ouest par l'ancien émetteur de Masina sans
fil :
Ø Au Nord par l'institut technique industriel de Masina
III ;
Ø Au Sud par la concession des témoins de
Jéhovah et l'hôpital BIAMBA Marie MUTOMBO.
c) ORGANISATION DE L'HOPITAL ET
FONCTIONNEMENT
Le CHRB 1er fonctionne avec ses organes
suivants :
A. Le conseil de gestion (C.G) : c'est un organe de
décisions du centre et défini la politique générale
en matière du personnel, de finances, d'approvisionnement et de
dispensation des soins médicaux préventifs, curatifs,
promotionnels et de réadaptation.
Le médecin directeur convoque une réunion en
séance extraordinaire chaque fois qu'une question d'intérêt
général se pose au sein du centre. Il se réunit une fois
par trimestre en séance ordinaire.
Le conseil de gestion est composé des membres
ci-après :
v Le médecin inspecteur provincial ;
v Le médecin directeur ;
v Le médecin chef de zone de santé de Masina ou
son délégué
v La directrice de nursing ;
v Le responsable de l'armée du salut ;
v Le représentant de l'armée du salut et de la
commune de Masina ;
v L'administrateur gestionnaire titulaire ;
v Le médecin chef de staff ;
v Le directeur de la division biotechnique ;
v Le médecin inspecteur du district sanitaire de
ndjili.
d) ASPECT FONDAMENTAUX
Les activités du CHRB 1er
devraient se dérouler conformément au plan d'implantation des
zones de santé de la ville de Kinshasa ou application des
stratégies des soins de santé primaires. Par ailleurs, en raison
de sa situation géographique, non loin du plus grand axe routier de la
ville, il constitue le premier contact pour les malades et les
accidentés de l'axe routier du boulevard Lumumba.
En bref, le CHRB 1er poursuit sa mission
essentielle à savoir :
Ø La restauration de la santé
Ø La prévention des maladies
Ø L'enseignement et la recherche.
e) CAPACITE D'ACCEUIL
A travers sa production locale et sa
capacité d'accueil, le CHRB 1er dispose sur l'ensemble de sa
capacité d'accueil de 150 lits budgétaires dont 133 sont
automatiques opérationnels et ces lits sont répartis de la
manière suivante :
|
SERVICES
|
LITS
|
|
Pédiatrie
|
15
|
|
Médecine interne
|
24
|
|
Chirurgie
|
40
|
|
Gynéco-obstétrique
|
32
|
|
Les autres services
|
24
|
|
TOTAL
|
134
|
Source : service de mouvement et
statistiques. Période : Mai 2013, une raison est avancée de
façon que les 150 lits budgétaires ne soient pas tous
fonctionnels parce que d'autres salles des malades ont été
transformées en bureaux et sur l'ensemble de 150 lits budgétaires
16 lits sont non opérationnels.
f) HORAIRE DE TRAVAIL :
Le premier service débute de 08 heures 30 à 15
heures 30'
Le deuxième service va de 15 heure 30
jusqu'à 08 heure 30'.
II.2. METHODOLOGIE
1. TYPE - D'ETUDE : il s'agit
d'une étude, rétrospective, multicentrique ; de Janvier 2011
au Décembre 2013.
2. CADRE D'ETUDE : la
maternité du CHRB 1erMasina.
3. POPULATION : la population
étudiée concerne :
· Toutes les femmes qui avaient présentées
une RPM et porteuse d'une grossesse d'au moins 24 semaines.
· Les patientes n'ayant pas accouché dans les 72
heures, suivant la RPM, c'est-à-dire présentant une
période de latence de minimum 12 heures.
4. CRITERE D'EXCLUSION : nous
avons exclu :
- Les patientes ayant accouchées moins de 72 heures
après la rupture, spontanément ou après
déclenchement du travail ;
- Celles qui ont rompue les membranes avant 23 SA et 6 jours,
dont le diagnostic de la rupture a été fait au-delà de 42
SA ;
- Les grossesses gémellaires.
RECUEIL DES DONNEES
Cette étude nous a permis de retenir
402 cas des ruptures prématurées des membranes sur 2845
accouchements, soit une fréquence de 14,1% de RPM pour une
période allant de janvier 2011 au décembre 2013 au CHRB
1er.
Les patientes ont été
sélectionnées sur base des dossiers médicaux et
obstétricaux (DMO). La requête s'est faite par recherche des
termes, RPM, fissuration ; consultation des grossesses et hospitalisation,
ainsi que par la recherche dans le menu déroulant de la fiche
consultation concernant la perte de liquide amniotique : «
doute » ou « positive ».
LES VARIABLES RECEUILLIES
v Concernant la population étudiée, nous avons
recueilli ;
1. Age de la gestante
2. Parité
3. Durée de la RPM
4. Age gestationnel
5. Mode d'accouchement
6. Délai de la RPM par rapport à
l'accouchement
7. APGAR à la 1ère minute
8. Poids à la naissance
9. Traitement d'ATB et d'autres médicaments
reçus
10. Présentation
CHAPITRE III. RESULTATS
TABLEAU 1. Age de la gestante
|
Tranche d'âge
|
Cas
|
%
|
|
=19 ans
|
94
|
23,38
|
|
20-24 ans
|
139
|
34,58
|
|
25-29 ans
|
114
|
28,36
|
|
30-34 ans
|
30
|
7,46
|
|
= 35
|
19
|
4,73
|
|
Age inconnue
|
6
|
1,49
|
|
TOTAL
|
402
|
100
|
Sur ce tableau, nous pouvons voir que la
majorité des gestantes avait un age compris entre 20 et 24 ans soit
34,58% ; en suite viens l'age compris entre 25 à 29 ans
représent 28,36% et les adolescents ont représentés
23,38%. Dans les 1,49% de cas, l'age des gestantes n'était pas repris
dans les dossiers
TABLEAU 2. Parité des gestantes
|
Parité
|
Cas
|
%
|
|
Primipare
|
181
|
45,02
|
|
Multipare
|
128
|
31,84
|
|
Grande multipare
|
60
|
14,93
|
|
Autres
|
33
|
8,21
|
|
TOTAL
|
402
|
100
|
Presque la moitié des gestantes était de
primipare soit 45,02%. Les multipares ont représentés 31,84%.
Dans 8,21% de dossier, la parité n'était pas reprise ; enfin
14,93% de cas pour les grandes multipares.
TABLEAU 3. Temps de latence de la RPM (durée de
la RPM)
|
Heure
|
Cas
|
%
|
|
12 heures
|
206
|
51,24
|
|
24 heures
|
134
|
33,33
|
|
Non signalés
|
62
|
15,42
|
|
TOTAL
|
402
|
100
|
Plus que la moitié des gestantes
avait consulté avant les 12 premières heures, soit 51,24% contre
15,42% de cas dont le temps de latence n'était pas signalé dans
les dossiers.
TABLEAU 4. Age gestationnel (âge de la
grossesse)
|
Age de la grossesse
|
Cas
|
%
|
|
= 24 SA
|
19
|
4,73
|
|
25 - 34 SA
|
145
|
36,07
|
|
35 - 37 SA
|
114
|
28,36
|
|
38 - 42 SA
|
124
|
30,85
|
|
TOTAL
|
402
|
100
|
La grande majorité des gestantes
était porteuse d'une grossesse non à terme soit 36,07% contre
30,85% de grossesse à terme. Dans 4,73% des cas, l'âge
gestationnel était inférieur ou égal à 24 SA.
TABLEAU 5. Mode d'accouchement
|
Mode d'accouchement
|
Cas
|
%
|
|
Basse
|
318
|
79,10
|
|
Haute (césarienne)
|
58
|
14,43
|
|
Non signalé
|
26
|
6,47
|
|
TOTAL
|
402
|
100
|
La grande majorité des gestantes
avait accouchée par voie basse, soit 79,10% contre 14,43% cas de
césarienne indiqué soit pour présentation transversale,
soit pour S.F.A, soit pour macrosomie foetale. Par ailleurs, la voie
d'accouchement n'était pas signalée dans 6,47% de cas.
TABLEAU 6. Temps de latence entre la RPM et
l'accouchement
|
Temps de latence
|
Cas
|
%
|
|
24 H
|
186
|
46,27
|
|
48 H
|
113
|
28,11
|
|
72 H
|
44
|
10,95
|
|
Non signalé
|
59
|
14,68
|
|
TOTAL
|
402
|
100
|
Un bon nombre de gestante avait
accouché dans les 24 heures qui ont suivi la rupture soit 46,27% contre
28,11% dans les 48 heures et 10,95% après 72 heures qui ont suivi la
rupture. Dans 14,68%, le temps de latence entre la rupture et l'accouchement
n'était pas signalé dansle table
TABLEAU 7. APGAR à la naissance (dès la
première minute)
|
APGAR
|
Cas
|
%
|
|
Bon
|
111
|
27,61
|
|
Mauvais
|
280
|
69,65
|
|
Non signalé
|
11
|
2,74
|
|
TOTAL
|
402
|
100
|
La grande majorité de
nouveau-né avait un mauvais APGAR à la naissance, soit 69,65%
contre 27,61% d'enfant né avec un bon APGAR.
TABLEAU 8. Poids des Nnés.
|
Poids à la naissance
|
Cas
|
%
|
|
= 2500 grammes
|
225
|
55,97
|
|
> 2500 grammes
|
145
|
36,07
|
|
Autres
|
32
|
7,96
|
|
TOTAL
|
402
|
100
|
Les nouveaux nés de poids normal
ont représenté 36,07% contre 55,97% d'enfant né avec
faible poids. Dans 7,96% de cas, le poids à la naissance n'était
pas signalé dans les dossiers.
TABLEAU 9. Antibiothérapie pré-partum
(traitement)
|
ATB
|
Cas
|
%
|
|
Avec ATB
|
200
|
49,75%
|
|
Sans ATB
|
149
|
37,06%
|
|
Non signalé
|
53
|
13,18%
|
|
TOTAL
|
402
|
100
|
La grande majorité des gestantes
a bénéficiée d'une antibiothérapie soit 49,75%
contre 37,06% de cas qui n'avait rien reçu comme antibiotique. Dans
13,18% de cas, la prise ou non d'antibiotique n'a pas été
signalée.
TABLEAU 10. Présentation des foetus
|
Présentation
|
Cas
|
%
|
|
Céphalique
|
296
|
73,63
|
|
Transversale
|
16
|
3,98
|
|
Siège
|
62
|
15,42
|
|
Autres
|
28
|
6,97
|
|
TOTAL
|
402
|
100
|
Les foetus se sont
présenté en céphalique dans 73,63% de cas, dans 3,98%
en transversale et 15,42% de cas en siège. 6,97% de cas, la
présentation n'a pas été signalée dans les dossi
CHAPITRE IV. DISCUSSIONS
Les recherches antérieures ont
notées que la parité et l'âge semblent nettement en cause.
GILLIBRAND trouve près de 50 % de rupture prématurée des
membranes chez les femmes de plus de 35 ans.
La rupture prématurée des membranes
est également plus fréquente chez la multipare que chez la
primipare (GILLIBRAND) et (PLAVANIL) par contre, dans notre étude, nous
trouvons 34,589% des cas de rupture prématurée des membranes chez
les femmes dont l'âge est compris entre 20 et 24 ans.
Quant à la parité, nous remarquons
que les grandes multipares représentent un taux faible par rapport aux
primipares.
Nos résultats sont en contradiction avec ceux
des auteurs ci-hauts cités. Cette contraction pourrait s'expliquer par
l'approche méthodique du fait que GILLIBRAND et PLAVANIL ont
utilisé un grand échantillonnage avec une recherche qui a
duré plusieurs années.
PLAVANIL trouve, dans ses travaux, que la rupture
prématurée des membranes est plus fréquente aux alentours
du terme, puisque dans 1,78 % des cas, l'enfant pèse plus de 2.500 Gr
à la naissance contre 2,77 % d'enfants naissent avec faible poids. De
même, dans notre travail, la plupart des cas de RPM surviennent de 25
à la 34ème semaine soit 36,07 % contre 28,36% des cas
entre 35 et 37 semaines, 30,85 % des cas entre 38ème et
42ème semaine.
Ainsi, pour le poids, nous trouvons 36,07
%d'enfants avec un poids supérieur à 2500 grammes. Selon
GILLIBRAND, la rupture prématurée des membranes est
trouvée dans 20 à 30 % d'accouchent prématurées.
Nos résultats sont inférieurs à ceux
trouvés dans la littérature. Ceci peut s'expliquer par une
différence dans la méthodologie.
Selon PLAVANIL, la présentation siège
est de 17 % lorsque la rupture a lieu avant la 38ème semaine.
Nos résultats (15, 42%) sont inférieurs par rapport à ceux
trouvés par l'auteur ci haut cité. Sa littérature place en
première position l'ampicilline et les céphalosporines comme
l'antibiotique de base. Nous constatons dans nos résultats que 49,75%des
cas de rupture prématurée des membranes ont reçu une
antibiothérapie systématique.
Certaines contradictions et différences
trouvées par rapport aux recherches antérieures (parité et
âge). Nous pensons que la méthodologie utilisée, les
campagnes de sensibilisation pour une maternité sans risque
instaurés par SONU et le Programme National de Naissances
désirables, ont joué un rôle très important en
faveur de certaines évolutions
CONCLUSION
Cette étude rétrospective
consacrée à la Rupture Prématurée des Membranes au
Centre Hospitalier Roi Baudouin 1er avec pour objectif de
contribuer à l'amélioration de la prise en charge de la rupture
prématurée des membranes afin de réduire le taux de
mortalité périnatale et celui des accouchements
prématurés dus à la RPM et avons abouti à des
conclusions suivantes :
v Le profil de la gestante qui présente une rupture
prématurée des membranes est celui d'une primipare jeune,
âgée de 20 à 24 ans ; soit 34,58% porteuse d'une
grossesse non à terme (25-34 SA) avec une proportion de 36,07% et 30,85%
des grossesses à terme (38-42 SA) avec foetus en présentation
céphalique 73,63%.
v La voie basse a été le mode d'accouchement
prédominent 79,10% et la césarienne occupe 14,43% dont les
indications obstétricales : présentation transversale, SFA,
macrosomie foetale et autres.
v Le temps de latence entre la rupture et l'accouchement a
été de 24 heures dans la majorité de cas 46,27%.
v La majorité de nouveau-nés sont nés
avec un mauvais APGAR
v L'antibiothérapie pré-partum a
été de forts usages dans 49,75% de cas contre 37,06% de cas qui
n'ont presque pas fait usage des antibiotiques.
RECOMMENDATIONS
Nos recommandations concernent les autorités
gouvernementales, le personnel médical et les gestantes pour une
meilleure prise en charge et une politique de prévention de la rupture
prématurée des membranes.
Ainsi, pour :
Ø Le gouvernement : nous ne recommandons que le
ministère de la santé de mettre en oeuvre des stratégies
et des programmes efficaces d'éducation sanitaire et de promotion des
soins préventifs des infections génitales.
Ø Le personnel médical : nous exhortons le
médecin et l'infirmier à comprendre l'impotence de l'examen
clinique, des examens de surveillance médicale de la femme
enceinte, des gestes médicaux essentiels de la consultation
prénatale, des examens complémentaires à demander et des
thérapeutiques chez la gestante ; de la prévention des
infections vaginales qui fragilisent les membranes et leur rupture. Nous leurs
demandons en plus à respecter le délai maximal de 24 heure pour
obtenir l'accouchement en cas de RPM afin d'améliorer le pronostic
néonatal.
Ø La gestante ; nous recommandons que toute femme
enceinte puisse se présenter à la consultation prénatale
au moins trois fois durent sa grossesse afin d'atteindre la plus grande
efficacité de dépistage des complications précoces et
tardives de la grossesse ;qu'elle se soucie de faire les soin intimes
normaux visant à réduire les infections vaginales, et enfin,
qu'elle évite les mauvaises habitudes d'usage systématique
d'antiseptiques vaginales, qui favorisent la survenue de la vaginose
bactérienne la quelle favorise la RPM.
Références
1. COURTE JOIE J. Dictionnaire Médical pour les
régions tropicales KANGU MAYOMBE 1989 édition St. Paul ;
2. CREPING : le syndrome d'infection amniotique, 5eme
journée nationale de la Médecine périnatale, 1976,
Paris ;
3. MERGER R, LEVY et MEL CHIOR J. : précis
d'obstétrique, 2001, 6ieme édition Ed. Masson, Paris ;
4. ROUVILLOIS J.L : prophylaxie de l'infection en cas de
RPM, Gynéco-obstétrique et Biol. Rep.973, N°271-287,
éd. Masson, Paris ;
5. PLAVANIL : Pronostic dans la rupture
prématuré des membranes, thèse de médecine,
Bordeaux, 1964 P.11 ;
6. ELONGI J. : les urgences en
gynéco-obstétrique ; 2012
7. Journal de gynécologie obstétrique et
biologie de la reproduction vol.29 N°6 Page 588 ;
8. Journal de gynéco-obstétrique et biologie de
la reproduction 2012 P.14-25
9. Marc Mangin : rupture prématurée des
membranes ; Ecole de sages femmes de CAEN(CHU), France 2013 ;
10. HofmeyrGJ,Essilfie-Appiah G, Lawrie TD. Amnio infusion en
cas de rupture prématuré des membranes avant terme
11. European journal of obstetrics & Gynecology and
reproductive Biology 2010 ;148 :3-12 ;
12. Balouet P. Anomalie de la quantité de liquide
amniotique. In Marpeau L. Traité d'obstétrique. EL Servier
Masson, 2010, P. 202-205 ;
13. Lansac J, Berger C, MagninGyn. obstétrique. Masson
4eme éd. Paris, 2003, Page 473 ;
14. Beillat T. Rupture prématurée des membranes.
In Marpeau L. Traité d'obstétrique. Elsevier Masson, 2010,
Page176-182 ;
15. Marion Lucet, Rupture prématurée des
membranes ; université Paris Descartes 2013 ;
16. LEOLA C.T. la rupture prématurée des
membranes, étude rétrospective à l'HGRK 2003.
TABLE DES MATIERES
LISTE DES ABREVIATIONS 0
EPIGRAPHE I
DEDICACE II
REMERCIEMENT III
PLAN V
0. INTRODUCTION 1
0.2. OBJECTIFS 2
0.3. IMPORTANCE DE L'ETUDE 3
0.4. DELIMITATION DE L'ETUDE 3
0.5. SUBDIVISION DE L'ETUDE 4
0.6. HYPOTHESE 4
CHAPITRE I : GENERALITES 5
I.1. APERCU GENERAL SUR LA RUPTURE PREMATUREE DES
MEMBRANES 5
I.1.1. Définition 5
I.1.2. Rappel théorique sur les membranes et
le liquide amniotique 5
I.1.3. Anatomie pathologique 17
I.1.4. Etiologie et pathologie 17
I.1.5. Classification des RPM 19
I.1.6. Symptomatologie et diagnostic de la rupture
prématurée des membranes 20
I.1.7. Diagnostic différentiel 23
I.1.8. CONDUITE A TENIR 23
I.1.9. Les complications 31
I.1.10. Le pronostic 32
I.1.11. LES ELEMENTS DE SURVEILLANCE 32
CHAPITRE II. MATERIEL ET METHODES 33
II.1. MATERIEL 33
CHAPITRE III. RESULTATS 37
CHAPITRE IV. DISCUSSIONS 41
CONCLUSION 43
RECOMMENDATIONS 44
Bibliographie 45
Table des
matieres..........................................................................46
| 


