EPIGRAPHE
« Les Lois de la Vie sont plus importantes que la
Matière de la vie, parce que, connaissant les premières, nous
dominons la seconde. »
« Rien ne peut atteindre plus haut que sa propre
source ; rien n'est appliqué qui ne soit déjà
impliqué ; rien ne se manifeste dans l'effet qui ne soit
déjà dans la cause. »
BAMWISHO BALINGENE Ganelon
DEDICACE
A vous mes parents, Je vous dédie ce travail pour tous
les sacrifices Que vous avez consentis dans l'accompagnement de ce que je suis
maintenant à ce niveau d'ingénieur agrochimiste.
À vous majestés lecteurs et aux personnes de
grands esprits scientifiques révolutionnaires qui comprennent que la
chimie industrielle agricole et la chimie verteen générale est
ici d'une ingéniosité sans limiteet constituedonc le seul pont
vers la transformation socio-économique tout en préservant
l'environnement et le climat.
BAMWISHO BALINGENE Ganelon
REMERCIEMENTS
La réalisation du présent travail est le fruit
des efforts conjugués de plusieurs personnes pendant ces années
assiduités que nous venons de faire à l'Université de Goma
« UNIGOM ».
C'est pourquoi nous tenons à remercier le Directeur du
travail Ir Professeur Docteur SAILE ISAKA et l'encadreur du
travail C.T Gabriel MBUSAMUVUGHE de nous avoir dirigés
afin de parachever nos études de fin de cycle d'ingénieur
agrochimiste.
Nos sentiments de gratitude s'adressent aussi à nos
parents, frères et soeurs, camarades pour la franche dans les
laboratoires de recherche et de contrôle pendant notre parcours
académique.
À la mère nature, à l'univers qui
nourrissent notre âme, source de vie et des connaissances.
À tout notre entourage, dont les noms n'ont pas
été cités ici, grande est notre gratitude, nous vous
gardons dans notre coeur.
RESUME
L'utilisation de biocarburants constitut l'un des axes pour
favoriser l'optimisation de la production agricole, favoriser la
mobilité durable. A quand parles-t-on de biocarburants ?
Les biocarburantssont produits à partir des
matières premières biosourcées donc renouvelable.
Départ leur nature sont des hydrocarburesqui peuvent être
mélangé dans les carburants conventionnels.
De quelle matière première biosourcées
parles-ton ? il y a 3 filières (bioéthanol, biodiesel et
biogaz) dans le cadre de notre étude nous nous situons dans la
filière biodiesel dont on peut utiliser les huiles
végétales, des huiles usagées ou des graisses animales.
Celles-ci subissent soit une estérification pour
obtenir l'ester d'alkyle où la transestérification
accompagnés des catalyseurs pour obtenir de l'EMAG.
Le but de cette étude est de synthétiser un
biodiesel à partir de l'huile de palme, en réduisant sa
densité et sa viscosité élevée par
laréaction de transestérification. Pourun soutien à
l'agriculture, l'indépendance énergétique (les machines
agricoles et de transport,), aménagement du territoire ou encore dans la
lutte contre le changement climatique.
Mots clés :Biocarburant, Huilede Palme,
Synthèse et Transestérification.
ABSTRACT
The use of biofuels is one of the axes for promoting the
optimization of agricultural production, promoting sustainable mobility. When
are we talking about biofuels?
Biofuels are produced from biobased raw materials and
therefore renewable. Starting their nature are hydrocarbons which can be mixed
into conventional fuels.
What bio-based raw material are you talking about? there are 3
sectors (bioethanol, biodiesel and biogas) within the framework of our study we
are in the biodiesel sector from which we can use vegetable oils, waste oils or
animal fats.
These undergo either esterification to obtain the alkyl ester
or transesterification accompanied by catalysts to obtain EMAG.
The aim of this study is to synthesize biodiesel from palm
oil, reducing its density and high viscosity through the transesterification
reaction. To support agriculture, energy independence (agricultural and
transport machinery), land use planning or even in the fight against climate
change.
Keywords: Biofuel, Palm Oil, Synthesis and
Transesterification.
LISTE DES ACRONYMES ET
ABREVIATIONS
% : Pourcentage
°C : Degré Celsius
B7* : Correspond à 7%v maximum d'EMAG dans 1L de
diesel
BioGNV : Biocarburant gaz naturel des
véhicules
CO2 : Dioxyde de carbone
CT : Chef de travaux
Dr : Docteur
E10* : Correspond à 10%v maximum
d'éthanol dans 1L d'essence
EMAG : Esters Méthyliques des acides gras
g : Gramme
H2SO4 : Sulfate
d'hydrogène (Acide sulfurique)
HVO : Huiles végétales
hydrotraitée
Ir : Ingénieur
KOH : Hydroxyde de potassium
m.s-1 : Mètre par seconde
MG : Monoglycéride
mL : Millilitres
n : Nombre de moles
NaOH : Hydroxyde de sodium (soude)
O2 : Dioxygène
PCI : Le pouvoir calorifique inférieur
PE : Le point d'éclair (PE)
Prof : Professeur
TG : Triglycéride
UNIGOM : Université de Goma
V : Volume
LISTE DES FIGURES
Figure n°1 équation 1 :
Estérification de triglycéride
Figure n°2 Réaction de
transestérification
Figure n°3 Rection d'Hydrolyse de
triglycéride et de formation des savons
Figure n°4 Mesure de la densité de
biodiesel
Figure n°5 Mécanisme de distillation
et calcul de condensat
Figure n°6 Mécanisme de prise et
calcul de couleur
Figure n°7 Mangement de l'indice
d'atomisation (flash point).
Figure n°8 Exemple de prise de poids de
catalyseur (Hydroxyde de potassium)
Figure n°9 Réaction de
transestérification catalytique de l'huile de palme
Figure n°10 Appréciation de la
séparation des phases (liquide-liquide) non
miscible
Figure n°11 Appréciation de la
séparation des phases (liquide-liquide) non miscible après lavage
à l'eau distillé
Figure n°12 Appréciation de la
séparation des Distillat d'EMAG à 362°C
Figure n°13 Evolution de la courbe d'indice
d'acide
Figure n°14 Evolution de la courbe de
densité
Figure n°15 Evolution de la courbe de
viscosité cinématique
Figure n°16 Appréciation de formation
de condensat après distillation
Figure n°17 Appréciation de la couleur
du biodiesel
Figure n°18 Evolution de l'indice
d'acidité des huiles et biodiesels
Figure n°19 Evolution de l'indice de
densité des huiles et biodiesels
Figure n°20 Evolution de la viscosité
en terme de vitesse des huiles et biodiesels
LISTE DES TABLEAUX
Tableau n°1 Classification des huiles
végétales selon l'indice d'iode
Tableau n°2 La composition Chimique de
diverses huiles végétales
Tableau n°3 Structures chimiques des
acides gras cités au tableau 2.
Tableau n°4 Conditions optimales de la
méthanolyse de quelques huiles
végétales.
Tableau n°5 Propriétés du
carburant du biodiesel et du carburant diesel.
Tableau n°6 Comparaison des
propriétés des esters d'huile de palme par rapport aux
propriétés des huiles minérales.
Tableau n°7 Liste d'équipement
utilisé dans l'expérimentation
Tableau n°8 Caractéristiques de
l'huile de marque « Palmolin »
Tableau n°9 Composition en pourcentage
d'acides gras de l'huile PALMOLIN.
Tableau n°9 Caractérisation
physico-chimique par paramètre de
Volatilité.
Tableau n°10 Propriétés des
esters éthyliques d'acides gras
TABLE DES MATIERES
EPIGRAPHE
ERREUR ! SIGNET NON
DÉFINI.
DEDICACE
II
REMERCIEMENTS
III
RESUME
IV
ABSTRACT
ERREUR ! SIGNET NON
DÉFINI.
LISTE DES ACRONYMES ET ABREVIATIONS
VI
LISTE DES FIGURES
VII
LISTE DES TABLEAUX
VIII
TABLE DES MATIERES
IX
INTRODUCTION
1
CHAPITRE I. ETUDE BIBLIOGRAPHIQUE
4
I.1. LES HUILES VEGETALES
4
I.1.1. LES HUILES VEGETALES COMME
CARBURANTS
4
1.1.2. LES PROPRIETES DES HUILES DANS LA
SYNTHESE DU BIOCARBURANT
4
I.2. LES BIOENERGIES
6
I.2.1. FILIERE DE BIOGAZ
6
UTILISATION DU BIOGAZ
7
I.2.2. FILIERE DE BIOETHANOL
7
UTILISATION DE L'ETHANOL COMME CARBURANT
7
I.2.3. FILIERE DE BIODIESEL
8
A. PROBLEMATIQUE
8
B. BIODIESEL RENOUVELABLE
9
C. BIODIESEL DANS LA REDUCTION DES
GAZ A EFFET DE SERRE
9
D. NIVEAUX DE POLLUTION DE BIODIESEL
PLUS FAIBLES
10
E. DEVERSEMENTS ET CONTAMINATION DE
SURFACE NEGLIGEABLE
10
F. LA CONVERSION DES TRIGLYCERIDES EN
BIODIESEL
10
I.2.3.1. LA REACTION DE
TRANSESTERIFICATION
11
I.2.3.2. LA TRANSESTERIFICATION EN CATALYSE
HOMOGENE
12
I.2.3.3. LA TRANSESTERIFICATION CATALYTIQUE
HETEROGENE
12
I.2.3.4. LE RAPPORT ALCOOL/HUILE
12
I.2.3.5. LA NATURE ET LA QUALITE DE
L'HUILE
13
I.2.3.6. LA NATURE, LA QUANTITE ET LE TYPE
DE CATALYSEUR
13
I.2.3.7. LE BIODIESEL EST UNE SOURCE
D'ENERGIE DE SUBSTITUTION AU DIESEL
14
CHAPITRE II. PARTIE EXPERIMENTALE
15
II.1. MATERIEL ET PRODUCTION
15
II.2. PARAMETRES PHYSIQUES ET CHIMIQUES
16
II.2.1. INDICE D'ACIDE
16
II.2.3. MESURE DE VISCOSITE
16
II.2.4. CALCUL DE LA DENSITE
17
II.2.5. LA DISTILLATION
18
II.2.6 COULEUR
18
II.2.7 INDICE D'INFLAMABILITE
19
II. 3. PROTOCOLE DE SYNTHESE DU
BIODIESEL
20
II.3.1. PRESENTATION DE NOS HUILES
20
II.3.2. FORMULE BRUTE DU TRIGLYCERIDE
CORRESPONDANT (PALMOLIN)
20
II.3.3. MASSES DE REACTIFS CHIMIQUES
POUR LA SYNTHESE DE BIODIESEL
21
II.3.4. SYNTHESE DU BIODIESEL
22
II.3.4.1. REACTION DE SYNTHESE
22
II.3.4.2. DECANTATION ET SEPARATION DES
PHASES
22
II.3.4.3 ETAPE DE LAVAGE
(RINÇAGE)
23
II.3.4.4. ÉTAPE DE DISTILLATION
24
II.3.4.5. CARACTERISTIQUES DU BIODIESEL
24
II.3.5. TESTS DU BIODIESEL
24
II.3.5.1 TEST DE MISCIBILITE
24
II.3.5.2 TEST DE DENSITE
25
II.3.5.2 ESSAI D'INFLAMMABILITE
25
II.3.5.3 RENDEMENT DE LA SYNTHESE
25
CHAPITRE III. RESULTATS ET DISCUSSIONS
26
III.1. RESULTATS
26
III.1.1. DIFFERENTS TYPES D'HUILES
COMMERCIALISEES EN VILLE DE GOMA
26
III.1.2. ETUDE PHYSICO-CHIMIQUE DU
BIODIESEL
26
III.1.3. COMPARAISON AVEC LES ANALYSES
RECENTES DES CARACTERISTIQUES PHYSICO-CHIMIQUES DU BIODIESEL
30
III.2. DISCUSSIONS
32
III.2.1. COMPARAISON ENTRE LES TYPES
D'HUILES ET LES BIODIESELS
32
III.2.1.A INDICE D'ACIDE
32
III.2.1.B INDICE DE DENSITE
32
III.2.1.C INDICE DE VISCOSITE
33
III.2.2 OPINIONS ET RECHERCHES SUR LE
BIODIESEL EN RD CONGO
33
CONCLUSION
GÉNÉRALITÉS
35
REFERENCIEMENTS
37
BIBLIOGRAPHIE
37
WEBOGRAPHIE
39
INTRODUCTION
De nombreuses réactions chimiques permettent de
produire de l'énergie, ce qui est le cas des réactions de
combustion, la découverte de la combustion par l'O2 est
imputable au chimiste français Lavoisier, en 1775. Elle a cependant
conduit pendant l'ère industrielle à l'émission massive de
CO2, qui est un gaz à effet de serre contribuant pour une
large part aux phénomènes de dérèglement climatique
(David Soissons & Nathan 2000).
La communauté internationale se préoccupe de
l'environnement : la question de pollution en tout genre, le
réchauffement climatique et l'économie des énergies.
L'assainissement et la préservation de l'environnement, ainsi que la
recherche de nouvelles sources d'énergies propres et renouvelables sont
devenus la priorité du 21ème siècle (Nidhal
Attia Mars 2018).
A l'heure actuelle, environ 95 % des besoins
énergétiques mondiaux sont assurés par les carburants
fossiles et on estime que la demande globale en énergie devrait
s'accroitre de 57% d'ici 2030. Dans ce contexte, les biocarburants ont souvent
été présentés comme la panacée vers un bilan
carbone neutre, moins d'émissions néfastes et une
biodégradation plus rapide en cas de déversement accidentel
(Patrice LEVAN G, D. SHEIL et Markku K., 2015).
Les huiles végétales peuvent être
utilisées directement comme carburants car leur pouvoir calorifique est
important (environ 80 % de celui du carburant fossile). Mais elles ont des
viscosités cinématiques importantes, au moins 10 fois
supérieures à celles du diesel à 40°C, ce qui
occasionne une mauvaise atomisation dans la chambre de combustion du moteur
(Conceicao M., Silva F.C., and Souza A.G.) & (Kulkarni M.G., and Bakhshi
N.(2007). D'autre part, leurs combustions y provoquent la formation
d'importants dépôts(Altin R. C., and Yücesu H.S.,
(2001),Ropkins K., Li H., and Andrews G., (2007). Pour les raisons
citées précédemment, l'utilisation directe des huiles dans
les moteurs est à éviter en général. Les huiles
végétales sont transformées par transestérification
en biodiesel dont les propriétés physico-chimiques sont voisines
de celles du carburant fossile (essence, diesel).
Les biocarburants sont produits par des matières
premières biosourcées donc renouvelable, départ leurs
origines, une problématique s'est alors imposée, celle de
l'équilibre de la demande de plus en plus forte de l'énergie non
fossile et la quantité de terres à consacrer pour celle-ci (TOTAL
Foundation 2020).
Avec 62 millions de tonnes produites en 2016, l'huile de palme
est l'huile végétale la plus produite au monde devant l'huile de
soja, l'huile de colza et l'huile de tournesol, l'huile d'arachide. Plusieurs
atouts la rendent particulièrement attractive, d'abord pour l'industrie
: ses faibles coûts de production, son rendement élevé
à l'hectare, ainsi que ses propriétés physico-chimiques.
Grâce à ces avantages comparatifs, l'huile de palme est devenue
omniprésente dans de nombreux produits de consommation, que ce soit dans
l'industrie alimentaire, les cosmétiques, les produits d'entretien
où ces dernières années pour la production
d'agro-carburants ou d'électricité (Rapport : Dossier, mythe
de l'huile de palme 100% durable, Les limites des initiatives
volontaires : le cas de la RSPO et de l'Alliance Belge pour une huile de
palme durable 2018).
Le biocarburant présente de nombreux avantages face au
carburant d'origine fossile. Il possède généralement un
indice d'octane plus élevé ainsi qu'une meilleure
efficacité de combustion. L'un des plus importants aspects porte sur les
émissions de gaz à effet de serre et autres polluants. En effet,
sa combustion produit moins de soufre, moins de CO2, moins de
composés aromatiques, moins de monoxydes d'hydrocarbures non
brulés.
A la lumière de notre problématique, les
questions suivantes méritent d'être posées :
- Les propriétés physico-chimiques de l'huile de
palme influencent-elles le rendement de biocarburant ?
- Les catalyseurs acides et bases appliqués
améliores-t-ils le rendement ?
- Le produit synthétiser as-t-il les mêmes
caractéristique physico-chimique que les carburants fossiles ?
Faisant suite logique à notre questionnement, nous
formulons les hypothèses suivantes :
- Les propriétés physico-chimiques de l'huile de
palme influenceraient le rendement de biocarburant.
- Les catalyseurs acides et bases utilisés
amélioreraient le rendement du biocarburant.
- Le biocarburant obtenu aurait les caractéristiques
physico- chimiques proches des carburants fossiles comme le diesel.
Ce travail a pour objectif global, la synthèse du
biocarburant par transestérification catalytique de l'huile de palme.
Les objectifs spécifiques poursuivis sont :
- Déterminer les propriétés
physico-chimiques de l'échantillon de l'huile de palme que nous allons
utiliser pour synthétiser le biocarburant ;
- Evaluer le rendement du biocarburant vis-à-vis des
catalyseurs acide et base.
- Déterminer les propriétés
physico-chimiques du biocarburant synthétiser ;
Notre étude expérimentale s'étend sur une
période allant du 25 septembre 2021 au 15Novembre 2021, avec plusieurs
des travaux en laboratoire de l'ISTM KATOYI et de l'OCC Goma, les manipulations
ont été orientées vers la transestérification
hétérogène de l'huile de palme raffiné (PALMOLIN)
et l'huile de palme (MAWESA) encore brute en présence d'un excès
de méthanol et des catalyseurs comme le KOH, H2SO4
pour obtenir un mélange d'esters d'acides gras qui après
être lavé et séché on obtient le
biodiesel.
Le travail est harmonisé comme suit :
- Partie introductive.
- Le chapitre I est consacré à une mise au point
bibliographique.
- La partie expérimentale, qui englobe les
méthodes et techniques utilisées, est exposée dans le
chapitre II.
- Les résultats et discussions de la réaction de
transestérification de l'huile de palme sont analysés et
commentés dans le chapitre III
- Et enfin, nous terminerons avec une conclusion
générale.
Après avoir présenté la
problématique, les hypothèses et les objectifs de notre
étude, le chapitre premier ci-dessous décrisles généralités sur notre
thème de travail.
CHAPITRE I. ETUDE BIBLIOGRAPHIQUE
Dans ce chapitre sont présentées les
données en rapport avec la généralité des huiles
végétales comme carburants, les bioénergies et leurs
utilisationset importance en agriculture, dans le transport et sur
l'environnement.
I.1.
LES HUILES VEGETALES
I.1.1. LES HUILES VEGETALES COMME CARBURANTS
Les huiles végétales peuvent être
utilisées directement comme carburants car leur pouvoir calorifique est
important (environ 80 % de celui du carburant fossile). Mais elles ont des
viscosités cinématiques importantes, au moins 10 fois
supérieures à celles du diesel à 40°C, ce qui
occasionne une mauvaise atomisation dans la chambre de combustion du moteur
(Conceicao M.M., Bezerra,A.F., Jr., and Souza A.G., 2007) &(Kulkarni M.G.,
and Bakhshi N.,(2007). D'autre part, leurs combustions y provoquent la
formation d'importants dépôts (Altin R. C., and Yücesu H.S.,
(2001) &(Li H., Tate J., and Andrews G., 2007).
Pour les raisons citées ci-dessus, l'utilisation
directe des huiles dans les moteurs est à éviter en
général. Les huiles végétales sont
transformées par transestérification en biocarburant dont les
propriétés sont voisines de celles du carburant fossile (essence,
mazout,).
1.1.2. LES PROPRIETES DES HUILES DANS LA SYNTHESE DU
BIOCARBURANT
Les principales caractéristiques physico-chimiques des
huiles végétales engagé dans la synthèse de
biocarburant présentent plusieurs paramètres.
Tableau n°1 Classification des huiles
végétales selon l'indice d'iode
|
Indice d'iode
|
5-50
|
50(100
|
100-150
|
>150
|
|
Huiles
|
Saturée
|
Mono-insaturée
|
Di-insaturée
|
Tri-insaturée
|
|
Type
|
Laurique
|
Palmitique
|
Stéarique
|
Oléique
|
Linoléique
|
Linoléinique
|
Eléostarique
|
|
Exemple
|
Babasse
Coprah
Palmiste*
|
Buriri
Palme*
|
Karité
|
Arachide
Colza*
Jatropha
Olive
Ricin
|
Coton
Maïs
Soja
Tournesol*
|
Lin
|
bois de chine
|
(*) Huiles classiques.
Tableau n°2 La composition Chimique de
diverses huiles végétales
|
Huile de palme
|
Huile de soja
|
Huile de colza
|
Huile de tournesol
|
Huile d'olive
|
|
Acides gras saturés
|
45-55
|
11-21
|
2-8
|
10-16
|
9-26
|
|
- Acide myristique C14 :O
|
0,5-2
|
<0,2
|
<0,2
|
<0,2
|
7,5-20
|
|
- Acide palmitique C16 :O
|
39,5-47,5
|
8-13
|
1-5
|
5-8
|
7,5-20
|
|
- Acide stéarique C18 :O
|
3,5-6
|
3-6
|
1-2
|
4,6
|
0,5-6
|
|
Acides gras monoinsaturés
|
38-45
|
17-26
|
56-65
|
15-26
|
56-87
|
|
- Acide oléique C18.1n-9
|
36-44
|
17-26
|
55-62
|
15-25
|
55-83
|
|
Acides gras polyinsaturés
|
9-12
|
54-72
|
26-32
|
62-70
|
4-22
|
|
-Acide linoléique C18 ;2n-6
|
9-12
|
50-62
|
18-22
|
62-70
|
3-31
|
|
-Acide linolénique C18:3n-3
|
<0,5
|
4-10
|
8-10
|
<0,2
|
<1
|
(Fonds français Alimentaire & Santé 2015)
Tableau n°3 Structures chimiques des
acides gras cités au tableau 2.
|
Acides
|
Formules
|
Notation
|
|
Dénominations communes
|
Désignations chimiques
|
|
Caprylique
|
Octanoïque
|
CH3(CH2)6COOH
|
C8:O
|
|
Caprique
|
Décanoïque
|
CH3(CH2)8COOH
|
C10:O
|
|
Laurique
|
Dodécanoïque
|
CH3(CH2)10COOH
|
C12:O
|
|
Myristique
|
Tétradécanoïque
|
CH3(CH2)12COOH
|
C14:O
|
|
Palmitique
|
Héxadéanoïque
|
CH3(CH2)14COOH
|
C16:O
|
|
Stéarique
|
Octadécanoïque
|
CH3(CH2)18COOH
|
C18:O
|
|
Oléique
|
9-Octadécanoïque
|
CH3(CH2)7CH=CH(CH2)7COOH
|
C18:1  9 9
|
|
Linoléique
|
9,12-
|
CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH
|
C18:2  6 6
|
|
  -Linolénique -Linolénique
|
6,9,12-
|
CH3(CH2)4CH=CHCH2CH=CHCH2CH=CH(CH2)4CO
|
C18:3  6 6
|
|
  -Linolénique -Linolénique
|
9,12,15-
|
CH3CH2)CH=CHCH2CH=CHCH2CH=CH(CH2)7COOH
|
C18:3  3 3
|
|
Eicosénoïque
|
Cis-11-éicosénoïque
|
CH3(CH2)6CHOHCH=CH(CH2)9COOH
|
0:1
|
|
Bethénique
|
Docosanoïque
|
CH3(CH2)20COOH
|
2:O
|
|
Erucique
|
13-docosénoïque
|
CH3(CH2)7CH=CH(CH2)11COOH
|
2:1
|
I.2.
LES BIOENERGIES
Les bioénergies désignent l'ensemble des
filières de valorisation énergétique de la biomasse.
La biomasse est l'ensemble de la matière organique
d'origine végétale, animale ainsi que leurs produits de
transformation. La biomasse est une source d'énergie alternative et
propre. L'avantage de la conversion énergétique de la biomasse,
par rapport aux autres sources énergétiques renouvelables,
réside dans le fait qu'en plus de la production d'énergie, elle
participe activement aux traitements des déchets organiques contribuant
ainsi à l'assainissement de l'environnement. On peut distinguer trois
types de biomasse:
- La biomasse animale telle que, graisses animales, rejets
d'abattoirs, ...
- La biomasse végétale indirecte issue des
déchets agroalimentaires, d'élevages d'animaux, de papeteries,
des ménages, ...
- La biomasse végétale directe issue des
différentes plantes (bois, Palmier à huile, betterave, canne
à sucre, maïs, tournesol, colza, algues, ...)
La valorisation de la biomasse en énergie peut
être réalisée selon trois procédés :
- Biochimiques : Fermentation et méthanisation
- Thermochimiques : Combustion, pyrolyse et
gazéification
- Physicochimiques: ExtractionsPurificationsAfin la
transestérification d'huiles végétales.
Par conséquent les bioénergies sont
séparées en plusieurs filières selon le type de
procédé, la forme de l'énergie ou vecteur (gazeux, liquide
ou solide) d'énergie propre et renouvelable dont on peut citer :
þ Filière biogaz,
þ Filière bioéthanol,
þ Filière biodiesel...
I.2.1. FILIEREDE BIOGAZ
Le biogaz est un gaz issu des dégradations biochimiques
complexes, naturelles, des matières organiques en absence
d'oxygène (anaérobie) : la fermentation méthanique ou
biométhanisation (J. C. Verchin, (2004). La biométhanisation est
un processus biochimique qui se déroule en trois étapes
principales :
- L'acidogénèse : hydrolyse et
fermentation des macromolécules en molécules organiques simples
sous l'action de bactéries acidogènes.
- L'acétogénèse:
transformation, par des bactéries acétogènes, des
molécules simples en précurseurs (acide acétique,
méthylamines, méthanol, ...) du méthane.
- La méthanogénèse:
formation du méthane par des bactéries
méthanogènes. Les réactions sont exothermiques et lentes
mais qui 70% de CH4 dont 50% environ provient de l'acide
acétique.
Le biogaz est un mélange principalement de
méthane (CH4), de dioxyde de carbone (CO2) ; mais
il contient aussi de la vapeur d'eau (H2O), du sulfure
d'hydrogène (H2S), des composés fluorés (F.
Maramba, 1978)& (B. Kaltwasser, 1980).
UTILISATION DU BIOGAZ
Le biogaz peut être utilisé soit directement,
soit après épuration ; sa valorisation énergétique
peut être sous forme :
- Chaleur : cuisson, chaudière, ... Chaleur +
électricité (cogénération) : moteur+alternateur,
frigos, ....
- Carburant pour véhicules (:
www.cf.ac.uk/archi/research/cost8
/case/sweden.html&
www.zeus-europe.org/stock.html
)
I.2.2. FILIEREDE BIOETHANOL
L'éthanol est produit à partir de plantes
sucrières (canne à sucre, betterave, sorgho, ...) et de plantes
amylacées et céréalières (pomme de terre,
maïs, manioc, ...). Le sucre est extrait et obtenu par hydrolyse de grosse
molécules composées en molécules simple ; il est ensuite
fermenté. L'éthanol issu de la fermentation est distillé
et peut être incorporé soit directement dans l'essence soit sous
forme d'ETBE (Méthyl Tertio Butyle Ether) lequel est obtenu par
éthérification de l'alcool. L'ETBE est un produit de la
réaction de l'éthanol avec l'isobutène (F. Maramba,
1978)& (B. Kaltwasser, 1980).
UTILISATION DE L'ETHANOL COMME CARBURANT
La production mondiale de bioéthanol dans le monde est
estimée à 52% au Brésil à partir de la canne
à sucre, de 43% aux USA à partir du maïs et 5% pour le reste
du monde. Son utilisation comme carburant, dans le monde, suit ces chiffres de
production ; en effet au Brésil l'éthanol est
mélangé à l'essence entre 20 et 25% tandis qu'USA ce taux
atteint les 10%. En Europe son incorporation, dans l'essence, est
autorisée jusqu'à 5%. Néanmoins des mélanges
élevés à 85% d'éthanol se développent
grâce à la technologie des « flex fuel vehicules
» qui admettent des mélanges à des taux
variables.L'affinité de l'éthanol pour l'eau et sa grande
volatilité engendre des difficultés techniques dans les
mélanges essence - éthanol(F. Maramba, 1978) & (B.
Kaltwasser, 2010).
I.2.3.FILIEREDE BIODIESEL
A.
PROBLEMATIQUE
Le biodiesel est constitué d'esters monoalkyliques
d'acides gras à longue chaîne dérivés de
matières premières renouvelables telles que l'huile
végétale ou les graisses animales, destinés à
être utilisés dans les moteurs. Le concept d'utilisation du
biodiesel comme carburant en agriculture comme dans de transport remonte
à la première démonstration du moteur diesel pour lequel
Rudolph Diesel a utilisé du biodiesel fabriqué à partir
d'huile d'arachide en 1893. Le biodiesel a des propriétés
physiques très similaires au diesel conventionnel. Il était
caractérisé par ses propriétés physiques et
énergétiques, notamment ; densité, viscosité,
pouvoir calorifique élevé, indice de cétane, point de
trouble, point d'écoulement et points d'éclair selon les normes
ISO(M. Balat., 2000)
En 2017 SINGH & G. CHAUDHARY ont estimésqu'une
capacité de production de près de 30 millions de tonnes de
biodiesel existe dans le monde. D'autre part, il existe une production annuelle
totale d'huiles végétales d'environ 110 millions de tonnes par
an, qui est principalement utilisée à des fins alimentaires. Car
la production d'huiles végétales ne peut pas être
augmentée de manière à ce qu'il y ait une demande de
biodiesel et une concurrence avec le marché alimentaire. En outre, les
préoccupations concernant la production non durable de plantes
oléagineuses comme l'huile de palme ont conduit à de longues
discussions menant à la recherche de graines oléagineuses non
comestibles. Toutes les huiles végétales et graisses animales
sans oublier les huiles usées peuvent être utilisées comme
matière première pour la production de biodiesel. La plupart de
ces huiles et graisses ont une composition chimique similaire.
Les principaux acides gras sont ceux avec une longueur de
chaîne de 16 et 18 atomes de carbone où la chaîne pourrait
être saturée ou insaturée. Les esters méthyliques
produits à partir de ces acides gras ont des caractéristiques de
combustion très similaires dans un moteur diesel car les principaux
composants du carburant diesel fossile sont également des hydrocarbures
à chaîne droite avec une longueur de chaîne d'environ 16
carbones (hexadécane). Les principales matières premières
pour la production de biodiesel aujourd'hui sont l'huile de palme et l'huile de
colza (canola), l'huile de soja. De plus, une série d'autres huiles
végétales à une distribution d'acides gras assez
similaire, elle peut être utilisée comme mélange. Seules
l'huile de coco et l'huile de palmiste ont des acides gras à 12 ou 14
carbones comme composants majeurs (M. Mittelbach., 2009)
La production de biocarburant à petite échelle
pourrait répondre à la demande énergétique locale
(agriculture, transport rurale, groupes électrogènes fixes,
chauffage, ...); ce dernier nécessiterait une qualité et une
quantité constante qui ne peut être obtenue que par une production
à grande échelle.
En 2030, on estime à environ 10% la part des
biocarburants dans l'agriculture et le transport dans les pays
développés et envoies de développement(F.O. Licht
Consulting Company, 17 Juillet 2007).
B.
BIODIESEL RENOUVELABLE
La plupart des combustibles fossiles expireront et finiront en
fumée un jour. Étant donné que la plupart des sources
comme le fumier, les céréales, les déchets des cultures et
des plantes sont renouvelables et ne risquent pas de s'épuiser
sitôt. L'éthanol est un alcool. Il est fabriqué en
fermentant toute biomasse riche en glucides (amidons, sucres ou celluloses,
pectine, ...). L'éthanol est principalement utilisé comme additif
de carburant pour réduire le monoxyde de carbone d'un véhicule.
Le biodiesel est fabriqué en combinant l'alcool,
généralement du méthanol, avec de l'huile
végétale, des graisses animales ou des graisses de cuisson
recyclées. Il peut être utilisé comme additif pour
réduire les émissions des véhicules
généralement de 20% ou dans sa forme pure comme carburant
alternatif renouvelable pour les moteurs diesel. Puisqu'ils utilisent des
matières végétales et animales pour la production. Ils
sont considérés comme une source d'énergie renouvelable.
Ils sont utilisés comme additifs dans les carburants diesel et peuvent
être utilisés dans les moteurs diesel sans nécessiter de
modifications dans la conception ou le type du moteur. Advantages of bio
fuels-biofuels :
(
http://biofuel.org.uk/advantages-of-biofuels.html).
C.
BIODIESEL DANS LA REDUCTION DES GAZ A EFFET DE SERRE
Les Combustibles fossiles lorsqu'ils sont brûlés.
Ils produisent une grande quantité de gaz à effet de serre, par
exemple du dioxyde de carbone dans l'atmosphère. Ces gaz à effet
de serre piègent la lumière du soleil et provoquent le
réchauffement de la planète. La combustion du charbon et du
pétrole augmente la température et provoque une alerte mondiale.
Pour réduire l'impact des gaz à effet de serre, l'activité
humaine dépendante de l'énergie dans son évolution
technologique doit utiliser les bioénergies. Des études
suggèrent que les bioénergies réduisent les gaz à
effet de serre jusqu'à 65% (
http://biofuel.org.uk/advantages-of-biofuels.html).
D.
NIVEAUX DE POLLUTION DE BIODIESEL PLUS FAIBLES
Puisque les biocarburants peuvent être fabriqués
à partir de ressources renouvelables. Ils causent moins de pollution
à la planète. Cependant, ce n'est pas la seule raison pour
laquelle l'utilisation de biocarburants est encouragée. Ils
libèrent des niveaux inférieurs de dioxyde de carbone. Les
émissions produites par la combustion de biocarburants sont nettement
inférieures à celles produites à partir de combustibles
fossiles. Les émissions de CO2 provenant de la combustion de
bioéthanol et de biodiesel sont jusqu'à neuf fois
inférieures à celles de la combustion d'essence. Selon une
technique appelée analyse du cycle de vie (ACV), les biocarburants de
première génération permettent d'économiser
jusqu'à 60 % et les biocarburants de deuxième
génération permettent d'économiser jusqu'à 80 % des
émissions de carbone par rapport aux autres combustibles fossiles (
http://biofuel.org.uk/advantages-of-biofuels.html).
E.
DEVERSEMENTS ET CONTAMINATION DE SURFACENEGLIGEABLE
Les biocarburants ne sont pas sûrs à 100 %, mais
ils sont beaucoup plus sûrs que les combustibles fossiles. Les
biocarburants sont des molécules biologiques et cela signifie qu'ils
sont biodégradables. Les bactéries et autres organismes qui
vivent naturellement dans le sol et l'eau sont capables d'utiliser des
molécules de biocarburant comme sources d'énergie et de les
décomposer en produits inoffensifs. Cela signifie que même si les
déversements concentrés de biocarburants peuvent tuer des choses
comme les plantes et les petits animaux, ils ne persisteront pas dans
l'environnement et ne causeront pas de dommages ou rendront une zone
inhabitable pendant de longues périodes (
http://biofuel.org.uk/advantages-of-biofuels.html).
F.
LA CONVERSION DES TRIGLYCERIDES EN BIODIESEL
Le Biodiesel est un carburant qui a plus ou moins les
mêmes caractéristiques que le Carburant diesel.
Généralement, des huiles végétales sont
employées comme l'huile de tournesol, l'huile de soja, l'huile de colza
ou l'huile de palme. Elles sont soumises à une réaction chimique
: Tableau n°4 Conditions optimales de la méthanolyse
de quelques huiles végétales.
|
Huiles (H)
|
Méthanol/H
|
Catalyseur/H % en masse
|
Temp. (°C)
|
Temps (h)
|
Rends.(%)
|
Réf.
|
|
Palme
|
6/1
|
1-4
|
40-60
|
3-10
|
91-98
|
42-45
|
|
Ricin
|
6/1
|
1-2
|
80-100
|
+5
|
80
|
36
|
|
Soja
|
12/1-20/1
|
5-8
|
65-120
|
1-1,5
|
92-98
|
27,30,37
|
|
Tournesol
|
6/1, 12/1, 41/1
|
0,1-3
|
50 et 252
|
0,1-10
|
85-90
|
32-35
|
I.2.3.1. LA REACTION DE TRANSESTERIFICATION
La transestérification est une réaction
catalytique homogène ou hétérogène des
triglycérides et d'alcool. Le catalyseur est un acide ou une base au
sens de Bronsted et/ou de Lewis. Si l'alcool (méthanol) on a une
méthanolyse, si l'alcool est l'éthanol on a une
éthanolyse. La réaction est constituée de trois
étapes réversibles consécutives au cours desquelles les
triglycérides sont convertis d'abord en diglycérides, puis en
monoglycéride et en glycérol. Après chaque étape,
un ester est formé (Figure n°1 équation
1 : Estérification de triglycéride).
Les monoglycéride issus du glycérol peuvent
être ajoutés au biocarburant d'une part ; d'autre part ils ont un
intérêt particulier dans la synthèse de médicaments,
de produits cosmétiques, de détergents, savons, etc. .... (Rieger
M. 1990).
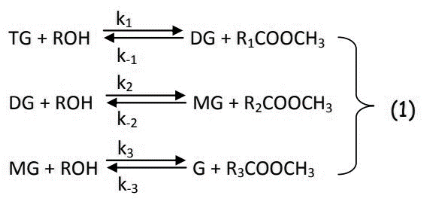
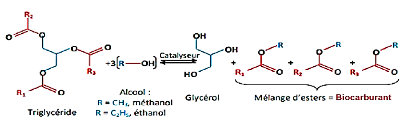
Dans la réaction globale, 3 moles d'esters et une mole
de glycérol sont produites à partir 1 mole de
triglycéride.
Figure n°2 Réaction de
transestérification
Les taux et type d'acides gras non libres
(triglycérides) présents dans l'huile déterminent les
monoesters produits en fin de réaction (Fernando S., Karra P., Hernandez
R., and Johan S.K., 2007). La plupart des études sur la
transestérification ont été réalisée
à l'aide d'huiles comestibles traditionnelles. La
transestérification de l'huile de soja a été
étudiée au plus, principalement aux Etats-Unis et en
Amérique du sud (Zhou W. and Boocock, 2006) & (Liu X., and X. Piao,
2008). En Asie, au Canada et en Espagne, c'est l'huile de tournesol à
teneur élevée en acide oléique qui est couramment
utilisé dans les études de transestérification (Zhou W.,
and D.G.B. Boocock, 2003)&(Stamenkovic, O. S., and D. U. Skala 2008). Outre
ces huiles, celles du coton, du ricin, du colza, du maïs et de coco ont
été également utilisés lors de plusieurs
études sur la transestérification (Zhou W., and D.G.B. Boocock,
2003., Meneghetti, S., and H. V. Carvalho, 2006., & Kusdiana, D. and S.
Saka, 2001).
D'autres huiles qui proviennent de plantes spécifiques
d'Afrique et d'Asie telles que l'huile de palme, de jatropha, de karanja, etc.
... ont été les sujets de la recherche ces dernières
années (Jitputti, J., B. and P. Jenvanitpanjakul, 2006)&(Encinar
J.M., Gonzalez J.F., and Rodriguez Reinares A., 2007).
I.2.3.2. LA TRANSESTERIFICATION EN CATALYSE HOMOGENE
La production courante industrielle du biocarburant est
effectuée par la transestérification catalyse alcaline
homogène d'huiles végétales avec du méthanol. Les
catalyseurs les plus utilisés pour les études de
transestérification sont les hydroxydes de sodium et de potassium (NaOH
et KOH) et les méthoxydes de sodium, de potassium et l'acide sulfurique
(CH3ONa, CH3OK et H2SO4) (Zhou W.,
S. K. Konar, 2003., Darnoko, D. and M. Cheryan, 2000., Reis, S. C. M. dos, E.
R. Lachter, R.S. V. Nascimento, J. A. Rodrigues Jr., and M. G. Reid, 2005).
I.2.3.3. LA TRANSESTERIFICATION CATALYTIQUE HETEROGENE
Les oxydes des métaux sont les plus testés en
catalyse de conversion des huiles en esters. Les catalyseurs à base
d'alumine arrivent en tête suivi par les oxydes des métaux du
groupe IIA (CaO, Mg0, BaO et Sr0) et oxydes mixtes (CaCeO3, CaMnO3, CaZrO3,
CaO-MgO) et enfin des oxydes de métaux de transition supportés
sur différents supports poreux (alumine, zéolithes, ...). Ces
catalyseurs sont soit acides soit basiques (Noureddini H. and D. Zhu, 1997&
Darnoko, D. and M. Cheryan, 2000).
I.2.3.4. LE RAPPORT ALCOOL/HUILE
La réaction étant dans les deux sens
(transestérification et condensation) ; donc pour déplacer
l'équilibre dans le sens de la formation des esters il faut un
excès de l'un des deux réactifs. La stoechiométrie de la
réaction de transestérification montre que le nombre de moles
d'alcool soit le triple de celui des triglycérides. Donc au minimum il
faut doubler le nombre de moles de l'un des réactifs. Pour
différentes raisons l'alcool est pris en excès ; le rapport
molaire alcool/huile est de 6 au minimum. La littérature montre que ce
rapport est très variable selon la nature de l'huile et du catalyseur
utilisé.
I.2.3.5. LA NATURE ET LA QUALITE DE L'HUILE
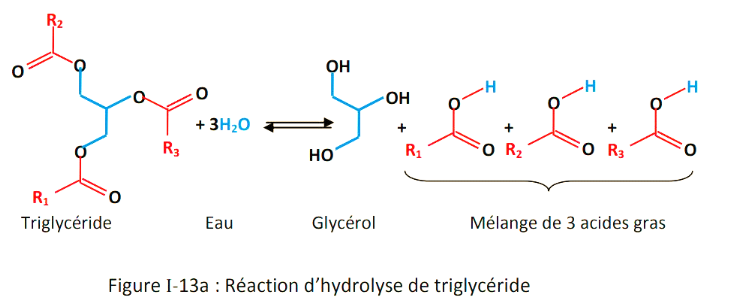
Des réactions secondaires (parasites) peuvent avoir
lieu si l'huile contient de l'eau et d'acides gras libres. Et par suite la
cinétique de transestérification est affectée (Darnoko, D.
and M. Cheryan, 2000). En effet la présence d'eau favorise l'hydrolyse
du triglycéride selon la réaction représentée sur
la figure (Réaction d'hydrolyse de triglycéride).
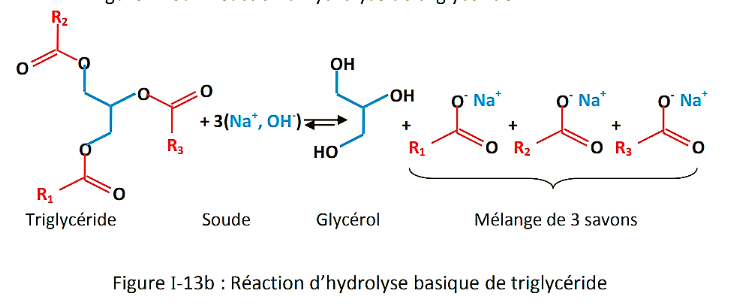
Figure n°3 Rection d'Hydrolyse de
triglycéride et de formation des savons
Cette réaction d'hydrolyse peut être
amorcée en milieu basique et/ou par effet de température. Elle se
déroule en trois étapes, la première donne un acide gras
libre et du diglycérides, après la seconde étape un autre
acide gras et du monoglycéride sont formés enfin après la
troisième étape un dernier acide gras et du glycérol sont
obtenus (Darbha Srinivas & Jitendra K. Satyarthi, 2011).
I.2.3.6. LA NATURE, LA QUANTITE ET LE TYPE DE CATALYSEUR
La transestérification est souvent
réalisée avec un catalyseur. Le catalyseur peut être une
substance chimique (catalyses homogène et
hétérogène) ou une enzyme (catalyse
enzymatique)(Hernandez-Martyn, E. and C. Otero 2008)., Tamalampudi S., M.R.
Talukder, and H. Fukuda, 2008) & (Garcia, E., and J. Aracil, 2001); la
transestérification sans catalyseur a été signalée
dans la littérature. En effet ces études utilisent les
propriétés supercritiques des alcools dans la production de
biodiesel par transestérification : l'alcoolyse supercritique (Demirbas
A., 2007., Kusdiana, D. and S. Saka, 2001)& (Kusdiana, D. and S. Saka,
2001).
I.2.3.7. LE BIODIESEL EST UNE SOURCE D'ENERGIE DE SUBSTITUTION
AU DIESEL
La possibilité d'utiliser des huiles
végétales comme carburant est reconnue depuis le début des
moteurs diesel. L'huile végétale a une viscosité trop
élevée pour être utilisée dans la plupart des
moteurs diesel existants en tant que mazout de remplacement direct. L'une des
méthodes les plus couramment utilisées pour réduire la
viscosité de l'huile dans l'industrie du biodiesel est la
transestérification. C'est la réaction d'un triglycéride
gras ou huileux avec un alcool pour former des esters et du glycérol. Un
catalyseur est généralement utilisé pour améliorer
la vitesse de réaction et le rendement car la réaction est
réversible. L'excès d'alcool est utilisé pour
déplacer l'équilibre du côté du produit. Pour
obtenir un rendement élevé de l'ester, cela signifie que les
alcools doivent être utilisés en excès (Pinto et al. 2005.,
cité par Z. Bettahar, B. Cheknane and K. Boutemak. 2016).
Avec la densité, c'est un paramètre important
pour l'atomisation et la distribution du carburant. La mesure de la
densité est utile pour déterminer la quantité et la
qualité du carburant. La densité du biodiesel est liée
à la teneur en esters méthyliques et à la quantité
de méthanol (Pinto et al. 2005., cité par Z. Bettahar, B.
Cheknane and K. Boutemak. 2016).
Tableau n°5 Propriétés du
carburant du biodiesel et du carburant diesel.
|
Propriétés
|
Diesel dérivé de fossile
|
Biodiesel
|
|
Densité (kg/m3) à 15°C
|
837
|
870
|
|
Pouvoir Calorifique (kJ/kg)
|
3.9
|
5.2
|
|
Viscosité (mm2/s) à 40°C
|
43300
|
39600
|
(Karabektas. M, Ergen. G and Hosoz. M.2008).
Tableau n°6 Comparaison des
propriétés des esters d'huile de palme par rapport aux
propriétés des huiles minérales.
|
Propriétés
|
Ester d'huile de palme
|
Huile minérale
|
|
Densité (g/cc) à 15°C
|
0,86
|
0,88
|
|
Viscosité cinématique, cSt à 40°C
|
5,06
|
8,13
|
|
Point éclair (°C)
|
186
|
152
|
|
Point d'écoulement (°C)
|
-32,5
|
-45
|
|
Valeur de neutralisation (mg de KOH/g)
|
0,005
|
<0,01
|
|
Constante diélectrique
|
2,95
|
2,2
|
|
Résistivité volumique (Ohm.cm-1)
|
7,1
|
7,6
|
|
Tension de claquage (kV)
|
81
|
70 à 75
|
(Norhafiz .A, Jasronita .J, Mohd .Z.A, A. Kadir and Mohd
.N.M.2013)
CHAPITRE II. PARTIE
EXPERIMENTALE
II.1.
MATERIEL ET PRODUCTION
A travers ce chapitre expérimental, nous examinerons
les études physiques et chimiques de l'huile raffiné
importé et l'huile locale ainsi que du BIODIESL Synthétiser. En
définissant des caractérisations et des indices tels que la
densité relative, la viscosité en terme de vitesse et d'indice
d'acide. Nous verrons comment synthétiser à travers les
étapes du Protocol ; en commençant par la réaction de
transestérification, la séparation de phases, jusqu'à la
fin avec l'étape de lavage et séchage ou purification par
distillation. Ensuite, nous ferons à nouveau des tests sur les types de
biodiesels. Les matières premières utilisées pour
réaliser ce travail représentent une huile de marque PALMOLIN et
du type MAWESA. Les différents réactifs utilisés pour nos
expériences sont à 96% du Méthanol.L'hydroxyde de
potassium KOH et 98% de concentration de l'H2SO4.
Tableau n°7 Liste d'équipement
utilisé dans l'expérimentation
|
N°
|
Equipements
|
Description
|
|
01
|
BECHER
|
Le bécher ou le vase de Berlin, un vase à volume
variant en millilitre et possède un bec verseur.
|
|
02
|
ERLENMEYER
|
L'Erlenmeyer ou Erlen est un récipient à corps
resserre avec une capacité variante en millilitre, il ne possède
pas de bec verseur.
|
|
03
|
CYLINDRE GRADUE
|
Le Cylindre gradué ou éprouvette gradué
possède une graduation précise, il est doté d'un bec
verseur et sa contenance est également variable.
|
|
04
|
PIPETTE GRADUE
|
La pipette graduée permet de prélever un volume
variable compris entre 0,1 et 50mL selon sa capacité.
|
|
05
|
BALANCE (PRECISION)
|
Employé pour peser
|
|
07
|
BURETTE
|
Utiliser lors du dosage
|
|
08
|
EPROUVETTE
|
Pour contenir le volume exactes de mesure
|
|
09
|
AMPOUL A DEANTER
|
Intervient dans la séparation des phases
|
|
11
|
RECHAUD
|
Un Dap-gaz et sa marmite nous ont aidé à
apporter les solutions au température souhaitées
|
II.2.
PARAMETRES PHYSIQUES ET CHIMIQUES
II.2.1. INDICE D'ACIDE
C'est le nombre qui exprime en milligrammes la quantité
de potassium hydroxyde nécessaire pour neutraliser les acides gras
libres présents dans 1g de substance. Il mesure l'état de
détérioration d'une huile ou la qualité du raffinage (T.
Kumar, A. Kumar and A. Raheman 2007). Il s'agit également de dissoudre
la matière grasse dans de l'éthanol neutralisé, puis de
titrer l'acide gras libre à l'aide d'une solution étalon de KOH
en présence de phénolphtaléine comme indicateur
(Moussouni. I., 2016).
- Mode de fonctionnement :
Peser 1g d'huile dans un Erlenmeyer de 250ml.
Prenez 10 ml d'éthanol et ajoutez-les dans
l'erlenmeyer, et mélangez bien.
Ajoutez quelques gouttes de phénolphtaléine
à la solution comme indicateur de couleur.
Titrer avec la solution de KOH (0,1 M) jusqu'à
coloration rose
Enregistrez précisément le volume de KOH.
- Méthode de calcul :
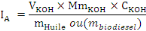
IA : Indice d'acide (%) MmKOH :
56,1g/mole
VKOH : Volume de solution KOHCKOH :
Concentration de la solution KOH (0,1M)
II.2.3. MESURE DE VISCOSITE
La viscosité est la caractéristique la plus
importante d'un fluide. Elle est définie comme le rapport de la force de
cisaillement et de l'épaisseur de l'huile. Dans cette expérience,
nous allons étudier comment la vitesse d'une sphère tombant
à travers un liquide visqueux dépend de la taille de la
sphère et mesurer la viscosité des huiles et du biodiesel
à température ambiante (J.R.W Van et al. 1963). La
viscosité est définie comme la résistance à
l'écoulement uniforme sans turbulence dans la masse d'un
matériau. Nous allons maintenant déterminer la viscosité
de notre biodiesel formé ainsi que celle du pétrole. Pour cela,
il faut déterminer la vitesse de chute d'une goutte de permanganate de
potassium dans l'huile puis dans le biodiesel. On peut en déduire la
viscosité (C. Ehren and J. Bucholtz 2007).
- Mode de fonctionnement :
Remplir un cylindre gradué autant que possible avec de
l'huile.
A l'aide d'un compte-gouttes, une goutte de permanganate de
potassium dans l'huile puis dans le biodiesel.
Nous démarrons le chronomètre lorsque la goutte
est tombée dans l'huile. Ensuite, nous l'arrêtons lorsque la
goutte atteint la graduation finale.
Notez le temps qu'il a fallu à la goutte pour parcourir
cette distance (Ät).
On mesure la distance (d) en mètre parcourue par la
goutte avec une règle sur la burette.
On calcule la vitesse de la chute en (m.s-1).
II.2.4. CALCUL DE LA DENSITE
La densité est une grandeur dimensionnelle
définie comme le rapport de la masse d'un volume d'huile (ou de
biodiesel) à cette masse du même volume d'eau à
4°C.
Nous avons pesé 10ml de notre huile (ou biodiesel) et
nous avons calculé la densité : d = m/V, avec m : la masse de
l'huile et V =10ml.
Ensuite pour calculer la densité. On a donc : d = d
(biodiesel/huiles) / d (eau), Avec densité d'eau = 1000g/L


Figure n°4Mesure de la densité de
biodiesel
- Mode Opératoire
Matériels : Eprouvette
gradué à 1000mL, Thermodensimètre et l'entonnoir.
Remplir notre éprouvette gradué jusqu'à
1000mL de l'échantillon
Plonger le thermodensimètre correspondant pour le
diesel la graduation varie (0,8100-0,8900)
Lisez la densité et la température et notez les
résultats qu'il faut comparer dans un tableau de correction ou
introduire les données dans un logiciel de correction.
II.2.5. LA DISTILLATION
La distillation étant une pratique physico-chimique de
séparations des constituants volatils d'un mélange et les obtenir
pratiquement à l'Etat pure. Pour les hydrocarbures l'OCC adopte ce
paramètre pour vérifier l'état de volatilité d'un
produit pétrolier finis et non brut.

Ballon conténant la solution attacher au thermomètre au
dessus
Distillat
Reglage
de la plaque chauffante
Figure n°5 Mécanisme de distillation
et calcul de condensat
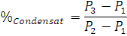
Avec : P1 : poids du vide,
P2 :poids de solution + contenu, P3 : Poids de
condasat lourd.
- Mode Opératoire
Matériels :
Ballon jaugé, distillateur, Balance à précision
et thermomètre.
Pesez le poids vide du ballon jaugé
Prélever 100mL de l'échantillon fini (biodiesel)
puis verser dans le ballon jaugé et pesez encore
Installer le thermomètre et le ballon jaugé
contenant l'échantillon prêt des plaques chauffantes dans le
distillateur afin allumer l'appareil et surveillez l'opération.
II.2.6 COULEUR

Selon l'origine des hydrocarbures, leurs compositions ils sont
différents en terme des certains paramètres physiques,
premièrement la couleur.
Echantillon + Solution de Reference
Ecran de lecture
Figure n°6
Mécanisme de prise et calcul de
couleur
- Mode de Fonctionnement
Matériels : Disposez de 2 tubes
à essais, un échantillon de référence et un
comparateur des couleurs.
Remplissez nos deux tubes l'échantillon jusqu'à
leurs ¾ du volume
Prépararer l'échantillon de
référence
Posez avec soins et propreté les trois
échantillons dans le comparateur
Fermer et allumer le comparateur
Lisez et notez les résultats.
II.2.7 INDICE
D'INFLAMABILITE
Le point d'inflammabilité est une opération de
vérification si le produit peut s'enflammer à de basse
température généralement autours de 40°C à
150°C et pour vérifier aussi le degré de volatilité
du produit. Ce une technique est une simulation d'un moteur à combustion
ou (Flash point). Nos échantillons ont tous atteint le point
d'inflammabilité autours de 82°C.
FLAMME

Figure n°7 Mangement de l'indice
d'atomisation (flash point).
- Mode de Fonctionnement
Matériels : Disposez de votre
hydrocarbure dans notre travail c'est le biodiesel, un flash point une
allumette, une source de gaz (Dap-Gaz).
Remplissez la marmite de l'échantillon jusqu'au train
d'indication
Prépararer le gaz et vérifier les pompes
d'injections
Allumer le flash point et homogénéisez
l'échantillon jusqu'à la température de
détonation
Faite entrée l'air et le feu et apprécier
l'inflammabilité du produit.
II. 3. PROTOCOLE DE
SYNTHESE DU BIODIESEL
II.3.1. PRESENTATION DE NOS HUILES
Nous utilisons des huiles de marque PALMOLIN et MAWESA. Ces
huiles sont constituées d'acides gras: Acides linoléiques, acides
oléiques, acides palmitiques, acide stéarique et acide
linoléique. Ces huiles totalement végétales interviennent
dans la cuisson des aliments, la pâtisserie à des
températures ne dépassant pas 330°C par contre l'acide gras
est dénaturé.
Les caractéristiques de l'huile marque « PALMOLIN
» telles que nous les avons dans le tableau (n°8) pour 100g d'huile
Palmolin(
http://www.cevital-agro-industrie.com/en/produit
grand-public/huile-palmolin-p2 ). La composition chimique (MAWESA) ne
pas bien connu.
Tableau n°8 Caractéristiques de
l'huile de marque « Palmolin »
|
Caractéristiques
|
|
|
Énergie
|
900KCAL/3700KJ
|
|
Lipides 100g
|
Acides gras saturés 15g
|
|
Acides gras mono insaturés 25g
|
|
Acides gras polyinsaturés 60g
|
|
Cholestérol
|
Aucun
|
|
Glucide
|
0g
|
|
Protéine
|
0g
|
|
Vitamine E
|
100mg (833%AJR)
|
II.3.2. FORMULE BRUTE DU TRIGLYCERIDE CORRESPONDANT
(PALMOLIN)
- Acide Palmitique :
CH3(CH2)14COOH = 256g-mol-1
- Acide Oléique :
CH3(CH2)7CH=CH(CH2)7COOH=
282g-mol-1
- Acide stéarique :
CH3(CH2)18COOH= 312g-mol-1
- Acide linoléique :
CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH=
280g-mol-1, nous aurons la masse d'huile suivante :
Mm =1 ×(256 +282+312+ 280)
Mm =1130g-mol-1
II.3.3. MASSES DE REACTIFS CHIMIQUES POUR LA SYNTHESE DE
BIODIESEL
Les biodiesels ou esters méthyliques sont obtenus par
la réaction de transestérification de triglycérides avec
du méthanol. On a une mole de triglycéride et trois moles de
méthanol puis on va produire trois mole de mélange d'esters gras
et une mole de glycérine (
https://www.e-education.psu.edu/egee439/node/684):
- Quantités de réactifs
utilisées :
On prend le ratio (1:10) pour de bonnes performances : donc
:
n(méthanol)= rapport x n(huile) = 10 x n(huile)
Avec n(huile)= 250/1130=0,221
D'où n(Méthanol)= 10 × 0,221 mole = 2,21
mole
On sait que la masse molaire du méthanol est de 32,04
g/mole. Alors, on devrait dire :
m (méthanol) = M (méthanol) × n
(méthanol)
m (méthanol) = 32,04 g/mole × 2,21 mole = 71g
Aussi, nous considérerons de la quantité de
catalyseur KOH : Nous avons KOH 1% masse d'huile alors :
m (catalyseur)= 2.5g
D'où : (Echantillonnage en fonction de KOH :
250g d'huiles 2,5g d'hydroxyde de potassium et 71g de méthanol) et
(Echantillonnage en fonction de l'H2SO4 : 250mL
d'huiles 2,5mL de l'acide sulfurique et 217 mL de méthanol).

Figure n°8 Exemple de prise de poids de
catalyseur (Hydroxyde de potassium)
II.3.4. SYNTHESE DU BIODIESEL
La synthèse du biodiesel passe avec les étapes
successives de production qui sont ;
II.3.4.1. REACTION DE SYNTHESE
La transestérification est l'une des méthodes
les plus importantes utilisées pour transformer les huiles
végétales en carburant diesel. C'est un procédé
dans lequel des huiles végétales, des graisses animales ou des
huiles à base de micro-algues. Ils sont mélangés à
un alcool éthanol ou méthanol en présence d'un catalyseur
(Pinto et al. 2005). Nous utilisons un catalyseur pour améliorer la
vitesse de réaction et le rendement. Le but de cette réaction est
d'abaisser la viscosité de l'huile et la densité de l'huile pour
faciliter sa combustion (Demirbas 2003).
H2SO4
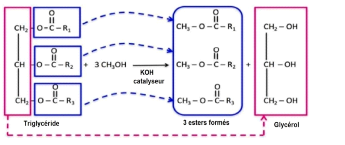
Figure n°9 Réaction de
transestérification catalytique de l'huile de palme
- Mode de fonctionnement :
a) Dissoudre le catalyseur dans le méthanol, ce qui
nécessite d'agiter le mélange et de chauffer très
légèrement
b) Verser la solution obtenue dans l'huile et agiter
vigoureusement en chauffant légèrement le milieu
réactionnel entre 40 et 55°C. Tous les tests ont été
réalisés avec un réchaud de DAP-GAZ.
La configuration de la réaction était
très simple. Il s'agit d'une fiole de 500mL, l'agitation est
assurée mécaniquement à l'aide d'un bâton de verre.
II.3.4.2. DECANTATION ET SEPARATION DES PHASES
Après 120 minutes d'agitation, laisser reposer le
mélange pour que la séparation ait lieu. Il faut savoir que la
décantation est très longue il faut attendre au moins une
demi-journée ou 24h. Le succès d'une réaction de
transestérification est matérialisé par la présence
de deux phases (ester et glycérol). Le glycérol a une
densité plus élevée que l'ester. Il est situé au
fond de l'ampoule et décanté après 24h de
décantation.

Figure n°10 Appréciation de la
séparation des phases (liquide-liquide) non
miscible
II.3.4.3 ETAPE DE LAVAGE (RINÇAGE)
Le biodiesel obtenu doit être lavé pour
éliminer l'excès d'alcool et de catalyseur. Placer le biodiesel
dans une ampoule à décanter et verser lentement l'eau pour le
rinçage. Cette opération est délicate ; elle doit
être réalisée très doucement avec le moins
d'agitation possible car l'agitation provoque la formation d'une
émulsion, ce qui diminue le rendement de la synthèse. Laisser
reposer environ 24 heures puis récupérer le biodiesel.

Figure n°11 Appréciation de la
séparation des phases (liquide-liquide) non miscible après lavage
à l'eau distillé
II.3.4.4. ÉTAPE DE DISTILLATION

La distillation est l'étape finale permettant
d'éliminer l'excès d'eau et de méthanol du biodiesel. La
distillation est l'une des méthodes de séparation chimique les
plus anciennes et les plus courantes. Historiquement l'une des applications les
plus connues. C'est le processus de chauffage d'une solution liquide ou d'un
mélange liquide-vapeur pour en tirer une vapeur. Le but est typiquement
l'élimination d'un composant léger d'un mélange de
composants lourds, ou l'inverse de la séparation d'un produit lourd d'un
mélange de composants légers. À la fin de tout ce
processus, nous obtiendrons différents biodiesels.
Figure n°12 Appréciation de la
séparation des Distillat d'EMAG à 362°C
II.3.4.5. CARACTERISTIQUES DU BIODIESEL
Comme nous l'avons vu au début de ce chapitre, à
propos de la détermination de certaines caractéristiques des
huiles par des indices tels que l'indice d'acide, la mesure de la
viscosité et la densité relative. Nous ferons la même
détermination pour le biodiesel.
II.3.5. TESTS DU BIODIESEL
II.3.5.1 TEST DE MISCIBILITE
Pour vérifier la miscibilité entre notre
biodiesel et le fioul, nous suivrons le protocole suivant ; dans une
éprouvette graduée de 25 ml, nous allons verser 10 ml de notre
biodiesel préalablement synthétisé ainsi que 10 ml mazout.
Après agitation et décantation, il y aura trois cas possibles
- Cas n°1 : Si deux phases distinctes sont visibles et
ont le même volume, alors les deux liquides sont non miscibles.
- Cas n°2 : Si deux phases distinctes sont visibles mais
que leurs volumes sont différents, cela indique que les deux liquides
sont partiellement miscibles entre eux. On peut alors définir une
certaine solubilité.
(
http://solutionbiodiesel.blogspot.com/p/comment-ca-marche.html
)
- Cas n°3 : Si une seule phase homogène est
visible, alors les deux liquides sont miscibles. Pour ces proportions, s'ils
sont miscibles quelles que soient les proportions. On peut dire qu'ils sont
miscibles en toutes proportions
II.3.5.2 TEST DE DENSITE
La densité n'a pas d'unité, pour les produits
pétrolier et les hydrocarbure en générale elle est
exprimée en g.ml-1 où Kg.L-1, pour les
hydrocarbures ce test est réalisé grâce à un
thermodensimètre et les résultats sont corrigés, d'abord
on converti les g.ml-1 en Kg.L-1 afin pour un produit
fini on utilise la table 53B de correction.
II.3.5.2 ESSAI
D'INFLAMMABILITE
Au cours du processus de combustion, les gaz produits
réagissent avec l'oxygène de l'air. La réaction produit
suffisamment de chaleur pour former une flamme, qui traverse le mélange
constitué de gaz émanant du produit et de l'air. Lorsque le gaz
au-dessus du liquide s'enflamme, la chaleur produite est
généralement suffisante pour évaporer suffisamment de gaz
supplémentaire pour entretenir la flamme et on dira qu'il s'agit de
liquide enflammé. En fait, c'est le gaz qui brûle et qui est
continuellement renouvelé par le liquide (Méthode ASTM D6664,
Spécification de B 100).
II.3.5.3 RENDEMENT DE LA SYNTHESE
Selon HUAYANG et.al (HUAYANG HE, SHIYAO SUN, TAO WANG, SHENLIN
ZHU, 2006) et d'autres articles, le rendement de la réaction se calcule
par la formule suivante :
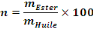
Après lavage de la synthèse, l'huile de palme
raffiné (PALMOLIN) a donné un meilleur rendement avec 212.5 g
d'EMAG soit 85% de biodiesel dans 250g de l'huile, tandis que l'huile de Palme
locale MAWESA a présenté un rendement de 157g d'EMAG à
62,9% de biodiesel pour 250g de l'huile.
CHAPITRE III. RESULTATS ET DISCUSSIONS
Dans cette partie, on va représenter et traiter
certains excipients par la méthode quantitative d'analyse de l'huile de
palme PALMOLIN, MAWESA et de DIESEL
FOSSILEpour confirmer certains résultats, ainsi pour faire une
comparaison avec nos résultats obtenus par la synthèse du
BIODIESEL.
III.1. RESULTATS
III.1.1. DIFFERENTS TYPES D'HUILES COMMERCIALISEES EN VILLE DE
GOMA
En effet, Il existe différentes marques d'huiles
végétales alimentaires sur le marché à Goma. Ils
sont fabriqués localement autour du chef de la province du Nord-Kivu
comme (MAWESA) ou importés (les huiles raffinés, PALMOLIN, ...).
Les huiles végétales sont destinées
à la cuisson des aliments. L'huile de palmeMAWESA et PALMOLIN cette
année ont étés les plus répandues sur le
marché de Goma et ses environs cette année 2020-2021. A noter que
les unités de raffinage d'huiles végétales les plus
importantes sont indonésiennes quelques très peu sont africaines.
Par conséquent, nous avons une composition en pourcentage d'acides gras
de l'huile PALMOLIN.
Tableau n°9 Composition en pourcentage
d'acides gras de l'huile PALMOLIN.
|
C(16 :0)
|
C(16 :1)
|
C(14 :0)
|
18 :0
|
18 :1
|
18 :2
|
18 :3
|
|
51%
|
Oligo-élément
|
2%
|
6%
|
30.4%
|
11.6%
|
<0,5 %
|
C (16 : O) Constitut plus de 50% de composition chimique
de l'huile PALMOLIN.
III.2. ETUDE PHYSICO-CHIMIQUE DU
BIODIESEL
III.2.1. BIODIESEL, LES ENJEUX DE LA REACTION DE
TRANSESTERIFICATION
Dans le processus de transestérification,
différents chercheurs ont rapporté des temps de réaction
différents. Cependant, la réaction peut être lente au
début de l'expérience en raison de la dispersion entre l'huile et
l'alcool, qui est favorisée par l'agitation. Un temps de réaction
excessif conduit probablement à une réduction du rendement de
conversion en raison des conditions de température, ce qui
entraîne finalement la formation de savons plus d'acides gras,
entraînant une perte d'esters (Ganaprakasam A, Sivakumar V M, Surendhar
A, Thirumarimurugan M and Kannadasan T., 2013).
III.1.2. CARACTERISATION PHYSICO-CHIMIQUE PAR INDICES
POUR LES TYPES DE BIODIESEL
Après avoir complètement terminé la
réaction de transestérification, en mélangeant avec une
grande quantité de méthanol et de catalyseur KOH. Nous obtenons
des types de biodiesel et les soumettons à plusieurs expériences
afin que nous puissions déterminer les paramètres
physico-chimiques de volatilité.
Tableau n°9 Caractérisation
physico-chimique par paramètre de
Volatilité.
|
PARAMETRES
DE VOLATILITE
|
TYPE MAWESA
|
MARQUE PALMOLIN
|
BIO1
|
BIO2
|
BIO3
|
BIO4
|
|
Indice d'acide A (%)
|
0.168
|
0.561
|
1,065
|
1,165
|
1,243
|
1,374
|
|
Densité (g.mL-1)
|
0,928
|
0,912
|
0,853
|
0,865
|
0,893
|
0,840
|
|
Viscosité[m/s].10-3 (%)
|
5.300
|
8.605
|
10.450
|
11.400
|
11.900
|
12.001
|
|
Distillation (%)
|
-
|
-
|
1,152
|
1,110
|
1,281
|
1,519
|
|
Couleur
|
-
|
-
|
5.0-5.5
|
5.0-5.5
|
5.0-5.0
|
5.5-5.5
|
|
Point d'inflammabilité (°C)
|
-
|
-
|
82
|
81,9
|
82,1
|
82,1
|
D'après le tableau (IV.7) ci-dessus, nous pouvons voir
que l'indice d'acide augmente de 0,168% avec l'huile type MAWESA ; 0,561%
marque PALMOLINet duBIO11,122% du type MAWESA et augmente à
1, 374 % avec le BIO4 de l'huile marque PALMOLIN.
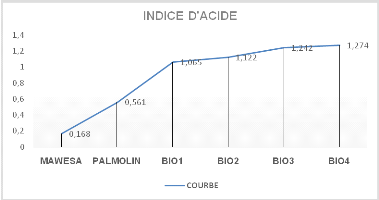
Figure n°13 Evolution dela courbe d'indice
d'acide
La part croissante est due au fait que les
triglycérides sont encore majoritaires dans l'huile non
transformé en acide gras libre compte tenu de la température dans
le processus de transestérification (40C°- 60C°) avec les
huiles types PALMOLIN et MAWESA. Cependant, une partie décroissante
prouve que les acides gras libres dans les synthèses BIO1,
BIO2, BIO3 et BIO4 se sont transformés
en esters méthylique par le processus de transestérification.
Pour la densité, on remarque qu'elle passe après
correction dans le tableau B50 de produit finis, nos résultats varient
de 0,853 à 0,891. Car cette densité est une
caractéristique importante, principalement pour le biodiesel, car elle
conditionne le dimensionnement et les particularités technologiques des
organes d'alimentation moteur (pompes, injecteurs). Toute en signalant que
l'huile de palme MAWESA et PALMOLIN sont léger par rapport à
l'eau à 4°C.
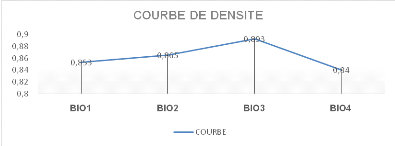
Figure n°14 Evolution de la courbe de
densité
La viscosité étant très importante aussi
dans la filière biodiesel, car elle affecte le fonctionnement des
équipements d'injection de carburant. Il est bien connu que les huiles
végétales ont la viscosité la plus faible en termes de
vitesse, ce qui signifie qu'elles sont très visqueuses. Et le but de la
réaction de transestérification est aussi de réduire la
viscosité élevée des huiles. Cette viscosité en
terme de vitesse augmente de (5, 300 x 10-3m/s) avec du biodiesel de
nouvelle huile à (12,001 x 10-3m/s) en raison de la
réduction de la viscosité élevée. Moins visqueux
signifie moins de difficulté pour le moteur à injection et des
caractéristiques de volatilité plus élevées des
biodiesels pour mieux remplacer les carburants diesel.
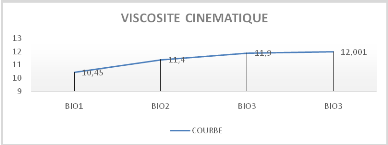
Figure n°15 Evolution de la courbe de
viscosité cinématique
La Distillationest typiquement l'élimination d'un
composant léger d'un mélange de composants lourds, ou l'inverse
de la séparation d'un produit lourd d'un mélange de composants
légers. À la fin de tout ce processus, nous obtiendrons
différents poids en pourcentage des résidus lourds qui
renseignent sur la volatilité du produit qui varient entre 1,152% et
1,5199% de condensat lourd. Nos résultats étant proche de celle
de diesel qui enregistre des résidus < 2%.
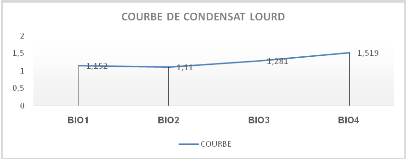
Figure n°16 Appréciation de
formation de condensat après distillation
La couleur est aussi l'un de paramètre physico-chimique
pour les produits pétroliers finis et comme dans notre cas de biodiesel
nous le déterminons par le comparateur de couleur avec de valeurs
Variant entre (5.0-5.5) à (5.5-5.5) de nos résultats.
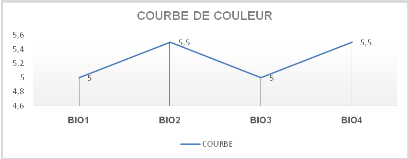
Figure n°17 Appréciation de la
couleur du biodiesel
III.1.2. COMPARAISON AVEC LES
ANALYSES RECENTES DES CARACTERISTIQUES PHYSICO-CHIMIQUES DU BIODIESEL
Jun Cong Ge et al ont compris que la densité et la
viscosité du carburant biodiesel sont des facteurs importants dans le
fonctionnement du moteur. La densité affectera directement le
mélange de biodiesel et diesel, et une densité excessivement
élevée conduira à la stratification des huiles
mélangées. En outre, ils ont signalé que la
viscosité est un facteur important qui affecte directement les
performances de combustion et les caractéristiques d'échappement
d'un moteur. Une viscosité élevée détériore
l'efficacité d'atomisation, prolonge le temps d'allumage, réduit
la pression d'injection et empêche la combustion complète du
carburant. Ils ont étudié une variété de carburants
mélangés au biodiesel (mélange de diesel avec des huiles
de tournesol, de coton, de soja, de maïs et d'huile de palme
usagée) et ont également découvert que les
viscosités des carburants mélangés à 20 % sont
très proches de celles du carburant diesel pur (Jun Cong G, S K Yoon and
N J Choi., 2017)
Ypatia Zannikou et al, ils ont étudié quatre
types d'esters éthyliques et méthylique en fonction de leurs
propriétés physico-chimiques. Ensuite d'étudier si leurs
paramètres de qualité se situent bien dans la norme
européenne EN. Les résultats de l'analyse sont donnés dans
le tableau (IV.8). On constate que trois types d'esters éthyliques sur
quatre satisfont à la norme européenne de viscosité.
L'ester qui était différent des trois autres étaient
l'ester éthylique de friture utilisé, qui semblait être
au-dessus de la limite la plus élevée (5cSt) de la
spécification européenne. D'autre part, chaque type d'ester
éthylique avait une densité comprise entre 860 et 900 kg/m3 (G.
Anastopoulos, Y. Zannikou 1, S. Stournas and Stamatis Kalligeros., 2009).
Tableau n°10 Propriétés des
esters éthyliques d'acides gras
|
PROPRIETES
|
Huile de Sunflower
|
Huile de Rapeseed
|
Huile d'Olive
|
Huile de friture
|
EN 14214 limites
|
|
Densité (Kg/m3)
|
882,7
|
881,2
|
882,7
|
881,2
|
860-900
|
|
Viscosité cinématique (mm2.s-1)
|
4,63
|
4,84
|
4
|
5,81
|
3,50-5,0
|
|
Indice d'acide (mgKOH/g)
|
0.15
|
0.35
|
0.19
|
0.46
|
0.5 max
|
Sivaramakrishnan et Ravikumar dans leur rapport pour la
détermination de l'indice de cétane du biodiesel et ses
influences sur les propriétés physiques. Ils ont souligné
l'importance de la mesure de la densité relative et de la
viscosité pour le fonctionnement des usines de biodiesels et des
moteurs. Ainsi, ils ont signalé que la densité relative est une
propriété importante du biocarburant. La densité est la
masse par unité de volume de tout liquide à une
température donnée. La viscosité est une mesure de la
friction interne du fluide ou de la résistance de l'huile à
s'écouler, qui tend à s'opposer à tout changement
dynamique dans le mouvement du fluide. Ils ont découvert que la
température de la réaction de transestérification augmente
la viscosité des biodiesels diminue et qu'il est donc capable de
s'écouler plus facilement. Plus la viscosité des biodiesels est
faible, plus il est facile de pomper, d'atomiser et d'obtenir des gouttelettes
plus fines. Particulièrement à basse température lorsque
l'augmentation de la viscosité affecte la fluidité du carburant.
Une viscosité élevée entraîne une moins bonne
atomisation du jet de carburant et un fonctionnement moins précis des
injecteurs de carburant. (K. Sivaramakrishnan and P.
Ravikumar.102).
III.2. DISCUSSIONS
III.2.1. COMPARAISON ENTRE LES
TYPES D'HUILES ET LES BIODIESELS
III.2.1.A INDICE D'ACIDE
La figure (IV.10) montre clairement que l'indice
d'acidité est en augmentation pour les huiles mais presque stable pour
les biodiesels, ce qui donne l'impression que le biodiesel est différent
de celui de l'huile utilisée. Parce que les huiles après le
processus de friture, elles contiennent des triglycérides qui se sont
brisés en acides gras libres en plus grande quantité. Cependant,
grâce à la réaction de transestérification, ces
acides gras libres mélangés au méthanol se transforment en
esters (biodiesels) et la quantité d'acides gras libres diminue
progressivement.
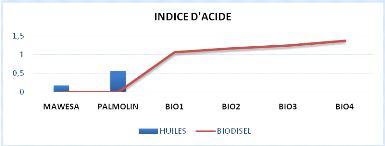
Figure n°18Evolution de l'indice
d'acidité des huiles et biodiesels
III.2.1.BINDICE DE DENSITE
Les valeurs de densité des huiles de friture sont plus
élevées que celles des types de biodiesel qui y sont
dérivés. En raison de cette densité qui est un
paramètre important pourl'atomisation dans le moteur.
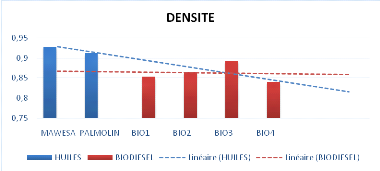
Figure n°19 Evolution de l'indice de
densité des huiles et biodiesels
III.2.1.CINDICE DE VISCOSITE
La figure (IV.12) montre clairement que les viscosités
en terme de vitesse des huiles sont stables avec l'augmentation de la
température, mais avec l'augmentation pour les biodiesels. En raison du
but de la réaction de transestérification pour réduire la
viscosité élevée des huiles. Plus la viscosité d'un
liquide est élevée, plus sa susceptibilité à
s'écouler est faible. Plus la viscosité est faible, plus grande
est la fluidité de ce liquide qui lui convient comme
caractéristiques des carburants. Comme nous l'avons dit dans des
résultats récents, moins visqueux signifie moins de
difficulté pour le moteur à injection et des
caractéristiques de volatilité plus élevées des
biodiesels pour mieux remplacer le diesel.
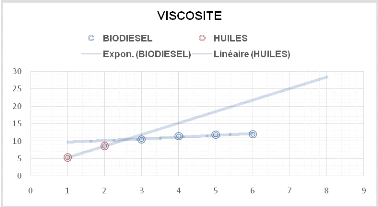
Figure n°20Evolution de la viscosité
en terme de vitesse des huiles et biodiesels
III.1.2OPINIONS ET RECHERCHES
SUR LE BIODIESEL EN RD CONGO
La République Démocratique du Congo est
située dans une zone stratégique pour sa capacité à
réduire le dioxyde de carbone avec le bassin du Congo.Vulnérable
à la déforestation dont les populations environnantes en
dépendent. Aujourd'hui, consciente de l'intérêt croissant
pour les énergies renouvelables et de leurs enjeux, La RD Congo a
intégré le développement de ce type d'énergie dans
sa politique énergétique. L'adoption d'un cadre juridique
favorable au développement de ces énergies, la planification de
projets en est la parfaite illustration malgré le développement
de la bioénergie encore à une échelle expérimentale
dans les laboratoires de recherche. Concernant les cultures
énergétiques, matières premières pour la production
de biocarburants, dans le cas de la RD Congo, il est possible de faire recours
à des sources comestibles pour cette tâche vu les statistiques de
production artisanale grandissante et quelques variétés de
palmier non comestible avec des vielles plantation non exploité au
maximum comme dans les années 50. (INFOCOMM, 2016)
« La RDC est un pays situé dans une zone tropicale
et équatoriale, vulnérable quand même aux effets
néfastes du changement climatique, même s'il ne fait pas partie du
Top 50 des pays pollueurs. L'utilisation de biocarburants peut
représenter une alternative intéressante et un moyen de
contribuer à réduire l'effet de serre. Il n'est pourtant pas
question d'utiliser des produits alimentaires comme l'arachide ou le maïs
pour les produire, l'alternative des déchets et des cultures non
destinées à l'alimentation comme certaine variété
de palmier à huile s'avère intéressante ».
CONCLUSION GÉNÉRALITÉS
Les bioénergieset particulièrement le biodiesel
est la meilleure alternative au carburantdérivé de pétrole
comme le diesel par exemple. La machine diesel joue un rôle important
dans l'économie des pays développés et en voie de
développement à travers le secteur agricole, de transport et de
l'environnement, il y a présence des quantités importantes des
produits de première nécessités pour l'alimentation et le
bien-être des populations mais avec un seul inconvénient la chaine
diesel n'est pas renouvelable et empoisonne l'environnement qui pourrait avoir
des graves répercussions sur le bien-être des vies qui en
dépendent.
Ces biocarburants sont principalement issus de la
matière première biosourcées donc renouvelable. Les
produits riches en sucre pour produire du bioéthanol et les produits
gras pour le biodiesel. Il y a de nombreux avantages comme une
biodégradabilité élevée, une réduction des
émissions de gaz à effet de serre et est obtenu à partir
de sources renouvelables comme les huiles végétales, les graisses
animales et les déchets organiques.
L'étude a montré que le biodiesel est une
alternative renouvelable au carburant diesel avec des propriétés
physiques rapprochés. Le biodiesel est synthétisé par
transestérification, qui est la technique la plus utilisée pour
la synthèse du biodiesel. Ce procédé est largement
utilisé pour réduire la viscosité des triglycérides
pour devenir un bon combustible pour le moteur. Comme nous l'avons
déjà dit, moins visqueux signifie moins de difficulté pour
le moteur à injection et des caractéristiques de
volatilité plus élevées des biodiesels pour mieux
remplacer les carburants diesel. La recherche prouve avec des résultats
que le biodiesel est très similaire au diesel ; la densité
relative et de la viscosité, l'indice d'inflammabilité,
l'acidité total et la couleur.
Ainsi, les huiles végétales utilisées
comme matières premières peuvent être obtenues à
partir de différentes cultures oléagineuses pouvant être
cultivées avec des gros avantagesde produire une variété
non comestible. Les biocarburants représentent une source
d'énergie écologique et remplaçable, contrairement aux
carburants à base des produits pétroliers qui ne le sont pas.
C'est pourquoi les pays en voie de développementet le
monde entier fontà ces jours des lois de recherche pour cultiver ces
plantes de manière intensive et aussi pour réduire la
dépendance énergétique de produitpétrolier pour
fabriquer leur propre pouvoir de production du biodiesel et de distillat
d'huiles végétales pour l'alimentation.Aussi pour soutenir les
machines agricoles et l'aménagement du territoire, en cultivant sans
polluer et à de coûts de carburant très bas, les
productions des vivres de premières nécessités vont
constituerdes richessespour les pays agriculteurs source même de la
création d'emplois. La production de biodiesel va contribuer à
réduire l'émissions de CO2 dans l'atmosphère
responsable de réchauffement climatique, avec le biodiesel contrairement
au carburants fossiles les quantités de dioxydes émises sont
égales aux quantités de dioxydes fixés par les
végétaux.
C'est pourquoi le gouvernement congolaisà travers le
ministère de l'ESU, de l'agriculture et de l'industrie comme
recommandation devront envisager cette solution, du fait que le sous-sol
présente un bilan stagnant depuis les indépendances
jusqu'aujourd'hui, la population congolaise souffre toujours de la
pauvreté, une pauvretémaccabre. La meilleure piste pour aider la
population congolaise à combattre cette pauvreté, cette vie
misérable est de l'outiller dans son activité principale
l'agriculture, une campagne agricole intensive par ce que tous les autres
domaines de développement en dépendant.
REFERENCIEMENTS
BIBLIOGRAPHIE
Altin R. C., Etinkaya S., and Yücesu H.S., (2001),
«The potential of using vegetable oil fuel for diesel engines».
Energy Conversion and Management, 42, pp. 529-538.
B. Kaltwasser, (1980), «biogas» wesbaden FRG,
pp. 35-36
BALLERINI. D et ALAZARD-TOUX. N, 2006 les Biocarburants,
Etats de lieux, Perspectives et enjeux du développement. Institut
Français du Pétrole (IFP). France. Technip, 348p.
C. Ehren and J. Bucholtz, (2007). Biodiesel Synthesis and
Evaluation an Organic Chemistry Experiment Chem.
C. Ehren and J. Bucholtz, Biodiesel Synthesis and
Evaluation an Organic Chemistry Experiment Chem. (2007).
Conceicao M.M., Candeia R.A., Silva F.C., Bezerra,A.F., Jr.,
Fernandes V.J., and Souza A.G., (2007), «Thermoanalytical
characterization of castor oil biodiesel». Renewable and Sustainable
Energy Reviews, 11, pp. 964-975.
Darbha Srinivas and Jitendra K. Satyarthi, (2011),
«Biodiesel Production from Vegetable Oils and Animal Fat over Solid
Acid Double-Metal Cyanide Catalysts «. Catal. Surv. Asia, 15, pp. 145 -
160
Darnoko, D. and M. Cheryan, (2000), «Kinetics of palm
oil transesterification in a batch reactor». J. Am. Oil Chem. Soc., 77,
pp. 1263 - 1267.
David Soissons citer par Nathan 2000, 1re
générale - enseignement de spécialité :
Constitution et transformation de la matière, Dossier 2
Efficacité énergétique des combustibles.
Demirbas. (2003) Biodiesel from triglycerides via
transesterification.
Encinar J.M., Gonzalez J.F., and Rodriguez Reinares A.,
(2007),»Ethanolysis of used frying oil. Biodiesel preparation and
characterization». Fuel Processing Technology, 88, pp. 513 - 522.
F. Maramba, (1978), «Biogaz and waste -The Phillipine
experience», MetroManila, p. 43
F. Maramba, (1978), «Biogaz and waste -The Phillipine
experience», MetroManila, p. 43
Fernando S., Karra P., Hernandez R., and Johan S.K., (2007),
«Effect of incompletely converted soybean oil on biodiesel
quality». Energy, 32, pp. 844-851.
G. Pahl, (2008), «Biodiesel : growing a new energy
economy», Chelsea Green Publishing
Garcia, E., F. Ferrari, T. Garcia, M. Martinez, and J. Aracil,
(2001), «Optimization of the enzymatic esterification of diglycerol
and lauric acid». J. Surfac. Detergents, 4, pp. 257-262.
Hernandez-Martyn, E. and C. Otero (2008) «Different
enzyme requirements for the synthesis of biodiesel: Novozym 435 and Lipozyme_TL
IM». Bioresour. Technol., 99, pp. 277- 286.
HUAYANG HE, SHIYAO SUN, TAO WANG, SHENLIN ZHU, 2007
Transesterification kinetics of soybean oil for production of biodiesel in
supercrital methanol. J Amer Oil Chem Soc
IEA (2020),«Bioenergy - A sustainable reliable energy
source», World Energy Outlook »
J. Barrault, S. Bancquart, Y. Pouilloux , (2004), «
Selective glycerol transesterification over mesoporous basic catalysts«
Comptes Rendus Chimie, vol.7, (6 - 7), 593 - 599.
J. C. Verchin, (2004), «Dossier biogaz »,
Supplément Energie plus n°322 mars
J.R.W Van et al. (1963). Viscosity and Flow Measurement.
Pages: 272-275. Interscience.
J.R.W Van et al. Viscosity and Flow Measurement. Pages:
272-275. Interscience. (1963).
Jitputti, J., B. Kitiyanan, P. Rangsunvigit, K. Bunyakiat, L.
Attanatho, and P. Jenvanitpanjakul, (2006), «Transesterification of
crude palm kernel oil and crude coconut oil by different solid catalysts».
Chemical Eng. J., 116, pp. 61-66
Karabektas. M, Ergen. G and Hosoz. M. (2008). The effects of
preheated cottonseed oil methyl ester on the performance and exhaust emissions
of a diesel engine, Applied Thermal Engineering. Volume 28. Pages: 2136-2143.
Kulkarni M.G., Dalai A.K., and Bakhshi N.N.,(2007),
«Transesterification of canola oil in mixed methanol/ethanol system
and use of esters as lubricity additive». Bioresource Technology, 98, pp.
2027-2033.
Kusdiana, D. and S. Saka, (2001), «Kinetics of
transesterification in rapeseed oil to biodiesel fuel as treated in
supercritical methanol». Fuel, 80, pp. 693-698.
Kusdiana, D. and S. Saka, (2001), «Kinetics of
transesterification in rapeseed oil to biodiesel fuel as treated in
supercritical methanol». Fuel, 80, pp. 693-698.
L.K. Singh and G. Chaudhary. (2017). Advances in
Biofeedstocks and Biofuels. Volume 2. Production Technologies for Biofuels.
Pages.162-163.
Liu X., H. Hea, Y. Wang, S. Zhua, and X. Piao, (2008),
«Transesterification of soybean oil to biodiesel using CaO as a solid
base catalyst». Fuel, 87, pp. 216-221.
M. Balat. (2000) Fuels from Biomass - Overview. Sila
Science, University Mah, Mekan Sok. No.24.Trabzon, Turkey.
M. Mittelbach., (2009). Biofuels. Wiley Series in
Renewable Resource. Page 79.
Meneghetti, S. M. P., M. R. Meneghetti, C. R. Wolf, E. C.
Silva, G. E. S. Lima, M. de A. Coimbra, J. I. Soletti, and H. V. Carvalho,
(2006), «Ethanolysis of castor and cottonseed oil: A systematic study
using classical catalysts. J. Am. Oil Chem. Soc., 83, pp. 819- 822.
Moussouni .I . (2016). Mémoire en vue de
l'obtention du Diplôme de MASTER en Sciences des aliments. Contribution
à L'étude physico-chimique des échantillons d'huile
d'olive et leur mélange.
Nidhal Attia Mars 2018, Le guide de l'accord de paris sur
le climat, Heinrich böll stiftung-Afrique du Nord/Tunis.
Norhafiz .A, Jasronita .J, Mohd .Z.A, A. Kadir and Mohd .N.M.
Suitability of palm based oil as dielectric insulating fluid in Transformers. J
Electr Eng Technol. Vol: 8. Page: 742. (2013).
Noureddini H. and D. Zhu, (1997), «Kinetics of
Transesterification of Soybean Oil». J. Am. Oil Chem. Soc., 74, pp.
1457-1463.
Patrice LEVAN G, D. SHEIL et Markku K., 2015
Biodiversité, énergie et changements climatiques, Le palmier
à huile, Dr Jekill pour l'énergie, Mr Hyde pour la
biodiversité CIFOR à Bogor-Indonésie).
Pinto et al. (2005) Biodiesel from triglycerides via
transesterification
Rapport Dossier, le mythe de l'huile de palme 100%
durable, Les limites des initiatives volontaires : le cas de la RSPO et de
l'Alliance Belge pour une huile de palme durable 2018.
Reis, S. C. M. dos, E. R. Lachter, R. S. V. Nascimento, J. A.
Rodrigues Jr., and M. G. Reid, (2005), «Transesterification of
Brazilian vegetable oils with methanol over ion-exchange resins». J. Am.
Oil Chem. Soc., 82, pp. 661-665.
Rieger M. M. (1990). «Glyceryl stearate, chemistry
and use». Cosmetics and Toiletries, 105, pp. 51-7.
Ropkins K., Quinn R., Beebe J., Li H., Daham B., Tate J., Bell
M., and Andrews G., (2007), «Real-world comparison of probe vehicle
emissions and fuel consumption using diesel and 5% biodiesel (B5) blend».
The Science of the Total Environment, 376, pp. 267-284.
Stamenkovic, O. S., Z. B. Todorovic, M. L. Lazic, V. B.
Veljkovic, and D. U. Skala (2008) Kinetics of sunflower oil methanolysis at
low temperatures. Bioresour. Technol., 99, pp. 1131-1140.
T. Kumar, A. Kumar and A. Raheman. (2007). Biodiesel
production from Jatropha oil with high free fatty acids: An optimized process.
Biomass and Bioenergy.
Tamalampudi S., M.R. Talukder, S. Hamad, T. Numata, A. Kondo,
and H. Fukuda, (2008), «Enzymatic production of biodiesel from
Jatropha oil: A comparative study of immobilizedwhole cell and commercial
lipases as a biocatalyst». Biochemical Eng. J., 39, pp. 185-18
Z. Bettahar, B. Cheknane and K. Boutemak. (2016). Etude
de la transestérification d'un mélange des huiles usagées
pour la production du biodiesel.
Zhou W. and D.G.B. Boocock, (2006), «Phase
distributions of alcohol, glycerol, and catalyst in the transesterification of
soybean oil.» J. Am. Oil Chem. Soc., 83, pp. 1047-1052.
Zhou W., S. K. Konar, and D.G.B. Boocock, (2003),
«Ethyl esters from the single-phase base-catalyzed ethanolysis of
vegetable oils». J. Am. Oil Chem. Soc., 80, PP. 367-371.
Zhou W., S. K. Konar, and D.G.B. Boocock, (2003),
«Ethyl esters from the single-phase base-catalyzed ethanolysis of
vegetable oils». J. Am. Oil Chem. Soc., 80, PP. 367-371.
Ganaprakasam A, Sivakumar V M, Surendhar A,
Thirumarimurugan M and Kannadasan T., (2013) Recent strategy of biodiesel
production from waste cooking oil and process influencing parameters: A review
Journal of Energy. Pages: 1-10.
Fonds de la CNUCED (2016)pour l'information sur les
marchés des produits de base agricoles, New York et
Genève
K. Sivaramakrishnan and P. Ravikumar.(February
2012).Determination of cetane number of biodiesel and its influence on physical
properties. Vol (7). N°2.
WEBOGRAPHIE
www.cf.ac.uk/archi/research/cost8
/case/sweden.html
www.zeus-europe.org/stock.html
Advantages of bio fuels-biofuels. (
http://biofuel.org.uk/advantages-of-biofuels.html).



