1.2.1. Les monosaccharides
Les monosaccharides, également appelés sucres
simples ou oses, sont les structures élémentaires constitutives
des oligo- ou polysaccharides. Possédant de 3 à 7 carbones, ils
sont caractérisés par la présence d'un groupe carbonyle et
de fonctions alcool sur les autres carbones. Les monosaccharides sont
classés selon leur nombre d'atomes de carbone et suivant leur groupement
fonctionnel aldéhyde ou cétone. Selon cette nomenclature, un
sucre à six carbones comportant un groupement aldéhyde sera
appelé aldohexose, alors qu'un cétohexose sera un hexose portant
un groupement cétonique.8 (Tableau 1)
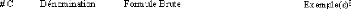

Tableau 1: Différents monosaccharides classés selon
leur nombre de carbone et selon leur groupement fonctionnel dans le cas des
hexoses.
1.2.1.1. Stéréochimie: le système
D/L
Un sucre simple typique est composé d'un certain nombre
de carbones asymétriques ou centres chiraux. Une méthode efficace
pour désigner les différentes configurations engendrées
par ces carbones asymétriques consiste à utiliser les deux
énantiomères du glycéraldehyde comme composés de
référence. Les monosaccharides sont alors vus comme
dérivant du D-glycéraldehyde ou du Lglycéraldehyde (Figure
2). Les désignations D- (pour dextrogyre) et L- (pour lévogyre)
des oses donnent donc une information sur la stéréochimie de la
molécule mais en aucun cas sur leur activité optique (sauf dans
le cas du glycéraldehyde bien évidemment).
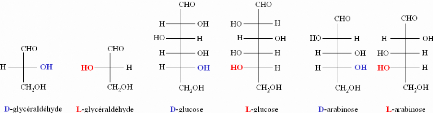
Figure 2: Les deux éniantomères du
glycéraldehyde sont utilisés comme composés de
référence dans les désignations D- et L- des hydrates de
carbone.
1.2.1.2. Cyclisation et nomenclature
Les monosaccharides de 5 à 6 carbones se cyclisent en
solution aqueuse et font ainsi apparaître un carbone asymétrique
supplémentaire, le carbone anomérique C1. La cyclisation des
hexoses ou pentoses conduit à la formation de deux structures
anomériques cycliqueset. La réaction de mutarotation permet
l'interconversion des formeset. Notons que, à l'équilibre
tautomère, une solution de D-glucose contient 35% d'-D-glucopyranose,
65% de-D-glucopyranose, et enfin 0,5% de D-Glucose dans sa forme
linéaire (Figure 3). Si la prédominance de la formen'a rien de
général, en revanche, la forme linéaire est toujours
présente sous forme de traces.
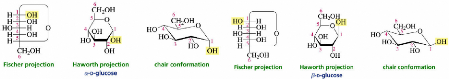
Figure 3: La molécule de D-Glucose sous forme cyclique
dessinée dans différentes représentations (projections de
Fisher, d'Harworth et conformation chaise-bateau)
1.2.1.3. Le glucose et le fructose
Parmi les huit diastéréoisomères des
aldohéxoses, seulement trois se trouvent de manière courante dans
la nature : le D-glucose, le D-mannose et le D-galactose. Le glucose est de
loin le plus important des monosaccharides naturels, il a une fonction de
transport via le sang entre les organes de stockage (le foie) et les organes
dits « consommateurs » tels que les muscles, le cerveau ou les tissus
nerveux. Parmi tous les oses, il est l'unique hexose à posséder
dans sa forme fi tous les groupements hydroxyles en position
équatoriale. Le fructose, qui est un isomère du glucose, fait
partie des héxocétoses, on le trouve abondamment dans les fruits
et le miel.
| 


