|
ANNEE UNIVERSITAIRE 2010/2011
REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET
POPULAIRE
MINISTERE DE L'ENSEIGNEMENT SUPERIEUR
ET DE LA
RECHERCHE SCIENTIFIQUE
UNIVERSITE SAAD DAHLEB DE BLIDA
FACULTE DES SCIENCES
AGRO-VETERINAIRES
DEPARTEMENT DES SCIENCES AGRONOMIQUES
L'effet des amendements organiques sur la structure
des
communautés de nématodes sur culture de tomate dans
la
région de Touggourt
Mémoire de fin d'étude en vue de l'obtention du
diplôme
de Master Académique en sciences
de la nature et la
vie
Spécialité : Phytopharmacie
appliquée
Présenter par : Melle. BELLAHAMMOU
Soumya
Soutenu publiquement le 12 Décembre 2011
Devant les membres de jury composé de :
|
Mme. KARA F.
|
MCA
|
U.S.D.B.
|
Président
|
|
Mme. NEBIH D.
|
MAA
|
U.S.D.B.
|
Promotrice
|
|
Mme. Baba Ali A.
|
MAA
|
U.S.D.B
|
Examinatrice
|
|
Mme. Djennas K.
|
MAB
|
U.S.D.B
|
Examinatrice
|
Je tiens à remercier avant
tout dieu le tout puissant de m'avoir accordé la force et la patience
pour accomplir ce modeste travail.
Ma profonde gratitude s'adresse
tout d'abord à :
Madame Nebih D., chargée de
cours de département de zoologie agricole à Blida, d'avoir
accepté de m'encadrer et de diriger ce travail.
Ma reconnaissance va
également à Madame Xara pour l''honneur qu'il m'a fait
d''accepter la présidence du jury de cette thèse.
J'adresse mes vifs remerciements
à Madame Baba Ali A. (MAA) et Madame Djennas X. (MAB) Université
de Blida, qui ont bien voulu faire partie de mon jury.
Ma profonde gratitude va
également à Mlle Amina, technicienne du laboratoire de
Zoologie pour leur disponibilité et pour le temps
consacré.

Je dédie ce modeste travail
:
A être la plus cher au
monde, ma mère que dieu t'offre à ton âme le
paradis.
A mon trésor
éternel et raison de ma vie, symbole du sacrifice à mon
père.
A ma source de confiance et
d'énergie est mon frère
A toutes les personnes que j'aime:
Fatima zohra, Fadila, Yacine A la joie de la maison
BELLAHAMMOU.
A toute la famille SOUDANI
..
A tous mes amis fidèles :
Houria, Karima, Lila, Nadjet, Khadidja , Kaouthar, Sana, Mariem, Souad, Salim,
Hamzy....que le destin nous réunis pour n'être qu'un seul, et dont
la vie nous a appris le respect de soi et comment partager ensemble les moments
les plus heureux
comme les plus pénibles A ma promotion.
BELLAHAMMOU Soumya
ÊÑÞÊ
ÉÞØäã í
ãØÇãØáÇ
áæÕÍã ìáÚ
ÉíØíÎáÇ
ÊÇÚãÊÌãáÇ
ÉíäÈ ìáÚ
ÉíæÖÚáÇ
ÊáÇíÏÚÊáÇ
ÑíËÊ
ÉÑãÇÄã í
ãØÇãØáÇ
áæÕÍã ìáÚ
ÇÏæÊÇãíäáÇ
ÊÇÚãÊÌãáá
ÉíäãÒáÇ
ÊÇÑíÛÊáÇ
ìáÚ ÉíæÖÚáÇ
ÊáÇíÏÚÊáÇ
ÑíËÊ ÉÓÇÑÏ
ÊãÊ
áËæ
삋
ÊáÇíÏÚÊáÇ
ÑÇÈÊÎÇ ãÊíæ
.ÊÑÞÊ ÉÞØäã í
áíÎäáÇ
ßáÐ ìáÅ
ÉÇÖáÅÇÈ
.ÊÞæáÇ ÑæÑã
Úã áÊÎí
ÉíÆÇÐÛáÇ
ÊÇÚæãÌãáÇæ
ÇÏæÊÇãíäáÇ
ÊÇÚãÊÌãáá
ÉÇËßáÇ
ØÓæÊã ä
ÌÆÇÊäáÇ
ÊÑåÙæ
ÉíáÈÇÞ
Çåá ÉÏÏÍãáÇ
ÉíØíÎáÇ
äÇÏíÏáÇ
ÚíÒæÊ .ÉííÙæ
ÊÇÚÇãÌæ
ÉíØíÎáÇ
äÇÏíÏáÇ ÉÑæ
äã
ÊáÇíÏÚÊáÇ
áÊÎã áßÔÈ
ÑËÄÊ
.ÊÞæáÇæ
ÌáÇÚáÇ Úã
ÉäíÚã
ãÑæáÇ äã
ÏÏÚ ìáÚ Meloidogyne
ÊÇÞÑí ÉÇËß
ØÓæÊãáá
ÉíäãÒáÇ
ÊÇáÇÊÎáÇÇ
íå
ÉãÏÎÊÓãáÇ
ÉíæÖÚáÇ
ÊáÇíÏÚÊáÇ
Çåá ä Çãß
ãØÇãØáÇ í
ÉíØíÎáÇ
äÇÏíÏáÇ
ÑÐÌáÇ ÉÏÞÚ
ÑíæØÊ ìáÚ
ÇÑíÈß ÇÑíËÊ
ÑËÄÊ
ÊÇÌáÇÚáÇ
åÐå ãÏÞÊ ä
ÌÆÇÊäáÇ
ÑåÙÊæ
.ãØÇãØáÇ
ÑæÐÌ í
ËÇäáÅÇ
ÑíæØÊ í
áËÇãã ÑíËÊ
.Meloidogyne
ãØÇãØ
ÉíÆÇÐÛáÇ
ÊÇÚæãÌãáÇæ
ÉíØíÎáÇ
äÇÏíÏáÇ ÉÑæ
ÉíæÖÚáÇ
ÊáÇíÏÚÊ :
ÉíÓíÆÑáÇ
ÊÇãáßáÇ
L'effet des amendements organiques sur la
structure des communautés de nématodes
sur culture de tomate
dans la région de Touggourt.
Résumé :
L'effet des amendements organiques sur les variations
temporelles des communautés de nématodes ont été
étudié sur culture de tomate dans une parcelle sous palmeraie
dans la région de Touggourt. Les amendements testés sont le
fumier et le grignon d'olive.
Les résultats révèlent que les
densités moyennes des communautés de nématodes et les
groupes trophiques varient en fonction du temps. Par ailleurs, les amendements
apportés affectent différemment l'abondance des nématodes
et des groupes fonctionnels. La distribution des nématodes
identifiée présente une certaine affinité avec les
traitements et le temps.
Les amendements organiques utilisés présentent
des variations temporelles des densités moyennes des larves de
Meloidogyne. Concernant le nombre de galles,les résultats
montrent que ces traitements apportés affectent significativement le
développement des nématodes à galles au sein de la
culture.Par ailleurs, ils ont un effet comparable dans le développement
des femelles dans les racines de tomate.
Mots clés : Amendements
organiques, Abondance des nématodes, Groupes
trophiques, Tomate, Meloidogyne.
The effect of organic amendments on the structure of
nematode
communities on tomato crop in the region of Touggourt.
Summary:
The effect of organic amendments on temporal variations of the
nematode communities was studied on tomato crop in a plot in palm area
Touggourt. The amendments are tested manure and pomace.
The results show that the average densities of nematode
communities and trophic groups vary over time. In addition, the amendments
rapports affecting different abundance of nematodes and functional groups. The
distribution of nematodes identified has a certain affinity with treatment and
time.
The organic amendments used are temporal variations of mean
densities of larvae of Meloidogyne. On the number of galls, the
results show that these treatments provided significantly affect the
development of root-knot nematodes in the crop. They also have a similar effect
in the development of females in the roots of tomato.
Key words: organic amendments, nematode
abundance, trophic groups, Tomato, Meloidogyne.
Sommaire
Introduction générale 1
Partie bibliographique
Partie Bibliographique
Chapitre I : Données bibliographiques sur les
communautés
de nématodes associés aux cultures
maraîchères ..3
I.1.Généralités sur les nématodes
3
I.2.Les communautés de nématodes associés
aux cultures maraîchères 5
I.3.Bio écologie des nématodes 6
I.4. La diversité trophique des nématodes 8
I.5. Importance des nématodes dans les
écosystèmes 11
I.6.Action des facteurs abiotiques et biotiques sur les
nématodes 14
I.6.1.Influence des facteurs abiotiques 14
I.6.2.Influence des facteurs biotiques 14
Chapitre II. Donnés bibliographiques sur les
amendements organiques ...16
II.1. Généralités sur les amendements
organiques 16
II.2. Différents types d'amendements organiques 16
II.3. Importance des amendements organiques 19
II.3.I. Effet sur le sol, la culture et les microorganismes
19
II.3.2. Effet sur les nématodes 20
Chapitre III. : Description de la plante hôte
« Tomate » .22
III.1. Généralités sur la tomate
maraichère 22
III.2. Taxonomie 23
III.3. Importance de la tomate en Algérie 23
III.4. Types de croissance et variétés de tomate
maraichère existantes en
Algérie 23
III.5. Exigence de la culture de tomate 24
III.5.1. Type de sol 24
III.5.2. Irrigation 24
III.6. Mode de conduite 24
III.6.1. Semis et repiquage 24
III.6.2. Eclaircissage 25
III.6.3. Eclaircissage des fruits 25
III.6.4. Effeuillage ..25
III.6.5. Tuteurage ...25
III.6.6. Taille 26
III.6.7. Aération 26
III.6.8. Gestion des mauvaises herbes 26
III.6.9.Récolte 26
Chapitre IV : Présentation de la région
d'étude
"D'Oued Righ" 27
IV.1-La situation géographique 27
IV.2-Facteurs édaphiques 28
IV.2.1- Géologie de la région 28
IV.2.2- Caractéristiques pédologiques 29
IV.2.3 -Hydrologie de la région 29
IV.3-Les facteurs climatiques 29
IV.3.1.Températures 29
IV.3.2. Pluviométrie et précipitation 30
IV.3.3. Durée d'insolation: 30
IV.3.4. Vents 30
IV.3.5. Humidité 30
IV.3.6. Evaporation ...30
IV.3.7.Synthèse climatique de la région de
Touggourt
IV.3.7.1- Diagramme ombrothermique de Gaussen dans la
région étudiée
de Touggourt 31
IV.3.7.2-Climagramme d'Emberger appliqué au niveau de la
région de
Touggourt 31
Partie Expérimentale
|
Chapitre I : Matériels et méthodes
I.1. Description des amendements utilisés
|
32
..32
|
|
I.1.1. Les grignons d'olives
|
32
|
|
I.1.2. Caractéristiques chimiques
|
32
|
|
I.2. Matériels
|
33
|
|
I.2.1. Origine les amendements organiques utilisés
|
..33
|
|
I.3.Méthodologie
|
33
|
|
I.3.2. Préparation de la parcelle de travail
|
33
|
|
I.3.3. Prélèvement des échantillons
|
34
|
|
I.3.4. Extraction des nématodes du sol
|
.34
|
|
I.3.5. Dénombrement et identification des taxons
|
35
|
I.3.5.1. L'effet des traitements sur estimation du taux
d'infestation des racines
par les larves (L2) de Meloidogyne .35
I.3.5.2. Estimation du taux de développement des larves
(L2) en femelles
36
I.4. Exploitation des résultats 37
I.4.1. L'analyse multi variée 37
I.4.2. Analyses de variance (SYSTAT vers. 12, SPSS 2009) 38
CHAPITRE II : Résultats et Discussion
II.1. Inventaire de la communauté de nématodes
rencontrés dans la parcelle d'étude
sur cultures maraîchères ..39
II.2. Répartition temporelle de la densité moyenne
globale des nématodes (N/50g de
sol) en fonction des traitements 42
II.3.Répartition temporelle des groupes trophiques en
fonction des
traitements 44
II.4. Effet des traitements sur la
répartition des nématodes phytophages ...47
II.5.Effets des traitements sur la répartition des
Meloidogyne 50
II.6. L'effet des traitements sur le nombre de galles ...53
II.7.Effet des traitements sur le nombre des femelles: 54
Discussion générale 56
Conclusion générale 61
Référence bibliographique
63
Annexes
Table des matières
LISTES DES SYMBOLES ET ABREVIATIONS
P : Probabilité
L2 : Larve de stade 2 de développement
de Meloidogyne
Fig. : Figure
MS : Matière sèche
N/50g de sol : Nématodes par 50g de
sol
LISTE DES FIGURES
|
Fig.01 : Morphologie de Pratylenchus
Fig.02 : Morphologie de Meloidogyne
Fig.03 : Morphologie d'Aphelenchus
Fig.04 : Morphologie de Tylenchorhynchus
|
|
7
|
7
7
7
|
|
Fig.05 : Fruits de tomate
|
|
|
22
|
|
Fig.06 : Feuilles de tomate
|
|
|
22
|
|
Fig.07 : Fleur de tomate
|
|
|
22
|
|
Fig.08 : Carte géographique
représentant la vallée d'Oued Righ
|
28
|
|
|
|
Fig.09 : Dispositif d'extraction des
nématodes du sol
|
|
35
|
|
|
Fig.10 : Estimation du taux d'infestation des
racines par les larves (L2) (Grx10).
|
|
|
36
|
Fig.11 : Dénombrement des femelles de
Meloidogyne au niveau des
galles. (Grx10). 37
Fig.12 : Morphologie de Scutelonema
G(x400)
(Bellahammou, 2011) 40
Fig.13 : Morphologie
de Xiphinema G(x400)
(Bellahammou ,2011) 40
Fig.14 : Partie
antérieure de Xiphinema G(x400)
(Bellahammou, 2011) 40
Fig.15 : Morphologie de femelle de
Xiphinema G(x400) 40
Fig.16 : Partie postérieure de
Xiphinema G(x400) 41
Fig.17 : Morphologie de Pratylenchus
G(x400) 41
Fig.18: Partie antérieure de
Ditylenchus G(x400) 42
Fig.19: Partie postérieure de femelle
Ditylenchus G(x400) 42
Fig.20: Partie antérieure de
Dorylaimus G(x400) 42
Fig.21: Partie postérieure de
Dorylaimus G(x400) 42
Fig.22 : Distribution temporelle des
densités moyennes globales des nématodes en
fonction des traitements 43
Fig.23: Répartition temporelle des
groupes trophiques en fonction des traitements 44
Fig.24 : Répartition temporelle des
groupes trophiques en
fonction des traitements 46
Fig.25 : Répartition temporelle des
abondances moyennes globales des groupes
trophiques en fonction des traitements. 47
Fig.26 : Répartition temporelle des
nématodes phytophages en fonction de
traitements 49
Fig.27 : Classification ascendante
hiérarchique de la structure des nématodes
phytophages en fonction des traitements 50
Fig.28: Distribution temporelle des
densités moyennes des Meloidogyne en fonction
des traitements 51
Fig.29 : Variation temporelles des Meloidogyne
en fonction des traitements
51
Fig.30: Effet des traitements sur le
développement des Meloidogyne sur les plants
de tomate 52
Fig.31: Effet des traitements le nombre de
galles moyennes 53
Fig.32 : Effet des traitements sur le
développement des femelles des
Meloidogyne 54
Fig.33 : Effet des
différents traitements sur le développement des femelles moyen
55
LISTE DES TABLEAUX
Tableau 1 : La densité globale des
nématodes rencontrés dans la pareille expérimentale
(annexe)
Tableau 2 : Modèle G.L.M. appliqué
à la variation temporelle des nématodes en fonction
des traitements 43
Tableau 3 : Modèle G.L.M. appliqué
sur la variation temporelle des groupes trophiques
en fonction du traitement 46
Tableau 4 :Effet des traitements sur les
densités moyennes des Meloidogyne à travers
l'analyse de la variance 52
Tableau 5 : Modèle G.L.M. appliqué
au développement des
Meloidogyne sur les plants de tomate 53
Tableau 6: Effet des différents
traitements sur le nombre de femelle
moyen 55
Tableau 7 : Nombre de galles rencontrés
sur les racines (annexe)
Tableau 8 : Nombre des femelles dans des galles
de racines de grignon d'olive (annexe) Tableau 9 : Nombre des
femelles dans des galles de racines de fumier (annexe) Tableau 10 :
Nombre des femelles dans des galles de racines de témoin
(annexe) Tableau 11 : Nombre des femelles dans des galles de
racines de vydate (annexe)

INTRODUCTION GENERALE
L'agriculture saharienne a été depuis longtemps
de type familial, avec un système oasien basé sur la
phoeniciculture couvrant environ 60.000 hectares (80.000.000 de palmiers), en
association avec la céréaliculture et le maraîchage. Parmi
ce dernier, nous notons une dominance des solanacées:
tomate-poivron-piment-aubergine et des cucurbitacées (Djarroudi,
2001).
Le mode de culture en palmeraie offre un microclimat qui
réunit d'une part, les conditions édaphiques et climatiques
typiques pour accroître la production et augmenter le rendement. Mais, il
favorise la pullulation des nématodes phytoparasites, notamment, le
genre Meloïdogyne qui cause de nombreux problèmes aux
cultures des zones sahariennes. Il est très connu par son
agressivité et les pertes considérables de rendements dans les
cultures maraîchères sahéliennes (Senghor, 1998 ; Villenave
et al., 1998). Cependant, les nématodes peuvent avoir un impact
substantiel sur la dynamique nutritive dans le sol, en agissant sur la
décomposition de la matière organique du sol et en augmentant la
minéralisation des éléments nutritifs des plantes
(Griffiths, 1994 ; Bardgett et al., 1999 ; in Verschoor et
al. 2002).
La préparation du sol et l'apport de compost permettent
d'améliorer le statut organique du sol, en conséquence un
meilleur développement de la plante cultivée. Par ailleurs ces
traitements induisent des modifications de la structure spécifique des
communautés de nématodes phytoparasites en augmentant l'abondance
d'une espèce peu pathogène qui pourra limiter les
dégâts dus aux nématodes (Villenave et al.,
1998).
Plusieurs travaux signalent qu'un apport d'amendement
organiques (animale ou végétale) par les producteurs est une
alternative de gestion des cultures visant à réduire ou à
éliminer les intrants synthétiques (Mian et Rodrigue- Kabana,
1982 ; Abawi et Widmer, 2000 ; Mc Sorley et Fredirick, 1999 in Nahar et
al., 2006). En effet ces amendements améliorent la
qualité (la fertilité et la structure) du sol et peut
réduire des pertes dues aux phytoparasites sans la pollution
environnementale liée à
l'utilisation d'engrais et des pesticides chimique tout en
augmentant la récolte et les rendements (Boehm et al., 1993 ;
Jobin et Petit, 2004 et Oka, 2010)
.
En rapport avec les travaux sus cités, nous avons
entrepris la présente étude. Les objectifs visés sont
d'une part d'évaluer l'effet des amendements organiques sur les
variations temporelles des communautés de nématodes
rencontrés sur tomate dans un biotope saharien (la région de
Touggourt), et d'autre part estimer leur action sur les nématodes
à galle (Meloidogyne).
Pour atteindre les objectifs visés, nous avons
adopté une méthodologie de recherche visant :
+ Une analyse bibliographique en quatre chapitres
+ Chapitre I : Arbore une synthèse bibliographique sur
les communautés de nématodes associés aux cultures
maraichères.
+ Chapitre II : Traite des généralités sur
les amendements organiques.
+ Chapitre III : Description de la plante hôte «
Tomate »
+ Chapitre IV : Présentation de la région
d'étude "D'Oued Righ"
+ Une partie expérimentale portant deux chapitres
+ Chapitre I : Présente la méthodologie de travail
utilisée.
+ Chapitre II : Traite les résultats obtenus, suivi par
la discussion et une conclusion générale.
I
111/
' Ir.,M
- ~
·
__
Les nématodes possèdent un appareil
excréteur, mais chez les phytoparasites, la seule partie habituellement
visible est le segment de tube
Chapitre I: Données bibliographiques sur les
communautés de nématodes associés aux cultures
maraichères
I.1.Généralités sur les
nématodes
Les Nématodes ou Anguillules sont de
petits vers ronds microscopiques mesurant presque tous moins d'un
millimètre de long. Ils sont le plus souvent invisibles (Sonneville,
2006). Ils sont vermiformes et forment un groupe zoologique très
important du fait qu'ils contiennent un grand nombre d'espèces qui
vivent dans des milieux divers (De Guiran, 1983).
Les nématodes sont parmi les animaux les plus
diversifiées, généralement les plus abondantes des
métazoaires et les plus importants consommateurs secondaires dans le sol
(Mulder et al., 2005). Ils sont largement distribués et
occupent une position centrale dans le réseau trophique du sol (Moore et
de Ruiter, 1991). Ils ont des effets profonds sur la décomposition des
matières organiques, et la minéralisation des
éléments nutritifs (Seastedt et al., 1988; Sohlenius et
al., 1988), la transformation et le transfert d'énergie
(Anderson et al., 1981; Freckman,1988; Yeates et Bongers, 1999; Neher,
2001, Coleman et al.,2004). De nombreux rapports indiquent que les
nématodes possèdent plusieurs particularités qui font
d'eux des bio-indicateurs écologiques utiles dans le sol et les
écosystèmes aquatiques (Freckman, 1988).
Morphologiquement, les nématodes sont constitués
d'un tube externe (cuticule) enveloppant deux tubes internes superposés,
le tube digestif et le tractus génital (Cayrol et al.,
1992).Les nématodes phytoparasites se caractérisent par la
présence dans la cavité buccale d'un stylet performant. C'est cet
organe en forme d'aiguille creuse que l'animal enfonce dans les tissus du
végétal pour absorber le contenu prédigéré
des cellules. Il est suivi d'un canal oesophagien qui comprend une partie
musculaire qui se termine par le bulbe médian et d'une partie
glandulaire.
La partie musculaire, véritable pompe aspirante et
refoulante, injecte le produit des glandes dans les cellules
végétales à travers le stylet, puis en absorbe le contenu
prédigéré (De Guiran, 1983).
excréteur aboutissant au pore excréteur. Le pore
se présente comme un orifice rond sur la face ventrale (Taylor,
1968).
Le système nerveux est très complexe, mais peu
visible à l'exception de l'anneau nerveux et de l'hémizonide.
L'anneau nerveux entoure l'oesophage immédiatement en arrière du
bulbe médian. En général, la paroi ventrale
présente un léger renflement à cet endroit (Taylor,
1968).
Les méthodes d'identification des nématodes sont
liées à l'examen morphologique des caractéristiques
phénologiques. Les critères comme : la longueur et la largeur du
corps, la forme de la tête et de la queue, la longueur du stylet,
position de la vulve, le type de recouvrement de la glande oesophagienne par
rapport à l'intestin ; sont tous utilisées pour l'identification
des genres de nématode. Pour identifier les espèces, d'autres
caractéristiques additionnelles sont nécessaires comme la
structure de la cuticule, la présence ou l'absence de soies
céphalique, bursa caudale, phasmides, la structure oesophagienne et le
nombre des ovaires (Heyns, 1981; Eisenback, 1998).
La reconnaissance d'environ 20 000 espèces
décrites est basée principalement sur les caractéristiques
morphologiques et anatomiques complétée par les marqueurs
moléculaires qui sont de plus en plus importants dans l'identification
la et classification des nématodes (Blaxter et al., 1998 ;
Thomas et al., 1997).
Les conséquences du parasitisme des nématodes
sur la plante sont extrêmement difficiles à quantifier. Cependant,
les nématodes agissent sur la fonction assimilatrice du système
racinaire et peuvent limiter l'absorption des éléments nutritifs
nécessaires au développement de la plante (Villenave, 2000). Ils
contribuent ainsi à la baisse de la production des cultures, en cas de
forte infestation des sols, ils entraînent des altérations
caractéristiques ou des déformations typiques de l'ensemble du
végétal. Ils provoquent des maladies de
dépérissement accompagnées de différents
symptômes ; nanisme, retard végétatif, voir même la
mort des plantes (Sonneville, 2006).
I.2. Les communautés de nématodes
associés aux cultures maraîchères
Des études réalisées sur l'inventaire des
nématodes associés aux cultures légumières Netscher
et Luc (1974) en Mauritanie ; Diongue (1996) au Niger. Bezaz (2006), Hadri,
2006 et Hedibel (2007) en Algérie ont signalé la présence
de divers genres de nématodes phytophages dans les sols
maraîchers. Ils sont représentés par Pratylenchus,
Ditylenchus, Aphelenchus, Aphelenchoides, Tylenchorhynchus Helicotylenchus,
Tylenchus, Meloidogyne, Psilenchus et Heterodera. La
répartition des taxons identifiés varie en fonction des zones
prospectées.
La structure d'une communauté de nématodes, y
compris les espèces phytophages, reflète l'état sanitaire
d'un sol. Dans les régions tempérées comme dans ceux
tropicales et subtropicales, les systèmes fortement anthropisés
présentent des communautés peu diversifiées : moins de 10
espèces phytoparasites dans un même échantillon de sol
(Evans et al. ,1993 ; Luc et al., 1990).
En Algérie, le travail de Bezaz (2006) et Hedibel
(2007) a révélé que le nombre et la répartition des
espèces de nématodes phytophages dans les sols maraîchers
varient en fonction des biotopes étudiés. Les systèmes
agricoles des zones des montagnes (Hedibel, 2007) et des zones des plaines
intérieures (Hadri, 2006), présentent généralement
une diversité nématologique est plus importante. Mateille et
al. (2004), affirment que l'effet pathogène d'une
communauté est inversement proportionnel au nombre d'espèces qui
la constituent, parce que en absence de compétition, les
nématodes endoparasites sédentaires (Meloidogyne spp)
sont très agressives et provoquent des dégâts importants
aux racines et affaiblissent la plante infestée.
Dans certain cas, le concept fondamental du rapport entre
diversité nématologique et la pathogénie d'une
communauté peut être considérée comme un auxiliaire
de gestion des nématodes Werner et Peacor (2003) ; in Hedibel (2007).
Les populations de nématodes ne restent pas
stationnaires. Elles subissent l'influence des cultures, des engrais organiques
et des traitements de désinfection du sol. Parmi ces facteurs, la nature
de la plante cultivée affecte fortement ces fluctuations (Taylor, 1968).
Selon Villenave et al. (1998), la préparation du sol et
l'apport de compost permettent d'améliorer le statut organique du sol,
en conséquence, un meilleur développement de la plante
cultivée. Par ailleurs ces
traitements induisent des modifications de la structure
spécifique des communautés de nématodes phytoparasites en
augmentant l'abondance d'une espèce peu pathogène qui pourra
limiter les dégâts dus aux nématodes. Cadet et al.
(2000) ont montré que dans les jachères d'âges
croissants (dans la zone soudano sahélienne), la diversité du
peuplement et l'abondance des nématodes augmentent
régulièrement.
I.3. Bio écologie des nématodes
A l'origine, vivant dans l'eau ; les nématodes ont
colonisé tous les milieux. Actuellement, 25 000 espèces sont
décrites (Maggenti, 1991 et Noir, 2002). Ils se situent au
deuxième rang après les insectes en termes de nombre
d'espèces différentes. Dans le sol, les nématodes
constituent la partie la plus importante de la biomasse. Le peuplement normal
d'un sol agricole en formes libres est de l'ordre de 20 à 30 000
individus par kg de sol (Regnault-Roger et al., 2002).
Les nématodes phytophages et les nématodes
libres sont extrêmement nombreux dans les sols cultivés. Le type,
le nombre et la répartition des espèces de nématodes dans
les sols cultivés dépendent du climat, de la nature du sol, du
type de culture, pratiques culturales et autres. Dans les cultures
pérennes ou dans un milieu naturel tel que la forêt ou la prairie,
la communauté de nématodes est un peu plus stable, mais toujours
sujette à des fluctuations qui sont en fonction de la croissance des
racines, de la température et de l'humidité (Taylor, 1968 in El
Aimouche). Certaines espèces deviennent fortement colonisatrices en
l'absence de compétition et par conséquent très agressives
ce qui engendrent des dégâts importants (Evans et al.,
1993 ; Luc et al., 1990 in El Aimouche).
Selon leur mode de parasitisme ils sont classés en
trois catégories les ectoparasites, les endoparasites et les semi
endoparasites chacune d'elles étant subdivisée en deux groupes
sédentaire et migrateur, (Ritter, 1971).
Les endoparasites sédentaires ou migrateurs deviennent
adultes et pondent toujours à l'intérieur des tissus
végétaux, le plus souvent dans les racines exemple les genres
Meloidogyne, Heterodera et Pratylenchus mais aussi
pour quelques espèces, dans les feuilles, les tiges et les
inflorescences (Lacroix, 2006 in Mazigh).
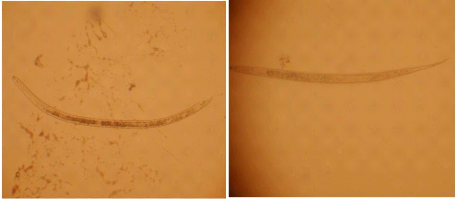
Fig.1: Morphologie de Pratylenchus Fig.2:
Morphologie de Meloidogyne
Les ectoparasites sédentaires ou migrateurs se tiennent
dans le sol à l'extérieur de la racine. Tel que les genres
Rotylenchus, Tylenchorhynchus, Aphelenchus. (Luc et
al., 1990 in Mazigh).
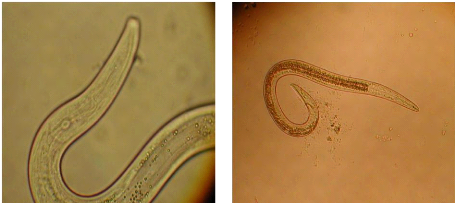
Fig.3 : Morphologie d'Aphelenchus Fig.4 :
Morphologie de Tylenchorhynchus
Les semi endoparasites, on range dans cette
catégorie les individus qui pénètrent partiellement dans
la racine pour se nourrir, on peut distinguer les migrateurs et les
sédentaires, comme les genres Helicotylenchus et
Rotylenchulus (Luc et al., 1990).
Selon De Guiran (1983 in Mazigh) les nématodes
s'attaquent à plusieurs cultures, on cite principalement : les cultures
maraîchères, les céréales, les cultures florales qui
sont attaquées par les genres Meloidogyne, Pratylenchus
et Ditylenchus. Selon le même auteur, d'autres cultures
comme les cultures fruitières qui sont également attaquées
par les Meloidogyne, les Pratylenchus, Tylenchulus,
Helicotylenchus et Rotylenchus. Cependant la vigne est surtout
attaquée par les nématodes du genre Xiphinema.
La reproduction des nématodes est selon les
espèces soit sexuée soit parthénogénétique.
Chez les espèces parthénogénétiques, les
mâles n'interviennent pas dans la reproduction (Agios, 1978). Les
nématodes passent par une série de cinq stades de
développement, distincts séparés par des mues. Le cycle
diffère selon les groupes de nématodes et selon le mode de
parasitisme sédentaire ou migrateur (Taylor, 1968). Les nématodes
phytoparasites ont un cycle approximativement mensuel. La longueur du cycle de
reproduction est très dépendante de la température. Dans
les pays tempérés, il n'y a pas de reproduction en hiver, souvent
se produit qu'une génération par an. Par contre dans les pays
tropicaux, plusieurs générations par an sont signalées.
Ceci explique que les dégâts y sont généralement
plus importants. A titre d'exemple chez les Meloidogyne la
durée du cycle de vie est très variable selon les conditions de 3
à 8 semaines, elle est de 6 semaines à 25°C (Bertrand et
al., 2001). Cependant, Les nématodes libres (non parasites) ont
un cycle hebdomadaire. Ce qui leur permet de recoloniser le sol très
rapidement (Mateille et al., 1995).
I.4. La diversité trophique des nématodes
Les nématodes sont largement répartis dans le
sol, leurs communautés sont composées de diverses espèces
selon leurs tendances alimentaires (Gomes, et al., 2003). Les
connaissances sur les habitudes alimentaires des nématodes sont encore
fragmentaires, l'examen le plus récent des nématodes dans le sol
a distingué huit types (Yeates et al., 1993a). Pour faciliter
l'interprétation de la structure de la communauté, il faut
distinguer les nématodes associés aux plantes des formes qui s'y
alimentent (Yeates et al., 1993b).
Gomes et al., (2003) classent les nématodes
dans cinq majeurs groupes, les fungivores, les bactérivores, les
parasites des plantes (phytophages), les prédateurs et les omnivores.
La plupart des nématodes utilisent l'énergie
résultant de la photosynthèse des plantes. Ils peuvent
s'alimenter directement sur les producteurs primaires, tels que les plantes
supérieures (par exemple Aphelenchoides sur les feuilles,
Ditylenchus sur des tiges, Pratylenchus et Meloidogyne
sur des racines), les algues unicellulaires (par exemple Chromadorita,
Pareudiplogaster et Daptonema sur des diatomées), ou sur
des microorganismes associés à la décomposition de la
matière végétale (par exemple Aphelenchus, Filenchus
sur les mycéliums fongiques ; Rhabditis, Plectus, Leptolaimus
et beaucoup de Monohysteridae sur des bactéries). Les
fèces animales et les cadavres sont des ressources importantes pour le
développement des microorganismes et les nématodes qui s'y
alimentent (fungivores et bactérivores).
Les niveaux trophiques supérieurs comme
prédateurs des nématodes et d'autre
micro-invertébré (par exemple Mononchus, Nygolaimus,
Enoploides, Sphaerolaimus) ou comme parasites des
invertébrés ou vertébrés (par exemple
Thelastoma, Ascaride) eux-mêmes dépendants des plantes.
Cependant, les nématodes s'alimentant sur plus d'un niveau trophique se
classent dans le groupe des omnivores (Polz et al., 2000;Van Gaever et
al., 2006).
Les groupes trophiques définis par Yeates et al.
(1993a), sont représentés par :
? Les nématodes phytophages, à
titre d'exemple (Meloidogyne, Heterodera, Helicotylenchus, Pratylenchus,
Xiphinema....), utilisant leur stylet pour se nourrir au niveau des
vaisseaux conducteurs des plantes. Un grand nombre de ces nématodes sont
associés à la réduction des récoltes en rapport
avec leur densité de population. Certaines espèces de
Longidoridae et Trichodoridae transmettent des maladies
virales aux plantes.
? Les nématodes associés aux
plantes, comme Tylenchus et Dorylaimellus, possédant
un stylet se développent en grand nombre dans la rhizosphère des
plantes sans réduction de récoltes.
s Les nématodes fungivores, (Aphelenchus,
Aphelenchoides, Leptonchus, Diphtherophora) utilisant leur stylet pour se
nourrir sur les hyphes mycéliens.
s Les nématodes bactérivores, citons
(Rhabditis, Caenorhabditis,
Diplogaster,
Cephalobus, Alaimus), se nourrissant de procaryotes
utilisant leur stoma tubulaire inerme.
s Les nématodes prédateurs se nourrissant de
sources alimentaires d'origine animale en l'ingérant leur proies
à travers une large cavité munie de dents (Diplogaster,
Mononchus, Nygolaimus) ou en aspirant le contenu du corps
prédigéré à travers lumen de leur stylet
(Seinura, Labronema).
s Les nématodes omnivores, enfermant certain
Dorylaimidae (Dorylaimus) il parait qu'ils utilisent comme
source alimentaire les bactéries, les champignons, des proies de la
microfaune, des diatomées et des algues.
s Nématodes parasites des animaux, dont les stades
infestant se rencontrent dans le sol, (Deladenus) et
(Heterorhabditis).
Les groupes trophiques des nématodes répondent
différemment aux divers conditions de l'environnement et pratiques
culturales. Les nématodes bactérivores réagissent
couramment aux variations d'abondance de leur source alimentaire (Zeleney et
al., 2004) et pullulent toujours dans les sols très riches en
matière organique (Yeates et King, 1997). Les nématodes
prédateurs et omnivores sont plus abondant dans les zones naturels que
dans les champs agricoles ceci est du à leur grande sensibilité
aux modifications des sols (Neher, 2000).
L'étude de Wardle et al., (1995), sur l'effet
du travail du sol et de la jachère sur les variations des
différents groupes trophiques a montré que le travail du sol
stimule modérément les bactérivores et les fungivores
alors que les phytophages, les prédateurs et les omnivores sont
modérément inhibé. Cependant les jachères
discontinue stimulent les prédateurs et les omnivores par contre elles
inhibent les bactérivores, les fungivores et les phytophages.
II.5. Importance des nématodes dans les
écosystèmes
Les nématodes sont parmi les organismes
multicellulaires les plus abondants et les plus évolué. Ils ont
la capacité d'adaptation physiologique et comportementale envers divers
habitats et niches écologiques riche en carbone organique (Howard,
2004). D'après Bongers et Ferris (1999), les quatre cinquième du
monde animal multicellulaire de la planète sont
représentés par les nématodes. De nombreuses
espèces sont libres, vivant dans les sols, les eaux douces ou marines ;
certaines sont parasites de vertébrés (ascaris, oxyures,
trichines, strongles...), ou d'insectes ; d'autres sont phytophages (Maurin,
1999 in Kadem). Ils se développent sous une large gamme de conditions
environnementales, et ils répondent facilement aux modifications de
l'environnement (Bongers et Ferris, 1999; Urzelai et al., 2000;
Diemont et al., 2006; Ferris et Bongers, 2006).
Dans des écosystèmes naturels, les
nématodes contribuent à la diversité spatiale et
temporelle des plantes (De Deyn et Van der Putten, 2005). L'activité
d'alimentation des nématodes contribue à la stabilité de
la chaine trophique du sol. Quand des sols sont dégradés il peut
y avoir des effets néfastes sur la qualité du sol et de l'eau
(Viglierchio, 1991). D'après Gupta et Yeates (1997), Les
nématodes (libres et phytoparasites) représentent l'outil le plus
adapté car ils sont les plus étudiés taxonomiquement,
connus par leur habitude alimentaire et par les dégâts qu'ils
causent aux cultures agricoles. Les nématodes jouent un rôle
important dans les processus des composants de la plupart des
écosystèmes. Les travaux de Ingham et aI., (1985) ;
Ferris et aI., (1998) affirment que dans la chaîne trophique du
sol, des nématodes sont impliqués dans la transformation de la
matière organique en des éléments minéraux et
organiques qui peuvent être mis au profit de la croissance et la
production des plantes. Selon, Seastedt, (1984) ; Seastedt et al.
(1988) ; Trofymow et Coleman (1982) ; et Yeates et Coleman
(1982) les nématodes agissent sur la croissance et l'activité
métabolique des microorganismes, en modifiant les communautés
microbiennes, régulent ainsi le taux de décomposition des
matières organiques et la minéralisation des
éléments nutritifs.
Les assemblages des nématodes du sol sont divers et
renferment un grand nombre d'individus de petite taille qui sont en contact
avec la solution de sol et utilisent une large gamme des ressources
alimentaire. Ils ont un cycle de vie court et sont aisément
prélevés et identifiés. Par conséquent, plusieurs
études récentes ont employé l'analyse des
communautés de nématode pour évaluer la "santé de
sol" ou sa "durabilité" en particulier les sols cultivés (Yeates
et al., 19981 ; Freckman et Ettema, 1993; Yeates et al.,
1994).
Une gamme d'indices (diversité, abondance,
maturité) basés sur les proportions de la communauté de
nématodes destinés aux taxons, aux stratégies
reproductrices, ou groupes trophiques sont employées. Ces indices de la
nématofaune reflètent les changements réels de la
communauté de nématodes dans beaucoup de conditions. Ces
changements indiquent des changements de sol et de processus
écologiques. Par la compréhension du rôle des
nématodes dans ces processus qu'une meilleure compréhension du
rapport entre les plantes et les communautés de nématode de sol
peuvent être obtenu.
Diverses investigations mettent en évidence un
rôle important des nématodes dans les processus essentiels du sol.
A titre d'exemple la contribution directe des nématodes à la
minéralisation de l'azote et à la distribution de la biomasse
dans les plantes, les travaux de Trofymow et Coleman, (1982), montrent qu'en
présence des nématodes bactérivores et fungivores plus
d'azote est disponibles sous la forme d'ammonium qu'en leur absence. Dans des
conditions sur champs, les nématodes bactérivores et
prédateurs participent de la minéralisation de l'azote
(directement et indirectement) d'environ 8% et 19% respectivement, dans les
systèmes de l'agriculture conventionnelle et intégrée
(Beare, 1997).
Depuis les années 1970, les nématodes ont
été utilisés comme bio moniteurs (bio surveillance) de
l'environnement dans les systèmes aquatiques (Deborah et Neher, 2001).
Cas de Panagrellus redivivus pour détecter les concentrations
de
toxines qui affectent la mue et la croissance de l'organisme
par la stimulation, l'inhibition ou létalité, et fournit un test
biologique rapide efficace et économique.
Ce nématode a été utilisé pour
détecter les effets toxiques d'environ 400 produits chimiques
(Samoiloff, 1987). Dés les années 1980, l'intérêt
accru pour l'utilisation de communautés nématodes comme des
indicateurs pour surveiller l'environnement terrestre (Bongers, 1990 et
Freckman, 1988).
Plusieurs auteurs attestent que l'utilisation des
nématodes comme des bio indicateurs est due à plusieurs de leur
caractéristiques biologiques.
D'une part d'ordre morphologique, ils sont doté d'une
cuticule perméable, qui leur permet de réagir à une gamme
de polluants et de répondre avec la capacité de
rétablissement des écosystèmes des sols (Saly et Ragala,
1984; Wasilewska, 1979, 1989). Cette cuticule est également transparente
facilitant leur identification morphologique sans recourt à la
dissection, (Bongers et Ferris, 1999). D'autre part d'ordre physiologique,
certains nématodes ont des formes de résistance comme
anhydrobiose ou enkystement (formation des kystes) qui leur permettent de
survivre à conditions environnementales défavorables. Bien que
d'autres sont plus sensibles, comme les espèces de l'ordre des
Dorylaimida n'ont pas de stades résistants, ce qui les rend
plus sensibles aux changements environnementaux (Bongers, 1999).
Ces caractéristiques peuvent également
être de nature biochimique, selon Hashmi et al. (1997), les
nématodes ont des protéines de choc thermique qui sont hautement
conservées. Selon, Kammenga et al. (1998), l'expression de ces
protéines est améliorée lorsqu'ils sont exposés
à des stress comme la chaleur, des ions métalliques, ou toxines
organiques. Ces protéines pourraient servir de biomarqueurs pour
l'évaluation écotoxicologique des sols (Guven et al.,
1994, 1999; Kammenga et al., 2000).
Dans le cadre de la recherche de solution alternative aux
nématicides pour le contrôle des nématodes phytoparasites,
il s'agit de déterminer des pratiques qui permettent de réduire
les dégâts sans forcément réduire l'abondance des
nématodes (Cadet et al, 1997 ; Cadet, 1998). Pour pallier
à cette difficulté, il est apparu nécessaire d'examiner la
situation sous l'angle qualitatif (Spaull et Cadet, 1990 ; Baujard et Martiny
,1995).
I.6.Action des facteurs abiotiques et biotiques sur les
nématodes
Tout organisme est soumis, dans le milieu ou il vit à
des actions simultanées des différents agents, physiques,
chimiques, édaphiques, climatiques et biotiques contrôlant ses
diverses activités.
De par leur statut de parasite, l'abondance des
nématodes est dépendante de la présence de la plante
hôte, mais si cette condition est nécessaire, elle n'est pas
suffisante. Il faut aussi que l'environnement édaphique permette le
déroulement de la phase tellurique du cycle biologique des
nématodes (Stirling, 1991).
En effet, d'après Norton(1989), Kandji et al.
(2001) ; Cadet et al. (2005) les caractéristiques du sol
affectent l'abondance, la distribution et la structure des communautés
de nématode, indépendamment de l'influence directe de la plante
hôte.
I.6.1.Influence des facteurs abiotiques Type du
sol
La relation (nématode-type de sol), nommée
relation mésologique, est connue depuis longtemps. De nombreux auteurs
ont observé que la répartition des nématodes
phytoparasites est en relation avec le sol (Seinhorst ,1956 ;
Quénéhervé, 1988 ; Blair et al., 1999). En effet
une récente étude faite par Zhao et al. (2000), sur 5
types de sols différents limoneux, sableux, argileux, limoneux-sableux,
et argileux-limoneux et sur chaque type de sol inoculé (de 2000 à
2500 L2) de Meloidogyne ont remarqué que le taux de
développement des nématodes et plus élevé dans les
types de sol : Limoneux, sableux et limoneux-sableux. Brown et Swain (1974
cité par Bachelier,1978) ont montré que la structure, par
l'instabilité des agrégats du sol peut devenir un facteur
limitant dans la distribution des nématodes en déterminant une
forte compacité des sols et un manque d'aération.
La présence d'une plante ne déterminant pas
obligatoirement celle des espèces de nématodes qui sont capables
de la parasiter. Estioko et Reyes (1984) affirment que pour une même
plante, les espèces de nématodes présentes dans les sols
sableux sont souvent différentes de celles que l'on rencontre dans les
sols argileux. L'étude de Cadet et Debouzie (1990) dans les parcelles de
la canne à
sucre au nord de la Côte d'Ivoire montrent, que sur les
plateaux gravillonnaires les plantes sont surtout attaquées par
Meloidogyne, alors que sur celles situées sur les
zones limono-argileuses en bordure des rivières se sont
les attaques par
Pratylenchus qui sont observées.
Prot et Van Gundy (1981) ont démontré
expérimentalement l'influence de la texture du sol (teneur en argile)
sur le déplacement de Meloidogyne. La texture du sol agit
également sur la répartition d'une même espèce.
Cadet et al. (1994) signalent au sud de la Martinique dans les
vertisols (sols à argile de type smectite) la présence
espèce d'Helicotylenchus, H. retusus ; par contre celle-ci est
absente dans les andosols (sols à minéraux argileux de type
allophane) situés à faible distance, mais on y trouve H.
erythrinae ou H. dihystera. Or, ces espèces ectoparasites,
morphologiquement comparables, sont présentes sur une même plante,
par exemple la tomate, cultivée sur toute l'île.
I.6.2.Influence des facteurs biotiques Matière
organique
La matière organique dans le sol permet la
réduction des nématodes. Lors de sa décomposition, elle
libère certains produits toxiques tels que l'acide butyrique (Jones,
1982). D'après Mohammed et Abdoul, (2000), l'amendement organique
stimule l'activité des micro-organismes du sol qui sont des antagonistes
des nématodes parasites des plantes. Sa décomposition et son
accumulation dans le sol, peut être comme un nématicide car ce
produit et principalement biologique peut provenir des friches et des
déchets agricoles.
L'incorporation de matières organiques (par exemple:
fumier) dans le sol, stimule l'activité microbienne et fournit des
ressources pour des espèces de nématodes opportunistes ; par
conséquence, il ya une diminution rapide de la Indice de Maturité
(IM) suivie par une augmentation progressive au cours de succession
ultérieure (Ferris, Venette et Lau, 1996). Le IM augmente au cours de la
succession et avec la diminution de l'activité microbienne. (Ettema et
Bongers, 1993).
Chapitre II. Donnés bibliographiques sur les
amendements organiques
II.1. Généralités sur les
amendements organiques
Le contrôle biologique des nématodes a
été étudié comme une approche alternative ou
complémentaire à l'intégrité physique ou aux
méthodes chimiques (Weller, 1988).
Parmi ces moyens, les techniques basées sur l'addition
de matière organique au sol ont a été exploré comme
méthode alternative aux moyens chimiques. Il s'agit de débris de
plantes, de cultures, de foin (Mian et Rodriguez Kabana, 1982), de compost de
déchets de crevettes (Dia, 1995), les plantes nématicides, les
déchets protéiques et les résidus végétaux
(Oka, 2010). L'application des amendements organiques est une méthode
traditionnelle afin de contrôler les nématodes phytoparasites
d'une part (Mankau, 1962; Khan et al., 1974 ; Badra et Oteifa, 1979)
et d'autre part améliorer la fertilité et la structure des sols.
Les apports en amendements organiques d'origine animale ou
végétale s'avèrent favorables pour les cultures. Singh et
al. (1966) ont observé que le fumier de vache, le terreau de
feuilles et les tourteaux de ricin, de moutarde diminuent les populations de
Meloidogyne tout en augmentant la croissance de plants et en diminuant
les problèmes de champignons parasitaires. D'après les
mêmes auteurs Singh et al. (1983) les tourteaux
d'oléagineux semblent particulièrement efficaces contre les
nématodes. Ces substances augmentent les phénols et les acides
aminés dans la plante ce qui rebute ces nématodes.
II.2. Différents types d'amendements
organiques
Le terme amendement organique recouvre une très large
gamme d'intrants, ayant des propriétés très variables. Les
amendements organiques sont le plus souvent des produits principalement
composés de résidus de végétaux, fermentés
ou fermentescibles. Mais il existe aussi des amendements organiques avec une
moindre proportion de végétaux, notamment ceux à base de
déjections animales (Janvier, 2007).
Un premier type d'amendement est composé de
déchets organiques. Les fumiers compostés ou non, les lisiers ou
les composts de déchets ménagers appartiennent à cette
catégorie. Ils sont utilisés depuis très longtemps en
agriculture, surtout pour l'entretien du pool de matière organique dans
le sol, mais possèdent aussi un effet bénéfique sur la
stabilité structurale du sol. A noter que l'amendement organique se
distingue de l'engrais organique, qui contient plus d'éléments
fertilisants (Villenave et al., 2007).
Les résidus de cultures est un autre type d'amendement
organique. Ces résidus, incorporés dans le sol, forment un
engrais vert, riche en matière organique fraîche, non
préalablement décomposée ou fermentée. Cette
matière organique peut être beaucoup plus labile et facilement
dégradable que celle des produits compostés, selon la teneur en
cellulose et en lignine du matériel de départ. De nombreux
composés actifs peuvent être produits lors de la
dégradation biologique de ces résidus de culture (Janvier,
2007).
Amendement organique d'origine
végétale
En raison de la conjoncture actuelle, les biopesticides
d'origine botanique sont appelés à un meilleur avenir. La demande
en produits phytosanitaires sans danger, de faible rémanence et
qualifiés de produits verts est présentement en hausse
(Philogene et al., 2005). D'après Ranasingh
(2007), 2121 espèces de plantes possèdent des
propriétés de lutte antiparasitaire. De nombreuses plantes ont
été utilisées comme amendement pour lutter contre les
nématodes dans les expériences à petite échelle,
seuls quelques rapports ont identifié le composé
nématicide de ces plantes (Oka, 2010).
La production de substances nématicides par les
végétaux supérieures est connue depuis très
longtemps. Les données acquises sur le terrain, démontrent
l'efficacité de certains végétaux introduits
traditionnellement dans les assolements, en culture intercalaire ou sous forme
broyats pour lutter contre les nématodes phytoparasites.
Diverses espèces peuvent être utilisé tel
que (Tagetes spp, Crotalaria spectabilis, Chrysanthemums
spp, Allium sativum, Cinnamomum verum « Cannelle
» et Azardiracta indica « Neem ») (Duke,1999 ;Kong et
al.,2007 ;Lee et al,2001 ;Park et al,2005 ; Satti et
al ,2003; Satti et Naser ,2006 ).
Certaines plantes sont utilisées comme engrais vert tel
que la Crotalaire, le Radis fourrager. La Crotalaire constitue un engrais vert
nématicide intéressant (comme c'est une légumineuse, son
enfouissement constitue une fumure azotée non négligeable), Il
faut impérativement l'enfouir pour avoir une action nématicide
(Bertrand et al., 2001).
Des auteurs affirment que la décomposition des engrais
verts, libère dans le sol différent acide gras volatil dont
l'effet nématicide pourrait s'ajouter à celui des
molécules contenues dans les tissus des plantes enfouies.
L'utilisation des résidus de végétaux
comme les grignons d'olive comme biopesticide exprime un décroissement
des maladies causées par les nématodes mais les recherches
restent toujours en voie d'exploitation (Cayuela et al., 2008).
Les déchets d'olive sont connus pour contenir un
certain nombre de substances biologiquement actives. Les
propriétés phytotoxiques et antimicrobiennes de ces
résidus ont été largement étudié et sont
associés à la présence de composés
phénoliques et composés des acides gras libres (Obeid et
al., 2005). Plusieurs chercheurs ont signalé l'inhibition de la
croissance des plantes et des microbes par les phénols à faible
poids moléculaire présents dans les déchets d'olive (Della
Greca et al, 2001 ; Fiorentino et al, 2003 ; Isidori et
al., 2005). Bien que les polyphénols de haut poids
moléculaire comme l'oleuropéine ou des polymères de la
lignine ont également montré activité toxiques (Aziz et
al., 1998 ; Bisignano et al., 1999) ; Hydroxytyrosol a
été identifié comme l'un des majeurs composés
phénoliques naturelles présents dans les déchets d'olive
(Lesage-Meessen et al., 2001; Romero et al., 2002;.
Fiorentino et al., 2003). Toutefois, de nombreux composés
restent non identifiés et il y'a encore une controverse sur le type et
le nombre exactes des composants phytotoxique de grignons d'olive. Cependant,
certains chercheurs ont constaté la toxicité des grignons
d'olive, même après l'extraction totale des phénols, ce qui
suggère que autres produits chimiques contribuent à la
toxicité globale (Capasso et al., 1992; Greco et al.,
2006).
Les propriétés phytotoxiques et antimicrobiennes
des déchets d'olive ont souvent été la cause limitant
utilisation de ces matériaux. Ainsi, plusieurs méthodes ont
été développées ces dernières années
afin de dégrader les phénols dans les résidus liquides et
solides des olives (Martirani et al., 1996; Linares et al.,
2003; Greco et al., 2006).
Les déchets d'olive pourraient être
utilisés comme bio-pesticide vu les composés naturels qu'ils
contiennent qui pourraient agir contre divers champignons, mauvaises herbes et
les nématodes (Cayuela et al., 2008).
II.3. Importance des amendements organiques
II.3.I. Effet sur le sol, la culture et les
microorganismes
La matière organique apportée sert de base
trophique à la communauté microbienne du sol. Elle entraîne
le plus souvent une augmentation de l'activité et de la densité
microbienne. Ainsi, l'environnement du sol devient un milieu dans lequel la
compétition entre les microorganismes est forte (Paulitz, 1989),
concourant au phénomène de résistance
générale des sols (Aryantha et al., 2000 ; Scheuerell et
al., 2005 ; Termorshuizen et al., 2006).
Outre activation de la résistance
générale régit par l'amendement, des mécanismes de
résistance spécifique peuvent aussi se mettre en place suite
à ces apports. Notamment, lorsqu'il s'agit d'un compost
additionné de microorganismes antagonistes. Ceux-ci peuvent agir par
antibiose (Fravel, 1988) ou parasitisme (Hoitink et Boehm, 1999). Comme pour la
résistance naturelle des sols, l'effet suppressif des composts peut bien
sûr provenir d'une combinaison de modes d'action (Pitt et al.,
1998).
Les amendements organiques peuvent modifier les
propriétés physiques du sol, qui à leur tour peuvent
affecter négativement les comportements des nématodes tels que
l'éclosion, les mouvements et la survie. Ces changements des sols
comprennent de pH, la salinité et la conductivité
électrique « CE », le dioxyde de carbone et les concentrations
d'oxygène, (Oka, 2010).
Selon (Villenave et al., 2007), l'apport de compost
pendant 6 années successives a eu un effet positif sur les
caractéristiques physico-chimiques des sols. Les teneurs en
matière organique, en bases échangeables et en phosphore
assimilable sont plus élevées dans les parcelles à apport
de compost.
De nombreuses études ont été
menées, concluant le plus souvent de l'effet bénéfique des
amendements organiques sur la santé des plantes. Plusieurs
mécanismes expliquent ces effets bénéfiques (De Clercq et
al., 2004). Les composts peuvent permettre l'activation des
mécanismes de défense de la plante (Vallad et al.,
2003).
La préparation du sol (et éventuellement reprise
du travail) et l'apport de compost permettent d'améliorer le statut
organique du sol par rapport aux autres modes de conduite favorisant, en
conséquence, un meilleur développement de la plante
cultivée. A titre d'exemple, la production végétale de
maïs est plus élevée pour les traitements ayant reçu
du compost que pour les traitements avec travail du sol mais sans apport de
compost (Villenave et al., 2007).
La production de composés toxiques dans le sol peut
aussi être à l'origine de la réduction des populations
d'agents pathogènes (Coventry et al., 2006). Lors de la
dégradation des amendements riches en azote, en fonction des
caractéristiques physico-chimiques du sol, il y a production
d'ammoniaque, toxique pour de nombreux organismes et pour certaines formes de
conservation des agents pathogènes (Bailey et Lazarovits, 2003). Ainsi,
Tenuta et Lazarovits (2004) ont montré que les microsclérotes
peuvent être détruits par l'ammoniaque et l'acide nitreux.
Cependant, cette activité est très fortement dépendante du
pH du sol.
II.3.2. Effet sur les nématodes
Le travail du sol, ainsi que l'apport des amendements
organiques peuvent avoir une action significative sur la dynamique des
populations de nématodes. Ces traitements induisent des modifications de
la structure spécifique des peuplements de nématodes
phytoparasites en augmentant l'abondance d'une espèce peu
pathogène qui pourrait limiter les dégâts dus aux
nématodes (Villenave et al., 1998).
L'accroissement de l'activité biologique est plus forte
avec un amendement frais que composté. Pour lutter contre les
nématodes, l'apport de fumier brut est plus efficace que l'apport de ce
même fumier composté, car pendant la décomposition du
fumier, dans le sol, il y a production de composés azotés
nématicides (Nahar et al., 2006). L'effet suppressif du compost
augmente généralement avec la quantité appliquée
(Noble et Coventry, 2005).
Les cultures de couverture sont des amendements organiques
très utilisés pour la fertilité du sol et le
contrôle des maladies. McSorley et Frederick (1999) signalent que
l'incorporation des résidus végétaux augmente
généralement le nombre de nématodes libres. Le type de
résidus végétaux incorporés au sol agit
spécifiquement sur le développement des organismes antagonistes,
comme les nématodes prédateurs ou les champignons parasites. Par
exemple Wang et al., (2001) rapportent que l'incorporation de
crotalaire (Crotalaria juncea) au sol a augmenté
développement des champignons prédateurs de nématodes et
des champignons parasites des oeufs de Rotylenchulus reniformis. Elle
favorise également la pullulation des nématodes
bactérivores plus que les amendements aux Brassica napus ou
Tagetes erecta.
Une augmentation du nombre de nématodes
prédateurs est souvent observée après amendement des sols
avec des résidus végétaux, probablement en raison de la
prolifération des nématodes libres comme des proies. En effet,
l'application de poudre de feuilles de neem ou de la sciure a augmenté
le nombre de prédateurs et de nématodes libres dans le sol,
tandis les nématodes phytoparasites ont diminué (Akhtar,
1998).
Chapitre III : Description de la plante hôte «
Tomate » III.1. Généralités sur la tomate
maraichère
La tomate sauvage est d'origine américaine, en
particulier d'Amérique centrale et Amérique du Sud (Mexique,
Pérou, Equateur et Bolivie) (Kolev, 1976). La tomate est une plante
annuelle de la famille des Solanacées, dont le fruit est une baie. Cette
dernière est rouge, parfois jaune ou orangée, de forme ronde ou
plus ou moins allongée, lisse ou creusée de sillons. Les fruits
sont de grosses baies, toujours charnues, tantôt lisses, tantôt
côtelées, qui contiennent, noyées dans la pulpe une grande
quantité de petites graines blanches, plates, réniformes,
feutrées lorsqu'elles sont sèches. (Chaux et Foury, 1994 ;
Shankara et al 2005).

Fig.5 : Fruits de tomate Fig.6:
Feuilles de tomate

Fig.7: Fleur de tomate
III.2. Taxonomie :
D'après Arbaoui (1997), la tomate est classée dans
:
Règne Végétal
Groupe Eucaryote
Embranchement Spermaphyte
Sous embranchement Angiosperme
Classe Dicotylédone
Sous-classe Gamopétale
Ordre Polémoniacée
Famille Solanacée
Genre Lycopersicum
Espèce Lycopersicum
esculentum
III.3. Importance de la tomate en Algérie
La culture de la tomate occupe une place
prépondérante dans l'économie agricole algérienne.
Près de 33 000 ha sont consacrés annuellement à la culture
de tomate (maraîchère et industrielle), donnant une production
moyenne de 11 millions de quintaux et des rendements moyens d'environ 311 Qx/ha
(Madr, 2009). Ces derniers demeurent faibles et assez éloignés de
ceux enregistrés dans d'autres pays du bassin
méditerranéen (Tunisie, Maroc, Espagne, France, Italie)
producteurs de tomate, où les rendements varient entre 350 Qx/ha
à 1500 Qx/ha (FAO, 2008).
III.4. Types de croissance et variétés de
tomate maraichère existantes en Algérie
Les variétés de tomate sont très
nombreuses. A cet effet, ces dernières peuvent être
classées selon leur croissance qui peut être du type
indéterminé ou du type déterminé. Les
variétés de tomate utilisées pour la production en frais
sont principalement de type indéterminé. La plante ne cesse de
croitre en hauteur jusqu'à épuisement de toutes les
réserves (Snoussi, 2010).
L'intervention de l'agronome est parfois nécessaire
pour limiter le nombre de bouquets floraux et ce dans le but de l'obtention de
fruits de gros calibres. Il est
recommandé de laisser deux feuilles au-dessus du
bouquet choisi et de pratiquer un étêtage afin de limiter la
croissance des plantes. Parmi ce type de croissance, il existe : les
variétés fixées dont les caractéristiques
génotypiques et phénotypiques se transmettent pour les
générations descendantes où on peut citer les
variétés les plus utilisées en Algérie telles que
la Marmande et la Saint Pierre (Snoussi, 2010).
III.5. Exigence de la culture de tomate
III.5.1. Type de sol
La tomate n'a pas d'exigence particulière en
matière de sol. Elle s'adapte bien dans les sols profonds, meubles, bien
aérés et bien drainés (Snoussi, 2010)
Une texture sablonneuse ou sablo-limoneuse est
préférable (Chibane, 1999). Aussi, selon Verolet 2001
l'espèce de tomate est adaptée à de nombreux types de sol
tant sur le plan de la texture que vis-à-vis du pH. Les sols
sablo-argileux, limono-sableux ou limoneux, drainants à pH compris entre
6 et 7 semblent les plus conseillés pour exprimer au mieux le potentiel
de la culture.
III.5.2. Irrigation
Les besoins en eau de la tomate se situent entre 4000 et 5000
m3/Ha. Il faux maintenir la plante à la limite de ses
besoins, toute irrégularité entraîne au moment de la
maturation des éclatements de fruits (Chaux, 1972).
III.6. Mode de conduite
III.6.1. Semis et repiquage
L'entretien et la surveillance de la spéculation
végétale sont des opérations peu difficiles mais demandent
un minimum d'expérience dès le semis. Il est en effet très
important à ce stade de semis d'éviter les alternances
sécheresse, humidité qui, outre un ralentissement de croissance,
offrent des conditions très favorables au développement de
certaines maladies (fonte de semis). Il peut même dans une serre
pratiquer des bassinages si l'humidité relative est trop faible. Le
repiquage ou transplantation des jeunes plantules de la pépinière
en place définitive s'effectue après un maximum de 35 jours de
pépinière, car plus le plant est jeune et plus la
reprise est bonne. Le repiquage est réalisé
manuellement, mais l'opération peur être mécanisée
dès que la culture et la grosseur du plant le permettent, (Snoussi,
2010) L'amélioration des techniques de semis permet d'entreprendre un
semis direct en motte ou en godet très clair supprimant ainsi le
repiquage à racine nue. « Le repiquage effectué sera en
motte » L'arrosage est indispensable après le repiquage,
néanmoins il faut veiller à ce que les racines trouvent un milieu
humide sans excès qui peut entrainer la pourriture des racines. Les
besoins en eau deviennent importants à partir du stade
4ème feuille, (Snoussi, 2010).
III.6.2. Eclaircissage
Cette opération se pratique uniquement sur les semis en
place. Elle consiste à supprimer les plants en excès de
manière à assurer un développement correct de la
végétation, (Snoussi, 2010).
III.6.3. Eclaircissage des fruits
C'est une opération qui consiste à supprimer les
fruits malades, mal développés et ce afin d'éviter des
contaminations et permettre d'améliorer le calibre des fruits produits,
(Snoussi, 2010).
III.6.4. Effeuillage
Cette opération a été pratiquée au
moment où les fruits commencent à changer de couleur (changement
qui indique que la maturité approche). Les feuilles qui cachent les
grappes de fruits sont enlevées pour permettre à ceux-ci de se
colorer plus facilement. Aussi, cette opération peut concerner les
feuilles de la base qui touchent le sol et peut donc constituer des foyers de
contaminations au contact de l'eau et du sol. Cette opération peut
également permettre une bonne aération de la culture, (Snoussi,
2010).
III.6.5. Tuteurage
Les tiges de la tomate demandent à être
soutenues, sinon elles risquent d'être brisées par le vent pour la
culture de saison et d'arrière saison. Il est plus pratique de suspendre
de la ficelle au niveau de chaque plante accrochée à du fil de
fer. Les tiges sont enroulées sur cette ficelle au fur et à
mesure de leur accroissement (Snoussi, 2010).
III.6.6. Taille
Les pieds de tomate abandonnés à leur
végétation fournissent généralement en abondance,
mais tardivement des petits fruits pour obtenir de beaux produits
mûrissant hâtivement, il est nécessaire de tailler. Les
systèmes de taille sont variables selon les variétés et
selon encore qu'on vise à une production rapide ou à un rendement
échelonné, (Snoussi, 2010).
III.6.7. Aération
Elle a pour objectif de renouveler l'air de la serre,
d'abaisser la température et le degré hygrométrique quand
cela est nécessaire. Ceci permettra d'éliminer les excès
d'humidité et de chaleur qui favorisent de développement des
maladies cryptogamiques, (Snoussi, 2010).
III.6.8. Gestion des mauvaises herbes
Pour une gestion efficace des mauvaises herbes la pratique de
binage est indispensable car elle permet de briser la croûte du sol
(permettre donc une bonne aération du sol) et de supprimer les mauvaises
herbes qui se développent autour du plant (Snoussi, 2010).
De nombreux herbicides sélectifs s'utilisent en culture
maraichère .Dans chaque cas, il faut s'en tenir strictement aux
indications des fabricants , traiter avec la pression des pulvérisateurs
réduite et veiller particulièrement au rinçage des
appareil de traitement .
III.6.9. Récolte
Pour permettre aux fruits de tomate de supporter
convenablement les manipulations de conditionnement, d'emballage et aussi les
transports, ces derniers doivent être récoltés au point de
maturation de chacun des fruits et ce, au fur et à mesure des besoins si
on les consomme immédiatement ; quand ils sont rouges, mais toujours
fermes.
Chapitre IV : Présentation de la région
d'étude "D'Oued Righ" IV.1-La situation géographique
La vallée d'Oued Righ est une entité
économique bien précise, puisque l'on désigne sous ce
terme, une vallée de palmeraies constituée d'un chapelet de
47oasis ; qui regroupe plus de 35 villages, se positionnant au Nord- Est du
Sahara algérien.
La vallée s'étend sur une longueur de 150 Km et
une largeur de 20 á 30 Km. Elle est comprise entre les latitudes Nord de
32°54' et 34°9'. Elle est caractérisée par sa grande
dimension et la concentration de la majeure partie de sa population dans les
oasis. Elle est estimée à environ 357.855 habitants (Anonyme,
2005b). Le palmier dattier constitue la culture dominante dans la
vallée. Elle s'étend sur une superficie de plus de 28.000 ha avec
5.057513 palmiers (Anonyme, 2005c).
Elle débute au nord d'Oum EL Thiour à 110 Km au
Sud-Est de Biskra et se termine au sud avec le village El Goug á 150 Km.
Oued Righ se devise en deux grandes parties principales :
Partie nord: Regroupe les daïras d'El M'ghaier et de
Djamâa qui appartiennent á la wilaya d'El Oued.
Partie sud: Représenté par Touggourt,
appartenant à la wilaya d'Ouargla (Anonyme, 1999a).
La ville de Touggourt fut capitale de l'Oued Righ, (Benlamoudi et
Bouzenada, 1979).
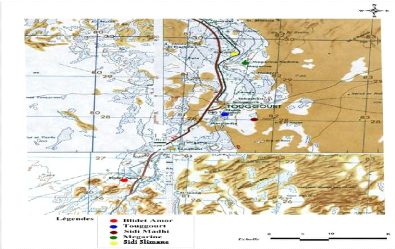
Fig.8 : Carte géographique
représentant la vallée d'Oued Righ
IV.2-Facteurs édaphiques
Sous le terme facteurs édaphiques nous allons
étudier les facteurs physiques de la région (le sol, le relief
géomorphologie et l'hydrologie).
IV.2.1- Géologie de la région
La vallée d'Oued Righ est un large fossé de
direction Sud-Nord prenant son origine au Sud de la palmeraie d'El-Goug et
débouchant sur le chott Merouane. La pente générale est de
l'ordre de 10/00.
La dénivellation entre le haut et le bas du paysage est
de quelques mètres seulement, les pentes sont faibles et le relief est
peu marqué reposant sur les formations Mio-pliocènes et
Eocènes qui s'enfoncent progressivement vers le Nord (Rouvillois, 1975),
on trouve sur les parties hautes de la vallée un niveau quaternaire
ancien à encroutement gypso-calcaire, recouvert par endroits de
formations dunaires ; le fond de la vallée est constituée de
dépôts sablo-argileux.
Tout au long de la vallée, les Sebkhas et les massifs
dunaires alternent avec les fonds sur lesquelles se sont installées les
cultures irriguées et les centres de peuplement (Rouvillois, 1975).
IV.2.2- Caractéristiques pédologiques
Les sols de la vallée de l'Oued Righ sont d'origine
Allu-colluviale à prédominance sableux, ils sont
caractérisés par un faible taux de matière organique, un
pH alcalin, une bonne aération et une faible activité biologique
(Halilat, 1993) et d'après Toutain (1979), les sols sahariens sont en
général pourvus en ca++, Mg++ et K+ ainsi
que les oligo-éléments essentiels.
La plupart de ces sols sont salins à cause du mauvais
lessivage des eaux salées de la remontée des eaux de la nappe
phréatique (Kafi et al, 1977 in Belaroussi, 1994). Ce sont des
sols généralement meubles et bien aérés en surface
(Serrai, 2009). IV.2.3 -Hydrologie de la région
La région d'Oued Righ est très riche en
ressources hydriques, malgré la rareté des précipitations.
Elle possède des ressources hydriques souterraines
représentées essentiellement par les nappes.
IV.3-Les facteurs climatiques
Le climat régional de la vallée de l'Oued Righ
est typiquement saharien. Il est très chaud en été,
très froid et sec en hiver. Il est caractérisé par des
faibles précipitations, de fréquents vents de sable, une
évaporation intense, de fortes températures avec des
écarts de température très importants, une
luminosité importante et une humidité de l'air relativement
faible. Tous ces facteurs conduisent à une forte aridité
(Toutain, 1979).
IV.3.1. Températures
Nous constatons au niveau cette région que les
données de l'année (2009), que la température moyenne du
mois le plus froid (Janvier) est de 6,8°C, celle du mois le plus chaud
(juillet) et de 44,6°C. La région est caractérisée
par une température moyenne minimale de 12,3 °C au mois de
janvier.
IV.3.2. Pluviométrie et précipitation
Les précipitations sont en effet très
irrégulières et très faibles dans cette région.
Toutefois, le mois le plus arrosé est Janvier avec une
précipitation de 54,1mm. IV.3.3. Durée
d'insolation:
La région de Touggourt reçoit une
quantité de la lumière solaire relativement très forte. Le
maximum étant enregistré au mois d'Août, avec une
durée de 344 heures d'insolation et le minimum au mois de Janvier avec
une durée de 196 heures, avec une moyenne annuelle de 285,6 heures.
IV.3.4. Vents
Les vents de sable sont relativement fréquents dans la
région, constituant un handicap pour l'activité agricole,
notamment la mise en valeur des terres (Bneder, 1992 in Zergoun, 1997). Ils
s'étalent sur toute l'année, avec une vitesse moyenne annuelle de
3,08 m/s et une vitesse maximale au mois de Mai de 5 m/s et le minimum en
Décembre est de 1,4 m/s (Anonyme, 2009). Ils sont plus importants
encore, durant la période allant du mois de mars au mois de mai.
Selon Dubief (1963), dans la région d'Ouargla, les
vents soufflent du Nord-est et du Sud. En hiver, on a les vents d'Ouest, au
printemps, les verts du Nord-est et de l'Ouest qui dominent ; en
été, ils soufflent du Nord-Est et en automne du Nord-est et du
Sud-ouest.
IV.3.5. Humidité
L'humidité relative moyenne annuelle pendant
l'année d'étude 2009 est d'environ 44,4%. Elle atteint son
maximum, pendant le mois de janvier 70% et son minimum 25%, pendant le mois de
juillet.
IV.3.6. Evaporation:
L'évaporation moyenne annuelle mesurée est de
l'ordre de 201,5 mm. Les mois présentant un maximum d'évaporation
sont: juin, juillet et août avec 45% du total annuel.
IV.3.7.Synthèse climatique de la région de
Touggourt
La synthèse des données climatiques est
représentée par le diagramme ombrothermique de Gaussen et par le
climagramme d'Emberger.
La classification écologique des climats est faite en
utilisant essentiellement les deux facteurs les plus importants et les mieux
connus: la température et la pluviosité (Dajoz, 1971).
IV.3.7.1- Diagramme ombrothermique de Gaussen dans la
région étudiée de Touggourt
Les analyses des données climatiques
représentent la synthèse climatique sur 10 ans (2000-2009)
(Anonyme, 2009). Le diagramme ombrothermique de la région de Touggourt
au cours de cette période montre la présence d'une longue
période sèche durant presque toute l'année avec un maximum
au mois de Juillet (43,2°C).
IV.3.7.2- Climagramme d'Emberger appliqué au
niveau de la région de Touggourt
Le quotient pluviométrique est l'indice d'Emberger
permettant d'identifier l'étage bioclimatique de la région
d'étude. La température et les précipitations sont les
facteurs essentiels pour donner ce quotient. Cet indice n'est vraiment
établi que pour la région méditerranéenne (Faurie
et al., 1998).
Le quotient pluviométrique d'Emberger est
déterminé selon la formule suivante (Stewart, 1969).
Le quotient Q de la région d'étude est à
7,91, calculer à partir des données climatiques obtenues durant
une période s'étalant sur 10 ans de 2000 jusqu'en 2009. En
rapportant cette valeur sur le climagramme d'Emberger, il est à
constater que la région de Touggourt se situe dans l'étage
bioclimatique saharien à hivers chaud.

CHAPITRE I
MATERIELS ET MÉTHODES
C/5/AP Ti1LE
~EiFFELS
Chapitre I : Matériels et méthodes
I.1. Description des amendements utilisés I.1.1.
Les grignons d'olives
Grignon d'olive sont des résidus végétaux
issu après extraction de l'huile d'olive. Il renferme une grande partie
de la matière sèche de l'olive composée de peau, pulpe,
petits morceaux de noyau et une certaine proportion d'eau de
végétation qui contient à son tour les composants
hydrosolubles de l'olive (Anonyme 2, 2002).
I.1.2. Caractéristiques chimiques
La composition chimique des grignons d'olive varie selon le
stade de maturité des olives, le procédé d'extraction de
l'huile et l'épuisement par les solvants.
Les teneurs en matières grasses et en cellulose brute
présentent les variations, les procédés technologiques
modifient ces proportions relatives des différents composants des
grignons (épicarpe, mésocarpe, endocarpe et amendons) qui ont des
compositions chimiques différentes. La teneur en matières grasses
est relativement élevée. L'épuisement, opération
économiquement indispensable permet d'avoir un produit dont la teneur
oscille entre 3 et 4% de la matière sèche (MS).
Les proportions en cellulose brute sont élevées
(32 à 47%) et le tamisage les réduit à des valeurs de 14
à 26%. Une analyse plus poussée de la fraction fibreuse a permet
de constater que les grignons ont des teneurs élevées en
constituants pariétaux et surtout en lignine (acid detergent lignin) qui
monte jusqu'à 30% du total des fibres. (Nefzaoui, 1983 ; Nefzaoui, 1985
; Nefzaoui et Vanbelle, 1986 ; Nefzaoui et Zidani, 1987).
La teneur en cendres est normalement faible (3 à 5%).
Les teneurs élevées qu'on rencontre sont dues à l'absence
de lavage et à la présence des olives ramassées du sol.
Les matières azotées varient moins fortement, elles sont en
moyenne de l'ordre de 10%.
Les substances phénoliques : l'olive contient des
quantités élevées de polyphénols (0,3 à
5% de la MS). Ce sont surtout des orthophénols,
l'oleiropéine. Cependant le glucoside amer, est le composé
phénolique le plus abondant et le plus caractéristique des
oléagineux (Vazquez Roncero et al., 1970).
Depuis longtemps on a cru que la valeur nutritive
limitée des grignons serait due à la présence des
substances phénoliques (Thériez et Boule, 1970). Les dosages
réalisés par Nefzaoui (1983, 1985, 1987) ont montré que
ces teneurs ne dépassent guère le 1% de la MS.
I.2. Matériels
Le travail expérimental est réalisé en
fonctions des étapes suivantes : I.2.1. Origine les amendements
organiques utilisés
Le fumier testé d'origine animal (bovin et ovin),
provient de la palmeraie à Touggourt.
Les grignons d'olive sont collectés de la huilerai
(Maasra) à Sidi Abd El Kader, Blida. Ces dernières ont
été étalées sur un papier journal et
séchées à l'ombre pendant 5 jours, puis sont
rangées dans un sac en papier jusqu'au moment de son utilisation.
I.3. Méthodologie
I.3.1. Préparation de la parcelle de travail
Notre étude s'est déroulée au niveau
d'une parcelle dans la palmeraie de la région de Touggourt. La parcelle
a été labourée le (01 mars 2011), une partie de celle-ci a
été partagée en 4 blocs destinés aux traitements
(fumier, grignon d'olive, un traitement chimique « l'Oxamyl » et un
bloc témoin). Chaque bloc a une superficie de (4.88 m2). Nous
avons réparti chaque bloc en 2 lignes qui vont recevoir les traitements.
Les apports organiques ont été réalisés le (5 mars
2011). Ces amendements ont été utilisés d'une
manière localisés. Pour cela des trous au niveau des lignes de
chaque bloc ont été creusé à l'aide d'une binette
à une profondeur de (30cm). Dans chaque trou nous déposons (10 g)
de chaque type d'amendement, ces trous sont ensuite recouvert de terre et
marqué à l'aide d'un petit bâton. On les laisse agir ainsi
pendant 10 jours avant la transplantation des plants de la tomate.
Les plants de tomate de 10 à 15 cm de hauteur sont
transplantés dans tous les blocs le (15 mars). Chaque bloc comprend 8
plants distants l'un de l'autre de (30cm), la distance entre les lignes est de
(70cm).
Pour comparer nos résultats nous avons
préparé un bloc témoin négatif sans aucun
traitement et un témoin positif au traitement chimique. Ce dernier a
été apporté trois jours avant la transplantation de la
tomate (12 mars 2011).
Des travaux d'entretien ont été
réalisés au niveau des blocs, le désherbage, tuteurage.
I.3.3. Prélèvement des
échantillons.
Des prélèvements sont effectués tous les
15 jours de la période du 05 Mars au 15 juin. Les échantillons au
niveau de chaque bloc sont réalisés à l'aide d'une binette
au niveau de cinq plants choisi au hasard, des prélèvements
élémentaires de sol de 200 à 250g chacun sont
récoltés autour de la rhizosphère des plants à une
profondeur de 30 cm. Ces derniers sont mis dans des sacs en plastique
référenciés et conservés au froid jusqu'au moment
de l'extraction.
· Premier échantillonnage de sol est
réalisé avant traitement de chaque bloc (sol nu) le 5 mars
2011.
· Le deuxième échantillonnage est fait
avant la transplantation, autour des points traités (15 mars).
|
·
|
L'échantillonnage après transplantation, s'est
déroulé les 15 jours du (30mars au 15 juin).
|
.
I.3.4. Extraction des nématodes du sol
La méthode d'extraction utilisée est la
technique modifiée des filtres de Baermann (Hooper, 1986). Pour cela on
prépare les tamis en plastique avec des filtres Kleenex
humidifiés. On pèse 50g de sol après avoir bien
homogénéisé le sol échantillonné au niveau
de chaque bloc sur un papier journal. Deux répétitions (50 g x 2)
sont réalisées pour chaque bloc. Les deux échantillons
sont déposé sur les
tamis préparés puis placés dans les
boites de Pétri contenant de l'eau
jusqu'affleurement de la surface
du tamis (Fig.9). On laisse la diffusion pendant 3 jours. Passer ce
délai, le contenu de chaque boite de Pétri est
récupéré dans des tube à essai de 100 ml, puis
laissé se décanté pendant 1 heure. Ensuite il sera
réajusté à la graduation adéquate (25, 50,75 ou
100ml) en fonction de la densité des nématodes dans le tube.

Fig.9: Dispositif d'extraction des nématodes du
sol.
I.3.5. Dénombrement et identification des taxons
Pour évaluer la densité totale et celles des
taxons dans nos échantillons. Nous prélevons 5 ml après
homogénéisation des tubes. Ils sont déposés dans la
cellule de comptage pour le dénombrement et l'identification
morphologique basée sur l'observation de certains caractères
discriminants (la longueur et la forme du stylet, la forme de la tête, de
la queue, la longueur du corps, la disposition de la glande oesophagienne par
rapport à l'intestin) sous loupe binoculaire en basant sur la clé
d'identification de (Jaccob et Middepiaats, 1988).
Les populations de nématodes du sol sont
exprimées en nombre de nématode par 50 g de sol.
I.3.5.1. L'effet des traitements sur estimation du taux
d'infestation des racines par les larves (L2) de
Meloidogyne.
Pour évaluer l'effet des traitements sur le taux
d'infestation des racines par les Meloidogyne nous avons
réalisé le 15 juin déraciné 4 plants entiers de
tomate au hasard de chaque bloc. Ces derniers sont nettoyés à
l'eau pour les débarrassés des restes de particules de sol.
Après cette opération ils sont asséchés au papier
absorbant, puis sont pesés, ensuite ; elles sont examinées sous
loupe binoculaire (x10) afin de dénombrer les galles sur tout le
système racinaire (Fig.10).
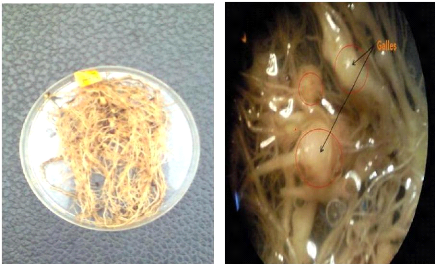
Fig.10 : Estimation du taux d'infestation des racines par
les larves (L2)
(Grx10).
I.3.5.2. Estimation du taux de développement des
larves (L2) en femelles
Le dénombrement des femelles est réalisé
à partir de 2 g de racines pour les différents traitements et
répétitions. Les racines sont dilacérées au niveau
de 10 galles choisi au hasard sous loupe binoculaire par forceps à
l'aide de deux aiguilles entomologique et les femelles sont extraites et
comptées (Fig.11).
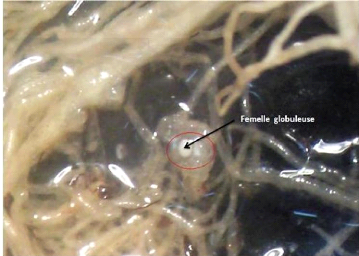
Fig.11: Dénombrement des femelles de
Meloidogyne au niveau des galles.
(Grx10).
I.4. Exploitation des résultats
Les données recueillies sur les populations des
nématodes recensées sont analysées afin d'émaner
les caractéristiques majeurs. Pour cela nous avons fait appel à
l'analyse de variance model « G.L.M > (Modèle Linéaire
Global) avec le SYSTAT VERS. 12, SPSS 2009) et l'analyse multivariée
« ACP > avec le logiciel PAST - PAlaeontological STatistics, ver.
1.81.
I.4.1. L'analyse multivariée
Les corrélations existantes entre la répartition
des nématodes rencontrés dans les sites d'étude et des
nématodes phytophages sur la culture pratiquée (tomate) ont mises
en évidence par l'analyse multivariée du type (DCA) et (ACP). Le
principe de cette analyse est de représenter un phénomène
multidimensionnel par un graphique à deux ou plusieurs dimensions. Ce
test permet de résumer la plus grande variabilité des
nématodes quantifiées pour un nombre plus réduit de
variables appelées axes factoriels qui ont des coordonnées
comprises entre - 1 et + 1 et appartiennent à un cercle des
corrélations. L'interprétation se fait à partir de
l'examen du cercle des
corrélations et de la position du statut des variables
sur les axes factoriels (Phillippeau, 1986).
L'hypothèse d'égalité de la variation
dans les stations est testée par le modèle de la distance
euclidienne à un facteur contrôlé par le logiciel PAST -
PAlaeontological STatistics, ver. 1.81.
I.4.2. Analyses de variance (SYSTAT vers. 12, SPSS
2009)
Lorsque le problème est de savoir si la moyenne d'une
variable quantitative varie significativement selon les conditions (classes de
précipitations, classes d'altitude, type de végétation,
présence-absence de mauvaises herbes, etc....), il est
préconisé de réaliser une analyse de variance. Dans les
conditions paramétriques (ANOVA pour ANalysis Of Variance), la
distribution de la variable quantitative doit être normale. Dans certains
cas, une transformation logarithmique a été nécessaire
afin de normaliser cette distribution.
Dans les cas ou plusieurs facteurs sont en jeu, il peut
arriver que toutes les interactions entre facteurs ne soient pas pertinentes
à tester. Nous avons alors utilisé le modèle
linéaire global (G.L.M). Par exemple, si on désire connaitre
l'effet des facteurs A, B et C et seulement l'interaction entre A et C, il
suffit de sélectionner explicitement ces 4 catégories.
CHAP I TRE II R.
RÉSULTATS ET DISCUSSION
C/YAPIT[iE\\
~ri!/LTATS ET O\SC\~~S\®~-_
3- Nématodes fungivores (Aphelenchus,
Ditylenchus)
Chapitre II : Résultats et Discussion
II.1. Inventaire de la communauté de
nématodes rencontrés dans la parcelle d'étude sur cultures
maraîchères.
Notre travail a été réalisé dans
une parcelle au niveau d'une palmeraie de la région de Touggourt. Les
échantillons ont porté sur des prélèvements de sol
dans la rhizosphère de la tomate dans la station prospectée.
Après les analyses nématologique des
échantillons de sol (la population initiale), nous avons
identifié 16 taxons de nématodes. Ils sont
représentés par les genres
Ditylenchus, Aphelenchus, Psilenchus, Pratylenchus,
Scutellonema,
Tylenchorhynchus, Meloidogyne, Tylenchus, Trophurus,
Pratylenchoides, Xiphinema, Paratrichodorus, Mononchus, Coslenchus, Dorylaimus
et Ecumenicus et des espèces des nématodes non
identifiés pour la plupart des bactérivores classés dans
le groupe des nématodes libres (groupe 1).
En fonction de leur régime alimentaire ces
nématodes sont distribués en quatre groupes trophiques (Tableau
globale 1, annexe).
2-Nématodes phytophages (Ditylenchus, Pratylenchus,
Scutellonema, Meloidogyne, Tylenchorhynchus, Xiphinema, Paratrichodorus,
Psilenchus, Trophurus, Tylenchus, Coslenchus et
Pratylenchoides).
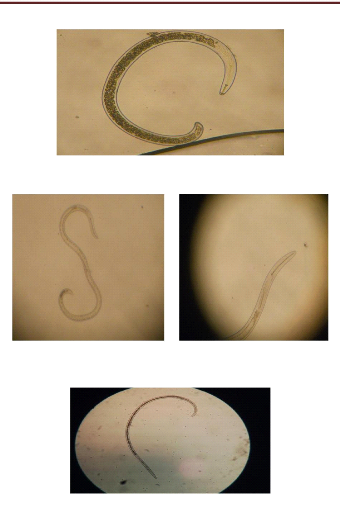
4- Nématodes prédateurs-omnivores (Mononchus,
Dorylaimus et Ecumenicus)
Fig.12 : Morphologie de Scutelonema
G(x400) (Bellahammou, 2011)
Fig.13 : Morphologie de Xiphinema
G(x400) Fig.14: Partie antérieure de Xiphinema
G(x400)
(Bellahammou, 2011)
Fig.15: Morphologie de femelle de Xiphinema
G(x400)
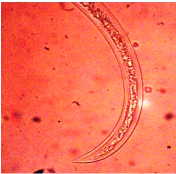
Fig.16 : Partie postérieure de
Xiphinema G(x400)
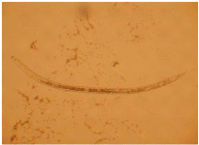
Fig.17: Morphologie de Pratylenchus
G(x400)
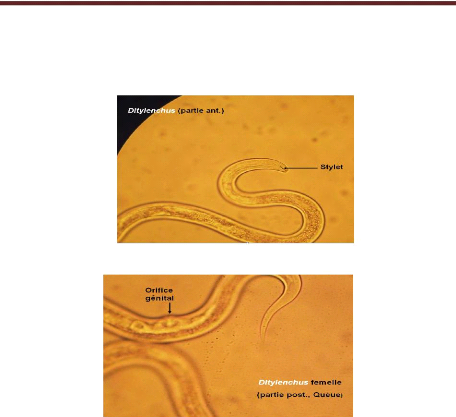
Fig.18: Partie antérieure de
Ditylenchus G(x400)
Fig.19: Partie postérieure de femelle
Ditylenchus G(x400)
Fig.20: Partie antérieure de Dorylaimus
G(x400) Fig.21: Partie postérieure de
Dorylaimus
G(x400)
II.2. Répartition temporelle de la densité
moyenne globale des nématodes (N/50g de sol) en fonction des
traitements.
Les résultats représentés par la figure
22, montrent en général que la densité moyenne globale des
nématodes varie en fonction du temps et des traitements apportés.
Les densités moyennes les plus élevées sont
enregistrées aux temps T1 (15 Mars) après l'application des
traitements fumier (868 N/50g de sol) et grignon d'olive (672N/50g de sol).
Alors que nous avons noté une nette diminution après traitement
au Vydate (47N/50 g de sol).
Pour les autres prélèvements de T4 (1Mai)
à T7 (15 juin), les densités globales moyennes des
nématodes sont faibles pour les trois traitements apportés.
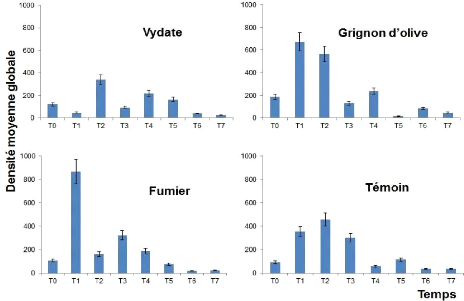
Fig.22: Distribution temporelle des densités
moyennes globales des nématodes en
fonction des
traitements
T0= 5 mars (sol nu avant traitement) ;
T1=15mars (transplantation); T2=30mars:
T3=14avril ; T4=01 mai ;
T5=15 mai ; T6=01juin ;
T7=15 juin
N/50g de sol : Nématodes par 50g de
sol
Pour évaluer l'effet des traitements sur les variations
temporelles de la densité globale des nématodes, nous avons
réalisé l'analyse de la variance modèle (G.L.M.). Le
tableau (2) révèle une différence très hautement
significative dans le temps (P=0.000 ; p < 0.05). Par contre, elle est non
significative entre les traitements (P=0,404 ; p >0.05).
Tableau 2: Modèle G.L.M. appliqué
à la variation temporelle des nématodes en fonction des
traitements.
|
Facteurs
|
Somme des carrés
|
DDL
|
Moyens carrés
|
F- ratio
|
P
|
|
Traitements
|
114866.187
|
3
|
38288.729
|
0.990
|
0.404
|
|
Temps
|
1467070.938
|
7
|
209581.562
|
5.422
|
0.000
|
|
Erreur
|
2048800.312
|
53
|
38656.610
|
|
|
L'analyse de la figure 23, confirme la variation temporelle
des populations de nématodes. Les densités moyennes les plus
élevées sont enregistrées en T1 et T2 (15 et 30 mars),
notamment après apport du fumier et des grignons d'olives. Les
abondances globales moyennes les plus faibles plus faibles sont
signalées en T5, T6 et T7 (mai et juin).
En ce qui concerne les variations des densités de
nématodes en fonction des traitements l'analyse révèle que
les populations nématologiques les plus importantes sont
observées avec le traitement au grignon d'olive, les plus faibles sont
celles dans le sol a subi un traitement chimique (Oxamyl). Cependant, les ces
tendances dans les densités de nématodes ne se sont pas
significatives (p=0.404).
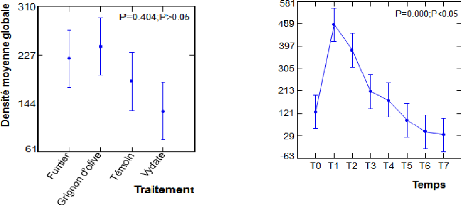
Fig.23: Effet des traitements sur les variations
temporelles des densités de
nématodes.
II.3.Répartition temporelle des groupes trophiques
en fonction des traitements
Les résultats obtenus (Fig.24) montrent des
variabilités dans les abondances moyennes globales des groupes
trophiques dans les différents blocs en fonction du temps quelque soit
le traitement. Généralement, pour les différents
traitements les abondances moyennes des groupes trophiques les plus
élevées sont enregistrées aux temps T1 et T2 (mars).
Toutefois, les plus faibles sont signalées pendant la fin du cycle T6 et
T7 (juin).
Les traitements apportés ont affecté
considérablement ces groupes. L'amendement du sol au fumier montre en T1
avant transplantation une forte diminution des phytophages. Ils sont
passés de 52 (T0 : 5 mars) à 0 N/50g de sol (T1 :15 mars). Alors
qu'on enregistre une augmentation très rapide des nématodes
libres (représentés en grande partie par les nématodes
bactérivores) (866 N/ 50g de sol) comparé au
prélèvement avant traitement T0 (56 N/50g de sol). Cependant, en
T2 (mars) les populations des nématodes libres ont diminué
sensiblement (140 N/ 50g de sol), avec une reprise de développement des
phytophages avec une densité de (38 N/ 50g de sol). En T3 (avril) nous
notons des pullulations respectives des prédateurs-omnivores (12N/ 50g
de sol) et des nématodes libres (312 N/ 50gde sol). Toutefois à
partir de T4 (mai) jusqu'à T7 (juin) les différents groupes ont
régressés sensiblement.
En ce qui concerne l'apport des grignons d'olive, nous
enregistrons en générale une abondance du groupe fungivores
notamment dans les échantillons de T1 et T2 (mars). Les valeurs
respectives sont de 654 et de 515 N/50g de sol.
En ce qui concerne les phytophages une diminution est
signalés en T1 (mars) après l'apport de cet amendement. Ils sont
passés de 68 (T0) à 24 N/50g de sol. Les nématodes
prédateurs-omnivores et des nématodes libres sont faiblement
représenté dans ce bloc quelques soit le temps
d'échantillonnage.
L'application de l'Oxamyl (nématicide
systémique) a montré en T1 (mars) une suppression des
nématodes phytophages, fungivores et prédateurs-omnivores et une
diminution des nématodes libres. Ces derniers sont passés de 90
(T0) à 42 N/50g de
sol. Dans les échantillons du 30 mars (T2), nous notons
un rétablissement des nématodes phytophages (65 N/50g de sol) et
augmentation de la densité des nématodes libres (272 N/50g de
sol). Dans l'échantillon de T3 (14 Avril) apparait de faibles
densités des nématodes prédateurs-omnivores avec un
effectif de (28 N/ 50 g de sol).
En général les prélèvements des
mois mai et juin (T5, T6 et T7), pour le bloc traité à l'Oxamyl
et celui amendé au fumier présentent des faibles densités
moyennes des groupes trophiques qui sont similaire au bloc témoin.
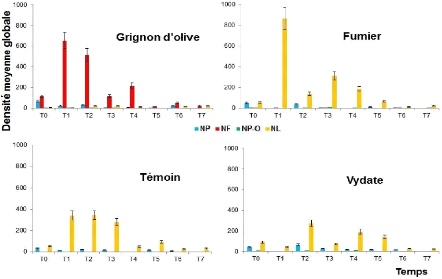
Fig.24: Répartition temporelle des groupes
trophiques en fonction des traitements
L'application du Modèle Linéaire
Général (G.L.M) à la répartition temporelle des
groupes trophiques en fonction des traitements (tableau 3), montre des
différences très hautement significatives entre les abondances
moyennes des groupes trophiques en fonction du temps (P=0,000 et P=0,000;
P<0,05). Par contre la différence et non significative pour les
traitements avec une probabilité de (P=0,479 ; P>0,05).
Tableau3: Modèle G.L.M. appliqué sur la
variation temporelle des groupes trophiques en fonction du
traitement.
|
Source
|
Somme des carrés DDL
|
Moyenne carré F-ratio
|
P
|
|
Traitements
|
30277.047
|
3
|
10092.349
|
0.830
|
0.479
|
|
Temps
|
349810.109
|
7
|
49972.873
|
4.108
|
0,000
|
|
Groupes trophiques
|
1295839.547
|
3
|
431946.516
|
35.504
|
0,000
|
|
Erreur
|
2944188.281
|
242
|
12166.067
|
|
|
L'analyse de la figure 25 confirme nos résultats qui
stipulent une variation temporelle des groupes fonctionnels des
nématodes rencontrés. Les densités moyennes les plus
élevées sont enregistrées au cours des temps (15 mars)
(T1) et 30 mars (T2). Les abondances moyennes des différents groupes
diminuent progressivement dans le temps, pour atteindre les effectifs les plus
faibles aux temps de 1 juin (T6) et 15 juin (T7).
Les groupes fonctionnels présentent des
différences significatives d'un point de vue densités. En effet,
les nématodes libres dominent les autres groupes de nématodes
(phytophages, fungivores et prédateurs-omnivores).
En ce qui concerne les traitements, ces derniers affectent les
groupes trophiques des nématodes comparés au témoin. Les
densités moyennes les plus importantes sont observées avec le
traitement au grignon d'olive et le fumier, les plus faibles sont
signalées sur la tomate qui a subi un traitement chimique (Oxamyl).
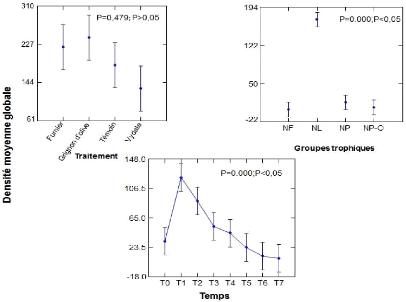
Le groupe (1), représente en général les
prélèvements du 1er juin du bloc amendé au
grignon d'olive (GT6), du 30 Mars (T2) et 1er Juin (T6) pour le
bloc
Fig25: Répartition temporelle des abondances
moyennes globales des groupes trophiques en fonction des
traitements.
II.4. Effet des traitements sur la répartition des
nématodes phytophages
L'analyse de la distribution des nématodes phytophages
rencontrés dans la parcelle d'étude en fonction des traitements,
est réalisée à travers l'analyse l'ACP(Fig.26). Les
premiers axes (1 et 2) de l'ACP expliquent (plus 80%) de l'information, l'axe 1
représente les taxons phytophages de nématodes et l'axe 2 les
prélèvements.
La classification hiérarchique ascendante et le calcul
de distance Euclidien sur la base de similarité de (-6), (Fig.27) a
montré la présence de quatre groupes. La projection des groupes
sur les axes factoriels met en évidence l'affinité de certains
taxons phytophages avec les relevés et les traitements.
témoin et du 1er Juin (V6) pour le bloc
traité à l'Oxamyl. C'est prélevement sont
caractérisé par la présence des genres
Tylenchorhynchus et Paratrichodorus.
Le groupe (2) réunit les prélèvements ou
abonde le genre Meloidogyne. Ils
sont représentés par les échantillons du
15 Mai bloc témoin (T5), bloc Oxamyl (V5) et bloc fumier
(FT5).
Le groupe (3) rassemble le plus grand nombre de
prélèvements ceux du bloc fumier des mois 14 avril (T3),
1er Mai (T4), 15 Mai (T5), 1er Juin (T6) et 15 Juin (T7).
Pour le bloc grignon d'olive nous avons les relevés du 15 Mai (T5) et du
15 Juin (T7) ; le bloc témoin les prélèvements
réalisés le 14 avril (T4) et le 15 Juin (T7) et enfin le bloc
Oxamyl avec les relevés du 15 Mars (T1) et 15 Juin (T7). Ce groupe 3 se
retrouvent du coté négative des axes, donc les
échantillons de sol sont très pauvre en phytophages.
Quant au groupe (4), comprend les prélèvements
du témoin le 15 mars (T1) et de traitement au vydate
échantillonné le1 Mai (V4) qui est attrait
Scutellonema.
Les taxons positionner au centre des axes (Psilenchus,
Pratylenchus , Coslenchus, Tylenchus, Trophurus
et Pratylenchoides) sont faiblement représentés
dans les différents prélevements quelque soit le traitement.
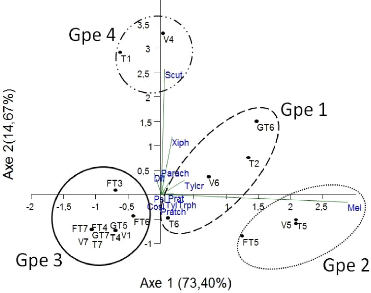
Fig.26:Répartition temporelle des nématodes
phytophages en fonction de traitements
Scut : Scutellonema, Xiph :
Xiphinema, Psil : Psilenchus, Mel:
Meloidogyne, Tylcr : Tylenchorhynchus, Prat :
Pratylenchus, Pratch : Pratylenchoides, Dit:
Ditylenchus, Tyl : Tylenchus, Trph :
Trophurus, Cosl : Coslencus, Parach :
Paratrichodorus
Gpe :Groupe ;V1 :Vydate T1
;V4 :Vydate T4 ;V5 :Vydate T5 ;FT3
:Fumier T3 ;V6 :Vydate
T6 ;FT4 :Fumier T4 ;T1
:Témoin T1 ;T2 :Témoin T2 ;FT5
:Fumier T5 ;V7 :Vydate T7 ;T4
:Témoin T4 ;FT6 : Fumier T6 ;FT7
:Fumier T7 ; GT5: Grignon d'olive T5; GT6:
Grignon d'olive T6;T5:Témoin T5;
T6:Témoin T6;GT7: Grignon d'olive T7;
T7:Témoin T7
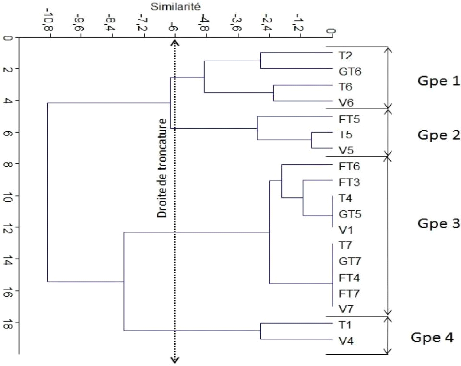
Fig.27: Classification ascendante hiérarchique de
la structure des nématodes phytophages en fonction des
traitements
II.5.Effets des traitements sur la répartition des
Meloidogyne
D'après les résultats représentés
par la figure (28) les densités moyennes des larves de Meloidogyne
du sol varient dans le temps en fonction des traitements.
En comparant l'efficacité des deux amendements (fumier
; grignon d'olive) et le produit chimique (Oxamyl), nous notons que le fumier
s'avère plus actif sur les larves de Meloidogyne. En effet,
nous avons enregistré une suppression des larves dans les
échantillons de sols du 15 mars (T1). Cependant, dans les mêmes
prélèvements (T1) pour les grignons d'olive et le produit
chimique nous avons constatés une diminution des larves (L2) dans le
sol.
Après la transplantation en T2; on remarquant un
rétablissement des populations des Meloidogyne. En effet, les
échantillons du 30 mars (T2) révèlent une augmentation des
densités moyennes des larves de Meloidogyne pour les
différents traitements. Toutefois, dans le bloc amendé au fumier
l'abondance moyenne des L2 est plus élevée (26 N/50 g) suivi par
celle du bloc traité à l'Oxamyl (16 N/50 g de sol). Par contre la
plus faible est signalé dans le bloc avec apport aux grignons d'olive (6
N/50g de sol).
En ce qui concerne les prélèvements T3
(14avril), T4 (1 mai), T5 (15 mai), T6 (1juin) et T7 (15 juin), les populations
de Meloidogyne fluctuent fortement quelque soit le traitement.
Toutefois, les très faibles densités sont enregistrées
avec l'application des grignons d'olives.
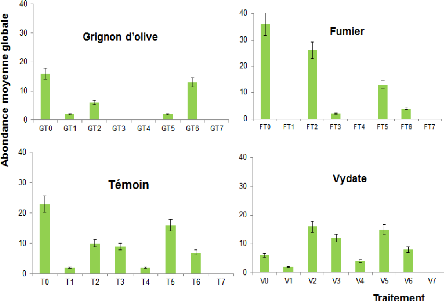
Fig.28: Distribution temporelle des densités
moyennes des Meloidogyne en fonction
des traitements
L'application du modèle G.L.M. pour les
résultats obtenus (tableau 4 et figure 29), montre que les
différents traitements n'affectent pas les densités moyennes des
Meloidogyne (P=0.529; p > 0.05). Par contre, les abondances
moyennes des larves
(L2) de nématodes à galles varient d'une
manière très hautement significative dans le temps avec une
probabilité de (P=0.000 ; p < 0.05).
Tableau.4: Effet des traitements sur les
densités moyennes des Meloidogyne à travers l'analyse de
la variance
|
Facteurs
|
Somme des carrés
|
DDL
|
Carrés moyens
|
F- ratio
|
P
|
|
Traitements
|
133.187
|
3
|
44.396
|
0.747
|
0.529
|
|
Temps
|
2692.938
|
7
|
384.705
|
6.474
|
0.000
|
|
Erreur
|
3149.313
|
53
|
59.421
|
|
|
La figure (29) relative à l'analyse statistique
modèle G.L.M. révèle que les faibles densités des
larves de Meloidogyne dans le sol sont signalées avec l'apport
des grignons d'olive. Alors que l'effet du fumier est comparable à celui
du témoin et de l'Oxamyl.
En ce qui concerne les variations temporelles des abondances
moyennes des larves ; l'analyse révèle qu'elles fluctuent
considérablement dans le temps. En effet des pics sont enregistré
le 5 Mars (T0), le 30 Mars (T2) et le15 Mai (T5).
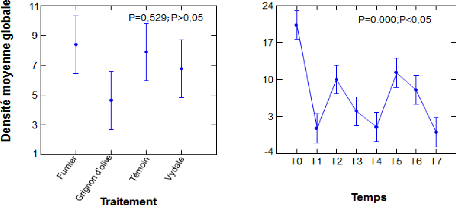
Fig.29: Variation temporelles des Meloidogyne
en fonction des traitements.
II.6. L'effet des traitements sur le nombre de galles
Pour évaluer l'efficacité des traitements
utilisés dans le contrôle des Meloidogyne, nous avons
tenu compte du nombre de galles produit par ces nématodes sur les
racines de tomate en fin de culture.
D'après les résultats représentés
dans la figure 30, nous constatons que le nombre de galles varie en fonction
des traitements. En effet, l'application des grignons d'olive dans le sol
affecte le développement des nématodes à galles sur les
racines de tomate. Ce traitement a montré le plus faible effectif moyen
de galles sur les racines (41 galles) comparé au fumier (144 galles) et
à l'Oxamyl (99,5 galles).
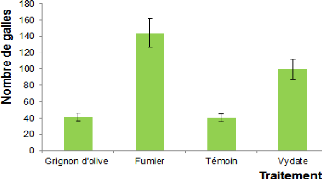
Fig.30: Effet des traitements sur le
développement des Meloidogyne sur les
plants de tomate
Tableau 5 : Modèle G.L.M. appliqué au
développement des Meloidogyne sur de tomate
Source Somme des carrés DDL Moyenne carré
F-ratio P
Traitements 15102.500 3 5034.167 25.717 0.004
Erreur 783.000 4 195.750
L'application du modèle G.L.M. pour les données
obtenues (tableau 5) et figure (31), nous permet de déduire que le
nombre moyen de galles varie d'une manière très significative
d'un point de vue traitements testées (p=0.004 ; p < 0.05).
La figure (31) relative aux différents traitements montre
l'efficacité des grignons d'olive dans le contrôle du
développement des Meloidogyne sur les plants de tomate,
comparé au fumier et au Vydate.
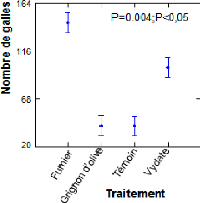
Fig.31: Effet des traitements le nombre de galles
moyen
II.7.Effet des traitements sur le nombre des femelles:
Pour évaluer l'effet des traitements appliqués sur
le développement des femelles de Meloidogyne nous avons
compté le nombre de femelles dans 10 galles choisi au hasard.
Les résultats obtenus (fig.32) révèlent
que le nombre moyen des femelles varie en fonction des traitements
testés. L'effectif moyen le plus faible est obtenu avec l'application de
grignon d'olive (8 femelles). Alors que pour le fumier et le traitement
chimique les effectifs moyens en femelles sont similaires au
témoin.Elles sont respectivement de (10,10.5 et 10.5 femelles).
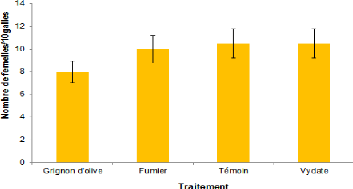
Fig.32: Effet des traitements sur le développement
des femelles des Meloidogyne
L'application du modèle G.L.M. à la variation des
effectifs moyens des femelles en fonction des traitements montre (Tableau 6)
l'existence d'une différence non significative avec une
probabilité de (P=0.975; p > 0.05).
Tableau6 : Effet des différents traitements sur le
nombre de femelle moyen
Facteurs Somme des carrés DDL Carrés moyens
F-ratio P
Traitements 0.075 3 0.025 0.071 0.975
Erreur 12.700 36 0.353
Il apparaît dans la figure (33) que les traitements
apportés présentent un effet comparable dans l'infestation des
larves et le développement des femelles dans les racines de tomate.
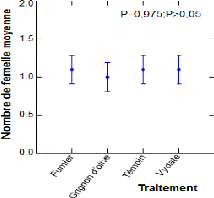
Fig.33:Effet des différents traitements sur le
développement des femelles moyen

Chapitre II : Résultats et Discussion
DISCUSSION GENERALE
En raison des restrictions qui régissent l'utilisation de
nématicides et les fumigants du sol, des méthodes respectueuses
de l'environnement ou de développement durable ont pris un rôle
plus important dans les stratégies de contrôle des
nématodes phytoparasites. Une grande variété d'amendements
organiques ont été utilisés pour lutter contre les
nématodes dans diverses cultures.
1. Inventaire de la communauté de nématodes
rencontrés dans la parcelle d'étude sur tomate
L'étude de la diversité et des assemblages des
communautés des nématodes associés aux cultures
maraichères dans notre milieu saharien ; la région de Touggourt
(wilaya d'Ouargla), fait ressortir une diversité de taxons importante
(16 taxons identifiés). Comparée aux résultats accomplies
sur l'inventaire des nématodes des cultures maraîchères
dans d'autres biotopes (humides et sub humides) nous constatons que Hadri,
(2006) et Hedibel (2007) ont dénombré 10 taxons alors qu'El
Aimouche, en 2009 a inventorié 16 taxons. Les différences au
niveau de la richesse nématofaunique seraient éventuellement
liés à la méthodologie adoptée par les
différents auteurs ; ou probablement aux conditions édaphiques.
En effet, divers auteurs ont démontré que les amendements
organiques peuvent modifier les propriétés physiques du sol, qui
à leur tour peuvent affecter négativement les comportements des
nématodes tels que l'éclosion, le mouvement et la survie
(Sohlenius, 1980 ; Bongers, 1990 ; de Goede, 1993 ; de Goede et al.,
1993 ; Neher et al., 1995 et Oka, 2010).
Les conditions climatiques ne sont pas à exclure, car
ils sont spécifiques à notre biotope. Cette hypothèse est
en concordance avec les travaux de Sánchez-Moreno et al. (2006)
qui affirment que les nématodes répondent naturellement aux
variations de l'environnement.
Les enquêtes réalisées au cours de cette
étude montrent que les communautés de nématodes dans le
sol varient en fonction du temps et des traitements apportés. Ces
résultats rejoints les recherches de Verschoor et
al., (2002) qui assurent que l'abondance et la
structure des populations de nématodes changent en fonction de la
saison.
Les résultats obtenus révèlent
après labour de la parcelle de travail le 5 Mars (T0) une faible
densité de nématodes. Il est probable que l'absence de cultures
dans le sol expliquerait cette faible richesse. Cette hypothèse rejoint
le travail de recherche réalisée par Taylor (1968) qui affirme
que la plante cultivée affecte fortement les fluctuations des
nématodes. D'autres investigations stipulent que l'apport de compost,
ainsi que le travail du sol, induit une modification des
caractéristiques physico-chimiques du sol ainsi qu'une modification de
la structure spécifique du peuplement de nématodes phytoparasites
(Villenave et al., 1998).
2. Répartition temporelle de la densité
moyenne globale des nématodes en fonction des traitements
Les densités moyennes obtenues les plus
élevées sont enregistrées au mois Mars. Cependant les plus
faibles sont signalées en Mai et Juin. Contrairement à nos
résultats, les travaux d'El Aimouche (2009) sur choux montrent que les
densités moyennes globales des nématodes sont plus importantes en
période hivernale. Il serait probable que les divers conditions de
l'environnement et pratiques culturales ont contribué à ces
différences d'abondance des nématodes ; cette hypothèse
rejoint les investigations de Zeleney et al., (2004) et Neher
(2000).
L'abondance globale moyenne des nématodes est
affectée par les amendements apportés. En conséquence, les
populations nématologiques les plus importantes sont observées
avec le traitement au fumier, suivi par le grignon d'olive comparé au
témoin. Tandis que, les plus faibles sont celles dans le sol a subi un
traitement chimique (Oxamyl). Par ailleurs, les analyses statistiques (G.L.M)
prouvent des différences non significatives entre les amendements
apportés (p=0.404). Nos résultats rejoint l'étude de Crow
(2005) qui déclare que l'effet de certains amendements peut être
faible, voire inexistantes. En outre Oka (2010) confirme qu'aucun amendement
organique seul ne semble être capable de remplacer des nématicides
systémiques ou des fumigants, mais l'intégration de cette
méthode avec d'autres techniques culturale comme l'utilisation de
cultivars résistants ou la
solarisation du sol, permettra d'améliorer le
contrôle de son efficacité et le rendement des cultures.
3. Répartition temporelle des groupes
trophiques en fonction des traitements
L'étude de la répartition des taxons
rencontrés en groupes fonctionnels montre que ces derniers se classent,
en quatre groupes trophiques, constitués spécialement de groupe
des nématodes libres qui rassemble pour la plupart des espèces
bactérivores en première position, suivi par les
phytophages en deuxième position, avec la présence de
(Ditylenchus, Pratylenchus, Scutellonema, Meloidogyne, Tylenchorhynchus,
Xiphinema, Paratrichodorus, Psilenchus, Trophurus, Tylenchus, Coslenchus et
Pratylenchoides) ; vient ensuite le groupe prédateur-omnivore
renfermant trois taxons ; Mononchus, Dorylaimus et Ecumenicus
; enfin le groupe fungivore ou figure Ditylenchus, Aphelenchus.
Il s'avère d'après nos résultats sur les groupes
trophiques des nématodes dans les sols maraîchers en
Algérie que sont comparables à ceux de Kadem (2007), Belahammou
(2010) et Mami (2011).
Le modèle G.L.M appliqué à la
répartition des groupes trophiques en fonction du temps montre une
différence très hautement significatives (p=0.000). Les groupes
les plus abondants sont signalés en Mars les plus faibles en Mai et
Juin. Le groupe des nématodes libres pullulent en forte densité
par rapport aux trois autres (Phytophages, fungivores et
prédateurs-omnivores). Cette
hétérogénéité de la distribution des groupes
fonctionnels rencontrés serait due à plusieurs facteurs. Selon
Norton et Niblack (1991), elle est en relation avec les différences dans
les cycles de vie des espèces, des relations biotiques avec les
microorganismes du sol et des facteurs physico-chimiques du milieu. Ou bien ils
sont en relation avec des changements de leurs ressources alimentaires
(Hânel ,1995 ; Gomes et al., 2003). Les résultats de
l'application du Modèle Linéaire Général (G.L.M)
montrent que les amendements organiques n'affectent pas d'une manière
significative les densités des groupes trophiques. Toutefois, le fumier
a entrainé une prolifération du groupe de nématodes
libres. Ces résultats rejoignent les observations de McSorley et
Frederick (1999) ; Nahar et al. (2006) et Oka (2010)
qui témoignent que
l'incorporation des amendements organiques
(engrais et compost) augmente les densités des nématodes
bactériophages et des mycophages mais diminue les populations de
nématodes phytoparasites. Alors que les grignons d'olive ont
montré
une abondance des nématodes fungivores. On peut
supposer probablement que ce type de résidus organiques est à un
stade d'évolution assez avancé qui a induit une fongistase qui a
contribué à la pullulation des nématodes mycophages (Oka,
2010). Concernant les autres groupes, nous constatons une réduction en
T1 (Mars) des phytophages et faibles représentations des
nématodes prédateurs-omnivores et des nématodes libres
dans ce bloc quelques soit le temps d'échantillonnage. Ces
résultats seraient probablement liée aux plusieurs
composés phénoliques qui contiennent les déchets
d'industries d'olive qui possèdent une activité
nématicide
(Chitwood, 2002 ; Cayuela et al., 2008).
4. Effet des traitements sur la répartition des
nématodes phytophages
L'analyse multivarie (ACP) de la distribution temporelle des
nématodes en fonction des traitements montrent une affinité des
espèces phytophages rencontrés avec les différents
prélèvements dans les blocs testés. On peut dire
probablement que ces tendances sont en relation avec les traits de vie et la
dynamique de population de chaque espèce dans leur milieu de vie. Ceci
s'accorde aux travaux de Norton et Niblack (1991) ; Ndiaye
(1999) qui assurent que la température du sol et l'humidité sont
considérées comme les facteurs les plus importants affectants la
dynamique saisonnière des populations des nématodes. Elles
peuvent agir directement en modifiant l'activité métabolique des
nématodes (Atkinson, 1980 ; Duncan et Klekowski, 1975) ou indirectement
en affectant la qualité de leur source de nourriture (Yeates, 1982).
5. Effets des traitements sur la répartition des
Meloidogyne
A travers les résultats rapportés sur l'analyse
statistique (modèle G.L.M.) appliquée à l'effet des
traitements sur les variations temporelles des Meloidogyne on
constatant que les abondances moyennes des larves (L2) de nématodes
à galles dans le sol varient d'une manière très hautement
significative dans le temps avec une probabilité de (P=0.000 ; p <
0.05). Des pics sont enregistrés en période printanière le
5 Mars (T0), le 30 Mars (T2) et le 15 Mai (T5). Par contre les traitements
testés affectent faiblement les densités moyennes des
nématodes à galles. En effet l'apport des grignons d'olive a
révélé de faibles densités des larves de
Meloidogyne dans le sol comparé au fumier. Selon Norton (1979),
l'apport d'amendements organiques induit de façon générale
une diminution du nombre de
nématodes phytoparasites. Hominick (1999) explique que,
l'accumulation progressive de la matière organique dans le sol favorise
l'apparition des organismes antagoniques qui maintiennent les populations des
nématodes parasites de plantes au-dessous du seuil de nuisance. Par
ailleurs, Gamliel et Stapleton (1993) confirment que plusieurs composés
volatiles et non volatiles peuvent être produits au cours de la
décomposition des amendements organiques dans le sol. Comme le dioxyde
de carbone, l'éthylène, l'hydrogène, les acides
organiques, les alcools, le diméthyle, les sulfures et les
aldéhydes. Certains de ces composés sont connus pour leur
activité nématicides (Oka, 2010).
6. L'effet des traitements sur le nombre de galles et
le développement des femelles
Pour évaluer l'efficacité des amendements
organiques testés (fumier et grignon d'olive) sur le
développement des nématodes à galles dans la culture de
tomate ; nous avons tenu compte de l'état d'infestation des racines par
les larves (L2) de Meloidogyne (nombre de galles), le
développement du nombre de femelles.
Les résultats ont révélé que le
nombre de galles varie d'une manière très significative avec les
traitements apportés (p=0.004 ; p < 0.05). Les grignons d'olive
entraine une diminution de l'infestation des racines par les larves de
Meloidogyne d'où un faible développement de galles.
D'autre part, ces apports n'affectent pas le nombre de
femelles qui s'est établie sur les racines de tomate. Toutefois, nous
enregistrons que l'effectif moyen le plus faible des femelles est obtenu avec
l'application de grignon d'olive. Divers travaux confirment nos
résultats en expliquant que l'efficacité de la biofumigation du
sol avec des plantes Brassicaceae principalement le colza (Brassica
napus) et la moutarde indienne (Brassica juncea) dans la
suppression des nématodes (Mojtahedi et al., 1991 ; Mojtahedi
et al., 1993 ; Walker et Morey, 1999 ; Ploeg et Stapleton, 2001 ;
Stirling et Stirling, 2003 ; Zasada et Ferris, 2004 et Rahman et Somer,
2005).
L'amendement du sol avec les herbes orientales à 0.2%
(poids/ volume de sol) réduit l'infestation des racines de tomate par
M.incognita. Les plus efficace sont les traitements par les
écorces des racines de Paeonia suffructicosa et les
écorces des tiges de Cinnamomum cassia (Kim et al.,
2003).
CONCLUSION GRt»i
®~cLvs7oNC~E~~
CONCLUSION GENERALE
Pour protéger les cultures contre les maladies, une
large gamme de méthodes alternatives est déjà disponible.
Certaines de ces méthodes sont déjà utilisées, plus
ou moins empiriquement, par les producteurs. C'est le cas par exemple des
amendements organiques, sans que la protection des cultures soit
forcément l'objectif principal.
La réalisation de cette étude sur l'effet des
amendements organiques sur les communautés de nématodes dans le
milieu saharien fait ressortir une diversité de taxons importante (16
taxons identifiés). Ils sont représentés par
Ditylenchus, Aphelenchus, Psilenchus, Pratylenchus, Scutellonema,
Tylenchorhynchus, Meloidogyne, Tylenchus, Trophurus, Pratylenchoides,
Xiphinema, Paratrichodorus, Mononchus, Coslenchus, Dorylaimus et
Ecumenicus.
Les densités moyennes des communautés de
nématodes dans le sol varient en fonction du temps. Les densités
moyennes obtenues les plus élevées sont enregistrées aux
mois Mars. Cependant les plus faibles sont signalées en Mai et Juin. Les
traitements apportés non pas d'effet sur les densités globales
des communautés de nématodes l'analyse statistique (GLM) prouvent
des différences non significatives entre les amendements apportés
(p=0.404).
La répartition des groupes trophiques montre en
général qu'elle reste en faveur du groupe de nématodes
libres représenté par les nématodes bactérivores.
Le groupe des nématodes libres pullulent en forte densité par
rapport aux trois autres (Phytophages, fungivores et prédateurs
omnivores. La distribution des groupes fonctionnels varie en fonction du temps.
Les groupes les plus abondants sont signalés en Mars les plus faibles en
Mai et Juin.
L'analyse statistique (G.L.M) montre que les amendements
organiques n'affectent pas d'une manière significative les
densités des groupes trophiques. Toutefois le fumier a entrainé
une pullulation du groupe de nématodes libres alors que les grignons
d'olives favorisent le développement des fungivores.
L'analyse la distribution des nématodes phytophages en
fonction des différents prélèvements est
réalisée à travers l'ACP. La classification
hiérarchique ascendante a dévoilé la présence de
quatre groupes présentant une certaine affinité avec les
traitements et le temps.
Les abondances moyennes des larves (L2) de nématodes
à galles dans le sol varient très significativement dans le
temps. Des pics sont enregistré en période printanière le
5 Mars (T0), le 30 Mars (T2) et le 15 Mai (T5). Par contre les traitements
testés affectent faiblement les densités moyennes des larves (l2)
de Meloidogyne dans le sol. Par ailleurs les traitements agissent
différemment sur le degré d'infestation des racines par les
larves. Les grignons d'olive entrainent une diminution du nombre de galles
moyen sur les racines comparé au fumier. Par contre ces apports non
aucun effet sur le nombre de femelles qui s'est établie sur les racines
de tomate. Mais, visiblement avec l'application des grignons d'olive nous
enregistrons l'effectif moyen le plus faible des femelles sur les racines.
Quoique divers recherches ont prouvé les bienfaits des
amendements organiques qu'ils soient d'origine animale ou
végétale aussi bien pour le sol en l'enrichissant en divers
éléments essentiels que pour les cultures en augmentant les
récoltes et les rendements de ces derniers. Cette étude nous ne
permet pas de statuer avec précision sur l'effet des amendements
organiques testés dans la structure des communautés de
nématodes notamment les phytophages.
En effet, notre site de travail n'était pas très
infesté par les nématodes phytophages qui sont à cibler.
Les investigations doivent se poursuivre dans les systèmes de culture
intensive ou les phytoparasites posent de réels problèmes afin de
valider non seulement leur efficacité biologique, mais aussi leur
faisabilité technique et économique, avant de promouvoir
l'utilisation de telles pratiques auprès des producteurs.
Références bibliographiques
1- Anonyme1, 2011-Tomate-article de
Wikipédia l'encyclopédie libre
2-Anonyme2, 2002-
www.oleiculteur
.com/huil.2005-Qu'est-ce que l'huile de grignon ?
3-Anonyme3, 2006-Chapitre II-Grignons
d'olive.
4-Akhtar M. et Mahmood I., 1996-le
contrôle des nématodes phytoparasites des amendements organiques
et minéraux dans les sols agricoles, Appl. Sols Ecol. 4 (1996), pp.
243-247. Résumé | Article | PDF (316 K) | Voir la notice de
Scopus | Titre du Scopus (18).
5-AkhtarM., 1998- Biological
control of plant-parasitic nematodes by neem products in agricultural soil,
Appl. Soil Ecol. 7 ,pp 219-223.
6-Agrios G.N., 1978 - Plant pathology, Acad.
Press .I.N.C, London, San-Francisco, New York, 853 p.
7-Bellahammou S.,2010- Contribution à
l'étude de la diversité de la nématofaune associés
aux cultures maraichères dans la vallée d'oued Righ,Wilaya
d'ouargla.Thès.Ing.Agro.Blida.78p.
8- Bertrand C.; Lizot J. et Mazollier C., 2001 -
Lutter contre les nématodes à galles en Agriculture biologique,
Rev. : GRAB AVINON, France, pp. 25-29.
9-Bezaz H., 2006- Etude de la
diversité des communautés des nématodes phytophages des
cultures maraîchères dans quelques régions de
l'Algérie.Projet de fin d'étude, d'ingénieur d'état
en agronomie, Protection des végétaux, Dep.Agr., Univ.Saad
Dahlab, Blida, 66 P.
10- Bongers T. et Ferris H.,1999-Nematode
community structure as a bioindicator in environmental monitoring.Rev.Vol.14,no
6,pp. 224-228.
11-Boummada A.B., 1995- Etude de
l'état d'infestation des cultures maraîchères par les
nématodes (Meloïdogyne) dans la région d'Ouargla.
Institut Nationale De Formation Supérieur en Agronomie saharienne.
Mém. Ing. Agronomie saharienne.Univ.Kasdi Merbah, Ouargla.
12-Bressoud F., Arrufat
A.;2009- Amendements organiques et maraîchage biologique sous
abri - Observations après 6 années d'apport. Innovations
Agronomiques 4, pp. 15-21.
13-Cadet P., 1998 - Gestion écologique
des nématodes phytoparasites tropicaux. Cahiersagricultures,
n°7, Dakar, Sénégal, PP:9-187.
14-Cadet P., 1998 - Gestion écologique
des nématodes phytoparasites tropicaux. Laboratoire de
bio-pédologie,ORSTOM,BP 1386, Dakar,Sénégal. Eur.J.Soil
Biol.,35,pp.91-97.
15-Cadet P., Masse D. and Thioulouse, J.,
2005-Relationships between plant-parasitic nematode community, fallow
duration and soil factors in the Sudano-Sahelian area of Senegal.Agriculture,
Ecosystems and Environment , 102, 302-317. 16-Cayrol
J.C. ; Caporalino C.D. ; Mattei E.P., 1992- La lutte biologique contre
les nématodes phytoparasites. Laboratoire de Biologie des
invertébrés INRA, BP 2078,06606 Antibes.15p.
17-Cayuel M.L., Millner P.D., Meyer S.L.F., Roig A.,
2008-Potential of olive mill waste and compost as biobased pesticides
against weeds, fungi and nematode. Science
Direct.www.elsevier.com/locate/scitotenv;
Science of the total envirenment 399(2008)11-18.
18-Chitwood D.J.,2002- Phytochemical based
strategies for nematode control, Annu. Rev. Phytopathol. 40 (2002), pp.
221-249.
19-De Guiran G. et Netscher C., 1970 - les
nématodes du genre Meloidogyne, parasite des cultures tropicales,
Cahier. O.R.S.T.O.M., sér. Biol., n°11, pp 151-185.
20-De Guiran G., 1983 -Nématodes, les
ennemis invisibles .Les nématodes parasites des cultures en pays
tempérés .Ed.La littorale, S.A.Beziers, France, 40p.
21-De Guiran G., 1983 - Les nématodes
parasites des cultures en pays tempérés .Ed. Littorale,
S.A.Beziers, France, 41p.
22-Denni A., 2011- Contribution à
l'étude de l'efficacité de deux espèces de Moutarde «
Sinapisarvensis etHirshfeldiaincana » in vitro et in
vivo dans le contrôle des nématodes à galle
(Nematoda-Meloidogynidae) et sur le développement des
plants de tomate (var. Marmande). Projet de fin d'étude,
d'ingénieur d'état en agronomie, Protection des
végétaux, Dep.Agr., Univ.Saad Dahlab, Blida, 60 p.
23-Djerroudi (O.Z.), 2001-Contribution
à l'étude de la nuisibilité de Meloïdogyne
javanica(Nematoda : Meloïdogynidae) sur aubergine.
Essais de traitements chimique, biologique et solaire contre ce nématode
sous abris plastique dans la région d'Ouargla. Diplôme de
Magister. Scien. Agro.INA El Harrach, Alger.
24-Diongue A., 1996- lnitiation à la
nématologie :application des cultures
maraîchères ,
Dép. formation en protection des végétaux, centre AGRHYMET
. Niamey, 52p.
25-El Aimouche F ., 2009-FLUctuation
saisonnières de la nématofaune associés aux cultures
maraîchères dans deux stations (Soomaa et Staouali ). Projet de
fin d'étude, d'ingénieur d'état en agronomie, Protection
des végétaux, Dep.Agr., Univ. Saad Dahlab, Blida, 87p.
26- Fademi O.A. et Bayero
A.,2003-Nématodes parasites des plantaint et des bananiers dans
le sud-ouest et le centre du Nigeria, pp 13-14.
27-Ferris H. et Bongers T., 2006- Nematode
indicators of organic enrichment.The Society of Nematologists .Journal of
Nematology 38(1):3-12.
28-Freckman, D.w., 1988- Bacterivorous
nematodes and organic matter decomposition.Agriculture Ecosystemes and
Envirenment24, 196-217.
29-Freckman, D.w., Ettama C.H., 1993-
Assessing nematode communities in agroecosystemes of varying human
intervention. Agric. Ecosyst. Environ., 45, pp.239-261.
30-Gomes G.S., Huang S.P. et Cares J.E.,
2003-Nematode Community, Trophic Structure and Population Fluctuation
in Soybean Fields, Fitopatologia Brasileira 28, pp. 258-266.
31-Hamadi A, 1991- Contribution à
l'utilisation de variétés résistantes de tomate en vue
d'une lutte contre lesMeloïdogyne(Nematoda,
Meloïdogynidae) sous abris plastiques dans la région
d'Ouargla (I.T.D.A.S.Hassi Ben Abdellah). Mém. Ing. Agronomie
saharienne.Univ.Kasdi Merbah, Ouargla.
32-Hadri H., 2006-Evaluation de la structure
des communautés de nématodes des cultures maraichéres et
leurs impact sur le développement de deux variétés de
tomate sensible (Marmande) et résistante (Piersol) , ). Projet de fin
d'étude, d'ingénieur d'état en agronomie, Protection des
végétaux, Dep.Agr., Univ. Saad Dahlab, Blida, 55p.
33-Hedibel A., 2006-Inventaire des
nématodes phytophages des cultures maraîchères dans la
wilaya de Jijel et leurs pathogénies sur le développent de deux
variétés de tomate sensible (Marmande) et
résistante(Carmello), Projet de fin d'étude, d'ingénieur
d'état en agronomie, Protection des végétaux, Dep.Agr.,
Univ.Saad Dahlab, Blida, 58 p.
34-Hoceini F., 2010- Etude de la
diversité des peuplements de nématodes phytoparasites dans
quelques zones oléicoles en Algérie.Mémoire de Magisteren
agronomie, Protection des plantes et l'environnement,Dep.Agr., Univ.Saad
Dahlab, Blida, 98 p.
35-Hooper D.J., 1986- Extraction of
free-living stages from soil. Pp. 5-30. In: Laboratory Methods for Work with
Plant and Soil Nematodes(Southey, J.F., ed.). Ministry of Agriculture,
Fisheries and Food No. 402, Her Majesty's Stationery Office, London, UK.
36-Ingham,R.E., Trofymow, J.A., Ingham, E.R., Coleman,
D.C. 1985- Interaction of bacteria, fungi and their nematode grazers:
effects on nutrient cycling and plant growth. Ecological Monographs 55,
119-140.
37-Ioannis O. Giannakou, Dimitrios G. Karpouzas ,
Demetra Prophetou-Athanasiadou ,2003-A novel non-chemical nematicide
for the control of root-knot nematodes.Applied Soil Ecology 26, pp. 69-79.
38-Jaccob J.J. et Middepiaats W.C.T., 1988 -
Fascicule de détermination des principaux nématodes
phytoparasites au stéréoscope, cours de nématologie, TSP,
Vol. 2, Niamey, Niger, 175 p.
39-JanvierC., 2007- Recherche d'indicateurs
de la santé des sols. Pour l'obtention du grade de Docteur de l'Institut
National Agronomique Paris-GrignonDiscipline : Microbiologie du sol,Institut
National Agronomique Paris-Grignon
Ecole doctorale ABIES,64p.
40-Kadem N., 2007-Etude de la toxicité
de deux espèces d'algues marines benthiques sur le développement
des plants de tomate (var.Marmande) et sur l'évolution des
communautés de nématodes phytophages,Projet de fin
d'étude, d'ingénieur d'état en agronomie, Protection des
végétaux, Dep.Agr.,Univ.Saad Dahlab, Blida, 48p.
41-Kandji S. T., Ogol Callistus K . P . O.,Albrecht
A., 2001-with some soi physical-chemical characteristics in improved
fallows in western Kenya. Applied Soil Ecology 18, pp. 134-157.
42-Khelili M, 1999-Etude de l'effet des doses
d'inoculum de Meloïdogyne sp sur quelques plantes
cultivées et contribution à l'étude de l'effet
nématicides de quelques plantes. Mém. Ing. Agronomie
saharienne.Univ.Kasdi Merbah, Ouargla.
43-Kheir N., 2011- Evaluation de la
toxicité de deux espèces d'Armoise
« Artemisia herba alba » « Artemisia judaca
» sur les Meloidogyne spp. (Nematoda-Meloidogynidae) in Vivo
et in Vitro.Projet de fin d'étude, d'ingénieur d'état en
agronomie, Protection des végétaux, Dep.Agr., Univ.Saad Dahlab,
Blida, 59 p. 44-Khouazem B, 1997-Utilisation de
différents produits nématicides contre les nématodes
à galle (Meloïdogyne sp) sur une culture d'aubergine
(Solanum melongena) sous abris serres (Ouargla). Mém. Ing. Agronomie
saharienne.Univ.Kasdi Merbah, Ouargla.
45-Larroum H, 1996- Contribution à
l'étude de l'influence des extrais de quelques plantes sur
l'activité et la mortalité des Meloïdogyne
(nématodes à galles).Institut Nationale De Formation
Supérieur en Agronomie saharienne.Département de phytotechnie.
Mém. Ing. Agronomie saharienne.Univ.Kasdi Merbah, Ouargla.
46-Loubad D, 1996-Etude comparative de trois
méthodes de lutte contre les nématodes à galle
(Meloïdogyne) sous serre (Ouargla). Mém.Ing.Agronomie
saharienne.Univ.Kasdi Merbah, Ouargla.
47-Luc, M., Sikora, R.A., Bridge, J., 1990.
Nématodes parasites des plantes
dans l'agriculture tropicale et subtropicale. CAB
International,
Wallingford.
-48Mahi F.Z., 2010- Contribution à
l'étude écobiologique de la mineuse de la tomate, Tuta
absoluta (Meyrick, 1917) (Lepidoptera, Gelechiidae) dans la
wilaya de Mostaganem. Projet de fin d'étude, d'ingénieur
d'état en agronomie, Protection des
végétaux, Dep.Agr., Univ.Saad Dahlab, Blida, 98
p.
49-Mateille T., Duponnois R., Diop M.T.,
1995-Influence des facteurs telluriques abiotiques et de la plante
hôte sur l'infection des nématodes phytoparasites du genre
Meloidogyne par l'actinomycéte parasitoide Pasteuria pentrans. Rev.
Agronomie, FRA, Vol. 15, pp.581-591.
50-Mahni K, 2005-Contribution à
l'étude de l'impact de quelques contraintes physico-chimiques du sol sur
le rendement du palmier dattier chez la variété
Déglet.Nour (dans la région d'Ouargla). Mém. Ing.
Agronomie saharienne.Univ.Kasdi Merbah, Ouargla.
51-Mazollier C., 2001- Le maraîchage en
Agriculture biologique : Quelques principes de base. Alter Agri 50, 13-16.
52-McSorley R. et Frederick J.J.,
1999-Nematode population fluctuations during decomposition of specific
organic amendments, J. Nematol.
3(1999)1, pp. 37- 44. View Record in
Scopus | Cited By in Scopus (38)
53-Nadji S, 1990-Enquête sur
l'état d'infestation des cultures maraîchères par les
Meloïdogyne (Nematoda, Meloïdogynidae)
dans les régions d'Adrar et d'Ouargla.Mém. Ing. Agronomie
saharienne.Univ.Kasdi Merbah, Ouargla.
54-Ndiaye A., 1994 -Influence de facteurs
abiotiques et biotiques sur la multiplication et la morphologie de quelques
Nématodes phytoparasites de la région
soudano-sahélienne.Projet d'obtention le grade de docteur de 3ème
cycle de Biologie Animale, n0d'ordre 10, Univ. Cheikh Anta Diop,
Dakar, Fac. des Sciences et Techniques,82p.
55-Ndiaye N., 1999-Les nématodes du
sol dans les systèmes de cultures à jachères du
Sénégal : Dynamique des peuplements et relations avec les
facteurs abiotiques et biotiques telluriques. Projet d'obtention le grade de
docteur de 3ème cycle de Biologie Animale, n0d'ordre 40,
Univ. Cheikh Anta Diop, Dakar, Fac.des Sciences et Techniques,157 p.
56-Nebih Hadj-Sadok., 2000- Etude de la
biologie des Meloidogynespp.( Nematoda- Meloidogynidae)dans quelques
régions du littoral algérien . Thèse Thèse
Magister.Inst.Nat . Agro., El-Harrach, 176p.
57-Nadji S, 1990-Enquête sur
l'état d'infestation des cultures maraîchères par les
Meloïdogyne (Nematoda, Meloïdogynidae)
dans les régions d'Adrar et d'Ouargla.Mém. Ing. Agronomie
saharienne.Univ.Kasdi Merbah, Ouargla.
58-Nebih Hadj-Sadok D., Belkahla H et Belkacem F.,
2008- Effet du filtrat de la culture de Fusarium Solani sur
morlitaté des oeufs des Meloidogyne Incognita et Meloidogyne Arenaria,
Seminaire National sur les interactions faune-flore et impact des changements
globeaux dans les espèces naturels et anthoposés.2-3
Décembre 2008.Scientifiques et techniques phytosanitaires, El-Harrach.
20-21 Juin.
59-Nebih Hadj-Sadok D., Aouni., 2006- Effet
des protéines (Cytoplasmique et pariétale) des tagets minuta sur
les larves infectantes (L2) de Meloidogyne spp. Dans les conditions de
laboratoire 6iem j.
60-Nefzaoui A., 1991-Valorisation des
sous-produits de l'olivier. CIHEAM- Options Méditerranéennes,
Laboratoire de nutrition animale. INRA de Tunisie 2080 Ariana, Tunisie, 108
p.
61-Netstcher C. et luc M., 1974-
Nématodes associés aux cultures maraicheres en
Mauritanie, Agronomie tropicale, Extrait du Vol xxlx, N° 6-7, p.-p. :
697-701.
62-Netscher, C., Sikora, R.A., 1990.des
nématodes parasites des légumes. Dans: Luc, M., Sikora, RA,
Bridge, J. (Eds.), plante parasite Les nématodes dans l'agriculture
tropicale et subtropicale. CAB International, Wallingford, p. 237-283
63-Norton, D.C.; 1979- Relationship of
physical and chemical factors to populations of plant parasitic nematodes.
Annual Review of Phytopatology 17, 279-299.
64-Norton, D.C., 1989 - Abiotic soil factors
and plant-parasitic nematode communities. Journal of Nematology, 21 ,pp.
299-307.
73-Singh R.S. et Sitaramaiah K., 1966-
Incidence of root knot of okra and tomatoes in oil caked amended
soils.Pt.Dis.Reptr 50,668-672.
65-Oka Y., 2010 - Mechanisms of nematode
suppression by organic soil amendments--A review,Applied Soil Ecology,
Vol.44, Issue 2, Nematology ,Unit, Gilat Research Center, M.P. Negev 85280,
Israel,pp 101-115.
66-Ritter M.,1971 - Les nématodes et
l'agriculture »les nématodes des cultures» Journées
d'études et d'information, A. C. T. A. FNGPC, Paris, pp. 9-65.
67-Ritter ; 1971- in Mordelet , p ., Barot, S. &
Abbadie , L., 1996- Root foraging strategies and soil patchiness in a
humide savanna. Plant and soil , 182-171-176.
68-Robitaille R., -Le point sur la
fertilisation en production biologique de la tomate de serre. Conseiller
régional en conservation des ressources, MAPAQ
Abitibi-TémiscamingueConseiller local en horticulture, Bureau de
renseignement agricole de La Sarre 357,Québec,15p.
69-Safiddine F., 2009-Contribution à
l'étude de la biodiversité de nématodes en Algérie
viticole,Projet de fin d'étude, d'ingénieur d'état en
agronomie, Protection des végétaux, Dep.Agr.,Univ.Saad Dahlab,
Blida, 44p.
70-Sánchez-Moreno S., Minoshima H.,
Ferris H and Jackson L. E.,1997 -Linking soil properties and nematode
community composition: effects of soil management on soil food webs.
71-Senghor K., 1998- Etude de l'incidence du
nématode phytoparasite Meloidogyne javanica sur la croissance
et la symbiose fixatrice d'azote de douze espèces d'Acacia (Africains et
Australiens) et mise en évidence du rôle des symbiotes endo et
ectomycorhiziens contre ce nématode. Projet d'obtention le grade de
docteur de 3ème cycle de Biologie Animale, n0 d'ordre 27,
Univ. Cheikh Anta Diop, Dakar, Fac. des Sciences et Techniques,123p.
72-Serrai O., 2009-La dégradation de
l'Oued Righ et son impact sur les oasis périphériques,
thèse .Magester.Hydraulique, Dep. D'Hydraulique et Génie
civil,Univ.Kasdi Merbah, Ouargla 85p.
74-Slifi M., 2009-Diversité de la
nématofaune dans quelques biotopes maraichers ; relations
nématodes propriétés physico-chimiques du sol,Projet de
fin d'étude, d'ingénieur d'état en agronomie, Protection
des végétaux, Dep.Agr.,Univ.Saad Dahlab, Blida, 87p.
75-Taylor L., 1968- Introduction à la
recherche sur les nématodes phytoparasites. Manuel FAO, Rome, 135p.
76-Villenave C., Fernadez P., Badiane A., Sène
M., Ganry F. et Oliver R., 1998 - Influence du travail du sol et
l'apport de compost sur les peuplements de nématodes phytophages. CD -
rom, Poster, Symposium n0 :32
,XVIè Congrès Mondial de
l'Association Internationale de science du sol.
77-Wardele, D.A.,Yeates, G.W.,Watson, R.N.,
Nicholason, K.S. , 1995-Development of decomposer food-web, trophic
relationships and ecosystem properties during a three-year primary succession
in sawdust. Oikos 73, 155-166.
78-Weill A. et Duval J., 2009-Tous droits
réservés. Equiterre, Module 7, Amendements et fertilisation --
Chapitre 12,« Les amendements organiques : fumiers et composts »,
manuscrit du Guide de gestion globale de la ferme maraîchère
biologique et diversifiée,19 p.
79-Yeates G.W., Bongers T., de Goede R.G.M., Freckman
D.W. et Georgieva S.S., 1993 - Feeding habits in soil nematode
families and genera-an outline for soil ecologists. J. Nematol. 25,
pp: 31-315.
80-Yeates G.W., Wardel D.A., Watson R.N., 1993b-
Relationships between nematodes ,soil microbial biomass and weed
management strategies in maize and asparagus cropping systems. Soil Biol.
Biochem. 25:869-76.
81-Yeates G. W., Orchard V.A., Speir T.W. Hunt J.L. et
Hermans MCC., 1994-Impact of pasture contamination by copper,
chromium, arsenic timber preservative on soil biological activity. Biol.
Fertil. Soils , 18 pp. 200-536.
82-Yeates G. W. et King, K. L., 1997 - Soil
nematodes as indicators of the effect of management on grasslands in the New
England Tablelands (NSW): Comparison of native and improved grasslands.
Pedobiologia 41, pp: 526-536.
.
ANNEXE
Tableau 7 : Nombre de galles rencontrés sur les
racines
|
Traitement
|
Nombre de galles
|
|
Grignon d'olive
|
41
|
|
Fumier
|
144
|
|
Témoin
|
40,5
|
|
vydate
|
99,5
|
Nombre des femelles dans des galles de racines dans :
Tableau 8 : Racine de grignon d'olive
|
Galles
|
Nombre de femelles(1)
|
Nombre de femelles(2)
|
|
1
|
0
|
2
|
|
2
|
1
|
0
|
|
3
|
1
|
1
|
|
4
|
0
|
1
|
|
5
|
1
|
1
|
|
6
|
1
|
2
|
|
7
|
0
|
0
|
|
8
|
1
|
0
|
|
9
|
1
|
1
|
|
10
|
1
|
1
|
Tableau 9 : Racine de fumier
|
Galles
|
Nombre des femelles(1)
|
Nombre des femelles(2)
|
|
1
|
0
|
1
|
|
2
|
0
|
2
|
|
3
|
3
|
1
|
|
4
|
1
|
0
|
|
5
|
0
|
1
|
|
6
|
1
|
2
|
|
7
|
0
|
1
|
|
8
|
1
|
2
|
|
9
|
1
|
1
|
|
10
|
1
|
1
|
Tableau 10: Racine de témoin
|
Galles
|
Nombre des femelles(1)
|
Nombre des femelles(2)
|
|
1
|
2
|
0
|
|
2
|
1
|
1
|
|
3
|
2
|
1
|
|
4
|
2
|
0
|
|
5
|
1
|
0
|
|
6
|
0
|
1
|
|
7
|
2
|
1
|
|
8
|
2
|
2
|
|
9
|
1
|
1
|
|
10
|
0
|
1
|
Tableau 11 : Racine de vydate
|
Galles
|
Nombre des femelles(1)
|
Nbre des femelles(2)
|
|
1
|
3
|
0
|
|
2
|
0
|
0
|
|
3
|
1
|
1
|
|
4
|
2
|
1
|
|
5
|
1
|
2
|
|
6
|
1
|
1
|
|
7
|
0
|
0
|
|
8
|
1
|
1
|
|
9
|
1
|
3
|
|
10
|
1
|
1
|
Tableau 11 : Nombre de femelles dans 10
galles
|
Traitement
|
Nombre de femelles
|
|
Grignon d'olive
|
8
|
|
Fumier
|
10
|
|
Témoin
|
10,5
|
|
Vydate
|
10,5
|
TABLE DES MATIERES
REMERCIEMENT
DEDICACES
ÕÎJ ã
RESUME
SUMMARY
SOMMAIRE
LISTE DES SYMBOLES ET ABREVIATIONS
LISTE DES FIGURES
LISTE DES TABLAUX
INTRODUCTION 1
Introduction générale 1
Partie bibliographique
Partie Bibliographique
Chapitre I : Données bibliographiques sur les
communautés
de nématodes associés aux cultures
maraîchères ..3
I.1.Généralités sur les nématodes
3
I.2.Les communautés de nématodes associés
aux cultures maraîchères 5
I.3.Bio écologie des nématodes 6
I.4. La diversité trophique des nématodes 8
I.5. Importance des nématodes dans les
écosystèmes 11
I.6.Action des facteurs abiotiques et biotiques sur les
nématodes 14
I.6.1.Influence des facteurs abiotiques 14
I.6.2.Influence des facteurs biotiques 14
Chapitre II. Donnés bibliographiques sur les
amendements organiques ...16
II.1. Généralités sur les amendements
organiques ..16
II.2. Différents types d'amendements organiques 16
II.3. Importance des amendements organiques 19
II.3.I. Effet sur le sol, la culture et les microorganismes
19
II.3.2. Effet sur les nématodes 20
Chapitre III. : Description de la plante hôte
« Tomate » .22
III.1. Généralités sur la tomate
maraichère 22
III.2. Taxonomie 23
III.3. Importance de la tomate en Algérie 23
III.4. Types de croissance et variétés de tomate
maraichère existantes en
Algérie 23
III.5. Exigence de la culture de tomate 24
III.5.1. Type de sol 24
III.5.2. Irrigation 24
III.6. Mode de conduite 24
III.6.1. Semis et repiquage 24
III.6.2. Eclaircissage 25
III.6.3. Eclaircissage des fruits 25
III.6.4. Effeuillage 25
III.6.5. Tuteurage 25
III.6.6. Taille 26
III.6.7. Aération 26
III.6.8. Gestion des mauvaises herbes 26
III.6.9.Récolte 26
Chapitre IV : Présentation de la région
d'étude
"D'Oued Righ" 27
IV.1-La situation géographique 27
IV.2-Facteurs édaphiques 28
IV.2.1- Géologie de la région 28
IV.2.2- Caractéristiques pédologiques 29
IV.2.3 -Hydrologie de la région 29
IV.3-Les facteurs climatiques 29
IV.3.1.Températures 29
IV.3.2. Pluviométrie et précipitation 30
IV.3.3. Durée d'insolation: 30
IV.3.4. Vents 30
IV.3.5. Humidité 30
IV.3.6. Evaporation 30
IV.3.7.Synthèse climatique de la région de
Touggourt
IV.3.7.1- Diagramme ombrothermique de Gaussen dans la
région étudiée
de Touggourt 31
IV.3.7.2-Climagramme d'Emberger appliqué au niveau de la
région de
Touggourt 31
Partie Expérimentale
|
Chapitre I : Matériels et méthodes
I.1. Description des amendements utilisés
|
32
..32
|
|
I.1.1. Les grignons d'olives
|
32
|
|
I.1.2. Caractéristiques chimiques
|
32
|
|
I.2. Matériels
|
33
|
|
I.2.1. Origine les amendements organiques utilisés
|
..33
|
|
I.3.Méthodologie
|
33
|
|
I.3.2. Préparation de la parcelle de travail
|
33
|
|
I.3.3. Prélèvement des échantillons
|
34
|
|
I.3.4. Extraction des nématodes du sol
|
. .34
|
|
I.3.5. Dénombrement et identification des taxons
|
.35
|
I.3.5.1. L'effet des traitements sur estimation du taux
d'infestation des racines
par les larves (L2) de Meloidogyne .35
I.3.5.2. Estimation du taux de développement des larves
(L2) en femelles
36
|
I.4. Exploitation des résultats
|
37
|
|
I.4.1. L'analyse multi variée
|
37
|
|
I.4.2. Analyses de variance (SYSTAT vers. 12, SPSS 2009)
|
.38
|
CHAPITRE II : Résultats et Discussion
II.1. Inventaire de la communauté de nématodes
rencontrés dans la parcelle d'étude
sur cultures maraîchères 39
II.2. Répartition temporelle de la densité moyenne
globale des nématodes (N/50g de
sol) en fonction des traitements 42
II.3.Répartition temporelle des groupes trophiques en
fonction des
traitements 44
II.4. Effet des traitements sur la
répartition des nématodes phytophages ...47
II.5.Effets des traitements sur la répartition des
Meloidogyne 50
II.6. L'effet des traitements sur le nombre de galles ...53
II.7.Effet des traitements sur le nombre des femelles: 54
Discussion générale 56
Conclusion générale 61
Références bibliographique 63
Annexes
Table des matières
| 


