
REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET POPULAIRE
Ministère de l'Enseignement Supérieur et de la Recherche
Scientifique
Université IBN KHALDOUN -Tiaret-
Faculté des Sciences Agronomiques et
Vétérinaires
Département des Sciences Agronomiques et
Biologiques
Mémoire de fin d'études
En vue de l'obtention du diplôme d'étude
supérieures
En biologie
Spécialité : Biochimie
|
Effet de la température sur l'évolution
de l'HMF dans les miels
Algériens
|
Présenté par : Melle MAZROU
KELTOUMA
Membres de jury
Président :
Promoteur : Mr. HOCINE. L
Examinateurs : Mme. MAKHLOUFI.C
Promotion 2007 - 2008
Remerciements
Je tiens à remercier tous ceux qui,
D'une façon ou d'une autre, m'ont aidé
pendant mon travail de fin d'études.
Certains par leurs conseils et
leurs connaissances scientifiques, d'autres par
Leur soutien et leur
présence dans les moments les plus pénibles.
Mes premiers
remerciements vont à mon promoteur Mr HOCINE.L, pour avoir
accepter
de m'encadrer et de me suivre tout au long de la réalisation
de ce mémoire de fin d'étude.
Je voudrais également
rendre un hommage particulier à Mr SASSI pour son soutien et
son
aide.
Merci à tous les membres de jury qui ont
accepté de juger mon travail,
Tous ceux qui m'ont accueilli et aidé un moment ou
à un
Autre de mon travail. Je leur en sais gré.
La vie d'un laboratoire ne se limite heureusement pas
à la pratique de la
Science. Merci à tous mes collègues
du labo pour tous les bons moments passés,
également à
MEDKOUR, CHAHRA, HANANE, SOUMIA,RATIBA, FATY et son
trinôme , CHERIFA,
AMINE, MERIEME,SAFA et son trinôme, DENIA et son
binôme, pour
leur
Gentillesse, leur disponibilité et leur
compétence, Merci du fond du coeur.
Je terminerais en rendant hommage
à tous les enseignants du primaire, du
Secondaire et de
l'université qui m'ont donné le goût des études.
Leur tâche
Est ingrate et trop peu souvent reconnue. Je leur dois
beaucoup.
Dédicace
Au nom du DIEU clément et
miséricordieux et que le salut de DIEU soit sur son
prophète
MOHAMED
De ma part, et avec des grands sentiments et d'une joie
immense que je dédie ce travail à mes chers parents, qui sont
à l'origine de mon existence, que DIEU les protège, ils m'ont
soutenu le long de l'élaboration de ce travail.
A ma très chère mère mon modèle
à suivre qui m'a entouré d'amour et de tendresse et m'a
appris la patience et le défit.
Amon très cher père qui m'a encouragé
et conseillé pendant mes plus pénibles moments et qui
m'a guidé vers le chemin droit.
A ma très chère frangine NASSIMA pour son
aide, son encourage sans oublier ses amis et mon
très cher frangin
SOFIANE.
A mes très chères tantes HAKIMA et SEDDA et
mes oncles KARIM, REDOUANE, FOUDEL
et REZAK.
A ma délicieuse petite soeur SANDRINE que je
remercie pour ses prières.
A mes grands pères : LEHSEN,
MADJID.
A mes grands-mères : THAKLIT, FATIMA.
A AMINE et BOUCHRA qui m'ont encouragé et
conseillé pendant mes plus pénibles moments et à
tous
les gens de KSAR CHELLALA.
A tous mes cousins en particulier LYES qui m'a beaucoup
aidé.
A mes soeurs : AMINA, BOUCHRA, NOURA,
LAMIA, MALIKA, AMINA, AICHA, FATIMA,
NAJET, WARDA, KHADIJA, TASSADITE,
FATOUM, KARIMA, YAMNA et SIMLA sans
oublier ma jolie FATY qui ma beaucoup
aidé.
ET enfin, à tous mes collègues de la
promotion 4ème année Biochimie, Microbiologie, physio
A et
Agronomie (200 7/2008) Et à tous les
vétérinaires.
A tous les membres de la famille : SAIBI surtout les petits
MOHAMED et OUMAIMA.
SOMMAIRE
Partie bibliographique
Introduction
Chapitre ² : Généralités sur le
miel
1-Définition du miel 02
2-Origine du miel 02
2-1-Nectar 02
2-2-Miellat 02
3-Autres origine du miel 02
4-Foramation du miel 03
5-Recolte et extraction du miel 04
6-composition chimique du miel 05
6-1-composition majeurs 05
6-1-1-Eau 05
6-1-2-Glucides 05
6-2-composition mineurs 05
7-Propriétés physico-chimiques du miel 06
7-1- Propriétés physique 06
7-2- Propriétés chimique 08
8-Autre produit de la ruche 08
9-Qualités des miels 10
9-1-Critéres de qualités des miels 10
9-1-1-Humidité ou teneur en eau 10
9-1-2-Teneur en HMF 10
9-1-3-Acidité diastasique ou amylasique 11
9-1-4-Acidité libre 11
9-1-5-Teneur en glycérol 11
Chapitre ²² : Importance de l 'H.M.F dans le
miel.
1-Définition du H.M.F 12
2-Structure et propriétés du HMF 12
3-Formation du HMF 13
4-Les paramètres influencent l'apparition d'HMF dans le
miel 14
4-1- pH 15
4-2- teneur en eau 15
4-3- vieillissement 15
4-4- température 16
5-Utilisation 18
6-conseils pou limiter l'HMF dans le miel 18
Partie expérimentale
Chapitre ² :
Matériels et Méthodes
1 -Etude expérimentale 19
2-Echantillons de miel 19
3-protocole expérimental 20
4-appareillge 21
5-produit chimiques 21
6- Méthodes 22
6-1- Méthodes physico-chimique 22
6-1-1-Détermination de la teneur en eau 22
6-1-2-Détermination de l'HMF 23
Chapitre ²² : Résultats et
Discussions
1-Analyse physicochimique 25
1-1- La teneur en eau 25
1-2-H.M.F 27
2- Analyse sensorielles 30
Conclusion
Référence bibliographique Annexe
INTRODUCTION
Le miel est un aliment énergétique que
l'humanité connaît depuis la nuit des temps. Il est très
riche en sucre, acides, vitamines.. .etc.
L'origine du mot miel est à rechercher dans le mot
sanskrit medhu connue sous le non de melikraton durant toute
l'antiquité.
Les livres saints comme le coron et la bible ne manquent pas de
louer les vertus du miel, il est le symbole de la prospérité et
de l'abondance.
Le miel a fait, ces dernières années, l'objet de
plusieurs recherches, puisque le miel comme d'autres denrées
alimentaires présente des caractéristiques physiques et chimiques
qui nécessitent des études approfondies.
Comme tout produit biologique, le miel subit au cours du temps
des modifications qui ont une importance plus ou moins grande pour sa
conservation. Il est donc utile de bien connaître les principaux facteurs
qui peuvent altérer sa qualité dont la température est le
principal facteur qui dégrade les sucres conduisant ainsi à la
formation d'hydroxyméthylfurfural qui altère la qualité du
miel.
Dans le but d'étudier l'évaluation des effets du
chauffage du miel à différentes températures sur les
principaux paramètres de qualité du produit, nous avons
effectué cette étude qui a apporté certaines informations
de l'effet de la température sur l'évolution d'H.M.F dans le
miel.
C'est pour cette raison nous avons traité les
échantillons à différentes températures de
40°C à 100°C .et nous avons fait des analyses pour la
détermination d'éventuelles modifications survenue dans les
différents paramètres physique et chimiques.
1-Définition du miel :
D'après DONADIEU (2003), Le miel est
la denrée produite par les abeilles mellifiques à partir du
nectar des fleurs ou de certaines sécrétions provenant de parties
vivantes de plantes ou se trouvant sur elles, qu'elles butinent, transforment,
combinent avec des matières spécifiques propres, emmagasinent et
laissent mûrir dans les rayons de la ruche. Cette denrée peut
être fluide, épaisse ou cristallisée.
2-Origine du miel :
Selon ANCHLING (2005), le miel est
élaboré par les abeilles à partir de sucres produits par
des végétaux, soit sous forme de nectar, soit sous forme de
miellat.
2-1-Nectar :
Liquide plus ou moins doux et parfumé produit par les
fleurs des plantes supérieures (BIRI ,1976).
D'après SCHWEITZER (2005a) Selon leurs
origines végétales, les nectars contiennent plus ou moins du
saccharose. On les classe en :
Des nectars à saccharose prédominant ;
Des nectars à taux égaux de saccharose, fructose et
glucose ;
Des nectars avec prédominance du glucose et du
fructose.
2-2-Miellat :
Selon BIRI (1999), le miellat est un liquide
sucré produit par plusieurs espèces d'insectes parasites vivant
sur les feuilles de nombreuses plantes.
Le miel de miellat présente une couleur ombre
foncé. Son goût est agréable, il est très riche en
sels minéraux.
Contrairement aux nectars, les miellats contiennent beaucoup
d'éléments indigestes pour l'abeille y compris certains sucres
polyholosides (SCHWEITZER, 2004a).
3-Autres origines du miel :
Il existe aussi du « miel de sucre »; miel produit par
des abeilles nourries à l'aide de sucre (APFELBAUM et
al, 2004), et quelquefois fruits, cannes à sucre,etc
(SCHWETZER,2004a ).
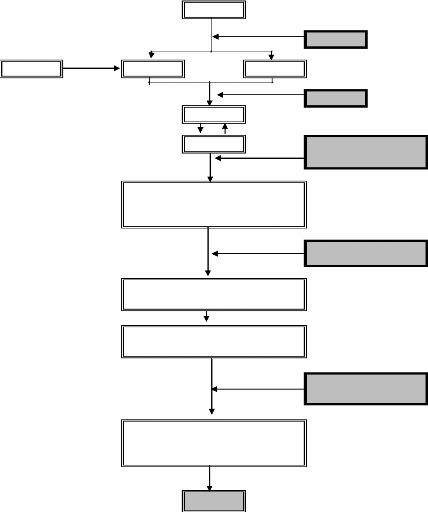
4-formation du miel
:
La figure N° 01 résume les
différentes étapes de la formation du miel
Abeille
Miel
Augmentation du taux de sucre (glucose,fructose..)
sous l'action de l'invertase.
Miellat
Nectar
Jabot
Jabot
Protection dans les rayons
de cire
Evaporation dans les rayons
par battement des
ailes
Evaporation d'eau, en refoulant le contenu qui s'ecoule
en une goutte étalée sous la trompe .
puceron
Recolte
Stockage
Séchage actif 15 à 20 min
Séchage passif
4 à 5 jours
Transformation
chimique
Figure N° 01 1: les principales
étapes de la formation du miel. (MAURIZIO (1965) cité par
CHAUVIN (1968) et ANCHLING ( 2005 ) ) 5-Recolte et extraction de miel
:
La période de prélèvement des cadres de
miel varie suivant les années, les régions et la flore
mellifère. En principe on opère quand les cadres de miel sont aux
2/3 operculés (IDPE, 1985), lorsque ces conditions
seront remplies, nous choisirons une belle journée sans vent, pour
récolter dans des conditions optimales de sécurité, tant
pour l'apiculteur que pour l'environnement humain ou animal (CARTEL
,2002), ensuite on procède à l'extraction du miel dont
les principales étapes sont résumées dans le
tableau N° 01.
Tableau N°01 : les étapes d'extraction de
miel.
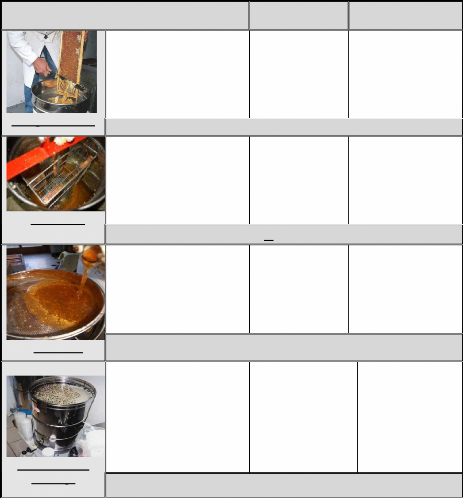
Désoperculation
Maturation et
stockage
Extraction
Les étapes d'extraction dans l'ordre
Filtration
Désoperculer les alvéoles au moyen d'un couteau
à désoperculer.
Faire séjourner le miel dans un maturateur, puis
conditionner le miel dans des pots. Il est ensuite stocké, autant que
possible dans un local sain, à une température la plus
constante possible.
Le miel est extrait des cellules par la force centrifuge.
Le miel est alors recueilli sur un filtre, pour retenir les
débris de cire.
(IDPE ,1985 ; MARY, 2003 et CARTEL ,2006)
(DANADIEU ,1981 et ANCHLING ,2005)
(HUCHET et al, 1996 et BIRI ,1976)
(IDPE, 1985 et PHILIPPE ,1999)
La vitesse de rotation doit au début être lente puis
augmentée progressivement sans excès.
Seuls l'inox et le plastique alimentaire sont autorisés
pour son élaboration ou sa conservation.
Il est préférable de maintenir la
température du tranchant de la lame voisine à 49°C.
La température idéale de conservation est de
14/16°C .mais c'est aussi celle favorable à une cristallisation
rapide.
Remarque
Parce que les températures supérieures
provoquent l'apparition de HMF.
Pour que les rayons ne soient pas endommager.
Parce que le miel est acide.
Parce que à plus grande température la
cristallisation est ralentie, mais le processus de vieillissement
accéléré
Pourquoi
6-Composition chimique du miel :
6-1-Composition majeure :
6-1-1-Eau :
Selon HUCHET et al (1996), l'eau est
présente en quantité non négligeable puisque sa teneure
moyenne est de 17,2%, mais comme le miel est un produit biologique, cette
valeur peut varier. En fait, les abeilles operculent les alvéoles
lorsque la teneur en eau avoisine 18%.
6-1-2- Glucides :
D'après LOUVEAUX (1968) les glucides
représentent de 95 à plus de 99% de la matière
sèche des miels
Parmi ces sucres, figurent le fructose et le glucose, que l'on
trouve en quantité voisine dans les miels. Cependant, le rapport de la
quantité de fructose sur la quantité de glucose est très
importante et varie de 0,76 à 1,76 environ , ainsi le saccharose dont la
quantité peut aller jusqu'à 7% et le maltose dont la
quantité varie de 2 à 7% (KHENFER et FETTAL,
2001).
6-2- Composants mineurs :
Ce sont les acides, les protéines et amino-acides, les
vitamines, les enzymes, les minéraux. Ces différents
éléments ont été regroupés dans le
tableau N°02
Tableau N 02° : les composants mineurs du
miel.
|
Acides 0,3%
|
Protéines Amino-acides 0,4%
|
Vitamines
|
Minéraux
0,2%
|
Divers
|
Enzymes
|
|
Acide
gluconique A-acétique A-citrique
A-lactique A-malique A-oxalique A-butyrique
A-pyroglutamique A-succinique A-formique
|
-Matières albuminoïdes
-Matières azotées
-Traces : Trypsine Leucine Hystidine Alamine
Glycine Méthionine
A. Aspartique
|
Thiamine Riboflavine Pyridoxine Acide pantothénique A-
ascorbique A- nicotinique Biotine
A- folique
|
-Calcium -Chlore -Cuivre
-Fer
-Magnésium -Manganèse -Phosphore -Potassium
-Silicium -Sodium -Soufre
|
-Esthers volatiles
-Acétylcholine -Pigments
-Colloïdes -Facteur antibiotique
|
-Invertase -Amylase
-Catalase -Phosphatase
-Gluco-oxyase
|
|
HUCHET et
al (1996)
|
KHENFER
et FETTAL
(2001)
|
LOUVEAUX
(1968)
|
DONADIEU
(1978)
|
KHENFER
et FETTAL
(2001)
|
LOUVEAUX
(1985)
|
On sait peu de chose sur les pigments qui donnent au miel sa
couleur. Il est probable qu'ils appartiennent aux groupes des
caroténoïdes et des flavonodes (LOUVEAUX, 1985) et
un certain nombre de substances encore mal connues donnent au miel des
propriétés antibactérienne (CLEMENT
,2003).
7-Propriétés physico-chimiques du
miel :
7-1-Propriétés physiques :
7-1-1-Densité :
D'après KERRAR (1994), NACER
(1994), HENNI (1997) la densité des miels
algériens varie entre 1,422 1 et 1,4328 cité par BENRAHAL
(1997).
7-1-2-Viscosités :
Elle diminue quant la température s'élève
jusqu'à 30°C. Elle est fonction de la température, de la
teneur en eau et des autres constituants du miel, en particulier de la
composition des différents sucres (JEAN-PROST,
2005).
7-1-3-Chaleur spécifique :
Pour se réchauffer le miel demande deux fois moins de
calories que le même poids d'eau. Mais il transmet très mal la
chaleur qu'il reçoit de sorte qu'il peut être
réchauffé rapidement en un point et rester froid tout à
coté (JEAN-PROST, 1987).
7-1-4-Conductivité thermique :
La conductivité thermique du miel est de
1,29.10-4 calorie par cm (cal/cm) (GONNET, 1982).
7-1-5-Conductivité électrique :
La conductivité électrique représente un
bon critère pour la détermination de l'origine botanique du miel.
Cette mesure dépend de la teneur en minéraux et de
l'acidité du miel, plus elles sont élevées, plus la
conductivité correspondante est élevée (PIAZZA et
al, 1991) in (BOGDANOV, 1999).
7-1-6-Indice de réfraction :
D'après DONADIEU (1978), plus l'indice de
réfraction augmente, plus la teneur en eau du miel diminue. Il est de
1,47 à 1,50 à la température de 20°C.
7-1-7-Coloration :
La coloration des miels est une donnée importante parce
que c'est une caractéristique physique dépendant de l'origine du
produit mais également un élément sensoriel primordial qui
détermine en partie le choix du consommateur (SCHWEITZER,
2001a).
7-1-8-L'hygroscopicité du miel :
D'après JEAN-PROST et LE CONTE (2005),
elle est telle qu'un miel à 18% d'eau se trouve en équilibre dans
une atmosphère, dont l'humidité relative est de 60%.
7-1-9-Flurescence :
Sous l'action d'une lumière ultraviolette, beaucoup de
miels présentent une légère fluorescence (CHAUVIN,
1968)
7-2-Propriétés chimiques : 7-2-1-
Acidité :
L'acidité est un critère de qualité,
dû aux acides organiques présent dans le miel
(BOGDANOV, 1999). La norme européenne
pour le miel fixe une valeur maximale de 50milliéquivalent/kg
(BOGDANOV, 2005).
7-2-2- pH :
Sa valeur varie en général entre 3,5 et 5,5 ; elle
est due à la présence des acides organiques (BOGDANOV et
al, 2004).
Selon SCHWEITZER (2005a), les miels de nectar,
très acides, ont un pH compris entre 3,5 et 4,5. Les miels de miellats,
moins acides, ont un pH supérieur à 4,5.
7-2-3- HMF :
Au niveau mondial le miel ne doit pas posséder une teneur
en HMF supérieure à 80 mg/kg, le taux maximum a été
fixé à 40mg/kg dans l'union européenne (JEAN-PROST
et LE CONTE, 2005)
8- Autres produits de la ruche
:
Le tableau N° 03 englobe les
définitions, compositions et propriétés des produits de la
ruche (la cire, gelée royale, pollen, propolis et venin )
Tableau N°03 : les produits de la ruche.
|
produit
|
définition
|
Composition
|
propriétés
|
|
La cire est une substance grasse secrétée par les
quatre paires de glandes à cires, ce sont des corps chimiquement stables
.elles résistent à l'hydrolyse et à l'oxydation.
|
Hydrocarbure 12% Acide libres 13% Esters 72%
|
Emollientes Cicatrisantes Anti-inflammatoire
|
|
PHILIPPE (1999) et
CHAUVIN (1968)
|
D'après WARTH (1947) in
BARBIER
(1968)
|
DONADIEU et
MARCHISET
(1984)
|
|
C'est une sécrétion produite par des glandes
situées dans la tête des abeilles ouvrières, et
particulièrement actives chez les abeilles entre 5 et 14
jours.
|
Eau 60 à 70 %
Hydrates de carbone 11 à
23%
Protéine et acides aminées 9à 18%
Lipides 4 à 8 %
Et une petite quantité de sels minéraux et
vitamines.
|
Stimulante et tonifiante. Rééquilibrante et
revitalisante.
|
|
BIRI (1999)
|
BOGDANOV et al (2006)
|
DONADIEU (1999)
|
|
C'est une fine poussière produite par les étamines
des fleurs, les abeilles le récoltent sous forme de petites pelotes
qu'elles transportent à la ruche dans les corbeilles de leurs pattes.
|
Eau
Hydrate de carbone Fibre alimentaire
Protéine et acide aminé Lipide
Sels et minéraux
Vitamine
|
Tonifiant et
stimulant générateur. Rééquilibrant
Désintoxiquant.
|
|
LAGACHERIE et CABANNES (2001)
|
MSDA (2004)
|
DONADIEU (1982)
|
|
C'est une résine employée par les abeilles ayant
une origine externe ; la récolte sur les bourgeons d'arbre, et une
origine interne ; régurgutation des substances résineuses
provenant des pollens.
|
Résine et baumes 50-55% Cire 25-35%
Huiles volatiles 10%
Pollen 5%
Matières diverses organiques et minérale 5%
|
Antiseptiques Cicatrisantes. Anti-inflammatoires Antivirales
|
|
LAVIE (1968)
|
DONADIEU (1998)
|
JEAN-PROST et
LE CONTE (2005)
|
|
C'est un liquide semblable à un sirop, de couleur
jaunâtre et opalescent. Son goût est amer, son odeur semblable
à celle du miel et son pH est acide.
|
Beaucoup d'eau,
Une histamine, la melittine, protéine
relativement simple, Une lysolécithine, l'apamine, 2
enzymes.
Un peptide.
|
Hypothétiques (favoriserait la défense de
l'organisme contre
la genèse de certaines maladies tissulaires)
|
|
BOGDANOV et al (2006)
|
JEAN-PROST (1987)
|
DONADIEU et
MARCHISET
(1984)
|
9- Qualités des miels :
9-1-Critères de qualités des miels :
9-1-1-Humidité ou teneur en eau :
D'après le CETAM (2002) cité
par AMRAOUI et DROUI (2005), l'humidité est un
paramètre de qualité, car la teneur en eau conditionne l'avenir
du miel : cristallisation et fermentation. Le risque de fermentation est
d'autant plus élevé que la teneur en eau est grande, Comme le
montre le tableau N° 04
Tableau N° 04 : Effet de la teneur en eau
sur le risque de fermentation dans le miel (SCHWEITZER,
2001b).
|
Teneur en eau
|
Son effet sur le risque de fermentation dans le
miel
|
|
A moins de
17,1%
|
Quel que soit leur nombre, les levures ne peuvent se
multiplier, la pression osmotique est importante, le miel ne peut
donc fermenter.
|
|
De 17,1 à 18%
|
Pas de fermentation si le nombre de levure est inférieur
à 1000 par gramme.
|
|
De 18,1 à 19%
|
Pas de fermentation si le nombre de levures est inférieur
à 10.
|
|
De 19,1 à 20%
|
Pas de fermentation si le nombre de levures est inférieur
à 1.
|
|
Au dessus de
20%
|
Risque de fermentation dans tous les cas.
|
9-1-2-Teneur en HMF :
D'après FREYTAGE (2007), L'HMF est un
des facteurs de la qualité du miel. À la récolte, le miel
n'en possède pas, mais le temps et la température favorisent sa
formation. Or, les normes légales acceptent jusqu'à 40 mg
d'HMF/kg.
9-1-3-Activité diastasique ou amylasique
:
D'après LOUVEAUX (1968), au cours de
vieillissement à la température ordinaire, la teneur en enzymes
du miel tend progressivement vers zéro.
9-1-4-Acidité libre :
La teneur en acide libre varie selon la variété
de miel. Dans les miels de miellat, elle est généralement
supérieure à celle des miels de fleurs. C'est également
une mesure pour la fermentation du miel (BOGDANOV et al,
2005).
9-1-5- Teneur en glycérol :
D'après BECKER et SCHWEITZER (2000),
la présence du glycérol est naturellement faible dans les miels
du fait de quelques levures. La corrélation est parfaite entre le taux
de glycérol dans le miel et l'importance de la fermentation subie par
celui-ci.
Les miels ne doivent pas contenir plus de 300mg/kg de
glycérol, sinon il ne sera plus commercialisé CETAM
(2002).
1-Définition du HMF :
Selon SCHWEITZER (2001c) et ANDRIEN
(2006), L'HMF est l'abréviation usuelle du 5-
HydroxyMéthyl-2-Furfural. Sous cette dénomination se cache un
aldéhyde aromatique isolé pour la première fois en 1832,
que l'on synthétise à partir du fructose obtenu à partir
de produits agricoles.

L'HMF est un produit intermédiaire dans la réaction
de Maillard (ANGEL et al, 2001). 2- Structure et
propriétés du HMF:
Le Tableau N°05 montre les
différentes propriétés de l'HMF.
Tableau N°05 : les différentes
propriétés de l'HMF (WIKIPEDIA, 2008 ; MAHLOUFI et ROGE,
2008).
|
Hydroxymethylfurfural
|
|
Formule cyclique
|
|
|
Formule moléculaire
|
C6H6O3
|
|
Masse molaire
|
126,11 g/mole
|
|
Densité
|
1,29 g/cm3
|
|
Couleur
|
absence
|
|
Odeur
|
absence
|
|
saveur
|
Amère
astringente
|
D'après BORNECK et GONNET
(1976) cité par BETTAHER et YAKDOUMI
(2006), l'hydroxyméthylfurfural (HMF) n'entre pas normalement
dans la composition des miels, sa présence à l'état de
traces est toutefois tolérée, mais elle ne doit pas
dépasser un seuil fixé par la loi, qui est de 40mg/kg à
l'exception du miel distiné à l'industrie et pas plus de 80mg/kg
pour les régions tropicales (Journal officie des
Communité Européen, 2002).


Donc ce paramètre est un bon indicateur de la
fraîcheur du miel (BOGDANOV et al, 2000), puisque l'HMF
est un composé mutagène mais qui reste controversé
(JANZOWSKI et al, 2000 ; et LEE et al, 1995 ; cité par AIT
AMEUR, 2006).
D'ailleurs, il a été retrouvé responsable de
l'initiation de la promotion de tumeur chez le rat (GIOVANNUCCI, 1995 ;
WCRF, 1997 ; cité par KESS, 2002).
3- Formation d'HMF :
La formation d'HMF provient d'une dégradation lente du
fructose lequel, en milieu acide, se décompose et perd trois
molécules d'eau selon la réaction suivante :
CHOH-CHOH HC-CH
-3H2O
HO-CH2-CHOH CHOH-CHO HO-CH2-C C-CHO
O
hexose HMF

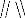

Ce processus est également accéléré
par le chauffage.
La présence d'HMF dans les miels est donc un
révélateur de dégradation plus ou moins avancé de
produit (GONNET, 1992 ; cité par MAKHLOUFI, 2001).
Et comme l'HMF est utilisé dans d'autres
intérêts, des chercheurs de l'Université du Wisconsin-
Madison aux Etats-Unis viennent de développer un nouveau
procédé de synthèse du HMF à partir du fructose
caractérisé par un rendement amélioré et une
extraction plus facile du produit. La déshydratation du fructose est
réalisée en phase aqueuse en présence d'un catalyseur
acide (acide chlorhydrique ou résine échangeuse d'ions acide)
additionné de DMSO (dimethylsulfoxyde) afin d'éviter des
réactions parasites.
Les chercheurs ont également augmenté la
solubilité du HMF dans le solvant réactionnel, la MIBK (methyl
iso butylène cétone), en lui ajoutant de petites quantités
de butanol-2, ce qui facilite l'extraction du HMF de la phase aqueuse en cours
de procédé et avant qu'il ne réagisse avec elle.
La récupération du produit se fait ensuite
après distillation du solvant, avec l'avantage que la MBIK
possède un point d'ébullition relativement bas qui
améliore le rendement d'extraction du HMF (ANDRIEN,
2006).
La figure ci- dessus montre en série : Fructopyranose
(1), fructofuranose (2), et deux intermédiaires de l'étape de la
déshydratation (non isolé) (3, 4) et finalement HMF (5)
(WIKIPEDIA, 2008).
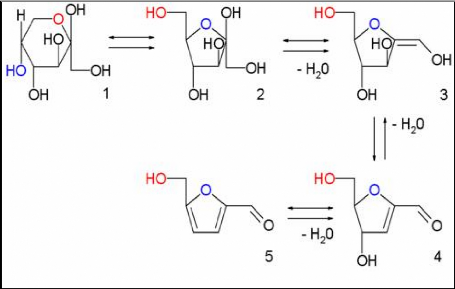
La figure N°02 : synthèse
d'HMF (WIKIPEDIA, 2008). 4- Paramètres influençant
l'apparition d'HMF dans le miel :
D'après MORCEAU et al (1994),
l'apparition de ce composé est le résultat de la transformation
des sucres simples et plus particulièrement du fructose en
hydroxymethylfurfurale, 5-(hydroxyméthyl)-2 furaldehyde (HMF).
L'acidité et la teneure en eau élevées
favorisent cette transformation, mais l'excès de chaleur et un
entreposage prolongé sont des facteurs encore plus importants dans ce
processus.
4-1- pH :
Selon SCHWEITZER (2001c), les miels acides
sont plus sensibles à la production d'HMF : un miel avec un pH de 3,5
à 4,0 en produit rapidement, alors que les miels de miellat qui ont des
pH élevés (sapin, châtaignier) en produisent beaucoup moins
rapidement.
4-2-Teneur en eau :
L'activité de l'eau est un paramètre
fondamentale dans la production de l'HMF (KROH, 1994 cité par
AIT AMEUR, 2006 ). D'un coté la quantité d'eau doit
suffire pour la solubilisation et l'hydrolyse du saccharose mais d'un autre
coté, la formation d'une mole d'HMF par une mole de fructose ou bien
glucose, a besoin de libérer 3 moles d'eau, ce qui explique que beaucoup
d'eau inhibe la réaction et celle-ci est valable aussi pour la
réaction de maillard (AIT AMEUR, 2006).
4-3-Vieillissement :
Selon CHAUVIN (1968), le vieillissement du miel
à la température ordinaire aboutit à une
dégradation progressive qui se traduit par :
> Une perte de substances volatiles qui contribuent à
l'arome du miel,
> Une augmentation de la coloration, de la teneur en HMF, de
l'acidité,
> Une modification du spectre des sucres dans le sens d'un
enrichissement en sucres supérieures. > Une réduction de
l'importance des hexoses, une destruction des diastases.
L'indice du HMF n'augmente pratiquement pas la première
année, mais s'accroît fortement aux cours des deux années
suivantes (PHILIPPE, 1999), comme le montre bien le
tableau N°06
Tableau N°06 : effet du stockage sur l'HMF
et l'activité enzymatique (BOGDANOV, 1999).
|
Température de
stockage
|
Temps nécessaire
à la formation de 40mg HMF /kg
|
Durée de demi-vie diastase
|
Durée de demi-vie invertase
|
|
10°C
|
10-20 années
|
35 années
|
26 années
|
|
20°C
|
2-4 années
|
4 années
|
2 années
|
|
30°C
|
0,5-1 années
|
200 jours
|
83 jours
|
|
40°C
|
1-2 mois
|
31 jours
|
9,6 jours
|
|
50°C
|
5-10 jours
|
5,4 jours
|
1,3 jours
|
|
60°C
|
1-2 jours
|
1 jours
|
4,7 heures
|
|
70°C
|
6-20 heures
|
5,3 heures
|
41 minutes
|
D'après SCHWEITZER (2004b), tous les
miels vieillissent et se dégradent pourtant certains le font plus ou
moins vite. Il existe des miels de longue et de courte conservation, ce qui
influe sur la rapidité de vieillissement, la température de
stockage et l'acidité.
4-4-Température :
CERVANTES et al (2000), rapportent que la
température est le principal élément qui doit être
contrôlé pour avoir un miel de bonne qualité. Le chauffage
du miel peut accélérer certaines réactions chimiques
susceptibles d'entraîner la baisse de la qualité du produit durant
l'entreposage. Ce phénomène pourrait être la
conséquence d'une action catalytique des acides présents dans le
miel sur les sucres déterminant la hausse du taux de certains
composantes, dont le HMF et l'apparition dans le même temps des pigments
de couleur foncée qui altèrent la couleur initiale.
BOGDANOV (1999), affirme que la couleur du
miel devient plus foncée lors du stockage à la chaleur et
à la lumière comme le montre bien la figure N°03
où la dégradation de la couleur des trois
échantillons du même miel, conservés de manières
différentes, est bien constatée :
Miel de gauche, stocké à la lumière et
à température ambiante. Miel du milieu, stocké dans
l'obscurité et à température ambiante. Miel de droite,
stocké dans l'obscurité et à température de
15°C.

Figure N° 03 : la dégradation de
la couleur des trois échantillons du même miel qui ont
été conservés de manières différentes
(BOGDANOV, 1999).
Mais le taux d'HMF est le critère le plus important et
le plus fiable pour détecter les miels surchauffés, d'autant plus
que si l'HMF est absent, les miels sont frais (KARABOURNIOTI et
ZERVALAKI, 2001).
SCHWEITZER (2005b), affirme que plus la
température augmente plus un miel contient d'HMF et voit ses enzymes
disparaître. D'ailleurs, les températures élevées
ont sur le miel un effet assez semblable à celui du vieillissement. Les
basses températures ont, au contraire, un effet de protection contre le
vieillissement par blocage des réactions enzymatiques et chimiques.
Le miel stocké à la température ambiante
à 20°C pendant 2 à 4ans, atteint le seuil critique
(SCHWEITZER, 2004c).
Donc l'utilisation du traitement thermique dans le but
d'élimination de cristallisation ou bien pasteurisation, peut augmenter
la quantité de l'HMF. Et pour cela le temps du traitement thermique doit
être plus court que possible, par exemple : un traitement pendant 90s
à 130°C donne approximativement la même augmentation d'HMF
que pendant 30s à 150°C de traitement, voir
figure, (TOSI et al, 2002).
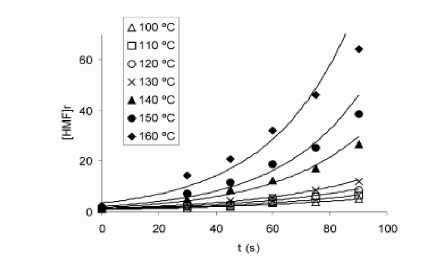
Figure N° 04 : l'évolution de
H.M.F à différentes températures pendant différent
temps (TOSI et al,
2002).
5-Utilisation :
Il peut servir de molécule de base pour fabriquer ensuite
des composés organiques, matières plastiques ou carburants
(ANDRIEN, 2006).
Cependant, il est souvent dosé dans les aliments
sucrés comme indicateur de la qualité du traitement thermique
appliqué à l'aliment.


Il est très utilisé pour évaluer la
conservation du miel et l'utilisation de la chaleur pour faire fondre les
cristaux de sucres (TOSI et al ,2002 ; ZAPPALA et al ,2005 ;
cité par AIT AMEUR, 2006).
6-Conseil pour limiter l'HMF dans le miel :
Selon LE BRUN (2006), les conseilles pour
limiter l'HMF dans le miel :
> Eviter au maximum de chauffer le miel dans toutes les
étapes d'extraction.
> Stocker son miel dans de bonnes conditions. Un stockage
à15°C ou moins est le plus adéquat, mais difficile à
réaliser. En tout état de cause, il faudrait ne pas
dépasser les 20°C.
> Ne jamais laisser un miel aux rayons du soleil.
> Dans la limite du possible, le consommer assez
rapidement.
1-Etude expérimentale :
L'étude expérimentale a été
réalisée au niveau du laboratoire de biochimie du
département des Sciences agronomiques et biologiques. Elle s'est
déroulée entre le 19 février jusqu'à le 08 mars
2008.
2-Echantillons de miel :
Les échantillons des miels étudiés
proviennent de différentes régions (Tiaret et Boukaddir.)
L'étude a porté sur 05 échantillons de différentes
années, 2005,2006 et 2007. Nous avons attribué à chaque
échantillon un numéro comme il est montré sur le tableau
N° 07.
Chaque échantillon est réparti en 05 lots, avec
des étiquettes portant la température de traitement. L'un a
été analysé sans chauffage et les quatre autres ont
été chauffés à différentes
températures (40°C, 60°C, 80°C, 100°C) pendant 1
heure, puis après chauffage, nous avons procédé aux
analyses de la teneur en eau et détermination de l'HMF de tous les
échantillons.
Les échantillons des miels sont présentés
dans la figure N°05

Figure N°05 : présentation des
échantillons des miels étudiés. Tableau N°07
: présentation des échantillons de miel
étudiés.
|
Ech
|
Région
|
Origine florale
|
Année de récolte
|
|
01
|
Boukadire
|
Eucalyptus
|
2007
|
|
02
|
Oued djamaa
|
Agrume
|
2007
|
|
03
|
Melakou
|
Toutes fleurs
|
2007
|
|
04
|
Melakou
|
Toutes fleurs
|
2006
|
|
05
|
Tiaret (tagdempt)
|
Forêt
|
2005
|
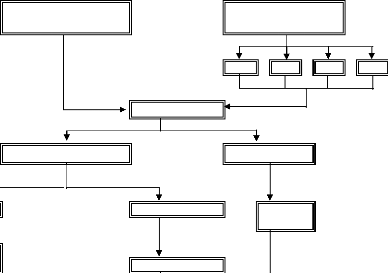
3-Protocole expérimental :
Pour notre travail nous avons adapté le protocole
expérimental représenté dans la figure N°06.
Chimique
HMF
couleur
aspect
Miels Algériens
Répartition dans
des étuis
Répartition en
05 lots
les autres
1lot 4 lots
Sans chauffage, analyses directes
Physico-chimique
Analyses
40°C
Visuelle
chauffage des échantillons à
60°C
80°C 100°C
Physique

Indice de
Refraction


1er lot 40°C
2éme lot 60°C
3éme lot 80°C
4ème lot 100°C
qualité des miels
Evaluation de la
FigureN°06: Schéma du protocole
expérimentale.
4-Appareillage :
? Agitateur magnétique.
? Balance analytique.
? Four électrique.
? Bain marie muni d'un thermomètre.
> Spectrophotomètre de type abbé relié
à un bain thermo staté par circulation d'eau grâce à
une pompe RL2.
5-Produits chimiques : ? Acide
acétique.
? Acide barbiturique. ? Propanol.
? Para toluidine.
6-Méthodes
6-1-Méthodes physicochimiques :
6-1-1-Détermination de la teneur en eau
:
L'indice de réfraction est une mesure optique qui varie en
fonction de la concentration en matière du produit à analyser et
de la température (La commission internationale du miel,
2002).
La détermination de la teneur en eau s'effectue par la
mesure optique de l'indice de réfraction (IR) du miel à 20°C
.Cette mesure est réalisé par un réfractomètre de
type Abbé relié à un bain thermo staté par
circulation d'eau grâce à une pompe RL2.
Technique :
Le miel à analyser doit être
homogénéisé et parfaitement liquide. Dans le cas où
l'échantillon est cristallisé, on le met dans un flacon
fermé hermétiquement et on le place à l'étuve
à 40°C ou dans un bain marie à 50°C, jusqu'à ce
que tous les cristaux de sucres soient dissous.
Après refroidissement à température
ambiante à l'aide d'une spatule, une goutte de miel est
déposée et étalée en couche mince sur la surface du
prisme. La lecture de l'I R est effectuée à travers
l'oculaire.
La lecture est faite à 20°C, et si elle est faite au
dessus de 20°C, on ajoute 0,00023 par degré et dans le cas
contraire on soustrait 0,00023 par 1°C.
Les résultas obtenus seront comparé à la
table standard de la commission internationale du miel (2002)
qui indique la teneur en eau correspondante (voir annexe
01).
6-1-2-Détermination de l'HMF :
L'HMF est un dérivé de déshydratation des
sucres ; qui apparaît par réaction chimique naturelle lors du
vieillissement ou du chauffage des miels (PERDRIX, 2003).
L'analyse a été effectuée selon la
méthode de WINKLER parue dans le rapport de la
commission international du miel (2002). Cette mesure de la
teneur en HMF est basée sur la mesure de l'absorbance de cette
molécule par spectrophotométrie réglée à une
longueur d'onde de 550nm, en présence d'acide barbiturique et de la
paratoluidine.
Solution d'acide barbiturique :
Dans une fiole jaugée de 100 ml, on dissout 500 mg d'acide
barbiturique dans 70 ml d'eau distillée au bain marie, on refroidit et
en complète avec de l'eau distillée jusqu'au trait de jauge
Solution de paratoluidine :
Dans une fiole jaugée de 250 ml, on dissout 25 g de
paratoluidine dans 50 ml de isopropanole, on ajoute 25 ml d'acide
acétique cristallisable puis on complète jusqu'au trait de jauge
avec le isopropanole.
Laisser la solution de paratoluidine à l'obscurité
24 heures avant son utilisation.
- Mode opératoire :- dissoudre 2 g de
miel dans 10 ml d'eau distillée (2tubes par échantillon).
Le dosage est réalisé selon le tableau suivant
Tableau N°08 : préparation des
échantillons et de la solution étalon.
|
Essai
Réactifs
|
Tube d'essai
|
Tube témoin
|
|
Solution de miel
|
1 ml
|
1 ml
|
|
Réactif de la paratoluidine à
10%
|
2,5 ml
|
2,5 ml
|
|
Solution d'acide
barbiturique à 0,5%
|
0,5 ml
|
-
|
|
Eau distillée
|
-
|
0,5 ml
|
La préparation du tube à essai ne doit pas
dépasser deux minutes. Expression des résultats
:
L'absorbance d'essai est mesurée par rapport au blanc
à 550 nm dans les trois à quatre minutes en maximum.
La teneur en HMF est exprimée en mg pour 1 kg de miel,
elle est donnée par la formule suivante :
HMF (mg/kg)= (192 x A x 10) / prise d'essai en
g
Dont :
192 : facteur de dilution et coefficient d'extinction, obtenue
expérimentalement à
partir de l'HMF pur. A : absorbance.
1-Analyse physicochimique : 1-1-la teneur en eau
:
En générale, la détermination de la
teneur en eau conditionne l'état de maturation et de conservation du
miel. D'après GONNET (1982), en moyenne cette teneur se
situe entre 17-18% pour la plupart des miels.
La teneur en eau des miels étudiés avant chauffage
est représentée dans le tableau N°09 Tableau
N°09 : les résultats de l'indice de réfraction et
de la teneur en eau des échantillons des miels sans traitement
thermique.
|
échantillon paramètre
|
01
|
02
|
03
|
04
|
05
|
|
Indice de
réfraction
|
1,494685
|
1,490685
|
1,49735
|
1,491185
|
1,50385
|
|
La teneur en eau
(%)
|
16,8
|
18,3
|
15,8
|
18,1
|
15,6
|
On constate que la teneur en eau des échantillons
analysés fluctue entre 15,6 et 18,3% avec une moyenne de 16,92 %.
Les échantillons N° 02 et 04 ont montré un
taux plus ou moins élevé par rapport aux autres , ce qui les
expose aux risques de fermentation contrairement aux échantillons
restant qui peuvent se conserver sans risque d'altération de leurs
propriétés physico-chimiques (GONNET, 1982).
CHIBANE et DJILLALI (2007), en analysant des
miels d'origines diverses ont trouvé des valeurs variant entre 13-19,2%
avec une moyenne de 17%. L'étude effectuée par AMROUCHE
et KESSI (2003) sur les miels algériens a
révélé des valeurs comprises entre 15 et 22,6% avec une
moyenne de 17,68 %.
Les 05 échantillons de miels traités par la chaleur
à différentes températures ont donné les
résultats regroupés dans la figure N°07
chauffage à 40°C chauffage à
60°C chauffage à 80°C chauffage à
100°C

Eau %
1 2 3 4 5
Echantillon
Figure N°07 : teneur en eau des
échantillon de miel après chauffage à différentes
températures.

La teneur en eau de nos échantillons après
traitement thermique à différentes températures varie
entre 15,4 et 18,3 % avec une moyenne de 16,55 %. La plupart des
échantillons marque une légère diminution de la teneur en
eau. Cette diminution peut être expliquée par l'effet de
vaporisation par la chaleur et à l'hygroscopicité du miel (peut
aussi bien absorber de l'humidité de l'air, que de perdre de l'eau
suivant que l'atmosphère est humide ou sèche) (POLUS,
2007 et COUGNET, 2007), tandis que 03 échantillons
traités à 80°C, montrent une légère
augmentation de leur teneur en eau. Cette augmentation peut être
expliquée par une forte altération du miel sous l'effet de la
température ce qui provoque la déshydratation du fructose et du
glucose et la production d'HMF puisque ce dernier est fortement
influencé par le traitement thermique (CERVANTES et al,
2000).
Ces variations de la teneur en eau peuvent être
expliquées par une mauvaise étanchéité des bouchons
des étuis.
1-2-H.M.F :
L' H.M.F représente un critère de qualité
qui nous renseigne sur « l'état de fraîcheur d'un miel »
et du sur chauffage.
Selon la législation française, on ne peut
commercialiser le miel comme « miel de table » que si celui-ci
présente un taux d'H.M.F inférieur à 40mg/kg de miel.
L'analyse spectrométrique des échantillons du
miel avant traitement thermique révèle des teneurs en H.M.F
représentée dans la figure N° 08. Elles se situent entre
17,28 et 71,04 mg/kg avec une moyenne de 40,89 mg/kg.
80
70
60
50
HMFmg/kg
40
30
20
10
0
1 2 3 4 5
Echantilon
Figure N°08 : HMF des échantillons
de miel avant traitement thermique.
Les résultats des échantillons N° 02, 03,
04 présentent des taux d'H.M.F fluctuant entre 17,28 et 38,40 mg/kg,
ceci pourrait s'expliquer par un vieillissement. Malgré que
l'échantillon N°04 étant plus vieux que les
échantillons N° 02 et 03 , celui-ci présente la teneur la
moins faible (17.28 mg/kg)
L'échantillon N°01 présente une teneur
légèrement supérieure à la norme, par contre
l'échantillon N°05 présente une teneur très
supérieure à la norme. Cette teneur élevée de 71
,28mg/kg pourrait être due :
A la décomposition partielle du fructose
Au vieillissement naturel du produit qui favorise ainsi la
transformation du fructose en H.M.F et le mode d'extraction.
MAKHLOUFI (2001), en analysant des
échantillons de miels algériens a trouvé des valeurs
variant entre 9,6 et 157,44 mg/kg avec une moyenne de 42,6 mg/kg.
La présence d'H.M.F dans un miel est
révélatrice d'une perte de la qualité organoleptique.
Cette teneur en H.M.F est influencée par certains facteurs
notamment le type de sucre, sa concentration, la durée de conservation,
la température et l'acidité ou la valeur de pH.
La figure N°09 nous montre les valeurs obtenues pour l'H.M.F
des cinq échantillons soumis à différentes
températures.
|
160 140 120 100 80 60 40 20
0
|
|
Echantillon N°01 Echantillon N°02
Echantillon N°03 Echantillon N°04 Echantillon N°05

25°C 40°C 60°C 80°C
100°C
température
Figure N°09 : variation du taux d'H.M.F
des miels en fonction de la température.
Suite à ce traitement thermique, nous constatons que l'HMF
des échantillons chauffés a augmenté
différemment.
L'H.M.F a augmenté à la suite du traitement
thermique.
La dégradation du fructose est très rapide, elle
démarre déjà à 40°C.
Tous les échantillons enregistrent une augmentation de la
teneur en H.M.F.
À 100°C, elle varie entre 46,77 et 86,25% avec une
moyenne de 63,76% du taux initiale.
Les résultas que nous avons enregistrés montrent
que le chauffage du miel à différentes températures
pendant 1h entraîne à 100°C une hausse d'H.M.F très
significative et qui dépasse 100mg/kg pour tous les miels
analysés, à l'exception du miel N°02 où sa teneur en
H.M.F a augmenté lentement et à 100°C son HMF arrive
à 59,52mg/kg. Contrairement à l'échantillon N°04 qui
débute avec un taux d'H.M.F < à 20mg/kg mais qui a
augmenté finalement rapidement au cour du traitement thermique et
à 100°C a augmenté de 86,25%. Cela peut être
expliqué par une résistance à la chaleur qui varie en
fonction de l'origine botanique du miel et de sa composition.
AMRAOUI et DROUI (2005), en analysant des
miels algériens ont trouvé des valeurs d'une moyenne de 12,4
1mg/kg et après un stockage à 30°C pendant 2 mois la moyenne
enregistrée étant de 20,23 mg/kg.
La production d'H.M.F est donc un phénomène
naturel dont le processus est lent à température ambiante. Par
contre le chauffage du miel l'accélère énormément
et ce quel que soit la nature du miel (plus ou moins acides) (PREDRIX,
2003).
2-Analyses sensorielles : 2-1-Couleur et aspect :
La couleur des miels est une donnée importante parce
c'est une caractéristique physique dépendant de l'origine du
produit mais également un élément sensoriel primordial qui
détermine en partie le choix du consommateur. L'état de structure
du miel, liquide ou cristallisée, est le premier paramètre qu'on
peut évaluer et qui peut être important
Tableau N°10 : Analyse visuelle des
différents types de miels à température ambiante.
|
Echantillon
|
Couleur
|
Aspect
|
|
01
|
Marron brun
|
Semi solide
|
|
02
|
Marron brun
|
Semi solide
|
|
03
|
Marron très foncé
|
Très liquide
|
|
04
|
Blanc jaunâtre claire
|
cristalliser
|
|
05
|
Brun rougeâtre
|
Presque solide
|
Après traitement thermique, on a constaté que
pour tous les miels, la couleur est devenue plus foncée en fonction de
la température du chauffage appliqué. Mais le processus a
remarquablement démarré à partir du 80°C, cette
dégradation de couleur aux cours du traitement thermique était
très nette et visible dans l'échantillon N° 04 (voir la
figure N°10).

Figure N°10 : le changement de la couleur
d'échantillon N°04 au cour du traitement thermique.
CONCLUSION
Le miel, cet aliment tant apprécié par l'homme
présente un éventail très large en goût et en
couleur. Devant cette diversité de choix, le consommateur est
confronté à faire une distinction entre le miel frais et celui
qui ne l'est pas.
A la lumière de notre étude effectuée sur 05
échantillons de miel en déterminant essentiellement l'HMF et la
teneur en eau, nous avons pu tirer les conclusions suivantes :
- un miel surchauffé conduit à la formation d'H.M.F
qui contribue à la dégradation de la
qualité du miel,
- en outre l'augmentation de la température de
façon importante a aussi des
conséquences sur le changement de la couleur du miel qui
brunit, donc le miel vieillit avec le temps, mais sa qualité ne
s'améliore pas au cour du stockage.
Et pour que le miel garde sa fraîcheur et ainsi son
parfum, sa couleur, et sa composition énergétique en sucre et en
vitamine il faut éviter de le conserver à température
élevée et de le conserver assez rapidement.
Références Bibliographiques
AIT AMEUR L, (2006) : Evolution de la
qualité nutritionnelle des protéines de biscuits modèles
au cours de cuisson au travers d'indicateurs de la réaction de Maillard:
l'intérêt de la fluorescence frontale. Doctorat en chimie
analytique .Institut National Agronomique Paris Grignon. 209 p.
AMROUCHE L et KESSI L, (2003) : étude de
la qualité physico-chimique de quelques miels. Mémoire.
Ingénieur. U.S.T.H.B. ALGER. 49p.
AMRAOUI A et DROUI F, (2005) : effet de la
température (3 0°C) sur les propriétés physico-
chimiques des miels algériens. Production 2004. Mémoire. DES.
Biologie. Tiaret. 50p.
ANCHLING F, (2005): juin, sommet de
développement des colonies, mais quid de la première
récolte. Revue j'abeille de France N° 915. 07p.
ANDRIEN, (2006): fabriquer carburant et
composé organique à partir du fructose. Extrait du BE U.S.A
N°43. 1p.
APFELBAUM M, ROMON M, ET DUBUS M, (2004) :
Diététique et nutrition .6éme
édition (c) Masson .paris .345p.
BARBIER M, (1968): Biochimie de l'abeille.
Biologie et physiologie générale in traité de biologie de
l'abeille .tome ². Ed Masson et Cie. 536p
BECKER M et SCHWEITZER P, (2000): Fermentation
des miels. Intérêt du dosage du glycérol. CETAM Lorraine.
Revue l'abeille de France .N° 856 .04p.
BENRAHAL F, (1997): caractérisation des
miels purs et essais de détection de leur falsification courante.
Mémoire. Agro. ISA. Tiaret. 41p.
BENTTAHER K et YAKDOUMI H, (2006): étude
physico-chimique de quelque miels importé. Mémoire .DES. TIARET
.42p.
BIRI M, (1976): l'élevage moderne des
abeilles. Ed vecchi S.A paris . 321p.
BIRI M, (1999): le grand livre des abeilles
.l'apiculture moderne. Ed vecchi S.A paris.260p.
BOGDANOV S, (1999): Stockage - cristallisation e
liquéfaction du mile. Centre suisse de recherche apicoles .05p.
BOGDANOV S, (2005): Miels mono floraux suisses.
Ed station de recherche agro scope liebefeld. Posieux ALP forum 23.55p.
BOGDANOV S, GALLMANN P, STANGACIU S, THEODORE CT, (2006):
Produit apicole et santé. ALP Forum. N°41F. 52p .
BOGDANOV S, LULLMANN C, MARTIN P, (1999):
qualité du miel et norme international relative au miel.
Rapport de la commission international du miel du miel. Abeille Cie
N° 71-4.1 2p.
BOGDANOV S, LULLMANN C, MARTIN P, et al, (2000):
honney quality and international commission Swiss bee research centre
p 1-15
BOGDANOV S, RUOFF K, ODDO PL, (2004):
physicochemical methods for the characterisation of unifloral honeys
.apidologie 35. 17p.
CARTEL B, (2002): l'heure de
vérité. Revue l'abeille de France N° 882.08p
CARTEL B, (2006): fleure de juin pour le miel
nouveau. Revue l'abeille de France N° 926.06p.
CERVANTES R, GONZALEZ S.A, SAURI, (2000): les
effet du traitement thermique sur la qualité du miel pendant
l'entreposage. Ed APIACTA. 35(4). P 162-170.
CETAM LORRAINE, (2002): les contrôles de
qualité du miel .laboratoire d'analyse et d'écologie apicole.
Avec autorisation d'abeille de France N° 882 .05p.
CHAUVIN R, (1968): les glandes cirières
et la cire .biologie et physiologie générale in traité de
biologie de l'abeille. TomeÉ Ed Masson et Cie.536p.
CHIBANE Y et DJILLALI S, (2007): contrôles
de qualité de quelque miels d'origine diverses et étude de leur
effets sur quelque micro-organisme .Mémoire . Ingénieur. U.
S.T.H.B. ALGER. p 30.
CLEMENT H, (2003): les cahier de
l'élevage. Crée son rucher. Ed RUSTICA .paris. 111p.
COUGNET P, (2007) : guide nature et apiculture.
Contrôler le facteur "humidité dans la miellerie " revue abeille
et Cie. N° 117. p 18.
DONADIEU Y, (1982): pollen :
thérapeutique naturelles. 5éme Ed Maloine S.A .Paris.3
1p.
DONADIEU Y, (1978): le miel
thérapeutique.2éme Ed Maloine S.A .Paris.28 p.
DONADIEU Y, (1981): la propolis :
thérapeutique naturelles.2éme Ed Maloine S.A
.Paris.32p.
DONADIEU Y, (1999): gelée royale :
thérapeutique naturelles.7éme Ed Maloine S.A
.Paris.30p. DONADIEU Y, (1981): le miel thérapeutique
naturelles. Ed Maloine S.A .Paris. 30p.
DONADIEU Y et MARCHISET, (1984): la cire
thérapeutique naturelles. Ed Maloine S.A .Paris. p 69.
DONADIEU Y, (2003):qu'est que le miel .chapitre
É. Faculté de médecine de paris .07p .
FREYTAGE I, (2007): Qualité des miels de
commerce. Revue abeille et Cie .N° 118.08p. GONNET M, (1982):
le miel, composition, propriétés et conservation. Ed
OPIDA. 29p.
HUCHET E, COUSTEL J, GUINOT L, (1996): Les
constituant chimiques du miel. Méthode d'analyse chimique.
Département de science et l'aliment. Ecole Nationale Supérieure
des Industries Agricoles et Alimentaire. France. 16p.
ITDE, (1985): guide d'élevage .3.
Conduite d'un rucher. Ministère de l'agriculture et de la
pêche.13p.
JEAN-PROST P, (1987): l'apiculture
.connaître l'abeille .conduire le rucher. 6éme
édition Lavoisier.597p.
JEAN-PROST P, (2005): l'apiculture,
connaître l'abeille. Conduire le rucher. 7éme
édition Lavoisier. 682p.
Journal Officiel des Communités Européen,
(2002): Annexe ÉÉ. Direction 2001 /1 10/ce du conseille
du 20 décembre 2001 relative au miel caractéristique de
composition des miels.06p.
KARABOURNIOTI S et ZERVALAK P, (2001): les
effets du chauffage sur l'HMF et l'invertase des miels. Laboratry of
qualité centrale APIACTA. 36(4), 178-181p
KESS E, (2002): Etude de la relation entre
certains facteurs alimentaires et
Le risque de tumeurs colorectal .Doctorat en Nutrition Humaine
Institut National Agronomique Paris Grignon. 178p.
KHENFER A et FETTAL M, (2001): le miel. .
Ministère de l'agriculture .direction de la formation de la recherche et
de la vulgarisation.23p.
LAGACHERI M et CABBANES B, (2001): les
plantation mellifères. Revue l'abeille de France .N° 635.
LAVIE P, (1968): les substances antibiotique
dans la colonie d'abeille. Les produits de la ruche in traité de
biologie de l'abeille. Tome 03. Ed Masson et Cie. 389p.
LE BRUN, (2006) : tout savoir sur l'HMF .une
analyse de miel. Coopérative apicole de jura. P 12. LOUVEAUX,
(1985): les abeilles et leur élevage .Ed OPIDA.256p.
LOUVEAUX, (1968): Composition
propriété et technologie du miel. Les produits de la ruche in
traité de biologie de l'abeille. Tome 03.Ed Masson et Cie. 389p.
MAHLOUFI et ROGE, (2008): le caramel. Dossier
CEDUS .avec la collaboration de l'université de Reins. 11p.
http://www.lesucre.com/uploads/doc/Fiche7_Caramel.pdf
MAKHLOUFI C, (2001): étude phisico-
chimique et palynologique de quelque miel du nord algérien .impact du
role de l'abeille sur l'equilibre ecologique .Mémoire mag ou agraunomie.
Tiaret.100p.
MARCEAU J, NOREAU J et HOULE E, (1994): Les HMF
et la qualité du miel. Volume 15 numéros 2.
Fédération des Apiculteurs du Québec .service de
zootechnie, MAPAQ.04p.
MARY M, (2003): conditionement du miel et sa
vente en pots . revue abeille et fleur N° 635.
MAURIZIO, (1968): la formation du miel . les
produits de la ruche in traité de biologie de l'abeille . tome 03 .Ed
Masson et cie .389p.
MSDA, (2004): produit apicole. Revue par le
groupe d'expert, .produit apicole.32p. PHILIPPE J.M, (1999):
le guide de l'apiculture 3éme édition EDISUD.
France.345p.
POLUS P, (2007): récolte et
conditionnement du miel. Revue l'abeille de France N°937 .laboratoire
d'analyse et d'écologie apicole. 13p.
PREDRIX J.L, (2003): critères de
qualités du miel. Bulletin de liaison N°41.
SCHWEITZER P, (2001a): la couleur du miel .Revue
l'abeille de France N°872 .laboratoire d'analyse et d'écologie
apicole.08p.
SCHWEITZER P, (2001b): journée de
l'abeille à Sombernon. Revue l'abeille de France N° 866
.laboratoire d'analyse et d'écologie apicole. 04p.
SCHWEITZER P, (2001c): l'HMF et les
miels. Revue l'abeille de France .laboratoire d'analyse et
d'écologie apicole. 02p.
SCHWEITZER P, (2004a): le monde des
miellats. Revue l'abeille de France N°908 .laboratoire
d'analyse et d'écologie apicole.04p.
SCHWEITZER P, (2004b): les critères de
qualité du miel. Revue l'abeille de France N°916 .laboratoire
d'analyse et d'écologie apicole.02p.
SCHWEITZER P, (2004c): deux ans ? Revue
l'abeille de France N°988 .laboratoire d'analyse et d'écologie
apicole.05p.
SCHWEITZER P, (2005a): encore des miels hors
normes. Revue l'abeille de France N°917 .laboratoire d'analyse et
d'écologie apicole. 03p.
SCHWEITZER P, (2005b): miel étranger.
Revue l'abeille de France N°920 .laboratoire d'analyse et
d'écologie apicole. 04p.
TOSI E, CIAPPINI M, and Ré E, LUCERO H,
(2002): honey thermal treatment effect on hydroxymethylfurfural
cpontent food chemistry 77. Elsevier science LTD all. Rights reserved p
71.74
WIKIPEDIA, (2008): Hydroxymethylfurfural. From
Wikipedia, the free encyclopedia.3p.
http://en.wikipedia.org/wiki/Hydroxymethylfurfural
Annexe 01 :
Tableau N°11 : Relation entre la teneur en
eau et l'indice de réfraction du miel. (Commission internationale du
miel, 2002).
|
Teneur en eau
g/100g
|
Indice de réfraction
20°C
|
Teneur en eau
g/100g
|
Indice de réfraction
20°C
|
|
13.0
|
1.5044
|
19.0
|
1.4890
|
|
13.2
|
1.5038
|
19.2
|
1.4885
|
|
13.4
|
1.5033
|
19.4
|
1.4880
|
|
13.6
|
1.5028
|
19.6
|
1.4875
|
|
13.8
|
1.5023
|
19.8
|
1.4870
|
|
14.0
|
1.5018
|
20.0
|
1.4865
|
|
14.2
|
1.5012
|
20.2
|
1.4860
|
|
14.4
|
1.5007
|
20.4
|
1.4855
|
|
14.6
|
1.5002
|
20.6
|
1.4850
|
|
14.8
|
1.4997
|
20.8
|
1.4845
|
|
15.0
|
1.4992
|
21.0
|
1.4840
|
|
15.2
|
1.4987
|
21.2
|
1.4835
|
|
15.4
|
1.4982
|
21.4
|
1.4830
|
|
15.6
|
1.4976
|
21.6
|
1.4825
|
|
15.8
|
1.4971
|
21.8
|
1.4820
|
|
16.0
|
1.4966
|
22.0
|
1.4815
|
|
16.2
|
1.4961
|
22.2
|
1.4810
|
|
16.4
|
1.4956
|
22.4
|
1.4805
|
|
16.6
|
1.4951
|
22.6
|
1.4800
|
|
16.8
|
1.4946
|
22.8
|
1.4795
|
|
17.0
|
1.4940
|
23.0
|
1.4790
|
|
17.2
|
1.4935
|
23.2
|
1.4785
|
|
17.4
|
1.4930
|
23.4
|
1.4780
|
|
17.6
|
1.4925
|
23.6
|
1.4775
|
|
17.8
|
1.4920
|
23.8
|
1.4770
|
|
18.0
|
1.4915
|
24.0
|
1.4765
|
|
18.2
|
1.4910
|
24.2
|
1.4760
|
|
18.4
|
1.4905
|
24.4
|
1.4755
|
|
18.6
|
1.4900
|
24.6
|
1.4750
|
|
18.8
|
1.4895
|
24.8
|
1.4745
|
Annexe 02 :
Tableau N°12 : HMF des échantillons
de miel avant et après le traitement thermique.
|
Teneur en HMF des cinq échantillons de miel en mg/kg
|
|
Température
du traitement
thermique
|
Echantillon
N°01
|
Echantillon
N°02
|
Echantillon
N°03
|
Echantillon
N°04
|
Echantillon
N°05
|
|
Sans
traitement
|
46,08
|
31,68
|
38,40
|
17,28
|
71,04
|
|
40°C
|
72,96
|
34,56
|
47,04
|
27,84
|
92,16
|
|
60°C
|
73,92
|
39,36
|
68,12
|
38,4
|
96
|
|
80°C
|
105,6
|
47,04
|
86,40
|
63,36
|
99,84
|
|
100°C
|
119,04
|
59,52
|
150,72
|
123,84
|
142,08
|
|
La moyenne
|
83,52
|
42,43
|
78,13
|
54,14
|
100,22
|
Annexe 03 :
Tableau N°12 : teneur en eau des
échantillons de miel avant et après le traitement thermique.
|
Teneur en eau des cinq échantillons de miel
|
|
Température
du traitement
thermique
|
Echantillon
N°01
|
Echantillon
N°02
|
Echantillon
N°03
|
Echantillon
N°04
|
Echantillon
N°05
|
|
Sans
traitement
|
16,8
|
18,3
|
15,8
|
18,1
|
15,6
|
|
40°C
|
16,6
|
18,3
|
15,8
|
18,1
|
15,4
|
|
60°C
|
16,2
|
17,7
|
15,8
|
16,6
|
15,4
|
|
80°C
|
16,4
|
17,8
|
16
|
16,6
|
15,4
|
|
100°C
|
15,8
|
17,7
|
15,8
|
16,5
|
15,4
|
|
La moyenne
|
16,36
|
17,96
|
15,84
|
17,18
|
15,44
|
Résumé :
Notre travail a porté sur l'étude de l'effet de la
température sur l'évolution de l'H.M.F dans les miels
algériens.
Les résultats obtenus montrent qu'il y'a une forte
augmentation de l'H.M.F durant les traitements thermiques ce qui entraîne
une dégradation de la qualité du miel. Plus la température
et la durée d'exposition augmentent et plus la teneur en HMF devient
importante.
Mots clés :
Miel, analyse, température, H.M.F, qualité,
vieillissement, altération.

Summary:
Our work brings on the survey of the effect of the temperature on
the evolution of the HMF in Algerian honeys.
The gotten results show that there is a big increase of the
HMF during the thermal treatments what entails a deterioration of the quality
of the honey. More the temperature and the length of exhibition increase and
more the content in HMF becomes important.
The words keys:
Honey, analysis, temperature, quality, ageing, change.



