|
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
1
INTRODUCTION
Les petits ruminants contribuent pour une large part au
produit intérieur brut du Niger. Cette importance économique qui
paraît évidente aujourd'hui, n'a pas toujours été le
cas étant donné que les ovins et les caprins ont
été souvent victimes de préjugés dont entre autres
leur supposé rôle dans la désertification.
C'est pourquoi, pendant les périodes coloniales et post
- coloniales, les efforts ont été essentiellement orientés
vers les bovins qui ont bénéficié d'importantes ressources
pour l'amélioration des conditions d'élevage ainsi que
l'intensification de leurs productions (LEFEVRE, 1984)
Comparées avec les travaux réalisés sur
les bovins, les connaissances actuelles sur les petits ruminants sont
fragmentaires et incomplètes. Déjà en 1971, ROBINET
remarquait qu'il naissait au Niger en année normale, près de 5
millions de chevreaux dont la moitié succombait avant l'âge de 1
an pour cause de malnutrition, de maladies parasitaires et infectieuses. A cela
s'ajoutait la mortalité de près de 500 000 adultes.
De nos jours, la situation sanitaire est
caractérisée par la persistance de quatre principales maladies
réputées légalement contagieuses dont la Peste des Petits
Ruminants. Cela s'explique par le caractère essentiellement transhumant
de l'élevage et le faible niveau de couverture vaccinale (MRA,
2005-2006).
La Peste des Petits Ruminants est une maladie virale,
infectieuse et très contagieuse des ruminants domestiques et sauvages.
S'exprimant souvent sous forme épizootique, elle revêt une
importance économique sérieuse du fait des fortes
mortalités qu'elle entraîne. En vue de contribuer à une
meilleure
connaissance de cette maladie au Niger, nous avons choisi d'en
faire une étude épidémiologique en utilisant les
méthodes modernes de diagnostic. Compte tenu des moyens importants que
requiert cette démarche, nos investigations se sont concentrées
sur trois régions du Niger : Niamey, Ta houa et Tilla béry.
L'objectif de la présente étude est
d'évaluer, par la technique ELISA (Enzyme Linked Immunosorbent Assay),
la séroprévalence de la Peste des Petits Ruminants et à
confirmer la présence du virus dans les échantillons
prélevés en utilisant la PCR (Polymerase Chain Reaction).
La présente étude sera abordée en deux
grandes parties :
· la première sera consacrée à une
synthèse bibliographique sur l'élevage des petits ruminants au
Niger et la peste des petits ruminants ;
· la deuxième partie présentera le protocole
expérimental avec d'une part
le matériel et les
méthodes et d'autre part les résultats et la discussion.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008

PREMIERE PARTIE :
SYNTH ESE
BIBLIOGRAPHIQUE
GAGARA H. Mariama
3

CHAPITRE 1 : L'ELEVAGE DES PETITS
RUMINANTS AU NIGER
1. Importance de l'élevage
L'élevage constitue, après l'agriculture, la
deuxième activité économique du Niger. Si par le
passé le cheptel était essentiellement concentré dans la
partie nord, zone à vocation pastorale, aujourd'hui il devient de plus
en plus important au sud, dans les villes et les campagnes de la zone reconnue
à vocation agricole (MRA, 2003).
L'élevage intéresse la quasi-totalité de
la population rurale soit 85 p. cent de la population totale du Niger. Le
Ministère des Ressources Animales a estimé, en 2007, les
effectifs du cheptel national à 7.336.088 bovins, 9.192.017 ovins,
11.238.268 caprins et près de 1.565.420 camelins (MDA-MRA,
2004-2007).
L'entretien de tout ce important cheptel, exception faite du
cheptel aviaire, est assuré par les pâturages naturels, les
résidus de culture et les sous produits agro-industriels. D'une
manière générale, les terres destinées au
pâturage, constituées de la zone pastorale et des jachères
en zone agricole, diminuent d'année en année en raison de la
pression agricole et de la désertification.
L'étude de l'évolution des effectifs de la
période coloniale à nos jours, montre une évolution en
dents de scie ; les effets combinés des maladies et/ou de
déficits fourragers étant la cause de ce type d'évolution.
La taille des troupeaux des ruminants qui est en moyenne de 30 bovins, 50
ovins, 50 caprins et 40 camelins chez les éleveurs purs varie du nord au
sud. En général ces troupeaux sont mixtes (MRA, 2003).
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
5
L'élevage des petits ruminants occupe de plus en plus
une place importante et se pratique dans toutes les zones climatiques, depuis
la zone soudanienne jusqu'aux oasis du Ténéré. Il occupe
toute la population aussi bien sédentaire que nomade. Cet aspect
révèle le caractère extensif de l'élevage
nigérien, marqué par une transhumance de grande amplitude
à côté duquel se situe un noyau sédentaire
d'embouche uniquement en zone agricole (MRA, 2003).
2. Les principales races ovines élevées
au Niger
L'espèce ovine du Niger est essentiellement
constituée de cinq races de moutons à poils et accessoirement de
3 races de moutons à laine (MRA, 2003).
2.1. Mouton Oudah (figure 1)
Son nom provient de la tribu qui l'élève au
Niger (Oudawa). On le rencontre également dans les pays frontaliers du
Niger. C'est un mouton d'assez grande taille (environ 80cm au garrot) souvent
élevé en groupe et dont le poids moyen adulte peut atteindre 50
kg. La robe est bicolore avec une partie antérieure qui varie de la
couleur fauve à noire et une partie postérieure blanche. La ligne
de démarcation entre les 2 parties est circulaire. La couleur fauve ou
noire englobe une partie de l'abdomen. La queue est longue et descend en
dessous des jarrets. Le mouton Oudah est un bon animal de boucherie. Son
rendement carcasse oscille entre 48 et 50 p. cent (Ibrahim, 1975). Ces moutons
représenteraient 50 p. cent du cheptel ovin (INRAN, 1996).


Figure 1 : Mouton Oudah (source : INRAN 1996)
2.2. Mouton Ara-ara (figure 2)
Ara-ara en Peulh signifie mouton court à petites
oreilles et possédant des pendeloques. Le mouton Ara-ara est connu sous
le nom de « mouton targui », Bouzou (Haoussa) et Agora (Djerma) au
Niger. Il est élevé dans le nord du pays. Il est rustique et
mesure 60 à 80cm au garrot. C'est un mouton à petites oreilles et
à cornes spiralées chez les mâles et absentes chez les
femelles. Les pendeloques sont quasi constantes chez les deux sexes. C'est un
animal qui s'engraisse facilement même en élevage extensif et la
femelle est assez bonne laitière, mais les rendements sont mal connus au
Niger. Le mouton Ara-ara constitue 36 p. cent du cheptel ovin (INRAN, 1996).

Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
7

Figure 2 : Mouton Ara-ara (source : INRAN 1996)
2.3 Mouton Bali-bali (figure 3)
C'est un mouton Peulh qui se rencontre au Niger et au Mali.
De grande taille (plus de 80cm au garrot), la couleur dominante est le blanc,
mais certains sujets peuvent être pie-noir (tableau I). L'adulte porte
des cornes très développées chez les mâles. Les
oreilles sont longues (19cm) et larges (8,5cm). Bien que reconnu comme animal
de boucherie, ses aptitudes et ses effectifs sont mal connus (INRAN, 1996).

Figure 3 : Mouton Bali-bali (source : INRAN 1996)
Tableau I : Récapitulatifs des paramètres
zootechniques du mouton Oudah, Bali-bali et Ara-ara (source : MRA, 2003)
Paramètres zootechniques
|
Oudah
|
Bali-bali
|
Ara-ara
|
Système d'élevage
|
Durée oestrus
|
36-56 heures
|
25,6#177;1,3 heures
|
33,3#177;2,7 heures
|
Station
|
Durée cycle oestral
|
16-19 jours
|
18-21 jours
|
16-20 jours
|
Station
|
Age à la 1ère mise bas
|
17,3#177; 1,1 mois
|
16,6#177;1,5 mois
|
-
|
Traditionnel
|
Intervalles entre naissances
|
9,6#177;0,6 mois
|
10#177;0,7 mois
|
-
|
Traditionnel
|
Taux de prolificité
|
106,8 p. 100
|
103,6 p. 100
|
100 p. 100
|
Station et traditionnel
|
Durée de gestation
|
149-152 jours
|
150-156 jours
|
150-157 jours
|
Station
|
Poids à la naissance
|
3,5-5,4kg
|
3,3#177;0,93kg
|
3,44#177;0,68kg
|
Station
|
GMQ (3 mois)
|
72,222g/jour
|
58,77g/jour
|
77,2g/jour
|
Station
|
Volume éjaculat
|
0,72-1,5 ml
|
0,9#177;0,31 ml
|
1,13#177;0,31 ml
|
Station
|
Concentration en
spermatozoïdes/ml
|
3485#177;5335.106
|
3777#177;1246.106
|
4156#177;791.106
|
station
|
|

G.M.Q : Gain Moyen Quotidien, g : gramme, kg : kilogramme, ml :
millilitre

Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
9
2.4. Mouton Balami (figure 4)
Cette race est surtout rencontrée dans
l'arrondissement de Dakoro (Département de Maradi) dans une
localité appelée Sakabal. D'un effectif très
réduit, le Balami se reconnait par sa robe uniforme blanche, des
oreilles très longues et larges, une grosse tête, une grosse et
longue queue qui descend en dessous des jarrets. La race Balami comporte deux
variétés : une variété dont les mâles portent
des cornes spiralées et une autre au sein de laquelle les mâles
sont sans cornes. C'est un mouton de grande taille apprécié pour
l'élevage d'embouche. Ses aptitudes sont mal connues (1996).

2.6. Mouton Koundoum (figure 5)
Le Koundoum est un mouton élevé par les
Kourtèyes sur les bords du fleuve Niger et dans les îles. De
taille variant entre 50 et 60cm au garrot et d'un poids atteignant 40 kg, le
Koundoum possède des cornes le plus souvent en spirale et entourant ses
oreilles courtes (DOUMA et SANI, 1997). Bien nourri, il prend vite du poids
avec un rendement de 47 à 48 p. cent. Avec deux tontes par an, il
fournit 1,2 à 1,5kg de laine de qualité appréciable. Chez
certains sujets, la laine couvre tout le corps alors que chez d'autres elle
n'apparait qu'au niveau des jarrets. Le noir est la couleur originelle de cette
toison, mais de nos jours, par suite de métissage, on rencontre
très souvent des animaux à toison blanche. C'est un mouton
très fertile.

Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
11
2.8. Mouton Hadine
C'est un mouton noir toubou qui vit dans l'arrondissement de
N'guigmi à la frontière Tchadienne. Il n'a pas fait l'objet
d'étude au Niger.
3. Les principales races caprines du Niger 3.1. La
chèvre du sahel
Elle est de grande taille (80cm) avec une robe
extrêmement variable (noire, blanche, fauve, tachetée, etc.). Le
type bariolé est très représenté au Niger. C'est un
animal qui a de grandes prédispositions pour la spéculation
viande et la production laitière.
L'adulte peut atteindre un poids de 35kg. Le poil est ras et
fin. Le bouc porte une barbiche et aussi une crinière qui s'étend
parfois jusqu'à la croupe. Chez le mâle, le front convexe porte
une touffe de poils. C'est un animal rencontré dans tous les pays du
sahel.
3.2. Chèvre Rousse de Maradi (figure 6)
Elle a des traits communs avec la race naine guinéenne
du Fouta Djallon, mais son individualité bien marquée permet de
la considérer comme une variété bien fixée.
Le poids des mâles adultes se situe entre 25 et 30kg,
celui des femelles entre 23 et 28kg. En station, le poids moyen à la
naissance est de 2,0kg. Du point de vue phénotypique, la chèvre
Rousse de Maradi est harmonieuse, assez élancée, de type
médioligne, eumétrique. La robe est homogène, brillante
à reflet

acajou, le poil est ras, dense, sur une peau souple. Tout
allongement accompagné d'un éclaircissement du pelage, de
l'apparition des teintes délavées et surtout de poils blancs,
marque un signe rédhibitoire de la pureté du type. Le mâle
présente constamment une teinte plus foncée allant jusqu'à
l'apparition d'une raie dorsale noire ; les muqueuses visibles sont noires ; la
tête est fine, le chanfrein est convexe, couvert de poils longs plus
foncés chez le mâle que chez la femelle. Les oreilles sont
longues, horizontales ou tombantes, le chanfrein est rectiligne, parfois
subconcave. Le cornage est moyennement développé et les cornes
sont peu épaisses, toujours présentes, aplaties d'avant en
arrière et à insertion rapprochée offrant un léger
mouvement de la torsion. L'encolure est courte, la poitrine ample, le garrot
noyé, le dos rectiligne. La mamelle est bien développée
gênant l'animal en déplacement. La queue, aux poils plus touffus
et souvent noirs, est courte et relevée à son
extrémité.
La chèvre Rousse de Maradi, par ses qualités
économiques, est un animal à retenir pour la diffusion et la
constitution des troupeaux caprins familiaux. Toutefois, cette diffusion ne
peut s'effectuer qu'en zone agricole pure, car la race pure ne peut effectuer
de longues marches et nécessite un appoint alimentaire pour
extérioriser ses performances. Elle ne peut en aucun cas se substituer
à la race sahélienne apte à la marche et résistante
aux privations (MRA, 2003).

Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
13
4.1.1. - Le sous-système basé sur le
nomadisme
Il est caractérisé par des mouvements entrepris
par certains groupes pastoraux à des dates et sur des itinéraires
non prévisibles, de durée indéterminée et sur des
distances considérables, à la recherche d'eau et de
pâturage. Il est surtout pratiqué par les Peulhs Bororo et les
Touaregs. C'est un système qui a un faible niveau d'utilisation des
intrants. Les espèces élevées par les nomades sont les
bovins, les ovins, les caprins et les camelins. Les asins sont utilisés
pour le transport et dans une moindre mesure pour l'exhaure (MRA, 2003).
4.1.2. - Le sous-système basé sur la
transhumance
Il concerne toutes les espèces animales et est
caractérisé par la mobilisation des troupeaux de grande ou de
faible amplitude. Les mouvements de transhumance sont des mouvements
saisonniers à caractère cyclique de troupeaux à la
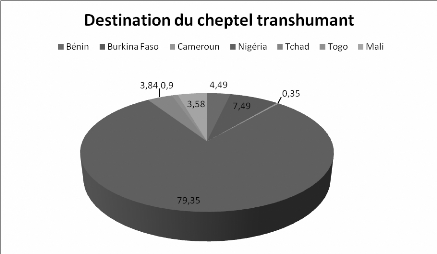
recherche d'eau et de pâturage. Les mouvements de transhumance
transfrontalière en direction du Bénin, du Nigéria, du
Burkina Faso et du Mali se sont intensifiés ces dernières
années (figure 7). Cette transhumance qui intéresse
particulièrement les Peulhs et les Boudoumas concerne tous les ruminants
à l'exception des caprins. Les asins et parfois les équins sont
utilisés pour le transport et ou l'exhaure.

Ce sous-système, tout comme celui basé sur le
nomadisme, se caractérise par un faible niveau d'utilisation des
intrants (MRA, 2003).
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
15
Figure 7 : Transhumance externe (source : MRA, 2003)
4.2. Le système de production agropastorale
Le système de production agropastorale est un
système dans lequel 10 à 50 p. cent du revenu brut est
tiré de l'élevage. En d'autres termes, 50 p. cent au plus du
revenu proviennent de l'agriculture ou d'autres activités. C'est un
système mixte qui intègre l'agriculture et l'élevage. Les
systèmes de production agropastoraux sont évolutifs et peuvent
être à dominante agricole ou pastorale.
Le système de production agropastorale à
dominante agricole est observé au niveau des villages et autour des
centres urbains. Dans ce système, l'agriculture constitue la principale
activité de la population qui en tire l'essentiel de ses revenus. Les
principales cultures pratiquées sont les céréales (mil,
sorgho) et les légumineuses (arachide et niébé).
Toutefois, l'élevage occupe une place de choix en tant que moyen
d'investissement, de sécurité
alimentaire et de source de revenus supplémentaires.
Ce système est caractéristique de la zone agricole située
au sud du pays où les agriculteurs confient souvent une partie de leurs
troupeaux en gardiennage aux éleveurs transhumants, tout en gardant un
noyau d'animaux, généralement quelques vaches laitières,
pour pourvoir à la subsistance des membres de famille, des bovins de
trait et des petits ruminants. Le système d'élevage
pratiqué est sédentaire. Parfois on observe une petite
transhumance caractérisée par des déplacements de
troupeaux de faible amplitude en raison de la réduction des aires de
pâturage et de risques de dégâts champêtres. Les
troupeaux sont alors conduits en dehors des zones de culture jusqu'à la
fin des récoltes. Le système agropastoral à dominante
agricole est un système qui se caractérise par une utilisation
moyenne des intrants (fourrages récoltés, sous produits
d'agriculture et d'autres intrants zootechniques). Les espèces
concernées par ce type de système sont essentiellement les
bovins, les moutons et chèvres. La production intensive de bovins et
ovins (embouche bovine et ovine) répond plus aux normes d'un
système de haut niveau d'utilisation des intrants.

Dans le système de production agropastorale à
dominante pastorale, l'élevage assure l'autoconsommation du lait, de la
viande et l'essentiel, sinon l'exclusivité des revenus
monétaires. L'agriculture revêt un caractère
aléatoire de ce système caractéristique des zones
semi-arides et les principales cultures pratiquées sont le mil et le
sorgho. L'alimentation du cheptel est presque exclusivement basée sur
l'exploitation des pâturages naturels. L'utilisation des intrants est
assez faible en dehors de la complémentation minérale. Les
éleveurs pratiquant ce système de production adoptent souvent le
mode de vie de transhumance pour garantir à leur cheptel une
disponibilité permanente de
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
17
fourrage. Une partie de la famille se déplace avec les
animaux tandis que la deuxième partie se consacre aux activités
champêtres et au gardiennage du petit noyau d'animaux qui leur assure la
subsistance (MRA, 2003).
5. Contribution de l'élevage dans la vie
socio-économique du pays
Le Niger est un pays agropastoral où l'élevage
joue un rôle socio-économique important. Il occupe plusieurs
milliers d'éleveurs purs et d'agropasteurs en fournissant une gamme
variée d'emplois : éleveurs, agropasteurs, bergers,
intermédiaires de vente, vendeurs de cuirs et peaux, exportateurs des
produits pastoraux, industries de transformation et de vente de lait, etc.
L'élevage est pratiqué par près de 87 p.
cent de la population soit en tant qu'activité principale ou
activité secondaire après l'agriculture. Il permet la fourniture
de l'énergie (force de traction, culture attelée, transport), la
fumure organique, le capital et la valorisation des sous-produits agricoles. Il
permet l'utilisation des terres marginales impropres à l'agriculture. Le
capital bétail est évalué à plus de 1000 milliards
de francs CFA et contribue à hauteur de 12 p. cent au Produit
Intérieur Brut (PIB) et 35 p. cent à l'économie agricole
du pays.

Par ailleurs, l'élevage contribue et de façon
substantielle à la sécurité alimentaire, à la
balance de payement et à la lutte contre la pauvreté. Cette
contribution de l'élevage à la formation du PIB, bien que
qualifiée d'importante, ne reflète pas tout le potentiel de ce
secteur en raison d'une part de la sous estimation due à la non prise en
compte de la valeur de certains produits et services tels que le fumier, la
traction animale,
etc. et d'autre part,
du caractère traditionnel et extensif qui
caractérise l'élevage Nigérien (MRA, 2003).
Au plan individuel, l'élevage joue un rôle
extrêmement important. Ainsi pour l'éleveur, l'animal est un
placement qui sécurise l'argent et qui rapporte des
intérêts puisqu'il produit viande et lait, fumier et
progénitures. L'élevage représente la principale source de
revenus des pasteurs. En plus du rôle purement économique,
l'élevage joue un important rôle socioculturel qui apparait
à travers les multiples manifestations culturelles et les liens sociaux
entre personnes (MRA, 2003).
Les petits ruminants contribuent pour une large part à
l'économie nationale. Le capital bétail apporté par les
petits ruminants déjà en 1982 était de l'ordre de 6
milliards de francs CFA pour les caprins et de 3.450.000.000 de francs CFA pour
les ovins pour un capital bétail global de 60 milliards de francs CFA.
L'exploitation des chèvres et moutons pour la même année a
rapporté 37.487.000 francs CFA pour les exploitations et consommations
locales (animaux sur pieds) et 1.907.000.000 de francs CFA pour peaux de
moutons et chèvres (MRA, 2003). La production laitière tient
aussi une place non négligeable dans cette économie avec une
production annuelle de 209.365.000 litres de lait pour une valeur de
18.424.120.000 FCFA. La production de viande demeure un secteur important : sur
un total de 76.978 tonnes de viande produite, la part des petits ruminants est
de 37.578 tonnes soit 48,8 p. cent (MRA, 2003).

En milieu rural, l'animal est au centre de la vie sociale du
paysan. Les petits ruminants constituent un capital de départ pour la
constitution des troupeaux
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
19
bovins. C'est un trésor important qui contribue
à la renommée des familles. En société pastorale,
la chèvre occupe une place privilégiée. Son endurance au
climat, sa sobriété par rapport aux moutons et aux bovins, sa
prolificité, son aptitude aux longues marches lui confèrent
l'estime de l'homme Touareg qui en fait un animal de choix (MRA, 2003).
6. Contraintes liées à l'élevage
des petits ruminants au Niger 6.1. Obstacles nutritionnels à la
productivité
L'alimentation des animaux pose des problèmes au Niger
où la sécheresse sévit depuis plusieurs années. Les
animaux sont donc confrontés à une sous- alimentation chronique,
affectant toutes les productions. Les petits ruminants, surtout les ovins, en
meurent par troupeau. Les chèvres résistent mieux, car elles
profitent des pâturages aériens et se contentent de débris
végétaux lignifiés. Les jeunes en croissance, les animaux
âgés et les femelles gestantes sont les plus vulnérables.
On assiste alors à des avortements, des mortalités
prénatales et des dystocies maternelles par épuisement.
Pour pallier à ce phénomène, des
aliments complémentaires sous forme de graines de coton et de son de
blé sont distribués pendant la période de soudure.
Toutefois, cette mesure ne peut toucher qu'une minorité d'animaux, car
tous les besoins ne peuvent pas être couverts avec ces seuls aliments
(ZAKARA, 1985).
6.2. Facteurs affectant la croissance
La croissance est liée à l'alimentation.
Celle-ci étant insuffisante, on assiste à des baisses de poids
à certains moments de l'année, surtout pendant les
périodes de soudure, et à une légère hausse en
hivernage ; ce qui présente une courbe en dent de scie. Les jeunes
à la mamelle sont surtout les plus touchés. Il arrive que les
mères refusent leurs petits car, épuisés par l'exportation
de toutes les réserves alimentaires au cours de la gestation, elles se
trouvent incapables de les nourrir (ZAKARA, 1985).
6.3. Problèmes de santé et leur impact sur
la production
La santé est le facteur favorable à toute
production. Elle fait toutefois défaut assez souvent dans les troupeaux
contraignant à des interventions sanitaires perpétuelles. Cette
santé est perturbée par plusieurs maladies. Les plus importantes
fréquemment relevées au niveau des petits ruminants sont les
parasitismes gastro-intestinal et pulmonaire, les coccidioses, les affections
respiratoires sous forme de pneumonie, les affections digestives se traduisant
par des entérites diarrhéiques consécutives à un
déséquilibre alimentaire, les foyers isolés de peste des
petits ruminants, la pasteurellose et l'ecthyma.
Parmi toutes ces maladies, les parasitoses sont les plus
constantes et les petits ruminants lui paient un lourd tribut. Elles
contribuent avec la sous-alimentation à la baisse de la production et
demeurent les facteurs prédisposant à certaines maladies
infectieuses par affaiblissement de l'organisme.

Des déparasitages collectifs sont menés tous les
jours, touchant la majeure partie des effectifs contrôlables (ZAKARA,
1985).
6.4. Mortalités chez les petits ruminants
Les mortalités sont consécutives aux maladies
surtout parasitaires, aux affections respiratoires en périodes
fraîches pendant lesquelles les animaux sont exposés au froid et
à la pluie, mais aussi à la sous alimentation devenue un handicap
important ces dernières années. Des hécatombes
enregistrées en zones sahéliennes en 1973 et tout
récemment en 1984 - 1985 où des milliers d'animaux sont morts par
inanition restent encore dans les mémoires. Parmi les petits ruminants,
les ovins sont les premières victimes, car ils sont moins
résistants et plus fragiles que les caprins (ZAKARA, 1985).
GAGARA H. Mariama
21
CHAPITRE 2 : LA PESTE DES PETITS
RUMINANTS
Définition et dénominations
La Peste des Petits Ruminants (PPR) est une maladie virale,
infectieuse et très contagieuse qui touche les petits ruminants
domestiques. Elle peut cependant également toucher les ruminants
sauvages lorsque ces derniers entrent en contact avec les ruminants
domestiques. Cette maladie est d'évolution très rapide. Elle a
été décrite pour la première fois en Côte
d'Ivoire en 1942. La Peste des Petits Ruminants est due à un virus
antigénique très proche du virus de la Peste Bovine. Elle, se
caractérise cliniquement par un état typhique, des
érosions des muqueuses buccales et une atteinte pulmonaire. Sous forme
épizootique, elle entraine de fortes mortalités, et sous forme
enzootique elle favorise l'apparition de pneumopathies bactériennes
(FAO, 2000).
Répartition géographique

La PPR est une maladie longtemps considérée
comme cantonnée en Afrique de l'ouest où se firent les
premières observations (Côte d'Ivoire et Bénin) (LEFEVRE,
1991). Tous les pays situés entre le Sahara et l'équateur, de
l'océan Atlantique à la mer Rouge, se trouvent dans la zone
d'enzootiédémie de la PPR. En dehors de l'Egypte, l'Afrique du
nord, n'est pas touchée par la PPR. Il en est de même pour
l'Afrique Australe. La zone d'enzootiédémie de la PPR
s'arrête donc apparemment au nord du Kenya. Il existe toutefois dans
certains pays où la présence de la maladie n'a pas
été confirmée officiellement, des indications
sérologiques et/ou cliniques qui font suspecter la présence de
l'infection (FAO,
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
23
2000). Depuis quelques années, elle a
débordé le cadre africain en envahissant le Proche Orient et la
Péninsule Arabique, notamment la République Islamique d'Iran,
l'Iraq, Israël, la Jordanie, le Koweït, le Liban, le Sultanat d'Oman,
l'Arabie Saoudite, les Emirats Arabes Unis et le Yémen. Certains
relevés sérologiques montrent que l'infection existe aussi en
République Arabe Syrienne et en Turquie. De nombreux cas de PPR sont
signalés en Inde, au Népal, au Bengladesh, au Pakistan et en
Afghanistan (LEFEVRE, 1991).
Si on analyse la répartition géographique de la
maladie, il semble difficile de dire si l'expansion de l'aire d'enzootie de la
PPR constatée au cours de ces cinquante dernières années
est bien réelle ou si elle n'est que le reflet d'une plus grande
attention des services vétérinaires et de la disponibilité
d'outils de diagnostic plus performants, voire d'un changement dans le pouvoir
pathogène du virus (FAO, 2000).
3. Etiologie
La PPR est une maladie virale dont l'agent étiologique
est le Virus de la Peste des Petits Ruminants (PPRV). C'est un virus à
ARN, à symétrie hélicoïdale, enveloppé
(BOURDIN et LAURENT-VAUTIER, 1967), de la famille des Paramyxoviridae, du genre
Morbillivirus, qui comprend quatre virus (GIBBS et al, 1979).
La fiche signalétique du virus s'établit comme
suit (LEFEVRE, 1987) : subphyla : Ribo vira
classe : Ribohelica
ordre : Sagovirales
famille : Paramyxoviridae genre : Morbillivirus
avec le virus morbilleux, le virus de la maladie de Carré
et le virus de la Peste Bovine.
Tous ces virus présentent entre eux de grandes
relations antigéniques, mises en évidence par des tests de
protection croisée. Ces relations sont particulièrement
étroites entre le virus de la Peste Bovine et celui de la PPR.
Comme tous les Morbillivirus, le virus de la PPR est
relativement peu résistant en milieu extérieur, ce qui implique
un contact étroit pour sa transmission. Il est excrété
précocement dès l'apparition de l'hyperthermie, dans les
sécrétions conjonctivales, le jetage et la salive et, plus
tardivement, dans les fèces, ce qui explique sa grande
contagiosité (LEFEVRE, 1991).
4. Transmission et épizootiologie

La transmission se fait par voie aérienne, et la porte
d'entrée du virus est la muqueuse naso-pharyngée. Les animaux
infectés excrètent de grandes quantités de virus par le
jetage, les larmes, la salive et les matières fécales. De
très fines gouttelettes de matières virulentes se forment
à partir de ces sécrétions et excrétions et
contaminent l'air ambiant. La toux et les éternuements contribuent
à la formation de ces gouttelettes. Les animaux s'infectent en les
inhalant, d'où la transmission rapide de la maladie quand le contact
entre les animaux est étroit. D'autres ources de contaminations sont
représentées par l'eau, les aliments, les mangeoires, les
abreuvoirs et les
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
25
litières souillées par les matières
virulentes. Néanmoins, la contamination à partir de ces sources
n'est que de courte durée, car le virus de la PPR, tout comme celui de
Peste Bovine, ne survit pas longtemps dans le milieu extérieur en raison
de sa très grande fragilité (FAO, 2000). Par ailleurs, il
n'existe pas de porteur chronique, l'évolution se faisant soit vers la
mort, soit vers la guérison avec une immunité de longue
durée, voire de toute la vie économique de l'animal.
L'espèce et la race jouent un rôle important :
les chèvres sont nettement plus sensibles que les moutons, et parmi
elles, les races guinéennes (chèvres naines d'Afrique de l'Ouest,
chèvres Kirdi, chèvres des lagunes) sont plus sensibles que les
races Sahéliennes (LEFEVRE, 1991).
La PPR évolue sous forme épizootique avec une
mortalité élevée, de l'ordre de 70 à 80 p. cent
dans les pays côtiers du continent africain, de la Mauritanie au
Bénin, selon un cycle d'apparition, dans les villages, de quatre
à cinq ans, délai qui correspond à la reconstitution d'une
population réceptive. En revanche, dans les pays sahéliens de
l'Afrique occidentale et centrale (Mali, Niger, Tchad), la PPR est de type
enzootique : infections inapparentes avec une mortalité faible, mais qui
touche la plus part des animaux (au Tchad, près de 70 p. cent des
chèvres présentent des anticorps anti PPR). Cette relative
résistance des chèvres Sahéliennes pourrait s'expliquer
par le fait que les virus de la famille des Paramyxoviridae sont, à
température égale, plus stables en atmosphère sèche
qu'en atmosphère humide. Ce phénomène entraînerait
une persistance et une circulation du virus plus longue dans les troupeaux.
Deux conséquences sont alors possibles :
· à court terme, un contact précoce des
jeunes avec le virus alors qu'ils sont encore protégés par les
anticorps d'origine maternelle ;
· à long terme, une sélection des races et
l'acquisition d'une résistance
génétique sinon à
l'infection, du moins à ses manifestations cliniques.
Il en ressort que dans les régions arides ou
semi-arides où la PPR évolue de manière enzootique, les
foyers n'apparaissent que rarement et uniquement quand d'autres facteurs
viennent affaiblir les animaux. Par ailleurs, il faut signaler le rôle
joué par la PPR dans l'épizootologie de la Peste Bovine.
Après une atteinte par la PPR, les petits ruminants sont
protégés contre la Peste Bovine, ce qui signifie que dans les
régions où les deux maladies coexistent, les moutons et les
chèvres n'interviennent pas (ou très peu) dans la transmission du
virus bovipestique, contrairement à ce qui se passe dans les pays
où la PPR n'existe pas (LEFEVRE, 1991).
5. Symptomatologie

La durée moyenne de la période d'incubation
varie de deux à six jours. Cette phase est suivie de l'apparition
très rapide de fièvre (température rectale de 40 à
41°C, voire plus). Les animaux touchés semblent très
abattus, somnolents, et ont des poils hérissés qui leur donnent
un aspect ébouriffé, notamment pour les races à poils
courts. Un à deux jours après l'apparition de la fièvre,
les muqueuses buccale et oculaire deviennent rouges avec des
écoulements. Ceux- ci mouillent la face de l'animal (jusqu'à la
mâchoire). Initialement, ils sont séreux, mais deviennent
très vite mucopurulents, en raison de la surinfection bactérienne
et prennent alors une couleur jaunâtre. Ces écoulements sont
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
27
alors tellement épais qu'ils collent les paupières
entre elles ou obstruent les voies nasales, rendant la respiration
difficile.
De petites zones grises localisées, résultant de
la nécrose épithéliale, apparaissent sur les gencives, sur
le coussinet dentaire, sur le palais, les lèvres, à
l'intérieur des joues, et sur le dessus de la langue. Ces zones se
multiplient, augmentent de taille, puis fusionnent entre elles. La paroi
buccale change d'apparence et devient pâle et parsemée de cellules
mortes qui, parfois, forment une couche épaisse de matière
crémeuse. Si on les enlève, on découvre des lésions
érosives superficielles. Dans les cas les moins graves de la maladie,
ces lésions peuvent passer inaperçues et un examen très
approfondi est alors nécessaire pour les déceler. En passant les
doigts sur la face interne de la joue et du palais, on enlève facilement
le tissu nécrosé, nauséabond. Les foyers de nécrose
peuvent être présents au niveau des muqueuses nasales, de la vulve
et du vagin chez les femelles. Les lèvres sont
généralement enflammées, fissurées et couvertes de
croûtes (figure 8). A un stade avancé de la maladie, une haleine
fétide se dégage de la bouche. Les animaux malades ont alors
tendance à garder la bouche ouverte à cause de la forte douleur
qu'ils ressentent.
Au cours des premiers stades de développement de la
maladie, ou dans les cas un peu moins graves, la diarrhée peut ne pas
apparaître. En général, elle survient deux à trois
jours après le début de la fièvre. Les matières
fécales sont molles au début, puis deviennent de plus en plus
liquides, d'odeur nauséabonde, striées de sang et elles
renferment parfois des lambeaux de tissus nécrosés. Quand la
diarrhée n'est pas apparente, l'introduction d'un
coton tige dans le rectum peut révéler l'existence
de matières fécales molles, pouvant contenir du sang.
Les animaux malades ont alors une respiration telle que les
mouvements de leurs parois thoracique et abdominale donnent l'impression qu'ils
dansent. Dans les cas les plus graves, la respiration devient laborieuse,
bruyante avec dilatation des narines et une protubérance de la langue. A
cela s'ajoute une toux grasse et douloureuse. Les signes de pneumonie sont
évidents.
Ces animaux peuvent se déshydrater (les yeux
s'enfoncent dans les globes oculaires) et la mort survient en
général dans les sept à dix jours qui suivent le
début des signes cliniques, même si certains animaux
guérissent après une longue période de convalescence.
La formation de petites lésions nodulaires autour du
museau est une caractéristique de la maladie observée dans les
cas avancés. La cause exacte de leur apparition n'est pas connue, mais
elles sont probablement dues à une infection de Dermatophilus ou
à une réactivation d'une infection latente d'un ecthyma
contagieux. Ces lésions peuvent être confondues avec l'ecthyma
contagieux.

Dans un foyer de PPR, jusqu'à 100 p. cent des animaux
du troupeau peuvent être touchés, et les taux de mortalité
peuvent aller de 20 à 90 p. cent. Ces proportions sont
généralement plus faibles dans les zones enzootiques, car la
plupart des animaux les plus âgés ont survécu à des
infections précédentes et sont protégés à
vie (FAO, 2000).
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008


Figure 8 : Distribution des symptômes dans le temps
(source : LEFEVRE, 1991)
6. Diagnostic

GAGARA H. Mariama
29
Le diagnostic provisoire de la PPR peut être
établi à partir d'informations épizootologiques et
cliniques : maladie caractérisée par du larmoiement, du jetage,
de la diarrhée, associée à des problèmes
respiratoires et des mortalités chez les ovins et ou les caprins, mais
sans aucun effet sur les bovins qui sont en contact avec eux. A l'examen
post-mortem, les observations des lésions caractéristiques de la
maladie permettent de renforcer le diagnostic provisoire. Ce dernier n'est
confirmé que par les examens de laboratoire (FAO, 2000).

7. Méthodes de lutte

Les mesures de prophylaxie sanitaire (contrôle des
déplacements des animaux, quarantaine) et le contrôle
médical (vaccination autour des foyers et dans les zones à
risque) constituent la base de la lutte contre la PPR. Le vaccin contre la
Peste Bovine est fréquemment utilisé. Il existe également
un vaccin homologue contre la maladie qui est préférable à
celui de la Peste Bovine pour éviter les confusions en cas
d'enquêtes sérologiques rétrospectives. Ce vaccin peut
protéger les petits ruminants pendant trois ans (FAO, 2000).

Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008

DEUXIEME PARTIE :
ETUDE
EXPERI MENTALE
GAGARA H. Mariama
31
2008
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
CHAPITRE 1 : MATERIEL ET
METHODES
1. Présentation du Niger et de la zone
d'étude
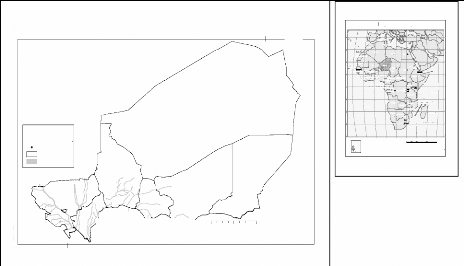
1.1. Situation géographique
Situé en Afrique de l'ouest, le Niger couvre une
superficie de 1 267 000 km2 dont les 2/3 se situent en zone
désertique. Il s'étend entre 11°37' et 23°23' de
latitude Nord et 0° et 16° de longitude Est (figure 9). Il est
à 700 km au Nord du golfe de Guinée, à 1200 km au Sud de
la mer Méditerranée et à 1900 km à l'Est de la
côte Atlantique. Le Niger est limité au Nord par l'Algérie
et la Libye, au Sud par le Bénin et le Nigéria, à l'Ouest
par le Burkina Faso et le Mali et à l'Est par le Tchad. Niamey, la
capitale est située à plus de 1000 km de la mer.
c
Burkina Faso
Mali
Légende
X Chef lieu de région
Gaya
Région
Cours d'eau
Tillaberi
X
REPUBLIQUE DU NIGER
Présentation du Niger
Bénin
Dosso
X
Algérie
GAYA
Système d'informations géographique du Niger
Tahoua
X
Maradi
Nigeria
(SIGNER)
e d'Info "SIGNER"
Réalisation: BAKO Mamane
X
Agadez
X
Zinder
X
0 75 150 300 Kilomètres
X Diffa
Libye
Tchad
Cape Verde
-30°
Guinea-Bissau
!( Capitale Lacs REGION GAYA
Légende
Tropic of Cancer
Equator
Tropic of Capricorn
Sahara Occidental
-20°
Océan Atlantique
Mal Niger
Tchad
Niamey
(!
Bamako
(! GAYA
Burkina Faso
!(
Sierra Leone
(! Benin Nigeria
!( Ghana Togo
Freetown Côte d'Ivoire
(! Lome
(! (!
Accra (!
Abidjan Lagos
Liberia (!
(!
(!
-20°
N ouakchott
Mauritanie
Guinea
St Helena
-10°
Moroc
-10°
Rabat
!(
Sao Tome & Principe !( Gabon
Congo
Golf de Guinée
Guinée Equatoriale
Projection Robinson Méridien central:
-60.00
Algerie
0°
0°
(!
Niger en Afrique
Algers
Tunisie
République Centrafricaine Cameroun
(
10°
!(
Brazzaville ! Kinshasa
!(
10°
Tunis
Yaounde
Mer Mediterranée
!(
(!
Luanda
Tripoli
(!
Namibia
Angola
NDjamena
Libye
(!
Windhoek
Système d'Information Géographique du
Niger : "SIGNER"
Mars 2007
L
Sud Afrique
ngo, DRC
20°
20°
Harare
!( Mozambique Antananarivo
(!
Zimbabwe Madagascar
Botswana
Zambia !(
Lus
Gaborone
!(Pret
(!
Egyp
Suda
Rwan !( Buru !(
30° 40°
30°
Ouganda
!(
oria Maputo (! aziland (!
Black Sea
(!
Tanzania
Malawi
!(
Lilongw e
Cairo
Khatoum
(! Eritrée
!(
Kam
Ethiopie
!(
!(
40°
(!
Dar es Salaam
Comores Glorioso Is
D jibouti
Somalia
Mayotte
!(
Océan Indian
Muqdisho
50°
50°
Seychelles
Mer Arabe
Mauritius
Reunion
60°
60°
2 625
Kilomètres
GAGARA H. Mariama
32
Figure 9 : Présentation de la République du
Niger (source IGN, 2008)
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
33
La zone d'étude est représentée par trois
régions parmi les huit que compte le pays. Il s'agit de :
- La région de Niamey, - La région de Tilla
béry, - La région de Tahoua.
Tableau II : Différentes régions du NIGER
avec leurs superficies (source : MRA, 2003)
|
REGIONS
|
SUPERFICIES (km2)
|
POURCENTAGE DU TERRITOIRE NATIONAL (%)
|
COMMUNES URBAINES
|
COMMUNES RURALES
|
|
AGADEZ
|
667 779
|
52,7
|
4
|
11
|
|
DIFFA
|
156906
|
12,38
|
3
|
9
|
|
DOSSO
|
33844
|
2,67
|
5
|
38
|
|
MARADI
|
38 500
|
3,03
|
10
|
37
|
|
TAH OUA
|
162347
|
12,81
|
9
|
35
|
|
TI LLABERY
|
91 199
|
7,19
|
6
|
38
|
|
ZI N DER
|
116170
|
9,16
|
10
|
45
|
|
NIAMEY
|
255
|
0,02
|
5
|
-
|
|
TOTAL
|
-
|
-
|
52
|
213
|
Km2 : kilomètre carré, % :
pourcentage
1.2. Démographie
La population du Niger est de 11 060 291habitants
(Ministère de l'Economie et des Finances, 2001) avec une densité
moyenne de 8,7 habitants au km2. Cette population est
composée de communautés sédentaires et nomades reparties
entre neuf groupes ethniques (haoussa, djarma, songhaï, peulh, touareg,
kanuri, toubou, arabe et gourmantché). L'ensemble de ces
communautés vit en parfaite harmonie du fait des liens solides (à
la fois historiques, sociaux et religieux) qui les unissent.
Le taux de croissance démographique est de 3,3 p. cent
(Direction de la Statistique et des Comptes Nationaux, 2001).
L'islam, religion majoritaire à plus de 90 p. cent de
la population (Ministère des Affaires Religieuses, 2007) se pratique sur
tout le territoire ; il existe cependant une minorité de
chrétiens et d'animistes.
La langue officielle est le français. Chacun des groupes
sociaux précités dispose de sa propre langue et toute langue a un
statut de langue nationale.
1.3. Etude
physique
1.3.1. Le climat
La position géographique du Niger (situé au
coeur de la zone sahélienne du continent africain) fait de lui un pays
fortement marqué par la continentalité. Les influences maritimes
sur le climat sont fortement atténuées du fait de sa position en
latitude et de son éloignement par rapport à la mer. Le
régime climatique et en particulier les précipitations sont
déterminés par l'alternance saisonnière des influences
maritimes et continentales.
Le Niger, compte quatre zones climatiques. Leurs
différentiations sont principalement liées à la latitude
et à la longitude. Ainsi, du Sud au Nord, on a : le climat Nord
soudanien, le climat sahélien (Sud et Nord), le climat aride et le
climat hyper aride. Cette différentiation est faite par rapport à
la pluviométrie, au vent et à la température.
1.3.2. La pluviométrie

Deux grandes saisons sont rencontrées au Niger :
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
35
- une longue saison sèche qui dure en moyenne huit mois
(octobre à mai), mais qui varie extrêmement en fonction des
régions, allant jusqu'à douze mois dans la partie Nord (SAADOU,
1990) ;
- une saison pluvieuse relativement courte de trois à cinq
mois. Les mois les plus pluvieux sont ceux de juillet et août.
1.3.3. L'humidité de l'air
- Humidité relative : ce facteur varie aussi bien au
cours de l'année en fonction des saisons, qu'au cours de la
journée. Dans la partie Sud du pays, l'humidité est la plus forte
en août, tandis que le minimum s'observe en février-mars. Les
amplitudes les plus fortes sont obtenues pendant la saison pluvieuse,
période qui correspond aux plus faibles amplitudes thermiques diurnes.
Mais au Nord et dans l'extrême Est, on a deux maxima en
août-décembre, puis août-janvier. Les minima correspondent
aux mois d'avril et octobre-novembre.
- L'évaporation : les valeurs moyennes maximales
s'observent en mars- avril (période la plus chaude de l'année) et
les valeurs moyennes minimales en août-septembre (période
où l'humidité relative est la plus forte).
- Les vents : le Niger est soumis aux influences des
alizés avec deux principaux vents qui soufflent en alternance selon les
périodes de l'année :
* l'harmattan, alizé continental Nord-est à Est,
est ressenti d'octobre à février (SAADOU, 1990). C'est un vent
régulier très sec ;

* la mousson, air humide océanique, est
caractéristique de la saison pluvieuse. Il est de direction Sud-ouest et
atteint la partie Sud le plus souvent de mars à avril (SAADOU, 1990).
- Les températures : d'une façon
générale, les températures sont élevées au
Niger. Il existe plusieurs saisons thermiques dans ce pays :
* une saison durant laquelle la température est d'abord
très haute de mars à mai avec des maxima absolus pouvant
dépasser 50°C ;
* une saison froide et sèche qui dure de novembre
à février avec une température pouvant descendre en
dessous de 10°C en décembre et janvier. Les écarts de
température sont plus forts au Nord qu'au Sud.
1.3.4. Les sols
Il y a six (6) catégories de sols au Niger :
- les sols bruts minéraux occupant plus de la
moitié du territoire national et qui sont sans valeur agronomique ;
- les sols peu évolués pauvres en matières
organiques ;
- les sols sub - arides caractérisés par
l'accumulation d'une matière organique très évoluée
;
- les sols ferrugineux tropicaux qui sont des sols très
évolués, faciles à travailler à cause de leur
texture sableuse ;
- les sols hydromorphes qui sont des sols argileux lourds et
durs à
travailler, mais qui conservent l'humidité même en
saison sèche ;
- les vertisols qui ont un très fort taux d'argile, ce
qui limite leur

utilisation.

Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
1.3.5. La végétation
2008
GAGARA H. Mariama
37
La physionomie et la composition de la végétation
sont étroitement liées au zonage climatique. Les subdivisions
climatiques suivantes sont observées :
- un climat Nord soudanien dont la limite Nord se situe au niveau
de l'isohyète 600 mm ;
- un climat sahélien dont les limites se situent entre les
isohyètes 600 mm et 900 mm ;
- un climat saharien limité au Sud par l'isohyète
200 mm.
1.3.6. Hydrographie
Le fleuve Niger traverse le pays dans sa partie extrême
Ouest sur environ 550 km. A l'extrême Est, se trouve le lac Tchad
(environ 3 000 km2). D'autres lacs et cours d'eau sont repartis sur
l'ensemble du territoire.
2. Présentation de la structure d'accueil
La DLV (Direction des Laboratoires Vétérinaires)
du Niger a été créée en 1965 à Niamey avec
une antenne à Zinder et une autre à Tahoua. Elle est
placée sous la tutelle du Ministère des Ressources Animales. Ses
principales missions sont :
- les diagnostics de laboratoire des maladies animales ;
- les enquêtes épidémiologiques des maladies
animales ;
- la production des produits biologiques, notamment les vaccins
et sérums à usage vétérinaire ;
- les contrôles de qualité des denrées
alimentaires d'origine animale ;
- le contrôle des produits biologiques (vaccins), les
analyses biologiques, chimiques et biochimiques vétérinaires ;
- le recyclage des agents d'élevage en cours d'emploi dans
les techniques de diagnostic de laboratoire.
La DLV produit et commercialise six types de vaccins dont :
* le vaccin contre la Péripneumonie Contagieuse Bovine
;
* le vaccin homologue contre la Peste des Petits Ruminants ; * le
vaccin contre le Charbon Symptomatique ;
* le vaccin contre le Charbon Bactéridien ;
* le vaccin contre la Pasteurellose des Petits Ruminants ; * le
vaccin contre la Peste Bovine à la demande ;
Avec comme perspectives :
* le vaccin contre la Clavelée et la Variole Caprine ; *
le vaccin contre la Variole Cameline ;
* le vaccin aviaire contre la maladie de Newcastle.

Sur le plan du diagnostic, des performances sont
enregistrées grâce à la spécialisation des cadres et
l'appui constant de l'AIEA aux nouvelles techniques de diagnostic et en
équipements.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
39
Les animaux
L'étude a concerné 519 animaux dont 253 ovins et
266 caprins issus de trois régions du Niger : Niamey, Tillabéry
et Tahoua qui constituent notre zone d'étude.
Le choix des animaux a été basé sur les
cas de suspicion des foyers de Peste des Petits Ruminants sur un ou plusieurs
troupeaux. Un échantillonnage aléatoire a été
ensuite réalisé dans un lot de sérums
prélevés par l'ONG Karkara sur des petits ruminants dans les
régions de Niamey et de Tilla béry.
L'élevage des animaux est de type semi intensif.
L'herbe constitue la base de l'alimentation des animaux en saison hivernale
sous forme d'herbe de pâture et en saison sèche sous forme de
foin. Cette alimentation est supplémentée de SPAI, de SPA et de
compléments minéraux (natron, sel, pierre à
lécher). Les SPAI sont constitués principalement de son de
maïs, de son de riz, de son de mil, de son de sorgho et de drèches
de brasserie.
L'abreuvement se fait à volonté au niveau du
fleuve, des mares et des marigots en saison hivernale et en saison sèche
au niveau du fleuve, des puits et des forages.
Les animaux vivent en stabulation libre tout le long de
l'année à l'exception de ceux destinés à l'engrais,
certaines femelles gestantes ou allaitantes.

La récolte des données
Elle a été effectuée en plusieurs
étapes :
n

les enquêtes auprès des fermiers détenteurs
des animaux sur lesquels des prélèvements ont été
faits ;
n la réalisation des prélèvements sur les
animaux ;
n la sélection de sérums par
échantillonnage aléatoire sur un lot de sérums ovin et
caprin ;
n l'analyse des prélèvements au laboratoire ;
n les analyses statistiques
4.1. Le questionnaire
Les enquêtes ont été
réalisées dans dix élevages. L'objectif fondamental de ce
questionnaire est de recueillir le maximum d'informations sur la structuration
des troupeaux, les caractéristiques de l'élevage, la conduite des
exploitations à savoir l'alimentation des animaux, le suivi sanitaire,
le système de production.
Des fiches d'enquêtes ont été
élaborées à cet effet (annexe N°1)
4.2. La réalisation des prélèvements
sur le terrain

La saison froide (novembre à février) est la
période pendant laquelle les agents du service de la santé
animale sur le terrain sont confrontés à diverses maladies
animales dont la PPR. Face à la variété des
symptômes faisant suspecter la PPR ou d'autres pathologies, ils font
appel aux agents du laboratoire pour confirmation. Les techniciens du
laboratoire se chargent alors d'effectuer les différents
prélèvements appropriés à la maladie
suspectée et
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
41
dans des conditions adéquates. Ils les acheminent ensuite
au laboratoire pour être analysés.
Dans le cadre de nos travaux, 219 prélèvements
dont 119 réalisés sur des ovins et 100 sur des caprins ont
été effectués parallèlement avec les équipes
mobiles du laboratoire sur le terrain.
Le sang recueilli au niveau de la veine jugulaire dans des
tubes vacutainers secs, a été entreposé dans une
glacière avant d'être acheminé au laboratoire où il
est centrifugé pour l'obtention du sérum. Les échantillons
de sérums sont ensuite transvasés dans des microtubes et
gardés à -20°C avant d'être analysés. Le kit
competitive-ELISA PPR CIRAD et le Kit competitive-ELISA PPR Pirbright ont
été utilisés.
4.3. La collecte des prélèvements par
échantillonnage
L'ONG Karkara, une structure traitant du domaine de la
santé et de la production animale, a collecté des sérums
bovins, ovins et caprins dans une partie de notre zone d'étude (Niamey
et Tillabéry) pour ses propres travaux. Dans le cadre de la bonne
collaboration, elle a mis l'intégralité des échantillons
de sérums ovins et caprins à la disposition du laboratoire pour
contribuer à la réalisation de notre étude.
Ne pouvant être tous analysés en ELISA de
compétition par insuffisance de réactifs, un
échantillonnage aléatoire a été
réalisé utilisant le « Random Number Table » (annexe
N°2).

Un total de 300 échantillons de sérums a
été sélectionné dont 134 provenaient de
l'espèce ovine et 166 de l'espèce caprine.

4.4. Analyse des prélèvements au
laboratoire
Deux types de tests ont été utilisés pour
analyser les prélèvements ayant servi à réaliser ce
travail :
- L'ELISA de compétition ;
- La PCR.
4.4.1. ELISA
a) Introduction
ELISA est l'acronyme d'un examen de laboratoire appelé
en anglais EnzymeLinked ImmunoSorbent Assay ou dosage d'immunosorption
liée à une enzyme, c'est-à-dire un dosage
immunoenzymatique sur support solide.
Ce test entre dans le cadre plus général des EIA
(Enzyme Immuno Assay), dans lequel le dosage est couplé à une
réaction catalysée par une enzyme libérant un composant
coloré suivi par spectroscopie. L'ELISA est une technique biochimique,
principalement utilisée en immunologie, afin de détecter la
présence d'un anticorps (Ac) ou d'un antigène (Ag) dans un
échantillon. La technique utilise un ou deux Ac dont l'un est
spécifique de l'Ag, et l'autre, réagissant aux complexes immuns
(Ag-Ac), est couplé à une enzyme. Cet Ac secondaire, responsable
du nom de la technique, peut aussi causer l'émission d'un signal par un
substrat chromogène ou fluorogène.

L'ELISA pouvant être utilisée tant pour
évaluer la présence d'un Ag que celle d'un Ac dans un
échantillon, est un outil efficace pour déterminer aussi bien des
concentrations sériques d'Ac (test HIV par exemple) que pour
détecter la présence d'un Ag. Il a aussi trouvé des
applications dans l'industrie alimentaire. L'ELISA est devenue un outil
important pour le diagnostic et les programmes
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
43
d'épidémiosurveillance de plusieurs maladies
importantes des animaux domestiques.
La division IAEA/FAO a développé des « Kits
» ELISA qui sont utilisés à large échelle pour le
diagnostic de la Peste Bovine, de la Peste des Petits Ruminants, de la
Péripneumonie Contagieuse Bovine, de la Fièvre aphteuse, de la
Brucellose, de la Babésiose, de la Leucose enzymatique et de la Trypa
nosomose.
Les avantages de l'ELISA sont multiples : c'est un test
simple, rapide, très sensible, peu coûteux, facile à
automatiser et qui permet d'analyser plusieurs sérums à la fois.
Mais la technique a aussi ses inconvénients et ses limites (GEERTS,
2006).
b) Principes
On distingue deux types d'ELISA : le type compétitif
appelé aussi « Blocking » ELISA, et le type non
compétitif.
Pour l'analyse de nos échantillons, nous avons eu recours
au « blocking » ELISA.

Dans un test ELISA de type compétitif, on évalue
dans quelle mesure les Ac qui sont présents dans l'échantillon
sont capables d'inhiber la réaction d'AC couplée à une
enzyme avec l'Ag (fixé sur le support solide). La quantité d'Ac
présente dans l'échantillon à tester, qui a réagi
avec l'Ag, est inversement proportionnelle à l'intensité de la
couleur qui se développe lors de la réaction.
Prélèvement positif Prélèvement
négatif
-
+
Ag

-

Ag
I- Immobilisation de l'antigène sur Support solide
(microplaque en Polystyrène)
Présence d'Ac spécifique Absence d'Ac
spécifique
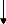
Compétition
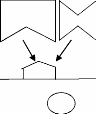
Prélèv Ac Lab Ac
Ag
E
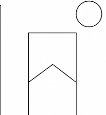
Prélèv.
Ac
Ag
S
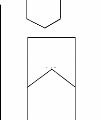
conj
Prélèv.
Ac
Ag
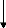
Pas de compétition
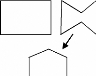
Lab Ac
Ag
Prélèv
Ac
II- Addition du
prélèv. et de l'Ac de
laboratoire
standardisé, hautement Spécifique à l'Ag
considéré
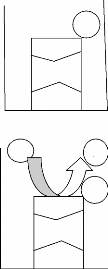
S P
Conj
Lab Ac
Ag
Conj Lab Ac Ag
E
E
Incubation-lavage
|
III- Addition d'Ig anti-espèce (anti-Lab) Conjuguée
à une enzyme ( EX : HRPO)
|
Incubation-lavage
IV- Addition du chromogène et du substrat de l'enzyme
Lecture de l'absorbance
Figure 10 : ELISA compétitive indirecte pour la
détection d'anticorps (source : IAEA, 1994)

Ac : anticorps, Ag : antigène, Conj : conjugué, E :
enzyme, HRPO : Horse Radish Peroxydase, Ig : immunoglobuline, Lab :
laboratoire, Prélèv : prélèvement, P : peroxydase,
S : substrat
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
c) Echantillon à tester
2008
GAGARA H. Mariama
45
A côté du sérum ou du plasma, on peut
aussi tester des échantillons de lait, d'urine, de salive ou même
de selles. L'avantage d'échantillons de lait ou de salive est qu'ils
sont plus faciles à prélever qu'un échantillon de sang.
L'inconvénient par contre est que souvent, le taux d'immunoglobulines y
est plus faible. Dans les selles, on peut rechercher des copro-Ag ou des
copro-Ac. Il est très important que la prise et la conservation des
échantillons de sérums soient faites de manière
adéquate, parce que cela peut influencer les résultats de l'ELISA
par la suite. La prise des échantillons de sang doit être faite de
façon aseptique afin d'éviter toute contamination
bactérienne.
La congélation - décongélation
répétée des sérums a un effet néfaste sur la
qualité des résultats surtout dans l'ELISA pour la
détection des Ac. Pour éviter les problèmes de ce genre,
il vaut mieux préparer de petites quantités (« aliquots
») et de les conserver dans des tubes bien fermés au
congélateur (GEERTS, 2006).
d) Matériel : Il est composé : - d'un incubateur
à 37° ;
- d'un lecteur ELISA ;
- d'un bain marie ;
- des pipettes multicanaux ajustables variables de 5-50 ul,
50-250 ul ; - des pipettes simples ajusta bles de 5-50 ul, 50-200ul, 100-200 ul
;
- des cônes ajustables de qualité ;
- des microplaques Nunc Maxishorp, normalement à fond plat
en polystyrène à 96 cupules ;
- des flacons avec couvercles pour contenir les
différentes dilutions des réactifs.
e) Réactifs et différentes phases de l'ELISA de
compétition
> L'antigène :
*la fiabilité (sensibilité et
spécificité) du test ELISA de compétition dépend
largement de la qualité de l'Ag.
La spécificité et la
répétitivité des résultats seront plus
élevées en utilisant des Ag purifiés (au lieu d'extraits
bruts), mais souvent la sensibilité diminue.
L'utilisation d'Ag recombinants permet une meilleure
standardisation. *la sensibilisation (« coating ») des microplaques
avec l'Ag (ou des immunoglobulines) se fait généralement dans un
tampon alcalin
(carbonate pH neutre ou même pH acide pour des Ag de
type polysaccaride sont aussi utilisés).
> Le blocage (« blocking »)
*But : éviter la fixation non spécifique des
réactifs sur la phase immuno - adsorbante au cours de la
réalisation de l'ELISA. Le blocage doit minimiser les fausses
réactions positives.

*La fixation non spécifique est empêchée de
façon curative ou préventive :
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
47
- Curative par le lavage adéquat des plaques
après chaque étape de l'ELISA en utilisant un tampon de lavage
contenant du tween 20 (acide laurique, détergent).
- Préventive en bloquant les sites libres (non couverts
par l'Ag spécifique) sur la phase solide avec des protéines non
relévantes (sérum - albumine bovine, caséine, lait
écrémé). Elle se fait dans une étape
séparée après la sensibilisation des plaques.
NB : on peut aussi ajouter ces protéines non
relévantes en excès dans les liquides de dilution du sérum
et ou du conjugué.
> Le conjugué
Le conjugué est le résultat du couplage entre
une enzyme et un Ac dirigé contre une immunoglobuline spécifique
d'une certaine espèce animale. Dans le commerce, un large spectre de
conjugué est disponible. Les abréviations suivantes sont souvent
utilisées :
- RAB (IgG/HRP =rabbit anti bovine IgG (Ac produit contre IgG de
bovins par immunisation de lapin) couplé à la « horse radish
peroxydase » (HRP) ;
- GAH (IgM/AP = goat anti horse IgM couplé à la
phosphatase alcaline
(AP).
Les enzymes les plus utilisées sont la peroxydase et la
phosphatase alcaline.

La dilution optimale du conjugué c'est-à-dire
celle qui produit la plus petite réaction non spécifique (couleur
de fond) avec les échantillons négatifs et qui distingue bien les
échantillons positifs, doit être identifiée pour chaque
lot.
> Le substrat/chromogène
Sous l'influence de l'enzyme, certains substrats ont la
propriété de donner des produits de réactions solubles
colorés, qui permettent des dosages précis de densité
optique. La réaction enzyme - substrat a une intensité
proportionnelle à la quantité d'enzyme présente dans le
milieu et donc indirectement avec la quantité d'Ag ou d'Ac qu'on veut
mesurer. Le substrat est différent selon l'enzyme utilisée.
La peroxydase réagit avec le chromogène en
présence d'eau oxygénée (H2O2). Une
couleur différente est obtenue en fonction du produit utilisé
:
-Ortho - phénylène diamine (OPD) ? couleur jaune
-Tétraméthylbenzidine (TMB) ? couleur bleue
-Azimo diéthyl Benzo Thiazoline Sulfonic acid (ABTS) ?
couleur verte
NB : H2O2 est un produit qui n'est pas
très stable. Il faut le protéger contre la lumière et le
conserver dans un réfrigérateur dans un flacon en verre non
transparent. Il faut renouveler régulièrement la solution (au
risque de voir la densité optique chuter). La réaction
enzymatique se fait à température ambiante, ou mieux à
température fixe et dans l'obscurité. Elle peut être
arrêtée en ajoutant une solution acide ou alcaline (changement de
pH).
Comme les lecteurs automatiques d'ELISA sont capables de lire
une plaque entière très vite, l'arrêt de la réaction
enzymatique n'est pas strictement nécessaire.
f) Lavage

Chaque étape de l'ELISA est suivie d'un lavage afin
d'éliminer l'excès de réactifs ; le lavage est très
important pour éviter les réactions non spécifiques.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
49
Pour éviter des problèmes, le lavage doit
être standardisé au maximum. Le plus souvent on utilise un tampon
de lavage (PBS) contenant du tween 20 comme tensio - actif. Le lavage peut se
faire manuellement ou en utilisant des appareils semi - automatiques. Si ces
derniers sont bien entretenus, ils peuvent diminuer la variabilité des
résultats. Souvent, les meilleurs résultats (bonne
réceptivité et reproductibilité) sont obtenus en faisant
le lavage manuel et en prenant soin que les dernières traces du tampon
de lavage soient enlevées en renversant la plaque et en tapant
vigoureusement contre une serviette.
NB : qualité de l'eau
Dans certains pays, la qualité de l'eau n'est souvent
pas optimale ; ce qui peut causer des problèmes dans la
réalisation de l'ELISA. L'eau utilisée pour la dilution du
conjugué est très importante parce que des impuretés
peuvent inhiber ou diminuer son activité enzymatique. De
préférence, on utilise l'eau distillée pour la
préparation des tampons ou du liquide de lavage en ELISA.
g) Lecture et expression des résultats
Les densités optiques (DO) ont été lues au
spectrophotomètre Multiskan EX à 492 nm de longueur d'onde.
Les valeurs des pourcentages d'inhibition (PI) pour les
échantillons des sérums ont été calculées
selon la formule suivante :
OD des sérums échantillons
PI = 100 - × 100
OD du contrôle du monoclonal
Le PI moyen d'un sérum a été calculé
sur deux puits. Les échantillons avec un
PI > à 50 p. 100 ont été
considérés positifs selon les indications du test.
h) Protocole
- Phase de sensibilisation :
L'antigène a été dilué au 1/100.
Pour une plaque : 6000 ul de PBS + 60 ul d'antigène ont
été préparés. La répartition a
été de 50 ul par puits. La plaque a été
incubée pendant 1 heure à 37°C sous agitation ou 1 nuit au
réfrigérateur (+ 4°C) ;
- Solution de lavage : du PBS a été dilué au
1/5 dans de l'eau distillée ou de l'eau désionisée. La
plaque a été lavée 3 fois ;
- Tampon de saturation :
Une solution contenant du PBS + 0,05% de tween 20 + 0,5% de
sérum négatif (v/v) a été
préparée.
Ainsi, pour 6000 ul × 3 (étapes) soit 18000 ul de
PBS par plaque, il a
fallu :
18000 × 0,05 = 9 ul de tween 20
100
18000 × 0,5 = 90 ul de sérum négatif
100
- Phase de compétition : ont été
successivement reparties les
composantes suivantes :

*tampon de saturation : 45u l dans toutes les cupules
GAGARA H. Mariama
51
+ 5 ul en F1, F2, G1,
G2 (Cm)
+ 55 ul en A1 et A2 (Cc)
* sérums à tester : 5u l dans les cupules
* strong positif (C++) : 5u l dans les cupules B1,
B2, C1, C2
* weak positif (C+) : 5u l dans les cupules D1,
D2, E1, E2
* sérum négatif (C-) : 5u l dans les cupules
H1 et H2
* monoclonal : 50u l dans toutes les cupules sauf A1
et A2
La plaque a été incubée 1 heure à
37°C sous légère agitation puis lavée 3 fois en
prenant le soin d'éviter le dessèchement des plaques dans le cas
où il y en a plusieurs ;
- Phase du conjugué :
Le conjugué a été dilué au 1/1000
(v/v) ; soit 600 ul de TS + 6 ul de conjugué
La répartition a été de 50 ul par cupule
dans toute la plaque qui a été ensuite incubée pendant 1
heure à 37°C sous légère agitation. La plaque a
été lavée 3 fois en évitant le dessèchement
;
- Phase du substrat chromogène :
Ont été dissous 1 comprimé d'OPD dans 75
ml d'eau distillée ou désionisée et 1 comprimé de
H2O2 dans 10 ml d'eau distillée ou
désionisée. Pour reconstituer la solution du
substrat/chromogène, ont été utilisés 4 ul de
H2O2 pour 1 ml de solution d'OPD ce qui représente
donc pour 1 plaque : 6 ml d'OPD + 24 ul de H2O2.
La répartition a été de 50 ul par cupule
dans toute la plaque (ainsi que les 8 cupules du blancking) ; la plaque a
été laissée 10 mn à l'obscurité.
- Phase d'arrêt :
Ont été repartis 50 ul d'acide sulfurique à
5,5%
Acide : H2SO4 à 5,5% = 55 ml
H2SO4 + 945 ml H2O distillé ou
désionisée - Lecture avec un filtre à 492 nm.
4.4.2. La PCR
a) Définition
La réaction en chaîne par polymérase (PCR
est l'abréviation anglophone de Polymerase Chain Reaction, acronyme
français ACP pour Amplification en Chaîne par
Polymérisation) est une méthode de biologie moléculaire
permettant d'amplifier plusieurs milliards de fois le nombre de copies d'une
séquence spécifique d'ADN (amplicon), même si la
quantité initiale est très faible (quelques Picogrammes).
b) Principe
La PCR est une technique basée sur une
répétition de cycles de transition de température. Sauf
pour certaines méthodologies, chaque cycle comprend trois étapes
:
La condition native se fait en général à
température ambiante. L'ADN bicaténaire adopte sa conformation en
double hélice.

La dénaturation initiale : avant de commencer les
cycles de PCR proprement dits, une étape de chauffage
(généralement 10 à 15 mn à 95°C) est
réalisée. Cette étape permet de déshybrider les ADN
double brins, de casser les structures secondaires,
d'homogénéiser le milieu réactionnel par agitation
thermique, d'activer les polymérases de type « Hot start », de
dénaturer d'autres enzymes qui pourraient être dans la
solution.
·
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
53
La phase de dénaturation : cette étape
(généralement de 0 à 1 mn à 95°C) permet de
déshyb rider les ADN, de « décrocher » les
polymérases qui seraient encore liées à une matrice et
d'homogénéiser le milieu réactionnel ;
· La phase d'hybridation ou d'appariement des amorces :
cette étape (généralement de 2 à 60 secondes
à 56 - 64°C) permet aux amorces sens et anti sens de s'hybrider aux
ADN matrice grâce à une température qui leur est
thermodynamiquement favorable. Peu de brins d'ADN matrice peuvent s'hybrider
(se lier) avec leur brin complémentaire, ce qui empêcherait la
fixation des amorces, car ces dernières sont bien plus courtes et en
concentration bien plus importante ;
· La phase d'élongation ou d'extension : cette
étape (généralement de 4 à 120 secondes à
72°C) permet aux polymérases de synthétiser le brin
complémentaire de leur ADN matrice à une température qui
leur est optimale. Ce brin est fabriqué à partir des dNTP libres
présents dans le milieu réactionnel. La durée de cette
étape dépend normalement de la longueur de l'amplicon.
c) Protocole
Etant donné que le virus de la PPR est à ARN,
il était nécessaire d'utiliser un protocole permettant de
convertir l'ARN en ADN avant la réalisation de la PCR. Aussi, pour
l'analyse de nos échantillons, avons-nous eu recours à la RT-PCR
one steep (en une étape). C'est un protocole mélangeant les
réactifs de la RT (Reverse Transcriptase qui est une enzyme transcrivant
l'ARN en ADN afin d'utiliser ce dernier en PCR) et de la PCR afin que les deux
étapes puissent se faire sans avoir à ouvrir le tube. Cela permet
de réduire le risque de
contamination ou d'inversion d'échantillons, mais il est
plus difficile
d'optimiser le milieu réactionnel pour chaque
étape.
d) Réalisation de la PCR > Les réactifs
utilisés
· Les primers :
Ce sont deux (2) oligonucléotides dénommés
NP3 et NP4 qui ont été utilisés comme amorces. Ils
amplifient 300 paires de bases :
NP3 (24 bases) : 5' - TCT CGG AAA TCG CCT CAC AGA CTG -3'
NP4 (24 bases): 5' - CCT CCT CCT GGT CCT CCA GAA TCT -3'
Ces amorces se présentent sous forme
lyophilisée à reconstituer avec 1 ml de tampon Tris EDTA (TAE) ou
dans l'eau distillée stérile selon les recommandations du
fabriquant. Ils sont à la concentration de 52,9 mol/ul pour NP3 et 21,9
mol/ul pour NP4 ; la concentration de travail étant de 15 pmol/ul et 2
ul ont été utilisés par réaction.
· Les dNTP

Le réactif utilisé est une solution
prémixée prête à l'emploi. Le
prémélange ou le stock solution est à une concentration de
10 mM de chaque dNTP (dATP, dCTP, dGTP, dTTP). La concentration de travail est
de 25 mM et 2 ul ont été utilisés par réaction. La
conservation a été faite à - 20°C.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
· Le kit de l'ADN polymérase
2008
GAGARA H. Mariama
55
- L'enzyme : il s'agit de la Taq polymérase extraite
à partir de Thermus aquatus, une bactérie thermophile très
résistante à des températures très
élevées. La solution stock est de 5 U/ul. La dilution a
été faite au 1/5 et 2 ul ont été utilisés
par réaction.
- Le tampon de réaction 5X (RT-PCR buffer) : il est
utilisé directement dans la réaction PCR à la dilution au
1/10 ; un volume de 10 ul a été utilisé par
réaction.
-H2O bi/distillée
· Le kit d'extraction de l'ARN
- tampon de lyse RLT,
- solutions de lavage RW1 et RPE, - eau traitée au
DEPC
> L'extraction de l'ARN avec le kit Qiagen
1) Dans un tube Eppendorf, ont été ajoutés
:
· 100 ìl de prélèvement à
tester,
· 350 ìl de tampon de lyse RLT
(mélangés pour une bonne homogénéisation),
· 3,5 ìl de â mercaptoethanol
2) Le lysat a été centrifugé dans une
microcentrifigeuse de paillasse pendant 3 mn pour récupérer le
surnagent homogénéisé ;
3) 350 ìl d'éthanol 70% ont été
ajoutés au lysat homogénéisé et
mélangés à l'aide d'une micropipette ;
4) Le mélange de l'étape 3) a été
mis sur une colonne « RNeasy Spin Column », adaptée à
un tube de 1,5ml et centrifugé 15 secondes à 10 000 tours/min
;
5) Le liquide écoulé a été
rejeté, et le même tube a été
réutilisé à l'étape N° 6 ;
6) Ont été ajoutés sur la colonne «
RNeasy Spin Column » 700 ìl du tampon de lavage RW1. Après
la centrifugation, le liquide écoulé a été
rejeté comme ci- dessus ;
7) La colonne « RNeasy Spin Column » a
été placée dans un nouveau tube de 1,5 ml. Ont
été mis 500 ìl de tampon de lavage RPE (voir NB) sur la
colonne. Une centrifugation comme la précédente a
été effectuée et le liquide écoulé a
été rejeté, mais le tube a été
réutilisé dans l'étape N° 8 ;

NB : Le tampon de lavage RPE est fourni sous forme
concentrée. Il faut ajouter 4 volumes d'éthanol 100% avant
d'obtenir la solution de travail du tampon de lavage RPE.
8) Ont été ajoutés 500 ìl de
tampon de lavage RPE (solution de travail) sur la colonne et la centrifugation
a été faite pendant 2 min à grande vitesse 10 000
tours/min pour éliminer toutes les traces d'éthanol ;
9) La colonne a été transférée dans
un nouveau tube de 1,5 ml pour faire l'élution du RNA avec de l'eau
traitée au DEPC 1% ;
50 ìl d'eau traitée au DEPC 1% ont
été ajoutés sur la colonne et la centrifugation a
été faite pendant 60 secondes à 10 000 tours/mn.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
57
La suspension de RNA ainsi obtenue a été
conservée à -70°C ou -80°C ou immédiatement
utilisée dans la synthèse du cDNA.
> Réaction de Reverse Transcription (RT)
7 ul du mix 1 (tableau III) et 5 ul d'ARN ont
été répartis par puits dans la plaquette ou barrette qui a
été ensuite placée dans le thermocycleur suivant ce
programme : 65°C pendant 5 minutes.
Tableau III : volume des réactifs du mix 1
5 ul
1 ul
1 ul
H20
dNTP
Mix 1
Volume pour 1 échantillon
Radom primer
8 ul par puits de mix 2 (tableau IV) sont ajoutés dans la
plaquette ou barrette qui a été placée dans le
thermocycleur selon le programme ci-dessous :
Programme : 37°C pendant 50 minutes 70°C pendant 15
minutes
Tableau IV : volumes des réactifs du mix 2
DTT
Mix 2
Volume pour 1 échantillon
Tampon 5X
4 ul
2 ul
RNase out
MMLV
1 ul
1 ul
> Réaction de PCR one step
50 ul de mix (tableau V) ont été répartis
par puits dans la plaque ou barrette. Ont été prévus les
contrôles suivants :
-contrôle positif : cDNA ou produit de la PCR
-contrôle négatif : H2O
bi/distillée
La plaque ou barrette a été placée dans le
thermocycleur et l'amplification de l'ADN a été lancée
selon le programme suivant :
1) 95°C pendant 10 min
2) 94°C pendant 45 s
3) 55°C pendant 30 s
4) 72°C pendant 30 s
Le cycle a été repris 29 fois de l'étape 2)
à l'étape 4)
5) 72°C pendant 5 min
6)

4°C pendant 1 min
Mix
Volume pour 1 échantillon
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
Tableau V : volumes des réactifs du mix de la
PCR
Echantillon (après la RT)
Tampon 5X (RT-PCR buffer)
dNTP
Mix primers (NP3, NP4)
Taq polymérase
H20 DEPC
Total
10 ul
10 ul
2 ul
2 ul
2 ul
24 ul
50
GAGARA H. Mariama
59
e) Analyse de l'amplifiât
> Electrophorèse en gel d'aga rose
Sa réalisation débute en général
avant la fin de l'amplification.
· Les tampons et réactifs
- Poudre d'Aga rose ;
- Tampon d'électrophorèse TAE 10X : le TAE 1X est
obtenu en diluant 10 fois la solution stock ;
- Gel loading buffer (GLB) ou marqueur
d'électrophorèse ou bleu de charge : ce composé sert
à la fois à faire descendre l'ADN amplifié au fond du
puits du gel et à suivre l'évolution de la migration grâce
à sa couleur ;
- Bromure d'éthidium : solution stock de 10mg/ml
utilisé à la concentration de travail de 0,5 ug/ml de gel
préparé ;
- Marqueur de poids moléculaire : solution stock de
concentration de 1 ug/ul dilué au 1/10 pour avoir la solution de
travail. Sa taille est de 100 paires de bases.
· Protocole
1) 2 g d'agarose ont été mélangés
à 150 ml de TAE 1X. La dissolution a été faite dans un
four à micro-onde ;
2) Après refroidissement (environ 40° C), la
solution a été mélangée avec 10 ul de bromure
d'éthidium ;
3) Dans le moule apprêté, un peigne de 12 dents
a été posé à 0,5 cm de l'un des bords puis le gel a
été coulé lentement au centre en prenant soin
d'éviter la formation des bulles qui, si elles se formaient,
étaient éliminées à l'aide d'une pointe de
micropipette pour ne pas gêner la migration ;
4) Après solidification, le peigne a été
retiré délicatement et le moule a été placé
dans la cuve à électrophorèse contenant du TAE 1X en
prenant soin de s'assurer que les puits sont du côté de la borne
négative, car la migration se déroule vers la borne positive ;
5) La quantité suffisante de TAE 1X a
été ajoutée pour couvrir le gel ;
6) Dans le premier puits du gel, ont été
introduits 5 ul de marqueur de poids moléculaire ;
7)
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
61
Dans les autres puits du gel, ont été
déposés un mélange contenant 5 ul de bleu de charge et 15
ul de produits PCR préalablement préparés sur
du papier parafilm (le deuxième puits contenant le
témoin positif et le troisième puits le témoin
négatif) ;
8) Après couverture du bac de migration, le
générateur a été réglé à 60 V.
La migration se poursuivait jusqu'à ce que le marqueur
d'électrophorèse atteigne la taille des produits PCR attendus.
> Visualisation sous rayonnement ultraviolet
A la fin de la migration, le DNA a été
visualisé directement sur une table d'ultraviolet. Le gel a
été ensuite photographié.
4.5. Analyses statistiques
La prévalence sérologique des anticorps anti-PPR
a été évaluée en rapportant le nombre de
sérums positifs au nombre total de sérums. Les résultats
obtenus ont été analysés avec le logiciel STATISTICA 6.1.
Ces résultats sont exprimés en pourcentage (%) et les
différences sont considérées significatives au seuil de
probabilité P < 0,05.

GAGARA H. Mariama
63
CHAPITRE 2 : RESULTATS ET
DISCUSSION
1. Résultats
1.1. Les
caractéristiques de l'élevage
1.1.1. Le système d'exploitation des animaux
L'exploitation des animaux est de type extensif et se fait sur
de vastes étendues avec des mouvements de transhumance à la
recherche d'eau et de pâturage.
1.1.2. Les caractérisations des troupeaux
La taille des troupeaux varie d'un effectif de 8 à 207
têtes. La répartition est la suivante :
· Effectif < 50 = 50,00 p. cent
· 50 < effectif < 100 = 20,00 p. cent
· 100 < effectif < 150 = 10,00 p. cent
· 150 < effectif < 200 = 10,00 p. cent
· 200 > effectif = 10,00 p. cent 1.1.3. Le
système de production
Pour la totalité des 10 exploitations ayant fait
l'objet de notre étude, le système de production est libre. Les
producteurs optent pour la monte naturelle surtout s'ils sont en possession
d'un géniteur ayant de bonnes
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
performances de production et de reproduction. La monte
naturelle est pratiquée depuis toujours et à la grande
satisfaction des éleveurs si les conditions d'élevage sont
satisfaisants. Ses avantages résident dans le fait qu'elle est moins
coûteuse et ne nécessite aucun contrôle.
1.1.4. Les mouvements des troupeaux
8 producteurs des 10 ne maîtrisent pas les mouvements
des troupeaux au sein de leurs exploitations car les mises- bas, les
mortalités, les ventes et autres types de sorties ne sont pas
répertoriés. De ce fait, nous disposons de peu d'informations sur
cet aspect.
Une mise- bas est recensée par femelle et par an si
les conditions alimentaires et sanitaires sont satisfaisantes. En
période de soudure où le pâturage se fait rare, les animaux
parcourent de longues distances à la recherche d'herbe et d'eau ; ce qui
occasionne des cas d'avortement (7 p. cent) chez les femelles gestantes. La
ration alimentaire est déficiente et les femelles ont un cycle de
reproduction qui n'est pas toujours favorable à une
fécondation.
Les mortalités sont rares (3 p. cent) dans les
exploitations où l'ont dispose des renseignements sur cet aspect et
où l'alimentation et le suivi sanitaire sont satisfaisants. Toutefois
elles peuvent atteindre 11 p. cent si ces aspects sont négligés,
surtout chez les jeunes ou en cas de maladies contagieuses dont la transmission
est favorisée par la promiscuité des animaux.
Les ventes et l'autoconsommation concernent surtout les
mâles (20 p. cent) qui sont parfois vendus très jeunes ; ce qui
explique d'ailleurs le nombre élevé de femelles et de jeunes
à la mamelle au sein des troupeaux.
1.2. La conduite des exploitations
1.2.1. Les habitats et infrastructures
L'habitat est de type traditionnel pour les 4/5 des
exploitations c'est-à-dire qu'il se résume en une clôture
faite de branchages ou de tiges de mil séchées. Pour le reste, un
enclos en banco avec une toiture en tiges de mil ou branchage, est
aménagé au sein des habitations. Les animaux sont attachés
à des piquets (figure 11).
Ces enclos sont équipés d'abreuvoirs et de
mangeoires en demi-fûts, bassines, seaux et tous autres ustensiles
ménagers usagés.
Les enclos sont nettoyés à une fréquence de
trois fois en moyenne dans la semaine.

Figure 11 : Hangar avec piquets pour ovins
1.2.2. Le suivi sanitaire des animaux
En saison hivernale, avec la pâture, les animaux
ingèrent d'importantes quantités de parasites ; ce qui engendre
des cas de parasitisme interne dans 7 exploitations sur les 10
concernées.
2008
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
En saison sèche et froide, les problèmes
d'ordre respiratoire s'observent durant tout le temps que dure cette
période et dans toutes les exploitations. On observe des symptômes
comme la toux, l'écoulement nasal, la respiration dyspnéique.
Quelques cas isolés de maladies à
caractère diarrhéique, des mammites, des dystocies sont
rencontrées (figures 12 et 13).
Le suivi sanitaire est assuré par les agents de
l'élevage de la zone, mais certains cas pathologiques leurs
échappent car ce ne sont pas toutes les fois que les producteurs font
appel à eux.
Les vaccinations s'effectuent selon le protocole du
Ministère des Ressources animales c'est-à-dire contre la
Péripneumonie Contagieuse Bovine (PPCB) qui est obligatoire, la Variole
ovine...

Figure 12 : Diarrhée chez un ovin Figure 13
: Encombrement nasal
chez un ovin
65
GAGARA H. Mariama

1.3. La prévalence de la Peste des Petits Ruminants
chez les ovins et les caprins
1.3.1. Prélèvements analysés en ELISA
de compétition
a) Prévalence globale de la Peste des Petits Ruminants
Le taux de prévalence de la Peste des Petits Ruminants
varie en fonction des espèces.
Ainsi chez les ovins, sur 253 sérums analysés, 105
sérums étaient positifs soit un taux de prévalence de
41,50 p. cent.
Chez les caprins, on enregistre un taux de prévalence de
47,36 p. cent représentant les 126 cas positifs sur les 266
sérums analysés.
La différence n'est pas pour autant statistiquement
significative au seuil de positivité de 5 p. cent.
Le taux de prévalence de la Peste des Petits Ruminants
dans la zone Nord-ouest du Niger est de 44,50 p. cent, car sur un total de 519
sérums analysés, 231 cas positifs ont été
enregistrés (Tableau III).
GAGARA H. Mariama
67
ESPECES
NOMBRE DE SERUMS
|
NOMBRE DE CAS POSITIFS
|
PREVALENCE (%)
|
Ovins
|
253
|
105
|
41,50a
|
Caprins
|
266
|
126
|
47,36a
|
TOTAL
|
519
|
231
|
44,50
|
|
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
Tableau VI : Prévalence globale de la PPR
008
Les pré valences de la même colonne suivies des
mêmes lettres en exposant ne sont pas statiquement différentes au
seuil de 5%
b) Prévalence de la Peste des Petits Ruminants chez les
ovins en fonction des localités
Le taux de prévalence de la Peste des Petits Ruminants
chez les ovins varie en fonction des localités (Tableau IV) :
· à Tillabéry, 78 cas de PPR ont
été identifiés sur 184 sérums analysés, soit
un taux de prévalence de 42,39 p. cent.
· à Niamey, sur un total de 25 sérums
analysés, 7 se sont révélés positifs ce qui
implique un taux de prévalence de 28,00 p. cent.
· en ce qui concerne la région de Tahoua, 20
sérums se sont révélés positifs sur un total de 44
sérums analysés ; ce qui équivaut à un taux de
prévalence de 45,45 p. cent.
Cependant, la différence entre les taux de
prévalences de ces 3 localités n'est pas statistiquement
significative au seuil de positivité de 5 p. cent.
Tableau VII : Prévalence de la PPR chez les ovins
en fonction des localités
LOCALITES
|
NOMBRE DE SERUMS
|
NOMBRE DE CAS POSITIFS
|
PREVALENCE
|
|
|
|
(%)
|
|
Tilla béry
|
184
|
78
|
42,39a
|
|
Niamey
|
25
|
7
|
28,00a
|
|
Ta houa
|
44
|
20
|
45,45a
|
|
TOTAL
|
253
|
105
|
41,50
|
Les pré valences de la même colonne suivies des
mêmes lettres en exposant ne sont pas statiquement différentes au
seuil de 5%
c) Prévalence de la Peste des Petits Ruminants chez les
caprins en fonction des localités
Pour les caprins, le taux de prévalence varie aussi en
fonction des localités.
Les taux de prévalence observés à Niamey et
à Tahoua qui sont
respectivement de l'ordre de 58,33 p. cent et 54,62
p. cent sont supérieurs à celui observé dans la
région de Tillabéry qui est de 37,70 p. cent. En effet, sur un
total de 36 sérums analysés à Niamey, 21 ont
été positifs et à Tahoua, 59 sérums sont positifs
sur les 108 analysés. Tandis que Tillabéry n'enregistre que 46
cas positifs sur un total de 122 sérums analysés (Tableau V).
Tableau VIII : Prévalence de la PPR chez les
caprins en fonction des localités
|
LOCALITES
|
NOMBRE DE SERUMS
|
NOMBRE DE CAS POSITIFS
|
PREVALENCE
|
|
|
|
(%)
|
|
Tilla béry
|
122
|
46
|
37,70b
|
|
Niamey
|
36
|
21
|
58,33a
|
|
Ta houa
|
108
|
59
|
54,62a
|
|
TOTAL
|
266
|
126
|
47,36
|

Les pré valences de la même colonne suivies des
lettres différentes en exposant sont statistiquement différentes
au seuil de 5%
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
69
Prévalence de la Peste des Petits Ruminants chez les
ovins en fonction du sexe
La prévalence de la Peste des Petits Ruminants est
variable d'un sexe à un autre.
Dans la région de Tillabéry, ont
été identifiés 51 animaux tous sexes confondus. Sur les 12
mâles, 7 se sont révélés positifs soit un taux de
prévalence de 58,33 p. cent. Chez les femelles, un taux de
prévalence de 58,97 p. cent représentant les 23 cas positifs sur
les 39 analysés ont été enregistrés. Cependant, le
taux de prévalence chez les mâles et celui des femelles ne sont
pas statistiquement différents au seuil de 5 p. cent.
Quant à la région de Niamey, 6 femelles
uniquement ont été identifiées et 2 se sont
révélées positives soit un taux de prévalence de
33,33 p. cent (tableau VI).
Tableau IX : Prévalence de la PPR chez les ovins en
fonction du sexe
|
LOCALITES
|
NOMBRE DE
|
NOMBRE/SEXE
|
NOMBRE DE
CAS POSITIFS
|
PREVALENCE
(%)
|
|
SERUMS
|
|
|
|
|
|
|
|
|
M
|
F
|
M
|
F
|
M
|
F
|
|
Tilla béry
|
51
|
12
|
39
|
7
|
23
|
58,33a
|
58,97a
|
|
Niamey
|
6
|
0
|
6
|
0
|
2
|
0,00
|
33,33
|
|
TOTAL
|
57
|
12
|
45
|
7
|
25
|
58,33a
|
55,55a
|
Les pré valences de la même ligne suivies des
mêmes lettres en exposant ne sont pas statistiquement différentes
au seuil de 5 p.100

M : mâle, F : femelle
) Prévalence de la Peste des Petits Ruminants chez les
caprins en fonction du sexe
En ce qui concerne les caprins, très peu de renseignements
ont été recueillis en ce qui concerne le sexe.
A Tillabéry, les 3 femelles identifiées se sont
toutes révélées positives soit un taux de
prévalence de 100 p. cent. Par contre il n'y a eu aucun cas positif pour
le sexe mâle.
Dans la région de Niamey, aucun cas positif n'a
été identifié (tableau VII).
Tableau X : Prévalence de la PPR chez les caprins
en fonction du sexe
|
LOCALITES
|
NOMBRE DE
|
NOMBRE
/SEXE
|
NOMBRE DE CAS
POSITIF
|
PREVALENCE
(%)
|
|
SERUMS
|
|
|
|
|
|
|
|
|
M
|
F
|
M
|
F
|
M
|
F
|
|
Tilla béry
|
4
|
1
|
3
|
0
|
3
|
0,00
|
100,00
|
|
Niamey
|
6
|
2
|
4
|
0
|
0
|
0,00
|
0,00
|
|
TOTAL
|
10
|
3
|
7
|
0
|
3
|
0,00
|
42,85
|
M : mâle, F : femelle
f) Prévalence de la Peste des Petits Ruminants chez
les ovins en fonction de l'âge
Le taux de prévalence de la Peste des Petits Ruminants
chez les ovins varie d'un âge à un autre :

· A Tillabéry, sur 17 jeunes, 12 cas positifs
ont été enregistrés soit un taux de prévalence de
70,58 p. cent. 17 cas positifs ont été relevés sur les 34
adultes ce qui représente un taux de prévalence de 50 p. cent. Le
taux de
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
71
prévalence chez les jeunes est significativement
supérieur à celui observé chez les adultes (p < 0,05 p.
cent).
· A Niamey par contre, 2 cas positifs ont
été rencontrés sur les 6 adultes ce qui représente
un taux de prévalence de 33,33 p. cent. Aucun jeune n'a pu être
enregistré (tableau VIII).
Tableau XI : Prévalence de la PPR chez les ovins en
fonction de l'âge
|
LOCALITES
|
NOMBRE DE
|
NOMBRE/AGE
|
NOMBRE DE
CAS POSITIFS
|
PREVALENCE
(%)
|
|
SERUMS
|
|
|
|
|
|
|
|
|
J
|
A
|
J
|
A
|
J
|
A
|
|
Tilla béry
|
51
|
17
|
34
|
12
|
17
|
70,58a
|
50,00b
|
|
Niamey
|
6
|
0
|
6
|
0
|
2
|
0,00
|
33,33
|
|
TOTAL
|
57
|
17
|
40
|
12
|
19
|
70,58a
|
47,50a
|
Les prévalences de la même ligne suivies des lettres
différentes en exposant sont statistiquement différentes au seuil
de 5%
A : adulte, J : jeune
g) Prévalence de la Peste des Petits Ruminants chez
les caprins en fonction de l'âge

Chez les caprins, très peu de renseignements ont
été recueillis en ce qui concerne l'âge. De ce fait, 3 cas
positifs ont été rencontrés sur les 4 adultes
traités ; ce qui représente un taux de prévalence de 75 p.
cent (tableau IX).
Tableau XII : Prévalence de la PPR chez les caprins
en fonction de l'âge
LOCALITES
|
NOMBRE DE
SERUMS
|
NOM BRE/AG E
|
NOMBRE DE CAS
POSITIFS
|
PREVALENCE
(%)
|
|
|
J
|
A
|
J
|
A
|
J
|
A
|
|
Tilla béry
|
4
|
0
|
4
|
0
|
3
|
0,00
|
75,00
|
|
Niamey
|
6
|
2
|
4
|
0
|
0
|
0,00
|
0,00
|
|
TOTAL
|
10
|
2
|
8
|
0
|
3
|
0,00
|
37,50
|
A : adulte, J : jeune
1.3.2 - Prélèvements analysés en PCR
La technique de diagnostic PCR a été
réalisée sur des écouvillons. Tous les animaux sur
lesquels le sang a été prélevé n'ont par
été concernés par l'écouvillonnage, car l'objectif
était de confirmer par une autre technique la présence de la
Peste des Petits Ruminants dans les élevages prospectés.
Sur les 26 prélèvements réalisés
dans les 4 localités sur des ovins et caprins
suspects (figure 14 A
et B), 8 ont été positifs (Figure 15) soit une prévalence
de
30,76 p. cent.
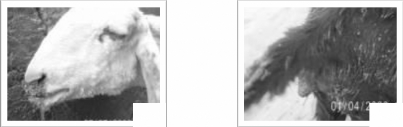
A B

Figure 14 : Etat des ovins dont les
prélèvements ont été positifs en PCR A : Ecoulement
nasal d'une brebis ; B : Diarrhée profuse d'une brebis
1 2 3 4 5 6 7 8 9 10 M

GAGARA H. Mariama
73
Figure 15: Gel d'agarose (1,5% W/V) des produits de
l'amplification, par PCR, réalisé sur des écouvillons
suspects d'ovin. Les amorces NP3 et NP4 qui amplifient une séquence de
300 paires de bases (pb) ont été utilisées. M : marqueur
de poids moléculaire ; + : témoin positif ;
- : témoin négatif ; 1 à 10 matériel
suspect. Echantillons positifs : 1 et 4
1.3.3. Prélèvements analysés à
la fois en ELISA et en PCR
13 ovins et 2 caprins, ont été concernés
à la fois par le prélèvement de sang (sérum) pour
l'ELISA et des écouvillons destinés à la PCR. Seuls 2
étaient positifs à la fois par l'ELISA et par le PCR ; ce qui
confirme la fiabilité des deux techniques dans la détection de la
présence du virus de la PPR chez les ovins et les caprins.
5 animaux ont été positifs en sérologie et
n'ont pas été positifs à la PCR.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
2. DISCUSSION
La prévalence de la Peste des Petits Ruminants a
été de 45,50 p. cent pour l'ensemble des sérums
analysés. Cette séroprévalence trouvée à
l'échelle de la zone Nord-ouest du Niger (Tahoua, Tillabéry et
Niamey) a été proche du taux obtenu dans certaines
régions. Au Gujarat en Inde, PRAKASH (2007), a trouvé une
prévalence de 36,70 p. cent ; Au Mali, TOUNKARA et al. (1996) SANGARE et
al. (2007), ont déterminé respectivement une
séroprévalence de 32,04 p. cent et 37 p. cent ; en 2002, la
séroprévalence de la PPR déterminée au Cameroun par
AWA et al. était de 30 p. cent.
Ces résultats peuvent s'expliquer par le fait que dans
les régions arides ou sémi-arides où la PPR évolue
de manière enzootique, les foyers n'apparaissent en
général que si d'autres facteurs viennent affaiblir les animaux.
Au Niger, pendant la période froide s'étendant de novembre
à février, les températures sont très basses ; ce
qui prédispose aux affections pulmonaires. D'autre part, cet intervalle
correspond à la période de soudure avec rareté ou
inexistence du pâturage naturel. La déficience alimentaire qui en
résulte amoindrit la résistance des animaux constituant ainsi un
champ favorable aux maladies.
En revanche, la séroprévalence a
été plus faible dans d'autres régions. C'est ainsi qu'au
Nord du Burkina Faso (SOW et al., 2008) elle a été de 28,90 p.
cent ; au Sultanat d'Oman (TAYLOR et al., 1990) elle a été de 24
p. cent et en Turquie (OZKULA et al., 2002) elle a été de 22,4 p.
cent. Elle a été encore plus faible en Côte d'Ivoire
(COUACY., 1994, cité par
COUACY. et al., 2002) soit d'environ 19
p. cent ainsi qu'en Ethiopie (ABRAHAM et al., 2005) avec environ 10 p. cent.
GAGARA H. Mariama
75
Cette étude a aussi montré que la
prévalence sérologique de la Peste des Petits Ruminants variait
d'une espèce à une autre. Ainsi, la prévalence
sérologique de la PPR a été relativement plus
élevée chez les caprins avec 47,36 p. cent que chez les ovins
avec 41,50 p. cent. En effet, lors de la transmission de la Peste des Petits
Ruminants, les chèvres sont nettement plus sensibles que les moutons.
Cette tendance est conforme à celle observée au
Cameroun en 2002 (AWA et al), où la prévalence sérologique
chez les caprins (44 p. cent) était supérieure à celle
observée chez les ovins (29 p. cent). Il en est de même au Punjab
une province du Pakistan où KHAN et al. en 2007, ont enregistré
une plus forte séropositivité chez les caprins avec 51,19 p. cent
que chez les ovins avec 39,02 p. cent ; au Nord ouest du Mali la
séroprévalence déterminée par SANGARE et al. (2007)
qui était de 44 p. cent chez les caprins est supérieure à
celle des ovins qui s élevait à 34 p. cent.
Par contre, ces résultats sont en contradiction avec
ceux observés par SOW et al., en 2008 au Nord du Burkina où la
prévalence sérologique est de 33,09 p. cent chez les ovins et
23,01 p. cent chez les caprins. En Turquie (OZKULA et al., 2002), elle
était de 29,2 p. cent chez les ovins et de 20 p. cent chez les caprins ;
au Gujarat en Inde (PRAKASH, 2007), elle était de 54,02 p. cent chez les
ovins et de 32,65 p. cent chez les caprins. En Ethiopie, ABRAHAM et al. ont
trouvé en 2005 une séroprévalence de 13 p. cent chez les
ovins et de 9 p. cent chez les caprins.
Ces résultats variés montrent que la
sensibilité à la PPR n'est pas nécessairement liée
à l'espèce de petits ruminants considérée, mais
certainement aux conditions d'élevage et aux facteurs individuels.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
Par ailleurs, il ressort de cette étude que la
prévalence sérologique de la Peste des Petits Ruminants varie en
fonction des localités.
Chez les ovins, la prévalence sérologique est de
42,39 p. cent à Tillabéry, de 28 p. cent à Niamey et de
45,45 p. cent à Tahoua. Mais ces résultats ne sont pas
statistiquement différents à cause des petits nombres de
sérums analysés à Niamey et à Tahoua.
Chez les caprins, la région de Niamey présente
la valeur la plus élevée (58,33 p. cent) suivie par celle de
Tahoua (54,62 p. cent). Cela pourrait être dû aux différents
foyers de PPR au sein desquels ont été effectués bon
nombre de prélèvements. Tillabéry enregistre la plus
faible prévalence sérologique (37,7 p. cent) qui peut être
dû au fait que les animaux proviennent du même élevage ce
qui peut biaiser l'échantillonnage.
En fonction du sexe, il a été constaté
que la séroprévalence chez les ovins à Tillabéry a
été de 58,97 p. cent chez les femelles et de 58,33 p. cent chez
les mâles. Ces résultats ne sont pas statistiquement
différents à cause de la petite taille des
prélèvements. Un grand nombre de prélèvements
était certes collecté mais très peu possèdent des
identifications en ce qui concerne le sexe des animaux.

La prévalence sérologique chez les ovins dans la
région de Tillabéry, a été plus
élevée chez les jeunes avec 70,58 p. cent que chez les adultes
avec 50 p. cent. Cela peut s'expliquer par le fait que la
réceptivité des animaux, lors de l'infection par le virus de la
PPR, est fonction de l'âge (LEFEVRE, 1987). Les jeunes animaux de 2
à 18 mois sont plus sensibles que les adultes. Ces résultats ne
sont pas conformes avec ceux établis par SOW et al. en 2008 et
GAGARA H. Mariama
77
TOUNKARA et al. en 1996 qui ont établi que la
prévalence sérologique était plus élevée
chez les animaux âgés que chez les animaux jeunes parce qu'en zone
d'enzootie, plus les animaux sont âgés, plus le risque de
contamination par le virus de la Peste des Petits Ruminants est grand,
entraînant lors de contamination, la présence d'anticorps
spécifiques dans leurs sérums.
Par rapport aux deux techniques utilisées, la RT-PCR
one step a permis la mise en évidence de la présence du virus par
la quantification de l'ARN viral transcrit en ADN. L'ELISA n'a permis que de
détecter les anticorps anti PPR présents dans les sérums
des animaux. Ces anticorps pouvant être acquis par la vaccination avec le
vaccin contre la Peste des Petits Ruminants. Et, bien que d'une importance
capitale, très peu de renseignements sur l'aspect vaccination contre la
PPR des animaux sur lesquels ont été effectués nos
prélèvements, sont à notre disposition.
Ce fait explique certainement l'existence de cas positifs en
ELISA qui ne l'étaient pas en PCR. Toutefois la lecture de la
séroprévalence globale obtenue, montre que l'incidence de la
vaccination sur les résultats obtenus est négligeable. En effet
la séroprévalence aurait approché les 100 p. cent si des
anticorps vaccinaux étaient présents chez les animaux des
élevages prospectés au moment des prélèvements.
CONCLUSION
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
Dans la région Nord ouest du Niger, bien que les
informations collectées soient fragmentaires et incomplètes, il
ressort de l'étude que la prévalence sérologique de la
Peste des Petits Ruminants soit relativement élevée : 44 p. cent
chez les ovins et caprins des zones prospectées.
Les conditions d'élevage défectueux, la
malnutrition et les carences
alimentaires dues à une saison pluvieuse
aléatoire, la rudesse des saisons (fraîcheur intense et
poussière) en sont pour une grande part les facteurs favorisants et
déclenchants.
Dans un pays où l'élevage contribue pour une
large part dans le PIB, il est important de protéger le cheptel contre
les maladies à incidence économique sérieuse telles que la
Peste des Petits Ruminants. Toutefois, le Niger se trouve aujourd'hui
confronté à des problématiques contradictoires
marqués par une démographie galopante et un accroissement des
besoins des populations en protéines animales alors que dans le
même temps, les ressources affectées à
l'amélioration sanitaire du cheptel stagnent, voire régressent.
Ces éléments rendent complexes les choix en matière de
recherche et de développement. Les thématiques prioritaires et
les stratégies devront être adaptées en tenant compte des
pathologies dominantes et des moyens d'intervention.

En considérant les impératifs
économiques, il conviendrait que des décisions judicieuses soient
prises pour affecter les crédits aux activités pouvant avoir des
effets optimaux sur la productivité du cheptel dans un minimum de temps.
La lutte contre la Peste des Petits Ruminants a une place de choix dans les
actions à mener.
SUGGESTIONS
GAGARA H. Mariama
79
+ Les informations sur la Peste des Petits Ruminants
étant souvent disparates et limitées, il conviendrait de mettre
en oeuvre les études épidémiologiques permettant
d'élaborer des stratégies de lutte visant à freiner la
dissémination de la maladie. La réorganisation des structures
d'élevage s'impose à cet effet pour obtenir de meilleurs
résultats.
+ En vue d'améliorer les moyens de lutte contre la
Peste des Petits Ruminants, le renforcement et la modernisation des structures
de diagnostic de même que la disponibilité d'un vaccin efficace et
d'anti infectieux s'impose. La production locale de produits biologiques peut
permettre d'en amoindrir les coûts tout en assurant leur large
diffusion.
+ Les infrastructures d'élevage doivent être
également améliorées et le personnel technique
qualifié renforcé pour obtenir de meilleurs résultats dans
la lutte contre la PPR
+ Il conviendrait enfin de poursuivre ce travail par la
recherche du rôle d'autres agents pathogènes et des facteurs de
risque environnementaux dans la dissémination de la maladie. Ceci,
permettra certainement de mieux comprendre les causes de l'émergence de
cette maladie et son impact socio-économique.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
REFERENCES BIBLIOGRAPHIQUES
ABRAHAM G., SINTAYEHU A., LIBEAU G., ALBIN A., ROGER F.,
LAEKEMARYAM Y., ABAY NEH D., AWOKE K. M., 2005. Antibody seroprevalence against
Peste des Petits Ruminants (PPR) virus in camels, cattle, goats and sheep in
Ethiopia. Prev. vet. Med., 70 : 51-57.
AWA D.N., NGAGNOU A., TEFIANG E., YAYA D., NJOYA A., 2002.
Post vaccination and colostral peste des petits ruminants antibody dynamics in
research flocks of north Cameroon. Prev. Vet. Med., 55 : 267-271.
BOURDIN P., LAURENT-VAUTIER A., 1967. Note sur la structure du
virus de la peste des petits ruminants. Rev. Elev. Méd. Vét. Pays
trop., 20: 383-386.
COUACY-HYMANN E., ROGER F., HUARD C., GUILLOU J. P., LIBEAU
G., DIALLO A., 2002. Rapid and sensitive detection of peste des petits
ruminants virus by a Polymerase Chain Reaction assay. J. Virol. Meth., 100 :
17-25.
Direction de la Statistique et des Comptes Nationaux, 2001.
Comptes de la nation
DOUMA A., SANI G., 1997. Politique de développement de
l'élevage, conservation et amélioration des ressources
génétiques animales au Niger. Actes du symposium tenu à
Ouagadougou du 1er au 5 décembre 1997

FAO, 2000. Reconnaître la peste des petits ruminants
.Manuel de terrain. 28p GEERTS S., 2006. Méthodes immunoenzymatiques
ELISA.
GAGARA H. Mariama
81
GIBBS E. P. J., TAYLOR W. P., LAWMAN M. J.P., BRYANT J., 1979.
Classification of peste des petits ruminants virus as the fourth member of the
genus Morbillivirus. Intervirology, 11 : 268-274.
IAEA, 1994. Recommended procedures for diseases and
serological surveillance as part of the Global Rinderpest Eradication Program
(GREP) IAEATECDOC- 747
IBRAHIM A. T., 1975. Contribution à l'étude de
l'élevage ovin au Niger. Etat actuel et proposition
d'amélioration. Thèse de doctorat de l'EISMV de Dakar
IGN Niger, 2008
INRAN, 1996. La recherche sur l'élevage et le
développement au Niger. Document cadre. 33 p.
KHAN H. A., SIDDIQUE M., ARSHAD M. J., KHAN Q. M., REHMAN S.
U., 2007. Séroprévalence de la peste des petits ruminants chez
les ovins et les caprins du Punjab province du Pakistan. Pakistan Vet. J., 27 :
109-112
LEFEVRE P. C., 1984. Réflexion sur les problèmes
posés par la pathologie des petits ruminants de l'Afrique
intertropicale. Etudes de synthèses de l'IEMVT. Maisons-Alford :
CIRAD-IEMVT, 15 p.
LEFEVRE P. C., 1987. Peste des petits ruminants et infection
bovipestique des ovins et des caprins. Etudes et synthèses de l'IEMVT.
Maisons-Alford : CIRAD-IEMVT, 99 p.
LEFEVRE P. C., 1991. Une maladie en pleine expansion: la peste
des petits ruminants. Revue mondiale de zootechnie, 66 : 55-58.
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
MDA, MRA, 2004-2005. Recensement Général de
l'Agriculture et du Cheptel (RGAC)
Ministère de l'Economie et des Finances, 2001. RGP/H
Niger. Rapport d'analyse. 11 p.
Ministère des Affaires Religieuses, 2007
MRA (CCN/GRGAD) République du Niger, 2003. Etat des
ressources génétiques animales dans le monde. Rapport national.
104 p.
MRA (Direction de la Production Animale/PF),
2005-2006.Campagne pastorale dans les régions de Maradi,
Tillabéry, Tahoua, Diffa et Zinder. Rapport de mission. 10 p.
OZKULA A., AKCA Y., ALKAN F., BARRETT T., KARAOGLU T., DAGALP
S. B., ANDERSON J., YESILBAG K., COKCLISTAN C., GENCAY A., BURGU I., 2002.
Prevalence, distribution and hoste range of peste des petits ruminants virus in
Turkey. Emmerg. Infect. Dis., 8 : 708-712.
PRAKASH K., 2007. Prévalence du PPRV dans la peste des
petits ruminants du Gujarat et sa caractérisation par la RT-PCR.
Thèse (Masters)
ROBINET A. H., 1971. La chèvre rousse de Maradi et
l'élevage caprin au Niger. Actes de la IIè conférence
internationale sur l'élevage caprin. Tours, France. 19 p.

SAADOU M., 1990. La végétation des milieux
drainés à l'est du fleuve Niger. Thèse d'Etat
présentée à la Faculté des Sciences de
l'université de Niamey
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
GAGARA H. Mariama
83
SANGARE O., GUITIAN J., SAMAKE K., KAMISSOKO B., NIANG M.,
LIBEAU G.,
DIALLO A., ROGER F., 2007. Serologycal survery of peste des
petits
ruminants in north west Mali. Revue Elev. Med. Vét. Pays
trop., 49 : 273- 277.
SOW A., OUATTARA L., COMPAORE Z., DOULKOM B. R., PARE M., PODA
G., NYAMBRE J., 2008. Prévalence sérologique de la peste des
petits ruminants dans la province de Soum au nord du Burkina Faso. Revue Elev.
Méd. Vét. Pays trop., 61 : 5-9.
TAYLOR W. P., AL BUSAIDY S., BARRETT T., 1990. The
epidemiology of peste des petits ruminants in the Sultanate of Oman. Vet.
Microbiol., 22: 341- 352.
TOUNKARA K., TRAORE A., SIDIBE S., SAMAKE K., DIALLO B. O.,
DIALLO A., 1996. Epidémiologie de la peste des petits ruminants (PPR) et
de la peste bovine au Mali: enquêtes sérologiques. Revue Elev.
Med. Vet. Pays trop., 49 : 273-271.
ZAKARA O., 1985. Les petits ruminants en République du
Niger. Conférence sur les petits ruminants dans l'agriculture africaine.
30 septembre au 4 octobre 1985
Sites webs consultés
http://fr.wikipedia.org/réactionenchaîneparpolymérase
Prévalence de la peste des petits ruminants au Niger :
enquête sérologique dans les régions de Niamey, Tahoua et
Tillabéry
2008
ANNEXES
Annexe 1 : FICHE D'ENQUETE
Identification de l'élevage et des enquêteurs
Date :
Nom du propriétaire :
Localité :
Nom des enquêteurs :
Caractéristiques de l'élevage :
Type d'élevage
11 Extensif 11 Semi intensif 11 Intensif
Type de logement (prendre une photo si possible)
11 Traditionnel 11 Amélioré 11 Autres
(préciser)
Matériau utilisé :
Effectifs
Effectif
Observations
GAGARA H. Mariama
84
Adultes mâles
|
|
|
Adultes femelles
|
|
Jeunes
|
|
Total
|
Moyenne
annuelle
|
|
En 2007
|
En 2008
|
|
Naissances
|
|
|
|
|
Mortalité
|
|
|
|
|
Vente
|
|
|
|
|
Autoconsommation
|
|
|
|
|
Autres (dons...)
|
|
|
|
Mouvements du troupeau
Hygiène et soins
Habitat et matériel
Le logement est - il bien entretenu ? Oui 11 Non 11
Si oui, fréquence du nettoyage
Le matériel est - il bien entretenu ? Oui 11 Non 11
Si oui fréquence du nettoyage
Santé animale
Vaccination contre la PPR dans le passé ? Oui 11 Non 11
Produits utilisés ?
Symptômes observés
sur les petits ruminants par les éleveurs :
présentement
Dans le passé
jamais
En permanence

Toux
Diarrhée
|
Mortalité des adultes
|
|
|
|
|
|
Mortalité des jeunes
|
|
|
|
|
|
Ecoulement nasal
|
|
|
|
|
|
Ecoulement oculaire
|
|
|
|
|
|
Salivation
|
|
|
|
|
GAGARA H. Mariama
86
Sollicitez- vous les services d'un agent de santé ? Oui 11
Non 11
Quels sont les produits souvent utilisés ?
Alimentation
Zero grazing ? Oui 11 Non 11
Composition ?
Pâturage ? Oui 11 Non 11
Composition ?
Autres ?

Point d'abreuvement

Privé ? Oui 11 Non 11
Commun ? Oui 11 Non 11
Autres ?
Système de production
Libre ? Oui 11 Non 11
Contrôlé ? Oui 11 Non 11

008
Annexe 2
.
88
| 


