|

Synthèse de nouveaux polyesters aliphatiques par
polymérisation de lactones
Fonctionnalisées par catalyse
organométallique
Jean-Claude TOMANI et Hamad ELKAROUS
Centre d'Etude et de Recherche sur les Macromolécules
Monsieur P. Lecomte
Laboratoire de Chimie Macromoléculaire et de Catalyse
Organique
Monsieur A. Demonceau
Sous la tutelle de Raphaël RIVA et
Yannick BORGUET
1er Master

Année académique 2009-2010
Sommaire
1. Introduction 2
2. Synthèse des monomères 4
2.1 Synthèse de 2-Bromocyclohexanone 4
2.2 Synthése de l'a-bromo-e-caprolactone 5
3. Synthèse du copolymère 6
3.1 Synthèse du copolymère statistique, le
poly a-Bromo-e-caprolactone-e-caprolactone 6
3.2 Synthése de l'oléfine, le benzoate de
3-butényle 8
4. Fonctionnalisation par ATRA 8
4.1 Fonctionnalisation de
l'a-bromocyclohexanone 9
4.2 Fonctionnalisation du copolymère par ATRA
9
4.3 Fonctionnalisation du copolymère par ATRA sous la
catalyse de cuivre 12
5. Conclusion 12
6. Remerciements 13
7. Références bibliographiques 13
1. Introduction
Un polyester est un polymère dont le squelette
macromoléculaire est constitué de motifs répétitifs
contenant la fonction chimique ester.
De nos jours, une attention toute particulière est
portée aux polymères aux propriétés
biodégradables et biocompatibles [1,2]. Ceux-ci sont soit issus du
milieu naturel, soit d'origine pétrochimique. Particulièrement,
les polyesters aliphatiques tels que la poly-åcaprolactone (PCL) et les
polylactides (PLA) occupent une place remarquable suite à leur possible
dégradation totale en molécules de faible masse molaire sous
l'action de stimuli biologique ou physico-chimique; en CH4, CO2, H2O et
biomasse [2]. En effet, du fait qu'ils sont biodégradables,
biorésorbables et perméables à beaucoup de
médicaments, ils sont très utilisés en industries
pharmaceutiques et en différentes formulations galéniques [3].
Cependant, le domaine d'application de ces thermoplastiques est limité
par de basses températures de fusion (60 pour la PCL et 50 pour PLA).
Plusieurs stratégies sont mises en oeuvre pour palier
à ces problèmes de température de fusion et pour
étendre leur gamme de propriétés afin d'élargir
leur champ d'application. On peut citer la modification chimique ainsi que
l'architecture macromoléculaire mais la copolymérisation reste la
plus générale. En effet, le changement de structure et de teneur
ainsi que la distribution des comonomères conduisent à une
variété de nouveaux matériaux [4].
Pour obtenir un polymère porteur d'une fonction
chimique désirée, on peut soit fonctionnaliser des
monomères et ensuite les (co)polymériser ou soit procéder
d'abord à la polymérisation et fonctionnaliser le polymère
lors d'une seconde étape. Pour aboutir au copolymère
désiré, plusieurs méthodes sont proposées. On peut
recourir soit à la cycloaddition 1,3-dipolaire de Huisgen sous la
catalyse de cuivre (I) (« Chimie Click »), soit à l'addition
radicalaire par transfert d'atome (ATRA). Cependant, deux problèmes
majeurs sont liés à la réaction dite « Click ».
Il s'agit de la formation des intermédiaires portant une fonction
azoture qui est potentiellement explosif d'une part et de la présence
des résidus catalytiques (Cu+) qui restreindraient leur
utilisation d'autre part.
Quant à la réaction d'ATRA, elle est avantageuse
car elle ne nécessite pas la préparation d'intermédiaires
azotures. En effet, la réaction d'ATRA est une réaction de
Kharasch catalysée par des complexes métalliques (schéma
1).
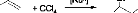
Schéma 1 : Réaction modèle d'ATRA
Récemment, quelques travaux en rapport avec l'ATRA ont
été reportés. S. Lenoir et al. [2] ont reporté en
2004 les résultats de l'ATRA sur une
poly(a-chloro-å-caprolactone-co-åcaprolactone)
(poly(aClåCL-co-åCL)) par catalyse au cuivre à 60°C
dans du DMF. Cependant, la quantité de catalyseur extrêmement
élevée ainsi que la présence de DMF reste un handicape
pour l'applicabilité de ces polymères. P. Jonlet, en 2009, dans
la perspective de palier à ces problèmes, a étudié
la fonctionnalisation de la poly(aClåCL-co-åCL) par ATRA sous la
catalyse de complexes de ruthénium mais le taux de fonctionnalisation
reste faible.
Ainsi, le but de notre travail était de préparer
des polyesters fonctionnels par ATRA, grace à l'intermédiaire
ct-bromo-å-caprolactone (ct-Br-å-CL), en présence de faible
quantité de catalyseur à basse température et en des temps
de réaction relativement courts. En effet, la liaison C-Br étant
plus labile que la liaison C-Cl, l'a-Br-å-CL est plus active que
a-Cl-å-CL, ce qui augmenterait le taux de fonctionnalisation par ATRA.
Au cours de notre stage, nous avons d'abord
synthétisé des monomères et réalisé leur
polymérisation avant de procéder à la fonctionnalisation
proprement dite. Typiquement, la cyclohexanone a été
bromée pour donner la 2-bromo-cyclohexanone qui ensuite a subi une
oxydation de Baeyer-Villiger pour donner l'a-Br-å-CL. Ensuite, nous avons
procédé à la copolymérisation de l'a-Br-å-CL
avec l'åCL. Le test de la réaction d'ATRA a été fait
sur la 2- bromocyclohexanone et sur le copolymère.
Pour le test sur la 2-bromocyclohexanone, 2 types de complexes
au ruthénium (Cata A et cata B), ont été utilisés
alors que sur le copolymère, seul le complexe bimétallique (cata
B) a été utilisé.

Cata A :
RuCl2(p-cymène)PPh3 Cata B :
Complexe de Severin [6]
2. Synthèse des monomères
2.1 Synthèse de 2-Bromocyclohexanone
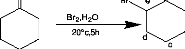

Schéma 2 : Synthèse de Bromocyclohexanone
La 2-bromocyclohexanone a été
synthétisée à partir de cyclohexanone comme décrit
par G. Wang et al [5]. Dans un ballon à deux tubulures de 250ml, muni
d'un thermomètre,
O
nous avons mélangé 15g de cyclohexanone avec
100ml d'eau distillée. Ensuite, 7,9 ml de
C
Br e
brome ont été ajoutés, goutte à
goutte pendant 4h. Puisque la réaction est exothermique, un
Br2,H2O C
bain de glace est utilisé pour rabaisser la
température de la réaction entre 20°C et 30°C.
Après
c,5 d
addition du brome, la solution est agitée
jusqu'à décoloration complète (pendant 1h). La phase
organique est ensuite séparée de la phase aqueuse et
séchée sur sulfate de magnésium anhydre. Le solvant est
évaporé sous pression réduite et le résidu est
distillé sous vide (5 10- 2mm de Hg/40°C). On
récupère 18,57g (68,77%) d'une huile incolore, qui se solidifie
lorsqu'on la place en chambre froide (-20°C), qui est alors
analysée par RMN.
RMN 1H (250MHz, CDCl3): ä (ppm) = 4,4 (m, 1H,
He); 2,8 (m, 2H, Ha); 1,7-2,3 (m, 6H, Hb, Hc,
Hd).
RMN 13C (63,5 MHz; CDCl3): ä(ppm) = 169,7 (CO);
53,6 (Ce); 37,9 (Cd); 36,8 (Ca); 226,7 (Cb); 22,1
(Cc).
| 


