|
REPUBLIQUE DU BENIN
----------
MINISTERE DE L'ENSEIGNEMENT SUPERIEUR ET DE LA RECHERCHE
SCIENTIFIQUE
-------------


UNIVERSITE D'ABOMEY-CALAVI
--------------------
ECOLE POLYTECHNIQUE D'ABOMEY-CALAVI
-----------------------
DEPARTEMENT DE PRODUCTION ET SANTE ANIMALES
--------------------------
MEMOIRE
Pour l'obtention du Diplôme d'Ingénieur des
Travaux (D.I.T)
![]()
Diagnostic nécropsique et causes
bactériologiques
de mortalité des lapins (Oryctolagus
cuniculus)
élevés au sud-Bénin.

![]()
![]()
Présenté et soutenu par :
Sous la direction de :
Raoufou DJIBRIL SALIFOU Souaïbou
FAROUGOU, DVM PhD
Maître - assistant des Universités
Année académique 2006-2007
13ème Promotion


DEDICACES
ü A ALLAH, le très miséricordieux,
l'immense, le rédempteur. Tu nous as protégés et soutenus
tout au long de notre formation. Que tes bénédictions saintes
nous accompagnent pour la suite du combat. Amen !
ü A notre feu père DJIBRIL Salifou, vous nous avez
quittés sans pour autant profiter des fruits de vos efforts. Vous avez
tout sacrifié pour nous par affection et amour. Cette oeuvre est la
réalisation concrète de vos efforts. Paix et joies
éternelles
ü A notre mère Hawa née ISSAKA, trouvez en
ce travail le résultat des multiples sacrifices consentis depuis notre
naissance pour faire de nous ce que nous sommes aujourd'hui
ü A nos frères et soeurs aînés,
Abdel-Aziz, Djahara, Sourakatou, Bintou, Sanni : vous nous avez soutenus
et aidé de diverses manières. C'est notre joie à tous.
ü A nos jeunes frères et soeurs : Ce travail
est un exemple à dépasser. Courage !
ü A nos oncles et tantes : vous avez apporté
votre pierre à l'édifice par vos prières. Soyez-en
remerciés
ü A nos cousins, cousines, neveux et nièces en
témoignage de la profonde affection qui nous unit.
HOMMAGE
ü A notre Maître de mémoire, le Docteur
Souaïbou FAROUGOU, votre humilité, votre indulgence, votre sens
d'altruisme et votre loyauté constituent pour nous un exemple à
suivre. Votre assistance inconditionnelle ne nous a manqué à
aucun moment jusqu'à la rédaction de ce mémoire que vous
avez bien voulu diriger malgré vos nombreuses occupations. Nous gardons
de vous le souvenir d'un Maître dévoué à la
tâche, soucieux d'un travail bien fait et doué de qualités
scientifiques inestimables.
ü A tous les enseignants de l'EPAC en particulier ceux du
département de Production et Santé Animales. Vous avez
participé à notre formation. Veuillez trouvez en ce travail
l'oeuvre de vos divers conseils.
ü A Monsieur le Président et aux autres membres du
jury, vous avez consenti à présider et à faire partie de
notre jury de mémoire. Daignez accepter notre profonde
déférence.
VIFS REMERCIEMENTS
Au terme de la réalisation de ce mémoire, qu'il
nous soit permis d'adresser nos vifs remerciements :
ü Au Professeur Agrégé Marc T. KPODEKON
pour nous avoir ouvert les portes du Centre Cunicole de Recherche et
d'Information (Ce.Cu.R.I).
ü A Monsieur Yaou A. DJAGO pour nous avoir guidé
et conseillé lors de nos travaux.
ü A Messieurs BOKO Cyrille et DOSSA François,
personnels du Complexe Clinique Laboratoire Pharmacie
Vétérinaires pour leur assistance inconditionnelle, leur
indulgence, leur souci d'un travail bien fait. Nous vous en sommes vraiment
reconnaissants.
ü Aux éleveurs membre de l'A.Be.C en particulier
à Monsieur HOUESSINON Adolphe pour son bon sens de collaboration et son
altruisme.
ü A la famille ATINDEHOU en particulier à
ATINDEHOU Rodrigue pour les bons et mauvais moments que nous avons su
gérer ensemble et son soutien tout au long de nos travaux. Nous
garderons de toi le souvenir d'un ami sociable.
ü A la famille ISSAKA plus particulièrement
à Madame ISSAKA Mamatou. Vous n'avez ménagé aucun effort
pour notre accueil et pour le soutien moral dont vous avez fait preuve
jusqu'à l'obtention de notre baccalauréat.
ü A tous les étudiants de la 13e
promotion pour avoir étudié dans une bonne ambiance pendant
quatre ans.
SOMMAIRE
DEDICACES
i
VIFS REMERCIEMENTS
iii
LISTE DES ABREVIATIONS
vii
LISTE DES FIGURES
viii
LISTE DES TABLEAUX
ix
LISTE DES ANNEXES
x
RESUME
xi
INTRODUCTION
1
Chapitre 1 : Revue bibliographie sur le lapin, ses
maladies bactériennes avec les principales lésions
3
1- Généralité sur le lapin
domestique
4
1.1- Importance du lapin
4
1.1.1- Place du lapin dans l'alimentation de
l'homme
4
1.1.2- Importance socio-économique
4
1.2- Aperçu sur la biologie du lapin
5
1.2.1- Taxonomie du lapin
5
1.2.2 - Extérieur du corps et
morphologie
5
1.2.3 - Comportement alimentaire et alimentation du
lapin
6
1.2.3.1 - Comportement alimentaire
6
1.2.3.2- Alimentation en eau et en aliment
9
1.2.4- Habitat
9
1.2.5- La reproduction
10
1.3- Elevage du lapin
10
1.3.1- La cuniculture au Bénin
10
1.3.2- Les pathologies dominantes du lapin
11
2- Bactéries et maladies
bactériennes
13
2.1- Bactérie
13
2.1.1- Place des bactéries dans le monde
vivant.
13
2.1.2- Morphologie et organisation
13
2.1.3- Structure
15
2.1.4- Physiologie
15
2.2- Maladies bactériennes et principales
lésions
16
2.2.1- Maladies bactériennes
fréquentes du lapin
16
2.2.1.1- Entérotoxémie
16
2.2.1.2- Staphylococcie
17
2.2.1.3- Colibacillose
17
2.2.1.4- Pasteurellose (avec ou sans bordetellose
associée)
18
2.2.1.5- L'entérite colibacillaire de
sevrage
18
2.2.2- Autres maladies bactériennes du
lapin
19
Chapitre 2 : Matériel et
méthodes
20
2.1- Matériels
21
2.1.1- Matériel animal
21
2.1.2- Matériel et produits de
laboratoire
21
2.2- Méthodes
21
2.2.1- La collecte des données
21
2.2.2- Méthode d'autopsie
22
2.2.3- Méthode d'identification des
germes
23
2.2.3.1- Prélèvement
23
2.2.3.2- Isolement
23
2.2.3.3- Identification
23
2.2.4- Analyses statistiques
25
CHAPITRE 3 : Résultats et
discussion
26
3.1- Résultats
27
3.1.1- Résultats des enquêtes
épidémiologiques
27
3.1.2- Les lésions et leur fréquence
en fonction des organes
29
3.1.3- Microorganismes identifiés
31
3.1.4- Fréquence des microorganismes par
élevage
33
3.1.5- Fréquence des paramètres
étudiés en fonction de l'âge et du sexe
35
3.1.5.1- En fonction de l'âge
35
3.1.5.2- En fonction du sexe
37
3.2- Discussion
39
3.2.1- Critique de nos résultats
39
3.2.1.2- Résultats des enquêtes
épidémiologiques
39
3.2.1.2- Les principales lésions et leur
fréquence en fonction des organes
40
3.2.1.3- Relation entre la situation sanitaire des
élevages et les fréquences des microorganismes
40
3.2.1.4- Relation entre les principaux signes
recensés chez le lapin (malade ou mort) et les principaux
microorganismes identifiés.
41
3.2.1.5- Fréquence des lésions et des
microorganismes en fonction de l'âge
42
3.2.1.6- Fréquence des lésions et des
microorganismes en fonction du sexe
42
3.2.1.7- Relation entre le taux de
létalité et les microorganismes identifiés
43
CONCLUSION ET SUGGESTIONS
44
REFERENCES BIBLIOGRAPHIQUES
46
LISTE DES ABREVIATIONS
A. Be. C. : Association Béninoise
des Cuniculteurs
Ce. Cu. R. I. : Centre Cunicole de
Recherche et d'Information
PIB : Produit Intérieur Brut
% : pour cent
LISTE DES FIGURES
Figure 1 : Différentes parties du corps du
lapin:
6
Figure 2 : Schéma des différents
éléments du tube digestif du lapin
7
Figure 3 : Schéma général de
fonctionnement de la digestion chez le lapin
8
Figure 4 : Différentes formes et
regroupement des bactéries
14
Figure 5 : Structure de la cellule
bactérienne
15
LISTE DES TABLEAUX
Tableau I : Les pathologies dominantes du lapin
....................................12
Tableau II : Place des bactéries dans le monde vivant
..............................13
Tableau III : Données épidémiologiques
et cliniques sur les élevages prospectés
..........................................................................28
Tableau IV : Fréquence des lésions en fonction
des organes .....................30
Tableau V : Principaux microorganismes identifiés
dans les 150 prélèvements effectués
.........................................................32
Tableau VI : Nombre de cas d'infection par organe
...................................32
Tableau VII : Fréquence des microorganismes en
fonction des élevages ....34
Tableau VIII : Fréquence des lésions en
fonction de l'âge ........................ 36
Tableau IX : Principaux microorganismes en fonction de
l'âge ..................36
Tableau X : Fréquence des lésions en fonction
du sexe ............................38
Tableau XI : Principaux microorganismes en fonction du sexe
..................38
LISTE DES ANNEXES
Annexe 1 :
Matériel....................................................................49
Annexe 2 : Fiches d'enquête et
d'autopsie....................................50
Annexe 3 : Milieux
utilisés..........................................................52
Annexe 4 : Tests
d'identification..................................................53
Annexe 5 : Caractères biochimiques de bacilles
identifiés..............55
RESUME
La présente étude s'est déroulée
de Novembre 2006 à Mai 2007 et a porté d'une part sur une
enquête épidémiologique réalisée dans 30
élevages cunicoles du sud-Bénin et d'autre part sur la mise en
évidence des pathologies du lapin sur 75 animaux, tous âges et
sexes confondus. Les cadavres des lapins ont été
collectés dans ces élevages et autopsiés pour la mise en
évidence des lésions et pour les analyses
bactériologiques visant à déterminer les causes de la
mortalité des lapins.
A l'issue de l'enquête, il s'est
révélé que les signes souvent observés chez
les lapins malades sont :
v la diarrhée et le ballonnement : ces signes ont
été très fréquents et sont enregistrés
dans 20 élevages sur les 30 prospectés.
v l'inappétence et l'agitation ont été
notées respectivement dans 9 et 8 élevages.
Les autres signes tels que la gale, les convulsions et la
prostration ont eu une fréquence négligeable.
Le taux de létalité varie entre 44 et 93% avec
une moyenne de 69%. Les principales lésions présentes chez le
lapin mort de maladies étaient la congestion du poumon, du foie, de
l'intestin et de la trachée ; la
dégénérescence du foie ; l'accumulation de gaz dans
le caecum ; un contenu diarrhéique du caecum et de
l'intestin ; un écoulement sanguinolent au niveau des naseaux.
Les analyses bactériologiques ont permis d'identifier
les microorganismes suivants : Escherichia
coli (50% des bactéries identifiées) ;
Clostridium spp (8%) ; Enterobacter
spp (7%) ; Shigella dysenteriae (5%) ;
Staphylococcus spp (5%) ; Pasteurella multocida
(3%) ; Citrobacter spp (3%) ; Proteus
mirabilis (3%) ; Edwarsiella tarda (3%) ;
Klebsiella pneumoniae (3%) ; Pasteurella haemolitica
(2%) ; Pseudomonas spp (2%) ; Bacillus firmus
(2%) ; Yersinia spp (1%) et Pasteurella pneumotropica
(1%).
Il est donc à noter que la bactérie
fréquente dans nos élevages cunicoles et qui pourrait
entraîner la mortalité des lapins est Escherichia coli.
Alors que les lésions d'organes et les
microorganismes identifiés ne varient pas significativement en fonction
du sexe, ils le sont en fonction de l'âge. Le niveau d'infection est en
rapport avec la situation sanitaire des élevages.
Mot clés : maladies
bactériennes, bactérie, lésion, lapin, Bénin.
INTRODUCTION
La cuniculture au Bénin connaît un
développement sans cesse croissant. En effet, en 1988, le Bénin
connaissait 450 élevages répartis dans tout le pays (KPODEKON,
1988a et b). Avec la création du Centre Cunicole de Recherche et
d'Information (Ce.Cu.R.I) en 1988, la cuniculture béninoise a connu une
importante vulgarisation. Ainsi, de 2002 à 2005, l'effectif des lapins
est passé de 5085 à 8727 (KENOUKON, 2005).
Aussi, la viande du lapin est-elle entrée de plus en
plus dans les habitudes alimentaires des béninois. Des études ont
montré que 64% de la population ont consommé au moins une fois la
viande du lapin et la quasi-totalité (95%) l'a appréciée
(KPODEKON ET TOMAGNIMENA, 1992). La viande du lapin occupe donc une place
importante dans l'alimentation des béninois, mais les cuniculteurs
n'arrivent pas à satisfaire la demande à cause des diverses
pathologies qui engendrent un énorme manque à gagner. Parmi ces
pathologies, les maladies bactériennes occupent une place très
importante dans les pays de l'Afrique de l'Ouest dont le Bénin (DJAGO et
KPODEKON, 2000). Malgré de nombreux travaux réalisés aussi
bien dans le domaine de l'alimentation (THOTO, 2006) que dans la pathologie
(LEBAS et al., 1996 ; DJAGO et KPODEKON, 2000), les
élevages cunicoles connaissent encore de nos jours un taux de
mortalité élevé.
Il s'avère donc impérieux d'associer au
diagnostic clinique depuis longtemps pratiqué par les cuniculteurs et
les agents d'élevage, un diagnostic nécropsique et de laboratoire
afin de mettre en évidence les pathologies du lapin et d'identifier les
principaux agents responsables de la mortalité de cet animal pour mettre
en place une stratégie efficace de lutte.
C'est dans l'optique d'apporter notre contribution à
la résolution de cet important problème que nous avons
jugé opportun de porter notre travail de fin d'études sur le
thème intitulé « Diagnostic nécropsique et
causes bactériologiques de mortalité des lapins (Oryctolagus
cuniculus) élevés au sud - Bénin »
Cette étude envisage :
ü de faire un état de lieux des élevages
cunicoles ;
ü de répertorier les principales lésions
chez les lapins morts de maladies ;
ü d'identifier les principales bactéries
responsables de la mortalité chez le lapin ;
ü de noter la fréquence des lésions et les
microorganismes identifiés en fonction de l'âge et du sexe.
Elle sera présentée en trois
chapitres :
- le premier sera consacré à une étude
bibliographique permettant de faire connaissance avec le lapin et les
différents paramètres étudiés ;
- le deuxième présentera le matériel et
les méthodes utilisés.
- le troisième abordera les résultats et la
discussion.
CHAPITRE 1 : REVUE BIBLIOGRAPHIE SUR LE LAPIN, SES
MALADIES BACTÉRIENNES AVEC LES PRINCIPALES
LÉSIONS
1- Généralité sur le lapin
domestique
1.1- Importance du lapin
1.1.1- Place du lapin dans l'alimentation de l'homme
Comparée à celle des autres espèces
animales, la viande du lapin est plus riche en protéines, en certaines
vitamines et en sel minéraux. Elle est par contre plus pauvre en graisse
(LEBAS et al., 1996). Selon DJAGO et KPODEKON (2000), la
viande du lapin présente des qualités diététiques
indiscutables et est souvent recommandée par les médecins.
Elle se situe parmi les viandes recherchées (LEBAS
et al., 1996). Au Bénin 64% de la population ont
consommé au moins une fois la viande du lapin et la
quasi-totalité (95%) des consommateurs l'a appréciée
(KPODEKON et TOMAGNIMENA, 1992).
1.1.2- Importance socio-économique
Les lapins sont destinés soit à
l'autoconsommation, soit à la commercialisation. Ces deux
phénomènes ont une importance comparable, mais l'autoconsommation
domine dans les pays en voie de développement. Il faut noter que la
participation de la cuniculture traditionnelle à l'économie de
certains pays est loin d'être négligeable comme l'ont
montré les relations entre valeur de la production cunicole et le PIB
(COLIN et LEBAS, 1995).
1.2- Aperçu sur la biologie du lapin
1.2.1- Taxonomie du lapin
La position taxonomique du lapin (Oryctolagus
cuniculus) est la suivante (GRASSE, 1949 ; LEBAS et al.,
1984) :
- Classe des mammifères
- Super Ordre des Glires
- Ordre des Lagomorphes
- Famille des Léporides (lièvre et lapin)
- Sous-famille des Leporinae
- Genre Oryctolagus
- Espèce : Oryctolagus cuniculus
1.2.2 - Extérieur du
corps et morphologie
Les principales parties du corps du lapin
sont identifiées sur la figure 1. Pour la majorité des races,
à l'exception des nains, l'allure générale du corps est
différente selon le sexe. Une tête large et forte, un thorax
développé, des membres relativement épais et une
musculature bien extériorisée sont généralement
caractéristiques du mâle. Les femelles présentent, toutes
proportions gardées, plus de finesse générale avec une
tête plus étroite, un corps paraissant plus allongé et une
ossature un peu plus légère. Seul l'arrière-train est plus
développé avec un bassin large.
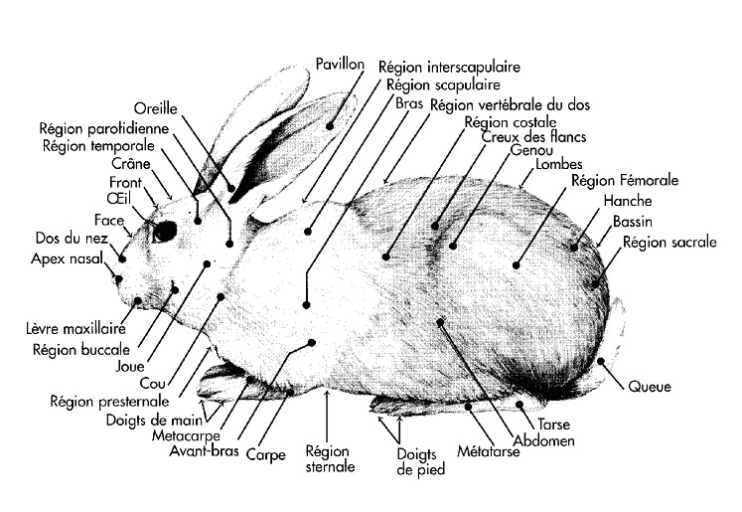
![]()
Figure 1 :
Différentes parties du corps du lapin:
Source : BARONE et al.
(1973)
1.2.3 - Comportement
alimentaire et alimentation du lapin
Le lapin est un rongeur monogastrique qui présente des
particularités anatomophysiologiques (LEBAS et al., 1996). Par
opposition aux autres monogastriques, le lapin est caecotrophe, bon
transformateur tirant le maximum de profit de la cellulose.
1.2.3.1 - Comportement
alimentaire
Le rythme des tétées est imposé par la
mère aux lapereaux nouveau-nés, mais à partir de la
troisième semaine, on note une modification extraordinaire du
comportement. Le lapereau passe d'une seule tétée par jour
à une multitude de repas solides et liquides plus ou moins
alternés et répartis régulièrement le long de la
journée: 25 à 30 repas solides ou liquides par 24 heures (LEBAS
et al., 1996), soit plus de 3 heures de repas dont les 2/3 sont
nocturnes. L'évolution des quantités de nourriture et d'eau
ingérées est fonction de la nature des aliments
présentés aux lapins, du type d'animal, de son âge et de
son stade de production (LEBAS et al., 1996).
Chez un lapin adulte (4-4,5 kg) ou subadulte (2,5 à 3
kg), le tube digestif a une longueur totale d'environ 4,5 à 5
mètres. L'organisation des segments digestifs et leurs
caractéristiques principales sont décrites sur la figure 2.
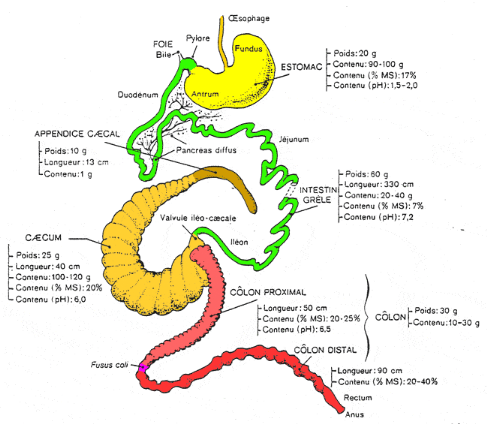
![]()
Figure 2 :
Schéma des différents éléments du tube digestif du
lapin
Source : LEBAS et al.
(1996)
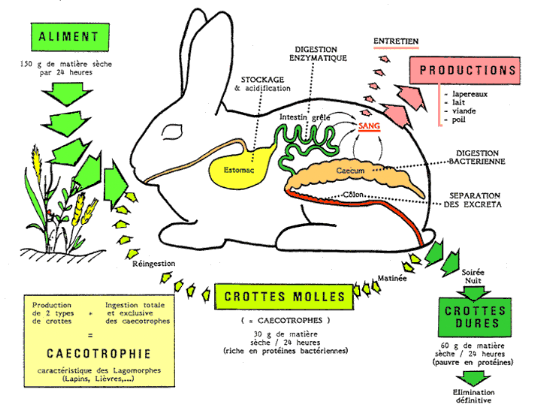
![]()
Figure 3 :
Schéma général de fonctionnement de la digestion chez le
lapin
Source : LEBAS et al.
(1996)
Lorsque le lapin se trouve face à plusieurs aliments,
il choisit en fonction de critère parfois difficilement
prévisible. La répartition et la prise de repas n'est pas
homogène au cours des 24 heures. La part de l'alimentation quotidienne
consommée chaque heure en période d'obscurité est
nettement plus importante que la part correspondante ingérée en
période d'éclairement, tant pour l'aliment solide que l'eau de
boisson. Au fur et à mesure que les lapins vieillissent, le
caractère nocturne du comportement alimentaire s'accentue (LEBAS
et al., 1996).
1.2.3.2- Alimentation en eau et en aliment
Les besoins alimentaires des lapins
dépendent de leur âge et de leurs stades physiologiques.
a) L'eau
Le lapin boit énormément surtout s'il est
alimenté exclusivement avec des aliments de types granulé et
farineux.
Il a été constaté que le lapin boit un
volume d'eau correspondant au double de celui de la ration sec consommée
(DJAGO et KPODEKON, 2000).
b) L'aliment
En élevage semi intensif, il se compose de fourrage et
d'un complément alimentaire au moment important de la production. Le
complément peut être de deux ordres :
- les produits simples (drèche de brasserie, grain de
maïs etc....) ;
- les provendes
En élevage, intensif l'aliment complet (provende) est
servi aux lapins avec un peu de fourrage (HULET, 2003).
1.2.4- Habitat
A l'état sauvage les lapins creusent des terriers
qui comportent des aires de repos où ils se réfugient à la
moindre alerte et où ils vivent en
« sociétés ». La femelle, avant de mettre
bas, creuse un terrier particulier dénommé
« rabouillère » dans lequel elle dépose ses
petits et vient leur donner à téter.
Pour les lapins domestiques, ils convient de prévoir
un habitat de sorte que les lapins soient hors ses agressions
extérieures telles que le bruit, la poussière, les
prédateurs, une température forte. Le lapin étant sensible
aux agents microbiens, une bonne hygiène s'avère indispensable en
cuniculture (LEBAS et al., 1996).
1.2.5- La reproduction
a) Le mâle
Les lapins mâles atteignent leur maturité
sexuelle autour de 5 mois ½ voire 6 mois avec un poids minimum de 2,5 kg
(DJAGO et KPODEKON, 2000). L'appareil génital mâle
comprend :
· les testicules au nombre de deux et qui peuvent monter
et descendre dans la cavité abdominale
· le canal épididymaire qui précède
le canal déférent. Le pénis est fin et long ; il
n'est visible qu'au moment de l'érection (BOUCHER et NOUAILLE, 2002).
b) La femelle
Les jeunes femelles atteignent leur maturité sexuelle
autour de 5 mois et ont un poids minimum de 2,2 kg si le poids des femelles
adultes est de 3 à 5 kg. Contrairement aux autres espèces, la
lapine est un animal à ovulation provoquée, car celle-ci a lieu
à la suite de l'accouplement. En outre, l'ovulation chez la lapine est
multiple ; ce qui peut donner des portées ayant jusqu'à 10
à 12 lapereaux à la naissance voire plus (DJAGO et KPODEKON,
2000). L'appareil génital femelle comprend deux ovaires, deux pavillons
et deux cornes utérines munies d'un col chacune. Le vagin
précède la vulve qui change de couleur en fonction des phases de
réceptivité de la lapine (BOUCHER et NOUAILLE, 2002).
1.3- Elevage du lapin
1.3.1- La cuniculture au Bénin
La cuniculture au Bénin connaît un
développement sans cesse croissant. En effet, en 1988, le Bénin
connaissait 450 élevages répartis dans tout le pays (KPODEKON
1988 a et b). Il est à noter qu'avec la création du Centre
Cunicole de Recherche et d'Information (Ce.Cu.R.I) la cuniculture au
Bénin a connu une importante vulgarisation. Ainsi chaque éleveur
de l'A.Be.C a un effectif compris entre 10 et 50 lapines mères. Ce qui a
fait qu'en 2005 la production annuelle de carcasse de lapin est
évaluée à environ 400 tonnes (KENOUKON, 2005).
1.3.2- Les pathologies dominantes du lapin
De plus en plus la viande du lapin entre dans les habitudes
alimentaires des béninois mais la croissance de la cuniculture est
handicapée par diverses pathologies (tableau I).
Tableau
I : Les pathologies dominantes du lapin
|
PATHOLOGIES
|
ETIOLOGIE
|
SYMPTOMES
|
|
Maladies digestives
|
Coccidiose
|
Eimeria
|
Diarrhée, perte de poids, gros ventre chez les
lapereaux, baisse de consommation d'eau et d'aliment
|
|
Entérotoxémie
|
Clostridium sp ou colibacilles
|
Mort brutal en quelques heures avec production de mucus, anus
à peine souillée, l'animal ballonne très rapidement
|
|
colibacillose
|
Colibacilles
(Eschenichia coli)
|
Mort des reproducteurs avec diarrhée
Mort des lapereaux au nid avec diarrhée
Mort des lapins à l'engraissement avec diarrhée
|
|
Maladies respiratoires
|
Pasteurellose (avec ou sans bordetellose associée)
|
Pasteurella multocida avec ou sans Bordetella
bronchiseptica
|
Inflammation suppurative, abcès mammaire ou
cutanée, métrite. En cas d'atteinte respiratoire, la respiration
devient difficile, bruyante, rauque. L'état général de
l'animal se dégrade.
|
|
Maladies cutanées
|
Gale des oreilles
|
Psoroptes cuniculi
|
L'animal secoue la tête et se gratte parfois.
Présence de croûte dans l'oreille
|
|
Gale du corps et de la tête
|
Sarcoptes scabiei ou Notoedres cati
|
Agitation, grattage entraînant dépilation et
apparition de croûtes sur le corps
|
|
Maladies liées à la
reproduction
|
Abcès et mammite
|
- pasteurelles
- staphylocoques
- streptocoques
|
Abcès
Les abcès d'origines Pasteurella sont
crémeux et souvent localisés sous le cou et la maxillaire.
En cas de staphylococcies, on a un pus blanchâtre et
croûteux au niveau des articulations, sur le corps, et sur les yeux des
jeunes lapereaux.
Mammite
Tuméfaction, chaleur, rougeur, agalactie
|
|
Frigidité et stérilité
|
Mauvaise alimentation
|
Refus d'accouplement
|
|
Mortalité au nid
|
Staphylococcus aureus
|
Taux de mortalité anormalement élevé et
mort en grande quantité des petits
|
Source : KPODEKON et DJAGO,
2000 ; BOUCHEUR et NOUAILLE, 2002
2- Bactéries et maladies
bactériennes
2.1- Bactérie
2.1.1- Place des
bactéries dans le monde vivant.
En 1886 le biologiste zoologiste Allemand Haeckel (1834 1919)
a établi grâce à la perfection du microscope qu'il existe
dans le monde des êtres vivants un troisième règne celui
des protistes regroupant algues protozoaires, champignons et bactéries.
Le tableau II présente la place des bactéries dans le groupe des
protistes.
Tableau II : Place des
bactéries dans le monde vivant
|
Organismes pluricellulaires
|
Organisme unicellulaire (protistes)
|
|
- Métaphytes (règne végétal)
- métazoaires (règne animal)
|
Supérieurs (Eucaryotes)
- Protophytes
- Protozoaires
|
Inférieurs (procaryotes)
- Algues bleues
- Bactéries
|
Source : Pilet et al.,
1981
2.1.2- Morphologie et
organisation
Les bactéries sont des procaryotes. Elles tirent leur
nom du grec bactérion qui signifie bâtonnet. La bactérie
est le plus petit organisme connu, douée de métabolisme et
capable de croître. Quatre formes sont habituellement connues chez les
bactéries à savoir.
· la forme sphérique
· la forme allongée ou bâtonnet ou bacille
· la forme spiralée
· la forme spiralée allongée.
Les bactéries en forme sphérique sont
appelée cocci (cocos= grains). Parmi les cocci, on rencontre des
bactéries qui se regroupent par deux, c'est les diplocoques ; par
trois, les sarcina ; par quatre, les tétracoques. Dans la nature,
il existe des bactéries qui vivent seules (gonocoques,
pneumocoques) ; il y en a qui se rassemblent en chaîne : ce
sont les streptocoques ; en amas : les staphylocoques. Les
bactéries en bâtonnet ont leurs bouts soit effilés sont
arrondis. On rencontre ses bactéries sous d'autres formes telles que les
coccobacilles et les leptospires (YAOU, 2007).
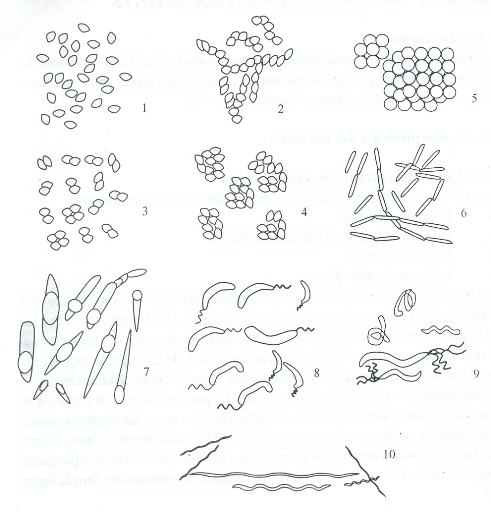
1- Microccoques 6- bâtonnets
ne formant pas de spores
2- Streptocoques 7- bâtonnets
formant de spores
3- Diplocoques 8- les vibrions
4- Staphylocoques 9- spiralés
5- Sarcina 10-
spiralés allongés
Figure 4 :
Différentes formes et regroupement des bactéries
Source : YAOU (2007)
2.1.3- Structure
La structure des bactéries est rudimentaire. Elles
sont limitées par une paroi rigide qui détermine leur forme. La
structure et la composition chimique de la paroi définissent deux
types : chez les bactéries Gram positif, la paroi est riche en
sucre aminés et en protéines et comprend seulement une couche
épaisse alors que chez les Gram négatif, elle est plus complexe
et contient en outre des lipides. Le cytoplasme est limité par une
membrane cytoplasmique qui joue le rôle fonctionnel des mitochondries. Il
contient des ribosomes, des inclusions (volutines, glycogène...) et
l'appareil nucléaire réduit à un seul chromosome
circulaire. La cellule bactérienne est de petite taille de l'ordre du
micron (GUIRAUD et GALZY, 1980).
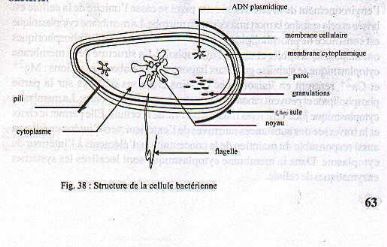
Capsule
Figure 5 : Structure
de la cellule bactérienne
Source : YAOU,
2007
2.1.4- Physiologie
Les bactéries présentent une diversité de
caractères physiologiques. Les germes intervenant dans le cadre de la
microbiologie alimentaire sont des hétérotrophes. Le comportement
par rapport aux substrats et aux conditions physiologiques est variable en
fonction des germes étudiés. Une caractéristique
importante des bactéries est leur grande vitesse de
prolifération.
Le pouvoir pathogène des bactéries peut
dépendre de plusieurs facteurs. Il existe des espèces :
- à pouvoir infectieux qui agissent par envahissent de
l'hôte (infection) ;
- à pouvoir toxinogène qui libèrent des
toxines dans l'aliment (intoxination) ;
- à caractères mixtes pouvant provoquer des toxi
- infections ;
- agissant par la transformation du substrat qu'elles rendent
toxique provoquant ainsi des intoxications.
Les bactéries saprophytes ont souvent un pouvoir
dégradant vis à vis des aliments. Les bactéries utiles
sont essentiellement les agents de fermentation lactique, acétique,
propionique (GUIRAUD et GALZY, 1980).
2.2- Maladies
bactériennes et principales lésions
2.2.1- Maladies
bactériennes fréquentes du lapin
Parmi les pathologies dominantes du lapin, les maladies
bactériennes occupent une place importante et entravent la cuniculture
béninoise. Au nombre de ces maladies, cinq seront décrites
à travers leurs étiologies et leurs principales lésions
(BOUCHER et NOUAILLE, 2002 ; DJAGO et KPODEKON, 2000).
2.2.1.1-
Entérotoxémie
a) Etiologie
La maladie est causée soit par Clostridium
perfringins de type E avec entérotoxémie vraie et production
de toxine (cas rare) soit par les colibacilles ou par Clostridium
perfringens du type (A) qui n'est pas présumé pathogène,
mais en provoquant un dérèglement cæcal, il conduit
à une anarchie dans la flore avec fermentation et auto-intoxication (cas
fréquent).
b) Lésions
On note un contenu cæcal liquide, malodorant avec
présence de gaz. La paroi peut être hémorragique. Le foie
est dégénéré, et les reins congestionnés.
2.2.1.2- Staphylococcie
a) Etiologie
La maladie est due à la multiplication de
Staphylococcus aureus qui est une bactérie GRAM positif.
b) Lésions
Cette bactérie provoque des lésions
suppuratives chez l'adulte, chez le jeune lapereau couramment appelées "
boutons " qui couvrent le corps du jeune animal. Il peut y avoir
mortalités brutales par septicémie.
2.2.1.3- Colibacillose
a) Etiologie
Les entérites bactériennes d'origine
colibacillaire sont dues à des variétés
particulières de colibacilles : Escherichia coli.
b) Lésions
A l'autopsie, le contenu intestinal et cæcal est liquide
avec ou sans hémorragie. Il y a congestion
généralisée de l'intestin et du caecum avec trace
hémorragique en coup de pinceau. Au niveau des lapereaux sous
mère, on note des points de nécrose hépatiques
marqués par la présence de petits points blancs sur le parenchyme
hépatique.
2.2.1.4- Pasteurellose (avec
ou sans bordetellose associée)
a) Etiologie
La maladie est due à Pasteurella multocida,
bactérie Gram négatif qui se localise dans les voies
respiratoires, la peau, les mamelles, l'appareil reproducteur. En cas
d'association de la bordeteullose il y a présence de Bordetella
bronchiseptica qui serait considéré comme germe favorisant,
car elle ne déclencherait pas des affections respiratoires mais se
localise au niveau du sinus et parfois dans les poumons.
b) Lésions
A l'autopsie on note des lésions
variées :
- Sinus : dépôt purulent
- Poumon : foyer d'hépatisation
avec un poumon rouge foncé, de consistance modifiée ;
abcès pulmonaire ; pleurésie.
- Mamelle : abcès
fréquente
- Appareil
génital : présence de pus à
l'ouverture
2.2.1.5- L'entérite
colibacillaire de sevrage
a) Etiologie
La maladie survient à la suite d'un
déséquilibre de la flore caecal lors d'un stress causé par
le sevrage et le changement de régime alimentaire entraînant ainsi
la multiplication des colibacilles.
b) Lésions
A l'autopsie le contenu caecal est liquide, l'estomac est
presque vide avec beaucoup de liquide.
2.2.2- Autres maladies
bactériennes du lapin
Outre les maladies précitées, le lapin est
aussi victime d'autres pathologies non fréquentes au Bénin. Ce
sont entre autres l'entérotyphlite à Clostridium
spiroforme, la salmonellose, la klebsiollose, les mycoplasmoses, la
turarémie, la tuberculose, la chlamydophilose, la syphilis à
trépanème etc. (DJAGO et KPODEKON, 2000 ; BOUCHEUR et
NOUAILLE, 2002).
CHAPITRE 2 :
MATÉRIEL ET MÉTHODES
2.1-
Matériels
2.1.1- Matériel
animal
L'étude a porté sur 75 lapins,
morts ou agonisants, collectés dans 30 élevages membres de
l'Association Béninoise des Cuniculteurs localisés au Sud du
Bénin. Les 75 lapins sont composés de 32 sous mères et de
43 sevrés d'une part et de 41 mâles et de 34 femelles d'autre
part. Le choix a été porté sur des élevages
disposant d'au moins 50 lapins. Les autopsies et l'identification des
bactéries ont été réalisées au Complexe
Clinique Laboratoire Pharmacie Vétérinaire du Département
de Production et Santé Animales de l'Ecole polytechnique
d'Abomey-Calavi.
2.1.2- Matériel et
produits de laboratoire
Un matériel varié et divers
réactifs de bactériologie (annexe 1) ont été
utilisés dans le cadre de l'autopsie et de l'identification des
bactéries responsables des diverses lésions.
2.2- Méthodes
2.2.1- La collecte des
données
Elle s'est déroulée en deux phases :
Ø les enquêtes épidémiologiques qui
ont permis d'évaluer l'importance de la mortalité des lapins, les
conditions d'élevage et globalement les pathologies dominantes des
lapins. Une fiche d'enquête (annexe 2) a été
élaborée à cet effet afin de recueillir les renseignements
nécessaires ;
Ø la mise en évidence des pathologies du lapin
sévissant dans les élevages cunicoles du sud Bénin par la
recherche des lésions après autopsie, ainsi que la mise en oeuvre
des analyses bactériologiques sur les prélèvements
effectués. Concernant les autopsies, il a été
élaboré une fiche individuelle de renseignement (annexe 2) pour
recueillir les informations sur l'identification de l'élevage et du
lapin, les commémoratifs, l'examen nécropsique, la liste des
lésions macroscopiques observées, les examens
complémentaires et la conclusion partielle.
2.2.2- Méthode
d'autopsie
L'autopsie est l'étude d'un cadavre dans le but
d'identifier les causes de la mort. Après avoir établi les
commémoratifs et examiné l'état général,
l'animal, s'il est agonisant a été sacrifié par
étirement et élongation de la colonne vertébrale. Le
cadavre obtenu a été placé en décubitus dorsal les
pattes écartés et les poils imbibés d'eau de robinet
afin de les maintenir collés. La peau a été incisée
avec une paire de ciseaux à dissection en partant du dessous du menton
jusqu'aux organes génitaux en ligne droite puis décollé
et récliné de chaque côté. Les pattes ont
été désarticulées de façon à les
écarter du tronc pour assurer la stabilité puis il a
été procédé à l'ouverture de la
cavité abdominale qui s'est réalisée comme suit :
· incision des muscles abdominaux sur la ligne blanche,
au milieu du corps.
· coupure des côtes de chaque côté et
décollement du diaphragme. Le plastron thoracique a été
levé. Ce qui a laissé voir au fur et à mesure les poumons,
le coeur, la trachée et l'oesophage.
L'opération précédente étant
terminée, la plupart des organes internes ont fait l'objet d'un examen
attentif pour déceler les éventuelles anomalies en tenant compte
de la couleur, la forme, la consistance, la présence
d'éléments anormaux etc.. . Pour les poumons, un test de
flottaison (docimasie) a été réalisé en cas de
lésion.
2.2.3- Méthode
d'identification des germes
2.2.3.1-
Prélèvement
Les prélèvements d'organes ont
été effectués de façon aseptique à l'aide
d'une pince hémostatique à dents de souris et d'une paire de
ciseaux stérilisées. Quant aux prélèvements
liquides, ils ont été réalisés à l'aide d'un
écouvillon stérile.
2.2.3.2- Isolement
Les organes prélevés ont été mis
en culture dans du bouillon enrichi (annexe 3), puis incubés une nuit
à l'étuve à 37°C. Ces cultures ont été
ensemencées par épuisement le lendemain sur de la gélose
enrichie (annexe 3) coulée en boîte de Pétri et
incubées à nouveau pendant 24 Heures à 37 ° C. En ce
qui concerne les prélèvements réalisés à
l'aide d'écouvillons, ils ont été directement
ensemencés sur de la gélose enrichie et incubés pendant 24
heures à 37 ° C.
2.2.3.3- Identification
A partir d'une culture pure, les étapes de
l'identification ont été :
- les tests d'orientations (annexe 4) : Il s'agit de la
coloration de Gram, du test de catalase, d'oxydase, de mobilité et d'O/F
(Oxydation-Fermentation)
- la recherche des caractères biochimiques par les
méthodes décrites par COWAN(1993) à l'aide d'une
mini-galerie.
a) Confection de frottis
L'opération débute par la coloration de Gram
qui se fait après l'obtention des colonies isolées. Chaque
colonie observée est émulsionnée dans une goutte d'eau
distillée stérile déposée sur une lame propre. A
l'aide d'une oëse la colonie est étalée,
séchée puis fixée à la flamme du bec Bunsen avant
d'être colorée par la méthode de Gram (annexe 4).
Cette coloration a permis de distinguer les coques des
bacilles ainsi que les bactéries Gram positif des bactéries Gram
négatif, ce qui a favorisé l'orientation du choix des
différents milieux sélectifs.
Les lames fixées et colorées ont
été observées à l'immersion à l'objectif
100.
b) Identification des bacilles
Gram-
Les bacilles Gram négatif isolés en culture
pure ont été ensemencés sur Mac-conkey (annexe 3). Les
colonies obtenues ont été soumises au test de mobilité,
de catalase, d'oxydase et de réduction de lactose afin de
différencier les entérobactéries, des non
entérobactéries et de diviser le groupe des
entérobactéries en coccobacilles et bacilles.
Ces tests ont été complétés par
une mini galerie (annexe 5) permettant d'identifier les différentes
espèces de bacilles Gram négatif, conformément à la
technique de COWAN (1993).
c) Identification des coques
Gram+
Les Coques Gram+ ont été
soumis au test de catalase afin de différencier les
staphylocoques (catalase+), des streptocoques (catalase-). Le dégagement
du bulle gazeuse signifie que la colonie est catalase (+).
Outre le test de la catalase, ces colonies ont
été ensemencées sur milieu de Chapman (annexe 3) ;
spécifique aux staphylocoques.
d) Identification des bacilles Gram+
Les bacilles Gram+ du genre Bacillus ont
été identifiés par les caractères biochimiques de
COWAN (1993) après les tests de catalase et d'oxydase. Pour la recherche
du genre Clostridium, nous avons utilisé le système
GasPaKR qui crée un milieu anaérobie strict.
2.2.4- Analyses
statistiques
Les données sur les microorganismes et les
lésions identifiés ont été enregistrées sur
tableur Excel. Les fréquences ont été calculées et
comparées à l'aide du logiciel STATISTICA.
CHAPITRE 3 :
RÉSULTATS ET DISCUSSION
3.1- Résultats
3.1.1- Résultats des
enquêtes épidémiologiques
La collecte des données lors de nos enquêtes
épidémiologiques nous a permis de réaliser le tableau
III.
Au total, 30 élevages ont été
prospectés. Les effectifs varient entre 50 et 789 lapins avec une
population totale de 6870 lapins. En 2006, le nombre de malades a varié
de 0 à 789 et le nombre de morts de 0 à 730, soit un taux de
létalité variant entre 0 et 92%.
R les élevages cunicoles du sud-Bénin ont pour
la plupart un logement de type traditionnel avec une assez - bonne situation
sanitaire.
R les signes souvent observés chez les lapins malades
ou tout juste après la mort sont pour la plupart la
diarrhée et le ballonnement d'abdomen, suivis dans une moindre
fréquence de l'inappétence et de l'agitation.
Il est à noter que tous les élevages
prospectés se font en cage
Tableau III :
Données épidémiologiques et cliniques sur les
élevages prospectés
|
Elevage
|
Localisation
|
Type de logement
|
Effectif total
|
Nombre de malade en 2006
|
Nombre de mort en 2006
|
Taux de létalité (%)
|
Situation
sanitaire
|
Signes souvent observés
|
Produits utilisés
|
|
GBEKE [ 1 ]
|
Womey
|
T
|
82
|
79
|
60
|
76
|
P
|
Agitation
|
Oxy, amin total
|
|
AHOYO [ 2 ]
|
Togoudo
|
PA
|
62
|
49
|
38
|
78
|
P
|
Prostration, agitation, inappétence
|
Trisulmicyne, amin total
|
|
KIDJO [ 3 ]
|
Atrokpocodji
|
T
|
101
|
50
|
30
|
60
|
AB
|
Gale
|
Oxy,ivermectine
|
|
EGUE [ 4 ]
|
Atrokpocodji
|
T
|
55
|
0
|
0
|
00
|
B
|
0
|
0
|
|
AHI [ 5 ]
|
Pahou
|
A
|
789
|
650
|
541
|
83
|
M
|
Ballonnement, dépilation,
amaigrissement, inappétence
|
Ivermectine, amin total, oxy
|
|
ADOLPHE [ 6 ]
|
Atrokpocodji
|
T
|
345
|
312
|
250
|
80
|
AB
|
Ballonnement, diarrhée
|
Oxy, anticox
|
|
VOITAN [ 7 ]
|
Abomey-Calavi
|
T
|
95
|
60
|
40
|
67
|
B
|
Ballonnement, diarrhée
|
Superhipracox-p, oxy
|
|
CECURI [ 8 ]
|
Abomey-Calavi
|
A
|
719
|
789
|
730
|
92
|
B
|
Ballonnement, diarrhée
|
Anticox,oxy
|
|
AHOZIN [ 9 ]
|
Pahou
|
A
|
675
|
241
|
133
|
55
|
B
|
Ballonnement, diarrhée
|
Anticox,oxy,amin total
|
|
BENIN-LAPIN [ 10 ]
|
Pahou
|
T
|
678
|
298
|
246
|
83
|
B
|
Ballonnement, diarrhée
|
CRD 92, anticox, oxy
|
|
METO [ 11 ]
|
Atrokpocodji
|
T
|
138
|
60
|
40
|
67
|
B
|
Plaie et gale
|
Huile+ sel de cuisine
|
|
PERE SANTOS [ 12 ]
|
Ouèdo
|
PA
|
291
|
100
|
80
|
80
|
B
|
Ballonnement, diarrhée
|
Superhipracox-p, oxy,amin total
|
|
ADOHO [ 13 ]
|
Ouèdo
|
PA
|
101
|
209
|
151
|
72
|
AB
|
Ballonnement, diarrhée
|
CRD 92, anticox, oxy
|
|
HOUEGBONOU [ 14 ]
|
Ouèdo
|
T
|
109
|
300
|
165
|
55
|
B
|
Ballonnement, diarrhée, gale
|
Ivermectine, oxy, superhipracox-p
|
|
AHINANDJE [ 15 ]
|
Dossounou
|
T
|
392
|
301
|
250
|
83
|
B
|
Ballonnement, diarrhée inappétence
|
CRD 92, superhipracox-p, oxy
|
|
ADJADOHOUN [ 16 ]
|
Ouèdo
|
T
|
205
|
450
|
200
|
44
|
AB
|
Diarrhée, ballonnement,
Epilepsie, inappétence
|
CRD 92, superhipracox-p, oxy
|
|
ADOUN [ 17 ]
|
Calavi
|
PA
|
72
|
50
|
40
|
80
|
P
|
Diarrhée, agitation, abcès
|
0
|
|
TCHIBOZO [ 18 ]
|
Pahou
|
T
|
182
|
206
|
152
|
74
|
AB
|
Agitation, diarrhée, ballonnement
|
Alfamec, trisulmycine, oxy
|
|
HOUNKPESSODE [ 19 ]
|
Atrokpocodji
|
T
|
96
|
9
|
5
|
56
|
AB
|
Gale, agitation puis mort
|
Trisulmycine, ivermectine,oxy
|
|
de SOUZA [ 20 ]
|
Womey
|
PA
|
72
|
50
|
30
|
60
|
AB
|
Diarrhée, ballonnement, inappétence, agitation
|
Trisulmycine,amino-life
|
|
HODONOU [ 21 ]
|
Womey
|
T
|
50
|
89
|
40
|
45
|
B
|
Mammite, diarrhée, agitation
|
Feuille de goyave (anticoccidien)
|
|
KAPKO [ 22 ]
|
Womey
|
T
|
61
|
2
|
1
|
50
|
B
|
Inappétence, lapin en boule
|
Superhipracox-p, amin-total
|
|
HADJI [ 23 ]
|
Womey
|
T
|
269
|
189
|
108
|
57
|
B
|
Inappétence, jetage,
ballonnement, convulsion
|
Oxy, coccontrol,amino-life
|
|
AGOUNPKE [ 24 ]
|
Womey
|
T
|
58
|
0
|
0
|
00
|
B
|
-
|
0
|
|
GBEDE [ 25 ]
|
Calavi
|
T
|
152
|
152
|
92
|
61
|
AB
|
Gale, diarrhée, ballonnement
|
Anticox, oxy, alfamec
|
|
HESSOU [ 26 ]
|
Womey
|
T
|
68
|
155
|
100
|
65
|
AB
|
Diarrhée, ballonnement, agitation
|
Coccontrol, oxy, amino-life
|
|
HOUETON [ 27 ]
|
Ouèdo
|
PA
|
242
|
600
|
545
|
91
|
AB
|
Inappétence, diarrhée, ballonnement, gale
|
Anticox, oxy, amino-life
|
|
AGOUA [ 28 ]
|
Womey
|
T
|
116
|
150
|
92
|
61
|
AB
|
Gale, diarrhée, convulsion, allonnement
|
Anticox, oxy, ivermectine
|
|
HOUEGBONOU [ 29 ]
|
Calavi
|
T
|
397
|
490
|
300
|
61
|
B
|
Diarrhée, ballonnement, gale, inappétence
|
Superhipracox-p, oxy, amin-total,
alfamec
|
|
DOLIVERA [ 30 ]
|
Pahou
|
T
|
198
|
200
|
175
|
88
|
AB
|
Diarrhée, ballonnement, agitation, gale
|
Superhipracox-p, oxy, alfamec
|
|
Total
|
6870
|
6289
|
4634
|
69
|
|
B : Bonne : logement et
matériels bien entretenus, utilisation de désinfectants et
traitement en cas de maladie
PA : Plein air
AB : Assez Bonne : logement en
plein air ou mal entretenus, matériels bien entretenus utilisation de
désinfectant et traitement en cas de maladie
Oxy : Oxytétracycline
P : Passable : logement en plein
air, matériels bien entretenus, utilisation de désinfectant et
traitement en cas de maladie
M : Mauvais : logement et
matériels mal entretenus, utilisation de désinfectant et
négligence de traitement
T : Traditionnel : sol non
cimenté, pas de fosse à déjection, non utilisation de
tétine pour abreuvement
A : Amélioré :
sol cimenté, présence de fosses à déjection,
utilisation de tétine pour abreuvement
3.1.2- Les lésions
et leur fréquence en fonction des organes
Le tableau IV présente les fréquences des
lésions en fonction des organes.
De l'analyse de ces lésions et de leur
fréquence en fonction des organes, il ressort que les principaux organes
lésés chez les lapins morts de maladies sont dans l'ordre
décroissante d'importance, le foie avec comme principale lésion
la congestion suivie de la dégénérescence, le poumon au
niveau duquel on observe principalement la congestion, le caecum où l'on
enregistre principalement une accumulation de gaz avec quelque fois un contenu
diarrhéique, l'intestin grêle où l'on note principalement
la congestion et un contenu diarrhéique, les naseaux avec un
écoulement sanguinolent, la trachée qui est principalement
congestionnée.
Tableau IV :
Fréquence des lésions en fonction des organes:
|
Organe
Elevage
|
Poumon
|
Foie
|
Coeur
|
Rein
|
Trachée
|
Caecum
|
Naseaux
|
Intestin
|
Estomac
|
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
|
[4]
|
02
|
3c
|
02
|
3c
|
01
|
50a
|
0
|
0a
|
0
|
0b
|
01
|
2cd
|
01
|
6b
|
0
|
0c
|
0
|
0a
|
|
[5]
|
01
|
2c
|
01
|
1c
|
0
|
0a
|
01
|
25a
|
0
|
0b
|
01
|
2cd
|
0
|
0b
|
01
|
4bc
|
0
|
0a
|
|
[6]
|
34
|
54 a
|
35
|
49 a
|
0
|
0a
|
01
|
25a
|
06
|
60a
|
32
|
54 a
|
10
|
59 a
|
11
|
41a
|
01
|
50a
|
|
[7]
|
02
|
3c
|
01
|
1c
|
0
|
0a
|
0
|
0a
|
02
|
20b
|
0
|
0d
|
0
|
0b
|
0
|
0c
|
0
|
0a
|
|
[8]
|
11
|
17b
|
18
|
25b
|
01
|
50a
|
01
|
25a
|
01
|
10b
|
12
|
20b
|
01
|
6b
|
07
|
26 ab
|
01
|
50a
|
|
[10]
|
02
|
3c
|
01
|
1c
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
04
|
7c
|
0
|
0b
|
02
|
7bc
|
0
|
0a
|
|
[12]
|
01
|
2c
|
01
|
1c
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
01
|
2cd
|
0
|
0b
|
0
|
0c
|
0
|
0a
|
|
[13]
|
01
|
2c
|
03
|
4c
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
02
|
3cd
|
01
|
6b
|
0
|
0c
|
0
|
0a
|
|
[15]
|
04
|
6bc
|
05
|
7c
|
0
|
0a
|
0
|
0a
|
01
|
10b
|
03
|
5cd
|
03
|
18b
|
04
|
15b
|
0
|
0a
|
|
[18]
|
03
|
5c
|
02
|
3c
|
0
|
0a
|
01
|
25a
|
0
|
0b
|
02
|
3cd
|
01
|
6b
|
0
|
0c
|
0
|
0a
|
|
[22]
|
01
|
2c
|
01
|
1c
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
01
|
2cd
|
0
|
0b
|
01
|
4bc
|
0
|
0a
|
|
[27]
|
01
|
2c
|
01
|
1c
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
0
|
0d
|
0
|
0b
|
01
|
4bc
|
0
|
0a
|
|
N total
|
63
|
71
|
02
|
04
|
10
|
59
|
17
|
27
|
02
|
Les fréquences de la même colonne
portant des lettres différentes en exposant sont significativement
différentes au seuil de 5%.
Lésions observées
Poumon Foie Rein
Trachée Caecum Intestin
Naseaux Estomac Coeur
- congestion (55*) - congestion (40) - congestion (02) -
congestion (10) - gaz (47) - congestion (12) -
écoulement - inflammation - congestion
- pétéchies (07) - pétéchies (07)
- pétéchies (01) - contenu - contenu
diarrhéique sanguinolent (02)
(02)
- nécrose (01) - nécrose (08) -
nécrose (01) diarrhéique (15)
(17)
- dégénérescence (16)
(12)
* Nombre de cas
F = 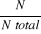 x 100 avec F : Fréquence et N : Nombre de
lésions x 100 avec F : Fréquence et N : Nombre de
lésions
3.1.3- Microorganismes
identifiés
Les microorganismes identifiés sont
présentés dans le tableau V
La lecture du tableau montre que :
R Escherichia coli est le plus
fréquent (p < 0,05) et représente 50% des bactéries
identifiés. Il a été rencontré dans 10 sur 12
élevages où les prélèvements ont été
effectués. Il est suivi de Clostridium spp (8%) et
Enterobacter spp (7%) ;
R la fréquence des douze autres bactéries varie
entre 1 et 5%.
Tableau V : Principaux
microorganismes identifiés dans les 150 prélèvements
effectués.
|
Bactéries identifiées
|
Elevage
|
Nombre d'organes infectés (N)
|
Fréquence (F) en %
|
|
Escheirichia coli [I]
|
[8], [6], [18], [5], [15], [7], [10], [12], [13], [22]
|
75
|
50a
|
|
Clostridium spp [II]
|
[8], [6], [18]
|
12
|
8b
|
|
Enterobater spp [III]
|
[8], [6]
|
10
|
7b
|
|
Citrobacter spp [IV]
|
[8], [6], [15]
|
04
|
3bc
|
|
Pseudomonas spp [V]
|
[8], [6]
|
03
|
2c
|
|
Proteus mirabilis [VI]
|
[6], [15], [10], [8]
|
05
|
3bc
|
|
Shigella dysenteriae [VII]
|
[6], [27]
|
08
|
5bc
|
|
Pasteurella multocida [VIII]
|
[6], [4]
|
07
|
5bc
|
|
pasteurella haemolitica [IX]
|
[7], [6]
|
03
|
2c
|
|
Pasteurella pneumotropica [X]
|
[6], [18]
|
02
|
1c
|
|
Edwardsiella tarda [XI]
|
[6], [10]
|
05
|
3bc
|
|
Bacillus firmus [XII]
|
[6], [15], [22]
|
03
|
2c
|
|
Klebsiella pneumoniae [XIII]
|
[8], [6]
|
04
|
3bc
|
|
staphylococcus spp [XIV]
|
[6], [15], [22]
|
07
|
5bc
|
|
Yersinia spp [XV]
|
[6], [15]
|
02
|
1c
|
Les fréquences de la même colonne
portant des lettres différentes en exposant sont significativement
différentes au seuil de 5%.
Tableau VI : Nombre de cas d'infections par
organe
|
Bactéries
Organes
|
[I]
|
[II]
|
[III]
|
[IV]
|
[V]
|
[VI]
|
[VII]
|
[VIII]
|
[IX]
|
[X]
|
[XI]
|
[XII]
|
[XIII]
|
[XIV]
|
[XV]
|
|
- Poumon
|
29
|
04
|
04
|
01
|
02
|
03
|
05
|
02
|
01
|
0
|
02
|
02
|
02
|
04
|
0
|
|
- Foie
|
27
|
06
|
04
|
02
|
01
|
01
|
03
|
01
|
0
|
0
|
03
|
01
|
01
|
02
|
02
|
|
- Caecum
|
03
|
01
|
02
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
- Intestin
|
10
|
0
|
0
|
01
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
01
|
0
|
|
- estomac
|
02
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
- Coeur
|
02
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
- Rein
|
02
|
01
|
0
|
0
|
0
|
01
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
- Trachée
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
03
|
01
|
01
|
0
|
0
|
01
|
0
|
01
|
|
- Naseaux
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
01
|
01
|
01
|
0
|
0
|
0
|
0
|
0
|
3.1.4- Fréquence des
microorganismes par élevage
Elles sont présentées dans le tableau VII
De l'analyse de ces résultats, il ressort que :
- Escherichia coli, Clostridium spp, Anterobacter
spp sont plus fréquents dans l'élevage [6] et dans
l'élevage [8] ;
- les autres espèces bactériennes ont
été souvent rencontrées en grande proportion surtout dans
l'élevage [6], même si la différence n'est pas
significative ;
- les élevages les plus infectés sont le [6] et le
[8]
Tableau VII :
Fréquence des microorganismes en fonction des
élevages
|
Microorga
nisme
Elevage
|
[I]
|
[II]
|
[III]
|
[IV]
|
[V]
|
[VI]
|
[VII]
|
[VIII]
|
[IX]
|
[X]
|
[XI]
|
[XII]
|
[VIII]
|
[XIV]
|
[XV]
|
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
|
[4]
|
0
|
0b
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
02
|
29 ab
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
|
[5]
|
01
|
1b
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
|
[6]
|
38
|
51 a
|
07
|
58 a
|
03
|
30ab
|
01
|
25a
|
01
|
33a
|
01
|
20a
|
05
|
63 a
|
15
|
71a
|
01
|
33a
|
01
|
50a
|
04
|
80a
|
01
|
33a
|
03
|
75a
|
03
|
43a
|
01
|
50a
|
|
[7]
|
01
|
1b
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
0
|
0b
|
02
|
66a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
|
[8]
|
22
|
29 a
|
04
|
33ab
|
07
|
70a
|
02
|
50a
|
02
|
66a
|
01
|
20a
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
01
|
25a
|
0
|
0a
|
0
|
0a
|
|
[10]
|
04
|
5b
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
01
|
20a
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
01
|
20a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
|
[12]
|
01
|
1b
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
|
[13]
|
03
|
4b
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
|
[15]
|
01
|
1b
|
0
|
0b
|
0
|
0b
|
01
|
25a
|
0
|
0a
|
02
|
40a
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
01
|
33a
|
0
|
0a
|
03
|
43a
|
01
|
50a
|
|
[18]
|
03
|
4b
|
01
|
8b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
01
|
50a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
|
[22]
|
01
|
1b
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
01
|
33a
|
0
|
0a
|
01
|
14a
|
0
|
0a
|
|
[27]
|
0
|
0b
|
0
|
0b
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
03
|
37ab
|
0
|
0b
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
0
|
0a
|
|
N total
|
75
|
12
|
10
|
04
|
03
|
05
|
08
|
07
|
03
|
02
|
05
|
03
|
04
|
07
|
02
|
Les fréquences de la même colonne portant des
lettres différentes en exposant sont significativement
différentes au seuil de 5%.
3.1.5- Fréquence des
paramètres étudiés en fonction de l'âge et du
sexe
3.1.5.1- En fonction de
l'âge
Les fréquences des lésions et des
microorganismes sont respectivement présentées dans les tableaux
VIII et IX.
Le tableau VIII révèle que les lésions
du foie, des reins, du caecum, et des intestins sont plus fréquentes
chez les lapins à l'engraissement que chez les lapins sous mère
(p < 0,05). Aucune différence significative n'a été
constatée en fonction de l'âge pour les lésions des autres
organes.
L'analyse du tableau IX montre que les lapins à
l'engraissement sont plus infectés par Esherichia coli et
Clostridium spp (p < 0,05) que les lapins non sevrés.
Tableau VIII :
Fréquence des lésions en fonction de l'âge:
|
Organes
Ages
(jrs)
|
Poumon
|
Foie
|
Coeur
|
Rein
|
Trachée
|
Caecum
|
Naseaux
|
Intestin
|
Estomac
|
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
|
[0-35]
|
29
|
46a
|
19
|
27a
|
00
|
00a
|
01
|
33a
|
06
|
60a
|
16
|
27a
|
09
|
53a
|
09
|
33a
|
01
|
50a
|
|
] 35-120]
|
34
|
54a
|
52
|
73b
|
02
|
100a
|
03
|
67b
|
04
|
40a
|
43
|
73b
|
08
|
47a
|
18
|
67b
|
01
|
50a
|
|
N total
|
63
|
|
71
|
|
02
|
|
04
|
|
10
|
|
59
|
|
17
|
|
27
|
|
02
|
|
Les fréquences de la même colonne portant des
lettres différentes en exposant sont significativement
différentes au seuil de 5%.
Tableau IX :
Principaux microorganismes en fonction de l'âge
|
Microorga-
nismes
Ages (jrs)
|
[ I ]
|
[ II ]
|
[ III ]
|
[ IV ]
|
[ V ]
|
[ VI ]
|
[ VII ]
|
[VIII ]
|
[ IX ]
|
[ X ]
|
[ XI ]
|
[ XII ]
|
[ XIII ]
|
[ XIV]
|
[ XV ]
|
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
|
[0-35]
|
23
|
31a
|
01
|
08a
|
05
|
50a
|
01
|
25a
|
01
|
33a
|
02
|
40a
|
05
|
62a
|
04
|
57a
|
02
|
67a
|
01
|
50a
|
03
|
60a
|
01
|
33a
|
01
|
25a
|
02
|
29a
|
01
|
50a
|
|
] 35-120]
|
52
|
69b
|
11
|
92b
|
05
|
50a
|
03
|
75a
|
02
|
67a
|
03
|
60a
|
03
|
38a
|
03
|
43a
|
01
|
33a
|
01
|
50a
|
02
|
40a
|
02
|
67a
|
03
|
75a
|
05
|
71a
|
01
|
50a
|
|
N total
|
75
|
|
12
|
|
10
|
|
04
|
|
03
|
|
05
|
|
08
|
|
07
|
|
03
|
|
02
|
|
05
|
|
03
|
|
04
|
|
07
|
|
02
|
|
Les fréquences de la même colonne portant des
lettres différentes en exposant sont significativement
différentes au seuil de 5%.
3.1.5.2- En fonction du
sexe
Les fréquences des lésions et des
microorganismes sont respectivement présentées dans les tableaux
X et XI.
Bien qu'en général les lésions des
différents organes sont plus fréquentes chez les males que chez
les femelles, aucune différence significative n'a été
notée en fonction du sexe (p > 0,05) (tableau X).
En ce qui concerne les microorganismes identifiés,
aucune différence significative n'a été enregistrée
en fonction du sexe (tableau XI).
Tableau X :
Fréquence des lésions en fonction du sexe
|
Organes
Lapins
|
Poumon
|
Foie
|
Coeur
|
Rein
|
Trachée
|
Caecum
|
Naseaux
|
Intestin
|
Estomac
|
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
|
Mâle
|
34
|
54a
|
37
|
52a
|
00
|
00a
|
02
|
50a
|
06
|
60a
|
29
|
49a
|
08
|
47a
|
14
|
52a
|
01
|
50a
|
|
Femelle
|
29
|
46a
|
34
|
48a
|
02
|
100a
|
02
|
50a
|
04
|
40a
|
30
|
51a
|
09
|
53a
|
13
|
48a
|
01
|
50a
|
|
N total
|
63
|
|
71
|
|
02
|
|
04
|
|
10
|
|
59
|
|
17
|
|
27
|
|
02
|
|
Les fréquences de la même colonne portant des
mêmes lettres en exposant ne sont pas significativement
différentes au seuil de 5%.
Tableau XI :
Principaux microorganismes en fonction du sexe
|
Microorga-
nismes
Lapins
|
[ I ]
|
[ II ]
|
[ III ]
|
[ IV ]
|
[ V ]
|
[ VI ]
|
[ VII ]
|
[VIII ]
|
[ IX ]
|
[ X ]
|
[ XI ]
|
[ XII ]
|
[ XIII ]
|
[ XIV]
|
[ XV ]
|
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
N
|
F
|
|
Mâle
|
39
|
52a
|
05
|
42a
|
06
|
60a
|
01
|
25a
|
01
|
33a
|
02
|
40a
|
05
|
63a
|
02
|
29a
|
02
|
67a
|
00
|
00a
|
04
|
80a
|
02
|
67a
|
01
|
25a
|
02
|
29a
|
01
|
50a
|
|
Femelle
|
36
|
48a
|
07
|
58a
|
04
|
40a
|
03
|
75a
|
02
|
67a
|
03
|
60a
|
03
|
37a
|
05
|
71a
|
01
|
33a
|
02
|
100a
|
01
|
20a
|
01
|
33a
|
03
|
75a
|
05
|
71a
|
01
|
50a
|
|
N total
|
75
|
|
12
|
|
10
|
|
04
|
|
03
|
|
05
|
|
08
|
|
07
|
|
03
|
|
02
|
|
05
|
|
03
|
|
04
|
|
07
|
|
02
|
|
Les fréquences de la même colonne portant des
mêmes lettres en exposant ne sont pas significativement
différentes au seuil de 5%.
3.2- Discussion
3.2.1- Critique de nos
résultats
3.2.1.2- Résultats des
enquêtes épidémiologiques
Au terme de cette étude, la plupart des
élevages cunicoles prospectés ont un logement traditionnel avec
une assez bonne situation sanitaire. Ces résultats sont en
désaccord avec les travaux de KPODEKON (1988 a) qui avait
remarqué en 1987 au Bénin des élevages de type fermier
réalisés dans de vieilles cases en banco, au sol non
cimenté et utilisant comme clapier, les caisses d'emballages
aménagées et les clapiers en maçonnerie. Le même
auteur a également constaté au terme de ses travaux que certains
cuniculteurs laissent leurs lapins baigner dans un mélange de crotte,
d'urine, et de reste d'aliments. La discordance entre ces deux résultats
traduit la modernisation subie par les élevages cunicoles du
Bénin depuis 1988.
Les principaux signes enregistrés au cours de nos
travaux sur des lapins malades ou après leur mort sont la
diarrhée et le ballonnement d'abdomen. Ces résultats sont en
partie en accord avec ceux de KPODEKON (1988 a) qui a signalé la
présence de coccidiose dans nos élevages et qui selon DJAGO et
KPODEKON (2000) entraînerait un gros ventre et une légère
diarrhée. Mais, le même auteur a signalé au cours de ses
enquêtes la présence d'autres maladies comme la gale, la teigne
favique, la cordylobiose et les abcès plantaires qui n'ont pas
été remarqués lors de nos enquêtes.
L'amélioration des conditions d'élevage et le suivi sanitaire
dont font preuve la plupart des éleveurs de nos jours pourrait justifier
la raréfaction des parasitoses et infections externes.
3.2.1.2- Les principales
lésions et leur fréquence en fonction des organes
Les principales lésions enregistrées dans cette
étude sont :
ü la congestion du poumon, du foie, de l'intestin et de
la trachée ;
ü la dégénérescence du
foie ;
ü l'accumulation de gaz dans le caecum ;
ü un contenu diarrhéique du caecum et de
l'intestin ;
ü un écoulement sanguinolent par les naseaux.
Certaines des lésions constatées sont en accord
avec les travaux de BOUCHER et NOUAILLE (2002) qui ont noté lors de
l'entérotoxémie chez le lapin, causée par Clostridium
perfringens la présence de gaz dans le caecum à contenu
diarrhéique et à paroi hémorragique, ainsi que la
dégénérescence du foie.
Ils ont par ailleurs noté lors de la colibacillose
causée par Escherichia coli un contenu intestinal et
caecal liquide avec une congestion généralisée de
l'intestin et des points de nécrose hépatique.
En outre, ces mêmes auteurs ont signalé lors de
la pasteurellose causée par Pasteurella multocida un
poumon rouge foncé.
La congestion de la trachée et l'écoulement
sanguinolent constatés au cours de ce travail pourrait être due
à la pasteurellose dont les symptômes (respiration difficile,
bruyante, rauque signalée, écoulement nasal) qui ont
été signalés par DJAGO et KPODEKON (2000).
3.2.1.3- Relation entre la
situation sanitaire des élevages et les fréquences des
microorganismes
La différence d'infection enregistrée au niveau
des élevages ayant une même situation sanitaire pourrait
s'expliquer par le nombre d'animaux autopsiés. En effet, un seul animal
provenant de l'élevage [4] et [27] a été autopsié
contre 30 pour l'élevage [8] et 25 pour l'élevage [6]. Toutefois,
le niveau d'infection relativement plus élevé dans
l'élevage [6] pourrait s'expliquer par les conditions d'élevage
et d'hygiène plus précaires. La fréquence importante de
bactérie pathogène au CeCuRI malgré les conditions
d'élevage jugées satisfaisantes pourrait être dû au
nombre relativement élevé de personnes qui accèdent aux
locaux d'élevage.
3.2.1.4- Relation entre les
principaux signes recensés chez le lapin (malade ou mort) et les
principaux microorganismes identifiés.
Les principaux signes identifiés dans cette
étude sont la diarrhée et le ballonnement de l'abdomen.
Les principaux microorganismes sont Escherichia
coli, suivi de Clostridium spp et d'Enterobacter spp.
Ces résultats sont en accord avec ceux des travaux de
BOUCHER et NOUAILLE (2002) qui ont signalé chez les lapins
diarrhéiques un déséquilibre de la flore intestinale
entraînant la multiplication de colibacilles dont Escherichia
coli.
Ces mêmes auteurs ont imputé le ballonnement
d'abdomen à la multiplication d'une bactérie anaérobie
stricte : Clostridium perfringens. Le genre Enterobacter
étant aussi un colibacille, sa présence importante pourrait
entraîner des troubles digestifs.
Notons aussi que CAMGUILHEM (1985) a isolé chez les
lapins diarrhéiques provenant d'un élevage, plusieurs souches
d'Escherichia coli appartenant toutes au sérogroupe 0103. La
présence de la diarrhée pourrait faire suspecter la
présence de coccidies comme l'ont montré les travaux de BOUCHER
et NOUAILE (2002). Mais en 1982, LICOIS et al cités par
CAMGUILHEM ont réalisé une infection expérimentale per
os à partir d'une souche d'Escherichia coli appartenant au
sérogroupe 0103 qui provoque à la dose de 104
bactéries par animal, une diarrhée mortelle sur 100% des lapins
de six semaines d'une souche indemne de coccidiose. Toutefois, étant
donné que ce travail ne s'est pas intéressé à la
coccidiose, certains cas de diarrhée peuvent être dus à des
coccidies.
3.2.1.5- Fréquence des
lésions et des microorganismes en fonction de l'âge
Les lapins en engraissement sont plus infectés par
Escherichia coli et Clostridium spp que ceux sous
mères. Ils ont aussi plus les lésions du foie, du caecum, des
reins et des intestins que ceux sous mères.
Ces résultats sont en accord avec ceux de
BOUCHEUR et NOUAILLE (2002) ; DJAGO et KPODEKON (2000) qui ont
signalé chez le lapin un stress causé par le sevrage et le
changement du régime alimentaire. Ceci se traduit par un
déséquilibre de la flore caecale et favorise la multiplication
des colibacilles entraînant une diarrhée très liquide. Les
mêmes auteurs ont souligné que l'entérotoxémie
causée par Clostridium perfringens attaque plus les
lapins en engraissement et entraîne une accumulation de gaz dans le
caecum de ceux-ci. Au cours de cette même maladie, le foie est
dégénéré, les reins et les intestins
congestionnés.
3.2.1.6- Fréquence des
lésions et des microorganismes en fonction du sexe
Ce travail a montré que les lésions d'organes
et les microorganismes identifiés ne varient pas en fonction du sexe
tant au niveau des lapins sous mères que ceux en engraissement.
Ces résultats pourraient s'expliquer par le
fait que les lapins des deux sexes sont élevés dans les
mêmes conditions et soumis au même régime alimentaire.
3.2.1.7- Relation entre le taux
de létalité et les microorganismes identifiés
La moyenne de létalité est
évaluée à 68% au cours de nos enquêtes et le
principal microorganisme identifié est Escherichia coli.
Ce taux pourrait s'expliquer par la présence d'une des
souches d'Escherichia coli qui entraînerait une mortalité
importante comme l'ont montré les travaux de CAMGUILHEM (1985). De
même LICOIS et al., cités par CAMGUILHEM (1985), ont
obtenu une mortalité de 100% avec une souche d'Escherichia coli
appartenant au sérogroupe O103 sur des lapins de six semaines
à la dose de 104 bactéries, sur des lapins indemnes de
coccidiose.
CONCLUSION ET
SUGGESTIONS
Cette étude a permis d'une part de faire un
état de lieu des élevages cunicoles du sud-Bénin et
d'autre part de mettre en évidence les pathologies du lapin par la
recherche des lésions ainsi que la mise en oeuvre des analyses
bactériologiques. La plupart des résultats ont été
comparés avec ceux des pays tempérés à cause de
l'inexistence d'une bibliographie propre aux espèces africaines. Au
terme de ces travaux, nous pouvons affirmer que :
ü le ballonnement d'abdomen et la diarrhée sont
les principaux signes dans les élevages cunicoles du
sud-Bénin.
ü les principales lésions chez les lapins morts de
maladies sont :
· la congestion du poumon, du foie, du l'intestin et de
la trachée ;
· la dégénérescence du
foie ;
· la présence de gaz dans le caecum à
contenu diarrhéique ;
· un contenu diarrhéique de l'intestin ;
· un écoulement sanguinolent.
ü les principaux microorganismes rencontrés dans
les élevages cunicoles sont Escherichia coli suivi dans une
moindre fréquence de Clostridium spp et d'Enterobacter
spp ;
ü pendant que les lésions d'organes et les
infections bactériennes varient en fonction de l'âge, ils ne le
sont pas en fonction du sexe.
En considérant les résultats de cette
étude, nous suggérons que :
v les travaux soient poursuivis pour identifier le
sérogroupe des souches d'Escherichia coli présentes dans
les élevages cunicoles du sud-Bénin ;
v les travaux soient menés sur des lapins indemnes de
coccidiose afin d'évaluer le rôle entéropathogène
des souches d' Escherichia
coli identifiées et de déterminer
à quelle dose ces derniers sont pathogènes ;
v après l'identification des souches pathogènes,
qu'un antibiogramme soit fait pour découvrir les antibiotiques les plus
efficaces pour lutter contre les souches d'Escherichia coli
afin de réduire la mortalité dans les élevages
cunicoles ;
v une bonne hygiène soit pratiquée dans les
élevages ;
v la transition alimentaire lors du sevrage soit faite de
façon progressive.
REFERENCES
BIBLIOGRAPHIQUES
1. Barone R., Pavaux C., Blin P.C., Cuq P.,
1973 : Atlas d'anatomie du lapin. Masson éditeur, Paris,
220 p.
2. BOUCHEUR S., NUOAILLE L., 2002 :
Maladies des lapins 2eme Edition France Agricole, Paris, 271p.
3. CAMGUILHEM R., 1985 : Isolement d'une
souche d'Escherichia coli (sérogroupe O103) responsable
d'entérite colibacillaire du lapin en engraissement. Mise en
évidence de son pouvoir pathogène. Revue Méd.,
136, 61- 67.
4. COLIN et LEBAS., 1985 : Le lapin dans
le monde Edition Association Française des Cuniculteurs, Paris,
287p.
5. COWAN and STEEL'S, 1993 : Manual for
the Identification of Medical Bacteria. Third Edition, Cambridge University
Press, 331p.
6. DJAGO Y., KPODEKON M., 2000 : Le
guide pratique de l'éleveur de lapin en Afrique de l'Ouest, Imprimerie
2000, Cotonou, 106p.
7. GRASSE P. P., 1949 : Traité de
Zoologie, Anatomie, Systématique, Biologie : Ed. Masson et Cie,
Paris, 979p.
8. GUIRAUD J., GALZY P., 1980 :
L'analyse microbiologique dans les industries alimentaires. Collection
Génie alimentaire. Editions Usine Nouvelle, Paris, 63p
9. HULET S., 2003 : Point sur la
filière cunicole au Bénin : perspectives d'avenir. Rapport
de troisième de graduation agronomie, Option agronomie des
régions chaudes, Ulg, 72p
10. KENOUKON C. 2005 : Répertoire
actualisé des éleveurs.-Cotonou : A. Be. C., 26p.
11. KPODEKON M., 1988(a) :
Hygiène et pathologies dans les élevages cunicoles du
Bénin. In: Proceeding of the 4thcongres of the word
Rabbit Science Association. Budapest, Hungary, October 10-14, 498-511
12. KPODEKON M., 1988(b) : Le point sur
l'élevage du lapin en République Populaire du Bénin.
Perspectives d'avenir. Cuni-Sciences 4, 15-26
13. KPODEKON M., TOMAGNIMENA P.,
1992 : Acceptabilité de la viande du lapin en
république du Bénin. Bulletin d'information du réseau
de recherche et développement cunicole en Afrique, 1, 15-21
14. LEBAS F., COUDERT P., ROUVIER R., ROCHAMBEAU
de H., 1984 : Le lapin élevage et pathologie, Edition
FAO, Rome, 298p
15. LEBAS F., COUDERT P., DE ROCHAMBEAU H.,
THÉBAULT R.G., 1996 : Le Lapin, Élevage et
Pathologie (nouvelle édition révisée). FAO éditeur,
Rome, 227 p
16. LICOIS D., COUDERT P., GUILLOT J. F., RENAULT
L. : Diarrhée expérimentale du lapin : Etude
de la pathologie due à des coccidioses intestinales (E.
intestinalis) et des E. Coli. IIIe journée de
la recherche cunicole INRA-ITAVI, 1982, Ed. ITAVI Paris, communication N°
27
17. PILET C., BOURDON L. J., TOMA B., MARCHAL N.,
BALBASTRE C., 1981 : Bactériologie médicale et
vétérinaire. DOIN Editeur -Paris, 437p
18. THOTO J. M., 2006 : Utilisation de
la Robénidine (cyscostat ND66G) en qualité d'addition
anticoccidien dans l'aliment : effet sur la croissance et le degré
d'infestation des lapins à l'engraissement. Thèse : Doctorat
en Médecine Vétérinaire, Dakar, 63p
19. YAOU B. I., 2007 : Microbiologie
générale Editeur : Imprimerie IPI, 168p
1. ANNEXES
Annexe 1 : Matériel
Pour l'autopsie, nous avons utilisé :
- une paire de ciseaux pour la dissection ;
- un plateau pour servir de bac d'autopsie ;
- les gants pour la protection des mains ;
- une pince anatomique pour servir de tenaille lors de la
dissection.
Pour l'identification des différentes bactéries
nous avons utilisé :
- Une paire de ciseaux et une pince anatomique
stérilisées pour les prélèvements d'organes
lésés ;
- des écouvillons stériles pour les
prélèvements liquides ;
- un bec Bunsen pour assurer un champ stérile lors des
manipulations microbiologiques ;
- un microscope photonique pour l'observation des
germes ;
- une étuve pour l'incubation des cultures ;
- un bain marie pour l'homogénéisation et la
stérilisation des milieux de culture ;
- un autoclave pour la stérilisation du
matériel et des milieux de culture ;
- une balance de précision pour les différents
pesés ;
- des boites de pétrie, des tubes à essaie, des
portoirs, des paniers, des pipettes Pasteur, des lames porte objets, une anse
de platine ;
- des milieux de culture (électifs et
sélectifs), d'isolement et d'identification des germes ;
- le papier acétate de plomb, l'huile de paraffine et
les réactifs comme H2O2, bandelette d'oxydase et
le milieu Kovac.
Annexe 2 : Fiches d'enquête et
d'autopsie
Fiche d'enquête
IDENTIFICATION DE L'ÉLEVAGE ET DES
ENQUÊTEURS
Nom du propriétaire :
Localité :
Date de l'enquête :
Nom des enquêteurs :
CARACTÉRISTIQUES DE
L'ÉLEVAGE
Type d'élevage
Au sol En cages Autres
(préciser)
Type de logement
Traditionnel Amélioré
Autres (préciser)
Effectifs
|
Effectif
|
Observations
|
|
Reproductrices
|
|
|
|
Reproducteurs
|
|
|
|
Lapereaux à l'engrais
|
|
|
|
Total
|
|
|
Hygiène et soins
Habitat et matériel
Le logement est-il bien entretenu ? Oui Non
Si oui, fréquence du nettoyage
..........................................
Le matériel est-il bien entretenu ? Oui
Non
Si oui, fréquence du nettoyage
..........................................
Les désinfectants sont-ils utilisés ? Oui
Non
Si oui, fréquence du nettoyage
..........................................
Animaux
Les animaux tombent-ils malades ? Oui
Non
Quels sont les signes souvent observés ?
...........................................
......................................................................................................
Quel est le nombre de malades en 2006 ?
........................................
Quel est le nombre de morts en 2006 ?
...........................................
En cas de maladies les soins sont-ils accordés aux
animaux ?
Oui Non
......................................................................................................
Si oui, quels sont les produits souvent utilisés ?
..............................
Compte rendu d'autopsie
N° d'enregistrement.............
PROPRIÉTAIRE
Adresse :
Boîte postale : Ville :
VÉTÉRINAIRE :
IDENTIFICATION DE L'ANIMAL :
COMMÉMORATIFS :
EXAMEN DE L'ANIMAL
- Etat général (embonpoint, téguments,
orifices et muqueuses) :
- Ouverture des grandes cavités :
Ø Appareil digestif :
Ø Appareil respiratoire :
Ø Appareil cardiovasculaire :
Ø Appareil uro-génital :
Ø S.R.H :
- Prélèvements effectués en vue des
examens
ü Bactériologiques :
.....................................................................
ü Histologiques :
.........................................................................
ü Parasitologiques :
.....................................................................
ü Toxicologiques :
.......................................................................
CONCLUSION :
Date : Signature :
Annexe 3 : Milieux
utilisés
- Gélose enrichie aux extraits de levure (G.E) :
c'est un milieu d'enrichissement et d'isolement qui permet la croissance des
diverses colonies pures.
- Bouillon enrichie aux extraits de levure (B.E) : c'est
un milieu de culture et d'isolement qui permet la croissance de divers
germes.
- Milieu de Chapman : c'est un milieu sélectif
pour la culture des staphylocoques mais exceptionnellement d'autres coques
peuvent y être cultivés sans virer le milieu.
- Milieu Mac-Conkey : c'est le milieu sélectif des
bacilles gram négatifs
Annexe 4 : Tests
d'identification
Coloration de Gram
C'est la coloration de base qui permet de distinguer les
bactéries Gram positifs en violet des bactéries Gram
négatifs en rose.
Technique
- Coloration par le violet de gentiane ;
· Recouvrir totalement la lame du violet de
gentiane ;
· Laisser agir le violet pendant une minute.
- Mordançage
· Rejeter ensuite le violet en l'entraînant avec
la solution de Lugol ;
· Laisser pendant quelques secondes puis le renouveler
(le temps de mordançage est égal à une minute).
- Décoloration par l'alcool
C'est le temps le plus délicat de la coloration.
Elle consiste à :
· laver la lame à l'alcool jusqu'à ce que
le liquide qui tombe de l'étalement devienne incolore ;
· Rincer immédiatement à l'eau.
- Recoloration à la fuchsine
· Couvrir la lame de la fuchsine pendant 10 à 20
secondes et rincer à l'eau.
- Séchage et observation
· Sécher délicatement la lame recouverte
avec du papier buvard
Recherche de mobilité
La mobilité est recherchée en
émulsionnant une colonie pure dans une goutte d'eau distillée
déposée sur une lame propre et recouverte d'une lamelle puis
observée au microscope à l'objectif 40.
Recherche de la catalase
La recherche de la catalase consiste à
émulsionner dans une goutte d'eau oxygénée
déposée sur une lame propre, une colonie pure. La réaction
est positive lorsqu'il y a effervescence.
Recherche de l'oxydase
L'oxydase est effectuée avec un stick sur lequel on
dépose une colonie pure. L'oxydase est positive lorsque le stick prend
une couleur bleu-violet.
ANNEXE 5 : Caractères
biochimiques de bacilles identifiés
|
Caractères biochimiques
|
BACILLES
|
|
[I]
|
[III]
|
[IV]
|
[V]
|
[VI]
|
[VII]
|
[VIII]
|
[IX]
|
[X]
|
[XI]
|
[XII]
|
[XIII]
|
[XV]
|
|
Gram
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
+
|
-
|
-
|
|
Mobilité
|
+ (-)
|
+
|
+
|
+
|
+ (-)
|
-
|
-
|
-
|
-
|
+
|
+
|
-
|
+ (-)
|
|
Catalase
|
+
|
+
|
+
|
+
|
+
|
+
|
+
|
+
|
+
|
+
|
+
|
+
|
+
|
|
Oxydase
|
-
|
-
|
-
|
+
|
-
|
-
|
+
|
+
|
+
|
-
|
-
|
-
|
-
|
|
Urée
|
-
|
+,-
|
d
|
+
|
+
|
-
|
-
|
-
|
+
|
-
|
-
|
+
|
-
|
|
Indole
|
+
|
-
|
-
|
nt
|
-
|
-
|
+
|
+
|
+
|
+
|
-
|
-
|
-
|
|
H2S
|
-
|
-
|
+,-
|
nt
|
+
|
-
|
-
|
-
|
-
|
+
|
nt
|
-
|
-
|
|
Glucose (gaz)
|
+
|
+
|
+
|
+
|
+
|
-
|
+
|
+
|
+
|
+
|
+
|
+
|
-
|
|
Lactose
|
+
|
v
|
d
|
-
|
-
|
-
|
-
|
+
|
+
|
-
|
nt
|
+
|
-
|
|
Maltose
|
+
|
+
|
+
|
-
|
-
|
-
|
-
|
+
|
+
|
+
|
nt
|
+
|
+
|
|
Mannitol
|
+
|
+
|
+
|
+
|
-
|
-
|
+
|
+
|
-
|
-
|
+
|
+
|
+
|
|
Sorbitol
|
+
|
+,-
|
+
|
nt
|
-
|
d
|
d
|
+
|
-
|
-
|
nt
|
+
|
-
|
|
Inositol
|
-
|
v
|
-
|
nt
|
-
|
nt
|
nt
|
nt
|
nt
|
nt
|
nt
|
nt
|
nt
|
| 


