CERTIFICATION
Je
certifie que la présente étude a été conduite par
LAWSON Vidégla S. Armel Joël au Département
de Production Végétale Option Sciences et Techniques de
Production Végétale (DPV/STPV) de la Faculté d'Agronomie
de l'Université de Parakou (FA/ UP).
Directeur de
Thèse
Dr. Ir.
Emmanuel SEKLOKA
DEDICACE
A toi cher Père Alfred K.
LAWSON
A toi chère Mère
Léontine A. KPEHOUNTON
A mes Frères Mariano et Oscar, et
à ma Soeur Lionelle
A mes Feux Grands Pères Joseph et
Théophile
A toi ma chérie Linda
AYEDADJOU
REMERCIEMENTS
La reconnaissance est une plante éminemment africaine.
Elle dit notre être et nous fait entrer dans la dynamique du vrai
développement. En nous permettant de conduire à terme ces essais,
vous avez balisé la voie à ce qui doit primer dans notre
formation intellectuelle. Nous avons apprécié cet engagement dont
vous avez fait montre en vous rendant disponible. C'est l'heure pour nous de
vous traduire en paroles de remerciement ce que tout notre être dit clame
et proclame. Ainsi, toute notre gratitude :
Au Dr. Ir Emmanuel SEKLOKA qui non seulement a supporté
nos caprices mais aussi a constamment oeuvré pour l'aboutissement de ce
travail et dont la riche expérimentation dans le domaine de la recherche
cotonnière nous a servi tout au long de nos travaux.
Au professeur Marc Abel AYEDOUN, Secrétaire
général de l'Université de Parakou pour ses sages conseils
et surtout pour son soutien.
A mes géniteurs Alfred LAWSON et Léontine
KPEHOUNTON ; que vos jours deviennent des années.
Aux techniciens Timothée HONTON, Eric ARAYE et Cyrille
GBAGUIDI.
Aux ingénieurs Germain FAYALO et Gustave BONNY du
CRA-CF, à la caissière et à tous les autres agents du
centre.
A tous les enseignants de la faculté en particulier
ceux du département de Production Végétale, pour la
qualité de l'enseignement qu'ils nous ont donné.
A mes oncles Herbert Prince AGBODJAN, Siméon
ACCROMBESSI, Maurice LAWSON et Robert GUINNOU pour votre assistance sans
faille.
A mes tantes Madeleine, Béatrice, Clarisse et
Madeleine dont le soutien m'a propulsé, soyez en bénies.
A mes Frères Mariano et Oscar et à ma soeur
Lionelle, que le seigneur nous garde toujours unis.
A mes cousins et cousines Donald, Wilfried, Ange, Delmis,
Joël, Fridolin, Thierry, Delphine, Bénoîte, Christelle,
Déo Gratias et Any.
A tous mes camarades de promotion en particulier ceux du
département.
Aux ingénieurs Haroll KOKOYE, Anique GODJO,
Bénédicte MONWANOU, Serge DANHOUSSI.
A tous mes amis Eric, Lionel, Serge, Marius, Lucas, Christel,
Edwige, Modeste, Raïmath, Lévy, Amal, Ella, Natacha.
A Madame BADOU et son époux.
A tout le groupe liturgique Saint Paul de Banikanni en
particulier les membres du bureau.
A vous tous qui avez donné sans mesure pour qu'advienne
cette oeuvre, que Dieu vous donne à la mesure sans
mesure de vos sacrifices.
TABLE DES MATIERES
CERTIFICATION
I
DEDICACE
II
REMERCIEMENTS
III
TABLE DES MATIERES
V
LISTE DES TABLEAUX
VII
LISTE DES FIGURES
VIII
LISTE DES PHOTOS
IX
LISTE DES ACRONYMES
XI
ABSTRACT
XIII
INTRODUCTION
1
1.1- Connaissance du cotonnier
5
1.1.1 - Classification et Origine des
espèces cultivées
5
1.1.2- Morphologie du plant de cotonnier
5
1.1.3- Physiologie du cotonnier et régime de
reproduction
8
1.1.4- Mode de croissance et développement
de la plante
11
1.1.5- Exigences écologiques du
cotonnier
12
1.1.6 - Cartographie du plant de cotonnier
14
1.2- Les principaux ennemis du
cotonnier
15
1.2.1 - Les adventices
15
1.2.2 Les insectes ravageurs des organes
aériens du plant
16
1.2.3- les ravageurs des racines
22
1.3- Faune utile
22
1.3.1- Les prédateurs
22
1.3.2 - Les parasitoïdes
23
1.4- Maladies et déficience
minérale
23
1.4.1- Maladies
23
1.4.2 Déficience en potassium
24
1.5- Zones de production et
itinéraires de culture du cotonnier
24
1.5.1- Aires de culture
24
1.5.2- Techniques culturales
27
2.1- Problématique et contraintes
abordées
29
2.2- Bilan des travaux
antérieurs
31
2.2.1 Effet de l'écimage sur le
rendement
31
2.2.2- Effet de l'écimage sur les
infestations de chenilles carpophages et les pucerons
32
2.3- Objectifs de l'étude
33
2.4- Hypothèses testées
33
3.1- Matériel utilisé
33
3.2- Site expérimental
35
3.3- Méthodes et dispositif
expérimental
36
3.4- Itinéraire de conduite des
essais
37
3.5- Les données
collectées
38
3.6 - Analyse des données
40
4- RÉSULTATS
41
4.1 - Effet de l'écimage sur la
précocité du cotonnier
41
4.1.1- semis de bonne date à faible
densité (42000 plants/ha)
41
4.1.2- Semis de bonne date à forte
densité (125000 plants/ha)
41
4.1.3- semis tardif à forte densité
(125000 plants/ha)
42
4.2- Effet de l'écimage sur la
charge en capsule
43
4.2.1 - Semis de bonne date à densité
faible
43
4.2.2 - Semis de bonne date à forte
densité
44
4.2.3 - Semis tardif à forte
densité
45
4.3- Effet de l'écimage sur le poids
des capsules
45
4.3.1 - Semis de bonne date à faible
densité
45
4.3.2 - Semis de bonne date à forte
densité
46
4.3.3 - Semis tardif à forte
densité
47
4.4- Effet de l'écimage sur le
volume capsulaire
48
4.5 - Effet de l'écimage sur la
rétention capsulaire du cotonnier
49
4.5.1 - Effet sur la rétention en
première position de branche fructifère
49
4.5.2 - Effet sur la rétention globale des
branches fructifères
50
4.6- Effet sur le rendement en coton
graine
51
4.7- Effet de l'écimage sur la
pression des ravageurs
52
5- DISCUSSION
53
CONCLUSIONS ET RECOMMANDATIONS
56
BIBLIOGRAPHIE
57
LISTE DES TABLEAUX
N° TITRES
0.1 : Principaux pays producteurs de coton
1.1 : Effet de la protection phytosanitaire, de la
distance à la source de pollen (Cameroon, 1987) ou de la densité
(Côte d'Ivoire, 1989) sur le taux d'allogamie
1.2 : Caractéristiques générales du
cycle du cotonnier
1.3 : Exigences du cotonnier et caractéristiques
des différentes zones agro - écologiques du Bénin
3.1 : Généalogie de H279-1
3.2 : Caractéristiques technologiques de la
variété de coton H279-1
4.1 : Effet de l'écimage sur la
précocité en semis de bonne date à faible
densité
4.2 : Effet de l'écimage sur la
précocité en semis de bonne date à forte densité
4.3 : Effet de l'écimage sur la
précocité en semis tardif et à forte densité
4.4 : Effet de l'écimage sur la charge en capsule
en semis de bonne date à faible densité
4.5 : Effet de l'écimage sur la charge en capsule
en semis de bonne date à forte densité
4.6 : Effet de l'écimage sur la charge en capsule
en semis tardif et à forte densité
4.7 : Effet de l'écimage sur le poids des capsules
en semis de bonne date à faible densité
4.8 : Effet de l'écimage sur le poids des capsules
en semis de bonne date à forte densité
4.9 : Effet de l'écimage sur le poids des capsules
en semis tardif à forte densité
4.10 : Effet de l'écimage sur le volume moyen des
capsules à l'état vert
4.11 : Effet de l'écimage sur la rétention
capsulaire en première position de BF
4.12 : Effet de l'écimage sur la rétention
capsulaire des BF
LISTE DES FIGURES
N° TITRES
0.1 : Organigramme des dérivés du
cotonnier
1.1 : Schéma d'un plant de cotonnier
1.2 : Représentation schématique de rameaux
végétatifs et de rameaux fructifères
1.3 : Représentation schématique du rythme
de floraison du cotonnier en conditions de croissance humides et sèches
au Congo - Kinshasa
1.4 : Répartition géographique des
principaux ravageurs du cotonnier au Bénin
1.5 : Zones de végétation du Bénin
avec les ishoyètes et les zones de production du coton
4.1 : Schéma comparatif de l'effet du pruning sur
la précocité d'ouverture des capsules
4.2 : Effet de l'écimage sur le rendement
LISTE DES PHOTOS
N° TITRES
1.1 : Feuilles de Okra et de H279-1
1.2 : Fibre de coton dans une capsule déhiscente
(vue de face et de profil)
1.3 : Chenille et dégâts de Helicoverpa
armigera
1.4 : Chenille et dégâts de Earias
sp.
1.5 : Dégâts de C. leucotreta
1.6 : Dégâts de P. gossypiela
(fleur en rosette)
1.7 : Cycle de reproduction
hétéroécique et colonnie de A. gossypii
1.8 : Dégâts de A. gossypii
1.9 : B. tabaci et ses dégâts
1.10 : Prédateurs de ravageurs du cotonnier
1.11 : Quelques parasitoïdes de ravageurs du
cotonnier
3.1 : Opération d'écimage
3.2 : Fleur du jour du cotonnier
LISTE DES ANNEXES
N° TITRES
1 : Schéma du dispositif
2 : Données pluviométriques
3 : Date d'apparition de la première fleur moyenne
(PFM)
4: Date d'ouverture de la première capsule (OPCM)
5 : Planning des écimages
6 : Tableau de bord des différentes observations
à réaliser
LISTE DES ACRONYMES
AF : Afrique Francophone
ASECNA: Agence Pour la Sécurité de la Navigation
en Afrique et à Madagascar
BF: Branche Fructifère
BV : Branche végétative
CIRAD : Centre de Coopération Internationale en
Recherches Agronomiques pour le Développement
CPE : Centre Permanent d'Expérimentation
CRA-CF: Centre de Recherches Agricoles Coton et Fibre
DDP : Direction Départementale de la
Prospection
HNR: Hauteur d'Entrenoeud (Height to Node Ratio
HT: Hauteur de la Tige principale
ICAC : International Advisory Committe (Comité
Consultatif International du Coton)
INRAB: Institut National de Recherches Agricoles du
Béin
Jal: Jours après levée
Jas: Jours après semis
MAEP: Ministère de l'Agriculture de l'Elevage et de la
Pêche
NAWF: Nombre de Noeuds au dessus de la Dernière Fleur
Blanche
OPCM: Ouverture Première Capsule Moyenne
PIB : Produit Intérieur Brut
PMC : Poids Moyen Capsulaire
PMCgb : Poids Moyen Capsulaire à l'état
vert (green boll)
PMCob : Poids Moyen Capsulaire à l'état
mûr (open boll)
RP1: Rétention en Première Position de BF
ULV : Ultra Low Volume
RESUME
Dans le but de contribuer à la recherche
d'itinéraires techniques permettant d'améliorer la
productivité de la culture cotonnière dans les conditions
pluviales de culture, nous avons étudié à Okpara au cours
de la campagne 2008-2009 les effets de différentes pratiques de taille
du cotonnier sur les performances agronomiques de la variété
vulgarisée H 279-1 dans trois itinéraires techniques : Semis
de juin à 42000 plantes par ha, semis de juin à 125000 plantes
par ha et semis tardif à 125000 plantes par ha. Les observations ont
porté essentiellement sur la phénologie et la floraison,
l'architecture, la rétention et le rendement en coton graine. Nous avons
montré que les écimages à une semaine et à quatre
semaines ont donné les meilleures augmentations de rendements par
rapport aux cotonniers non écimés. L'écimage permet
d'augmenter les taux de rétention capsulaire, d'accroître la
précocité de production des cotonniers, mais n'a pas
forcément d'effets positifs sur l'augmentation du poids et du volume
capsulaire moyen. Nous avons montré que l'ablation des branches
végétatives permet par contre d'obtenir des capsules plus grosses
et plus volumineuses. Cette pratique améliore comme l'écimage la
précocité de production du cotonnier.
Mots clés : Gossypium hirsutum L.,
écimage, branche végétative, rendement,
précocité, rétention capsulaire
.
ABSTRACT
In order to contribute on researches intend to improve cotton
productivity under rainfed cropping conditions, we studied at Okpara during
2008-2009 season the effects of various practices of cotton pruning on
agronomic performance of cultivated variety H 279-1 under tree cropping
systems: June sowing at 42000 plants per ha, June sowing at 125000 plants per
ha and late sowing at 125000 plants/ha. Data collected was primarily about
phenology and flowering habit, architecture, boll retention and yield. We
showed that topping at one week and four weeks gave the best yield increases
compared to cotton not topped, about 100 to 500 kg/ha. Topping makes it
possible to increase boll retention, earliness, but does not have positive
effects on boll weight and boll volume. We showed that vegetative branches
pruning makes it possible to obtain larger and voluminous bolls. This practice
improves, like topping, cotton plant earliness
Key words: Gossypium hirsutum L, topping,
vegetative branch, yield, earliness, boll retention
INTRODUCTION
Le cotonnier représente la plante à fibre la
plus cultivée au monde. Le coton est surtout produit pour sa fibre. Les
utilisations sous forme de tissus ou de tricot, mais aussi de fil et de fibre,
sont nombreuses. La première d'entre elle reste la confection
destinée à l'habillement, qui consomme plus de 50% de la
production mondiale. Viennent ensuite le linge et les articles domestiques
à hauteur de 30% (serviette, draps, couvertures, rideaux) et enfin les
produits industriels (fournitures médicales, bâches, fil,
chaussure...). (Bachelier, 1998).
Bien que principalement destinée à la
production de fibre, la culture cotonnière produit également
différents dérivés (fig 0.1). La valorisation de la graine
de coton est aussi une activité très importante. Les graines
issues de l'égrenage sont valorisées soit sous forme de semence,
soit par une exploitation en huilerie. Cette dernière consomme les
tonnages les plus élevés. Chez G. hirsutum L., les
graines contiennent 20 à 25% d'huile, sous forme d'acide gras
polyinsaturé (acide linoléique et oléique) et
saturés (acide palmitique). Elles sont destinées au marché
des huiles de table, des savons et des produits cosmétiques. De plus,
l'amande de la graine possède une teneur de 20 à 30% de
protéines. Ce taux élevé de protéines permet
d'orienter les tourteaux, issus de l'extraction de l'huile, vers l'alimentation
des ruminants (12% de la production mondiale) et place la farine de cotonnier
au deuxième rang des ressources végétales derrière
le soja (Courtant et al., 1991).
Les principaux pays producteurs que sont la Chine, les USA,
l'Inde, le Pakistan ont assuré eux seuls 68% de la production mondiale
de fibre en 2004 (ICAC, 2005) (Tableau 0.1). La surface emblavée en
coton dans le monde couvre actuellement environ 2,2% des terres arables, soit
plus de 30 millions d'hectares. Sa progression moyenne est de 84000 ha par an
depuis la fin de la seconde guerre mondiale. Pendant cette même
période, le rendement moyen en fibre a été
multiplié par trois, atteignant près de 600 kg/ha en 1991 - 1992,
selon une progression moyenne annuelle de 8 kg/ha. Une relative stagnation du
rendement en coton graine est cependant observée depuis les
années 90. Mais la production mondiale de fibre de coton, qui se situait
à peine à 5 millions dans les années 40 a
dépassé 20 millions de tonnes en 1995-1996 et a atteint 26
millions de tonnes en 2004-2005 (ICAC, 2005 ; Estur, 2006)
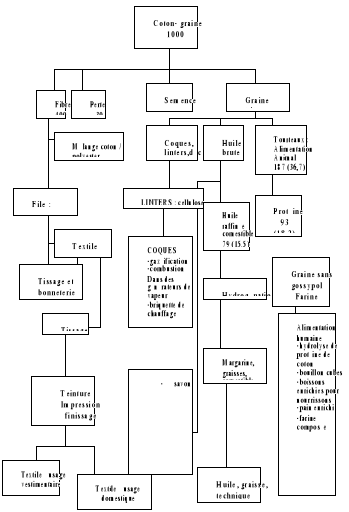 Figure 0.1 : Organigramme des
dérivés du cotonnier Figure 0.1 : Organigramme des
dérivés du cotonnier
Tableau 0.1 : Principaux pays
producteurs de coton
|
Pays
|
Superficie
(×1000ha)
|
Rendement
Kg/ha
|
Production
|
Consommation
|
Importation
|
Exportation
|
|
(×1000
|
tonnes de
|
fibres de
|
coton)
|
|
Chine
|
5650
|
1119
|
6320
|
8200
|
1394
|
7
|
|
USA
|
5284
|
958
|
5062
|
1361
|
7
|
3048
|
|
Inde
|
9300
|
439
|
4080
|
3300
|
150
|
175
|
|
Pakistan
|
3229
|
769
|
2482
|
2300
|
325
|
85
|
|
Brésil
|
1172
|
1124
|
1318
|
935
|
48
|
360
|
|
Afrique francophone(AF)
|
2564
|
443
|
1135
|
28
|
0
|
952
|
|
Monde
|
35757
|
733
|
26204
|
23400
|
7131
|
7653
|
AF : 11 pays de l'Afrique de l'Ouest et du Centre :
Bénin, Burkina Faso, Cameroun, Côte d'Ivoire, Guinée, Mali,
Niger, Rép. Centrafricaine, Sénégal, Tchad, Togo
* : Rendement en fibre à l'hectare
Source : ICAC, 2005
En Afrique et principalement dans les pays francophones
d'Afrique de l'Ouest et du centre, les superficies cotonnières
représentent environ 3% des surfaces cultivées. Le coton
représente en moyenne dans ces pays 15 à 20% des surfaces des
exploitations pratiquant cette culture (Lacape, 1998). D'après les
statistiques d'ICAC (2005), cet ensemble de pays avec plus de 2,5 millions de
tonnes de coton graine et plus de 1000000 de tonnes de fibres produites au
cours de la saison 2004/2005 se place au 6ème rang mondial pour la
production (Estur, 2006). Cette production est exportée à 95% et
ce groupe de pays représente environ 12% des exportations mondiales, et
se place au second rang des exportateurs après les USA (ICAC, 2005).
Dans ces pays, le coton est à la base du développement rural et
contribue considérablement à l'emploi et aux revenus des
populations rurales (Matthès et al., 2005).
Au Bénin, la filière coton constitue pour
plusieurs raisons la source principale de croissance de l'économie
nationale. La production cotonnière s'est accrue ces quinze
dernières années (en moyenne de 6,6% l'an) atteignant même
les 400 000 tonnes en 2001-2002 avant de se stabiliser en dessous de
la barre des 300 000 tonnes ces trois dernières campagnes.
Néanmoins, il demeure le produit le plus important dans
l'économie nationale. Au cours de la période 1990 à 2002,
la production cotonnière de fibre a constamment progressé passant
de 43 000 tonnes à 172000 tonnes ; soit une progression de 300%.
Cette production moyenne annuelle de coton graine estimée à
350000 tonnes représente environ 100 milliards de francs CFA qui sont
versés à plus de 325000 exploitants agricoles, procurant ainsi
des revenus monétaires à environ 3 millions de personnes. Les
exportations de coton participent pour 80% à la constitution des
recettes d'exportation officielle. La filière représente 45% des
rentrées fiscales (hors douane) et contribue en termes de valeur
ajoutée, pour 14% à la formation du PIB national. En 1999, le
coton a représenté 82% des exportations agricoles et 77% des
exportations totales (MAEP, 2001). Sur le plan industriel, le Bénin
possède 18 usines d'égrenage, 5 unités de textile, 3
usines de trituration des graines de coton et une usine de fabrication de coton
hydrophile. Les activités d'égrenage au cours d'une campagne
d'environ six mois génèrent plus de 3500 emplois au plan
national. Le revenu du coton crée par ailleurs des emplois à
travers ses effets multiplicateurs dans le transport, l'artisanat, le commerce
et la construction (Hazard 2003). En milieu rural, plusieurs infrastructures
sociocommunautaires (centres de santé, écoles, routes, puits,
maisons des jeunes et des loisirs, etc.) ont été
réalisées grâce aux revenus procurés par le coton.
Enfin, le coton a servi de tremplin au dynamisme du secteur privé et des
organisations paysannes. C'est fort de tout cela que la filière est
perçue comme un outil stratégique puissant et
privilégié de lutte contre la pauvreté. C'est
également pour cette raison que la recherche est constamment
sollicitée pour contribuer à résoudre les problèmes
de rentabilité de la filière et trouver des solutions pour
améliorer la productivité. Le présent travail s'inscrit
dans cette logique. Le document présente successivement, une revue de
littérature sur le fonctionnement du cotonnier et sa culture, une
justification de la problématique abordée, le bilan des travaux
réalisés sur la technique de taille du cotonnier, les
matériels et méthodes utilisés pour le travail, les
résultats obtenus suivi de discussions, le tout assorti de conclusion et
recommandations.
1.1- Connaissance du
cotonnier
1.1.1 - Classification et
Origine des espèces cultivées
Le cotonnier est une plante dicotylédone
dialypétale de l'ordre des Malvales, de la famille des Malvacées
et de la tribu des hibiscucées. Il appartient au genre
Gossypium dont quatre espèces constituent le groupe des
cotonniers cultivés : deux diploïdes (G.herbaceum L., G.
arboreum L.) et deux tétraploïdes (Gossypium hirsutum L.,
G. barbadense L.). Les deux diploïdes sont peu productives et donnent
un coton court, épais et peu tenace. On ne les retrouve que dans
certaines régions d'agriculture traditionnelle en Asie et en
Afrique ; elles représentent moins de 5% de la production mondiale
de fibre.
G. hirsutum est une espèce
allotétraploide (2n = 4x = 52 chromosomes). Elle représente de
loin l'espèce la plus importante des Gossypium cultivés
fournissant près de 95% de la production mondiale actuelle (Parry,
1982). Elle est plus productive, capable de s'adapter à un grand nombre
de situations. Elle produit des fibres de bonne qualité.
La naissance du genre Gossypium est très
ancienne ; elle remonte à 150 millions d'années,
probablement en Afrique à l'époque du Gondwana, avant la
formation des continents actuels qui a entraîné l'isolement des
populations (Wender et al., 1992). Le cotonnier allo -
tétraploïde cultivé en Afrique équatoriale a pour
origine l'Amérique. Les espèces primitives G. barbadense
et hirsutum ont été importées au
17ème siècle à l'époque de la traite des
esclaves. Au début du 20ème siècle, les colons
européens ont engagé une sélection systématique des
variétés pour obtenir une adaptation écologique. A l'heure
actuelle, la plupart des variétés modernes du cotonnier
appartiennent à G. hirsutum. L'espèce G.
hirsutum aurait comme centre de diversification, la presqu'île de
Yucatan au Guatemala.
1.1.2- Morphologie du plant de
cotonnier
Petit arbuste, atteignant le plus souvent 1 à 1,5m de
haut parfois plus, le cotonnier présente une partie souterraine et une
partie aérienne (fig.1.1).
La partie souterraine du cotonnier comprend une racine
pivotante pourvue de nombreuses ramifications latérales. Ces
ramifications réalisent la fixation de la plante au sol et assurent la
plus grande partie de son alimentation.
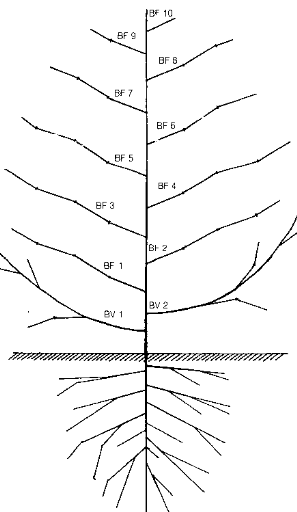
Figure 1.1 :
Schéma d'un plant de cotonnier dans l'ordre où les branches
apparaissent (d'après Parry, 1982).
La partie aérienne comprend :
1- une tige principale érigée, à
croissance terminale et continue (monopode) servant de support au reste de la
plante. De cette tige, partent des rameaux de deux natures : les branches
fructifères (BF) et les branches végétatives (BV)
2- des branches végétatives se
développant à partir des noeuds de base du plant situés au
dessus du noeud cotylédonaire. Ces branches en nombre variable suivant
les variétés et les cultivars sont parfois absentes (Parry,
1982). Elles présentent une croissance continue comme l'axe principal
avec des ramifications secondaires qui peuvent développer des fruits. A
la différence des branches fructifères, les branches
végétatives ne portent pas directement les fruits mais donnent
lieu à des ramifications secondaires qui peuvent produire des fruits
(Davidonis et al., 2004 ; Boquet et Moser., 2003). Leur
développement est initié avant l'apparition des branches
fructifères en général, mais elles peuvent encore
réapparaître plus haut sur le plant en cas de défaillance
de croissance (disparition du méristème de la tige principale du
fait de piqûre d'insectes) ou en cas de reprise de croissance
après la fin d'un cycle (émergence d'une branche
végétative à l'aisselle d'une branche
fructifère).
3- des branches fructifères ou rameaux
sympodiaux : elles se développent à partir de tous les
noeuds du tronc principal situés au dessus des branches
végétatives. Chez la plupart des variétés de G.
hirsutum, elles apparaissent vers les 5ième et
8ième noeuds à partir des cotylédons (Hearn and
Constable, 1984), sur la tige principale, ou dès le premier noeud sur
les branches végétatives. Elles présentent une croissance
discontinue, qui commence par la formation d'un entre - noeud, suivi de la
production d'une feuille et d'une fleur au niveau du méristème
terminal. Par la suite, une structure identique (entre - noeud, feuille, fleur)
se développe à partir du bouton axillaire de la feuille. De la
sorte, plusieurs fleurs peuvent apparaître sur le même rameau
fructifère. En raison de leur croissance sympodique, elles sont
formées de segments successifs. Chaque segment de branche correspond
à une période de croissance. Un bouton floral et une feuille se
développent à l'extrémité du segment. L'allongement
du segment suivant se réalise à partir d'un bourgeon situé
en position latérale, qui détermine l'aspect en « zig - zag
» de la branche fructifère (Parry, 1982) (fig. 1.2). Le nombre et
la longueur des branches fructifères peuvent être variables
suivant les conditions d'environnement ou le génotype de la
variété utilisée.
4- des feuilles : les feuilles du cotonnier apparaissent
à l'aisselle de chaque nouvelle branche et de chaque site
fructifère mis en place. En dehors des feuilles les plus basses
(feuilles cotylédonaires et premières vraies feuilles à
limbe entier), les feuilles du cotonnier sont palmées avec cinq lobes
plus ou moins échancrés ; et sont plus ou moins pileuses
(trichomes). La forme, la taille, la couleur, l'épaisseur sont des
caractéristiques variétales. Des formes particulières de
feuilles aux limbes très découpés se retrouvent dans
certaines variétés et sont appelées Okra ou Super Okra
(Photo 1.1).
5- des glandes terpénoïques chez certaines
variétés, réparties sur toutes les parties
aériennes de la plante (tige, feuilles, graines, capsules). Ces glandes
produisent du gossypol et leur présence peut aider à limiter les
attaques de certains ravageurs.
6- des organes fructifères : qui apparaissent
à un stade plus avancé du développement sur les
ramifications sympodiales à partir de boutons floraux ou «
squares», formes de petites structures vertes pyramidales, qui
évoluent en fleurs, puis en fruits. Ces derniers sont des capsules dont
la forme et la grosseur sont caractéristiques d'un cultivar (Demol et
al. ,1992). Une capsule est de forme ronde ou oblongue, mesure
à maturité 4 à 6cm de long sur 3 à 4cm de
diamètre en son renflement maximum et est divisée en 3 à 5
loges (Photo 1.2). Elle comprend un péricarpe qui constitue la paroi de
l'ovaire. A l'intérieur de celui - ci, se développe une trentaine
de graines sur le tégument desquelles croissent les fibres dont
l'ensemble est appelé coton - graine et constitue le produit de la
récolte de la culture cotonnière.
Différentes caractéristiques morphologiques des
organes reproducteurs (forme, taille, présence ou non de mucron, nombre
de loges carpellaires, type d'ouverture de la capsule, etc.) peuvent servir
à décrire les variétés.
monopodes
ou ramification végétative
sympodes
ou
ramification fructifère
Figure 1.2: Représentation
schématique de rameaux végétatifs et de rameaux
fructifères
  
Photo 1.1: Feuilles de Okra Photo
1.2: Fibre de coton dans une capsule déhiscente
1.1.3- Physiologie du cotonnier
et régime de reproduction
La physiologie du cotonnier répond dans sa
généralité à celle que nous connaissons de
nombreuses dicotylédones avec cependant quelques particularités
originales. Le cotonnier est une plante vivace mais cultivée comme une
culture annuelle. Les variétés cultivées ont alors
conservé de leurs ancêtres sauvages la possibilité de
refleurir après leur premier cycle de fructification. Elles ont une
croissance de type indéterminé et on rencontre sur la même
plante des boutons floraux, des fleurs et des capsules (Photo 1.3) à
tous les âges de développement. La fleur est hermaphrodite et le
mode de reproduction est préférentiellement autogame mais avec
des taux d'allogamie pouvant atteindre 30% dans certaines localités en
fonction de la densité des insectes pollinisateurs (Hau et al.,
1997). L'importance du taux d'allogamie chez le cotonnier dépend de
l'intervention des principaux pollinisateurs, des hyménoptères
parmi lesquels les abeilles (Apis sp.) et les bourdons (Bombus
sp.) sont les plus actifs en Afrique. Tous les facteurs pouvant intervenir
sur leur nombre, leur répartition ou leur efficacité modifient le
taux d'allogamie (Lançon, 1994 ; Lançon et al.,
2000d) : climat, géographie, calage des cycles, protection
phytosanitaire, distance entre plantes et itinéraire technique (Tableau
1.1).
Tableau 1.1: Effet de la protection
phytosanitaire (pyréthrinoïde), de la distance à la source
de pollen (Cameroun, 1987) ou de la densité (Côte d'ivoire, 1989)
sur le taux d'allogamie, d'après Lançon
|
Traitement
|
Dispositif
|
Taux d'allogamie
|
|
Protection hebdomadaire
|
Parcelles de 20 lignes
|
1,6 à 6,3%
|
|
Protection quotidienne
|
Parcelles de 20 lignes
|
0,4 à 5,0%
|
|
Allopollen à 1m
|
Parcelles de 20 lignes
|
5,60%
|
|
Allopollen à 5 m
|
Parcelles de 20 lignes
|
1,60%
|
|
Allopollen à 8 m
|
Parcelles de 20 lignes
|
1,00%
|
|
1000 plants/ha
|
Plants ou lignes isolées
|
10 à 13%
|
|
50000 plants/ha
|
Plants ou lignes isolées
|
2 à 6%
|
 Photo 1.3 : Plant de cotonnier portant
bouton floral, fleur et capsule
Photo 1.3 : Plant de cotonnier portant
bouton floral, fleur et capsule
La floraison chez le cotonnier progresse du bas vers le haut
et de l'intérieur vers l'extérieur de la plante. Il
s'écoule en moyenne 2 à 3 jours entre l'ouverture des deux fleurs
situées à la même position sur deux sympodes successifs et
6 à 9 jours entre deux positions successives d'un même sympode
(fig.1.3). Le rythme de floraison est accéléré par un
climat plus sec et plus chaud et peut être considéré comme
constant pour un climat donné (Demol, 1992).
Un phénomène important chez le cotonnier est la
coulure («shedding ») qui peut être d'origine parasitaire
ou physiologique. Il s'agit de la chute prématurée des organes
fructifères. Le « shedding » peut être aussi
dû à des stress affectant la vie du cotonnier. L'humidité
excessive ou déficitaire, la mauvaise nutrition ou une insuffisante
insolation peuvent être des causes importantes de la chute des organes
fructifères. Le « shedding » parasitaire est
causé par des piqûres d'insectes ou la pénétration
de chenilles dans les organes fructifères. Dans des conditions de
parasitisme particulièrement spectaculaires, le taux de
« shedding » peut atteindre 100% (Demol et al.,
1992). Mais le « shedding » dépend aussi de la
charge du cotonnier en capsules en cours de maturation (Parry, 1992).
Ces particularités du cycle du cotonnier peuvent
être décrites au moyen d'un certain nombre de paramètres
très exploitables par les agriculteurs et les phytotechniciens, les uns
pour la gestion de la culture, les autres pour des fins de recherche.
Gandajika (climat sec)
Bambesa (climat humide)
21 12 3
0 9 18
·
·
18 9
·
·
·
6 15 24
12 21
15
10
10
·
·
8 14
·
·
12 6
·
·
4 10 16
12 6
·
· 4 10 16
·
·
·
21 12 3
14 8 2
14 8 2
·
·
·
0 9 18
0 6 12
·
·
·
·
·
·
0 6 12
·
·
·
Figure 1.3 : Représentation
schématique du rythme de floraison du cotonnier en conditions de
croissance humides et sèches au Congo- Kinshasa. Les intervalles en
jours entre l'ouverture de la première fleur et l'ouverture des autres
fleurs sur des sympodes différents sont indiqués par des chiffres
sur les noeuds.
1.1.4- Mode de croissance et
développement de la plante
Le cotonnier est une plante à croissance continue, ce
qui signifie que les phases végétatives et fructifères ne
sont pas séparées dans le temps, comme chez les
céréales. Son mode de croissance est ainsi comparable à
celui du pois, Pisum sativum ou à celui du haricot,
Phaseolus vulgaris. La croissance végétative se poursuit
pendant que les premiers boutons floraux apparaissent. La mise en place des
fruits sur la plante, provoque un ralentissement progressif de la vigueur
végétative. Au fur et à mesure de leur maturation, les
fruits mobilisent de plus en plus les assimilâts issus de la
photosynthèse, au détriment du développement
végétatif. Celui-ci finit par s'arrêter lorsque la
production du plant est en place et mobilise tous les carbohydrates
synthétisés au niveau des feuilles.
La croissance du cotonnier peut être scindée en
quatre stades (Hesketh et al., 1972 ; Parry, 1982 ;
Mauney,1984) :
· Stade de levée : du semis à
l'étalement des cotylédons (6 à 10 jours dans les
conditions tropicales)
· Stade végétatif : de la plantule
à l'ouverture de la première fleur. Elle dure 40 à 60
jours après levée
· Stade de floraison : du début floraison
à l'arrêt de la croissance (appelé "Cutout"), atteint 80
à 100 jours après levée
· Stade de maturation : du "Cutout à
l'ouverture complète des capsules.
Du semis à la récolte, le cycle dure environ 140
à 180 jours selon les variétés et les conditions
environnementales (Pary, 1982).Les principales caractéristiques
phénologiques du cotonnier sont résumées dans le tableau
1.2.
Tableau 1.2 : Caractéristiques
générales du cycle du cotonnier
|
Phases du cycle
|
Caractéristiques et exigences
|
|
Levée
|
Germination à l'étalement des cotylédons
6 à 12 jours en conditions favorables
Température du sol de 25 à 30°C
Zéro de germination de 14°C
Humidité du sol située 90% de sa capacité
de rétention en eau (CRE)
|
|
Plantule
|
Se termine au stade 3 à 4 feuilles
Durée moyenne de 20 jours en conditions favorables
Température du sol supérieure à
20°C
Température de l'air de 25 à 30°C
Sol suffisamment humide et non saturé
|
|
Préfloraison
|
Du stade plantule à l'apparition du 1er
bouton floral
Durée moyenne de 20 jours
Apparition de branches végétatives et
fructifères
Conditions climatiques et édaphiques
déterminantes
|
|
Floraison
|
Peut durer 40 à 70 jours après la
préfloraison suivie de la fécondation
|
|
Maturation et déhiscence de la capsule
|
Grossissement des capsules, formation des fibres (20 à
25 jours)
Déhiscence des capsules
(20 40 jours en conditions favorables)
|
Source : Parry, (1982)
1.1.5- Exigences
écologiques du cotonnier
Le cotonnier nécessite une saison sèche
terminale bien marquée, indispensable à une bonne ouverture des
capsules et à la récolte. Le climat intertropical de savane
convient donc assez bien de ce point de vue.
La température
La croissance végétative et le
développement des organes reproducteurs chez le cotonnier sont fortement
influencés par la température. La durée des
différentes phases du cycle est généralement
exprimée en degré-jour (DJ). Elle représente la somme des
différences quotidiennes entre la température moyenne et la
température à la quelle le cotonnier arrête sa croissance
(13°C). Elle se calcule selon la formule : ?DJ - ?([(Tmax + Tmin)/2]-
13), avec DJ > 0 ; Tm désignant la température maximale
de la journée et Tmin la température minimale enregistrée
au cours de la même journée. D'après Mémento de
l'agronome (2002), la durée du cycle du cotonnier exprimée en DJ
est comprise entre 1450 et 1600 et se répartit comme ci-après
:
· levée : 35 à 40 DJ ;
· du semis à la première fleur : 530
à 650 DJ ;
· de la première fleur à la première
capsule ouverte : 600 à 750 DJ ;
La température de germination optimale des graines est
de l'ordre de 30°C. Toute levée est impossible en dessous de
15°C. L'environnement thermique le plus favorable pour la culture du
cotonnier varie entre 25° et 30°C pour les températures
diurnes et entre 15 et 20°C pour les températures nocturnes (Demol,
1992). L'exposition du cotonnier à des températures basses (0
à 10°C) provoque chez lui des dégâts appelés
« chilling » (perte de turgescence d'un nombre croissant de
feuilles pouvant aller dans les cas extrêmes jusqu'à la mort de la
plante).Les travaux effectués par Parry (1982) ont rapporté que
la température minimum de croissance est de 13°C et que la
température optimale se situe entre 27 et 32°C.
L'eau
Le système racinaire pivotant du cotonnier lui
confère une bonne résistance à la sécheresse. Ses
besoins en eau varient en fonction de son stade de développement. Les
besoins en eau s'accroissent avec le développement de la plante. Ils
sont plus élevés lorsque le cotonnier porte des boutons floraux
et des fleurs et lorsqu'il forme des capsules. Il faut compter 2 à 3mm
d'eau par jour en début de végétation et 4 à 7 mm
en période de floraison et de formation des capsules. Au moment de la
maturation des capsules, la saturation du sol n'est plus nécessaire et 2
à 3mm d'eau par jour suffisent. L'arrêt total des pluies en
période de déhiscence des capsules et de récolte est la
situation la plus favorable. En théorie, 400 à 500 mm d'eau
devraient suffir pour permettre au cotonnier de réaliser son cycle, mais
en pratique, à cause des diverses pertes, on estime ses besoins moyens
en eau à environ 700mm.
Le déficit hydrique perturbe moins le
développement reproducteur et la croissance des capsules que l'expansion
foliaire, la rétention des organes reproducteurs et la croissance
végétative. Il peut avoir une influence négative sur la
qualité de la fibre (Mémento ,2002).
L'ensoleillement
Le cotonnier est une plante héliophile par excellence.
L'ensoleillement est un facteur primordial de développement de la
culture, surtout au cours de la phase de développement du système
reproducteur : une réduction même légère de
l'ensoleillement a un effet défavorable sur la croissance et la
rétention des organes reproducteurs. L'activité optimale serait
atteinte avec 100000 lux (Parry, 1982). En Afrique, la durée du jour
n'exerce aucune influence sur le démarrage de la floraison du
cotonnier.
Le sol
En même temps qu'il supporte la plante, le sol constitue
le réservoir dans lequel elle puise sa nourriture. Un bon sol pour la
culture cotonnière doit être profond, riche en matière
organique, bien travaillé pour être aéré et
perméable à l'eau et aux racines. Ces sols doivent en outre
être homogènes, et riches en éléments
minéraux majeurs (Azote (N), Potassium (K), Phosphore (P)) ;
secondaires, et oligoéléments (Calcium (Ca), Magnésium
(Mg), Soufre (S), Fer (Fe), Bore (B), Cuivre (Cu), Zinc (Zn) etc.). Le pH
optimum se situe entre 6,0 et 7,0. Le cotonnier est très sensible
à la toxicité d'aluminium et de manganèse. Pour assurer
une bonne production, l'application d'un amendement calcaire est indispensable
dès que le pH est inférieur à 5,0. Le cotonnier
préfère les sols pas trop lourds de type argilo- sableux ou
sablo- argileux. Il ne supporte pas du tout les terres trop humides mais peut
s'accommoder d'un certain niveau de salinité. Toute augmentation de la
concentration en sels au-delà de 5 à 6% se traduit
généralement par une baisse de production. La résistance
à la salinité varie fortement d'une variété
à l'autre. Le cotonnier est particulièrement sensible à la
carence en Bore qui se traduit par des symptômes typiques (apparition
d'anneaux foncés sur le pétiole, nécroses à la
moelle du pétiole, fleurs malformées, plantes naines à
sommet anormal ou « crumple top »
1.1.6 - Cartographie du plant
de cotonnier
La cartographie du cotonnier est un outil qui s'intègre
dans une stratégie plus globale de modélisation de la croissance
et du développement du cotonnier appelée « cotton
monitoring ». Le but est de fournir dans des conditions
environnementales bien définies, des standards aux quels pourront
être comparées des données de
« monitoring » afin de prendre des décisions
concernant la gestion de la culture. La méthode repose sur les mesures
d'un certain nombre de paramètres dont majoritairement :
· La hauteur totale (HT)
· La longueur d'entre- noeud (HNR)
· Le nombre de noeuds au dessus de la dernière
fleur blanche en première position des branches fructifères
(NAWF)
· Le profil de répartition des sites
fructifères
· Le pourcentage de rétention des boutons floraux
ou de fruits.
Ø « Plant mapping » : outil de
prédiction de la production
L'utilisation du plant mapping pour prédire le
comportement d'un cultivar a fait l'objet de nombreuses études ces
dernières années. Elle permet une évaluation
précoce des variétés. Bourland et al.,
(1992) ; Oosthertuis et al. (1994) ont montré que le
potentiel de production de la plante est déjà totalement
installé lorsque le NAWF atteint la valeur 5 (cut out). A ce stade, on
pourrait donc déjà avoir une idée de la production totale.
Hake et Stair (1994) ont mis en évidence une relation positive entre le
NAWF des premiers stades de floraison et le rendement en fibre. Le pourcentage
de rétention capsulaire par noeud et par position est très
corrélé avec le rendement, beaucoup plus que ne l'est le nombre
de capsules par plant (Landivar et Hickey, 1997). La quantité de fleurs
nécessaires pour produire 0,5kg de coton graine serait relativement
constante entre les valeurs 10 et 6 du NAWF, et croîtrait rapidement
à partir de NAWF = 5 (Bourland et al., 1997).
1.2- Les principaux ennemis
du cotonnier
Le cotonnier est l'une des plantes les plus parasitées
au monde. Outre les adventices, on dénombre en Afrique tropicale environ
480 espèces d'insectes, acariens, myriapodes et nématodes qui
vivent aux dépens du cotonnier
1.2.1 - Les adventices
Une adventice est une plante indésirable qui entre en
concurrence avec les plantes cultivées pour les éléments
nutritifs, la lumière, l'eau et l'espace (Deuse et Lavrabre, 1979). Dans
les pays en développement et particulièrement en Afrique, les
pertes de rendement imputables aux adventices sont plus importantes.
Selon Parry (1982), en culture cotonnière, de
nombreuses expériences réalisées dans les conditions
différentes permettent d'estimer des pertes de récolte
jusqu'à 80% lorsque le désherbage est fait dans de très
mauvaises conditions. Tonato (1988) a montré qu'un enherbement pendant
les vingt premiers jours qui suivent le semis entraîne une baisse de
rendement de coton graine jusqu'à 18% et qu'une compétition entre
cotonniers et adventices pendant cinquante jours après semis ou durant
tout leur cycle entraînent respectivement une réduction du
rendement de 13 et de 50%. De ce fait les adventices revêtent une grande
importance. Celles rencontrées sur le site d'expérimentation
selon leur importance sont : Leucas martinensis, Setararia pumila,
Rottboelia exaltata, Commelina benghalensis, Boerhavia diffusa, Celosia
argenta, Ipomea eriocarpa, Digitaria horizontalis, Brachiaria lata.
1.2.2 Les insectes ravageurs
des organes aériens du plant
Chenilles phyllophages
Syllepte derogata (Lepidoptera
Pyralidae)
Les chenilles sont vertes claires, souvent translucides avec
une tête noire brillante. Leur longueur atteint 2 à 3
cm. S. derogata est encore appelé chenille
enrouleuse. Elle s'attaque aux feuilles qu'elle enroule sous forme de cigare,
à l'aide de fils soyeux. L'intérieur de la feuille
enroulée est souillé par de nombreux excréments noirs. Les
attaques de S. derogata sont souvent
localisées dans le champ et peuvent entraîner une
défoliation spectaculaire. Les organophosphorés acaricides sont
les plus fréquemment utilisés. Mais toutes les substances
alternatives recommandées contre Helicoverpa armigera
éliminent aussi cette espèce. Un labour de qualité
détruit les chenilles en diapause.
Spodoptera littoralis
Boisduval (Lepidoptera Noctuidae)
Les chenilles de cette espèce ont une coloration
très variable (brune, jaunâtre ou grise). Elles sont
caractérisées par deux rangées de triangles noirs sur le
dos et une ligne claire de chaque côté. Mais ces triangles peuvent
être présents seulement à l'avant ou à
l'arrière du corps. Les jeunes chenilles naissent à la face
inférieure des feuilles de cotonniers qu'elles rongent. Plus
âgées, elles se dispersent sur les plants dont elles consomment le
feuillage. En cas de fortes attaques, seules les nervures peuvent subsister.
Très vorace, ce ravageur peut aussi attaquer fleurs et capsules. Son
statut de ravageur de feuillage n'est donc pas strict et en cas de fortes
infestations S. littoralis, peut provoquer d'importants
dégâts aux organes fructifères. Les
pyréthrinoïdes sont considérés comme peu efficaces
aux doses usuellement employées ; seuls les organophosphorés
et surtout les régulateurs de croissance sont efficaces contre ce
ravageur.
Anomis flava (Lepidotera -
Noctuidae)
La chenille est vert clair, parfois même vert
jaunâtre. Elle porte cinq lignes blanches très fines sur le dos.
La tête est vert-jaune. Sa taille maximale environ 35 mm. Elle se
déplace d'une manière très caractéristique. Elle ne
s'alimente que du feuillage et son alimentation est essentiellement
limitée aux malvacées. La chrysalide est fixée au
feuillage dans un cocon. Les dégâts des chenilles se
présentent comme des perforations circulaires de 1 à 3 cm de
diamètre dans les feuilles.
Ravageurs des organes fructifères
Ce sont les chenilles carpophages à régime
exocarpique, ou endocarpique et les punaises.
1- Chenilles carpophages à régime
exocarpique
Helicoverpa armigera Hübner
(Lepidoptera, Noctuidae)
H. armigera est le plus
préjudiciable des ravageurs du cotonnier au Bénin.
L'espèce existe dans toutes les zones de culture cotonnière
à l'exception de l'Amérique. La chenille, très mobile,
mesure au dernier stade 3,5 - 4 cm. Elle présente des couleurs
très variables : vert, gris, marron, et est caractérisée
par une tête jaune et deux lignes latérales claires. Les chenilles
néonates consomment brièvement du feuillage juste après
leur éclosion. Elles se développent ensuite en consommant tous
les autres types d'organes de reproduction : boutons floraux, fleurs et
capsules. La larve est donc très vorace et une chenille consomme
plusieurs de ces organes pour compléter son cycle. Les organes
attaqués présentent un trou au contour circulaire très net
de 4 mm de diamètre. Les chenilles en consomment l'intérieur et
rejettent d'abondants excréments à l'extérieur. Les jeunes
organes tombent. Ces dégâts peuvent être très
importants et dans certains cas, la chenille peut attaquer les jeunes feuilles
et rameaux. Helicoverpa parasite aussi le maïs, le sorgho, la
tomate, le gombo et le tabac...Peu d'insecticides sont vraiment efficaces
contre ce ravageur qui est devenu résistant au
pyréthrinoïdes au Bénin depuis 1998. Le Tiham et d'autres
molécules comme l'indoxacarbe, le profénofos, le spinoscide ou
certains régulateurs de croissance sont cependant actifs.
  
Photo 1.4 : Chenille de H. armigera
Dégâts de Helicoverpa armigera
Earias sp. (Lepidoptera -
Noctuidae)
La chenille de forme trapue est facile à
reconnaître, car elle porte de nombreuses épines : c'est la
chenille épineuse. Elle attaque les jeunes plants en les écimant.
La chrysalide est formée dans un cocon de couleur crème-ivoire
fixé sur les tiges. Ces espèces consomment diverses plantes
proches des cotonniers. Les trous d'entrée sont assez grands et bien
visibles. Elle cause également des dégâts sur boutons
floraux, fleurs et capsules. Deux espèces se rencontrent au Bénin
: E. insulana surtout dans le nord et E. biplaga dans le
reste du pays.
 
Photo 1.5: Earias sp
Dégâts de Earias sp
Diparopsis watersi Roth (Lepidoptera
Gelechiidae)
La chenille jaunâtre, devient ensuite vert pâle
avec des traits transversaux rouges plus rapprochés vers la tête.
Elle atteint à son complet développement 2,5 à 3 cm. Elle
attaque en perforant boutons floraux, fleurs et capsules, qui restent parfois
suspendus au plant par des fils de soie. Ce dégât typique est
caractéristique de la présence de D.watersi dans la
culture. Devenue rare au Bénin dans les années 80, cette
espèce devient de plus en plus fréquente.
2- Chenilles carpophages à régime
endocarpique
Cryptophlebia leucotreta Meyrick
(LepidopteraTortricidae)
La chenille gris pâle, mesure 1,5 cm à son
complet développement. On peut la confondre avec le ver rose, seul
l'emploi d'une loupe permet de distinguer les deux espèces. Comme le ver
rose, elle pénètre dans l'organe fructifère dès son
éclosion et peut détruire plusieurs loges de la capsule
attaquée. Le coton graine est fortement déprécié
(quartiers d'oranges) et devient souvent non marchand.
Cryptophlebia est très polyphage. Il attaque le
maïs, les agrumes, le goyavier, l'avocatier, le gombo, ... La lutte
chimique repose à nouveau essentiellement sur l'emploi des
pyréthrinoïdes pour leur bonne action de contact contre les
adultes. L'association maïs - coton favorise le passage d'un hôte
à l'autre et nuit à la culture cotonnière.


![]()
Photo 1.6: Dégâts de
Cryptophlebia
Pectinophora gossypiella
(Lepidoptera Gelechiidae)
Connue sous le nom de `ver rose', la chenille présente
des segments marqués de bandes et traits transversaux rose sombre
d'où son nom. Elle mesure 1 à 1,5 cm à son complet
développement. P. gossypiella est confondue
avec Cryptophlebia. Elle attaque les fleurs et provoque un
symptôme spécifique : `fleur en rosette'. Comme
Cryptophlebia, elle pénètre directement dans la capsule
et se nourrit préférentiellement des graines. Les
dégâts sont suivis de pourritures secondaires. Le coton graine est
souillé, fortement déprécié et devient difficile
à vendre. Pectinophora ne vit que sur des plantes de la
même famille que le cotonnier. La lutte chimique vise essentiellement les
adultes, seul stade mobile extérieur.
 
Photo 1.7: Dégâts dus à
Pectinophora (Platyedra) gossypiella
3- Punaises
Helopeltis schoutedeni Reuter
(Heteroptera - Miridae)
C'est une punaise de forme allongée, de coloration
jaune orange ou rouge vif. Elle attaque les feuilles, rameaux, tiges et
capsules, avec production de chancres bruns ou noirs. En cas d'attaques
sévères, les feuilles sont gaufrées, craquelées
avec un aspect de `griffes'. La croissance de la plante est ralentie. Sur
capsules, le dégât se présente comme une pustule arrondie
et sombre. Sur les tiges, les chancres sont allongés et l'écorce
se craquelle. Les plants affaiblis produisent moins de fleurs et retiennent
moins bien les organes fructifères qui tombent, et forment de petites
capsules.
Dysdercus völkeris Schmidt
(Heteroptera - Pyrrochoridae)
Grosse punaise de 1 à 1,5 cm, rouge et noir qui vit en
colonie et dont les larves sont rouge vif. Elle pique les capsules vertes ou
celles ouvertes pour se nourrir de graines. Elle déprécie la
valeur germinative des semences et la fibre qu'elle colore. Des excroissances
typiques des piqûres de punaises apparaissent dans les capsules. Les
Dysdercus se développent essentiellement sur les plantes de la
famille du cotonnier et sur celles de la famille du kapokier et du baobab dont
la présence favorise leur pullulation. Cependant, ils peuvent aussi
effectuer leur cycle sur le sorgho et le maïs.
Coleopteres et Altises
Nisotra sp et Podagrica
sp
Ces petits insectes très mobiles ont plusieurs
couleurs. Ils font de nombreux trous dans les feuilles des jeunes cotonniers
sans glandes à gossypol (glandless). Les
dégâts sont surtout dangereux sur jeune plantule.
Aphis gossypii Glover (Homoptera
Aphididae)
Ils vivent essentiellement sur la face inférieure des
feuilles mais peuvent aussi coloniser d'autres parties vertes de la plante.
Ils se reproduisent très vite et sont favorisés par un temps
chaud et sec. Ils sont souvent en colonies où les individus peuvent
être jaune, vert jaune ou vert noir avec ou sans ailes. Ils s'alimentent
en suçant la sève des plants dans lesquels ils injectent leur
salive. Ceci provoque une crispation des feuilles qui se gaufrent, le bord se
recourbant vers le bas. On les rencontre sur cotonnier en début de cycle
sur jeunes plantules où ils appètent bien les jeunes feuilles du
bourgeon terminal (Discon 1986 et Ekulolé 1989), puis en fin de cycle
sur cotonniers âgés à l'ouverture des capsules. Sur jeunes
plantules les dégâts faits au feuillage retardent et limitent le
développement des plants. Les déchets qui sont des substances
sucrées (miellat) tombent sur les feuilles et la fibre. La fibre ainsi
souillée `coton collant', brille et peut, à cause de la
présence de champignon devenir noir : c'est la fumagine.
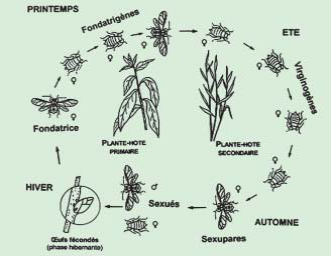 
Photo 1.8 : Cycle de reproduction
hétéroécique (dessin C. Villemant)
et colonie de A. gossypii
  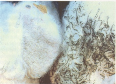
Photo 1.9 : Dégâts de
Aphis gossypii (coton collant/
souillé)
Bemisia tabaci (Homoptera
Aleyrodidae)
Les adultes sont de touts petits insectes avec deux paires
d'ailes blanches. Ils sont très mobiles et volent autour des plants
lorsqu'ils sont dérangés. Les larves ont une forme ovoïde,
aplatie et sont vertes lorsqu'elles sont jeunes. Les plus âgées
sont jaunâtres. Elles sont fixées à la face
inférieure des feuilles. De fortes populations provoquent un
jaunissement des feuilles et perturbent le développement des plants.
Comme les pucerons, ils produisent aussi du miellat qui souille le coton des
capsules ouvertes. Ce ravageur est aussi très polyphage, on le trouve
donc sur de nombreuses autres plantes cultivées en particulier des
cultures maraîchères comme la tomate.
  
Photo 1.10 : Mouches blanches
(coton souillé par B. tabaci)
1.2.3- les ravageurs des
racines
Syagrus calcaratus F. (Coleoptera chrysomelidae)
Petit coléoptère bleu-noir brillant dont le
thorax et la base des pattes sont orange fauve. Les larves de Syagrus
calcaratus vivent dans le sol où elles s'alimentent sur les
racines qu'elles décortiquent. Cette consommation des racines provoque
un flétrissement des plants. Les adultes consomment le feuillage dans
lequel ils provoquent des perforations de forme allongée.
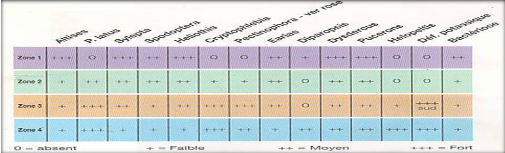
Figure 1.4 : Répartition
géographique des principaux ravageurs du cotonnier au Benin
Source : Fiche Technique :
reconnaissance pratique des ravageurs (CRA-CF)
1.3- Faune utile
1.3.1- Les
prédateurs
Les prédateurs sont les espèces qui consomment
leur proie en la tuant immédiatement, ce sont les espèces utiles
les plus visibles. Il s'agit des chrysopes, syrphes et coccinelles qui
consomment des pucerons, des aleurodes et accessoirement des oeufs de
papillons. Leur utilisation entre dans le cadre de la lutte biologique.
   
Photo 1.11 : Quelques prédateurs
de ravageurs du cotonnier
1.3.2 - Les
parasitoïdes
Les parasitoïdes sont aussi des insectes utiles comme les
prédateurs, mais ils sont généralement beaucoup plus
petits et moins visibles. Ils sont cependant présents et aident à
protéger les champs. Ils ne tuent pas immédiatement leur
hôte mais s'y développent lentement. Ils sont appelés des
« amis de l'agriculture »
   
Photo 1.12 : Quelques parasitoïdes
de ravageurs du cotonnier
1.4- Maladies et
déficience minérale
1.4.1- Maladies
Les agents pathogènes responsables des maladies du
cotonnier peuvent être des champignons, des bactéries, des virus
ou des mycoplasmes.
a) Fonte de Semis
Plusieurs maladies provoquent ce que l'on appelle fonte de
semis c'est-à-dire qu'elles induisent la pourriture des graines en cours
de germination, la nécrose des jeunes racines, ou une pourriture du
collet des plantules. Les principaux agents pathogènes qui sont
impliqués dans la fonte de semis du cotonnier peuvent être
portés par les graines elles - mêmes ou sont déjà
présents dans le sol au moment du semis. Les agents portés par
les graines sont les champignons : Colletotrichum
gossypii (infection uniquement externe) et Fusarium
oxysporum f .sp. vasinfectum (infection
externe et interne) et la bactérie Xamthomonas campestris
pv. Malvacearum infection externe et interne). Les infections
fongiques externes peuvent être éliminées par un traitement
fongicide ou par le traitement à l'acide sulfurique utilisé lors
du délintage dans plusieurs pays ; ce dernier élimine
également les infections bactériennes externes. Les principaux
champignons pathogènes présents dans le sol sont Rhizoctonia
solani, Pythium spp., Sclerotium rolfsii et Macrophomina
phaseolina. D'autres champignons peuvent également être
responsables de pourridiés. Il s'agit de formes Lignosus et
d'Armillaria mellea dont les infections se manifestent le plus souvent
lorsque le cotonnier est cultivé après le manioc et sur des
parcelles récemment déforestées.
b) Bactériose
Elle est la maladie la plus répandue
sur cotonnier au Bénin (Gaborel, 1987). Son importance économique
est variable. Les attaques portent sur tous les organes aériens,
(feuilles, tiges, branches, capsules, etc....) du début à la fin
du cycle. Les symptômes foliaires sont des taches anguleuses et
huileuses, ceux sur tiges des chancres, puis des pourritures sur capsules.
1.4.2 Déficience en
potassium
Cette déficience apparaît surtout sur la terre de
barre, en particulier dans le Sud du Zou et dans les départements
côtiers (Garborel, 1987). Les premières. On la reconnaît par
:
- la présence des taches jaunâtres entre les
nervures des feuilles dont les bords prennent une couleur brune.
- à un stade plus avancé, les feuilles se
dessèchent complètement mais restent accrochées comme des
« chauves-souris » aux plants.
1.5- Zones de production et
itinéraires de culture du cotonnier
1.5.1- Aires de culture
La culture cotonnière est répartie sur les cinq
continents, entre 45° de latitude Nord et 30° de latitude Sud
(Matthews 1989). Actuellement, le cotonnier est cultivé dans toutes les
zones suffisamment chaudes du globe. Les limites extrêmes de son aire de
culture vont de la Bulgarie, de l'Ouzébékistan et de la Chine au
Nord (plus ou moins 40° de latitude nord) à la partie
septentrionale de l'Argentine et de l'Australie au Sud (plus ou moins 35°
de latitude sud).
En Afrique, la culture du coton est pratiquée dans
presque toutes les régions de savanes Soudano- guinéennes et
soudaniennes. Elle se pratique également dans des zones plus
sèches (Afrique du sud, Algérie, Egypte, Maroc, Soudan...)
où elle nécessite l'apport d'irrigation. Aussi, retrouve t - on
la culture du coton en Afrique de l'Ouest en général, et au
Bénin en particulier. Les principales zones productrices au Bénin
se situent dans la zone intertropicale entre 6°30' et 12°30' latitude
nord. Elles appartiennent par conséquent au domaine des climats chauds
et humides. Compte tenu de l'allongement du Bénin en latitude, la saison
pluvieuse s'installe progressivement du Sud vers le Nord ; la saison
sèche, commence plutôt au Nord et dure longtemps dans cette
région. Ainsi donc, le Bénin est divisé en quatre zones de
production cotonnière auxquelles correspondent des
caractéristiques agro écologiques différentes (Mathess et
al, 2005) (fig 1.5).
La zone Nord correspond aux départements de l'Alibori
et de l'Atacora. On y rencontre un climat tropical sahélo- soudanien
avec une saison pluvieuse et une saison sèche. La
végétation est parsemée d'arbustes et de petites
herbes ; et le sol est du type ferrugineux.
La zone Nord - centre couvrant les départements du
Borgou et de la Donga. Elle est caractérisée aussi par un climat
tropical semi aride avec l'alternance d'une saison pluvieuse et d'une
saison sèche d'importance plus ou moins égales. La
végétation est parsemée d'arbres (karité,
néré, fromager etc.) ; le sol est du type ferrugineux.
La zone Centre représentée par les
départements de Zou et des Collines a un climat tropical humide
La zone Sud couvrant les départements de
l'Ouémé, du Plateau, du Couffo et du Mono est
caractérisée par un climat tropical humide ou guinéen avec
alternance de deux saisons pluvieuses et deux saisons sèches.
En général, le climat du Bénin est bien
approprié pour la production pluviale du coton avec une
précipitation annuelle entre 900 et 1300 mm (Ascecna Kandi) et une
température moyenne autour de 28°C. La partie du sud à
proximité de l'Océan Atlantique est peu propice au
développement du coton parce que l'humidité relative de l'air y
est trop élevée. Ceci cause un développement excessif de
la phase végétative sans formation de capsules (Franke 1976,
Mémento de l'Agronome). L'harmattan, vent froid et sec souffrant au Nord
est responsable de la baisse de l'humidité relative de l'air. IL
favorise l'ouverture des capsules en fin de cycle.
Le tableau 1.3 illustre les caractéristiques des
différentes zones agro écologiques du Bénin et les
exigences du cotonnier.
Tableau 1.3: Exigences du cotonnier et les
caractéristiques des différentes zones agro écologiques du
Bénin
|
Facteurs
Climatiques et écologiques
|
Exigences Nord Nord centre Centre
Sud
du cotonnier
|
|
Température optimale en °C
|
26-28 24,9 - 32,5 24,9 - 32,5 25 - 30
25 - 28
|
|
Pluviométrie
en mm
|
> 700 900 - 1100 1100 - 1300 851 - 1491
900 - 1200
|
|
Saison sèche bien marquée
|
une saison une saison une saison 2 saisons
2 saisons
sèche bien sèche
sèche sèches sèches
marquée
inégales inégales
|
|
Sols
|
limon argilo argilo argilo
argilo argilo
sableux ou sableux sableux sableux
sableux
sablo argileux
lessivé ferralitiques
|
|
Ensoleillement en heures journalières
|
> 12 > 12 > 12
> 12 > 12
|
Sources: MAEP/DDP (2000) ;
Mémento de l'agronome, 1993 ; Franke (1976) ; ASECNA -
Kandi
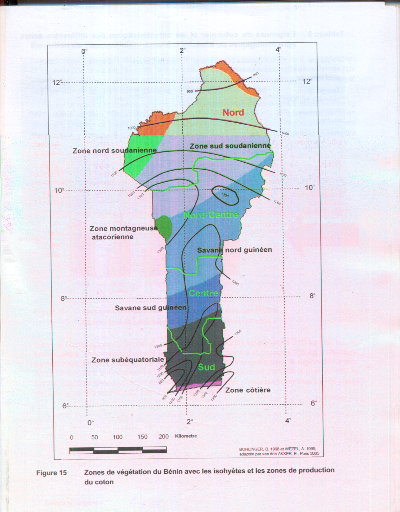
Figure 1.5 : Zone de
végétation du Bénin avec les isohyètes et les zones
de production de coton
1.5.2- Techniques
culturales
Les pratiques culturales varient suivant les aires de culture,
mais surtout suivant les moyens dont disposent les agriculteurs.
Dans les systèmes de culture permettant un strict
contrôle des conditions de milieu, la culture cotonnière est
conduite d'après les besoins en temps réel de la plante. Des
indicateurs de pilotage sont mesurés directement sur la plante ou sur le
peuplement. On peut citer le ratio de la hauteur des plants au nombre de noeuds
de la tige (« height to node ratio », HNR), le taux de croissance de
ces deux paramètres, la surface foliaire, ou encore le nombre de noeuds
au dessus de la dernière fleur blanche en première position de
branche fructifère (NAWF). Ces indicateurs sont utilisés pour
décider des interventions culturales telles que l'irrigation, la
fertilisation, les traitements insecticides, l'usage des régulateurs de
croissance etc. Une valeur de NAWF d'environ 5 par exemple apporte l'indication
de l'imminence de la cessation de croissance (cut out) et rend compte de la
diminution des besoins d'irrigation (Bourland et al., 1992).
L'adoption de fortes densités de peuplement (culture dite "narrow row
cotton"), et l'utilisation raisonnée d'hormones et de régulateurs
de croissance permettent de contrôler la croissance des plantes et
d'optimiser les coûts de production (Martin, 2000)
En Afrique de l'ouest et du Centre où la culture est
essentiellement pluviale et pratiquée par de petits paysans sur des
superficies dépassant rarement en moyenne 1 ha, le pilotage de la
culture est essentiellement basé sur les saisons de pluie. L'ensemble
des opérations culturales est calé par rapport à la date
de semis, en particulier, les dates d'apports des engrais, les dates
d'application des insecticides. Les densités pratiquées varient
de 42000 plantes par ha à 62000 plantes par ha au Bénin, mais
elles peuvent atteindre 80000 plants par ha en Côte d'Ivoire. Le labour
manuel est la pratique courante, la culture attelée étant aussi
de plus en plus utilisée. Seulement quelques paysans ont accès au
labour mécanique. La culture est semi - intensive avec un taux
d'adoption de plus de 95 % de l'utilisation des intrants (fumure
minérale, protection insecticide). Le désherbage manuel est
courant, mais des herbicides de pré - levée sont adoptés
par les producteurs ayant de grandes superficies ; la récolte est
partout manuelle.
De légères différences sont
observées suivant les zones agroécologiques, en particulier en ce
qui concerne les dates de semis (plus proche du 1er Juin au nord et un peu plus
tard au sud), les fumures minérales (apport complémentaire de Kcl
au sud).
L'efficacité des techniques culturales mises en oeuvre
dépend donc fortement de la régularité des pluies.
L'amélioration de l'alimentation hydrique de la plante dans ces zones
à risque climatique pourrait passer par des actions favorisant la mise
en place rapide de la production sur le plant et cela représente l'un
des objectifs visés par les pratiques de taille des cotonniers.
2.1- Problématique
et contraintes abordées
Le secteur cotonnier africain est aujourd'hui confronté
à de multiples problèmes : les niveaux de rendement sont
bas, les coûts de production sont élevés. Le coût
mondial du coton est souvent en baisse en raison des fortes subventions
accordées à la culture dans les pays développés
engendrant une concurrence déloyale sur le marché international
etc. L'incertitude sur le prix d'achat du coton graine aux producteurs et
l'accès aux facteurs de production entraîne une méfiance et
une modification du comportement des producteurs vis à vis de cette
culture. Floquet et al. (2002) constatent une moindre
disponibilité de la main d'oeuvre pour cette activité. En
parallèle, on observe une moindre efficacité des produits
classiques vis-à-vis de la protection phytosanitaire de la culture. A
titre d'illustration, Ferron et al. (2002) ont mis en évidence
l'acquisition d'une résistance aux pyrétrinoïdes de la part
de Helicoverpa armigera, principal ravageur du cotonnier au
Bénin. Le recours à de nouvelles molécules
renchérit le coût de la protection phytosanitaire. Enfin, dans un
contexte hautement compétitif, la production d'une fibre de
qualité représente un argument de poids dans la
négociation des contrats pour le coton béninois. Outre la
longueur fortement liée à des facteurs variétaux, la
maturité des fibres (impact sur la prise de teinture) et le collage sont
des caractéristiques liées aux conditions de culture.
Au Bénin comme dans la plupart des pays producteurs de
coton de l'Afrique de l'ouest et du centre, la culture est essentiellement
pluviale, donc tributaire des aléas pluviométriques. Dans les
régions septentrionales du Bénin, l'installation tardive des
pluies ces dernières années dans le nord limite fortement le
temps de préparation des sols et empêche assez souvent une bonne
installation des cultures ce qui entraîne des semis tardifs. L'analyse de
cette contrainte a révélé que les pertes encourues par les
cotonculteurs sont très élevées soit 30 à 35% de la
production (Glèlè et Adégbola, 2003).
Face à ces difficultés, la recherche est
sollicitée pour contribuer à résoudre les problèmes
de rentabilité de la production cotonnière. Le présent
travail s'inscrit dans ce cadre et contribue à rechercher les
itinéraires favorisant une meilleure allocation des assimilâts aux
organes fructifères dans le but d'optimiser le rendement de la culture
en fonction des conditions climatiques subies par la plante.
En effet, le cotonnier est une plante à croissance
indéterminée. Le développement végétatif ne
s'arrête pas avec l'entrée en floraison comme c'est le cas pour
d'autres plantes comme le maïs par exemple. De ce fait, la poursuite de la
croissance végétative se fait en compétition avec la mise
en place de nouveaux organes fructifères et le développement de
fruits déjà installés. Ainsi, les carbohydrates issus de
la photosynthèse sont utilisés à la fois pour la
poursuite de la croissance, la mise en place de nouveaux organes
fructifères et la maturation des fruits déjà
installés. Les assimilâts se répartissent entre organes
fructifères (bourgeons, fleurs et capsules) et végétatifs
(racines, tiges et feuilles) de telle manière que la plante ralentit
progressivement sa croissance végétative au fur et à
mesure que les capsules se mettent en place. Lorsque la plante porte toute la
charge fructifère qu'elle est capable de supporter, la floraison et la
croissance s'arrêtent ; ce stade est appelé "cutout" (Manney,
1986). La régulation de l'équilibre entre croissance
végétative et fructifère est ainsi d'une importance
capitale dans l'élaboration du rendement en culture cotonnière.
Aux USA, et dans la plupart des pays qui en ont les moyens, en
dehors de la sélection des variétés précoces et
compactes, des régulateurs de croissance sont utilisés pour
réduire, à partir de la floraison la croissance
végétative au profit du développement fructifère.
Ceci contribue à diriger une plus grande partie des assimilas vers les
puits fructifères.
En Chine, les producteurs font recours à des techniques
de taille qui consistent soit à supprimer les branches
végétatives, soit à écimer des bourgeons terminaux
des branches fructifères ou l'extrémité de la tige
principale (tipping out ou topping).
Dans les paysannats de culture pluviale comme le Bénin
où la durée du cycle des pluies utiles pour la culture peut
s'avérer parfois insuffisante, la technologie de taille des cotonniers
pourrait permettre aux producteurs de piloter la durée de cycle et
l'équilibre entre croissance végétative et
fructifère en regard d'objectifs de rendement et de qualité d'une
production accrus. Cette pratique se substitue à l'emploi de
régulateurs de croissance dont le coût viendrait limiter le revenu
des producteurs.
2.2- Bilan des travaux
antérieurs
2.2.1 Effet de l'écimage
sur le rendement
La technologie de taille du cotonnier est ancienne ; elle
se réfère à l'ablation des branches
végétatives, l'écimage du bourgeon terminal de la tige
principale (« tipping - out ou topping en anglais »),
l'écimage des bourgeons terminaux des branches fructifères ou
à l'ablation des bourgeons axillaires et des feuilles sénescentes
(Zhang and Sun, 2007). En Chine, la technologie s'est rapidement
répandue vers la fin du 19ème siècle avec
l'introduction des variétés de coton Upland (G. hirsutum
L., espèce la plus cultivée au monde, et donc aussi au
Bénin); cette espèce est plus tardive et présente un plus
grand développement végétatif que les
variétés de G. arboreum précédemment
cultivées dans cette région du monde (Zhang and Sun, 2007). La
taille du cotonnier permet alors de réduire les effets d'ombrage
exercé sur les organes reproducteurs par le développement
végétatif excessif des variétés de G. hirsutum
et d'améliorer le rendement au champ de la culture (Dong et
al., 2003). Elle permet en outre une production précoce
permettant d'éviter les problèmes de gelée en fin de cycle
(Zhang and Sun, 2007).
Les branches végétatives du cotonnier sont
situées en dessous des branches fructifères et ne portent pas
directement de fruits mais donnent naissance à des sympodes qui
produisent plus tard les fruits. Ainsi leur contribution à la production
de coton graine est faible et intervient souvent tardivement. Selon Davidonis
et al., (2006) ; Bednarz et al., (2006) leur taille est
bénéfique à la production et améliore le rendement
et la qualité des fibres de coton parce que les assimilâts
destinés à leur croissance sont redirigés vers les puits
fructifères.
Des études menées par Siddique et al.,
(2002) ; Brown et al., (2001) ; Sawaji et al., (1994) et Kittock et
Fry., (1997) ont également rapporté des augmentations de
rendement à la suite d'un écimage des cotonniers. D'autres
travaux associant l'écimage à certaines pratiques culturales
comme la densité de semis ont également mis en évidence
des effets positifs sur le rendement (Ahmed et al., 1989 ;
Rahaman et al., 1991 ; Abd - El - Malik and El Shahawy,
1999 ; Ma Fuyu et al., 2004 ; Obasi and Msaakpa, 2005). El -
Hanafi et al., 1982 et Damodoran et al., 1974 ont
rapporté que les effets bénéfiques de l'écimage sur
le rendement dépendaient de la date de réalisation de cet
écimage. Selon Dhamalingam et al. (1974) les effets de
l'écimage dépendent de la variété.
Au Mali, les études menées par Renou de 2002
à 2005, montrèrent que les plus ou moins bonnes performances de
l'écimage sont dues au taux de rétention des organes
fructifères, la potentialité de la culture et la densité
de plantation. Selon ce dernier, le niveau de potentialités au dessous
duquel les bénéfices d'un écimage sont plus incertains est
probablement variable en fonction des conditions du milieu (pluviométrie
et plus généralement les caractéristiques de la saison des
pluies en fin de campagne). Il conclut qu'en dessous de 1000 kg/ha, cette
pratique ne devrait pas être mise en oeuvre.
2.2.2- Effet de
l'écimage sur les infestations de chenilles carpophages et les
pucerons
Les effets positifs de l'écimage sur la
réduction des niveaux d'infestation ont également
été mentionnés dans la littérature. Au Cameroon,
l'écimage des premières feuilles de palmier infestées par
le mineur Coelaenomenodera minuta Ulm (coleoptère hispidae) a
un effet sur le deuxième stade larvaire de cet insecte (Syed,
1982 ; Syed and Ekulolé, 1983 ; Ekulolé, 1984).
L'écimage des cotonniers permet une réduction
des pontes d' Helicoverpa armigera (Sundaramurthy, 2002), de S.
littoralis (Nagib et Nasr - Kattab, 1978). Il permet également une
diminution des infestations de E. insulana (Nasr et Azab, 1969) et une
diminution des infestations d'A. gossypii (Ekukolé, 1992 et
Deguine et al., 2000), car ce sont sur les jeunes feuilles du bourgeon
terminal des plants de cotonnier que s'alimentent
préférentiellement les aphides (Dixon,1986 and Ekukole, 1989).
L'écimage a également pour effet de délocaliser la
production de fleurs vers le bas du plant, ce qui les rend moins attractif
vis-à-vis des ravageurs.
Les résultats d'investigations éditées
à Maroua au Cameroon ont montré que la taille réduit les
populations de puceron jusqu'à 45% (Ekukolé, 1989) et cette
tendance était indépendante du stade rencontré (nymphes,
adultes avec ou sans ailes). Une telle réduction résulterait
d'une diminution du nombre de foyer de pucerons. Leur diminution favorise leur
contrôle par leurs ennemis naturels.
2.3- Objectifs de
l'étude
L'objectif général de cette étude est
d'évaluer les effets de différentes pratiques de taille sur les
performances agronomiques du cotonnier dans les conditions de culture du
Bénin. Il s'agit plus spécifiquement d'évaluer :
- l'effet de l'ablation des BV sur les paramètres
agronomiques en semis précoce et en semis tardif.
- les effets de l'écimage du bourgeon terminal de la
tige principale sur les paramètres de précocité et de
rendement en coton graine.
- le moment optimum où l'écimage pourra produire
un effet bénéfique sur le rendement.
- l'impact de la taille sur l'infestation par les ravageurs du
cotonnier.
2.4- Hypothèses
testées
Pour atteindre ces objectifs, nous avons posé les
hypothèses suivantes :
H1 : L'ablation des BV améliore les performances
agronomiques du cotonnier.
H2 : Réaliser au moment opportun,
l'écimage améliore la précocité et le rendement en
coton graine.
H3 : la taille du cotonnier permet de réduire les
infestations par les chenilles et les populations des pucerons A.
gossypii en fin de cycle.
3.1- Matériel
utilisé
Le matériel végétal utilisé est la
variété H279-1, variété actuellement
cultivée au Bénin depuis 2002. Elle est originaire du Togo et
s'est montrée parfaitement adaptée à nos conditions
agroécologiques à l'issue d'expérimentations multilocales
et pluriannuelles. Elle provient d'un croisement multiple réalisé
en Côte-d'ivoire en 1981 (Tableau 3.1) et ces caractéristiques
sont consignées dans le tableau 3.2.
Tableau 3.1: Généalogie de
H279-1
|
Variété
|
H279-1
|
|
Type
De
Croisement
|
Multiple :
[(SR1 F4 × L 299 - 10) × (Stonville 213× G115 -
7)] ×
[(T120 - 7 × U585-12) × (T120- 7 ×Reba
P279)]
en 1981 à Bouaké en Côte d'Ivoire
|
|
Pedigree
|
Lignée issue de G18A en 1990
|
|
Etape
|
Variété en vulgarisation
|
Source : CRA-CF
Tableau 3.2 : Caractéristiques
de H279-1
|
Caractéristiques technologiques
|
Unités
|
Variété H279-1
|
|
Agronomiques
Production coton - graine
Rendement d'égrenage
Production fibre
Poids moyen capsulaire
|
Kg/ha
%
Kg/ha
G
|
1874
43,9
825
4,7
|
|
Technologie fibre
Longueur UHML
Longueur ML
Uniformité UI
Micronaire
Maturité FM
Finesse Hs
Ténacité STPI
Allongement
Brillance Rd
Indice de jaune +b
|
mm
mm
%
%
mtex
g/tex
%
%
|
28,8
24,1
84,2
04,0
77,8
192
30,6
06,1
75,3
9,2
|
|
Technologie de fil
Ténacité USTER
Allongement USTER
Irrégularité U
Neps totaux
Neps coque
|
cN/tex
%%
/1000 m
/1000 m
|
14,4
06,1
17,8
730
646
|
|
Technologie graine (Id)
Poids de 100 graines
Linter
Germination
|
g
%
%
|
08,2
09,8
73,3
|
Source : Résultats
d'expérimentation multi locale en milieu contrôlé :
CRA-CF/INRAB/MAEP 1994/95 à 1998/99
H279-1 a un port pyramidal élancé avec une tige
de couleur vert - pourpre et une pilosité moyenne à forte, et
possédant des branches végétatives
développées. Les feuilles sont pileuses et entièrement
lobées. Les bractées sont de tailles moyennes et moyennement
découpées. Les fleurs à pétales jaune - pâle
sans macule et à pollen crème. Les capsules de grande taille, de
forme conique à ronde, moyennement mucronées et à
insertion moyenne présentant une position demi - dressée et avec
des glandes à gossypol. Elle a une ouverture normale.
Les autres matériels utilisés dans le cadre de
notre étude se composent essentiellement de petits outils de champ et de
matériel de laboratoire :
- un cordeau pour la délimitation des blocs et des
unités parcellaires (U.P)
- des étiquettes pour l'identification /
étiquetage des U.P et les différents traitements.
- des piquets pour marquer les lignes de semis
- des ficelles marquées (0,3 m et 0,2 m) pour le semis
et pour le marquage des plants
- un coupe - coupe pour le fauchage des allées et des
alentours de notre parcelle
- d'une houe pour le nivellement de la bande
- d'une chaîne de 20 m pour délimiter les blocs
et les lignes
- d'un pulvérisateur ULV pour les traitements
insecticides
- des fiches de collecte des données
- d'un mètre ruban et d'une règle pour le
« plant mapping »
- une balance pour le poids des capsules et du coton graine
- un bécher et une pipette pour le biovolume des
capsules vertes
- des sacs, et des sachets en polysérène
- des étiquettes pour l'étiquetage des
parcelles
3.2- Site
expérimental
Les essais ont été conduits sur un Centre
Permanent d'Expérimentation (CPE) du CRA-CF à Okpara
(2°41'Est, 9°18' Nord, et 320 m d'altitude). Le CPE est situé
à environ 10 km à l'Est de Parakou via la voie passant devant
l'Université de Parakou. Le sol est de type ferrugineux tropical ;
la pluviométrie annuelle de 2008 a été de 1300 mm. A
l'instar des autres régions du Nord Bénin, le CPE jouit d'une
saison pluvieuse et d'une saison sèche bien marquée favorisant la
culture du coton. Les données pluviométriques
enregistrées journalièrement au cours de la période
d'expérimentation figurent en annexe. Les travaux de terrain ont
été menés de Juin à Décembre 2008 ; le
traitement des échantillons et le traitement des données
collectées ont eu lieu et à la direction régionale du
CRA-CF à Parakou.
3.3- Méthodes et
dispositif expérimental
Trois essais monofactoriels comparant chacun six
itinéraires de taille de cotonnier ont été
installés sur le Centre Permanent d'Expérimentation du CRA-CF
à Okpara. Ces trois essais correspondent à trois conduites de la
culture cotonnière susceptibles d'engendrer des réponses
différentes à l'écimage :
- 1ier essai : itinéraire
recommandé par la recherche, notamment : semis à date
recommandée (20 - 25 Juin), variété H279-1, densité
conventionnelle de semis (42000 plants/ha correspondant à un
écartement de 0,8 m × 0,3 m)
- 2ième essai : idem au premier mais
semis à forte densité (125000 plants/ha correspondant à un
écartement de 0,4 m × 0,2 m). Nous avons respecté les
mêmes dates de semis que celles indiquées ci - dessus ; cette
situation correspond à un itinéraire testé par la
recherche (SEKLOKA et al., 2006) et qui améliore le rendement.
L'effet de l'écimage est attendu comme plus marqué ici du fait de
la concentration des capsules sur les premières positions.
- 3ième essai : semis tardif (25 - 30
Juillet) soit 3 à 4 semaines après le premier et à forte
densité (125000 plants/ha correspondant à un écartement de
0,4m × 0,2 m). Cette situation correspond également à un
itinéraire proposé par la recherche (CRA - CF) pour les semis
tardifs. L'écimage et la forte densité sont attendus comme des
techniques susceptibles de compenser les pertes de rendement et de
précocité du semis tardif.
Dans chaque essai, le dispositif expérimental est un
bloc de Fisher (bloc complet) à un facteur (écimage) et à
quatre répétitions (Annexe 2). Les parcelles
élémentaires sont de 21,6 m² (3 lignes de 9 m pour la
densité de 42000 plants/ha, et 6 lignes de 9 m pour la densité de
125000 plants/ha), soit une superficie totale par essai de 518,4 m² hors
allées et bordures. Pour chacun des essais, le semis est fait à 5
graines par poquet avec démariage à un plant par poquet.
Les différents traitements
étudiés sont :
1- Suppression de toutes les branches
végétatives (BV) à la floraison.
2 - Ecimage du bourgeon terminal de la tige principale
à une semaine après la floraison.
3 - Ecimage du bourgeon terminal de la tige principale
à deux semaines après la floraison.
4 - Ecimage du bourgeon terminal de la tige principale
à trois semaines après la floraison
5 - Ecimage du bourgeon terminal de la tige principale
à quatre semaines après la floraison.
6 - Le témoin (pas de taille ou taille zéro)

Photo 3.1: Opération
d'écimage
3.4- Itinéraire de
conduite des essais
La culture a été conduite suivant les pratiques
culturales recommandées par la recherche. La fumure minérale a
été de 200 kg de NPKSB 14-23-14-5-1 appliquée à
environ 15 jours après levée suivi d'un apport de 50 kg/ha
d'Urée à environ 45 jours après levée sur les semis
précoces ; il n'y a pas eu apport d'urée sur le semis
tardif ; trois sarclages, réalisés suivant l'état
d'enherbement des parcelles, ainsi qu'un sarclobuttage à 50 jours
après levée ont permis de contrôler efficacement les
adventices. Une application insecticide tous les 10 jours a été
mise en place dès la floraison des premiers plants jusqu'à la
première récolte afin de contrôler efficacement la pression
parasitaire des insectes et limiter ainsi au maximum les
« shedding » d'origine parasitaire; les trois premiers
traitements insecticides étaient à base de Tihian O-Tecq ; les
traitements suivants combinaient un produit pyréthrinoïde et un
produit organophosphoré acaricide ou aphicide suivant qu'on se situait
à la mi-floraison ou en fin de floraison.
3.5- Les données
collectées
Les observations ont été
échelonnées durant tout le cycle du cotonnier.
Période avant entrée en
floraison
Avant l'entrée en floraison, la date de levée a
été la première donnée collectée. Elle a
été obtenue grâce à un passage quotidien sur le site
à partir du 4ième jour après semis. Nous avons
relevé par parcelle le nombre de poquets levés sur les lignes
d'observation (ligne centrale pour les parcelles de 3 lignes et les lignes 3 et
4 pour les parcelles de 6 lignes). La date de levée correspond à
la date où 50% des poquets ont levé. Après la
levée, les poquets levés ont été comptés au
15ème j.a.s. Ceci dans le but de réaliser un resemis
lorsque la levée n'est pas totale.
Période de floraison
A la floraison, les données relatives à la date
moyenne d'apparition de la première fleur (PFM) ont été
collectées. Ainsi, dès l'apparition de la première fleur
sur la ligne d'observation, nous avons relevé chaque matin le nombre de
fleurs blanches par parcelle (fleur du jour). La PFM est le nombre de jours
après levée où la somme du nombre de fleurs blanches est
égale au nombre de poquets levés. Ceci nous a permis de caller
dans le temps les différents traitements à réaliser sur
chaque parcelle (annexe 3).

Photo 3.2: Fleur du jour du cotonnier
Egalement, des observations entomologiques simplifiées
et non destructives ont été réalisées sur les
plants de cotonnier. Il s'agit de : comptage des organes attaqués
par les ravageurs, comptage des plants attaqués par les chenilles
phyllophages, comptage des fleurs en rosette.
Période d'ouverture des capsules
A l'ouverture des capsules, nous avons marqué avant la
première récolte (aux environs du 110ème
jour), cinq plants par ligne d'observation sur lesquels ont porté les
observations de post-récolte. Le marquage s'est réalisé
avec une ficelle et a porté sur le 5ième, 8ième,
11ième, 14ième et 17ième plant de chacune des lignes
d'observation de chaque parcelle élémentaire. Pour les parcelles
de 6 lignes, le marquage a été réalisé 10 plants
(5 par ligne d'observation). Dans le cas où un plant correspondant
à un de ces numéros est anormal (écimé par
Earias par exemple), systématiquement le plant normal suivant
est choisi. Aussi, lorsqu'un plant est absent, nous le remplaçons par
un autre plant bien encadré des 4 cotés. Les observations
ci-après ont été réalisées :
- Date moyenne d'ouverture de la première
capsule (OPCM): A partir de l'ouverture de la première capsule dans
une parcelle (entre 100 et 110 jal), nous avons relevé chaque matin le
nombre de capsules ouvertes par parcelle sur les lignes d'observation et ce
jusqu'au jour où le cumule donne le nombre de plants présents sur
la ligne (Annexe 4)
- Précocité de production (R1/RT) : une
première récolte a été faite aux environs de 110
à 120 jal uniquement sur les plants marqués (récolte plant
par plant). Ceci a permis, outre l'économie de main d'oeuvre, un
meilleur suivi, une récolte plus minutieuse capable de maintenir en
place les branches et les capsules pour un « plant mapping
final » ;
- Plant mapping final : il s'agit d'une description
complète de l'architecture du plant qui rend compte de la production de
chacune des positions fructifères du plant. Une fiche
élaborée pour la circonstance a permis d'identifier sur chaque
branche la présence ou l'absence de capsule aux différents sites
fructifères ou position. Ce plant mapping final a été
réalisé sur les 5 plants marqués par ligne d'observation
après ouverture totale des capsules. Il a été suivi de la
dernière récolte du plant. Ces 5 plants entièrement
récoltés ont été ensuite coupés et
rangés au bord des parcelles pour être pesés plus
tard ;
- Rendement en coton graine : le reste des cotonniers des
lignes d'observation nous a été récolté. Le
poids de coton graine ainsi obtenu a été ajouté au poids
de coton graine récolté sur les plants marqués pour
estimer le rendement de la parcelle ;
- Le poids moyen capsulaire (PMC) : après
ouverture totale des capsules, nous avons procédé sur 5 plants
des lignes latérales de chaque parcelle élémentaire
à la récolte de trois capsules par plant normalement
développées en position 1 de branches fructifères. Ces
capsules ont été récoltées en position basse, en
position médiane et en position haute (Hau and Gobel, 1987). Le PMC a
été calculé par parcelle en divisant le poids total de
coton graine ainsi récolté sur les cinq plants par le nombre de
capsules.
3.6 - Analyse des
données
Toutes les données ont été saisies avec
le logiciel Excel. Ce logiciel a servi à la construction des
histogrammes pour l'interprétation des résultats. L'analyse
statistique des données collectées a été faite
à l'aide du logiciel STAT ITCF. La séparation des moyennes a
été faite selon le test de Student Newman and Keuls
4- Résultats
4.1 - Effet de
l'écimage sur la précocité du cotonnier
4.1.1- semis de bonne date
à faible densité (42000 plants/ha)
Les cotonniers non écimés ont mis un peu plus de
temps que les cotonniers écimés pour ouvrir leurs
premières capsules (OPCM) ; en conséquence, leur
précocité de production (R1/RT) est plus faible. Mais ces
différences n'ont pas été significatives (Tableau 4.1)
Tableau 4.1 : Effet de l'écimage
sur la précocité en semis à bonne date et à faible
densité
|
Traitements
|
Date d'ouverture 1ère capsule (OPCM) en
nombre de jours après levée
|
Précocité de production (R1/RT) en %
|
|
Ecimage 1 semaf
|
111,25
|
#177; 0,48
|
|
24,83
|
#177; 7,20
|
|
|
Ecimage 2 semaf
|
111,75
|
#177; 1,13
|
|
19,83
|
#177; 5,90
|
|
|
Ecimage 3 semaf
|
112,25
|
#177; 0,89
|
|
21,38
|
#177; 4,93
|
|
|
Ecimage 4 semaf
|
112,00
|
#177; 0,67
|
|
19,35
|
#177; 3,18
|
|
|
Ablation des BV
|
112,25
|
#177; 1,00
|
|
20,50
|
#177; 10,9
|
|
|
Témoin
|
113,25
|
#177; 0,89
|
|
11,88
|
#177; 10,3
|
|
|
Moyenne
|
112,13
|
|
|
19,62
|
|
|
|
Ecartype
|
0,95
|
|
|
8,31
|
|
|
|
CV (%)
|
0,9
|
|
|
42.4
|
|
|
|
Test F
|
Ns
|
|
|
ns
|
|
|
|
Semaf=semaine après floraison ; BV= branches
végétatives ; OPCM=date moyenne d'ouverture des
premières capsules ; R1/RT=précocité de production,
le rapport de la première récolte à 120 jours après
semis à la récolte totale ; ns, * et ** signifient
respectivement différences non significatives, différences
significatives à 5% et différences significatives à
1%
|
4.1.2- Semis de bonne date
à forte densité (125000 plants/ha)
L'analyse de variance n'a mis en évidence aucun effet
significatif sur la précocité en général ;
mais l'ablation des BV a tendance à induire une ouverture plus rapide
des capsules et une production plus précoce de coton graine (Tableau
4.2). La précocité de production semble également
améliorée par un écimage à deux semaines
après floraison.
Tableau 4.2 : Effet de
l'écimage sur la précocité en semis à bonne date et
à forte densité (125000 plantes/ha)
|
Traitements
|
Date d'ouverture 1ère capsule (OPCM) en
nombre de jours après levée
|
Précocité de production (R1/RT) en %
|
|
Ecimage 1 semaf
|
115,50
|
#177; 0.82
|
|
17.50
|
#177; 7.23
|
|
|
Ecimage 2 semaf
|
117,38
|
#177; 0,86
|
|
19.75
|
#177; 8.78
|
|
|
Ecimage 3 semaf
|
116,25
|
#177; 1,40
|
|
12.25
|
#177; 4.47
|
|
|
Ecimage 4 semaf
|
116,00
|
#177; 1,07
|
|
17.75
|
#177; 7.21
|
|
|
Ablation des BV
|
115,00
|
#177; 1,52
|
|
20.25
|
#177; 3.49
|
|
|
Témoin
|
116,75
|
#177; 0,72
|
|
11.25
|
#177; 2.47
|
|
|
Moyenne
|
116,15
|
|
|
16.46
|
|
|
|
Ecartype
|
1,21
|
|
|
6.63
|
|
|
|
CV (%)
|
1 ,0
|
|
|
40.3
|
|
|
|
Test F
|
Ns
|
|
|
ns
|
|
|
|
Semaf=semaine après floraison ; BV= branches
végétatives ; OPCM=date moyenne d'ouverture des
premières capsules ; R1/RT=précocité de production,
le rapport de la première récolte à 120 jours après
semis à la récolte totale ; ns, * et ** signifient
respectivement différences non significatives, différences
significatives à 5% et différences significatives à
1%
|
4.1.3- semis tardif à
forte densité (125000 plants/ha)
Les analyses de variance n'ont révélé
aucune différence significative entre les différents niveaux de
traitement.
Tableau 4.3 : Effet de
l'écimage sur la précocité de production en semis tardif
à forte densité
|
Traitements
|
Date d'ouverture 1ère capsule (OPCM) en
nombre de jours après levée
|
Précocité de production
(R1/RT) en %
|
|
Ecimage 1 semaf
|
106, 75
|
#177; 0.80
|
|
-
|
-
|
|
|
Ecimage 2 semaf
|
105,75
|
#177; 0,58
|
|
-
|
-
|
|
|
Ecimage 3 semaf
|
107,63
|
#177; 0,99
|
|
-
|
-
|
|
|
Ecimage 4 semaf
|
106,13
|
#177; 1,49
|
|
-
|
-
|
|
|
Ablation des BV
|
107,38
|
#177; 1,60
|
|
-
|
-
|
|
|
Témoin
|
106,88
|
#177; 1,07
|
|
-
|
-
|
|
|
Moyenne
|
106,92
|
|
|
|
|
|
|
Ecartype
|
1,26
|
|
|
|
|
|
|
CV (%)
|
1,2
|
|
|
|
|
|
|
Test F
|
Ns
|
|
|
|
|
|
|
Semaf=semaine après floraison ; BV= branches
végétatives ; OPCM=date moyenne d'ouverture des
premières capsules ; R1/RT=précocité de production,
le rapport de la première récolte à 120 jours après
semis à la récolte totale ; ns, * et ** signifient
respectivement différences non significatives, différences
significatives à 5% et différences significatives à
1%
|
Les résultats de précocité de
production n'étaient pas encore disponibles au moment de la
rédaction
Il ressort également des résultats
précédents que les cotonniers semés tardivement ont des
dates moyennes d'ouverture capsulaire plus faibles que ceux semés
précocement ou à date normale. Nous pouvons également
observer qu'en semis à date normale, les cotonniers semés
à 125000 plantes/ha ont mis plus de temps que les cotonniers
semés à 42000 plantes/ha pour ouvrir leurs capsules (Figure
4.1)
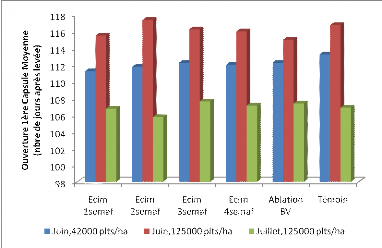
Figure 4.1 : Schéma comparatif de
l'effet du pruning sur la précocité d'ouverture capsulaire dans
les trois essais
4.2- Effet de
l'écimage sur la charge en capsule
4.2.1 - Semis de bonne date
à densité faible
L'analyse de l'effet de l'écimage sur les nombres de
capsules en semis à bonne date et à faible densité ne
révèle aucune différence significative entre les
traitements. Toutefois, les cotonniers écimés à une
semaine, à deux semaines et ceux écimés à quatre
semaines semblent portés légèrement plus de capsules par
plant que le témoin (respectivement + 1,75 ; +2,15 et + 3,30
capsules de plus). (Tableau 4.4)
Tableau 4.4: Effet de l'écimage
sur la charge en capsule en semis de bonne date à faible
densité
|
Traitements
|
Nombre de capsules sur branches fructifères (CBF)
|
Nombres de capsules par plant (CPP)
|
|
Ecimage 1 semaf
|
17,55
|
#177; 4,19
|
|
21,75
|
#177; 5,11
|
|
|
Ecimage 2 semaf
|
18,60
|
#177; 1,35
|
|
22,15
|
#177; 0,70
|
|
|
Ecimage 3 semaf
|
16,40
|
#177; 1,47
|
|
20,35
|
#177; 3,37
|
|
|
Ecimage 4 semaf
|
17,90
|
#177; 2,03
|
|
23,30
|
#177; 2,84
|
|
|
Ablation des BV
|
18,50
|
#177; 2,19
|
|
18,50
|
#177; 3,12
|
|
|
Témoin
|
16,65
|
#177; 2,01
|
|
20,00
|
#177; 2,13
|
|
|
Moyenne
|
17.60
|
|
|
21,01
|
|
|
|
Ecartype
|
2.63
|
|
|
3,47
|
|
|
|
CV (%)
|
14.9%
|
|
|
16,5%
|
|
|
|
Test F
|
Ns
|
|
|
ns
|
|
|
|
Semaf=semaine après floraison ; ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
|
4.2.2 - Semis de bonne date
à forte densité
Les différentes tailles de cotonnier n'ont eu aucun
effet significatif sur le nombre de capsules portées par le plant.
(Tableau 4.5)
Tableau 4.5: Effet de l'écimage
sur la charge en capsule en semis de bonne date à forte
densité
|
Traitements
|
Nombre de capsules sur branches fructifères (CBF)
|
Nombres de capsules par plant (CPP)
|
|
Ecimage 1 semaf
|
10,00
|
#177; 0.34
|
|
10,50
|
#177; 0,80
|
|
|
Ecimage 2 semaf
|
08,50
|
#177; 0,63
|
|
09,75
|
#177; 0,24
|
|
|
Ecimage 3 semaf
|
09,50
|
#177; 0,85
|
|
10,00
|
#177; 0,80
|
|
|
Ecimage 4 semaf
|
09,75
|
#177; 1,96
|
|
09,75
|
#177; 02,1
|
|
|
Ablation des BV
|
08,50
|
#177; 0,25
|
|
08,50
|
#177; 0,44
|
|
|
Témoin
|
09,50
|
|
|
10,00
|
|
|
|
Moyenne
|
9,29
|
|
|
9,75
|
|
|
|
Ecartype
|
1,33
|
|
|
1,46
|
|
|
|
CV (%)
|
14,3%
|
|
|
15,0%
|
|
|
|
Test F
|
Ns
|
|
|
ns
|
|
|
|
Semaf=semaine après floraison ; ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
|
4.2.3 - Semis tardif à
forte densité
A l'image du semis à bonne date et à forte
densité, les pratiques de taille n'ont pas eu d'effets significatifs sur
la charge en capsule du plant (Tableau 4.6)
Tableau 4.6: Effet de l'écimage
sur la charge en capsule en semis tardif à forte densité
|
Traitements
|
Nombre de capsules sur branches fructifères (CBF)
|
Nombres de capsules par plant (CPP)
|
|
Ecimage 1 semaf
|
5,50
|
#177; 0,76
|
|
5,75
|
#177; 0,65
|
|
|
Ecimage 2 semaf
|
5,75
|
#177; 0,37
|
|
6,00
|
#177; 0,48
|
|
|
Ecimage 3 semaf
|
5,00
|
#177; 0,93
|
|
5,00
|
#177; 0,82
|
|
|
Ecimage 4 semaf
|
5,25
|
#177; 0,28
|
|
5,50
|
#177; 0,35
|
|
|
Ablation des BV
|
5,25
|
#177; 1,24
|
|
5,25
|
#177; 1,37
|
|
|
Témoin
|
6,00
|
#177; 0,28
|
|
6,00
|
#177; 0,35
|
|
|
Moyenne
|
5,46
|
|
|
5,58
|
|
|
|
Ecartype
|
0,81
|
|
|
0,83
|
|
|
|
CV (%)
|
14,8
|
|
|
14,9
|
|
|
|
Test F
|
ns
|
|
|
ns
|
|
|
|
Semaf=semaine après floraison ; Ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
|
Nous pouvons également noter que le nombre de capsules
par plant est plus faible à forte densité qu'à faible
densité ; il est également plus faible en semis tardif qu'en
semis précoce (Tableau 4.4 ; 4.5 et 4.6)
4.3- Effet de
l'écimage sur le poids des capsules
4.3.1 - Semis de bonne date
à faible densité
Que ce soit les capsules à l'état vert ou le
coton graine récolté d'une capsule ouverte, les
différences de poids capsulaire n'ont pas été
significatives (Tableau 4.7).
Tableau 4.7: Effet de l'écimage
sur le poids des capsules en semis de bonne date à faible
densité
|
Traitements
|
Poids moyen des capsules à l'état vert (en
gramme)
|
Poids moyen de coton graine récolté par capsule
(en gramme)
|
|
Ecimage 1 semaf
|
20,60
|
#177; 0,56
|
|
4,73
|
#177; 0,10
|
|
|
Ecimage 2 semaf
|
20,42
|
#177; 1,46
|
|
4,88
|
#177; 0,41
|
|
|
Ecimage 3 semaf
|
19,52
|
#177; 0,94
|
|
4,08
|
#177; 0,53
|
|
|
Ecimage 4 semaf
|
21,22
|
#177; 0,43
|
|
4,90
|
#177; 0,44
|
|
|
Ablation des BV
|
21,42
|
#177; 1,30
|
|
4,93
|
#177; 0,39
|
|
|
Témoin
|
20,73
|
#177; 1,18
|
|
4,70
|
#177; 0,42
|
|
|
Moyenne
|
20,65
|
|
|
4,70
|
|
|
|
Ecartype
|
01,15
|
|
|
0,44
|
|
|
|
CV (%)
|
05,6
|
|
|
9,4
|
|
|
|
Test F
|
ns
|
|
|
ns
|
|
|
|
Semaf=semaine après floraison ; ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
|
4.3.2 - Semis de bonne date
à forte densité
A l'état vert (non encore ouvertes) les capsules issues
des cotonniers écimés semblent être plus grosses que celles
portées par les cotonniers non écimés ; mais les
différences n'ont pas été significatives
(Tableau 4.8).
A l'ouverture, les poids moyens capsulaires sont
significativement plus élevés sur les témoins et les
cotonniers dont les branches végétatives ont été
coupées (Tableau 4.8)
Tableau 4.8: Effet de l'écimage
sur le poids des capsules en semis de bonne date à forte
densité
|
Traitements
|
Poids moyen des capsules à l'état vert (en
gramme)
|
Poids moyen de coton graine récolté par capsule
(en gramme)
|
|
Ecimage 1 semaf
|
18,25
|
#177; 0,98
|
|
4,45
|
#177; 0,14
|
abc
|
|
Ecimage 2 semaf
|
18,50
|
#177; 0,92
|
|
4,10
|
#177; 0,07
|
c
|
|
Ecimage 3 semaf
|
18,25
|
#177; 0,63
|
|
4,20
|
#177; 0,25
|
bc
|
|
Ecimage 4 semaf
|
18,50
|
#177; 0,53
|
|
4,32
|
#177; 0,07
|
abc
|
|
Ablation des BV
|
18,00
|
#177; 0,58
|
|
4,60
|
#177; 0,22
|
a
|
|
Témoin
|
17,75
|
#177; 1,38
|
|
4,53
|
#177; 0,11
|
ab
|
|
Moyenne
|
18,21
|
|
|
4,37
|
|
|
|
Ecartype
|
0,97
|
|
|
0,17
|
|
|
|
CV (%)
|
5,3
|
|
|
4,0
|
|
|
|
Test F
|
ns
|
|
|
**
|
|
|
|
Semaf=semaine après floraison ; Ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
|
Les chiffres précédés des mêmes
lettres ne sont pas significativement différents au seuil de 1%.
4.3.3 - Semis tardif à
forte densité
Les données de poids moyen capsulaire en coton graine
n'étaient pas encore disponibles au moment de la rédaction de ce
mémoire. A l'état de capsules vertes, aucune différence
significative n'a été observée entre les différents
niveaux de taille de cotonnier (Tableau 4.9)
Tableau 4.9: Effet de l'écimage
sur la grosseur des capsules en semis tardif à forte densité
|
Traitements
|
Poids moyen des capsules à l'état vert (en
gramme)
|
Poids moyen de coton graine récolté par capsule
(en gramme)
|
|
Ecimage 1 semaf
|
15,02
|
#177; 1,06
|
|
-
|
-
|
|
|
Ecimage 2 semaf
|
14,66
|
#177; 0,71
|
|
-
|
-
|
|
|
Ecimage 3 semaf
|
16,47
|
#177; 1,24
|
|
-
|
-
|
|
|
Ecimage 4 semaf
|
15,45
|
#177; 0,69
|
|
-
|
-
|
|
|
Ablation des BV
|
15,68
|
#177; 0,33
|
|
-
|
-
|
|
|
Témoin
|
15,45
|
#177; 0,94
|
|
-
|
-
|
|
|
Moyenne
|
15,46
|
|
|
|
|
|
|
Ecartype
|
0,96
|
|
|
|
|
|
|
CV (%)
|
6,2
|
|
|
|
|
|
|
Test F
|
ns
|
|
|
|
|
|
|
Semaf=semaine après floraison ; Ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
|
Les résultats concernant le poids moyen capsulaire en
coton graine n'étaient pas encore disponibles au moment de la
rédaction
4.4- Effet de
l'écimage sur le volume capsulaire
En condition de semis précoce à faible
densité, les différentes pratiques de taille n'ont eu aucun effet
significatif sur le volume moyen des capsules. Par contre, en semis
précoce à forte densité, les cotonniers
écimés ont porté des capsules significativement plus
volumineuses que celles du témoin (Tableau 4.10)
Tableau 4.10: Effet de l'écimage
sur le volume moyen des capsules vertes (cm3)
|
Traitements
|
Semis de bonne date à faible densité
|
Semis de bonne date à forte densité
|
Semis tardif à forte densité
|
|
Ecimage 1 semaf
|
21,10
|
#177; 0,77
|
|
20,75
|
#177; 1,03
|
a
|
-
|
-
|
|
|
Ecimage 2 semaf
|
21,10
|
#177; 1,35
|
|
21,00
|
#177; 0,71
|
a
|
-
|
-
|
|
|
Ecimage 3 semaf
|
20,13
|
#177; 1,06
|
|
21,00
|
#177; 0,63
|
a
|
-
|
-
|
|
|
Ecimage 4 semaf
|
22,22
|
#177; 0,40
|
|
21,25
|
#177; 0,89
|
a
|
-
|
-
|
|
|
Ablation des BV
|
22,65
|
#177; 1,98
|
|
19,75
|
#177; 0,42
|
ab
|
-
|
-
|
|
|
Témoin
|
21,70
|
#177; 1,24
|
|
19,50
|
#177; 0,67
|
b
|
-
|
-
|
|
|
Moyenne
|
21,48
|
|
|
20,54
|
|
|
|
|
|
|
Ecartype
|
1,36
|
|
|
0,82
|
|
|
|
|
|
|
CV (%)
|
6,3%
|
|
|
4,0%
|
|
|
|
|
|
|
Test F
|
ns
|
|
|
*
|
|
|
|
|
|
|
Semaf=semaine après floraison ; Ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
Les chiffres précédés des mêmes
lettres ne sont pas significativement différents au seuil de 5%
|
Les résultats du semis tardif à forte
densité n'étaient pas encore disponibles au moment de la
rédaction.
4.5 - Effet de
l'écimage sur la rétention capsulaire du cotonnier
4.5.1 - Effet sur la
rétention en première position de branche fructifère
En condition de semis à bonne date et à faible
densité, les cotonniers écimés à une semaine et
ceux écimés à deux semaines après floraison
semblent avoir mieux retenu leurs capsules en première position de
branche fructifère (P1); les cotonniers non écimés ont
enregistré le taux de rétention en P1 les plus bas. Toutefois,
ces différences n'ont pas été significatives (tableau
4.11).
En semis de bonne date à forte densité, les
différences ont été hautement significatives entre les
différents niveaux du facteur étudié (p<0,01). Les
cotonniers écimés à une semaine après floraison ont
enregistré les taux de rétention les plus élevés
suivis de ceux écimés à 4 semaines après floraison.
Les cotonniers dont les branches végétatives ont
été coupées ont eu les taux de rétention en P1 les
plus faibles. Le taux de rétention des cotonniers non taillés
(témoin) a été également faible (tableau 4.11).
En semis tardif à forte densité, les cotonniers
écimés dans les deux premières semaines après la
floraison ont enregistré les taux de rétention les plus
élevés en première position de branches fructifères
(Tableau 4.11)
Tableau 4.11: Effet de l'écimage
sur la rétention capsulaire en première position de branche
fructifère
|
Traitements
|
Semis de bonne date à faible densité (en %)
|
Semis de bonne date à forte densité (en %)
|
Semis tardif à forte densité (en %)
|
|
Ecimage 1 semaf
|
70,00
|
#177; 7,42
|
|
59,88
|
#177; 2,20
|
a
|
50,97
|
#177; 4,46
|
ab
|
|
Ecimage 2 semaf
|
68,47
|
#177; 4,07
|
|
47,47
|
#177; 4,17
|
cd
|
54,20
|
#177; 5,95
|
a
|
|
Ecimage 3 semaf
|
63,10
|
#177; 2,87
|
|
50,82
|
#177; 4,89
|
bc
|
45,96
|
#177; 2,67
|
abc
|
|
Ecimage 4 semaf
|
60,03
|
#177; 0,83
|
|
54,07
|
#177; 3,52
|
b
|
46,95
|
#177; 3,92
|
abc
|
|
Ablation des BV
|
59,30
|
#177; 8,52
|
|
43,45
|
#177; 1,00
|
d
|
41,22
|
#177; 3,93
|
c
|
|
Témoin
|
57,50
|
#177; 5,54
|
|
45,60
|
#177; 1,46
|
cd
|
43,75
|
#177; 1,39
|
bc
|
|
Moyenne
|
63,07
|
|
|
50,22
|
|
|
47,18
|
|
|
|
Ecartype
|
6,06
|
|
|
3,51
|
|
|
4,36
|
|
|
|
CV (%)
|
9,6%
|
|
|
7,0%
|
|
|
9,2
|
|
|
|
Test F
|
ns
|
|
|
**
|
|
|
**
|
|
|
|
Semaf=semaine après floraison ; Ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
Les chiffres précédés des mêmes
lettres ne sont pas significativement différents au seuil de 1%.
|
4.5.2 - Effet sur la
rétention globale des branches fructifères
Comme dans le cas de la rétention en première
position de branche fructifère, les différences n'ont pas
été significatives pour le taux de rétention sur les
branches fructifères en semis de bonne date à faible
densité ; mais les tendances indiquent que les cotonniers
écimés à une et à deux semaines après
floraison ont eu les meilleurs taux de rétention sur BF.
En semis de bonne date à forte densité, les
cotonniers écimés à une semaine après floraison ont
enregistré le taux de rétention le plus élevé suivi
de ceux écimés à 4 semaines ; là aussi, les
taux de rétention les plus faibles ont été
enregistrés sur le témoin et les cotonniers privés de leur
branches végétatives à la floraison (Tableau 4.12).
Aussi, en semis tardif à forte densité les
cotonniers écimés dans les deux premières semaines ont
enregistré des taux de rétention capsulaire des branches
fructifères les plus élevés (Tableau 4.12).
Tableau 4.12: Effet de l'écimage
sur la rétention capsulaire des branches fructifères
|
Traitements
|
Semis de bonne date à faible densité (en %)
|
Semis de bonne date à forte densité (en %)
|
Semis tardif à forte densité (en %)
|
|
Ecimage 1 semaf
|
48,10
|
#177; 7,86
|
|
44,97
|
#177; 3,16
|
a
|
32,07
|
#177; 1,28
|
ab
|
|
Ecimage 2 semaf
|
50,55
|
#177; 7,01
|
|
39,13
|
#177; 3,14
|
bc
|
34,39
|
#177; 2,35
|
a
|
|
Ecimage 3 semaf
|
46,65
|
#177; 4,41
|
|
38,40
|
#177; 2,57
|
bc
|
29,37
|
#177; 1,75
|
b
|
|
Ecimage 4 semaf
|
45,60
|
#177; 3,46
|
|
42,22
|
#177; 2,86
|
ab
|
29,95
|
#177; 0,94
|
b
|
|
Ablation des BV
|
46,97
|
#177; 4,94
|
|
36,40
|
#177; 1,10
|
bc
|
28,10
|
#177; 3,13
|
b
|
|
Témoin
|
44,65
|
#177; 2,90
|
|
35,47
|
#177; 2,74
|
c
|
29,89
|
#177; 1,18
|
b
|
|
Moyenne
|
47,09
|
|
|
39,43
|
|
|
30,63
|
|
|
|
Ecartype
|
5,92
|
|
|
2,95
|
|
|
2,11
|
|
|
|
CV (%)
|
12,6%
|
|
|
7,5%
|
|
|
6,9
|
|
|
|
Test F
|
ns
|
|
|
**
|
|
|
**
|
|
|
|
Semaf=semaine après floraison ; Ns, * et **
signifient respectivement différences non significatives,
différences significatives à 5% et différences
significatives à 1%
|
Les taux de rétention capsulaire ont été
plus faibles à forte densité qu'à faible
densité ; ils sont également plus faibles en semis tardif
qu'en semis à date recommandée (Tableau 4.11 et Tableau 4.12).
4.6- Effet sur le
rendement en coton graine
Les différences de rendement entre les cotonniers
écimés à 1 semaine après floraison et les
cotonniers non écimés (témoin) ont été de
529 kg/ha en semis précoce faible densité et de 118 kg/ha en
semis précoce forte densité (Figure 4.2). Le rendement a
été également plus élevé que sur le
témoin lorsque l'écimage est réalisé à
quatre semaines après floraison : + 386 kg/ha à faible
densité et +124 kg/ha à forte densité; mais les
différences n'ont pas été significatives (p>0,05).
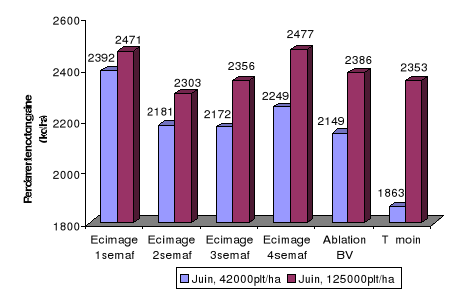
Figure 4.2: Effet de l'écimage sur le
rendement en coton graine (kg/ha)
Les résultats du semis tardif à forte
densité n'étaient pas encore disponibles au moment de la
rédaction.
Nous observons également que pour chaque traitement,
les rendements sont plus élevés en semis à forte
densité qu'en semis à densité recommandée ;
sur le témoin, l'augmentation de rendement a été de plus
de 20%.
4.7- Effet de
l'écimage sur la pression des ravageurs
Il faut noter que le parasitisme était
particulièrement faible cette année. Cependant des tendances ont
été observées lors de la collecte des
données ; mais du fait des contraintes de temps liées au
cycle de développement du cotonnier, nous n'avons pas pu traiter ces
données.
5- DISCUSSION
Les résultats obtenus pendant cette première
année de l'étude n'ont pas été significatifs sur
beaucoup de paramètres malgré des tendances parfois nettes. Cela
pourrait s'expliquer par une forte
hétérogénéité des parcelles
d'expérimentation ayant induit de fortes variances intra traitement et
par conséquent des variances résiduelles trop
élevées Il y a aussi les problèmes de re-semis
engendrés par des hétérogénéités de
levée qui pourraient également créer cette forte variance
intra parcelle, surtout sur les paramètres mesurés sur des plants
individuels comme par exemple la précocité de production R1/RT.
Mais malgré ces difficultés, les résultats sont en
harmonie avec ceux obtenus par Renou (2007) au Mali et qui suggèrent que
dans nos conditions de culture, l'écimage a des effets sur la
productivité du cotonnier, mais que ces effets sont relativement faibles
au regard de ce qui est relaté dans d'autres parties du monde (Dong et
al., 2003 ; Zang et sun, 2007).
Nos résultats suggèrent que l'écimage
à une semaine et l'écimage à quatre semaines après
floraison ont tendance à augmenter le rendement du cotonnier,
particulièrement en semis précoce à faible
densité ; ce résultat pourrait s'expliquer par une
amélioration des taux de rétention capsulaire ayant
entraîné une augmentation des nombres moyens de capsules par plant
en semis précoce à faible densité. El - Hanafi et
al. (1982) et Damodorant et al. (1974) postulaient que
l'effet significatif des pratiques de taille de cotonnier dépendait
plutôt de la date de réalisation de ces pratiques, mais ils n'ont
pu donner des indications précises sur le moment opportun où ces
pratiques pourraient avoir des effets bénéfiques. Les
résultats obtenus de la présente étude suggèrent
qu'une semaine après floraison et quatre semaines après floraison
seraient probablement les meilleures périodes dans nos conditions de
culture lorsque les semis sont installés à bonne date et à
densité recommandée.
Les résultats en semis précoce à forte
densité sont plus difficiles à interpréter. En effet, dans
cet itinéraire technique, les rendements sont améliorés
par un écimage à une semaine après floraison ainsi que les
taux de rétention capsulaire ; mais ces améliorations de
taux de rétention capsulaire ne sont pas accompagnées d'une
augmentation de la charge en capsule par plant, ni d'une amélioration du
poids moyen capsulaire si bien qu'on se demande ce qui explique
réellement cette légère amélioration du rendement,
certes non significative, dans cet itinéraire de culture. A
l'étape actuelle, il est difficile de répondre à cette
interrogation, mais les études ultérieures permettront
d'être plus explicatif.
L'effet de l'écimage sur la précocité a
été très faible ; il y a eu une tendance à une
ouverture plus rapide des capsules (OPCM) en semis précoce à
faible densité, une production plus précoce de coton graine
(R1/RT) dans les deux itinéraires testés en semis précoce,
mais à des degrés moindres par rapport à ceux
relatés dans la littérature ; néanmoins, nos
résultats se rapprochent de ceux obtenus par Zhang and Sun (2007) qui
ont également trouvé que l'écimage permet une production
précoce du cotonnier permettant d'éviter les problèmes de
gelée en fin de cycle dans les pays tempérés où
cette culture est pratiquée.
L'ablation des branches végétatives a permis
d'obtenir des capsules plus grosses et plus volumineuses. Ce résultat
pourrait s'expliquer par une redistribution plus importante des
assimilâts vers les organes fructifères étant
donné que les branches végétatives, parfois
appelées « food consomming organ », n'étaient
plus présentes.
Nos travaux ont confirmé par ailleurs que lorsqu'on
sème tardivement le cotonnier, la durée moyenne nécessaire
à l'ouverture des capsules (OPCM) se rétrécit, c'est
à dire que la vitesse d'ouverture s'accélère. Ce
résultat est conforme à ceux trouvés
précédemment (Sekloka, 2006) et pourrait résulter des
durées d'ensoleillement généralement plus longues
observées durant les derniers mois de la campagne cotonnière
entre septembre et octobre.
Des études ont également montré que
l'effet des pratiques de taille dépendait des structures
variétales expérimentées (Dharmaligam et al.,
1974). Nos travaux ont porté sur une seule variété et il
est recommandable que les résultats de ces derniers auteurs soient pris
en compte dans les études futures sur les pratiques de taille en
élargissant la gamme de variété à tester.
Les résultats que nous avons obtenu permettent
également de dire que l'augmentation de la densité en semis
à date recommandé réduit le nombre moyen de capsules par
plant, mais augmente le rendement à l'ha. Ce résultat est en
harmonie avec celui trouvé par Sekloka et al 2008. En effet, la
réduction du nombre de capsules par plant est compensée par
l'augmentation du nombre de plants par ha à forte densité, si
bien que le nombre de capsules par ha est plus élevé en semis
à forte densité, ce qui explique que le rendement soit plus
élevé.
CONCLUSIONS ET
RECOMMANDATIONS
Dans nos conditions de culture, les effets des pratiques de
taille sur le rendement du cotonnier sont plus importants en semis de bonne
date à faible densité qu'en semis à forte densité;
les écimages à une semaine et à quatre semaines ont
donné les meilleures augmentations de rendements par rapport au
témoin. Les effets sur la précocité de production sont
certes non significatifs, mais ils sont en faveur des cotonniers
écimés dans tous les itinéraires testés.
L'écimage permet donc d'accroître la
précocité de production des cotonniers, mais n'a pas
forcément d'effets positifs sur l'augmentation du poids et du volume
capsulaire moyen.
Compte tenu des fortes variances intra traitement
enregistrées pour cette première année de l'étude,
nous recommandons que ce travail soit reconduit sur au moins deux à
trois ans et sur un nombre plus important de sites afin de pouvoir tirer des
conclusions généralisables.
La présente étude n'a pris en compte qu'un seul
type variétal alors que des interactions entre pratiques de taille et
type de variété ont été mises en évidence
par ailleurs ; il serait alors intéressant que les études
futures sur l'écimage intègrent au moins deux
variétés assez contrastées sur les plans morphologiques et
phénologiques.
BIBLIOGRAPHIE
- Agriculture (2005) : le cotonnier. Journal de la
campagne de commercialisation du coton graine. 2004 - 2005, N°. 068,
Février 2005, p. 14 - 16.
- AIC, (2004) : Etude sur la situation filière
cotonnière. Financement AFD.
- BACHELIER B. (1998). Contribution à l'étude de
la variabilité et du déterminisme génétique de la
teneur en fragmentation de coques de la fibre de coton. Premières
applications pratiques en sélection chez G. hirsutum L.
Thèse de doctorat, France ENSA de Rennes. 271p
- BENNETT OL, ASHLEY DA, DOSS BD, SCARSBROOK CE. (1965).
Influence of topping and side pruning on cotton yield and other
characteristics. Agron. J. 57(1): 25-27
- BOURLAND F.M., OOSTERTUIS D. M., LAMMERS J.D. (1997).
Critical NAWF values for identifying the last effective boll population. In:
Proceedings Beltwide Cotton Conferences. National Cotton Council of
America, Menphis Tennesse, 1361-1362pp
- BOURLAND F.M., OOSTERTUIS D. M., TUGWELL N. P. (1992).
Concept for monitoring the growth and development of cotton plants using
main-stem counts. J. Prod. Agric. 5: 532-538
- CIRAD (1999) : Actes des journées coton
- Conférence Coton de l'Afrique de l'Ouest et du Centre
(CORAF/WECARD). Les évolutions en cours dans les filières
cotonnières : conséquences pour la recherche agronomique et
l'acquisition des intrants par les agriculteurs. Cotonou les 10, 11 et 12 mai
2005.
- COURTANT J.J., RAYMOND J., RAYMOND H., STYLIANOU N. (1991).
Le coton en Afrique de L'Ouest et du Centre. Ministère de la
Coopération et du Développement, France, 353p
- DAMODORANT AS, KAMALANATHAN A, CHAMY DS, AARON DS,
RAMAKRISHNAN PK. (1974). Influence of topping on the characters of American
cotton (G. hirsutum). Madras Agricultural Journal. 61 (9): 855-857
- CRA - CF/INRAB/ MAEP. Reconnaissance des principaux
ravageurs du cotonnier
- CRA-CF (S .a) : description de la variété
H279 -1
- CRA-CF (S .a) Répartition géographique
des principaux ravageurs .Fiche technique
- CRA-CF /INRAB/MAEP. Fiche technique produits phytosanitaires
utilisés pour la production du cotonnier 2001/02
- CRA-CF /INRAB/MAEP. Fiche technique. Exigences et
itinéraires techniques du cotonnier 2001/02
- DEGUINE JP, GOZE E, LECLANT F. (2000). The consequences of
late outbreaks of aphid Aphis gossypii in cotton growing in central Africa:
towards a possible method of the prevention of cotton stickiness.
International Journal of Pest Management. 46 (2):
85-89
- DEMOL J. 1992. Connaissance de la plante. In :
Cotonnier au Zaïre. Publication du service agricole N° 29,
Administration générale de la coopération au
développement, Bruxelles pp. 17 - 26.
- DEUSE, J. P. L. ET GUILLERM, J. L. (1976). Le
Désherbage du Maïs en Afrique de l'Ouest et les principales
adventices. I.R.A.T. - C.E.P.E. A.G.P.M., 80 p.
- DHAMALINGMAN VD, KRISHNADOSS, ROBINSON L, LYEMPERUMAL S.
(1974). Effet of topping rainfed cotton. Madras Agricultural Journal.
61 (9): 858-860
- DIXON A.F.G. (1986).The distribution of aphid infestation in
relation in the demography of plant parts. Am .Nat .127.410-413
- DONG H., W. LI., Z. LI., W. TANG, DONGMEI. Z. (2005).
Evaluation of a Production System in China that Uses Reduced Plant Densities
and Retention of Vegetatives Branches. Cotton Sci 9:
1 - 9.
- DONG HZ, LI WJ, LI ZH, TANG W, ZHANG DM. (2003). Review on
utilization of vegetatives branches of cotton plants. Cotton Sci. 15:
313-317
- EKUKOLE G. (1992). Preliminary results on the effect of
pruning cotton plants on Aphis gossypii Glover populations in Maroua, North
Cameroon. Coton Fibres Trop 47(2): 135
- EKULOLE G (1992) Prélimary results on the effet of
pruning cotton plants on Aphis gossypii Glover population Maroua, North
Cameroon. Coton fribres Trop 47 (2): 135-138
- EKULOLE G. (1984) A review of the status of the oil palm
leaf miner beetle in the west Africa .Nigerian J. Ent.5.1 and 2.89-94
- EL- HANAFI HR, ABD-EL-DAYEM MA, EL-OKKIA AFH. (1982).
Influence of topping on cotton yield and other characteristics.
Agricultural Research Review. 60 (9): 153-163
- ESTHUR G. (Janvier 2005): Is west African cotton competitive
with the U.S. on the world cotton market? CCIC, Washington, 7p.
- ESTUR G. (2006). Le marché mondial du coton. Cahiers
Agricultures 15 (1) : 9 - 16
- FERON P., DEGUINE J. P., EKORONG A., MOUTE J. (2006).
Evolution de la protection phythosanitaire du cotonnier : un cas
d'école. Cahiers Agricultures 15 (1) :
128-134
- FLOQUET A. AMADJI F. GERADEAU E. OKRY F. (2002). Etude des
facteurs de stagnation de la culture cotonnière au Bénin. SCAC et
CRA-CF, Bénin, 55p
- FRANKE G. (2003): Nutz pflanzen der Tropen und Stropen, Band
II, 2. edition Leipzig.
- GARBOREL C. (1987). La pré-vulgarisation des
traitements herbicides en culture cotonnière et en maïsiculture au
Bénin. Coton et Fibres Tropicales. XLII
2 :111-115
- HAKE K., STAIR K. (1994). Yield probability forecasts using
plant monitoring. In Proceedings Beltwide Cotton Conferences. National
Cotton Council of America, Menphis Tennesse, 1279p
- HAU B., GOEBEL S. (1987). Modifications du comportement du
cotonnier en fonction de l'environnement : 1. Evolution des
paramètres de productivité de neuf variétés
semées à trois écartements. Coton et Fibres
Tropicales XLI (2) : 165-173
- HAZARD. (2003). Le coton en Afrique de l'Ouest et du Centre
et son insertion dans les échanges internationaux. ENDA Prospectives,
Dialogues, Politiques, Dakar
- HEARN A. B., CONSTABLE G. (1984). Cotton. In «The
physiology of tropical food crops». P.R. Goldsworthy and N.M.E. Fisher.
Bath, Avo, John Wiley and Sons: 495-527.
- HESKETH J. D., BAKER D. N. DUNCAN W. G. (1972). Simulation
of growth and yield in cotton: II. Environmental Cotton of Morphogenesis.
Crop Sci. 12: 436-439
- HEZHONG D, WEIJIANG L, ZHENHUAI L, WEI T, DONGMEI Z. (2005).
Evaluation of a production system in China that uses reduced plant densities
and retention of vegetatives branches. Journal of cotton science
9: 1-9
- HOROWITZ H. (1969). Influence des conditions du milieu sur
la formation et la chute des organes floraux chez le cotonnier. Coton et
Fibres Tropicales : 17 (1) : 23-40
- ICAC (2005). Cotton: world statistics. Bulletin of the
international Cotton Advisory committee. September 2005:
1331p
- KHALIFA H., GAMEEL O. I. (1982). Control of cotton
stickiness trought breeding cultivars resistant to whitefly (Bemisia
tabaci Genn) infestation. Improvement of oil - seed industrial crops by
induced mutations. IAEA. Vienna. 180 - 186.
- LANÇON J. (1995). Effet de la densité de semis
en sélection sur l'amélioration génétique du
cotonnier : interaction, structures de corrélation,
hétérosis et valeur en lignées. Thèse de doctorat,
Paris, Universités de Paris -ORSAY .119 p.
- LANÇON J. HOUGNI A. SEKLOKA E. DJABOUTOU M. (2000d).
Mesure d'allogamie en parcelles de sélection. In : Actes des
Journées Coton du CIRAD, Montpellier, CIRAD: 77-84
- LANDIVAR J.A., HICKEY J.A. (1997). Using plant mapping to
determine potential lint yield of cotton crops. In Proceedings Beltwide
Cotton Conferences. National Cotton Council of America, Menphis Tennesse,
1362p
- MA, FUYU, CHENG, HAÏ TAO, LI, SHAOKUN, ZHANG, HONG,
YANG, JIANRONG, ZHENG, ZHONG, LI ANR LUHUA. (2004). A study of the fitness of
cotton on canopy regulated by topping under high yield condition. Scientia
Agricultura Sinincia 37 (12): 1843-1848
- MAEP (2001): Schéma directeur du développement
agricole et rural du Bénin, plan stratégique opérationnel,
Cotonou.
- MARTIN J. (2000). Note de synthèse sur l'Unrc et le
pux. In « Rapport de mission aux Betwilde Cotton Conference
2000. San Antonio, TX, USA, 5-8 Janv 2000. Restitution des participants et
visite de laboratoire ». P. SILVIE, H. CHAIR and J. Martin.
Montpellier, France, Cirad-Ca : 28p
- MATHEWS G. A. (1989). Cotton insect pests and their
management. Longman Scientific & Technical Ed. Harlow, Essese (G B) 199p
- MATTHESS A., VAN DEN AKKER E., CHOUGOUROU D., MIDINGOYI JUN
S. (2005). Compétitivité et durabilité de cinq
systèmes culturaux cotonniers dans le cadre de la filière. MAEP
et GTZ. 201p
- MAUNEY J.R. (1984). Anatomy and morphology of cultivated
cottons. In «cotton». R. H. KOHEL and C.F. LEWIS, Am. Soc. Agron.
Agronomy series 24, Madison (USA): 59-81
- MAUNEY J.R. (1986). Vegetative growth and development of
fruiting sites. In "cotton physiology «. J.R. MAUNEY and J. M.
STEWART : 18-28
- Ministère de la Coopération et du
Développement (1993) : Mémento de l'Agronome
- NAGUIB M., NASR-KATTAB. (1978). Effect of cutting the
terminal shoots (topping) of cotton plant on the population density of eggs -
masses of the cotton leafworm, Spodoptera littoralis (Boisd.) and on the cotton
yield. Agricultural Research Review, 56 (1): 9-15
- NASR E.A., AZAB A.K. (1969). Effect of cutting the terminal
shoots of cotton plants (topping) on rate of bollworm infestation, cotton yield
and fiber quality. Bulletin de la Société Entomologique
d'Egypte, 53: 325-337
- OBASI M. O., MSAAKPA T.S. (2005). Influence of topping, side
branch pruning and hill spacing on growth and development of cotton
(Gossypium barbadense L.) in the southem guinea savanna location of
Nigeria. Journal of Agriculture and Rural development in the tropics and
subtropics. 106 (2): 155-165
- PARRY G.1982. Le cotonnier et ses produits. G - P.
Maisonneuve & Larose, Paris (Ve), 502 p.
- REAMAKERS, R.H. (2001). Agriculture en
Afrique Tropical Ed. CIP. Bibliographie Royale Albert I, Bruxelles, 1634p
- RENOU A. (2007). Synthèse des études conduites
au Mali a propos de l'écimage des cotonniers en cours de campagne.
Rapport de synthèse, CIRAD UPR 102, 23 p.
- SEKLOKA E. (1998). Effets de la transgenèse et de la
culture in - vitro sur la variété Coker 310, DEA de
Génétique. Adaptations et Productions Végétales.
ENSA de RENNES. 31p.
- SEKLOKA E. (2006). Amélioration de
l'efficacité de la sélection par le rendement de coton-graine du
cotonnier Gossypium hitsutum L. dans un contexte de nouveaux
itinéraires technique, Thèse de doctorat, CRA-CF / INRAB .
CIRAD.CA (Montpellier,France .142 p
- SUNDARAMURTHY V.T. (2002). The integrated insect management
system and its effects on the environment and productivity of cotton.
Outlook on Agriculture. 31 (2): 95-105
- SYED R. A., EKUKOLE G. (1983). Some studies on the oil palm
leaf miner (Coelaenomenodera elaeidis Maulik) at Lobe Estate.
Cameroon. Harrisons and Fleming. London. 40p.
- SYED R.A. (1982). Studies on the oil palm leaf mimer.
2nd Progress Report. June 1982. 8p.
- TOMATO H. S. (1988). Etude de l'influence des adventices sur
le développement et le rendement du cotonnier. Mémoire de fin
d'études agronomiques ESA, Université du Bénin,
Lomé, Togo, 78p
- WENDEL J. F., ALBERT U.A. (1992). Phylogenetics of the
cottongenus (Gossypium): Character - state weighted parsimony analysis of
chloroplast - DNA restriction Site and its systematic and biogeographic
implications. Syst Bot 17: 115-143
- ZHANG X, SUN F (2007). Training course on cotton breeding
and management technology, Teaching material, Hebei Academy of Agriculture and
Foresty Sciences, Shijiazhuang, Hebei, 231 p.

| 


