Chapitre II
Les travaux sur le potentiel de corrosion des métaux
revêtus remontent à 1970 [13,14]. Ces travaux ont montré
l'importance du potentiel de corrosion et comment il se change avec le temps.
Le potentiel positif indique l'absence de la corrosion et le potentiel
négatif indique sa présence.
Ces mesures empiriques ont été suivies par des
études très complètes par Wormwell et Brasher[15]. Ils ont
noté que la forme de la courbe potentiel- temps pendant les
premières heures ou les premiers jours d'immersion, donne des
informations très importantes sur les propriétés
barrières des revêtements.
II.2.2.2. Courbes de polarisation
Le tracé des courbes de polarisation potentiodynamique,
consiste à suivre la réponse en courant de l'échantillon
à une rampe de potentiel permettant de le déplacer lentement de
manière linéaire de son état d'équilibre.
A l'aide d'un générateur extérieur et d'une
contre électrode, on fait passer un courant à travers
l'électrode métallique. Son état stationnaire est
modifié et sa surface prend une nouvelle valeur du potentiel. Les
courbes E =f (I) ou I = f (E) constituent les courbes de polarisation. Ces
méthodes présentent un double avantage, d'une part, elles
permettent de déterminer la résistance de polarisation, et
d'autre part, de déterminer le mécanisme de corrosion.
Pour tout couple redox, l'équation de Butler-Volumer
(Eq.II-6), pour le cas où les échanges à l'interface sont
contrôlés par l'étape de transfert de charge, donne une
relation entre le potentiel interfacial et les densités de courant.
Par exemple, si l'on considère une réaction
électrochimique interfaciale de la forme :
B ox + n e- Bred II-5
L'équation de
Butler-Volmmer permet de relier le courant interfacial en fonction du
potentiel
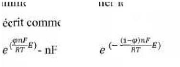
électrochimique et elle s' e suit :
I = Ia + Ic = n F KaCred,s Kc
Cox,s II-6
Avec:
I : courant global de la réaction Ic : courant cathodique
de la réaction
Ia : courant anodique de la réaction n : nombre
d'électrons d'échange
T : température E : potentiel ou surtenstion
Æ: facteur de symétrie. R : constante des gaz
parfaits
23
| 


