|
Prolifération des plantes aquatiques
envahissantes sur le fleuve Niger ; état des lieux de la pollution
en azote et en phosphore des eaux du fleuve.
MEMOIRE DE FIN DE CYCLE
POUR L'OBTENTION DU DIPLÔME DE MASTER
SPÉCIALISÉ
GIRE

Présenté et soutenu publiquement le 29 septembre
2010 par :
HASSANE YOUNOUSSOU Hamadou
Travaux dirigés par :
Encadreurs de terrain : Sous la
direction :
Dr. ADAMOU Rabani Pr. Zibo GARBA
Enseignant/Chercheur, Faculté des Sciences
Enseignant/Chercheur,
Techniques, Université Abdou Moumouni
Faculté des Sciences
de Niamey (UAM) Techniques, UAM
Dr. ALHOU Bassirou
Enseignant/Chercheur, Ecole Normale
Supérieure, UAM
Jury d'évaluation du
stage :
Président : Dr. WETHE
Joseph
Membres et correcteurs : KONATE Yacouba
SOU Mariama
KOUAKOU Marcelin
Promotion [2009/2010]
Dédicaces
Ce mémoire de fin de cycle est
dédié :
À mes parents pour m'avoir encouragé depuis le
jeune âge pour le travail bien fait ;
À mes frères et soeurs pour le soutien qu'ils
m'ont toujours apporté ;
À mes amis ;
Et à tous ceux qui oeuvrent inlassablement pour une
Gestion Intégrée des
Ressources en Eau.
REMERCIEMENTS
Au moment où j'achève ce mémoire qui a
été réalisé à l'Université Abdou
Moumouni de Niamey à la Faculté des Sciences Techniques au
département de chimie, laboratoire de photochimie analytique et
d'écotoxicologie il me tient à coeur d'exprimer ma gratitude
à tous ceux, qui d'une manière ou d'une autre, ont
contribué à sa réalisation.
J'exprime mon profond respect et toute ma
reconnaissance au Pr. ZIBO Garba Enseignant/Chercheur, pour la
confiance qu'il m'a témoignée en acceptant la direction et le
suivi de mes travaux.
J'exprime ma profonde reconnaissance à mes
encadreurs de terrain: Dr ADAMOU Rabani chimiste, enseignant/chercheur à
la Faculté des Sciences Techniques et Dr. ALHOU Bassirou biologiste
enseignant/chercheur à l'Ecole Normale Supérieure de
l'Université Abdou Moumouni de Niamey. Nous vous disons merci pour le
grand intérêt accordé à ce travail mais aussi
pour votre présence, votre enthousiasme et votre disponibilité,
tout au long de cette recherche. Nous vous disons grand merci pour la patience
dont vous avez fait preuve. Ce fut un réel plaisir de travailler sous
vos directions. Vos conseils et vos rigueurs ont beaucoup apporté
à ce travail.
Je pense également à tout le personnel de
l'ICRISAT et du laboratoire de biologie de l'école normale
supérieure de l'université Abdou Moumouni de Niamey pour leur
mansuétude et pour tous les conseils prodigués au moment de
l'analyse des échantillons.
Mes remerciements vont également au projet de gestion
intégrée des plantes aquatiques proliférantes en Afrique
de l'Ouest composante Niger pour son appui en réactifs et
matériels de laboratoire.
Ma reconnaissance va aussi à l'endroit de toute ma
famille qui n'a ménagé aucun effort pour me soutenir tout au long
de mes études et en particulier au cours de cette année.
Mes remerciements s'adressent aussi à tous mes
camarades de la promotion pour leur soutien dans les travaux de groupe et leur
collaboration pendant toute l'année académique
A tous les membres du jury qui malgré leurs multiples
occupations ont accepté d'examiner ce travail, je leur suis infiniment
reconnaissant. Les critiques et suggestions, qu'ils apporteront, contribuerons
certainement à rehausser la valeur scientifique de ce travail.
Je ne saurais terminer sans dire ma reconnaissance à
tous mes voisins, ainsi qu'à tous ceux qui de prés ou de loin ont
participé à la réalisation de ce travail et dont les noms
ne figurent pas ici. A tous ces anonymes, je dis un grand merci.
Résumé
Le fleuve Niger est long de 4.200 km. Il prend sa source en
Guinée et traverse successivement le Mali, le Niger, le Benin et le
Nigeria avant de se jeter dans l'océan Atlantique. Ce fleuve contribue
à l'approvisionnement en eau et aux besoins alimentaires de plus de 100
millions de personnes. Malheureusement, ce fleuve est fortement menacé
ces dernières années par les aléas climatiques et la
pollution anthropique.
La dégradation de la qualité de l'eau a
été un facteur déterminant de la prolifération
anarchique des plantes aquatiques en général et de la jacinthe
d'eau en particulier. Cette plante a bouleversée
l'écosystème local et semble être une contrainte majeure au
développement durable et à l'amélioration des conditions
de vie des populations. Il est donc urgent d'agir afin d'éviter tout
éventuel catastrophe. C'est dans ce cadre que s'inscrit notre
étude « prolifération des plantes aquatiques
envahissantes sur le fleuve Niger : état des lieux de la pollution
en azote et phosphore des eaux ».
A cet effet, des échantillons d'eau, et de
sédiment ont été prélevés au niveau de trois
(3) sites identifiés après consultation de la documentation
existante et des entretiens avec les personnes ressources. Pour se faire un
certain nombre de matériel et une méthodologie sur la base des
prélèvements sur le terrain et des analyses au laboratoire nous
ont permis d'atteindre nos objectifs fixés.
Les valeurs moyennes obtenues pour l'azote total sont de 15,83
mg/l, 17,66 mg/l et 15,33 mg/l respectivement à TON-G, Ny-G et Saga-G.
Quant au phosphore total, on enregistre 3,71 mg/l, 3,51 mg/l et 3,33 mg/l
respectivement à TON-G, Ny-G et Saga-G. On remarque de ce fait qu'il n'y
a pas de différence significative entre les paramètres
étudiés le long des sites retenus. Aussi, il n'existe pas de
corrélation significative entre la présence de la jacinthe et la
disponibilité des nutriments du milieu. Ce qui peut être du
à l'effet de dilution provoquée par les inondations qui eu lieu
cette année à Niamey. Globalement la pollution du fleuve Niger
n'est trop inquiétante mais des dispositions nécessaires doivent
être entreprises pour un futur proche.
Mots clés : Prolifération,
Plantes aquatiques, fleuve Niger, pollution, Azote, phosphore.
Abstract
The Niger River is 4.200 km long. It rises in Guinea and
passes successively through Mali, Niger, Benin and Nigeria before emptying into
the Atlantic Ocean. The river contributes to water and food needs of over 100
million people. Unfortunately, this river is severely threatened in recent
years by climatic and anthropogenic pollution.
The deteriorating water
quality has been a factor in the uncontrolled growth of aquatic plants in
general and water hyacinth in particular. This plant has upset the local
ecosystem and seems to be a major constraint to sustainable development and
improving living conditions of populations. It is therefore urgent to act to
avoid potential disaster. It is in this context that our study "proliferation
of invasive aquatic plants on the River Niger: current status of nitrogen and
phosphorus pollution of waters."
To that end, samples of water and sediment
were collected at three (3) sites identified after consulting the literature
and interviews with resource persons. To get a number of equipment and
methodology based on field sampling and laboratory analysis have allowed us to
achieve our goals.
The mean values for total nitrogen are 15.83 mg/l, 17.66
mg/l and 15.33 mg/l respectively TON-G, NY-G-G and Saga. As for total
phosphorus, was recorded 3.71 mg/l, 3.51 mg/l and 3.33 mg/l respectively TON-G,
NY-G-G and Saga. We note this because there is no significant difference
between the parameters studied along the chosen sites. Also, there is no
significant correlation between the presence of water hyacinth and nutrient
availability of the medium. This may be due to the dilution effect caused by
the floods which occurred this year in Niamey. Overall pollution of the Niger
River is too disturbing but necessary steps must be taken to the near future.
Keywords: Proliferation, Aquatic plants, Niger River,
pollution, nitrogen, phosphorus.
TABLE
DES MATIERES
REMERCIEMENTS
II
RÉSUMÉ
IV
LISTE DES FIGURES
VII
INTRODUCTION
1
1.1. PROBLÉMATIQUE
3
1.2. OBJECTIFS DE L'ÉTUDE
6
1.2.1. Objectif général
6
1.2.2. Objectifs spécifiques
6
CHAPITRE I: ETUDE BIBLIOGRAPHIQUE
7
I.1. CADRE DE L'ETUDE
7
I.1.1. Généralités Sur le
Bassin du Niger
7
I.1.2. Présentation de la zone
d'étude
8
I.1.2.1. Caractéristiques physiques
8
I.1.2.2 La végétation
12
I.1.3. Contexte Hydrologique
12
I.1.3.1. Débits du fleuve Niger
13
I.1.3.2. Hauteurs du fleuve
à Niamey
14
I.2. TYPOLOGIE DES SOURCES DE POLLUTION AU
NIGER
15
I.2.1. La pollution industrielle et
artisanale
15
I.2.1.1. La Braniger
15
I.2.1.2. Enitex
15
I.2.1.3. Abattoir frigorifique
15
I.2.1.4. Industrie de lait (SOLANI, Niger-Lait,
Laban)
16
I.2.1.5. Tannerie
16
Figure 6 : Photo rejets de la
tannerie.
17
I.2.2. La pollution urbaine
17
I.2.3. L'agriculture
18
I.2.4. Les mines
18
I.2.4.1. L'extraction d'or à petite
échelle dans l'ouest du pays
18
I.2.4.2. L'usine d'exploitation de l'or dans le
sous-bassin de la Rivière Sirba
18
I.3. RELATION ENTRE LA DISPONIBILITÉ EN
NUTRIMENT ET LA PROLIFÉRATION DES PLANTES AQUATIQUES
18
I.3.1. Généralités sur les
plantes aquatiques.
19
I.3.2. Nutrition minérale.
19
I.4. DESCRIPTION DE LA PLANTE AQUATIQUE
ENVAHISSANTE SUR LE NIGER : LA JACINTHE D'EAU : EICHHORNIA CRASSIPES
21
I.4.1. Systématique
21
I.4.2. Historique
21
I.4.3. Multiplication et Description de la
plante
21
I.4.4. Écologie de la plante
22
I.4.5. Nuisance exceptionnelle
22
CHAPITRE II. MATERIEL ET METHODE
24
II.1. MATERIEL
24
II.1.1. Présentation de la Station
d'étude
24
II.1.2. Instruments utilisés in situ
24
II.1.3. Matériel utilisés au
laboratoire
25
II.2. METHODOLOGIE
25
II.2.1. Choix des sites et points de
prélèvement
25
II.2.2. Choix des paramètres
26
II.2.3. Collecte des échantillons ou
échantillonnage
27
II.2.4. Evaluation de la densité de la
jacinthe d'eau au m²
28
II.2.5. Méthode de détermination
des caractéristiques chimiques
28
II.2.5.1. Méthodes
spectrophotométriques
28
II.2.5.2. Méthode de digestion par
réacteur
29
II.2.6. Traitement des données
30
CHAPITRE III: RESULTATS ET DISCUSSIONS
31
III.1. RESULTATS
31
III.1.1. Densité de la jacinthe d'eau au
m2 sur le fleuve
31
III.1.2. Etude des teneurs en azote et en
phosphore de la jacinthe d'eau
32
III.1.2.1. Teneurs en azote
32
III.1.2.2. Teneur en phosphore de la Jacinthe
d'eau
32
III.1.3. Etat des lieux de la
disponibilité en nutriments fondamentaux dans l'eau et les
sédiments
33
Etat des lieux de la disponibilité en
nutriments des sédiments, pour la jacinthe
33
III.1.4. Etat de la pollution anthropique du
fleuve Niger
33
III.1.4.1. Les paramètres physico-chimiques
généraux
33
III.1.4.2. Paramètres de pollution
organique
36
III.1.4.3. Paramètres azotés et
phosphorés
37
III.1.5. Corrélation entre les
caractéristiques physico-chimiques des sites et les densités de
jacinthe
39
III.2. DISCUSSION
39
CHAPITRE IV: RECOMMENDATIONS POUR UNE LUTTE
EFFICACE
44
IV.1. LA RÉDUCTION DES APPORTS
D'ORIGINE DOMESTIQUE
44
IV.1.1. Traitement de l'azote dans les eaux
usées urbaines
44
IV.1.2. Réduction du phosphore dans les
eaux usées urbaines
45
IV.2. LA RÉDUCTION DES APPORTS D'ORIGINE
AGRICOLE
46
IV.2.1. La fertilisation des sols
46
IV.2.2. La pollution liée à
l'élevage
46
CONCLUSION
47
RÉFÉRENCES
BIBLIOGRAPHIQUES
49
ANNEXES
52
Liste des figures
FIGURE 1 : BASSIN DU FLEUVE NIGER
(SOURCE : HTTP://FR.WIKIPEDIA.ORG/WIKI/NIAMEY)
8
FIGURE 2 : LOCALISATION DE LA ZONE D'ÉTUDE
À L'OUEST DU NIGER
9
FIGURE 3 : VALEURS MOYENNES ANNUELLES DES
PRÉCIPITATIONS DE NIAMEY-AÉROPORT
10
FIGURE 4 : DÉBITS MENSUELS DU FLEUVE NIGER
À NIAMEY
14
FIGURE 5 : PHOTO DU POINT DE REJET DANS LE
FLEUVE NIGER DE L'ABATTOIR
16
FIGURE 6 : PHOTO REJETS DE LA TANNERIE
17
FIGURE 7 : PHOTO REJETS URBAINS À
NIAMEY
17
FIGURE 8: TYPES DE PLANTES AQUATIQUES
19
FIGURE 9 : SITES RETENUS POUR LES
PRÉLÈVEMENTS
24
FIGURE 10 : DENSITÉ DE JACINTHE AU M²
PAR SITE
30
FIGURE 11 : TENEUR EN AZOTE ET EN PHOSPHORE DE
LA JACINTHE D'EAU PAR SITE ET PAR POINT DE PRÉLÈVEMENT
31
FIGURE 12 : COMPARAISON ENTRE LE RAPPORT
DEMANDE/OFFRE EN AZOTE ET PHOSPHORE ET LA DENSITÉ DE JACINTHE AU
M²
32
FIGURE 13 : COMPARAISON ENTRE LES VALEURS
MOYENNES EN AZOTE TOTAL ET PHOSPHORE TOTAL ET LA PROLIFÉRATION DE LA
JACINTHE D'EAU
33
FIGURE 14 : VALEURS MOYENNES DE
TEMPÉRATURE ET DU PH PAR SITE ET PAR POINT DE
PRÉLÈVEMENT
34
FIGURE 15 : EVOLUTION DES TENEURS EN SUSPENSION PAR
SITE ET PAR POINT DE PRÉLÈVEMENT
35
FIGURE 16 : EVOLUTION DES VALEUR DE LA
CONDUCTIVITÉ PAR SITE ET PAR POINT DE PRÉLÈVEMENT DE
L'AMONT À L'AVAL DE NIAMEY
36
FIGURE 17 : VARIATION DE LA DCO PAR SITE ET PAR
POINT DE PRÉLÈVEMENT DE PRÉLÈVEMENT
37
FIGURE 18 : TENEURS EN OXYGÈNE DISSOUS EN
FONCTION DES SITES RETENUS
38
FIGURE 19 : EVOLUTION DES CONCENTRATIONS EN
COMPOSÉS AZOTÉS (AMMONIUM ET AZOTE TOTAL) PAR SITE
39
FIGURE 20 : CONCENTRATION DES COMPOSÉS
PHOSPHORÉS (ORTHOPHOSPHATES ET PHOSPHORE TOTAL PAR SITE ET PAR POINT DE
PRÉLÈVEMENT
40
INTRODUCTION
Le fleuve Niger est long de 4.200 km. Il prend sa source en
Guinée et traverse successivement le Mali, le Niger, le Benin et le
Nigeria avant de se jeter dans l'océan Atlantique. Son bassin est
partagé par neuf pays: Bénin, Burkina Faso, Cameroun, Côte
d'Ivoire, Guinée, Mali, Niger, Nigéria et Tchad. Ce fleuve
contribue à l'approvisionnement en eau et aux besoins alimentaires de
plus de 100 millions de personnes.
L'Etat du Niger est recouvert à 75 % par le
désert du Sahara. Le fleuve est le seul grand cours d'eau du Niger (ABN,
2002). Il traverse le pays sur 550 km et relie les zones humides du sud aux
régions désertiques du nord. La population nigérienne
vivant sur le bassin du fleuve est estimée à 8,3 million
(RGP/H-2001) soit plus de la moitié de la population totale du pays. Le
fleuve Niger constitue donc une grande richesse pour le Niger et les autres
pays riverains.
Ces dernières années, le fleuve Niger est
fortement menacé par les aléas climatiques, la pression
démographique et la pollution anthropique. Cela compromettra la
durabilité de la ressource tant sur le plan qualitatif que quantitatif.
La quantité d'ordure ménagère que reçoive le
fleuve, quotidiennement est estimée à 273750 tonnes (ALHOU et
al., 2009). Il reçoit aussi des quantités importantes d'eaux
usées que produisent les grandes agglomérations riveraines (ABN,
2002). La diversité et la multiplicité des sources de pollution
(KERIM, M., 2006) et la prévalence des maladies d'origine hydrique,
deviennent de plus en plus préoccupantes (KOTSCHOUBEY,
N. & KONÉ, A. 2005). La situation actuelle va au
de-là des prévisions les plus pessimistes. Le fleuve est
pollué. Le rejet d'eaux usées s'est amplifié. Des
habitudes malsaines comme le lessivage dans le fleuve se sont
développées. Aucune police des eaux n'est fonctionnelle, aucun
règlement n'est applicable. Mêmes les méthodes ancestrales
de gestion de l'eau qui avaient leur cohérence environnementale ont
été oubliées. En conséquences, la flore, la faune
et l'écosystème local subissent durement les effets de cette
pollution. Ainsi, des espèces de poissons ne remontent plus le fleuve,
d'autres ne se renouvellent plus. Quant à la qualité des poissons
existants, la psychose commence à s'installer car les habitants
craignent d'en manger.
Le développement accéléré de nos
centres urbains, l'implantation anarchique des unités industrielles et
la mauvaise politique environnementale des états du bassin du Niger sont
en grande partie à la base de l'aggravation du phénomène
de dégradation de l'environnement du bassin du Niger (OUSMANE, B.,
2000).
En effet, en Afrique de l'ouest en général et
au Niger en particulier, le traitement des eaux usées urbaines n'est pas
une préoccupation; de ce fait, les rivières et les cours d'eau
traversant un centre urbain ou passant à proximité constituent de
véritable drains de pollution de toute sorte (liquide et solide) pour le
fleuve. D'après PICOUET (1999), «les pollutions chimiques notables
ne se produisent généralement qu'en ville et en milieu rural
à l'aval des zones agricoles et des périmètres
irrigués». La pollution des cours d'eau traversant certaines
grandes villes en Afrique de l'ouest illustre parfaitement cet état de
fait. On peut citer à titre d'exemple: Bamako, Niamey (ABN, 2005),
Lomé (AMEYAPOH et al., 2005), Kano (FMWR-IUCN-NCF-KYBP, 2006).
Cela n'est pas seulement observé dans les villes africaines mais
également dans certaines villes asiatiques. En Corée du sud, la
qualité de la rivière Han s'est drastiquement
détériorée au niveau de la section recevant les eaux
polluées provenant des affluents (Chang, 2005 rapporté par Sud
Sciences & Technologies n° 16, 2IE, 2008). En chine, les principales
rivières recevant les eaux provenant de la ville de Xi'an connaissent le
même sort (He, H. et al., 2007 rapporté par Sud Sciences
& Technologies n° 16, 2IE, 2008).
Pour répondre efficacement à cette pollution,
des mesures importantes de surveillance et de protection des cours d'eau
doivent être prises. Dans le bassin du Niger, les données
concernant la qualité des eaux et les caractéristiques de sources
de pollution sont rares De même, les interventions à des fins
d'amélioration de la qualité des eaux ne sont pas toujours
effectuées (ALHOU, 2007). A titre d'exemple, les villes riveraines du
Niger ne disposent pas de station publique d'épuration des eaux
usées. La seule station pilote de la JICA (Agence Japonaise de la
Coopération Internationale) a été longtemps
abandonnée. Les rares établissements qui traitent de
manière privée leurs eaux usées avant de les rejeter dans
le fleuve Niger ne respectent pas très souvent les normes nationales en
la matière (ALHOU, 2007).
La dégradation de la qualité de l'eau a
été un facteur déterminant de la prolifération
anarchique des plantes aquatiques en général et de la jacinthe
d'eau en particulier. Cette plante a bouleversée
l'écosystème local et semble être une contrainte majeure au
développement durable et à l'amélioration des conditions
de vie des populations.
De nombreuses actions ont été menées
souvent avec l'appui de la communauté internationale et des ONG pour
débarrasser le fleuve de cette plante colonisatrice nuisible. Cependant,
ces actions souvent spontanées et brèves n'ont pas permis
l'éradication complète du fléau par faute d'analyse
objective du phénomène. A travers la présente
étude, nous comptons faire d'une part l'analyse de la cause profonde de
la prolifération de la jacinthe d'eau et d'autre part d'attirer
davantage l'attention des décideurs sur le véritable danger que
constitue cette plante sur le fleuve Niger. Pour mener à bien cette
étude, nous avons :
- réalisé des analyses physico-chimiques de
l'eau et des sédiments du fleuve afin de déterminer l'apport
anthropique et les réserves du fleuve en nutriments indispensables
à la synthèse tissulaire de la jacinthe d'eau ;
- déterminé certains paramètres majeurs
et globaux de la pollution des eaux du Niger dans le but de mieux proposer aux
décideurs les mesures de protection efficace et de traitement convenable
du mal.
1.1.
Problématique
Le fleuve Niger est le troisième grand fleuve de
l'Afrique après le Nil et le Congo. Malheureusement, les
activités humaines mettent en danger les eaux du fleuve. Aux impacts de
dégradation attribuables aux changements climatiques s'ajoutent la
pollution des eaux et la prolifération des plantes aquatiques
attribuables aux activités des populations de son bassin.
Les eaux du Niger sont menacées par une
prolifération de la jacinthe d'eau, une plante aquatique
considérée comme la plus envahissante au monde. Si l'on n'y prend
pas garde, la qualité des eaux et l'équilibre des organismes qui
y vivent seront perturbés durablement. En effet, la prolifération
des plantes aquatiques induira une multiplication des cyanobactéries
présentes dans l'eau qui provoqueront à leur tour la disparition
des autres espèces algales et de l'oxygène dissout ainsi que la
minéralisation de la matière organique. Cela entrainera d'une
part la dégradation de la qualité de l'eau par l'eutrophisation
du cours d'eau et d'autre part la disparition des poissons et des autres
espèces aquatiques par la réduction de leurs habitats et par le
manque d'oxygène dissout. Ce qui pourrait influer durablement sur la
biodiversité des lieux et l'approvisionnement en eau potable des
populations riveraines.
Dans les conditions environnementales adéquates
(température, ensoleillement, pH, etc.), la prolifération des
plantes aquatiques dépend de la biodisponibilité des nutriments
essentiels à leurs croissances. Les plantes aquatiques flottantes
puisent directement leurs nutriments de l'eau et celles enracinées des
sédiments. C'est à partir des nutriments puisés que ces
plantes synthétisent leurs tissus. La composition moyenne d'un
végétal aquatique (algues et plantes aquatiques) montre que les
constituants tissulaires majeurs sont l'oxygène (80.5%, m/m),
l'hydrogène (9.7%, m/m), le carbone (6.5%, m/m) et le silicium (1.3%,
m/m) (BARROIN G., 2000). A côté de ces constituants majeurs, il
existe une quinzaine d'éléments à faible teneur
(0,000002% = teneur <1%) qui sont très déterminants à
la synthèse tissulaire (BARROIN G., 2000). Au delà de la demande
en nutriments des plantes aquatiques, c'est la disponibilité des
nutriments dans les cours d'eau (offre) qui conditionne la synthèse de
nouveaux tissus.
Ainsi, la prolifération des algues et plantes
aquatiques dans les cours d'eau dépend prioritairement de la teneur de
l'élément pour lequel le besoin tissulaire (Demande) est la plus
forte par rapport à la disponibilité dans le milieu (Offre). Cet
élément est considéré comme
l'élément-limitant de la prolifération.
En considérant la composition moyenne d'une eau
naturelle et en établissant pour chaque élément le rapport
[Demande de la plante/Offre du milieu], on constate qu'avec un rapport de 80
000, le phosphore vient en tête, devançant l'azote (30 000) et le
carbone (5 000) (Voir tableau I en annexe d'après BARROIN G. 2000). Le
phosphore est donc l'élément-limitant de la prolifération
des algues et plantes aquatiques dans les eaux douces. Le phosphore reste le
facteur-limitant même si l'azote disponible dans l'eau a
été consommé car cela engendrera la prolifération
d'organismes capables de capter l'azote molécule (N2)
disponible en grande quantité dans l'atmosphère et de le
transformer dans un processus de nitrification en nitrates assimilables par les
algues et les plantes aquatiques. Le phosphore présent dans les eaux
naturelles est essentiellement apporté (>90%) par les
activités humaines: agriculture, industrie, eaux usées,
détergents, etc. (BARROIN G. 2000). La cause de la prolifération
des plantes aquatiques dans nos cours d'eau est donc d'origine anthropique.
Pour solutionner ce problème, l'arrachage des plantes
aquatiques couramment organisé par les populations riveraines et les
autorités n'est donc pas la solution idoine. Cette pratique est d'une
part inutile car elle n'empêche pas une future repousse des plantes et
d'autre part elle est néfaste pour l'écosystème car elle
provoque une croissance accrue des algues et facilite la dispersion des
espèces envahissantes. Pour traiter efficacement et durablement la
question de la prolifération de la jacinthe d'eau sur le fleuve Niger,
il importe de régler le problème à la source en
réduisant l'apport anthropique de l'élément-limitant
(phosphore). Pour cela, il sera important de faire un état
préalable de la pollution en phosphore des eaux et des sédiments
sur les 4200 km du fleuve. En effet : (a) La mesure de la teneur
en phosphore des eaux permettra d'avoir une idée de la situation
présente en phosphore issu des pratiques agricoles et des eaux
usées des villes riveraines. Ce qui renseignera sur les zones à
risques pour une prolifération des plantes aquatiques en
général et de la Jacinthe d'eau en particulier qui tirent
directement leurs nutriments de l'eau. (b) L'analyse des teneurs en
phosphore des sédiments quant à elle renseignera sur l'ampleur
des pratiques antérieures car les sédiments fixent solidement le
phosphore qu'ils libèrent ensuite lentement dans l'eau au fil du temps.
Une pollution importante des sédiments donnera des
informations appréciables sur la profondeur du mal. Cela permettra de
connaitre le degré des mesures (limitation de produits contenant le
phosphore, traitement des eaux usées, etc.) à prendre pour
éviter une contamination plus importante du bassin du Niger qui sera
durablement préjudiciable aux eaux du fleuve. Les zones à
sédiments riches en phosphore seront identifiées comme
très propices pour la prolifération de la jacinthe d'eau et par
conséquent mériteront une surveillance plus accrue pour
éviter une colonisation future des lieux par cette plante
envahissante.
Dans ce travail nous avons prélevé sur les 20 Km
de parcours du fleuve aux alentours de Niamey (Capitale du Niger), des
échantillons d'eau et de sédiments que nous avons analysés
au laboratoire pour déterminer leurs teneurs en phosphore et en azote.
Au cours de l'échantillonnage, les lieux de prolifération
actuelle de jacinthe d'eau, les zones rizicoles, les avals des affluents
majeurs aux alentours de la ville de Niamey sont prospectés. Les
résultats de l'analyse des différents échantillons nous
permettrons d'avoir une idée de la situation présente et de faire
des propositions pertinentes de lutte contre la prolifération de la
jacinthe d'eau sur le Niger.
1.2. Objectifs de
l'étude
1.2.1. Objectif
général
L'objectif de cette étude est d'évaluer l'impact
de la pollution anthropique sur la prolifération de la jacinthe d'eau
sur le Niger.
1.2.2. Objectifs
spécifiques
Pour atteindre l'objectif général de ce travail
nous avons :
§ déterminer les teneurs en phosphore et en azote
des échantillons d'eau et des sédiments prélevés
sur les 20 km du fleuve Niger aux alentours de Niamey.
§ déterminer les teneurs en phosphore et en azote
de la jacinthe d'eau, principale plante aquatique envahissante sur le Niger;
§ faire un état des lieux de la
disponibilité en nutriments fondamentaux à la synthèse
tissulaire de la jacinthe d'eau des trois sites prospectés ;
§ mesurer les paramètres physico-chimiques globaux
des eaux du fleuve pour avoir une idée plus complète de sa
pollution.
CHAPITRE I: ETUDE
BIBLIOGRAPHIQUE
Ce chapitre traite de la revue de la littérature sur:
la zone d'étude, le fleuve Niger, la typologie des sources de pollution,
les plantes aquatiques, la relation entre la disponibilité en nutriments
et la prolifération des plantes aquatiques, etc.
I.1. CADRE DE L'ETUDE
I.1.1.
Généralités Sur le Bassin du Niger
Le bassin du Niger couvre dix pays pour une superficie active
de 1 500 000 km2 sur une superficie globale de 2 100 000 km2. Neuf
de ces pays sont organisés au sein d'une structure appelée
Autorité du Bassin du Niger (ABN). Il s'agit du Bénin, du Burkina
Faso, du Cameroun, de la Côte d'Ivoire, de la Guinée, du Mali, du
Niger, du Nigeria et du Tchad (Fig1).
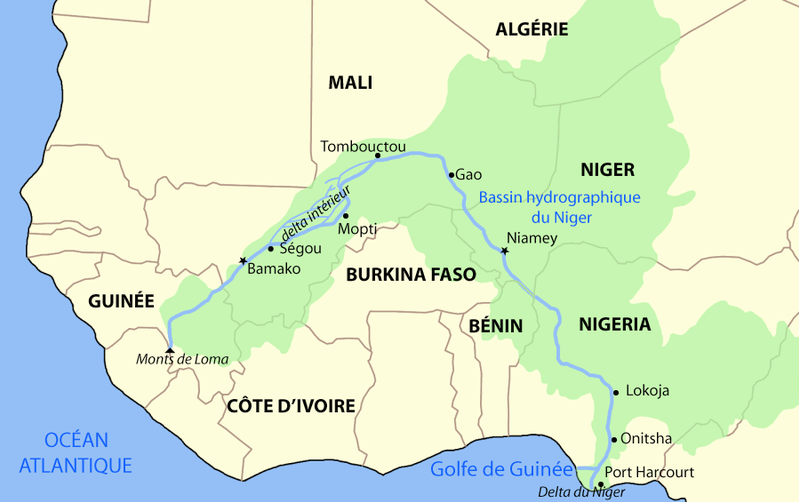
Figure 1 : Bassin du fleuve Niger
(source :
http://fr.wikipedia.org/wiki/Niamey)
Avec ses 4.200 Km, le fleuve Niger est le troisième
fleuve le plus long d'Afrique et le quatorzième au niveau mondial. En
termes de superficie du bassin (2,17 millions km2), il occupe la
neuvième place mondiale. Le Niger prend sa source dans le Fouta Djallon,
région guinéenne particulièrement pluvieuse pouvant
recevoir plus de 2 000 mm de précipitation annuelle. Il entre ensuite au
Mali, où commence son parcours en région aride au cours duquel
les apports des affluents sont faibles et limités aux quelques mois de
la saison des pluies (juillet à septembre). Au Mali, le fleuve se
disperse dans un des deltas intérieurs les plus étendus du monde
(entre 30 000 et 80 000 km² selon l'importance des crues),
où les apports de son seul affluent important, le Bani, ne suffisent pas
pour compenser les pertes par évaporation estimées entre 25 et 45
milliards de km3 par an (ABN, 2002). Il coule ensuite à
travers le Sud-Ouest du Niger où il reçoit les apports d'un
certain nombre d'affluents en rive droite issus du Burkina Faso (Sirba,
Gorouol, Dargol, Gouroubi) et du Bénin (Mékrou, Alibori, Sofo).
Après son entrée au Nigéria, les apports de ses
différents affluents, dont la Bénoué, deviennent plus
conséquents suite à l'augmentation de la pluviométrie. Le
fleuve se jette dans le golfe de Guinée, après un parcours de
près de 4200 km, avec un débit moyen estimé à 5600
m3/s. Il couvre donc un éventail de climats allant du
tropical humide (Fouta Djallon) au désertique (Algérie, Mali et
Niger).
I.1.2. Présentation de
la zone d'étude
I.1.2.1.
Caractéristiques physiques
Ø Localisation
Le cadre à prospecter est focalisé sur la ville
de Niamey, capitale du Niger. Il se trouve à l'ouest du Niger à
13°31' de latitude Nord et 2°26' de longitude Est (ALHOU 2007). Il se
situe à une altitude de 218 m. Le recensement général de
la population et de l'habitat de 2001 estime sa population à 707 951
habitants tandis qu'en 1988 elle était de 397 437 habitants. La
densité est de 1 057 habitants au km2. Le taux d'accroissement annuel de
la population est de 4,8 %. Il couvre une superficie de 670 km2. (Fig2).
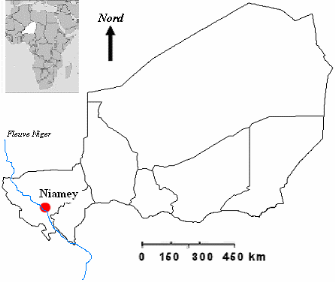
Figure 2 :
Localisation de la zone d'étude à l'Ouest du Niger (ALHOU,
2007)
Ø Le relief
La topographie des zones concernées est dans son
ensemble peu contrastée : les points culminants atteignent rarement
les 300 m d'altitude de part et d'autre du fleuve Niger ; les points bas
correspondent aux basses terrasses du fleuve. La pente moyenne du profil
longitudinal du fleuve Niger est de l'ordre de deux pour mille.
Ø La climatologie
Niamey appartient à un climat sahélien
(DESCONNETS, 1994) caractéristique des régions semi-arides avec
une alternance dans l'année d'une saison des pluies (juin, juillet,
août) et d'une saison sèche (septembre à mai). La
climatologie de la zone est caractérisée par les
paramètres météorologiques suivant les
précipitations, la température, et
l'évapotranspiration.
Ø La pluviométrie
La pluviométrie est déterminée par la
remontée du sud vers le nord du front intertropical (FIT) qui marque la
limite entre la masse d'air sec saharien ou l'harmattan et la masse d'air
humide ou mousson (ALHOU 2007). Elle est variable suivant les années,
telle qu'observe par la figure suivante.
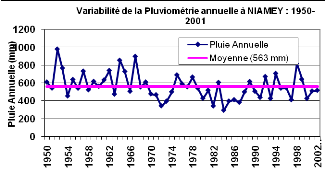
Figure 3 :
Valeurs moyennes annuelles des précipitations de
Niamey-aéroport
La moyenne annuelle de 1950 à 2001 est de 563 mm avec
un minimum de 386 mm en 1985 et un maximum exceptionnel de 1000 mm en 1952. Le
mois le plus pluvieux de l'année est le mois d'août avec 173 mm en
moyenne.
Ø La température
La température moyenne annuelle de 1995 à 2004 est
de 30°C. Les températures les plus élevées sont
enregistrées aux mois d'avril et de mai avec 35°C. Les mois de
décembre (26°C) et janvier (25°C) sont les plus frais.
L'écart-type est de 3°C.
Ø L'évapotranspiration (ETP)
L'ETP a été calculée selon la formule
complexe de Penman par la Direction de la Météorologie Nationale
(DMN). La moyenne annuelle de 1995 à 2004 est de 2 800 mm. Elle est plus
élevée en mai (mois chauds et secs) avec 286 mm et plus faible en
novembre avec 197 mm (Fig. 2.3). L'écartype est de 28 mm. Le rapport de
la pluviosité moyenne annuelle sur l'évapotranspiration moyenne
annuelle est égal à 0,18 donc caractéristique d'un climat
aride.
Conclusion
Parmi les facteurs du climat (précipitations,
température, évapotranspiration) seules les précipitations
agissent favorablement au développement des plans d'eau et cela pendant
une courte période de l'année (mai à septembre).
Ø Les sols
Ils sont pour l'essentiel peu structurés, avec une
faible capacité de rétention en eau, souvent pauvres sur le plan
géochimique et de forte érodabilité en l'absence d'une
biomasse protectrice.
Ø Ressources en eaux
Elles comprennent les eaux superficielles et les eaux
souterraines :
§ Eaux superficielles
Le réseau hydrographique de la ville de Niamey est
principalement marqué par le fleuve Niger et ses affluents. Certains de
ces affluents sont actifs pendant la saison des pluies (Goroual, Dargol, Sirba,
Goroubi, Diamangou, Tapoa, Mékrou) tandis que d'autres sont en voie de
fossilisation (Dallols Bosso et Maouri) suite à l'installation de sables
dunaires et d'ergs au Pléïstocène (DESCONNETS, 1994). Il
faut également signaler la présence d'importants koris (Ouallam
et Gountiyéna) appartenant à l'ancien réseau
hydrographique régional partiellement dégradé. Ils
drainent des superficies de plusieurs centaines à quelques milliers de
km2.
Outre le fleuve Niger et ses affluents, le réseau
hydrographique compte en saison des pluies des mares temporaires,
semi-permanentes ou permanentes installées dans des bassins
endoréiques. Dans la ville de Niamey pour éviter la stagnation de
l'eau, les activités de l'urbanisme ont transformé ces mares en
dépotoirs réceptionnant ainsi les décharges publiques
malgré les conséquences prévisibles sur les eaux
souterraines (ALHOU 2007).
§ Eaux souterraines
Les eaux souterraines sont contenues dans des
réservoirs appartenant à deux types de formations : le socle
cristallin du Liptako et les couches sédimentaires.
- Aquifères discontinus du socle
Les eaux sont logées uniquement dans la frange
fissurée et altérée du socle et parfois dans les failles
ouvertes plurikilométriques (BERNERT et al., 1985). Cette
porosité de fracture leur confère un écoulement discontinu
de l'eau contrairement aux formations sédimentaires à
porosités interstitielles. Les produits d'altération du socle
(les altérites) sont pour la plupart logées dans les
vallées entaillées par le réseau hydrographique.
- Aquifères à porosité interstitielle
Ces aquifères sont formés des alluvions
quaternaires des vallées et des grès tertiaires du continental
terminal (CT). Celui-ci est composé de trois aquifères (CT1, CT2,
et CT3) superposés, intercalés entre eux par des formations
argileuses très peu perméables. Les principales directions
d'écoulements souterrains sont nord-est/sud-ouest et nord-ouest/sud-est
(DODO, 1992). Ces écoulements convergent vers un axe de direction
nord-sud puis vers l'exutoire principal de tous les aquifères du CT, le
fleuve Niger dans la zone de confluence des Dallols Bosso et Maouri.
La réserve totale, pour la ville de Niamey et son
environ (sur un rayon de 100 km environ), est de l'ordre de 5 milliards de m3
pour une porosité efficace moyenne de 5 % et une épaisseur
moyenne de 5 m (ALHOU 2007).
I.1.2.2 La
végétation
Les formations végétales de la région du
fleuve sont distinguées par trois zones naturelles du Nord au Sud:
- La zone saharo- sindienne, caractérisé par une
végétation steppique rare et contractée;
- La zone sahélienne dont la végétation
est une steppe qui généralement, passe des formations
contactées ou arbustives claires dans la partie septentrionale, à
des types plus diffus et arborés dans le sud;
- La zone soudanienne plus boisée que le Sahel, porte
une végétation de savane caractérisée par une
strate herbacée continue où dominent les graminées vivaces
de grande taille.
La dégradation de la couverture végétale,
combinée avec les effets de l'eau et des vents fréquents ont
entraîné une intense érosion au niveau des bassins
versants. On estime à plusieurs milliers de tonnes, les terres qui sont
charriées dans les cours d'eau.
I.1.3. Contexte
Hydrologique
Le fleuve Niger prend sa source dans la partie Sud du
Fouta-Djalon, en Guinée, une région montagneuse d'environ mille
mètres d'altitude.
I.1.3.1. Débits du
fleuve Niger
Avant qu'il n'entre dans le Delta intérieur au Mali, au
Sud du désert du Sahara, le débit moyen annuel du fleuve est de
45.000 millions m3. La plaine d'inondation du fleuve qui coule le
long de la limite sud du Sahara, couvre environ 20.000 à 30.000
km2. Le bassin du fleuve Niger peut être divisé en
quatre grands sous - systèmes géographiquement distincts :
- la région du Haut Niger sert de château d'eau
effectif pour tout le bassin, à l'exception du Bas Niger. Le niveau
d'eau du fleuve fluctue en même temps que celui de ses principaux
affluents que sont le Tinkisso, le Milo, le Nianadan et le fleuve Niger
lui-même. La partie supérieure du bassin, d'une superficie de
140.000 km2, peut contribuer à une régulation partielle des
débits sur l'ensemble du fleuve.
- le Delta Intérieur du fleuve Niger est une vaste zone
au Mali qui a connu un important développement. Elle s'étend de
Ké-Macina, 200 km en aval de Bamako, à San au Sud, et à
Tombouctou au Nord. Elle est composée d'un système complexe
d'affluents, de lacs et de plaines d'inondation. Le Delta subit d'importants
changements hydrologiques au cours de l'année mais aussi d'une
année à l'autre. Les niveaux d'inondation dépendent des
volumes d'eau provenant du Haut Niger et de la rivière Bani qui se jette
dans le fleuve près de Mopti. Les surfaces inondées peuvent
varier de moins de 9500 km2 (1984) à 35.000 km2 (1967).
- le Moyen Niger (notre zone d'étude) s'étend de
Tassaoua (Tossaye) au Mali à Malanville au Bénin, et couvre un
bassin hydrographique de 900.000 km2, y compris 230.000 km2 de bassin inactif.
Sur sa rive droite, en amont de Niamey, le fleuve reçoit des affluents
prenant leur source au Burkina Faso tels que le Goroual, le Dargol et la Sirba.
Entre Niamey et Malanville (336km), le fleuve reçoit les apports des
rivières Goroubi, Diamangou, Tapoa et de la Mékrou qui
contribuent au débit maximal en début Septembre et fin janvier.
Ainsi la figure 4 ci-dessous relève les débits mensuels du fleuve
à Niamey.
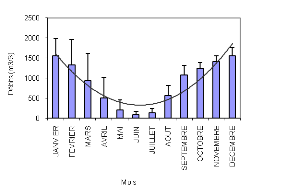
Figure 4 :
Débits mensuels du fleuve Niger à Niamey
Les débits du Moyen Niger sont affectés de
manière significative par ce qui se passe au niveau du Delta
Intérieur. La moyenne annuelle des écoulements à Niamey a
chuté de 1050 m3/s entre 1929 et 1970 à 697 m3/s entre
1971 et 2000.
- le Bas Niger est situé dans les zones humides du
bassin. Le fleuve reçoit plusieurs affluents importants comme les
rivières Sokoto et Kaduna et surtout, la Bénoué qui a un
bassin de 450.000 km2. La Bénoué prend sa source dans
les montagnes de l'Adamaoua au Cameroun (et au Tchad) et, à sa
confluence, la moyenne annuelle des écoulements est au moins
égale à celle du fleuve Niger. A Jebba, en aval des barrages de
Kainji et de Jebba, la moyenne annuelle des écoulements est de 1.454
m3/s puis culmine à 5.590 m3/s après la
confluence avec la Bénoué. La moyenne annuelle des
écoulements à l'embouchure est de même ampleur, les pertes
ayant généralement été compensées par les
apports des autres affluents.
I.1.3.2. Hauteurs du fleuve
à Niamey
Pour toutes les régions climatiques que traverse le
fleuve Niger, la saison des pluies est centrée sur le mois
d'Août. Cette zonalité latitudinale, montre à
l'évidence que le fonctionnement hydrologique de la cuvette lacustre du
fleuve Niger à Niamey est largement dépendant ; des
conditions d'écoulement exogènes, des conditions morphologiques
et climatologiques propres au delta intérieur, régissant des
écoulements (défluences, inondations) et le bilan hydrologique
(évaporation, infiltration).
I.2. TYPOLOGIE DES SOURCES
DE POLLUTION AU NIGER
Les sources de pollution rencontrées au Niger sont les
suivantes:
I.2.1. La pollution
industrielle et artisanale
La plupart des unités industrielles sont
concentrées dans la ville de Niamey. Parmi les plus importantes on peut
citer:
I.2.1.1. La Braniger
Elle produit la bière et met en bouteille des boissons
sucrées. Elle utilise l'eau de la SEEN, qu'elle traite
préalablement. Elle rejette 20 m3/h d'eau usée issue
du lavage des bouteilles et des fûts de brassage (Kotschoubey &
Koné, 2005) pour laquelle elle utilise la soude caustique. L'eau
usée subit ensuite un traitement aérobie et de décantation
avant d'être rejetée dans les collecteurs municipaux pour parvenir
au fleuve.
I.2.1.2. Enitex
L'ENITEX prélève 60 m3/h d'eau du
fleuve (Kotschoubey & Koné, 2005), la purifie (décantation,
floculation à la sulfate d'alumine) elle y ajoute de la chaux, pour
augmenter le pH. L'usine consomme d'importantes quantités de vapeur, et
rejette 30 à 40 m3/h d'eau usée qui s'écoulent
vers le fleuve. Les rejets contiennent des colorants, des métaux lourds
et de la matière organique.
I.2.1.3. Abattoir
frigorifique
L'abattoir frigorifique de Niamey a été
construit en 1967; il a une capacité d'abattage de 400 petits ruminants
et 200 bovins, pour une production de 25 t de viande par jour. L'abattoir
consomme 300 m3 d'eau par jour, et rejette les eaux usées
directement dans le fleuve, sans traitement préalable (Kotschoubey &
Koné, 2005).

Figure 5 :
Photo du point de rejet dans le fleuve Niger de l'abattoir
I.2.1.4. Industrie de lait
(SOLANI, Niger-Lait, Laban)
L'industrie laitière au Niger est essentiellement
constituée par la Société de Lait du Niger (SOLANI) et les
sociétés Niger-Lait SA et Laban Niger. La SOLANI produit entre
20.000 et 26.000 litres de produits laitiers par jour (Kotschoubey &
Koné, 2005).
La station d'épuration des eaux usées de la
société est en panne depuis trois ans, et les rejets sans
traitement vont directement dans le fleuve. Des autres sociétés
seul Niger Lait SA dispose d'un dispositif de traitement des eaux
usées.
I.2.1.5. Tannerie
La tannerie semi artisanale de la corniche de Gamkalla
à Niamey a une production moyenne de 30 peaux de bovins et 320 peaux de
petits ruminants par jour (Kotschoubey & Koné, 2005). Elle utilise
du natron (carbonate naturel de sodium), des tannins végétaux
à base de graine d'Acacia nilotica et de la chaux
éteinte dans le traitement des peaux. Elle évacue la plupart de
ses eaux usées par citerne, dans la nature, et évite ainsi de les
rejeter au fleuve. Ceci ne garantit pas pour autant que les nappes
phréatiques ne soient pas atteintes. Une inspection de terrain a
démontré que des risques de pollution existent, notamment
à partir de colorants et de déchets solides.

Figure 5 : Photo rejets de la tannerie.
I.2.2. La pollution urbaine
Malgré l'effort de l'état et des
collectivités, l'assainissement de la ville de Niamey n'est pas bien
maîtrisé. La majorité des eaux usées urbaines et
les eaux pluviales sont collectées par des caniveaux et rejetées
sans prétraitement dans le fleuve. Selon l'étude JICA, les eaux
usées urbaines collectées par le marigot naturel du Gounti Yena,
qui traverse la rive droite de Niamey du nord au sud, sont estimées
à 5 700 m3/j. Selon cette même étude, le volume
de déchets solides générés par les populations est
estimé à 300 000 m3/an. Une grande partie de ces
déchets solides parvient au fleuve.

Figure 6 :
Photo rejets urbains à Niamey
I.2.3. L'agriculture
Aux environs du fleuve Niger, on y cultive essentiellement le
riz. Et dans une moindre mesure des cultures de contre-saison, avec
maîtrise partielle de l'eau. On y pratique essentiellement le
maraîchage. L'utilisation excessive d'engrais peut entraîner
l'enrichissement du fleuve (eutrophisation) et une contamination de la nappe
souterraine. L'eutrophisation a pour conséquence la
prolifération des plantes aquatiques, du phytoplancton, source de
plusieurs nuisances.
L'utilisation des pesticides, surtout les
organochlorés, constituent une source de pollution diffuse pour les
ressources en eau. Ces pesticides peuvent s'accumuler dans la chaîne
alimentaire à travers les crustacés, mollusques et poissons.
I.2.4. Les mines
I.2.4.1. L'extraction d'or
à petite échelle dans l'ouest du pays
Peu de données sont connues sur cette industrie
artisanale, qui utilise des méthodes élémentaires, par
l'emploi du mercure. Les quantités utilisées sont inconnues.
I.2.4.2. L'usine
d'exploitation de l'or dans le sous-bassin de la Rivière Sirba
Peu de données sont connues sur cette entreprise, qui a
débuté en septembre 2004. Selon la Direction des Mines, d'autres
permis vont être livrés dans les années à venir pour
le même type d'exploitation.
I.3. Relation entre la
disponibilité en nutriment et la prolifération des plantes
aquatiques
La CEE, dans sa Directive du 21/05/1991 relative au traitement
des eaux urbaines résiduaires définissait: l'eutrophisation
comme: «l'enrichissement de l'eau en éléments nutritifs,
notamment des composés de l'azote et/ou du phosphore, provoquant un
développement accéléré des algues et des
végétaux d'espèces supérieures qui perturbe
l'équilibre des organismes présents dans l'eau et entraîne
une dégradation de la qualité de l'eau en question». Il
convient donc de traquer Les teneurs en azote et/ou en phosphore des cours
d'eau pour maîtriser le " développement
accéléré des algues et des végétaux
d'espèces supérieures".
Les lignes qui suivent ont pour but d'approfondir cette
thématique en commençant par décrire ce que sont les
végétaux aquatiques et la façon dont ils utilisent les
substances minérales pour se développer au point de perturber
l'équilibre des organismes présents dans l'eau
et d'entraîner une dégradation de la qualité
de l'eau en question.
I.3.1.
Généralités sur les plantes aquatiques.
Les plantes aquatiques, également appelées
macrophytes du fait qu'elles sont visibles à l'oeil nu, elles
comprennent pour l'essentiel des végétaux supérieurs qui,
munis de racines de tiges et de feuilles, portent des fleurs, produisent des
graines (angiospermes). On distingue les plantes qui flottent librement en
pleine eau de celles qui sont fixées au fond, ces dernières se
subdivisant à leur tour en plantes émergées
(jusqu'à 1,5m d'eau), plantes à feuilles flottantes
(jusqu'à 3m d'eau) et plantes immergées (dans toute la couche
euphotique, les angiospermes s'arrêtant à 10m de profondeur).
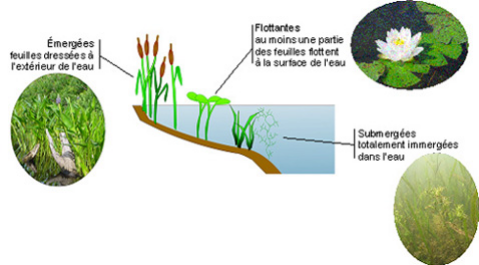
Figure 7: Types de
plantes aquatiques
I.3.2. Nutrition
minérale.
En supposant favorables la lumière, la
température, l'hydrodynamique et toutes les autres conditions
environnementales, c'est la biodisponibilité des nutriments
présents dans l'eau, gaz et minéraux en solution, qui commande la
prolifération des végétaux strictement aquatiques
(microalgues, macroalgues et macrophytes flottants). La demande exercée
par ceux-ci est fonction de la composition de leurs tissus vivants. La
composition moyenne du végétal aquatique, algues et plantes
aquatiques enracinées confondues, fait apparaître le carbone comme
constituant majeur, mis à part bien entendu l'oxygène et
l'hydrogène. Vient ensuite le silicium, peu abondant chez les
végétaux terrestres mais omniprésent dans le monde
aquatique au travers des diatomées, riche classe d'algues dont le
protoplasme est contenu dans un exo-squelette siliceux. L'azote est
l'élément suivant, précédent le calcium, le
potassium et le phosphore (BARROIN, 2000).
Les éléments nutritifs jouant un rôle
important dans ce processus sont le phosphore (sous forme de phosphates) et, de
moindre importance, l'azote (sous forme d'ammonium, de nitrates, et de
nitrites). Ces deux éléments présentent des ratios
«besoin/disponibilité» très élevés, ils
sont donc limitant pour la croissance des végétaux. Ainsi, une
augmentation de la concentration en phosphore dans l'eau permet une forte
croissance des végétaux, alors que le manque de phosphore limite
leur prolifération (BARROIN, 2000). L'eau se charge naturellement
d'éléments chimiques en solution (carbone, phosphore, azote,
calcium, magnésium, etc.) et de matières solides en suspension
(minéraux du bassin versant, matière organique) à travers
son parcours dans le bassin versant (ABRINORD, 2008).
Que du point de vue de la composition tissulaire le carbone
soit l'élément principal ne signifie pas que la
prolifération des algues et plantes aquatiques dépende de sa
biodisponibilité. En effet, la demande en nutriment est satisfaite en
puisant dans une eau où les éléments sont présents
à des concentrations différentes de celles de cette composition
tissulaire, c'est l'élément pour lequel la demande est la plus
forte par rapport à l'offre qui va limiter la synthèse de
nouveaux tissus. En considérant la composition moyenne d'une eau
naturelle, et en établissant pour chaque élément le
rapport [Demande/Offre], on constate qu'avec un rapport de 80 000 le phosphore
vient en tête, devançant l'azote (30 000) et le carbone (5 000).
Le phosphore est dit " facteur limitant ", concept emprunté à
l'agronomie, l'ordre d'importance des éléments en termes de
facteur limitant, P-N-C, étant très exactement l'inverse de ce
qu'il est en termes de composition tissulaire, C-N-P. Qu'en conditions
naturelles le phosphore soit facteur limitant signifie qu'il faut en augmenter
la quantité biodisponible pour augmenter la quantité d'algues et
plantes aquatiques produites, ce qui correspond à l'application
agronomique du concept. Mais cela signifie également qu'il faut en
réduire la quantité biodisponible pour réduire la
quantité d'algues et plantes aquatiques produites, type d'intervention
étrangère à la pensée agronomique.
En résumé, en conditions naturelles le phosphore
est le facteur limitant de l'augmentation de la prolifération des algues
et plantes aquatiques, il est également le facteur de maîtrise de
son augmentation autant que de sa réduction. Le phosphore est essentiel
à la croissance des organismes vivants. Il est, avec l'azote et le
potassium, un élément nutritif majeur et essentiel pour la
croissance des plantes. Le phosphore dans les eaux naturelles vient
principalement du drainage des terres agricoles, de l'utilisation des
détergents ainsi que des eaux usées provenant de déchets
humains ou domestiques. Un excès de phosphore dans les cours d'eau peut
provoquer des résultats indésirables, comme la
prolifération des plantes aquatiques. Une telle surabondance peut
entraîner l'eutrophisation du milieu.
I.4. Description de la
plante aquatique envahissante sur le Niger : La Jacinthe d'eau :
Eichhornia crassipes
I.4.1. Systématique
En 2005, Qaiser et al., présentent la
systématique de la jacinthe d'eau comme suit : la jacinthe d'eau
appartient au règne Végétal, au sous-règne des
Tracheobionta, à la division des Mogniolophyta (Angiosperme), à
la classe des Liliopsida (Monocotylédone), à l'Ordre des Liliale,
à la famille des Pontederiaceaes, au Genre Eichornia dont
l'Espèce est Eichornia crassipes.
I.4.2. Historique
Selon BARRET et al., (1982, cités par DAGNO
et al., 2007), la jacinthe d'eau serait originaire du bassin
amazonien. Mais très tôt, elle a été introduite en
Asie et en Afrique pour ses vertus ornementales. Elle est devenue depuis les
années cinquante un des véritables fléaux sur les cours
d'eau en Afrique, comme le Nil, le fleuve Congo et le fleuve Niger, les grands
lacs, les lagunes et les mares constituant un véritable calvaire pour
les populations riveraines.
I.4.3. Multiplication et
Description de la plante
La multiplication de la jacinthe s'effectue principalement par
voie végétative (filiations) et sa forte prolifération
pourrait être expliquée par la « non
inhibition » des bourgeons axillaires et l'absence d'ennemis naturels
dans les zones envahies. La propagation végétative est
très importante. Selon Babu et al. (2003), dix plants en
8 mois peuvent produire 655330 individus, soulignant ainsi le
potentiel invasif de la plante. Holm et al. (1977) ont obtenu
30 clones à partir de 2 plantes mères en
23 jours.
Du point de vue morphologique, la jacinthe d'eau peut avoir
une variabilité considérable dans la forme, la couleur de ses
feuilles et de ses fleurs, et selon l'âge de la plante (DAGNO et al.,
2007). Elle a une taille variant de quelques centimètres à
plus d'un mètre de haut (TOSSOU, 2004). Les feuilles d'un vert luisant
forment la base de la fleur et s'attachent à des pétioles
gonflés d'air. Sous cette architecture, se trouve le système
racinaire, qui permet à la plante de capter les nutriments
nécessaires à sa croissance dans l'eau. Mais le plus attrayant
des éléments constitutifs de cette herbacée est sa fleur,
qui attire par sa couleur mauve tirant sur le lilas. Un des pétales
porte habituellement une tache jaune d'or, encadrée par une ligne bleue
(DAGNO et al., 2007). Le pétiole (5 cm de diamètre et 30
à 50 cm de longueur) a une forme bulbeuse dans les conditions ouvertes,
effilée dans les conditions de forte densité de la plante. Ces
deux formes végétatives sont des adaptations morphologiques. Pour
bénéficier au maximum de la lumière solaire, les plants de
la jacinthe d'eau sont obligés de changer de formes (TOSSOU, 2004).
I.4.4. Écologie de la
plante
La jacinthe d'eau est décrite par plusieurs auteurs
comme étant la peste verte. Elle est dotée d'un pouvoir
phénoménal de reproduction. En combinant deux mécanismes
de reproduction (sexuée et asexuée) très efficaces, elle
colonise et peuple une grande diversité d'écosystèmes
aquatiques. Ainsi, la jacinthe d'eau s'installe dans les fleuves, lacs,
lagunes, étangs, marécages et bas-fonds.
I.4.5. Nuisance
exceptionnelle
Elle se reproduit de deux manières dont une principale,
la multiplication végétative, qui permet sa prolifération
sur une grande superficie du cours d'eau. La seconde multiplication dite
sexuée assure la pérennité de l'espèce.
En l'absence de ses ennemis naturels (ses consommateurs comme
le lamantin), la jacinthe d'eau se montre volontiers invasive. Elle forme
rapidement des tapis flottants monospécifiques denses, capables de
boucher canaux et ports ainsi que de bloquer les arrivées d'eau des
centrales hydrauliques et les canalisations d'eau dans les villes. La plante
provoque l'eutrophisation des eaux, c'est-à-dire l'accumulation de
débris organiques dans les eaux stagnantes, provoquant leur pollution
par désoxygénation. S'ensuit l'anoxie : les tapis flottants
réduisent la nuit le niveau d'oxygène de l'eau à un taux
insupportable pour de nombreuses espèces (plantes, amphibiens,
batraciens) qui se retrouvent alors asphyxiées. Ainsi elle
entraîne le déplacement de la flore et de la faune locale
incapables de concurrencer et/ou de survivre, d'où la perte de la
diversité des espèces. Par ailleurs, la jacinthe d'eau appauvrit
les eaux en phytoplanctons diminuant ainsi les chances de forte
productivité des eaux. En outre, lorsqu'elle meurt, elle libère
dans le milieu tous les polluants qu'elle a eus à piéger. Le
milieu aquatique devient très pollué. Des conséquences
telles que la pollution atmosphérique par suite de la
putréfaction et le comblement des fonds des vases en découlent.
Elle augmente aussi les pertes en eau en favorisant
l'évapotranspiration. D'autre part les tapis de jacinthe
hébergent des vecteurs de maladies (bilharziose, choléra,
paludisme) et des animaux dangereux (serpents venimeux). Inutile d'ajouter que
le commerce et le tourisme sont fortement affectés et la pêche,
fort perturbée par le blocage des hélices des barques et la
destruction des filets.
CHAPITRE II. MATERIEL ET METHODE
II.1. MATERIEL
Cette partie présente la station de l'étude et
le matériel utilisé.
II.1.1. Présentation de
la Station d'étude
Cette étude, s'est déroulée dans la
portion du fleuve Niger, située à Niamey dans le Niger
occidental. La station d'étude est définie comme une portion du
cours située dans la partie nigérienne plus
précisément aux alentours de la région de Niamey.
La station d'étude a été choisie en
tenant compte de son accessibilité, mais surtout de sa situation par
rapport aux sources de pollution et en fonction de la densité de la
population humaine du bassin versant. Parmi les activités
génératrices de revenus auxquelles s'adonne cette frange de la
population figurent la lessive et le tannage. Ces activités sont
pratiquées au bord du fleuve et contribuent en grande partie à la
pollution des eaux du fleuve. Niamey, est la région où sont
implantées les industries les plus importantes du pays.
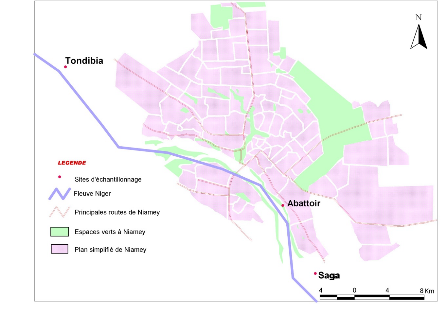
Figure 8 :
Sites retenus pour les prélèvements
II.1.2. Instruments
utilisés in situ
Pour conduire à bien notre étude nous avons
utilisé le matériel qui suit:
§ un GPS (Global Positionning System) pour la prise des
coordonnées géographiques des sites de l'étude;
§ un appareil multi- paramètre HI 9828 de la firme
HANNA, mesurant à la fois 13 paramètres dont entre autres :
la température, le pH, l'oxygène dissout, la conductivité,
la salinité de l'eau; le taux de solide dissous etc.
§ des pissettes d'eau distillée pour le
rinçage ;
§ un carré de rendement pour la mesure de la
densité de pied de jacinthe au m2 ;
§ une pirogue pour les traversées sur le fleuve,
un gilet de sauvetage, un marqueur pour l'identification des
échantillons, des flacons en polyéthylène d'un (1) litre
pour le prélèvement d'eau ;
§ un cahier de rapport pour les prises de note.
II.1.3. Matériel
utilisés au laboratoire
§ un spectrophotomètre DR/2800 de marque HANNA,
pour le dosage de l'Azote ammoniacal, orthophosphates et du phosphore
total ;
§ un spectrophotomètre DR/2000 pour le dosage de
la DCO ;
§ Une balance pour la pesée du poids des pieds de
jacinthe ;
§ une haute pour le séchage de la jacinthe avant
broyage ;
§ La verrerie (béchers, tubes d'Erlenméer,
pipettes, des cuves pour la mesure des échantillons au
spectrophotomètre, etc.
II.2. METHODOLOGIE
La méthodologie comporte le choix des paramètres
de suivi de la qualité de l'eau et des sédiments et du niveau
d'infestation des sites par la jacinthe d'eau d'une part. Et d'autre part, elle
porte sur la collecte des échantillons d'eau et des sédiments sur
le terrain et des dosages des échantillons au laboratoire.
II.2.1. Choix des sites et
points de prélèvement
Après des évaluations préliminaires par
la consultation de la documentation et des personnes ressources trois (3) sites
ont été retenus pour cette d'étude :
§ TONDIBIA à 7 km en amont de Niamey, situé
à 190 m d'altitude entre 13° 33' de latitude Nord et 2° 00' de
longitude Est. Il est principal lieu d'entrée des eaux du fleuve venant
de la partie malienne. C'est aussi une zone de forte production du riz, des
produits maraîchers et céréaliers. Il est surplombé
en rive gauche par le village de Tondibia et en rive droite par des formations
dunaires (ALHOU, 2007).
§ ABATTOIR Il est localisé en aval du point de
rejet des hôtels et en plein centre de la ville à 185 m d'altitude
entre 13°24' de latitude Nord et 2°07' de longitude Est;
§ SAGA à 4 km en aval de Niamey. C'est le premier
site situé en aval de tous les points de rejets entre 13°26' de
latitude Nord et 2°08' de longitude Est.
§ Il est à 175 m d'altitude.
Le choix des sites de prélèvement est
principalement basé sur l'accessibilité du site et la
présence ou non des sources de pollution susceptibles de modifier la
qualité des eaux du fleuve. Ce choix permet autant que possible de
mettre en évidence l'impact des rejets de la Communauté Urbaine
de Niamey (CUN) et des autres villes situées en amont sur la
qualité des eaux et l'apport anthropique en nutriments nécessaire
à la prolifération de la Jacinthe sur le fleuve.
Ces sites sont répartis sur une distance d'environ
vingt (20) kilomètres entre Tondibia et Saga. Sur chaque site trois (3)
points de prélèvement ont été retenus à
savoir la rive gauche, la rive droite du fleuve et le milieu du fleuve. Les
prélèvements ont été effectués sur une
distance de cinq (5) m de chaque berge.
II.2.2. Choix des
paramètres
L'accent est principalement mis sur les paramètres qui
déterminent la proliférante des plantes en milieux aquatiques.
Les paramètres suivants ont ainsi été retenus :
§ les paramètres physico-chimiques : il s'agit
pour :
ü les paramètres généraux de la
température, du pH, de la conductivité, la salinité et les
matières en suspension;
ü les indicateurs de la pollution organique dont la
demande chimique en oxygène (DCO) et l'oxygène dissous. Ce
dernier reflète tant par son déficit que par son excès une
pollution en milieu aquatique. La DCO traduit d'une part le processus de
dégradation de la matière organique qui s'accompagne d'une
consommation en oxygène dissous et d'autre part la prolifération
des autotrophes qui s'accompagne d'une augmentation en oxygène dissous
(ALHOU 2007);
ü les nutriments : il s'agit des composés
azotés sous forme d'ammonium (NH4+) et l'azote
total et des composés phosphorés à savoir les
orthophosphates (PO43-) et le phosphore total
(PTot) dont la présence en excès dans le milieu
récepteur peut se traduire entre autres par un développement
important du phytoplancton et des macrophytes (ERWIN et al., 1996, FRUGET et
al., 2000, GRADY et al., 2003,rapporté par ALHOU 2007).
ü les matières en suspension qui sont
déterminées par la méthode photométrique.
Ces paramètres ont été suivis sur
l'ensemble des sites répertoriés le long du fleuve Niger à
Niamey. Comme les nutriments nécessitent des traitements chimiques
(dosages), les échantillons prélevés ont été
conservés dans des bouteilles maintenues au froid (4 °C) pour les
analyses dans les 24h qui suivent au laboratoire Science de la vie et de la
terre de l'Ecole Normale Supérieure (Université Abdou Moumouni de
Niamey).
II.2.3. Collecte des
échantillons ou échantillonnage
L'échantillonnage est la procédure de
prélèvement d'une quantité représentative d'eau
à partir d'une rivière, d'un lac ou d'un puits (Rodier, 1978).
Il a été fait en bordure du fleuve Niger sur les
deux rives (au niveau des berges). Lieu privilégié de
prolifération des plantes aquatiques et où le courant et le
mouvement de l'eau entassent les plants de la jacinthe d'eau. Les mesures en
milieu du fleuve ont été faites en même temps pour des
mesures de comparaison et pour avoir une idée complète de la
pollution drainée par les eaux du fleuve.
Les échantillons ont été
prélevés à une profondeur d'environ 40cm et à cinq
(5) mètres de la berge pour éviter les phénomènes
d'hyponomos.
II.2.4. Evaluation de la
densité de la jacinthe d'eau au m²
Un carré de rendement qui délimite
1 m², est déposé de façon aléatoire
à la surface de l'eau. Toutes les jacinthes d'eau se trouvant dans
chacun des placeaux sont ramassées et comptées. Sur chaque site
le carrée est déposé trois (3) de suite. La moyenne du
nombre d'individus nous fournit la densité. La teneur en matière
sèche (MS) a été déterminée à partir
d'échantillons de E. crassipes pesés une première
fois au frais, puis placés à l'étuve à 70°C
pendant 48 h, laissés refroidir dans un dessiccateur, puis pesés
de nouveau pour évaluer le poids de la matière sèche et de
l'eau de constitution.
II.2.5. Méthode de
détermination des caractéristiques chimiques
II.2.5.1. Méthodes
spectrophotométriques
Le spectrophotomètre modèle DR/2800 est un
appareil à simple faisceau commandé par micropresseur pour
analyse au laboratoire ou sur le terrain. Il fonctionne sur pile ou sur secteur
en utilisant le transformateur / chargeur.
Les analyses au spectrophotomètre DR /2800 sont faites
en quatre étapes :
§ Préparation du spectrophotomètre
DR/2800 :
- Allumer l'appareil. S'il est sous tension, sur l'affichage
apparaît « test automatique » ;
-Sélectionner un programme d'analyse.
§ Préparation de l'échantillon
L'échantillon à blanc peut être
constitué de différentes solutions :
- échantillon à analyser sans réactif ;
- eau déminéralisée ;
Généralement la préparation de
l'échantillon consiste à ajouter le contenu d'un ou de plusieurs
sachets de réactifs prémesurés à 10 ou 25 ml
d'échantillon.
Il est important de respecter le temps prescrit dans la
méthode d'analyse pour être certain que la coloration obtenue
à la réaction du réactif avec la substance à
analyser se développe complètement.
Le spectrophotomètre à des temps de
développement, de coloration, de programmes et une série de bips
courts, avertit l'opérateur que le temps est écoulé.
Le minuteur doit être enclenché en pressant les
touches " Time" au moment où le décompte doit commencer.
§ Réglage du zéro de concentration
Le zéro de la concentration doit être
réglé avant chaque détermination pour établir une
référence de zéro pour la mesure.
- Placer l'échantillon à blanc dans le puits de
mesure en dirigeant le trait de mesure vers la droite.
- Presser la touche zéro. L'affichage indique
réglage à zéro puis indique que l'appareil est prêt
pour le premier échantillon.
§ Mesure de l'échantillon préparé
- Placer l'échantillon préparé dans le
puits de mesure, puis fermer puis fermer le couvercle.
- Presser la touche" MESURE" pour obtenir l'affichage de la
mesure et le résultat. L'affichage indique lecture, après six
secondes environ apparaît le résultat.
Les cuves colorimétriques doivent être
rigoureusement propres pour permettre d'obtenir des résultats exacts.
Nettoyer l'extérieur des cuves pour éliminer les traces des
doigts avec un tissu doux ou une serviette en papier avant de les placer dans
le puits de mesure en dirigeant toujours trait de mesure vers la droite.
II.2.5.2. Méthode de
digestion par réacteur
Pour mesurer la DCO, l'échantillon est oxydé par
une solution sulfurique de dichromate de potassium pendant 2 heures avec du
sulfate d'argent comme catalyseur. Les chlorures sont masqués par le
sulfate de mercure. La concentration des ions Cr3+ verts est ensuite
dosée par spectrophotométrie.
Le blanc a été utilisé plusieurs fois
pour les mesures utilisant la même eau.
II.2.6. Traitement des
données
Le traitement statistique des données
comporte :
- l'analyse de variance, après vérification de
l'homogénéité des variances par le test de LEVEN, afin
d'étudier la variabilité de la physico-chimie des eaux et des
sédiments du fleuve Niger à Niamey en fonction des sites. Le test
de Scheffé a été utilisé ;
- l'analyse de corrélation pour établir une
éventuelle variabilité de la densité de la jacinthe d'eau
en fonction des caractéristiques des sites.
Les analyses ont été réalisées au
seuil de 5%. Le logiciel utilisé est Statistica version 5.1.
- Le traçage de courbe et histogramme qui est
réalisé sous Windows Excel 2007 ;
- Et la saisie du corps du mémoire
réalisée par Word 2007.
CHAPITRE III: RESULTATS ET
DISCUSSIONS
III.1. RESULTATS
Ce chapitre comporte la présentation et
l'interprétation des différents résultats collectés
sur le terrain et ceux obtenus au laboratoire.
Les résultats des analyses physico-chimiques sont
présentés en annexe 2. Ils ont été examinés
en se référant aux projets de normes françaises des eaux
naturelles et polluées (annexe 3). Les paramètres de suivi sont
regroupés en paramètres physico-chimiques généraux,
en paramètres de pollution organique, de pollution azotée et
phosphorée pour mieux évaluer le type de risque qui pèse
sur le milieu récepteur.
III.1.1. Densité de la
jacinthe d'eau au m2 sur le fleuve
Les mesures de la densité de jacinthe d'eau le long des
sites d'étude donnent les résultats consignés dans la
figure 7. La plus forte densité s'observe à Niamey rive gauche
(41 pieds/m²) précédé de TON-G (37 pieds/m²) et
en fin SAGA-G (33 pieds/m²). Ces différences de densité,
entre les sites, ne sont pas très significatives (P > 0,05).
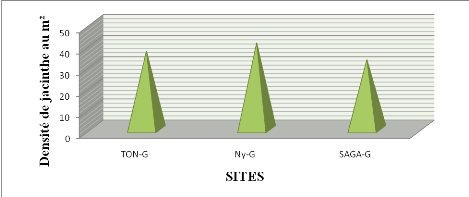
Figure 9 :
Densité de Jacinthe au m² par site
III.1.2. Etude des teneurs en
azote et en phosphore de la jacinthe d'eau
III.1.2.1. Teneurs en
azote
Les teneurs moyennes en azote de la jacinthe d'eau, prise sur
les sites, sont comprises entre 1,5% N et 2,4 % N. Ces teneurs augmentent en
passant de l'amont (TON) de Niamey vers l'aval (SAGA) (FIG 8). La teneur
minimale (1,5%) est enregistrée à TON-G et la maximale (2,4 %)
à SAGA-G.
L'assimilation des composés azotés et des
métaux lourds par cette plante constitue l'un des critères de son
choix dans l'épuration des eaux usées (MARTIN et al., 1978 ;
RADOUX, 1980 ; BRIX, 1991, rapporté par ENNABILI & RADOUX,
2006).
III.1.2.2. Teneur en
phosphore de la Jacinthe d'eau
Pour le cas du phosphore, les teneurs moyennes sont comprises
entre 0,09% P et 0,17 % P. Les teneurs les plus faibles sont
enregistrées à l'amont de Niamey à TON-D (0,09% P) et les
plus élevées à l'aval à SAGA-G (0,17%) (Figure 8).
Les hydrophytes, en particulier les plantes flottantes dont la
jacinthe d'eau, se montrent très avantagées par rapport aux
autres types biologiques dans l'accumulation des deux (2)
précédents bioéléments (ENNABILI & RADOUX,
2006).
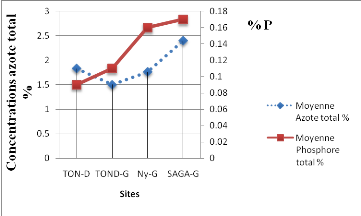
Figure 10 :
Teneur en azote et en phosphore de la Jacinthe d'eau par site et par point de
prélèvement
III.1.3. Etat des lieux de la
disponibilité en nutriments fondamentaux dans l'eau et les
sédiments
Etat des lieux de la
disponibilité en nutriments des sédiments, pour la jacinthe
Pour les sédiments, la valeur moyenne la plus
importante en azote total (1 252,5 mg N/kg) est observée à Ny-G.
La valeur minimale (781 mg N/kg) est enregistrée en aval (SAGA). Ce qui
dénote que la pollution par les sédiments est récente donc
le courant du fleuve ne les a pas encore emportés vers l'aval.
Concernant le phosphore, les concentrations décroisent
de l'amont vers l'aval de Niamey. La concentration maximale (615 mg N/kg) est
observée à TONDIBIA et celle minimale (273 mg N/kg) à saga
(Figure 13).
Densité de Jacinthe
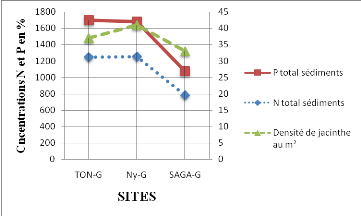
Figure 12 :
Comparaison entre les valeurs moyennes en azote total et phosphore total et la
prolifération de la jacinthe d'eau.
III.1.4. Etat de la pollution
anthropique du fleuve Niger
III.1.4.1. Les
paramètres physico-chimiques généraux
Les paramètres physico-chimiques retenus pour cette
étude sont : la température, le pH, la conductivité
et les matières en suspension.
§ La température
La température de l'eau varie peu d'un site à
l'autre (Figure 14), donc pas de différence significative (P > 0,05).
Ces températures sont caractéristiques des températures
naturelles élevées en zones tropicales. La moyenne minimale
(28,4°C) a été enregistrée à la rive gauche de
Niamey et la moyenne maximale (29,23°C) est observée en amont de
Niamey (TONDIBIA milieu du fleuve). Néanmoins, les valeurs de
température prises en milieu sans jacinthe sont toujours
supérieures à celles prises sous jacinthe. Ces valeurs sont
supérieures à la norme française fixée à
25°C.
§ Le pH
Les valeurs moyennes du pH sur tous les sites sont comprises
entre 7,6 et 8,4. Il n'y a pas de différence significative entre les
sites (P > 0,05). La valeur moyenne élevée (8,4) est
enregistrée au site situé en aval de Niamey et la plus faible
valeur à Niamey 7,6.
Les valeurs de la température et du pH en fonction des
sites de prélèvement sont consignées dans la figure
ci-dessous.
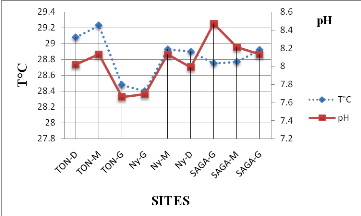
Figure 11 :
Valeurs moyennes de température et du pH par site et par point de
prélèvement
§ Les matières en suspension
(MES)
Les MES ou résidus secs représentent les
éléments solides non dissous dans l'eau. Elles ont une incidence
sur la composition chimique des eaux car leur surface peut concentrer certains
produits toxiques dissous par des phénomènes d'adsorption ou
d'échange d'ions.
Les teneurs de matière en suspension augmentent de la
rive droite vers la rive gauche (190 à la rive droite, 246 au milieu du
fleuve et 387 mg/l pour la rive gauche) pour le cas du site situé en
amont de Niamey. Globalement, la variation de la teneur en MES présente
une diminution de l'amont de Niamey à l'aval. Les plus faibles teneurs
en MES sont enregistrées sur les rives droites du fleuve tant disque les
plus fortes sont obtenues sur les rives gauches.
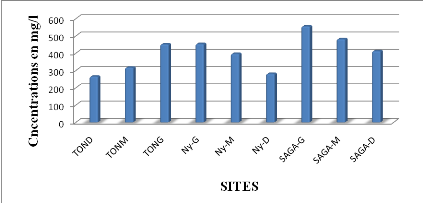
Figure 12 :
Evolution des teneurs en suspension par site et par point de
prélèvement
§ La conductivité
Il s'agit de la capacité de l'eau à conduire le
courant. Elle renseigne sur le degré de minéralisation d'une eau,
c'est-à-dire l'état ionique de l'eau brute.
Les plus fortes valeurs de la conductivité (350 uS/cm,
100 uS/cm) sont enregistrées à Niamey rive gauche et saga rive
gauche respectivement. Les valeurs moyennes pour tous les sites varient de la
rive droite à la rive gauche. La valeur maximale de la
conductivité a été enregistrée à Niamey rive
gauche avec 350 uS/cm. Et, la plus faible valeur est observée à
TONDIBIA rive gauche avec une valeur de 100 uS/cm.
La Figure 13 donne les valeurs de la conductivité en
fonction des sites et points de prélèvement.
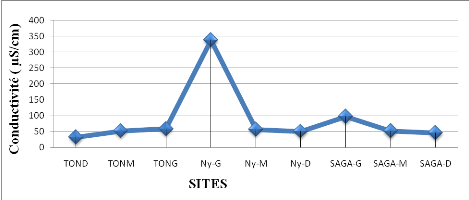
Figure 13 :
Evolution des valeur de la conductivité par site et par point de
prélèvement de l'amont à l'aval de Niamey.
III.1.4.2.
Paramètres de pollution organique
Deux paramètres ont été suivis dans le cadre
de cette étude. Il s'agit de la demande chimique en oxygène (DCO)
et de l'oxygène dissous (O2).
§ La demande chimique en oxygène
(DCO)
La demande chimique en oxygène est plus
élevée en amont et en aval de Niamey avec une moyenne respective
de 50 mg/l à TON-M et 40 SAGA-M. Les plus faibles valeurs sont
enregistrées aux niveaux des rives gauches de l'amont à l'aval de
Niamey et à la rive gauche de Niamey. Ces valeurs sont respectivement de
1 mg/l à TON-G, 0 mg/l à Ny-G et 1,66 mg/l SAGA-G. (FIG). Il
n'existe pas de différence significative (P> 0,05) entre ces valeurs
d'un site à un autre.
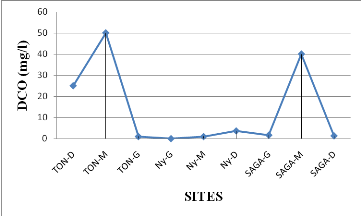
Figure 14 :
Variation de la DCO par site et par point de prélèvement de
prélèvement
§ Oxygène dissous
Les teneurs en oxygène dissous sont
déterminées principalement par la respiration des organismes
aquatiques, l'oxydation et la dégradation des polluants,
l'activité photosynthétique de la flore et les échanges
avec l'atmosphère (LAMIZINA-DIALLO & al., 2008).
Les moyennes obtenues montrent que les points de
prélèvement situés au milieu du fleuve et à la rive
droite sont plus oxygénés que ceux situé à la rive
gauche. La valeur minimale (3,02 mg/l) est enregistrée à Niamey
rive gauche et la maximale (5,74 mg/l) à Saga milieu du fleuve
(FIG 18).
Les résultats de tous les sites sont en dessous des
normes de qualité des eaux piscicoles (=7 mg/l) selon la directive du
conseil des communautés européennes et montre un degré
important de pollution des eaux du fleuve. La figure suivante donne un
aperçu sur l'oxygène dissout en fonction des sites et points de
prélèvement.
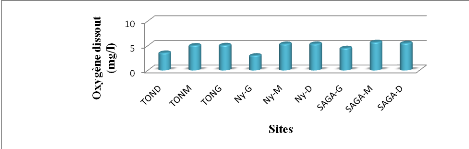
Figure 15 :
Teneurs en oxygène dissous en fonction des sites retenus
III.1.4.3.
Paramètres azotés et phosphorés
Quatre (4) paramètres ont été suivis. Il
s'agit des composés azotés, à savoir l'ammonium
(NH4+) et l'azote total et des composés
phosphorés, qui sont les orthophosphates (PO43+)
et le phosphore total (Ptot).
Ø Composés azotés
§ Azote ammoniacal
(NH4+)
La valeur moyenne maximale (5,63 mg/l) en azote ammoniacal est
observée à Ny-G et la minimale (0,7 mg/l) à Saga rive
droite en aval de Niamey. La valeur moyenne de l'azote ammoniacal sur tous les
sites est de 12,61 mg/l.
§ Azote total
Les concentrations les plus élevées en azote
total sont enregistrées à Niamey rive gauche et milieu du fleuve
avec respectivement 17,66 et 17,03 mg/l. Par contre les plus faibles valeurs
sont observées sur le site de TONDIBIA en amont de Niamey (FIG 19).
La moyenne globale pour tous les sites de l'étude est de 15,94 mg/l.
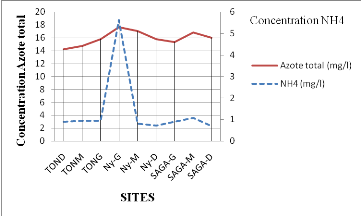
Figure 16 :
Evolution des concentrations en composés azotés (ammonium et
azote total) par site.
Ø Composés phosphorés
§ Les orthophosphates
Les plus fortes concentrations moyennes en orthophosphates
sont comprises entre 0,7 mg/l et 0,63 mg/l respectivement à TONDIBIA en
amont de Niamey et SAGA milieu du fleuve en aval de Niamey. Les valeurs
moyennes varient de la rive droite vers la rive gauche pour les sites amont et
aval de Niamey. Néanmoins il n'y a pas de différence
significative entre les différents sites (P > 0,05).
§ Le phosphore total
Concernant le phosphore total les plus fortes concentrations
(3,71 mg/l) sont enregistrées sur les rives gauches à TONDIBIA en
amont de Niamey et à Niamey. Par contre en aval de Niamey à Saga
la plus forte concentration est observée à la rive droite 3,79
mg/l. Cependant il n'existe pas de différence significative entre les
différents sites (P > 0,05).
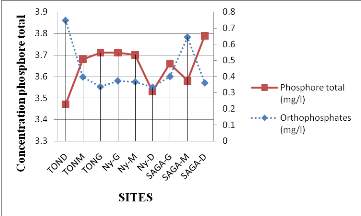
Figure 17 :
Concentration des composés phosphorés (orthophosphates et
phosphore total par site et par point de prélèvement
III.1.5. Corrélation
entre les caractéristiques physico-chimiques des sites et les
densités de jacinthe
Il n'existe pas de corrélation significative entre les
caractéristiques physico-chimiques des sites et les densités de
jacinthe. Cela pourrait s'expliquer par le fait que les travaux se sont
déroulés au moment de l'arrivée et de la stabilisation de
la jacinthe. La jacinthe n'a pas encore commencé à
proliférer en s'adaptant aux caractéristiques des sites dont
certains reçoivent la pollution de la ville de Niamey.
III.2. DISCUSSION
L'accumulation distincte de l'azote et du phosphore, en % de
la matière sèche, par la Jacinthe pourrait être due non
seulement aux milieux riches préférés par cette
espèce, mais aussi aux caractéristiques de ses organes
d'absorption. Des auteurs ont établi que les plantes submergées
(Zostera marina, Potamogeton pectinatus et Eichornia crassipes)
absorbent le phosphore aussi bien par les racines que par les tiges (WAISEL
& AGAMI 1991). De plus, ces plantes peuvent fixer les nutriments aussi bien
à partir de l'eau qu'à partir des sédiments (WESTLAKE 1979
rapporté par ENNABILI & RADOUX 2006).
Les valeurs moyennes du pH comprises entre 7,69 et 8,47 se
situent dans la limite du tolérable des normes françaises (6-9)
et nationales (6-9,5) pour la plus part des espèces
végétales et animales et particulièrement les poissons.
Ces résultats corroborent ceux trouvés par ALHOU & al., en
2009 sur le fleuve Niger. Au regard de ce constat, l'ensemble des valeurs
obtenues pour le pH est acceptable.
La seule valeur élevée de pH (8,47) est
enregistrée à l'aval de Niamey (SAGA rive gauche). Ce qui
être imputé aux déversements du trop plein d'eau des
rizières de SAGA contenant de fortes quantités d'engrais.
La température de l'eau de surface est
étroitement liée aux variations saisonnières et
journalières de la température ambiante. Cette variation de
température constitue un facteur très important pour le
fonctionnement des écosystèmes aquatiques. Elle agit sans doute
sur les réactions métaboliques qui se produisent dans les cours
d'eau (DJERMAKOYE, 2005).
Les températures moyennes (29,43 et 28,4°C) de
température enregistrées ne présentent pas de grandes
variations d'un site à l'autre. Ces températures montrent qu'il
n'y a pas de problème de pollution thermique. Le danger semble
s'écarter encore plus lorsqu'on considère que cette
température moyenne tombe dans les limites d'acceptabilité voire
de confort (= 40°C) de la flore et de la faune aquatiques tropicales du
Niger. Néanmoins, ces températures relativement
élevées peuvent favoriser le développement d'autres
phénomènes plus néfastes.
La teneur et la composition minérale et organique des
matières en suspension sont très variables selon les cours d'eau.
Elles sont fonction de la nature des terrains traversés et du flux et de
la composition des rejets (DJERMAKOYE, 2005).
Elles représentent la teneur en gramme/litre des
éléments de diverses granulométries transportées
par l'eau. Ces matières peuvent être minérales et inertes
ou plus ou moins actives vis a vis de l'oxygène.
Cependant des teneurs élevées peuvent
empêcher la pénétration des rayons solaires, diminuer
l'oxygène dissous et limiter alors le développement de la vie
aquatique par asphyxie des poissons suite au colmatage des branchies.
Les teneurs moyennes en matières en suspension pour les
sites de l'étude sont comprises entre 253 et 555 mg/l. Ces valeurs sont
largement supérieures aux normes françaises pour les eaux de
surface (20-100 mg/l). Cela s'explique par le phénomène
d'érosion qui affecte le bassin et la présence d'importants
déchets charriés par les eaux de ruissellement à la fois
dans les champs où sont répandus les déchets solides de la
ville et dans les caniveaux. Ces résultats sont inférieurs
à ceux trouvés par ALHOU en 2007 (934 à 1 495 mg/l) pour
la même période. Mais, il faut signaler toute fois que cette
année, les inondations exceptionnelles à Niamey pourraient
fortement expliquer cette différence par le phénomène de
la dilution. Ces fortes concentrations en matières en suspension jouent
sur la transparence de l'eau en saison des pluies qui devient faible (AKPAN,
2004 rapporté par ALHOU, 2007) et par conséquent diminue la
concentration en oxygène dissous.
Les valeurs obtenues (2,9 et 5 mg/l) de l'oxygène
dissous sont toutes inférieures à la norme française (>
5 mg/l) à l'exception de celles de SAGA milieu et rive droite du fleuve
(5,63 et 5,8 mg/l). Il est intéressant de noter que les faibles teneurs
en oxygène dissous peuvent être imputées à un fort
degré de minéralisation des eaux (BILLIEN & al.,
1999 rapporté par KOUASSY, 2002). Elles peuvent être aussi le fait
d'une forte turbidité (concentration en MES). En effet, l'abondance des
MES dans l'eau favorise la réduction de la lumière et abaisse la
production biologique du fait en particulier, d'une chute de l'oxygène
dissous consécutive à une réduction des
phénomènes de photosynthèse (LAMIZANA & al.,
en 2008).
La conductivité de l'eau est une mesure de sa
capacité à conduire le courant électrique. La mesure de la
conductivité permet d'apprécier rapidement mais très
approximativement la minéralisation de l'eau et de suivre son
évolution.
La valeur moyenne maximale de 337,33 uS/cm est
enregistrée à Niamey rive gauche. Ce lieu reçoit
directement les rejets domestiques et ceux de la tannerie qui présentent
des grandes valeurs de conductivités. Au milieu du fleuve et à la
rive droite, la conductivité baisse de manière importante et ceux
pour tous les sites de prélèvement, ce qui indique une dilution
des rejets polluants après un mélange avec les eaux du fleuve.
Néanmoins, les valeurs moyennes de la conductivité,
observées sur tous les sites, sont inférieures à la norme
nationale qui est fixée à 2 500 uS/cm. Globalement, il n'existe
pas de risque de pollution liée à la minéralisation des
eaux du fleuve.
La DCO est un paramètre qui nous permet
d'évaluer d'une manière plus exacte la quantité des
matières organique biodégradable ou non biodégradable
(LOTFI, 2009). Les valeurs moyennes obtenues dans le cadre de ce travail sont
comprises entre 0 et 40 mg/l. Ces valeurs sont très inférieures
à la norme nationale (= 125 mg/l), cela peut être dû aux
fortes inondations qui ont eu lieu cette année à Niamey par
l'effet de dilution. Par contre, elles sont largement supérieures aux
normes françaises admises qui sont de 25 mg/l. Cela peut être
imputable à la charge élevée des matières
organiques des eaux usées domestiques et aux déchets de toute
sorte charriés par le fleuve en saison des pluies à travers les
caniveaux de la ville et les affluents.
Selon LAMIZANA (2005), cet état de pollution n'affecte
pas la répartition des hygrophytes, le long d'un cours d'eau mais,
présente un effet très négatif sur les poissons.
Les teneurs en azote ammoniacal sont maximales à Niamey
rive gauche avec 5,63 mg/l. Cette teneur relativement faible peut être
liée à la dilution due aux inondations qui se sont produites
cette année à Niamey. La plus haute valeur observée
à Niamey rive gauche peut s'expliquer par un apport exogène
provenant des eaux de ruissellement en provenance des agglomérations
lieux de décharge des ordures ménagères de toutes sortes.
Ces dernières chargées en matières en suspension et en
matières organiques favorisent l'ammonification et diminuent le taux en
oxygène dissous des eaux et ralentissent par conséquent le
processus de nitrification.
En période de crue, l'importance des concentrations en
ammonium par rapport à celles des nitrates à certains points de
prélèvement provient d'une ammonification beaucoup plus
importante que la nitrification. Ainsi, les collecteurs d'eaux usées
rejettent alors plus d'ammonium que de nitrates et de nitrites dans les eaux du
fleuve. Il y a alors une fluctuation beaucoup plus remarquable des
concentrations en ammonium dans les eaux du fleuve comparativement aux
nitrates.
Les plus fortes concentrations (17,66 mg/l) en azote total
sont observées à Niamey et vers l'aval à SAGA (16,83
mg/l). Ces concentrations sont sans doute en relation avec les rejets
domestiques, industriels à Niamey et par la pratique de la riziculture
en aval à SAGA, activité grande consommatrice d'engrais NPK.
D'où les fortes concentrations en azote total en ces lieux.
Pour le cas du phosphore total, les concentrations sont
comprises entre 3,47 et 3,79 mg/l. Ces concentrations s`expliquent par l'apport
en nutriments des eaux de ruissellement en saison de pluies mais aussi par les
rejets d'eaux usées domestiques et industrielles dans le fleuve.
Malgré que le phosphore soit (avec l'azote) un des
grands responsable de l'eutrophisation, il n'y a pas de risque d'eutrophisation
de ce cours d'eau à cause de la grande capacité de dilution du
fleuve. Le risque n'existe que pour les bras morts et les berges où le
débit est très faible et le courant presque nul. Il faut note
à cet effet le développement d'un important couvert
végétal sur ce cours d'eau.
Les concentrations en orthophosphates sont également
plus élevées, ce qui peut s'expliquer de la même
manière que pour le phosphore total.
CHAPITRE IV:
RECOMMENDATIONS POUR UNE LUTTE EFFICACE
Il a été longtemps pensé que la meilleure
manière de maîtriser la jacinthe d'eau était de l'enlever,
puis de lui faire subir les transformations nécessaires pour l'utiliser
comme engrais, nourriture animale, pour obtenir des fibres pour la production
de papier, d'autres substances chimiques et pour obtenir du biogaz. Ce qui peut
se résumer en trois principales méthodes : la lutte physique
(manuelle et mécanique), la lutte chimique et la lutte biologique.
Néanmoins, force est de constater qu'aucune de ces
méthodes n'a permis l'éradication complète et la
prolifération de cette peste.
La prolifération des plantes aquatiques envahissantes
en général et de la jacinthe d'eau en particulier peut être
ainsi traitée de manière préventive en réduisant ou
même en supprimant les causes responsables de cette prolifération.
Il s'agit d'un travail de sensibilisation à l'endroit des pollueurs afin
de créer une prise de conscience collective.
IV.1.
La réduction des apports d'origine domestique
La plupart des stations d'épuration des services de
collecte et de traitement des eaux usées des communes ou de leurs
groupements sont conçues pour éliminer les matières en
suspension et une partie des matières dissoutes. Bon nombre de ces
stations n'éliminent, en ce qui concerne les matières dissoutes,
que peu d'azote et de phosphore. En effet, les stations d'épuration
n'ont été conçues jusqu'à présent que pour
l'élimination du carbone piégé dans les boues. L'azote et
le phosphore sont en fait minéralisés et redonnés à
la nature. Dans bien des cas, ce traitement partiel n'est pas suffisant pour
maintenir un équilibre écologique satisfaisant au sein du milieu
récepteur.
IV.1.1. Traitement de l'azote
dans les eaux usées urbaines
Les procédés d'épuration biologique de
nitrification et de dénitrification sont les mieux adaptés pour
éliminer l'azote des effluents urbains. En effet, les
procédés physico-chimiques qui comprennent essentiellement la
chloration, l'électrodialyse, les résines échangeuses
d'ions et le stripage de l'ammoniac, ne sont guère applicables en
traitement des eaux résiduaires urbaines en raison soit de leur faibles
rendements, soit de leurs coûts prohibitifs. Ce sont aujourd'hui les
procédés biologiques qui sont les plus compétitifs et les
mieux adaptés au traitement de l'azote des eaux usées
domestiques.
Nous proposons à cet effet :
La nitrification et la
dénitrification
§ Nitrification : c'est un procédé qui
permet la transformation de l'ammoniac en nitrates en présence
d'oxygène. En pratique, cette opération est
réalisée lors de la phase aérée de la biomasse par
l'intermédiaire de bactéries autotrophes du genre
Nitrosomonas et Nitrobacter qui assurent successivement la
conversion d'ammoniac en nitrites (nitritation) puis des nitrites en nitrates
(nitratation).
Ce sont les systèmes par boues activées, en
aération prolongée en bassin unique ou avec une zone d'anoxie en
tête. Le volume du bassin d'aération doit être suffisant
pour respecter la cinétique de nitrification. L'aération
théorique est de 4,6 kg d'oxygène par kg d'azote à oxyder
et il faut maintenir 1 à 2 mg/l en oxygène dans le bassin
d'aération (POUILLEUTE, 1996).
§ Dénitrification : c'est une technique qui
permet le passage des nitrates à l'azote gazeux atmosphérique en
milieu anoxique. Le procédé le plus répandu consiste
à réaliser une zone d'anoxie en amont de l'épuration
biologique ou à créer une zone d'anoxie dans le bassin
d'aération.
IV.1.2. Réduction du
phosphore dans les eaux usées urbaines
La réduction des apports phosphorés des eaux
usées est en général considérée comme le
facteur clé de la lutte contre l'eutrophisation des rivières, des
lacs et des fleuves. Il s'avère en effet que l'élimination de
l'azote soit insuffisante et ne constitue pas un facteur limitant dans la
mesure où certaines algues sont capables de fixer l'azote
atmosphérique.
Les principales sources de phosphore dans les effluents
domestiques sont les produits lessiviels et détergents car ils
constituent plus de la moitié des phosphates déversés. La
suppression des tripolyphosphates (TPP) des lessives semble donc
nécessaire. Les TPP utilisés comme adoucisseurs de lavage peuvent
être remplacés par d'autres substances.
IV.2. La réduction
des apports d'origine agricole
IV.2.1. La fertilisation des
sols
Le phosphore est avec l'azote et le potassium, la base de la
fertilisation dans le monde agricole. Il apparaît en effet que
l'érosion générée par les précipitations et
le ruissellement constitue un élément majeur du transport des
polluants vers les eaux de surface. Les substances présentes à la
surface du sol sont susceptibles d'être entraînées sous
forme soluble ou adsorbée aux particules de sol entraînées.
Comme dispositif capable de limiter les processus de transfert, nous proposons
le dispositif enherbé jouant un rôle de filtre face au
ruissellement. Les matières sont ainsi filtrées par la
végétation dense. Suivant leur implantation et leurs
caractéristiques, les bandes enherbées permettent de
piéger un grand nombre des particules du sol transportées par le
ruissellement. Elles sont donc capables d'abaisser les teneurs en nitrates.
Nous proposons aussi l'utilisation de la jachère
obligatoire dans sa forme fixe. En effet, la jachère obligatoire quand
il y a mise en place de bandes enherbées le long des rivières,
serait très bénéfique pour la séquestration des
polluants diffus et ponctuels.
IV.2.2. La pollution
liée à l'élevage
Les effluents d'élevage sont des fertilisants pour
l'agriculture. Mais, ils peuvent aussi être à l'origine de la
pollution des rivières, des plans d'eau et des nappes souterraines
compromettant notamment l'alimentation en eau potable. Nous proposons à
ce niveau l'encadrement et la sensibilisation des éleveurs sur les
méthodes de gestion des effluents.
Conclusion
Cette étude portant sur la prolifération des
plantes aquatiques envahissantes sur le fleuve Niger et état des lieux
de la pollution en azote et en phosphore des eaux est l'une des rares
études au Niger. Alors que le Niger pays sahélien dont les 3/4 de
son territoire sont désertiques a besoin d'une préservation de
ses ressources naturelles en générale et des
écosystèmes aquatiques en particuliers. Bien que ces
écosystèmes aquatiques revêtent un intérêt
environnemental, social, culturel et économique, les pressions
anthropiques les menacent dangereusement créant souvent des
déséquilibres écologiques. Le cas de la ville de Niamey,
installée le long du fleuve Niger est un exemple qui a permis
d'illustrer l'impact des activités humaines (domestiques et
industrielles) sur ce cours d'eau. Les rejets polluants qui se mélangent
aux eaux naturelles ont diverses origines ; ce qui permet leur
classification en eaux usées domestiques constituées par les eaux
vannes (issues des W-C, des latrines et des toilettes), les eaux usées
ménagères provenant des eaux de cuisine, de lessive et de
vaisselle, les eaux usées industrielles, agricoles et
hospitalières.
La prolifération de jacinthe d'eau, et l'énorme
biomasse que cette plante représente constitue un piège
considérable aux sels minéraux et nutritifs provenant de ces eaux
usées.
Ce travail basé sur une étude de la
qualité des eaux du fleuve Niger à Niamey plus
particulièrement les caractéristiques physico-chimiques de l'eau
et des sédiments cherche à établir une corrélation
entre la prolifération de la jacinthe d'eau et la disponibilité
en nutriment dans le milieu.
L'utilisation des méthodes statistiques simples telles
que les analyse de variance (Anova) et les analyses de corrélation ont
permis d'approcher une telle problématique même s'il n'existe pas
de différence significative entre les paramètres mesurés
et la prolifération de la jacinthe.
Il ressort principalement de cette étude que le
déversement dans le fleuve Niger des eaux usées de la ville de
Niamey présente un impact très faible sur l'ensemble de
l'écosystème grâce aux débits du fleuve qui sont
plus importants que ceux des rejets surtout avec les inondations de la ville de
Niamey cette année.
Il faut tout de même retenir que :
- Un pied de jacinthe de 572 g de poids frais peut contenir
jusqu'à 92% de teneur en eau. Ce qui interpelle sur le caractère
très consommateur d'eau de la jacinthe ;
- Les analyses statistiques (Anova, corrélation) ne
donnent pas de différence significative entre les sites
étudiés et ne permettent en plus d'établir de
corrélations significatives entre la présence de la jacinthe et
la disponibilité en nutriments dans l'eau et les sédiments.
Cette étude a permis également de prospecter
l'impact des rejets sur la qualité des eaux du fleuve Niger le long des
berges. Ce qui a permis de constater que les eaux du fleuve Niger à
Niamey subissent une altération liée à la matière
organique et aux nutriments (PO43-, PTot,
NH4+, NTot) détectable le long des
berges. Cette altération disparaît juste à quelque
mètre des points de rejet grâce à la capacité de
dilution du fleuve.
Au vu des résultats obtenus, ces eaux sont
déconseillées comme boisson humaine, sauf après des
traitements chimiques. L'apport du Na Cl pour élever le pH pourraient
les rendre plus douces et donc de bonne qualité pour être
consommées par les ménages.
Ainsi au terme de cette étude les recommandations
suivantes sont formulées :
§ un suivi régulier de la qualité des eaux
du fleuve Niger (surtout le long des berges) sur une gamme plus étendue
de descripteurs (matières organiques, nutriments, bactériologie,
micropolluants,...) ;
§ le respect par les industriels de la
règlementation des rejets d'eau usée ;
§ le renforcement des capacités des gestionnaires
des milieux aquatiques à travers des ateliers de formation ;
§ la sensibilisation des populations vivant dans cet
écosystème sur les mesures d'hygiène et
d'assainissement ;
§ le déguerpissement des dépotoirs
d'ordures ménagères des environs du fleuve.
Références
Bibliographiques
1. Abrinord., 2008. Guide des
problématiques reliées à l'eau. Le bassin versant de la
rivière du nord, 24 pp.
2. Alhou B. (2007). Impact des rejets de la
ville de Niamey (Niger) sur la qualité des eaux du fleuve Niger.
Thèse de Doctorat, Faculté université notre Dame de la
paix Namur, Belgique, 229 p.
3. Alhou B., MICA J-C., DODO A., et AWAISS A. (2009).
Etude de la qualité physico-chimique et biologique des eaux du
fleuve Niger à Niamey. Article publié in Iternational Jornal of
Biological and Chemical Sciences, 3(2): 240-254.
4. Ameyapoh Y., Hiheglo M., Bawa L. M. et De Souza C.,
2005. Impacts des contaminations microbiennes et chimiques de la
lagune de Lomé sur la qualité des poissons péchés
dans ses eaux. École Supérieure des Techniques Biologiques et
Alimentaires (ESTBA), Université de Lomé, Togo. 4 p.
5. Anonyme. 2006. Rapport
problématique sur la jacinthe d'eau ; Projet d'un Fleuve à
l'autre ; 15p. Site : www.usgl-glu.org. Date de consultation : 12.05.2008.
Hyperlien (url):
http://www.usgl-glu.org/myfiles/Proliferation.
Pdf
6. Autorité du Bassin du Niger (A.B.N.).,
2002. Mission, activités en cours et perspectives, Document
d'information, 9 p.
7. Autorité du Bassin du Niger., 2002.
Mission, activités en cours et perspectives, Document
d'information, 9 p.
8. Ayihonsi S., 2006. Effets des stocks
d'azote et de phosphore sur la distribution des plantes flottantes sur les eaux
du lac Nokoué: cas de la jacinthe d'eau (République du
Bénin). Mémoire de fin de formation en APE-DIT-EPAC-UAC,
Cotonou. 73 p.
9. Babu R., Sajeena A., Seetharaman K., 2003.
Bioassay of the potentiality of Alternaria alternata (Fr.) Keissler as
a bioherbicide to control water hyacinth and other aquatic weeds Cro p.
Prot. 22, p. 1 005-1013.
10. Barroin G., 2000 Gestion des risques.
Santé et environnement : le cas des nitrates Phosphore, azote et
prolifération des végétaux aquatiques. INRA -
Hydrobiologie et faune sauvage.
11. Besnier A.L., 2005. La mise en place de
la Gestion intégrée des ressources en eau dans le bassin du
fleuve Niger : le début d'un long processus, mémoire de DEA,
Paris, Université Paris X-Nanterre, 113 p.
12. Dagno K., Lahlali R., Friel D., Bajji M., Juakli
H., 2007. Synthèse bibliographique: problématique de la
jacinthe d'eau, Eichhornia crassipes, dans les zones tropicales et
subtropicales du monde, notamment son éradication par la lutte
biologique au moyen des phytopathogènes. Vol 11(2007), n°4:
299-311. Article. Date de consultation : 03.04.2008. Hyperlien (url):
http://popups.ulg.ac.be/Base/document.php?id=1706
13. Diallo L., Birguy M., Kenfack S., Milogo R.J.
(2008). Evaluation de la qualité physico-chimique de l'eau d'un
cours d'eau temporaire du Burkina Faso-le cas du Massili dans le Kadiogo.
6p.
14. Djermakoye M.M.H. (2005). Les eaux
résiduaires des tanneries et des teintures : caractéristique
physico-chimique, bactériologique et impacte sur la qualité des
eaux de surface et souterraines. Thèse de doctorat rn pharmacie.
Université de Bamako, 118 pp
15. Fao., 2000. Water weeds management in
West Africa/Ghana water bodies. Rome: FAO: document de projet
n°TCP/RAF/0066.
16. Harley KL., Julien MH., Wright AD., 1997.
Water hyacinth: A tropical worldwide problem and methods for its control.
Proceedings of the first meeting of the International Water Hyacinth
Consortium, 18-19 March. Washington: World Bank.
17. Holm LG.,
Plucknett DL., Pancho JV.,
Herberger JP., 1977. The world's worst weeds: distribution
and biology. Honolulu: University Press of HAWAÏ, 609 p.
18. Kerim M., 2006. Un syndicat pour
le fleuve Niger, Banc Public n°151 Nicolas.
19. Kotschoubey & Koné A., 2005.
Evaluation pour le suivi de la qualité de l'eau dans le bassin
du Niger/UNOPS: Banque mondiale.
20. Lotfi M. (2009). Etude
et caractérisation des eaux de l'Oued Soummon (Algérie).
Laboratoire de technique des matériaux et de génie des
procédés (LTMGP) Université de Béjaia.
21. Mounkeila G., 1984. Contribution à
l'étude de la flore et de la végétation des milieux
aquatiques et des sols hydromorphes de l'ouest de la République du
Niger, de la longitude de Dogondoutchi au fleuve Niger. Thèse de
Doctorat de 3ème cycle de Géographie tropicale -
écologie et Aménagement et développement.
Université de Niamey/Bordeaux II. 149 p + annexes.
22. Ouattara M. & Sokona M.F., 1997.
Lutte intégrée contre la jacinthe d'eau et autres
plantes aquatiques nuisibles. Rapport FAO.
23. Picouet C., 1999. Géodynamique
d'un hydrosystème tropical peu anthropisé: Le bassin
supérieur du Niger et son Delta Intérieur. Thèse.
Université de Montpellier II.
24. Pouillete E. (1996). Les
phénomènes d'eutrophisation. Mémoire DU « eau et
environnement », D.E.P, Amiens, 40 p.
25. Qaisar M., Zheng P., Siddiqi Mr., Islam E., Azim
Mr., Yousaf H., 2005. Anatomical studies on water hyacinth (Eichhornia
crassipes (MART.) Solms) under the influence of textile waste water. J.
Zhejlang. Univ.6B (10), p.991-998.
26. TOSSOU, Y. 2004. Evaluation des nuisances
causées par la prolifération de la jacinthe d'eau (Eichhornia
crassipes) (Mart.) Solms-Laubach sur le lac Nokoué et la lagune de
Porto Novo et la pollution par le dépôt des déchets urbains
sur le chenal de Cotonou (République du Bénin).
Mémoire de fin de formation en APE-DIT-EPAC-UAC, Cotonou. 53
p.
27. Unesco, 2006. Le fleuve Niger, les
îles et la vallée.
28. WILSON, J.R., HOLST, N., REES, M. 2005.
Determinants and patterns of populations growth in water hyacinth. Aquatic
Bot. 81, pp. 51-67.
29.
www.afdb.org/.../ADF-BD-IF-2008-50-FR-
NIGER
-EIES-programme-kandadji-de-regeneration-des-ecosystemes-et-de-mise-
en valeur des ressources naturelles.
ANNEXES
Annexe 1 : Concentration des
éléments dans le végétal (demande), dans une eau
naturelle (offre) et rapport demande/offre.
|
Eléments
|
SYMBOLE
|
Demande
|
offre
|
dem/offre
|
|
(végétal)
|
(eau)
|
|
|
%
|
%
|
(approx)
|
|
Oxygène
|
O
|
80,5
|
89
|
1
|
|
Hydrogène
|
H
|
9,7
|
11
|
1
|
|
Carbone
|
C
|
6,5
|
0,0012
|
5
|
|
Silicium
|
Si
|
1,3
|
0,00065
|
2
|
|
Azote
|
N
|
0,7
|
0,000023
|
30
|
|
Calcium
|
Ca
|
0,4
|
0,0015
|
<1.000
|
|
Potassium
|
K
|
0,3
|
0,00023
|
1.3
|
|
Phosphore
|
P
|
0,08
|
0,000001
|
80
|
|
Magnésium
|
Mg
|
0,07
|
0,0004
|
<1.000
|
|
Soufre
|
S
|
0,06
|
0,0004
|
<1.000
|
|
Chlore
|
Cl
|
0,06
|
0,0008
|
<1.000
|
|
Sodium
|
Na
|
0,04
|
0,0006
|
<1.000
|
|
Fer
|
Fe
|
0,02
|
0,00007
|
<1.000
|
|
Bore
|
B
|
0,001
|
0,00001
|
<1.000
|
|
Manganèse
|
Mn
|
0,0007
|
0,0000015
|
<1.000
|
|
Zinc
|
Zn
|
0,0003
|
0,000001
|
<1.000
|
|
Cuivre
|
Cu
|
0,0001
|
0,000001
|
<1.000
|
|
Molybdène
|
Mo
|
0,00005
|
0,0000003
|
<1.000
|
|
Cobalt
|
Co
|
0,000002
|
0,000000005
|
<1.000
|
(VALLENTYNE, 1974 rapporté par BARRION 2000).
Annexe 2 : Caractéristiques
physico-chimiques des eaux du fleuve Niger
|
Dates
|
Stations
|
NH3 mg/l
|
PO4 mg/l
|
PTot mg/l
|
T°C
|
pH
|
Oxy, dissout %
|
Oxy, dissout mg/l
|
Conductivité us/cm
|
DCO mg/l
|
MES mg/l
|
|
07/08/2010
|
Tondi,D
|
1,16
|
1,64
|
0,107
|
27,62
|
7,43
|
24,2
|
1,70
|
3,47
|
0
|
190
|
|
Tondi,M
|
1,54
|
0,53
|
0,104
|
28,18
|
7,97
|
75,2
|
5,63
|
67
|
119
|
246
|
|
Tondi,G
|
0,9
|
0,31
|
0,149
|
28,5
|
7,81
|
61,1
|
5,21
|
72
|
3
|
387
|
|
Ny,G
|
0,77
|
0,43
|
0,156
|
27,84
|
7,4
|
0,31
|
4,00
|
282
|
0
|
388
|
|
Ny,M
|
1,03
|
0,4
|
0,273
|
28,74
|
7,94
|
71,1
|
5,68
|
71
|
2
|
326
|
|
Ny,D
|
0,77
|
0,3
|
0,117
|
28,78
|
7,9
|
76,5
|
5,71
|
68
|
0
|
210
|
|
Sag,G
|
0,64
|
0,49
|
0,146
|
29,85
|
8,5
|
64,6
|
4,73
|
150
|
0
|
495
|
|
Sag,M
|
1,41
|
1,23
|
0,218
|
28,92
|
8,05
|
77,4
|
5,76
|
71
|
0
|
454
|
|
Sag,D
|
0,77
|
0,36
|
0,123
|
29,76
|
8,14
|
77
|
5,66
|
68
|
2
|
349
|
|
08/10/2010
|
Tondi,D
|
0,64
|
0,31
|
0,146
|
29,06
|
8,29
|
47,9
|
3,54
|
56
|
58
|
280
|
|
Tondi,M
|
0,64
|
0,36
|
0,156
|
29,55
|
8,22
|
68,8
|
5,04
|
38
|
0
|
346
|
|
Tondi,G
|
0,9
|
0,34
|
0,11
|
29,40
|
7,72
|
64,4
|
4,73
|
58
|
0
|
477
|
|
Ny,G
|
0,64
|
0,33
|
0,254
|
29,26
|
8,41
|
63,3
|
4,66
|
80
|
0
|
476
|
|
Ny,M
|
0,64
|
0,3
|
0,136
|
29,43
|
8,23
|
74,4
|
5,46
|
45
|
0
|
426
|
|
Ny,D
|
0,64
|
0,29
|
0,12
|
29,12
|
8,05
|
65,9
|
4,86
|
36
|
4
|
308
|
|
Sag,G
|
1,29
|
0,32
|
0,13
|
28,07
|
8,51
|
57,7
|
4,33
|
74
|
0
|
585
|
|
Sag,M
|
1,03
|
0,35
|
0,149
|
28,68
|
8,24
|
74,8
|
5,57
|
43
|
117
|
554
|
|
Sag,D
|
0,77
|
0,33
|
0,097
|
28,37
|
8,08
|
72,9
|
5,46
|
34
|
0
|
439
|
|
14/08/2010
|
Sag,G
|
0,77
|
0,39
|
0
|
28,33
|
8,42
|
60,4
|
4,53
|
69
|
5
|
586
|
|
Sag,M
|
0,77
|
0,35
|
0,192
|
28,73
|
8,34
|
79,3
|
5,90
|
42
|
3
|
567
|
|
Sag,D
|
0,64
|
0,39
|
0,156
|
28,63
|
8,17
|
74,1
|
5,52
|
36
|
2
|
449
|
|
Ny,G
|
15,48
|
0,36
|
0,407
|
28,11
|
7,26
|
5,6
|
0,42
|
650
|
0
|
496
|
|
Ny,M
|
0,77
|
0,4
|
0,205
|
28,62
|
8,24
|
67,4
|
5,03
|
56
|
1
|
437
|
|
Ny,D
|
0,77
|
0,23
|
0,091
|
28,88
|
8,04
|
75,8
|
5,63
|
49
|
7
|
324
|
|
Tondi,D
|
0,9
|
0,29
|
0,149
|
28,76
|
8,36
|
73,5
|
5,47
|
38
|
17
|
290
|
|
Tondi,M
|
0,64
|
0,3
|
0,179
|
29,98
|
8,20
|
62,6
|
4,56
|
53
|
31
|
357
|
|
Tondi,G
|
1,03
|
0,36
|
0,234
|
29,35
|
7,47
|
74,1
|
5,46
|
47
|
0
|
490
|
Annexe 3: Projet de normes nigériennes de
rejet de déchets liquides
|
Paramètres
|
normes
|
|
pH
|
6-9,5
|
|
T°C
|
= 50°C
|
|
Matières en suspension (MES)
|
= 1 g/l
|
|
Demande chimique en oxygène (DCO)
|
= 100 mg/l
|
|
Azote total
|
= 10 mg/l
|
|
Ammonium (NH4)
|
= 15 mg/l
|
|
Annexe 4: Teneurs en eau des pieds de Jacinthe
en fonction des sites de prélèvement
|
|
Date
|
Stations
|
Poids frais (g)
|
Poids sec (g) après séchage au four à
60° en 72H
|
Teneur en eau %
|
|
|
|
(Pf-Ps) ×100
|
|
|
|
Pf
|
|
|
|
07/08/2010
|
TOND
|
572,53
|
43,06
|
92,47
|
|
|
|
NYABATTOIR
|
239,45
|
16,74
|
93,00
|
|
|
|
SAGAG
|
190,84
|
13,35
|
93,00
|
|
|
|
08/10/2010
|
TOND
|
575,09
|
43,43
|
92,44
|
|
|
|
TONG
|
504,53
|
40,80
|
91,89
|
|
|
|
NYABATT-G
|
645,3
|
50,22
|
92,21
|
|
|
|
SAGAG
|
270,74
|
18,93
|
93,00
|
|
|
|
14/08/2010
|
SAGAG
|
294,49
|
20,6
|
93,00
|
|
|
|
NYABATT-G
|
389,73
|
35,1
|
90,99
|
|
|
|
TOND
|
450,26
|
17,06
|
96,21
|
|
|
|
TONG
|
219,44
|
29,53
|
86,54
|
|
|
Annexe 5 : Formule pour le calcul de la
demande/offre en azote et en Phosphore
% N = mN / (M- Me)
Avec :
-N azote ;
-mN massa de l'azote après analyse mg
N/kg ;
-M= masse volumique de l'échantillon brute ;
-Me = masse de l'eau désionisée.
% P = mP/ (M - Me)
Annexe 6 : Densité des pieds de
jacinthe au m² per site
|
Date
|
SITES
|
Nombre de pied au m²
|
|
|
TOND
|
Carré 1 : 49
|
|
|
Carré 2 : 61
|
|
|
Carré 3 : 28
|
|
|
Moyenne : 46
|
|
|
NY-ABATTOIRG
|
Carré 1 : 52
|
|
|
Carré 2 : 41
|
|
07/08/2010
|
Carré 3 : 43
|
|
|
Moyenne : 45
|
|
|
SAGAG
|
Carré 1 : 33
|
|
|
Carré 2 : 23
|
|
|
Carré 3 : 23
|
|
|
Moyenne : 26
|
|
|
TOND
|
Carré 1 : 52
|
|
|
Carré 2 : 28
|
|
|
Moyenne : 40
|
|
|
TONG
|
Carré 1 : 53
|
|
|
Carré 2 : 44
|
|
08/10/2010
|
Moyenne : 48
|
|
|
NY-ABATTOIRG
|
Carré 1 : 43
|
|
|
Carré 2 : 47
|
|
|
Moyenne : 45
|
|
|
SAGAG
|
Carré 1 : 57
|
|
|
Carré 2 : 37
|
|
|
Moyenne : 47
|
|
|
SAGAG
|
Carré 2 : 27
|
|
|
Moyenne : 32
|
|
|
NY-ABATTOIRG
|
Carré 1 : 30
|
|
|
Carré 2 : 38
|
|
|
Moyenne : 34
|
|
14/08/2010
|
TOND
|
Carré 1 : 50
|
|
|
Carré 2 : 18
|
|
|
Moyenne : 34
|
|
|
TONG
|
Carré 1 : 17
|
|
|
Carré 2 : 37
|
|
|
Moyenne : 27
|
Annexe 6 : Identité du souteneur
Nom : HASSANE
YOUNOUSSOU
Prénom : Hamadou
Titre du mémoire:
Prolifération des plantes aquatiques envahissantes
sur le fleuve Niger : état des lieux de la pollution en azote et en
phosphore des eaux
Année universitaire :
2009-2010
Ville de soutenance : Ouagadougou
Le pays d'origine : NIGER
Lieu de dépôt : Centre de
Documentation et d'Information du 2iE (CDI)
Secteur d'intérêt :
Gestion Intégrée des Ressources en Eau (GIRE)
| 


