8.2- Composés aromatiques
Les composés aromatiques sont moins fréquents, mais
néanmoins très importants: eugénol, anéthole,
etc.
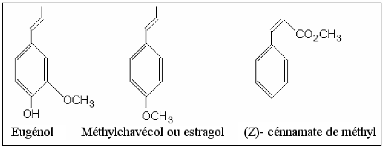
Fig. 4: Structures de quelques arènes
dérivées du phénylpropane (HURTEL, 2006).
Ces composés aromatiques constituent un ensemble
important, car ils sont généralement responsables des
caractères olfactifs et organoleptiques des H.E.: par exemple,
l'eugénol est responsable de l'odeur du clou de girofle (Syzygium
aromaticum) (HURTEL, 2006).
8.3- Composés d'origines diverses
Il s'agit là de produits résultants de la
transformation de molécules non volatiles. Ces composés
contribuent aux aromes de fruits. Compte tenu de leur mode de
préparation, les concrètes(1) et les
absolues(2) peuvent en renfermer. Il en est de même pour les
H.E. lorsqu'ils sont entraînables par la vapeur d'eau (BRUNETON,
1999).
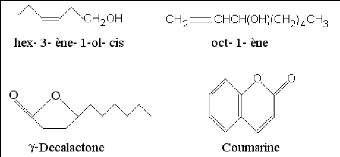
Fig. 5: Quelques composés d'origines diverses
(OCHOA, 2005).
(1) Concrète: produit solide ou semi-solide obtenu
après l'extraction au solvant (éther de pétrole) des
principes odorants de certaines matières premières
végétales (jasmin, rose, mousse de chêne, etc.,) (PIBIRI,
2006).
(2) Absolue: les absolues sont des essences obtenues à
partir de concrètes ou de résinoïdes par lavage de
concrète à l'alcool éthylique. Après glaçage
et filtrations pour éliminer les cires, elles sont concentrées
par distillation sous pression réduite afin d'éliminer l'alcool
(PIBIRI, 2006).
Il est important de signaler que parmi les H.E., on peut
rencontrer des huiles que l'on pourrait qualifier de simples (riches en un
composé prépondérant), de complexes (ne possédant
aucun composé prépondérant) et tous les
intermédiaires sont possibles.
L'un des exemples typiques d'une huile simple est celui de
l'huile de girofle qui contient au moins 80 % d'eugénol et de petites
quantités d'autres produits. Le cas extrême de complexité
peut être illustré par l'huile de vétiver (Vetiveria
zizanoides) qui contient une centaine de composants (JOUHANNEAU, 2000).
9- Paramètres influençant la composition
quantitative et qualitative des
plantes aromatiques
Selon VERRECK (2007), la composition d'une H.E. peut varier
fortement en fonction de: - L'origine de la plante;
- l'ensoleillement;
- la nature du sol;
- la source botanique;
- période de récolte;
- la technique d'extraction des H.E.
Le premier paramètre influençant la composition
chimique est sa biosynthèse et donc son profil génétique.
C'est la raison pour laquelle, une même espèce peut
présenter plusieurs chémotypes(1) de profils chimiques
différents (BENINI, 2007).
Les H.E. contiennent un nombre considérable de familles
biochimiques, dont on vérifiera la présence, par le biais d'un
Chromatogramme qui nous donnera la composition chimique exacte d'une H.E.
(JOCTEUR, 2006). Si tous les organes d'une même espèce peuvent
renfermer une H.E., la composition de cette dernière peut varier selon
sa localisation (NÉPOMUSCÈNE, 1995).
Selon COLETTE (2004), la plante change d'aspect et voit sa
composition chimique se modifier. Ceci se traduit par un changement d'odeur et
de couleur. C'est le cas, par exemple, pour les racines de valériane
(Valeriana officinalis) inodores à l'état frais et qui
deviennent nauséabondes en séchant par dégagement d'acide
valérianique.
La composition varie aussi suivant les organes de la plante
concernée. Les biosynthèses y sont différentes. Par
exemple, l'H.E. d'écorce de cannelle (Cinnamomum zeylanicum)
sera riche en cinnamaldéhyde, alors que l'H.E. de feuille le sera en
eugénol (BENINI, 2007).
(1): La composition chimique de l'H.E. de certaines plantes peut
varier à l'intérieur d'une même espèce; ces
variétés chimiques sont communément appelées
chémotypes.
Le chémotype, également appelé
chimiotype, permet de définir la ou les molécules biologiquement
actives majoritairement présentes dans l'H.E. Associé à la
dénomination latine, la précision du chémotype permet la
compréhension précise du mode d'action des H.E.
Les conditions environnementales influencent aussi la
composition. La température, la quantité de lumière, la
pluviométrie, les conditions édaphiques représentent
autant de causes potentielles de variations de la composition chimique d'une
plante aromatique donnée (CURADO et al., 2006).
Les conditions culturales telles que la date de semis, date de
récolte, les traitements phytosanitaires, l'emploi d'engrais, ainsi que
les techniques de récolte... influencent aussi la composition (ANTON
et al., 2005). Peut-être faut-il, à ce stade, s'attarder
sur la notion de chémotype qui sera utilisée à de
nombreuses reprises dans cette étude. Un chémotype est une race
chimique. En fait, une même espèce végétale peut
fournir des H.E. de compositions chimiques différentes. Ces
différences sont dues à la période de récolte des
plantes, au mode d'extraction utilisé, aux facteurs environnementaux
(altitude, ensoleillement, nature du sol, ...). Prenons l'exemple du basilic
(Ocimum basilicum) (DE MASI et al., 2005). On dira qu'il
s'agit d'un Ocimum basilicum à méthyl chavicol,
sous-entendu de chémotype méthyl chavicol.
On utilise également la notion de chémotype pour
établir une classification des H.E. et les caractériser (MOCKUTE
et al., 2006).
Le nombre des molécules chimiquement différentes
qui constituent une H.E. est variable (jusqu'à 500 molécules
différentes dans l' H.E. de Rose) (PIBIRI, 2006).
10- Stabilité des huiles essentielles
Les H.E. sont volatiles et généralement
très sensibles aux phénomènes d'oxydation. Elles sont
souvent associées à d'autres substances, telles que les gommes et
les résines et tendent même à se résinifier par
exposition à l'air. Ces phénomènes d'altération
modifient fortement la composition chimique des H.E. Les procédés
qui conduisent à l'altération naturelle sont en
général les activités causées par la chaleur et
l'oxygène (O2) de l'air et sont catalysées par la lumière
et la présence de certains métaux (CHIRON, 1996).
- Conservation des huiles essentielles
Les H.E. sont fragiles et volatiles (ANTON et LOBSTEIN,
2005). Elles doivent êtres conservées dans des flacons
colorés, hermétiquement fermés, à l'abri de l'air,
lumière et variations de température.
Si les conditions citées ci-dessus sont
respectées, les H.E. peuvent être conservées jusqu'à
2 à 5 ans en maintenant les flacons en position verticale.
11- Autooxydation des huiles essentielles
L'autooxydation des H.E. est spontanée dont font
l'objet certains solides ou liquides par l'oxygène moléculaire
dans son état fondamental triplet (3O2), à la
température ambiante ou à son voisinage et à la pression
atmosphérique (760 mm Hg) (ANONYME, 2005).
12- Photooxydation des huiles essentielles
La photooxydation est une action conjuguée de
l'oxygène et de la lumière en présence de sensibilisateurs
efficaces (bleu de méthylène, chlorophylle, rose de Bengale,
dicyanoanthracène, oxyde de titane....). Le rôle du
sensibilisateur est d'exciter l'oxygène afin de le faire passer de son
état fondamental triplet à son état excité singulet
(1O2)dans le cas de la sensibilisation par les colorants et de son
état fondamental triplet à son état de superoxyde dans le
cas de la sensibilisation par les composés pauvres en électrons
(e-). Ces deux états excités sont
moins stables, mais plus réactifs (ANONYME, 2005).
13- Chémotypes
Dans ce contexte, la science moderne nous fournit un outil
fondamental et incontournable, le "chémotype" (ou race biochimique de
l'H.E.). Il permet de définir avec précision les composants
biochimiques présents dans une H.E., et donc d'en déduire ses
propriétés thérapeutiques. Biochimiquement
différents, deux chémotypes issus d'une même plante
présenteront non seulement des activités thérapeutiques
différentes, mais aussi des toxicités variables. Les techniques
utilisées pour la détermination du chémotype permettent
également de contrôler la qualité d'une H.E. dans la mesure
où elles permettent de mettre en évidence les traces de
dénaturation par ajout de molécules de synthèse ou
d'autres H.E. ou la présence de résidus d'engrais ou de
pesticides (CHASSAING, 2006).
Le chémotype indique le ou les composants qui
confèrent à l' H.E. une action thérapeutique
particulière sans que ceux-ci soient nécessairement majoritaires
(JOCTEUR, 2006).
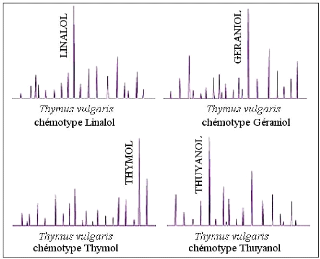
Fig. 6: Illustration simplifiée de CPG de 4
chémotypes différents de thym (PIBIRI,
2006).
14- Toxicité des huiles essentielles
Alors que de nombreux ouvrages font référence
à la toxicité de nombreux produits sur le marché, la
toxicité des H.E. est moins investiguée. Les interactions de ces
produits avec les médicaments ne sont pas bien connues (PIBIRI,
2006).
Les H.E. restent toujours notoires grâce à leurs
diverses propriétés médicinales en l'occurrence les
propriétés anti-inflammatoires, antiseptiques, antivirales,
stimulantes, toniques, calmantes, etc. (KABERA et al., 2002).
D'autres parts, elles peuvent être toxiques. Cette
toxicité est liée à la présence de certains sites
oxygénés (VIAUD, 1993). Parmi les propriétés
indésirables, on peut souligner entre autres : les
propriétés vésicantes, nécrosantes, allergiques,
hépatotoxiques, neurotoxiques, etc. (KABERA et al., 2002).
15- Applications thérapeutiques
Selon la plante dont elles proviennent, les H.E. sont
recommandées en usages antibiotiques, antiviraux, antiseptiques,
fongicides, cicatrisants, digestifs, anti-inflammatoires, sédatifs... on
les utilise par voie orale, à la manière d'un médicament,
usage en inhalation, en diffusion dans l'atmosphère avec un diffuseur
d'essence, en massage (mélangée à une huile de
base) (ODOUL, 2003).
16- Description des pantes utilisées
La flore méditerranéenne occupe une vaste aire
de répartition. Elle s'étend autour de la
Méditerranée, de l'Espagne à la Turquie en passant par les
côtes d'Afrique du Nord et plus particulièrement l'Algérie.
Ce qui caractérise ces plantes, c'est l'adaptation à leur
environnement et au climat méditerranéen
caractérisé par un été chaud et sec et hiver doux
et humide (MACAIRE, 2004).
- Classification des plantes utilisées
Embranchement: Spermatophytes;
Sous-embranchement: Angiospermes; Classe:
Magnoliopsides (Dicotylédones).
Les trois plantes suivantes (le girofle, l'eucalyptus et le
myrte) appartiennent à la famille des Myrtaceae.
16.1- Girofle
Espèce: Syzygium aromaticum.
Synonymes: Caryophyllus aromaticus,
Eugenia aromatica, E. caryophyllata, E.
caryophillus. Dénominations vernaculaires
- Français: clous de girofle, giroflier;
- Anglais: Clove tree.

Fig. 7: Clous de girofle
16.1.1- Caractéristiques
Le giroflier est un arbre petit à moyen, au feuillage
persistant et dense, originaire des petites îles volcaniques de
l'archipel des Moluques en Indonésie (HURTEL, 2001). Le fruit est une
baie appelée « anthofle » allongée de 2,5 à 3 cm
de long sur 1,3 à 1,5 cm le large, de couleur rouge foncé
à maturité. Le clou de girofle a un aspect caractéristique
brun foncé, à saveur chaude, brûlante,
légèrement amère et fortement aromatique (LAREDJ,
2004).
La floraison se déroule du mois de septembre au mois de
Mars (TEUSCHER et al., 2005).
Propriétés
thérapeutiques
Selon LAREDJ (2004), cette plante peut manifester plusieurs
activités entre autres: analgésique dentaire;
antiseptique; stimulant; stomachique.
16.1.2 - Composition chimique de l'H.E. des clous de
girofle
Selon BRUNETON (1999), la composition chimique de l'H.E. du
girofle est caractérisée par la présence d'un
propénylphénol largement prépondérant,
l'eugénol. Majoritairement libre et en partie sous forme
d'acétate d'eugényl, sa teneur oscille entre 70 et 85 %.
L'eugénol est accompagné de plusieurs dizaines de composés
terpéniques:
- des sesquiterpènes: á et â
caryophyllènes (de 7 à 10%), á et â
humulènes, á amorphène, á murolène,
calaménène, calacorène.
- des esters: hexanoates d'éthyle, acétates de
2-heptanyle, de 2-nonalyle, de styralyle, de benzyle, de terpényle et
d'éthylphényle;
- des oxydes: oxyde de caryophyllène, époxyde
d'humulène.
L'H.E. des clous de girofle, extraite par hydrodistillation,
contient principalement deux composés: l'eugénol et
l'acétyleugénol (TREINER, 1999).
D'après (TREINER, 1999), l'une des
caractéristiques fondamentales de l'H.E. des clous de girofle est sa
densité élevé (d= 1,066 > d eau = 1.00), ce qui nous
permet de les séparer par simple décantation: même
caractéristique partagée avec les huiles de cannelle et de
sassafras.
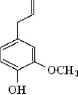
Eugénol
16.2- Eucalyptus 16.2.1-
Caractéristiques
Parmi les 4000 espèces de Myratceae, le genre
Eucalyptus en regroupe au moins 600 disséminées un peu partout
dans le monde (HURTEL, 2001). L'Eucalyptus globulus Labill. (du nom de
Labillardière qui le découvrit en 1800 lors d'un voyage en
Australie) est une espèce très cultivée. Il a
été introduit dans le sud de la France par Ramel, en 1860. Il
s'est très bien acclimaté dans l'ensemble des pays
méditerranéens.
Ses longues racines font qu'il joue un rôle important
dans la fixation des sols (retard à la désertification) et dans
le drainage des terrains marécageux (il a été introduit en
1857 en Algérie pour drainer les terrains de régions
touchées par la malaria) (TREINER, 2000).

Fig. 8: Feuilles d'eucalyptus.
16.2.3- Constituants de l'huile essentielle
D'après TREINER (2000) et HURTEL (2001), la teneur en
H.E. varie entre 0,5 et 3,5%. En 1870, le français CLOËZ donne au
principal constituant de l'huile d'Eucalyptus globulus Labill. le nom
d'eucalyptol. En 1884, JAHNS l'identifie comme étant le
1,8-cinéole (constituant majoritaire: environ 60 % à 80 %), le
pourcentage restant représente plus de vingt-cinq composés de
nature terpénique ont été identifiés,
principalement de á-pinène, puis de l'aromadendrène, du
globulol, viennent ensuite le limonène, le p-cymène, le
lédol....
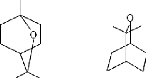
Eucalyptol (1,8-cinéole)
16.2.4- Utilisations
L'H.E. possède des propriétés
bactéricides, antiseptiques (efficace contre les puces, elle est
utilisée dans les colliers insecticides pour animaux). Mais elle a pour
principal débouché l'industrie pharmaceutique en raison de
propriétés antiasthmatique, expectorantes et stimulantes de
l'épithélium bronchique et mucolytique. On l'utilise aussi comme
aromatisant pour masquer le goût de certaines préparations
pharmaceutiques (TREINER, 2000).
16.3- Myrte commun
Le myrte commun (Rihane en Kabyle) forme le genre
Myrtus de la famille des myrtacées. Il a pour nom latin
Myrtus communis (MICROSOFT ENCARTA, 2008). Deux
variétés sont utilisées: l'une donnant une H.E. rouge et
l'autre une H.E. verte. Les feuilles donnent une huile jaune-orangée au
parfum frais et doux (HURTEL, 2001).
16.3.1- Caractéristiques
Le myrte commun est un arbuste persistant de 1 à 3 m de
haut, caractéristique des formations végétales de type
maquis(1). Il est originaire du bassin méditerranéen.
Les fleurs sont blanches et très odorantes, de même que les
fruits, de petites baies vertes devenant à maturité noire
violacées au parfum prononcé. Il est odorant, aux feuilles vert
vif, ovales, lisses, brillantes et petites (2 à 4 cm). Très
utilisé jusqu'au XVIIIème siècle, il est
maintenant un peu oublié (HURTEL, 2001).
D'après TEUSCHER (2005), Myrtus communis peut
vivre plus de 300 ans, comme le lentisque (Pistacia lentiscus) qui
sont des plantes qui poussent à l'état spontané en
Algérie. Contrairement aux autres espèces de sa famille
(myrtacées), pour la plupart originaires des zones tropicales de
l'hémisphère sud, le myrte se rencontre dans les régions
tempérées chaudes de l'hémisphère nord (MICROSOFT
ENCARTA, 2008).
(1) Zone de formation végétale dense,
caractéristique des sols siliceux, composée de petits arbustes
adaptés à la sécheresse, souvent épineux et pouvant
atteindre 3 à 4 m de haut.

Fig. 9: Myrte commun.
16.3.2- Composition chimique et
propriétés
Le myrte contient 0,3 à 0,5 % d'une H.E. aromatique,
composée d'un alcool primaire, le myrténol, et d'une substance
complexe, le myrtol, renfermant entre autres de l'eucalyptol. Il est
astringent, antiseptique, stimulant, le myrte a des emplois voisins de ceux de
l'eucalyptus (ENCYCLOPEDIA UNIVERSALIS, 2008).
16.3.3- Utilisations
Selon HURTEL (2001), l'huile en inhalation est utile dans les
infections bronchiques et des voies respiratoires supérieures. Elle est
aussi préconisée dans les infections urinaires.
Traditionnellement, l'infusion des feuilles (30 g par litre d'eau) est
utilisée comme cicatrisant antiseptique.
16.4- Sarriette
Cette plante appartient à la Famille des
Lmiaceae.
Dénominations vernaculaires
- Français: sarriette des jardins, sarriette commune,
sarriette annuelle, savourée, herbe aux pois, herbe aux haricots, herbe
de Sain-Julien.
- Anglais: savory, summer savory.
16.4.1- Caractéristiques
C'est une plante annuelle de 30 cm de haut (plus rarement 60
cm), à racine fuselée et fibreuse. Elle ne comprend qu'une seule
tige érigée qui se ramifie en de nombreux rameaux
étalés, ce qui lui confère une allure touffue rappelant le
thym (ex. Thymus vulgaris). Les rameaux rougeâtres sont
recouverts d'un fin duvet et se lignifient à la base avec l'âge
(TEUSCHER, 2005).
Les feuilles, de couleur vert cendré, ont 4 cm de long
sur 0,5 cm de large; elles sont opposées, entières,
linéaires, elles dégagent une odeur puissante et agréable
et une saveur aromatique, légèrement
poivrée (LINDBERG, 1996).
Les pays d'origine sont répartis de l'est des
régions méditerranéennes jusqu'à l'ouest, l'Iran et
au Caucase, l'ouest de l'Asie, l'Inde, l'Afrique du sud et l'Amérique du
Nord.

Fig. 10: Sarriette des jardins.
16.4.2- Composition chimique
Le rendement en H.E. est de l'ordre de 0,3 à 4,2 %; ses
principaux constituants sont le carvacrol (20 à 85 %), le
ã-terpinène (10 à 40 %) et le p-cymène (5
à 25 %); ils sont accompagnés de â-caryophyllène, de
myrcène, d'á-pinène, d'eugénol,
d'á-terpinène et de thymol; dans une H.E. provenat de
l'ex-Yougoslavie, le thymol domine ( 40 % ). Les dérivés d'acide
hydroxycinnamique (principe amer des Labiées) constituent environ 3,4 %
avec essentiellement de l'acide rosmarinique (0,4 à 2,6 %) (LAWRENCE,
1992). Selon LINDBERG (1996), les flavonoïdes, les triterpènes et
les sérols constituent aussi une partie de cette H.E.
16.4.3- Propriétés
MENPHINI (1993), ont rapporté que les H.E.
présentent des propriétés antimicrobiennes.
Les extraits de sarriette sont des accepteurs d'O2 et des capteurs de
radicaux libres, à cause de leur richesse en acide rosmarinique et en
flavonoïdes diphénoliques. Ce sont de bons antioxydants et peuvent
considérablement allonger la durée de conservation des produits
carnés (LINDBERG, 1996).

CHAPITRE II
Activités Biologiques des
H.E.
| 


