UNIVERSITE CHEIKH ANTA DIOP DE DAKAR
*****
FACULTE DE MEDECINE DE PHARMACIE ET D'ODONTO-STOMATOLOGIE
*****
DAKAR FANN REPUBLIQUE DU SENEGAL

Année 2009 N° ...
ETHIQUE DE LA RECHERCHE BIOMEDICALE AU
GABON
MEMOIRE
POUR L'OBTENTION DU C.E.S. DE MEDECINE LEGALE ET REPARATION
JURIDIQUE DU DOMMAGE CORPOREL
PRÉSENTÉ ET SOUTENU
LE 23 JUIN
PAR
DR. GUY AURELIEN MBATCHOU
DIRECTEUR DE MEMOIRE : Docteur
Mohamed SOUMAH
Assistant en Médecine Légale
JE DEDIE CE MEMOIRE A :
- A MON FEU PERE JEAN
MBATCHOU
- A MA FEUE MERE ROSALIE TCHUIGOUA
- A MON EPOUSE PHILIPPINE
- A MES ENFANTS ET NEVEUX
- A MES FRERES ET SOEURS
TOUTE MA GRATITUDE AU:
- PROFESSEUR MAMADOU LAMINE SOW.
- PROFESSEUR PIERRE EFFA
- DR HASSAN
BAH
- DR SOUMAH MOHAMED
- Me BADARA FALL
- MME MENDY VERONIQUE
- MME FATOU NDIAYE
- MES AMIS
ET A TOUS LES AUTRES ENSEIGNANTS DE L'UCAD DE DAKAR OU
D'AILLEURS QUI ONT CONTRIBUE A MA FORMATION ET A LA
REDACTION DE CE DOCUMENT.
ABREVIATIONS
|
C.E.S.V.S
|
Comité d'éthique pour les sciences de la vie et
de la santé
|
|
C.H.L
|
Centre hospitalier de Libreville
|
|
C.H.R
|
Centre hospitalier régional
|
|
C.I.O.M.S
|
Conseil des organisations internationales des sciences
médicales
|
|
H.P.I
|
Hôpital Paul Igamba
|
|
J.O
|
Journal officiel
|
|
N.E.B.R.A
|
Networking for Ethics on Biomedical Research in Africa
|
|
O.M.S
|
Organisation mondiale de la santé
|
|
P.A.B.I.N
|
Réseau panafricain de bioéthique
|
|
P.R
|
Présidence de la république
|
|
R.B.P.E.H
|
Recherches biomédicales portant sur les êtres
humains
|
|
S.I.D.A
|
Syndrome immunodéficitaire acquis
|
|
V.I.H
|
Virus de l'immunodéficience acquise
|
|
U.N.E.S.C.O
|
Organisation des nations unies pour l'éducation, la
science et la culture
|
SOMMAIRE
1- INTRODUCTION
2- CONTEXTE ET JUSTIFICATION
3- REVUE DE LA LITTERATURE
4- HYPOTHESE
5- OBJECTIFS
5-1 Objectif général
5-2 Objectifs spécifiques
6- METHODOLOGIE
7- RESULTATS
8- ANALYSE ET COMMENTAIRE
9- RECOMMANDATIONS
10- CONCLUSION
11- REFERENCES BIBLIOGRAPHIQUES
12- ANNEXES
TABLES DE MATIERE
|
1- Introduction
9
1-1 Généralités et problématique
10
2- Contexte et justification
14
3- Revue de la littérature
16
4- Hypothèse
18
5- Objectifs
20
5-1 Objectifs général
21
5-2 Objectifs spécifiques
21
6- Matériel et méthode
22
6-1 Cadre de l'étude
23
6-1-1 Caractéristique géographique
23
6-1-2 Organisation du système de santé
23
a- Conditions d'exercice de la médecine
24
b- conditions de recrutement des médecins
24
c- Profil des médecins
24
6-1-3 Cadre législatif et réglementaire
24
6-1-3-1 Constitution du Gabon
24
6-1-3-2 Loi n°22/2000
25
6-1-3-3 Décret n°001158/PR
25
6-1-3-4 Code de déontologie médicale
25
6-2 Population étudiée
25
6-3 Echantillonnage
25
6-4 Méthodologie utilisée
25
6-5 Difficultés rencontrées
2628
7- Résultats
29
7-1 Résultats globaux
30
7-2 Profil professionnel de la population
étudiée
30
7-2-1 Répartition du nombre de médecins par
qualification professionnelle
30
7-2-2 Répartition des médecins par
département de fonction
31
7-2-3 Répartition des médecins selon l'institution
sanitaire de fonction
32
7-3 Avis des médecins participants
33
7-3-1 Avis des médecins participants sur la
réalisation des RBPEH au Gabon
33
7-3-2 Avis des médecins participants sur la perception des
sujets expérimentaux comme ayant un...
33
7-3-3 Avis des médecins participants sur la perception de
l'éthique comme problème lors des RBPEH
33
7-3-4 Avis des médecins participants sur l'existence d'un
comité d'éthique
34
7-3-5 Avis des médecins participants sur la
nécessité d'évaluer les RBPEH
34
7-3-6 Avis des médecins participants sur la protection de
la confidentialité
34
7-4 Profil des RBPEH menées au Gabon
34
7-4-1 Recherches parrainées de l'extérieur
35
7-5 Attitude par rapport à la conception des
recherches
35
7-5-1 Prise en compte des considérations
éthiques
35
7-5-2 Prise en compte des particularités (sociales,) et
implication des communautés expérimentales
35
7-5-3 Prévision d'une couverture d'assurance
35
7-5-4 Evaluation des bénéfices et des risques
36
7-5-5 Inclusion des personnes vulnérables comme des
personnes légalement inaptes
36
7-6 Attitude par rapport aux
démarches
36
7-6-1 Soumission des recherches pour évaluation à
un comité d'éthique de la recherche
36
7-6-2 Recherches ayant fait l'objet de modifications après
avis rendu sur leur caractère éthique
36
7-6-3 Validation de la mise en oeuvre des recherches
parrainées de l'extérieur
37
7-7 Attitude par rapport à la pré
réalisation: L'Obtention du consentement
37
7-7-1 Information des participants à la recherche
37
7-7-2 Personne chargée de recueillir le consentement
38
7-7-3 Avis sur le temps de réflexion accordée au
sujet pressenti pour faire connaitre sa décision
38
7-7-4 Mode d'expression du consentement
38
7-7-5 Caractère volontaire du consentement
39
7-7-6 Implication de la communauté d'appartenance
39
7-7-7 Obtention du consentement des personnes ne pouvant
consentir par elles - mêmes
39
7-7-8 Documentation du consentement
40
7-8 Attitude par rapport à la réalisation
pratique
40
7-8-1 Information des participants en cas d'expériences
adverses
40
7-8-2 Exercice de représailles sur les auteurs de
dénonciations d'inconduites scientifiques
40
7-9 Attitude par rapport au suivi et à la fin des
travaux de recherche
40
7-9-1 Fourniture des informations sur l'état d'avancement
des recherches
40
7-9-2 Communication des résultats des recherches
41
7-9-3 Publication des résultats des recherches
42
8- Analyse et commentaire
43
9- Recommandations
50
10- Conclusion
53
11- Références bibliographiques
55
12- Annexes
60
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1- INTRODUCTION
La loi Huriet- Serusclat [3] définit la recherche
biomédicale comme étant « des essais ou
expérimentations organisés et pratiqués sur l'être
humain en vue du développement des connaissances biologiques et
médicales qu'ils soient ou non menées dans un but
thérapeutique ».
Cette définition fait ressortir le caractère
indispensable de la recherche biomédicale face à l'apparition des
nouvelles maladies, au développement de la résistance aux
antibiotiques, à la persistance des maladies non guérissables ou
à la nécessité d'améliorer les techniques
d'explorations et de soins.
Cette recherche va s'appliquer d'abord à des
modèles animaux, puis à l'être humain sain et enfin
à l'être humain malade.
Cependant la réalisation des recherches
biomédicales quoique indispensable est source de problèmes
majeurs, en l'occurrence lorsqu'elles portent sur les êtres humains car
la soif de savoir ou de développer les connaissances ne doit pas
pourtant s'exercer sans limites, ni précautions. Les règles de
validation scientifique d'une expérimentation doivent être
strictement respectées ainsi que l'indépendance et la
sécurité des patients inclus dans les études.
Ces règles sont tantôt inscrites dans les
recommandations internationales, des normes consensuelles, ou des textes
légaux et réglementaires [21].
1-1 Généralités et
problématique
Le mot éthique du grec [19] (êthicos
« qui concerne les moeurs, moral ») est la science de la
morale. Elle désigne l'ensemble des principes moraux à la base de
la conduite d'une personne.
La bioéthique vient du mot grec Bios (vie),
êthicos (moral) a donné lieu à plusieurs
définitions :
· Pour les anglo-saxons, elle est l'ensemble des
problèmes moraux soulevés par la protection de la vie. Cette
vision est celle qu'a retenue Van Ressenlar Potter [20] dans ses
écrits.
· Pour le Larousse, la bioéthique est un ensemble
des principes moraux et de règles déontologiques appliqués
à la recherche biomédicale et à la pratique de la
médecine.
· Pour le groupe de rédaction de la
déclaration [18] relative à des normes universelles en
matière de bioéthique on entend par bioéthique, un champ
d'étude systématique, pluraliste et interdisciplinaire qui aborde
les questions morales, théoriques et pratiques, que posent la
médecine et les sciences de la vie appliquées aux êtres
humains et au rapport de l'humanité à la biosphère.
Les questions d'éthique étaient au centre de la
pratique médicale déjà avec Hippocrate [5] il y a plus de
deux mille ans.
Mais la bioéthique en tant que domaine de
réflexion est née en 1945 lors du procès de
Nuremberg [22] chargé de juger les
expérimentations médicales perpétrées par les
nazies.
Ainsi, les grandes étapes qui ont progressivement
défini un cadre de recommandations pour l'organisation des recherches
biomédicales sont apparues après la seconde guerre
mondiale :
· Le Code de Nuremberg [6], élaboré en 1947
qui est le texte fondateur de la bioéthique, énonce le principe
du consentement volontaire des participants avant toute
expérimentation.
· La Déclaration universelle des droits de l'homme
[7] adoptée par l'assemblée générale des nations
unies le 10 décembre 1948 à Paris, stipule en son article 5
« Nul ne sera soumis à la torture, ni à des peines ou
traitements cruels, inhumains ou dégradants »
· La Déclaration d'Helsinki [8] qui regroupe les
principes éthiques dont les objectifs sont de fournir des
recommandations et de guider les médecins dans les recherches
biomédicales. Adoptée en 1964 elle a été
révisée sept fois (Tokyo, 1975 ; Venise, 1983 ;
Hong-Kong, 1989 ; Somerset West, 1996 ; Edimbourg, 2000 ;
Washington, 2002 ; Tokyo, 2004).
· Le Pacte international relatif aux droits civil et
politique [9] : adopté par l'assemblée
générale des nations unies en 1966, il stipule en son article 7
que « Nul ne sera soumis à la torture, ni à des peines
ou traitements cruels, inhumains ou dégradants, en particulier il est
interdit de soumettre une personne sans son libre consentement à une
expérimentation médicale ou scientifique »
Ce pacte énonce la valeur humaine fondamentale devant
régir toutes les recherches impliquant les sujets humains.
· Le Rapport Belmont [10] adopté en 1976 qui est
une déclaration des principes éthiques fondamentaux et des
directives qui devraient aider à résoudre les problèmes
éthiques liés à la conduite de la recherche avec les
sujets humains.
· Les Principes directeurs internationaux
d'éthiques de la recherche biomédicale concernant les sujets
humains (C.I.O.M.S) [11] adoptés en 1982, révisés en 1983
et 2002, comportent les dispositions détaillées sur le
consentement exigé dans le domaine de la recherche
· La Convention sur les droits de l'homme et la
biomédecine du conseil de l'Europe [14] adoptée en 1997 et ses
protocoles consacrent plusieurs articles à la question du consentement
libre et éclairé.
· Enfin la Déclaration universelle sur la
bioéthique et les droits de l'homme [12] adoptée en 2005 par
l'UNESCO qui consacre deux articles à la question du consentement :
l'article 6, traite du principe du consentement et l'article 7 couvre le cas
des personnes n'ayant pas la capacité de consentir.
· A l'échelle africaine nous avons la charte
africaine des droits de l'homme et des peuples [13] adoptés en 1981
à Nairobi qui stipule en son article 5 « tout individu a droit
au respect de la dignité inhérente à la personne humaine
et à la reconnaissance de sa personnalité juridique. Toutes
formes d'exploitation et d'avilissement de l'homme notamment l'esclavage, la
traite des personnes, la torture physique ou morale et les peines ou les
traitements cruels ou dégradants sont interdites »
Ainsi ces différents textes s'articulent autour de 3
principes fondamentaux d'éthique :
· Le respect de la personne : ce principe regroupe
deux convictions éthiques: premièrement les personnes doivent
être traitées comme des agents autonomes, deuxièmement les
personnes avec une autonomie diminuée ont droit à une
protection.
La conformité à ce principe passe par
l'obtention par l'investigateur du consentement libre, éclairé et
exprès [3] de tout sujet pressenti pour participer à une
recherche biomédicale impliquant les êtres humains. Le
consentement éclairé qui est le libre choix fait par un sujet
volontaire de participer à une recherche biomédicale après
en avoir été informé des objectif, de la
méthodologie, des contraintes, des bénéfices et des
risques éventuels
· La bienfaisance : La maxime d'Hippocrate [5] "ne
faite pas de tort" constitue le socle du principe de bienfaisance qui suppose
l'obligation éthique faite aux chercheurs dans une étude
biomédicale impliquant les êtres humains, d'apporter le plus grand
bien possible et de réduire au maximum ce qui peut porter
préjudice. Dans le même ordre d'idée, il est aussi admis
que les intérêts de la science et de la société ne
prévalent jamais sur le bien être du sujet. De ce principe,
proviennent les normes éthiques en matière de recherche
biomédicale portant sur les êtres humains qui recommandent une
validité scientifique et une justification éthique des recherches
biomédicales impliquant les êtres humains.
· La justice : Ce principe signifie l'obligation
éthique de traiter chacun conformément à ce qui est
moralement équitable et approprié, de donner à chacun ce
qui lui est dû. C'est de ce principe que découle la norme suivant
laquelle une recherche parrainée de l'extérieur doit en effet
correspondre aux besoins et priorités du pays hôte dans lequel est
envisagée son exécution ; elle doit en plus être
conforme aux exigences éthiques tant du pays ou de l'organisme de
provenance de la promotion que du pays hôte.
Ces textes en général, et la Déclaration
universelle sur la bioéthique et les droits de l'homme en particulier
devant servir de guide à l'élaboration des législations
et réglementations nationales en matière de recherches
biomédicales, nous amènent à nous interroger sur la mise
en application de ces principes fondamentaux d'éthiques depuis la
conception, jusqu'à la publication des résultats des
recherches biomédicales portant sur les êtres humains.
C'est pour répondre à cette question que
nous avons intitulé notre travail « Ethique de la
recherche biomédicale au Gabon »
:
2- CONTEXTE ET JUSTIFICATION
Les pays en voie de développement en
général, et ceux d'Afrique sub-saharienne doivent s'impliquer
davantage dans la promotion de la recherche en santé afin de trouver des
solutions spécifiques et adaptées aux innombrables
problèmes de santé publique qui constituent des handicaps au
développement socio-économique de ces pays [23].
Au Gabon, malgré l'absence d'infrastructures de
recherches comparable à celles des pays du nord quelques projets de
recherche ont néanmoins étés réalisés.
Dans le domaine des sciences biomédicales la
réalisation dans un « cadre informel » de quelques
essais cliniques concernant les pathologies infectieuses endémiques au
Gabon (paludisme, VIH/SIDA, fièvre hémorragique à virus
Ebola.....) impose d'urgence l'initiation d'une réflexion
éthique, la formation du personnel de santé et l'institution d'un
cadre réglementaire d'évaluation des protocoles de recherche.
3- REVUE DE LA LITTERATURE
Depuis les scandaleuses expérimentations humaines
nazies et le procès historique intenté contre leurs auteurs dit
procès de Nuremberg couronné par l'adoption d'un code qui porte
le nom de cette ville allemande une prise de conscience particulièrement
en occident a permis d'instaurer un débat permanent favorisant la mise
en place sans cesse adaptable à l'évolution des pratiques, des
normes encadrant la recherche biomédicale impliquant des personnes
humaines [38].
Concernant le Gabon très peu d'études ont
étés consacrées au débat éthique :
cependant l'étude [24] de monsieur Mazabalo Aleza intitulé
« Ethique de la recherche biomédicale : approche
normative » analyse les dispositifs juridiques en matière de
recherche biomédicale en Afrique, s'agissant du Gabon cette étude
fait référence à la loi N°22/2000 [2] qui
détermine les principes fondamentaux de la recherche scientifique en
république gabonaise. Et il conclut son analyse par le fait
que cette loi bien que définissant les missions du comité
national d'éthique en matière de recherche scientifique qu'elle
institue renvoie sa composition et son fonctionnement aux dispositions d'un
décret en conseil des ministres ; décret [4] qui a
été adopté le 26 mars 2009 soit plus de 8ans après
la loi et 3 ans après l'étude de monsieur Mazabalo.
Le mérite de cette étude, est d'avoir
révélé le caractère
« rudimentaire » ou l'absence des textes encadrant les
recherches biomédicales. Cependant un des points faibles c'est de
n'avoir pas fait allusion à la mise en pratique des principes
énoncés par ces différents textes.
4- HYPOTHESE
La recherche biomédicale peut-elle se concevoir sans un
respect strict des règles éthiques, déontologiques et
légales de notre profession ?
5- OBJECTIFS
5-1 Objectif général
- Vérifier que les principes fondamentaux
d'éthique guident l'élaboration des projets d'étude
scientifique.
5-2 Objectifs spécifiques
- Identifier le cadre juridique et institutionnel encadrant la
recherche biomédicale
- Identifier les acteurs de la recherche biomédicale
- Identifier le profil des différents projets de recherche
biomédicale
- Identifier l'instance chargée de valider les protocoles
de recherche
- Identifier le mode de recrutement des sujets
- Décrire les conditions de recueil du consentement
- Vérifier qu'un temps de réflexion est
accordé au sujet pour faire connaître sa décision
- Identifier le mode d'expression du consentement
- Décrire les modalités d'obtention du consentement
des personnes ne pouvant consentir par elles mêmes
- Identifier le mode de consignation du consentement.
- Identifier les personnes, les organismes, les autorités
à qui sont destinés les résultats des travaux des
recherches.
- Faire des propositions susceptibles d'améliorer le
respect des principes fondamentaux d'éthique lors des travaux de
recherche biomédicale.
6- MATERIEL ET METHODE
6-1 Cadre de l'étude
Notre étude s'est déroulée au Gabon
6-1-1 Caractéristique géographique
Le Gabon est un pays situé à l'ouest de
l'Afrique centrale sur l'équateur. Il est
délimité :
- au nord par le Cameroun
- au sud est par la république du Congo
- à l'ouest par l'océan atlantique
- au nord ouest par la république de Guinée
équatoriale
Le Gabon a une superficie de 267670 km2 avec une population
estimée à environ 1 300 000 habitants, selon
l'enquête démographique [24] et de santé 2000. Sa capitale
politique est Libreville, Port-Gentil étant sa capitale
économique.
Le Gabon est divisé en 09 régions :
- l'Estuaire
- l'Ogooué- Maritime
- le Haut-Ogooué
- le Woleu-Ntem
- le Moyen-Ogooué
- la Ngounié
- l'Ogooué-Lolo
- la Nyanga
- l'Ogooué-Ivindo
Chaque région est dirigée par un gouverneur
6-1-2 organisation du système de santé
Le découpage territorial du système gabonais de
santé se fait sur 6 niveaux :
- département sanitaire au nombre de 47
- case de santé au nombre de 66
- dispensaire au nombre de 366 dont 345 publics et 21
privés
- centre de soins au nombre de 42
- hôpital régional au nombre de 9
- hôpital national au nombre de 1
Les services publics, parapublics, militaires et privés
se superposent
a- Conditions d'exercice de la médecine [26]
- Etre titulaire du diplôme d'état de docteur en
médecine
- Etre inscrit à l'ordre des médecins du
Gabon
- Pour les étrangers être
détenteur d'une autorisation d'exercer la médecine en
république gabonaise délivrée par le ministère de
la santé publique, d'une autorisation individuelle d'emploi
délivrée par le ministère du travail, de l'emploi et de la
prévoyance sociale et de la carte de séjour.
b- Condition de recrutement :
- La fonction publique.
- Dans le cadre de la coopération.
c- Profils des médecins :
- Médecins généralistes
- Médecins spécialistes
- Enseignants
- Chercheurs
6-1-3 Le Cadre juridique
6-1-3-1 La Constitution de la République
Gabonaise
Le préambule de la constitution du Gabon [1] du 26 mars
1991, modifiée par les lois du 18 mars 1994, du 29 septembre 1995, du 25
avril 1997 et du 11 octobre 2000
Affirme solennellement son attachement aux droits de l'homme
et aux libertés fondamentales telles qu'ils résultent de la
déclaration des droits de l'homme et du citoyen de 1789
6-1-3-3 La loi n° 22/2000 [2]
Détermine les principes fondamentaux de la recherche
médicale au Gabon
6-1-3-4 Décret n° 001158/PR [4]
Décret pris en conseil de ministre le 26 mars 2009,
qui institue, le C.E.S.V.S et précise son rôle, notamment veiller
au respect de la dignité humaine et de la protection de la vie ainsi que
la maîtrise et l'encadrement nécessaire des applications de cette
rapide évolution de la science à la personne humaine dans le
pays.
6-1-3-5 Code de déontologie
Au Gabon, il n'existe aucun décret instituant le code de
déontologie médicale [27]
6-2 Population étudiée
- Est constituée des médecins remplissant les
conditions requises pour l'exercice de la médecine en république
Gabonaise et exerçant dans les structures hospitalières
privées et publiques de Libreville et de Port-Gentil.
6-3 L'échantillonnage
Entre le 01 janvier et le 31 janvier 2009 nous avons
procédé à un recensement des structures privées et
publiques susceptibles de nous permettre d'avoir une idée globale sur la
mise en application des principes fondamentaux d'éthique lors des
R.B.P.E.H au Gabon.
Nous avons choisi d'envoyer notre questionnaire dans les
structures hospitalières suivantes :
- pour la ville de Libreville : C.H.L, Fondation Jeanne
Ebori, Polyclinique Chambrier, polyclinique El Rapha.
- pour la ville de Port-Gentil : C.H.R, H.P.I, Clinique du
Littoral, Clinique Mandji, Clinique Ayile, Polyclinique Billie.
Ce choix s'expliquait par le fait que nous avons pu obtenir
les autorisations des différents responsables de ces hôpitaux et
cliniques qui disposent des départements ou services de médecine
et spécialités, de chirurgie, de gynéco
obstétrique, de pédiatrie, et de biologie clinique ; donc
étaient susceptibles de regrouper les médecins, les
médecins- chercheurs, les médecins chercheurs enseignant.
Ainsi nous avons distribué 90 questionnaires par la
méthode du porte à porte.
Notre échantillon était composé des
- Médecins remplissant les conditions d'exercice de la
médecine en république Gabonaise, qui ont été
rencontré dans ces différentes structures hospitalières
pendant la période de l'étude, qui ont accepté de
participer à l'étude, qui ont remplit et rendus les
questionnaires dans les délais impartis.
Soit 50 répondants à notre questionnaire.
6-4 Méthodologie utilisée
Il s'agissait d'une étude transversale menée de
février 2009 à mai 2009 auprès des médecins
exerçant dans les structures hospitalières publiques,
privées de Libreville et de Port-Gentil afin de recueillir des
informations sur le respect des principes fondamentaux d'éthique lors
des R.B.P.E.H au Gabon.
Pour cette étude nous avons retenu les variables
suivantes :
§ Profil professionnel de la population
étudiée
§ Qualification professionnelle
§ Département de fonction
§ Institution sanitaire de fonction
§ Avis des médecins sur :
- le caractère indispensable des RBPEH au Gabon
- l'existence d'intérêts pour le participant
à une RBPEH
- la nécessité d'une évaluation
scientifique ou éthique des RBPEH
§ Profil des RBPEH menées de 1998-2008
§ Attitude des médecins investigateurs par rapport
à :
- La conception des recherches
- Les démarches
- La pré réalisation : l'obtention du
consentement
- le suivi et la fin
Ainsi nous avons élaboré un questionnaire fait
de 7 parties :
§ Une première partie d'identification qui a
permis de retracer le profil professionnel de chaque médecin.
§ Une deuxième partie faite de 9 questions
reparties en 3 groupes comme suit :
- connaissances globales éthiques en
matière de recherche biomédicale et identification des
comités d'éthique.
- identification du profil des médecins
investigateurs.
- identification du profil des recherches
menées par chaque médecin investigateur
§ Les 3ème, 4ème,
5ème, 6ème et 7ème parties ont
permis :
- d'évaluer l'attitude éthique la
plus souvent adoptée par chaque médecin investigateur tout long
des différentes étapes des recherches qu'il a menées.
La récolte des informations s'est faite sur une
période de trois mois
Nous avons utilisé les logiciels Microsoft Word et
Excel pour le traitement et l'analyse des données.
Notre travail n'a pas été soumis à un
comité d'éthique pour la simple raison que celui-ci
n'était pas institué au début de notre travail.
L'anonymat et la confidentialité des informations
recueillies ont étés respectés
6-5 Difficultés rencontrées
Les difficultés rencontrées lors de la
réalisation de cette étude sont :
· La grève en cours dans les hôpitaux
publiques ne nous a pas permis de rencontrer les médecins de plusieurs
structures hospitalières telles que : l'hôpital
pédiatrique Owendo, l'hôpital N'kembo, hôpital
Mélen.
· L'absence de réponse à nos demandes
d'autorisations de la part de plusieurs structures dont le centre international
de recherches médicales de Franceville.
· La méfiance des répondants
vis-à-vis du questionnaire car ne sachant pas quelle serait
l'utilisation future des réponses.
· L'éloignement des villes de Libreville et de
Port-Gentil qui ne se sont desservis que par la voie aérienne et
maritime.
· Le temps mis par les participants pour rendre les
questionnaires remplis.
7- RESULTATS
7-1 Résultats globaux
Notre enquête a été réalisée
dans les formations hospitalières privées et publiques de
Libreville, Port-Gentil.
Le questionnaire a été distribué à 90
médecins en exercice dans ces centres hospitaliers.
Sur les 90 médecins, 50 ont remplis et rendu le
questionnaire soit un taux de participation de 55, 5%.
Des 50 médecins ayant remplis et rendus le questionnaire,
15 ont déclaré avoir été au moins une fois
investigateur sur les dix dernières années ; seuls 10 des
15 médecins investigateurs ayant rempli et rendu le questionnaire ont
affirmé avoir menées des RBPEH au Gabon soit une participation de
66,66%.
7-2 Profil professionnel de la population
étudiée
7-2-1 Répartition du nombre des médecins par
qualification professionnelle
Des 50 médecins ayant participé à
l'étude :
- 30 soit 60% n'étaient ni chercheurs ni enseignants
Des 10 médecins investigateurs ayant rempli et rendu le
questionnaire, 4 soit 40% ont déclaré n'être ni chercheurs
ni enseignants ; 3 soit 30% ont déclaré être des
enseignants et 3 soit 30% ont déclaré être médecins
- chercheurs.
Tableau I :
Répartition des médecins participants et des
médecins investigateurs selon la qualification
professionnelle
|
Médecins participants n (%)
|
Médecins investigateurs
n (%)
|
|
médecins
|
30 (60%)
|
4 (40%)
|
|
Médecins chercheurs
|
5 (10%)
|
3 (30%)
|
|
Médecins enseignants-chercheurs
|
15 (30%)
|
3 (30%)
|
|
Total
|
5O (100%)
|
10 (100%)
|
7-2-2 Répartition des médecins par
département de fonction
Des 50 médecins ayant participé à
l'étude :
- 30 (60%) étaient en fonction dans les
départements de médecine et spécialités.
- 5 (10%) étaient en fonction dans les
départements de gynécologie- obstétrique.
- 10 (20%) étaient en fonction dans les
départements de pédiatrie.
- 3 (6%) étaient en fonction dans le département
de biologie clinique.
- 2 (4%) étaient en fonction dans le département
de chirurgie
Des 10 médecins investigateurs ayant participé
à l'étude :
- 5 (50%) étaient en fonction dans les
départements de médecine et spécialités.
- 3 (30%) étaient en fonction dans le
département de pédiatrie.
- 1 (10%) était en fonction dans le département
de chirurgie.
- 1 (10%) était en fonction dans le département
de biologie clinique.
La figure 1 indique la répartition par
département de fonction des médecins ayant participé
à l'étude.
Figure 1 :
Répartition des médecins ayant participé à
l'étude par département de fonction

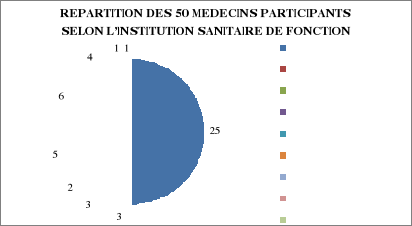
7-2-3 Répartition des médecins selon
l'institution sanitaire de fonction
Figure 2 :
Répartition des 50 médecins participants
selon l'institution sanitaire de fonction
7-3 Avis de médecins participants
7-3-1 Avis des médecins participants sur la
réalisation des RBPEH au Gabon
- 42 (84%) des médecins ayant participé à
l'étude ont pensé que la réalisation des RBPEH est
indispensable au Gabon
- 6 (12%) des médecins enquêtés ont
pensé que la réalisation des RBPEH est non indispensable au
Gabon
- 2 (4%) ne se sont pas prononcés
Le Tableau II indique la répartition des 50
médecins ayant rempli le questionnaire selon l'avis portant sur le
caractère indispensable ou non de la réalisation des RBPEH au
Gabon
Tableau II : avis
des 50 médecins participants ayant rempli le questionnaire selon l'avis
portant sur le caractère indispensable ou non de la
réalisation des RBPEH au Gabon
|
Caractère
|
Effectifs
|
Pourcentage
|
|
Indispensable
|
42
|
84%
|
|
Non indispensable
|
6
|
12%
|
|
Sans avis
|
2
|
4%
|
|
Total
|
50
|
100%
|
7-3-2 Avis des médecins participants sur la
perception des sujets expérimentaux comme ayant un intérêt
à tirer de la réalisation des RBPEH
- 37 (74%) des médecins ayant rempli le questionnaire
ont pensé que les sujets expérimentaux ont un
intérêt à tirer de la RBPEH.
7-3-3 Avis des médecins participants sur la
perception de l'éthique comme problème pouvant se poser lors de
la réalisation des RBPEH
- 35 (70%) des médecins participants ont pensé
que les problèmes éthiques peuvent se poser lors de la
réalisation des RBPEH
7-3-4 Avis des médecins participant sur l'existence
d'un comité d'éthique
- 50 (100%) des médecins ayant rempli et rendus le
questionnaire ont affirmé que leur institution sanitaire ne disposait
pas d'un comité d'éthique
7-3-5 Avis des médecins participants sur la
nécessité d'évaluer les RBPEH
- 47 (94%) des médecins ayant rempli et rendu le
questionnaire ont pensé qu'il est nécessaire d'évaluer les
RBPEH ; De ces 47 médecins, 8 soit 17,02 ont pensé que cette
évaluation devrait porter sur les seuls aspects scientifique et
éthique
Tableau III :
Répartition des médecins jugeant nécessaire
l'évaluation des RBPEH
|
Effectif
|
Pourcentage
|
|
Scientifique
|
8
|
17,02
|
|
Ethique
|
0
|
0,0
|
|
Scientifique et Ethique
|
8
|
17,02
|
|
Scientifique et éthique et P*
|
25
|
53,19%
|
|
Scientifique ou éthique et P*
|
4
|
8,5
|
|
Autre
|
2
|
4,25
|
|
Total
|
47
|
100%
|
P* : une au moins des propositions suivantes :
intérêt politique, intérêt économique,
conformité aux lois en vigueur
7-3-6 Protection de la confidentialité
- 9 médecins soit 90% des médecins
investigateurs ont déclaré prendre des mesures afin de
protéger la confidentialité des sujets expérimentaux.
7-4 Profil des RBPEH menées par les
médecins investigateurs :
- Les 10 médecins investigateurs soit 100% ont
déclaré avoir le plus souvent menées leurs recherches au
Gabon dont 6 (60%) dans un milieu de soins de santé et 4 (40%) au sein
d'une communauté.
- 4 soit 40% des médecins investigateurs ont
déclaré avoir dirigées des recherches dont le but
était de comprendre le mécanisme d'une maladie
Tableau IV :
Répartition des médecins investigateurs selon le but
assigné aux recherches
|
Effectifs
|
Pourcentage
|
|
Tester un programme de soins de santé
|
1
|
10%
|
|
Tester un médicament
|
4
|
40%
|
|
Comprendre la cause d'une maladie
|
1
|
10%
|
|
Comprendre le mécanisme d'une maladie
|
4
|
40%
|
|
Total
|
10
|
100%
|
7-4-1 Recherches parrainées de
l'extérieur
- 7 médecins investigateurs soit 70% ont
déclaré avoir dirigés des recherches qui étaient
parrainées de l'extérieur.
7-5 Attitude par rapport à la conception des
recherches
7-5-1 Prise en compte des considérations
éthiques
- 7 médecins investigateurs soit 70% ont
déclaré avoir le plus souvent pris en compte des
considérations éthiques dans la conception de leurs
recherches.
7-5-2 Prise en compte des particularités et
implication des communautés expérimentales.
- 8 médecins investigateurs (80%) ont
déclaré n'avoir pas le plus souvent pris en compte des
particularités (sociales, culturelles, politiques ou religieuses) des
communautés expérimentales dans la conception de leurs
recherches.
- 9 médecins investigateurs (90%) ont
déclaré n'avoir pas le plus souvent impliqué les
communautés expérimentales dans la conception de leurs
recherches.
7-5-3 Prévision d'une couverture d'assurance
- 10 médecins investigateurs (100%) ont
déclaré n'avoir pas le plus souvent prévu une couverture
d'assurance dans la conception de leurs recherches.
7-5-4 Evaluation des bénéfices et des
risques
- Aucun médecin investigateur ne soit 0% a
déclaré avoir réalisé dans la conception de ses
recherches une évaluation des bénéfices et risques
à la fois pour l'expérimentateur, les sujets expérimentaux
et leur communauté de provenance
Tableau V :
Répartition des 10 médecins investigateurs selon
l'attitude la plus souvent adoptée par rapport à
l'évaluation des bénéfices et des risques.
|
Pour l'expérimentateur
N%
|
Pour le sujet expérimental
N%
|
Pour la communauté
N%
|
|
Réalisation
|
9 (90%)
|
9 (90%)
|
8 (80%)
|
|
Non réalisation
|
1 (10%)
|
1(10%)
|
2 (20%)
|
|
Total
|
10 (100%)
|
10 (100%)
|
10 (10%)
|
7-5-5 Inclusion des personnes vulnérables comme des
personnes légalement inaptes ou en situation d'urgence
- 3 médecins investigateurs (30%) ont
déclaré avoir le plus souvent prévu d'inclure des
personnes vulnérables dans leurs recherches parce que les troubles sur
lesquels portaient ces études n'existaient que chez les personnes
vulnérables
- 7 médecins investigateurs (70%) ont
déclaré n'avoir pas le plus souvent prévu d'inclure des
personnes vulnérables dans leurs recherches.
7- 6 Attitude par rapport aux démarches
7-6-1 Soumission des recherches pour évaluation
à un comité d'éthique de la recherche
- (70%) médecins investigateurs ont affirmé que
les recherches qu'ils ont dirigées ont été soumises pour
évaluation à un comité d'éthique de la
recherche.
7-6-2 Recherches ayant fait l'objet de modifications
après avis rendu sur leur caractère éthique
- 1 (14,2%) médecin investigateur a
déclaré avoir dirigé des recherches qui ont fait l'objet
de modifications après avis rendu sur leur caractère
éthique
7-6-3 Validation de la mise en oeuvre des recherches
parrainées de l'extérieur par un comité d'éthique
du pays de provenance du parrainage
- (100%) des médecins investigateurs ayant
dirigés les recherches parrainées de l'extérieur ont
affirmé que les mises en oeuvre de ces recherches ont été
le plus souvent validées par un comité d'éthique du pays
de provenance du parrainage.
- (100%) des médecins investigateurs ayant
dirigés les recherches parrainées de l'extérieur dont les
mises en oeuvre ont été le plus souvent validées par un
comité d'éthique du pays de provenance du parrainage n'ont pas le
plus souvent soumis localement ses recherches à une évaluation
éthique.
7-7 Attitude par rapport à la
pré-réalisation : L'obtention du consentement
7-7-1 Information des participants à la
recherche
Tableau VI :
Répartition des médecins investigateurs en fonction de
l'explication intelligible et compréhensible fournie aux sujets
pressentis pour participer à l'étude :
|
Fourniture de l'explication n(%)
|
Non fourniture de l'explication n (%)
|
Total n(%)
|
|
Nature et objet de la recherche
|
10 (100%)
|
0 (100%)
|
10 (100%)
|
|
La méthodologie
|
10 (100%)
|
0 (0%)
|
10 (100%)
|
|
Durée de participation des sujets pressentis
|
8 (80%)
|
2 (20%)
|
10 (100%)
|
|
Bénéfices attendus pour le sujet ou pour d'autres
personnes
|
10 (10%)
|
0 (0%)
|
10 (100%)
|
|
Risques encourus
|
6 (60%)
|
4 (40%)
|
10 (100%)
|
|
Confidentialité des données de l'étude
|
3 (30%)
|
7 (70%)
|
10 (100%)
|
|
Remboursement des frais liés à l'étude
|
2 (20%)
|
8 (80%)
|
10 (100%)
|
|
Possibilité de se retirer librement du projet à
n'importe quel stade de ce dernier
|
3 (30%)
|
7 (70%)
|
10 (100%)
|
|
Responsabilité assumée par le chercheur
|
2 (20%)
|
8 (80%)
|
10 (100%)
|
7-7-2 Avis sur la personne chargée de recueillir le
consentement
- (70%) des 10 médecins investigateurs ont affirmé
que le consentement avait été recueilli par les
médecins.
- (20%) ont affirmé avoir eu recours au service des
interprètes pour recueillir le consentement
- 1 (10%) médecin investigateur a affirmé avoir eu
recours à un médiateur pour le recueil du consentement
7-7-3 Avis sur le temps de réflexion
- Tous les 10 médecins investigateurs ont
affirmé que le sujet pressenti disposait d'un temps de réflexion
avant de faire connaître sa décision :
Tableau VII :
Répartition des médecins investigateurs en fonction du
temps de réflexion accordée au sujet expérimental afin de
faire connaître sa décision
|
Temps
|
Effectifs
|
Pourcentage
|
|
15mn-30 mn
|
6
|
60%
|
|
30mn-1 heures
|
3
|
30%
|
|
1heure- 12 heures
|
1
|
10%
|
7-7-4 Mode d'expression du consentement
Tableau VIII :
Répartition des 10 médecins investigateurs selon le mode
d'expression du consentement
|
Effectifs
|
Pourcentage
|
|
Ecrit
|
3
|
(30%)
|
|
Oral
|
7
|
(70%)
|
|
Gestes
|
0
|
(0%)
|
|
Total
|
10
|
100%
|
- Tous les 7 médecins ayant recueilli le consentement oral
des sujets ont déclaré que ces derniers ne pouvaient pas le faire
de manière écrite car ils ne savaient ni lire, ni
écrire.
- Aucun de ces 7 médecins ne précise les
modalités de recueil du consentement
7-7-5 Caractère volontaire du consentement
- 7 médecins investigateurs (70%) ont affirmé
que le sujet fait son choix de participer à la recherche librement.
7-7-6 Implication de la communauté
d'appartenance
- Tous les 10 médecins investigateurs ont
affirmé que leurs recherches n'impliquaient pas l'accord de la
communauté
7-7-7 Obtention du consentement des personnes ne pouvant
consentir par elles-mêmes
- 3 médecins investigateurs soit 30% ont
affirmé que leurs recherches incluaient des mineurs de - de 18ans.
- aucun médecin investigateur n'a affirmé avoir
inclus dans leurs recherches des majeurs dont l'inaptitude a été
constatée judiciairement
Tableau IX :
Répartition des 3 médecins investigateurs ayant obtenu
l'accord des parents ou des représentants légaux des mineurs
pressentis pour prendre part aux recherches.
|
Effectifs
|
Pourcentage
|
|
Accords des parents
|
2
|
66 ,6%
|
|
Accords des représentants légaux
|
1
|
33,3%
|
|
Total
|
3
|
100%
|
7-7-8 Documentation du consentement
- Des 3 médecins investigateurs recueillant le
consentement de manière écrite seuls 2 soit 66,6% remettent un
exemplaire au sujet.
- Les 3 médecins investigateurs recueillant le
consentement de manière écrite soit 100% ont affirmé
conserver un exemplaire du formulaire de consentement.
7-8 Attitude par rapport à la
réalisation pratique
7-8-1 Information des participants en cas
d'expériences adverses
- 5 médecins investigateurs soit médecins
investigateurs (50%) ont déclaré avoir le plus souvent
informé les participants en cas d'expériences adverses
7-8-2 Exercice de représailles sur les auteurs de
dénonciations d'inconduites scientifiques
- 0 médecin investigateur (0%) a déclaré
que ses recherches ont le plus souvent fait l'objet d'une dénonciation
pour inconduite scientifique
7-9 Attitude par rapport au suivi et à la fin
des travaux de recherche
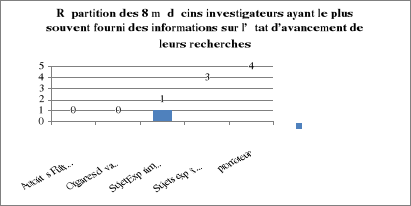
7-9-1 Fourniture des informations sur l'état des
recherches
- 8 médecins investigateurs soit 80% ont affirmé
avoir fourni des informations sur l'état d'avancement de leurs
recherches.
La figure 3 : indique la
répartition des 8 médecins ayant le plus souvent fourni des
informations sur l'état d'avancement de leurs recherches et les
destinataires de ces informations.
7-9-2 Communication des résultats
Tableau X :
Répartition des médecins investigateurs en fonction de
l'attitude adoptée pour la communication des résultats de leurs
recherches et les destinataires
|
Communication n (%)
|
Non communication
n (%)
|
Total
n (%)
|
|
Autorités publiques
|
2 (20%)
|
8 (80%)
|
10 (100%)
|
|
Promoteurs
|
7 (70%)
|
3 (30%)
|
10 (100%)
|
|
Organes d'évaluation scientifique et éthique
|
7 (70%)
|
3 (30%)
|
10 (100%)
|
|
Sujet expérimental
|
3 (30%)
|
7 (70%)
|
10 (100%)
|
7-9-3 Publication des résultats
- 8 médecins investigateurs ont déclaré
publier les résultats de leurs recherches à la communauté
scientifique et au public.
- 8 médecins soit 100% ont déclaré avoir
publié à la communauté scientifique et au public tous
leurs résultats (faux ou positifs).
8- ANALYSE ET COMMENTAIRES
8-1 Matériel et méthode
8-1-1 Limites de l'étude
La restriction du cadre d'étude à certains
hôpitaux des villes de Libreville et de Port-Gentil a sans doute
constitué des limites à la pertinence de notre travail.
En effet les données que nous aurions pu obtenir en
ayant étendue cette étude aux médecins des autres
structures sanitaires publiques ou privées de la ville de Libreville
telles que l'hôpital d'instruction des armées, l'hôpital
pédiatrique Owendo, l'hôpital de Melen et au centre de recherche
médicale de Franceville nous auraient certainement permis d'aboutir
à des résultats mieux représentatifs et plus aisés
à extrapoler à l'échelle nationale.
Dix années, période sur laquelle devait
remonter les informations à fournir par les médecins
investigateurs a pu du fait d'un biais de mémoire constituer une limite
à la fiabilité de nos résultats.
L'absence dans notre démarche d'éléments
objectifs de vérification des informations fournis par les
médecins investigateurs à contribuer à limiter la
fiabilité de notre étude.
8-1-2 Eléments de validité de
l'étude
- le Centre hospitalier de Libreville faisant office de centre
hospitalo-universitaire, et étant de ce fait le centre par excellence de
prestations des soins médicaux, de formation et de recherches, la chance
que nous avions d'y rencontrer une bonne concentration non seulement des
médecins mais aussi des chercheurs étaient à priori
grande.
- La pratique du porte à porte a sans doute
réduit le potentiel risque de ne pas rencontrer les médecins
- Recueillir les informations concernant dix années en
vue d'évaluer le respect des principes éthiques par les
médecins investigateurs ont indiscutablement accru la chance
d'élargir l'échantillon de ces médecins et le nombre de
leur recherche à prendre en compte.
8-2 Cadre législatif et
réglementaire
La recherche biomédicale au Gabon est régie par
la loi 22-2000 qui détermine les principes fondamentaux de la
recherche. Cependant cette loi n'est pas mise en oeuvre aujourd'hui :
seule la création d'un comité d'éthique en matière
de recherche scientifique est effective, et ceci à la suite d'un
décret pris en conseil de ministre le 26 mars 2009.
Cependant la plupart des structures hospitalières ne
possèdent pas de comité d'éthique de la recherche
susceptible de servir comme organes de contrôle des projets de recherche
proposés et aussi de surveiller si les principes éthiques
incluant les exigences importantes de bonne pratique (clinique, de laboratoire,
scientifique) sont respectées et accomplies pendant la
réalisation de la recherche [31]
Sur le plan institutionnel on note l'existence [17] de deux
comités d'éthique :
- le comité d'éthique de l'hôpital Albert
Schweitzer basé à Lambaréné qui a été
crée en 1988, dont le fonctionnement est altéré par sa
composition : c'est un comité mixte sur le plan de des origines
géographiques : la présidente réside en Allemagne.
- le comité d'éthique pour la recherche
biomédicale basé à Franceville et qui a été
crée en 2002, son fonctionnement n'est pas suffisamment
décrit.
Le code de déontologie devant préciser les
dispositions réglementaires concernant l'exercice professionnel de la
médecine n'existe pas et ceci pose un problème important dans la
mesure ou la déontologie et l'éthique doivent être comme
partout deux comportements complémentaires dans la bonne pratique de
tous les chercheurs et de tous les médecins dont le souci prioritaire
doit rester la protection et le bénéfice du malade et/ou du
volontaire [32]
8-3 Résultats globaux
Le taux de participation à notre étude a
été supérieur à 50% ce qui peut laisser penser que
les médecins ont eu un engouement à participer à notre
travail.
Cependant la rareté des recherches biomédicales
dans la plupart des pays du sud s'est traduite dans notre étude par un
taux de 20% de médecins investigateurs obtenu sur les dix
dernières années soit environ 2 médecins investigateurs
sur 100 chaque année.
8-4 Profil professionnel de la population
étudiée
- La majorité des médecins enquêtés
(60%) ont affirmé n'être ni enseignants, ni chercheurs ;
cette majorité d'enquêtés dont l'activité principale
n'était pas à priori la recherche, et qui n'avaient pas une
connaissance des questions éthiques portant sur les RBPEH a certainement
contribué à amortir nos résultats quant à
l'évaluation du niveau de ces connaissances.
Néanmoins, la qualification de médecin
étant reconnue suffisante par les instruments internationaux encadrant
la recherche biomédicale (Déclaration d'Helsinki et les lignes
directrices du C.I.O.M.S) pour diriger et surveiller une RBPEH, les
résultats obtenus peuvent être considérés comme
fiables, ce qui corrobore d'ailleurs nos résultats quant à
l'échantillon des médecins investigateurs ; en effet, des 10
médecins investigateurs 5 (50%) ont déclaré n'être
ni enseignants ni chercheurs.
- La distribution des médecins enquêtés
selon le département de fonction (60% en exercice dans un
département de médecine et spécialités), ceci peut
s'expliquer par la grève des personnels de santé du secteur
public, par le choix de ne pas participer à l'étude que nous
avons noté d'un département à un autre.
- La répartition des médecins
enquêtés selon l'institution sanitaire de fonction 50% (CHL),
6%(Fondation Jeanne Ebori), 6%(Polyclinique El Rapha), 4%(Polyclinique
Chambrier), 10%(CHR Ntchengue), 12%(HPI), 8%(Clinique du littoral), 2%(Clinique
mandji), 2%(Clinique Ayile) correspond parfaitement à la population
cible.
8-5 Avis des médecins participants
Des quatre questions relatives aux principes d'éthique
sur lesquelles les 50 médecins participants devaient se prononcer aucune
n'a fait l'objet d'un avis conforme aux principes éthiques :
- La majorité des 50 médecins soient respectivement
(84%, 74%, 70%, 94%) ont donné un avis conforme aux principes
éthiques applicables aux RBPEH.
- Les 50 médecins (100%) ont affirmé que leur
structure hospitalière ne disposait pas d'un comité
d'éthique. Cet absence de comités d'éthique locaux nous
amène à penser comme Raymond J., et Long H. [39] que la
médecine dans ces formations hospitalières est sujette au mirage
thérapeutique c'est-à-dire à la croyance que tout ce qui
est offert par la médecine moderne ait été prouvé
bénéfique.
8-6 Profil global des RBPEH menées par les 10
médecins investigateurs
L'évaluation de la mise en application des principes
éthiques de la RBPEH s'est faite sur les recherches menées au
Gabon par tous des 10 médecins investigateurs (100%) aussi bien au sein
de communauté (cas de 40% des médecins) , qu'en milieu
hospitalier (cas de 60% des médecins)
Elles avaient pour but de comprendre le mécanisme d'une
maladie (cas de 40% des médecins), tester un médicament (cas de
40% des médecins).
La plupart de ces recherches étaient parrainées
de l'extérieur (cas de 70% des médecins investigateurs).
8-7 Attitude dans la conception des recherches
La majorité des médecins investigateurs (70%) a
déclaré avoir le plus souvent pris en compte les
considérations éthiques dans la conception de leurs recherches,
affirmation qui ne s'est pas traduite dans les résultats.
En effet les attitudes dans la conception des recherches ont
été de ne prendre en compte ni les particularités
sociales, culturelles, politiques ou religieuses (80% des médecins), ni
d'impliquer (cas de 90% des médecins) les communautés
expérimentales.
Concernant la prévision d'une couverture d'assurance, tous
les 10 médecins investigateurs ont affirmé n'avoir pas
prévu cette dernière lors de la conception de leurs recherches.
L'évaluation des bénéfices et des risques
à la fois pour l'expérimentateur, le sujet expérimental et
la communauté dont celui-ci est issu a fait défaut (0% de
médecins investigateurs).
L'attitude des médecins investigateurs est contraire
à celle préconisée par Laplante Bernard [33] qui en
analysant le déroulement de 3 projets de recherche montre comment les
décisions prises à tout moment comportent fréquemment une
dimension éthique et que seule une réflexion soutenue de la part
de l'auteur peut lui permettre d'adopter un comportement éthique dans
ses relations avec les participants.
De ces constats, il se dégage dans l'ensemble que la
conception de leurs recherches n'était pas conforme aux principes
éthiques contrairement à l'avis donné.
Ceci peut s'expliquer par la méconnaissance des principes
éthiques guidant la recherche biomédicale.
8-8 Attitude par rapport aux démarches
- 7 médecins investigateurs (70%) ont affirmé
avoir soumis les recherches qu'ils ont dirigées pour évaluation
à un comité d'éthique de la recherche.
- 100% des médecins investigateurs dont les recherches
ont étés parrainés de l'extérieur ont
affirmé que la mise en oeuvre de ces recherches avait été
parrainée par un comité d'éthique du pays de provenance du
parrainage.
- Toutes les recherches parrainées de
l'extérieur n'ont pas été soumises localement à une
évaluation éthique ; cette attitude peut s'expliquer par
l'absence d'un comité d'éthique pendant la période de leur
recherche et ceci rejoint l'affirmation de tous les enquêtés qui
ont déclaré que leur structure hospitalière ne disposait
pas de comité d'éthique.
Il est cependant intéressant de retenir comme
l'affirment Doumbo O.K., Djimbe A.A , Thera M.A. [32] que « la
qualité scientifique d'un protocole de recherche , le passage devant un
comité d'éthique indépendant et le consentement
éclairé du volontaire sont des obligations auxquels les pays en
voie de développement ne doivent pas se soustraire sous prétexte
qu'ils sont loin d'avoir les mêmes moyens que les pays du nord, car la
qualité de l'éthique médicale et sa mise en pratique dans
un pays quel qu'il soit est le meilleur reflet de la qualité du
fonctionnement et du dynamisme de sa recherche scientifique »
8-9 Attitude par rapport à la pré
réalisation
· L'information des sujets pressentis pour prendre part
aux recherches a guidé l'attitude de tous les investigateurs, cependant
elle a souffert d'une insuffisance quant il s'est agit de :
- informer les participants à la recherche sur la
possibilité de se retirer librement du projet à n'importe quel
moment de ce dernier, seul 30% des médecins investigateurs a
affirmé avoir informé les sujets pressentis de cette
possibilité.
- informer les participants sur la responsabilité
assumée par le chercheur, seul 20% des médecins investigateurs a
affirmé l'avoir fait.
- De préciser avec quoi ils recueillaient ce
consentement ; ainsi la façon dont le consentement des volontaires
est obtenu peut être sujette à caution [34]
· Pour 70% des médecins investigateurs, le
médecin était chargé du recueil du consentement.10% des
investigateurs ont affirmé avoir eu recours au service d'un
médiateur pour recueillir le consentement.
· Pour la plupart des investigateurs (70%) le mode
d'expression du consentement était oral.
· 30% des médecins investigateurs ont
affirmé que leurs recherches incluaient des mineurs de - de 18 ans et
de ces 3 médecins 2(66,6%) ont affirmé avoir reçu l'accord
des parents et 1 (33,3%) a affirmé avoir reçu l'accord d'un
représentant légal de mineur.
· La majorité des médecins investigateurs
ont affirmé que les sujets pressentis faisaient librement leur choix de
participer aux recherches
· Tous les médecins investigateurs ont
affirmé que leurs recherches n'impliquaient pas l'accord de la
communauté.
· Tous les médecins investigateurs ont
affirmé accorder un délai de réflexion au sujet pressenti
pour prendre part aux recherches afin de faire connaître sa
décision ; ce délai est en moyenne de 1heure et
6minutes ; la plupart des médecins investigateurs accorde 0,375
heure de réflexion au sujet expérimental avec un écart-
type de 1,48
Cette relative amélioration du respect des principes
éthiques peut s'expliquer par le caractère répandu de la
notion du consentement dans le domaine médical : le Serment
d'Hippocrate [5]
Qui fixe un cadre éthique à l'intervention du
médecin en fait mention.
8-10 Attitude par rapport à la
réalisation pratique
Les médecins investigateurs ont observé le principe
éthique consistant à tenir informé les sujets
expérimentaux des cas d'expériences adverses.
Cependant, l'implication d'un comité d'éthique
susceptible de mettre en oeuvre des mécanismes d'examen et de
surveillance [35] des RBPEH devrait permettre de mieux garantir le respect de
ce principe de la part des médecins investigateurs.
8-11 Attitude par rapport au suivi et à la fin
des travaux de recherche.
L'information des sujets expérimentaux sur
l'état d'avancement de la recherche et les modalités pratique de
celles-ci n'a pas été le plus souvent observée. De
même la majorité des investigateurs (70%) a été en
marge du principe éthique de communiquer les résultats de leurs
recherches aux sujets expérimentaux.
8-12 Publication des résultats
· Le principe éthique qui recommande la
publication de tous les résultats positifs ou négatifs a
été respecté par les 8 médecins investigateurs qui
ont affirmé publier les résultats de leur recherche à la
communauté scientifique et au public.
Ce constat signifie une tendance de ratio 1, précisons
que la tendance de publication est la tendance des investigateurs, des
éditeurs à favoriser la publication des recherches avec des
résultats positifs sur les résultats négatifs. Ce constat
est cependant contraire à ceux faits par Easter Brook et al. [29]
et Dickersin [30] qui ont trouvé des tendances de publication en faveur
des résultats positifs compris entre 2,32 et 2, 93.
La nature de ce résultat peut s'expliquer par l'absence
d'un comité local d'éthique chargé de la validation et du
suivi de ces recherches.
9- RECOMMANDATIONS
Cette étude menée au Gabon sur une
période de 4 mois nous a permis de faire le point sur le respect des
principes fondamentaux d'éthique lors de la réalisation des
RBPEH.
Elle a ainsi permis de constater :
- Qu'il n'existe pas de dispositif national d'éthique
de la recherche biomédicale
- Que très peu d'acteurs de la recherche
biomédicale sont formés en éthique
Pour cela nous recommandons :
· L'amélioration du cadre législatif et
réglementaire sur la recherche biomédicale.
· L'adoption d'un code de déontologie
médicale.
· L'adoption d'une Politique nationale d'éthique
[36] qui précisera :
o Le calendrier de réunion du comité national
d'éthique.
o La documentation requise à joindre à une
demande d'approbation éthique.
o Les méthodes d'évaluation des dossiers.
o Les critères qui devront être examinés
par le comité d'éthique.
o Les délais nécessaires pour
l'évaluation des dossiers.
o L'implication du comité d'éthique dans
l'évaluation éthique du déroulement des activités
de recherche.
o La délivrance d'un certificat d'approbation
éthique à tout chercheur donc le projet aura été
validé et en fixera la date de validité et les conditions de
renouvellement
· La création d'un organe chargé de la
validation scientifique des protocoles de recherches.
· La création des comités d'éthiques
institutionnelles et régionales [28] capable
de procéder :
- A l'évaluation préalable des protocoles de
recherche
- Au suivi des recherches, à la mise en oeuvre
- A l'établissement dans certains des cas des
références et des directives.
· L'organisation des formations continues en
bioéthique pour les médecins en exercice.
· L'introduction de l'enseignement de la
bioéthique dans le programme de formation des médecins.
· Encourager les échanges entre les chercheurs et
une plus grande mobilité des résultats des recherches.
· La mise en application de La résolution
AHG/Rés.254 XXXII sur la bioéthique [15] adoptée en 1996
par la conférence des chefs d'états et de gouvernement de
l'organisation de l'unité africaine (actuellement union africaine) lors
de sa 32ème session ordinaire (Yaoundé, Cameroun, 8-10
juillet 1996).
· L'intensification des échanges avec les
organismes chargées de veiller au respect des principes fondamentaux
d'éthique lors de la réalisation des recherches
biomédicales portant sur les êtres humains , nous citerons le
P.A.B.I.N [16] crée en 2001 et chargée de la promotion de la
bioéthique en Afrique.
10- CONCLUSION
A l'issue de ce travail nous retenons que :
· La loi n°22/2000 déterminant les principes
fondamentaux de la recherche scientifique en république gabonaise
n'aborde pas à fond la recherche biomédicale impliquant les
sujets humains, cette loi pour l'essentiel ne décrit que les
différentes institutions de recherche et leur mode de financement. Ce
constat a également été dressé lors de
l'enquête menée dans le cadre du projet NEBRA [17]
· Il n'existe pas de dispositif national d'éthique
de la recherche biomédicale comme l'affirme le Professeur Ngou- Milama
[37]
· Sur le plan réglementaire il n'existe pas un
code de déontologie médicale au Gabon
· Les acteurs de la recherche biomédicale sont
majoritairement constitués des médecins qui ne sont ni
chercheurs, ni enseignants, c'est-à-dire qui n'ont pas à priori
la recherche comme activité principale.
· Les structures hospitalières ne disposent pas en
leur sein des comités d'éthiques de la recherche.
· Il n'existe pas un organe de validation scientifique
des protocoles de recherche.
· Les sujets pressentis pour participer à la
recherche ne sont pas informés des responsabilités des promoteurs
dans la majorité des cas
· Les recherches parrainées de l'extérieur
et ayant été soumises pour évaluation à un
comité d'éthique de la recherche du pays de provenance de la
promotion n'ont pas étés dans la totalité des cas soumis
localement à une évaluation par un comité éthique
de la recherche.
· De la conception à la publication des
résultats des RBPEH les principes éthiques ne sont pas
respectés par la grande majorité des médecins
investigateurs.
11- REFERENCES BIBLIOGRAPHIQUES
1- Constitution du Gabon du 26 mars 1991, modifiée par
les lois du 18 mars 1994, du 29 septembre 1995, du 25 avril 1997 et du 11
octobre 2000.
2- La loi 22-2000 déterminant les principes
fondamentaux de la recherche en république Gabonaise (J.O juin 2001
n°6)
3- La loi de protection de la personne se prêtant
à des recherches biomédicales dite Huriet- Serusclat (JO du
20-12-88 République française)
http : // www.legifrance.gouv-fr, consulté
le 13 janvier 2009
4- Décret du 26 mars 2009 fixant les attributions,
l'organisation et le fonctionnement du comité d'éthique pour les
sciences de la vie et de la santé (CEVS) (journal l'union du 27 mars
2009 page 2)
5- Serment d'Hippocrate
http://infodoc.inserm.fr/ethique/Ethique.nsf, consulté le 11
février 2009
6- Le Code de Nuremberg (1947)
http://infodoc.inserm.fr/ethique/Ethique.nsf,
consulté le 10 Janvier 2009
7- Déclaration universelle des droits de l'homme
(1948)
http://www.un.org/fr/documents/udhr
, consulté le 25 janvier 2009
8- Les déclarations internationales de l'Association
Médicale Mondiale :
- le code international d'éthique médicale
(1949)
- Déclaration d'Helsinki (1964)
http://www.wma.net/f/policy/pdf/17a.pdf,
consulté le 11 janvier 2009
http://infodoc.inserm.fr/ethique/Ethique.nsf, consulté le 11
janvier 2009
9- Pacte international relatif au droit civil et politique
http://www2.ohchr.org/French/law/ccpr.htm,
consulté le 25 janvier 2009
10- Le Rapport Belmont (1976) Traduction française dans
médecine et expérimentation, 1982. Les cahiers de
bioéthique n° 4, Québec, presses de l'université de
Laval (the US. National commission for the protection of human subjects of
biomedical and behavioral research et aussi sur :
http://www.fhi.org/training/fr/Rete/pdf_files/frenchBelmont.pdf,
consulté le 12 janvier 2009.
11- Les recommandations du C.I.O.M.S en collaboration avec
l'OMS et l'UNESCO, Directives internationales pour la recherche
biomédicale sur les sujets humains. 1982-1982-1993.
http://www.cioms.ch/frame_french-text.htm, consulté le 13 janvier
2009
12- Déclaration universelle sur la bioéthique et
les droits de l'homme de l'UNESCO (2005)
http://www.porta.uneco.org, consulté le
23 avril 2009
13- Charte africaine des droits de l'homme et des peuples
(1981)
www.aidh.org/Biblio/Txt_Afr/instr-81.htm
14- La convention sur les droits de l'homme et la
biomédecine du conseil de l'Europe (1997) dont l'article 5 fait
référence au consentement éclairé et l'article 6
à la protection des personnes n'ayant pas la capacité de
consentir
www.droitshumains.org/Europe/oocons_dates.htm
, consulté le 23 avril 2009
15- Résolution AHG/Rés. 254 XXX II sur la
bioéthique adoptée en 1996 par la conférence des chefs
d'état et de gouvernement de l'organisation de l'unité africaine
(actuellement union africaine) lors de sa 32ème session
ordinaire (Yaoundé, Cameroun, 8-10 juillet 1996.
16- Compte rendu des conférences de 2002 et 2003 du PABIN
sur les bonnes pratiques en recherche en santé en Afrique
http://www.who.int/sidcer/fora/en/pabin3rd.pdf,
consulté le 04 février 2009
17- Rapport NEBRA (2006) annexe 6 ; Loi 22/2000 du Gabon
portant code d'éthique pour la recherche en santé.
18- Mémoire explicatif sur l'élaboration d'une
déclaration relative à des normes universelles en matière
de bioéthique. Paris, le 10 janvier 2005
19- Wikipédia :
http://fr.wikipédia.org,
consulté le 5 janvier 2009
20- Potter VR What does bioethics mean? The AG Bioethics
Forum. 1998; 8-3
21- Recherche biomédicale : aspects
éthiques et légaux
http://www.recherchebiomedicaleaspectsethiquesetlegaux.htm
22- Le procès de Nuremberg. Y. Tenon
23- Actes du 1er « Séminaire
International sur l'éthique de la recherche (OMS /Afro du 22 au 24
juin 2004)
http://www.ccdc.ird.fr/pdf/oms_afro22062004.pdf
, consulté le 13 avril 2009
24-Mazabalo Aleza : L'éthique de la recherche
biomédicale en Afrique : approche normative.
Master II de
« Droit-santé-éthique »
www.refer.sn/rds/IMG/pdf/ALEZAMAZABALO.pdf,
consulté le 23 février 2009
25- Spécificités du Gabon
http://www.diplomatie.gouv.fr,
consulté le 25 février 2009
26- Conseil national de l'ordre des médecins du
Gabon
http://cnom.gabon.chez.alice.fr/CNOM,
consulté le 10 mai 2009
27- Roy J. Conditions d'exercice Professionnel de la
médecine légale au Gabon. Faculté de médecine,
de pharmacie et d'odontostomatologie Dakar, Mémoire Med 2007, 64p.
2009
28- Bouësseau M.C Nouveaux défis pour les
comités d'éthique de la recherche en Afrique.
1ères journées de
bioéthique pou l'Afrique de l'Ouest et du Centre : Quelle
éthique pour la recherche en Afrique ?
Dakar, 11-13 juillet
2005
29- Easter Brook PJ, Berlin JA, Gopalan R, Matthews DR.
Pubication bias in clinical research.lancet 1991;337: 867-72
30- Dickersin K. the existence of publication bias and
risk factors for its occurrence.JAMA. 1990, 263: 1385-89
31- Glasa J., Holoman J., Klepanec J., Soltes L. Ethics
Committees and achievement of good clinical practice dans Therapie.
[Thérapie.] 1996, vol.51, n°4, pp. 369-372
32- Doumbo O. K., Djimde A.A, Thera M.A. le
développement de vaccins antipaludiques et la nécessité
des essais cliniques conformes aux normes internationales en Afrique
Dans : Bulletin de la Société de pathologie
exotique. [Bull. Soc. patho. Exo...] 2008, vol.101, n°3, pp.249-253
33- Laplante Bernard, Cheminement éthique d'un
chercheur engagé en recherche collaboratrice : Médiation
entre recherche et pratique en éducation
Dans : Revue des sciences de l'éducation. [Rev.
Sci. Educ. ] 2005, vol. 31, n°2, pp.417-440
34- Bereterbide F. , Hirsch F. Essais cliniques dans
les pays en développement : qui doit « dire »
l'éthique ?
Dans : Bulletin de la Société de
pathologie exotique. [Bull.Soc.pathol.exo...] 2008, vol.101, n° 2, pp.
102-105
35- Bortolussi Robert, Nicholson Diann, Auditing of clinical
research ethics in a children's and women's academic hospital
Dans: Clinical and investigative medicine. [Clin. Invest.
Med...] 2002, vol. 25, n° 2, pp. 83- 88
36- Politique d'éthique de la recherché
biomédicale
http://www.ethiquedelarechercheaveclesêtreshumains.htm,
consulté le 24 mai 2009
37- Ngou- Milama E., Lindoye E., Nguele JC, Lemamy GJ,
Ovono F, Liamdia et al.
Obligation Ethique dans le schéma
organisationnel de la recherche : cas du Gabon
Dans : Objectifs de développement du
millénaire et avancement de la bioéthique
En Afrique.2006 ; 81 : 180.
38- Levine, R.J. The Nuremberg code. Ethics and regulation of
clinical research, 2ème ed, 1986, p.425-6
39- Raymond J., Long H. Science et éthique,
méprise et mirage thérapeutiques
Dans : Journal of neuroradiology. [J.
neuroradiol.] 2008, vol.35, n°5, pp.268-272
SUPPORTS DE COURS
40- « Quel consentement dans les Pays en voie
de développement ? »
41- Support de cours de l'université de
Reims : « La Bioéthique et critiques de la
Déclaration d'Helsinki » 2005
42- L'Evaluation Ethique de la Recherche
Biomédicale
Exemple du comité d'éthique de la
recherche de l'hôpital Sainte-Justine
Cours de J-M Thérien et G. Cardenal
43- Familly Heath international,
Cours de formation sur l'éthique de la
recherche
12- ANNEXES
QUESTIONNAIRE
I- IDENTIFICATION
1
INITIALES :.................................................................................
2 STATUT :
Médecin........................................................................
Médecin-chercheur............................................................
Médecin
-enseignant...........................................................
3
SPECIALITE :........................................................................
4 DEPARTEMENT
:......................................................
5 ANCIENNETE DANS LA
FONCTION ................................................
II- AVIS DES MEDECINS PARTICIPANTS
(Cochez la bonne réponse)
1- La réalisation des recherches biomédicales
portant sur les êtres humains au Gabon est-elle :
O Indispensable
O Non indispensable
O Sans avis
2- Selon vous est ce que les sujets expérimentaux ont un
intérêt à tirer de la réalisation des
RBPEH :
O Oui
O Non
RBPEH°= recherche biomédicale portant sur les
être humains
3- Les problèmes éthiques peuvent-ils se poser lors
de la réalisation des RBPEH°
O Oui Si oui
lesquels.......................................................................
O Non
4- Existe-il un comité d'éthique pour la recherche
au sein de votre formation hospitalière (donnez le nom de votre
structure hospitalière)...................
O Oui
O Non
Si oui quel est sa composition ?
.............................................................
.............................................................
...............................................................
..............................................................
............................................................
.............................................................
5- Selon vous est-il nécessaire d'évaluer les
RBPEH sur le plan :
O Scientifique
O Scientifique et Ethique
O Scientifique, Ethique et P°
O Scientifique ou Ethique et P°
O Autre
- P° := une au moins des propositions suivantes :
intérêt politique, intérêt économique,
conformité aux lois en vigueur
6- Avez-vous été une fois investigateur° ces
dix dernières années (1998-2008) :
O Oui
O Non
Investigateur ° = l'investigateur est toujours une personne
physique, docteur en médecine qui dirige et surveille la
réalisation de la recherche
Si oui répondez aux questions suivantes :
7- Avez-vous réalisé des recherches au Gabon ces
dernières années (1998-2008) :
O Dans un milieu de soins
O Au sein d'une communauté
8- Quel était le but assigné à vos
recherches :
O Tester un programme de soins de santé
O Tester un médicament
O Comprendre la cause d'une maladie
O Comprendre le mécanisme d'une maladie
9- Parmi les recherches que vous avez dirigées certaines
étaient-elles parrainées par l'extérieur :
O Oui
O Non
III- ATTITUDE PAR RAPPORT A LA CONCEPTION DES RECHERCHES
1- Avez-vous pris en compte les considérations
éthiques dans la conception de vos recherches ? :
O Oui
O Non
2- Les particularités (sociales, culturelles, politiques
ou religieuses) des communautés expérimentales ont-elles
étaient prises en compte dans les recherches que vous avez
dirigé ? :
O Oui
O Non
3- Les communautés expérimentales ont-elles
été impliquées dans vos recherches ?
O Oui
O Non
4- Avez- vous le plus souvent prévu une couverture
d'assurance dans la conception de vos recherches :
O Oui
O Non
5- Durant la conception de vos recherches évaluez- vous
les bénéfices et risques à la fois pour
l'expérimentateur, les sujets expérimentaux et leur
communauté de provenance :
O Oui
O Non
6- Prenez-vous dans la conception de vos recherches des mesures
pour protéger la confidentialité des sujets
expérimentaux :
O Oui
O Non
7- La recherche s'est-elle faite auprès des personnes
vulnérables comme des personnes légalement inaptes ou en
situation d'urgence médicale :
O Oui
O Non
IV- ATTITUDE PAR RAPPORT AUX DEMARCHES
1- Les recherches que vous avez dirigées ont-elles
été soumises pour évaluation à un comité
d'éthique de la recherche ?
O Oui
O Non
Si oui à quel comité d'éthique a
été soumis ces recherches pour validation :
O Comité d'éthique du pays de provenance
du parrainage
O Comité d'éthique national
O Comité d'éthique du pays de provenance
et Comité national d'éthique
2- Avez- vous dirigé des recherches qui ont fait l'objet
de modifications après avis rendu sur leur caractère
éthique :
O Oui
O Non
V- ATTITUDE PAR RAPPORT A LA PRE-REALISATION
1- Modalités de recrutement des participants
à la recherche (cocher la bonne réponse)
Les sujets pressentis pour prendre part à vos
recherches sont recrutés par :
O Annonce publicitaire
O Référence par des cliniques ou des
résidences
2- Le sujet pressenti pour participer à vos
recherches est-il informé de (répondre par oui ou
non dans la case correspondante)
|
OUI
|
NON
|
|
La nature et l'objet de la recherche envisagée
|
|
|
|
La méthodologie
|
|
|
|
La durée
|
|
|
|
Les bénéfices attendus pour lui ou pour d'autres
personnes
|
|
|
|
Les risques encourus
|
|
|
|
La confidentialité des données de l'étude et
qui aura connaissance de son identité
|
|
|
|
Le remboursement de ses frais liés à
l'étude
|
|
|
|
La possibilité de se retirer librement du projet à
n'importe quel stade de ce dernier
|
|
|
|
La responsabilité assumée par le chercheur
|
|
|
3- Conditions de recueil du consentement (cocher
la bonne réponse)
Quelle est la personne chargée de l'obtention du
consentement
O Le médecin/ chercheur
O L'infirmier ou l'infirmière
O L'interprète
O ° Médiateur
O Autres (préciser)
° Médiateur= personne appelé pour analyser les
informations fournies au patient ou au participant potentiel et rendre le
consentement plus compréhensible
4- Temps de réflexion (cocher la bonne
réponse)
Le patient dispose t-il d'un temps de réflexion avant de
faire connaître sa décision ?
O Oui
O Non
Si oui précisez le temps minimum
5- Mode d'expression du consentement (cocher la
bonne réponse)
Lors de vos recherches quel est le mode d'expression du
consentement :
O Ecrit
O Oral
O Gestes
En cas de consentement verbal justifiez les motifs pour lesquels
le consentement des participants ne peut être donné par
écrit et précisez les modalités selon lesquelles leur
consentement sera recueilli (enregistrement audio, vidéo, processus
électronique.)
6- Caractère volontaire du
consentement
Le sujet fait-il son choix de participer à la recherche
librement sans aucune forme de pressions indues
O Oui
O Non
7- Implication de la communauté
d'appartenance
La recherche implique tel l'accord de la communauté
d'appartenance ?
O Oui
O Non
Dans l'affirmative précisez comment vous entendez
procéder pour obtenir cet accord :
......................................................................................................
.......................................................................................................
......................................................................................................
8-Obtention du consentement des personnes ne pouvant
consentir par elles-mêmes :
Vos recherches incluent - elles :
- Des mineurs (- de 18 ans)
O Oui
O Non
- Des majeurs dont l'inaptitude a été
constatée judiciairement (majeurs sous tutelle, curatelle dont le mandat
d'inaptitude a été homologué)
O Oui
O Non
Dans l'affirmatif comment obtenez- vous leur
consentement..........................
...................................................................................................
.....................................................................................................
....................................................................................................
9- Documentation du consentement
Dans le cas ou le sujet vous donne son consentement par
écrit, lui remettez-vous un exemplaire du formulaire de consentement
O Oui
O Non
Si non ou sont conservés les formulaires de
consentement
.....................................................................
.......................................................................
.........................
V- ATTITUDE PAR RAPPORT A LA REALISATION PRATIQUE
1- Les participants à ses recherches sont-ils
informés en cas d'expériences adverses :
O Oui
O Non
2- Les auteurs de dénonciations d'inconduites
scientifiques ont-ils été victimes de
représailles :
O Oui
O Non
VI- ATTITUDE PAR RAPPORT AU SUIVI ET A LA FIN DES TRAVAUX DE
RECHERCHE
1- Fournissez-vous les informations sur l'état
d'avancement de vos recherches ?
O Oui
O Non
SI OUI A QUI ?
: O Autorités publiques
O Promoteur
O Organes d'évaluation scientifique ou
éthique
2- Communiquez- vous les résultats de vos
recherches ?
O Oui
O Non
SI OUI A QUI ?
O Autorités publiques
O Promoteur
O Organes d'évaluation scientifique ou éthique
O Sujet expérimental
3- Publiez- vous les résultats de vos
recherches ?
O OUI
O Non
SI OUI A QUI ?
O Public
O Communauté scientifique
O Public et communauté scientifique



