|
|
|
|
UNIVERSITE DE OUAGADOUGOU
Unité de Formation et de Recherche
en Science de la Vie et de la Terre (U.F.R/S.V.T)
|
****************
Département de Biochimie-Microbiologie
(DBM)
****************
CRSBAN
MEMOIRE
Présenté
Par
SAWADOGO Aïssama
Pour l'obtention
du
Diplôme de Licence Professionnelle
Option : Management de la Qualité en Industrie
Agroalimentaire
sur le thème :

DE KOSSODO DANS LE TRAITEMENT PHYSICOCHIMIQUE DE
L'EAU
ÉVALUATION DE LA PERFORMANCE DE LA STATION
D'ÉPURATION
Soutenu le 08 Mai 2014 devant le jury :
Président du jury: Dr Aly SAVADOGO, Maître
de Conférences, Université de Ouagadougou
Membres du jury : Dr Cheikna ZONGO, Maître
Assistant, Université de Ouagadougou
Dr Marius K. SOMDA, Assistant, Université de
Ouagadougou
Mr Francis D. KERE, Chef du Service Qualité Eau,
ONEA/OUAGA
DÉDICACE
A
Mon père SAWADOGO Halidou
A
Ma mère BOENA Salamata
A
Toute la grande famille SAWADOGO ET BOENA
A
Tous ceux qui m'ont soutenu, encouragé,
conseillé tout au
ii
long de cette quête toujours aussi
nécessaire et difficile.
III
REMERCIEMENTS
Ce travail a été réalisé au
laboratoire des eaux usées du Laboratoire Central de l'ONEA (LCO). Il
est le fruit de la collaboration et de l'implication de plusieurs personnes
à qui nous voudrions exprimer notre profonde reconnaissance.
Nous tenons à remercier particulièrement :
-Pr Alfred S. TRAORE, Professeur Titulaire de
Biochimie-Microbiologie à l'Université de Ouagadougou,
responsable pédagogique de la formation Doctorale en Biotechnologies,
Président du Réseau Ouest Africain de Biotechnologies
(RA-BIOTECH) et Directeur du Centre de Recherche en Sciences Biologiques,
Alimentaires et Nutritionnelles (CRSBAN) pour nous avoir accueilli dans son
centre et nous avoir offert l'opportunité de suivre cette formation
professionnelle ;
-Pr Nicolas BARRO, Professeur titulaire de
Biochimie-Microbiologie, Responsable de la filière Licence
Professionnelle en Management de la Qualité dans les Industries
Agroalimentaires (LP/MQIA) ;
-Dr Aly SAVADOGO, Maître de
conférences au département de Biochimie-Microbiologie, pour sa
disponibilité et l'honneur qu'il nous offre en acceptant présider
ce jury ;
Qu'il trouve ici l'expression de nos sincères
reconnaissances ;
-Dr Cheikna ZONGO, Maître assistant au
Département de Biochimie-Microbiologie, directeur de ce mémoire,
pour avoir accepté de superviser ce travail. Nous avons
bénéficié de votre encadrement scientifique, de vos
conseils et de votre constante disponibilité. Puissiez-vous trouver ici
l'expression de nos sentiments de reconnaissance et de nos sincères
remerciements ;
-Dr Marius K. SOMDA, Assistant au
Département de Biochimie-Microbiologie, pour l'honneur qu'il nous fait
en acceptant participer au jury et de juger la portée scientifique de ce
document. Merci pour les conseils dont nous avons
bénéficié au cours de ce travail ;
-Mr Francis D. KERE, chef du Service
Qualité Eau de l'ONEA, pour avoir accepté nous accueillir dans
son laboratoire et qui a bien voulu nous faire l'honneur de participer à
ce jury et de contribuer à l'appréciation finale de ce travail
;
-A tous les enseignants du CRSBAN pour
l'enseignement de qualité qu'ils ne cessent de dispenser ;
iv
Nous exprimons notre profonde gratitude à :
-Monsieur Ousmane OUEDRAOGO, chef de section
microbiologie pour son engagement
et ses suggestions ;
-Monsieur Robert BOUDA, maître de
stage, pour son encadrement sans faille durant tout
mon stage ;
-Monsieur Jean DIARRA, pour son encadrement
technique ;
-Monsieur Marcel KANTAGBA, pour ses conseils,
sa disponibilité et son soutien dès les
premiers instants de notre stage ;
A tout le personnel du Laboratoire Central l'ONEA, pour
l'ambiance qui a régné tout au long
de notre stage.
A tous nos amis et à tous ceux de près ou de
loin qui ont contribué à la réussite de ce travail.
V
SIGLES ET ABRÉVIATIONS
AFNOR : Association Française de
Normalisation
BA : Bassin Anaérobie
BF : Bassin Facultatif
BM : Bassin de Maturation
CRSBAN : Centre de Recherche en Sciences
Biologiques, Alimentaires et Nutritionnelles
DASS : Direction d'Assainissement
DBO5 : Demande Biochimique en Oxygène
au bout de 5 jours
DCL : Direction de Clientèle
DCO : Demande Chimique en Oxygène
DEX : Direction d'Exploitation
DF : Direction Financière
DMOZ : Direction de Maîtrise d'Ouvrage
de Ziga
DRB : Direction Régionale
Bobo-Dioulasso
DRH : Direction des Ressources Humaines
DRO : Direction Régionale de
Ouagadougou
DRNE : Direction Régionale du
Nord-Est
DRNO : Direction Régionale du
Nord-Ouest
EB: Eau Brute
ISO : International Standardisation
Organisation
LCO : Laboratoire Central de l'ONEA
MES : Matières en suspension
NO3-: Nitrates
OMS : Organisation Mondiale de la
Santé
ONEA : Office National de l'Eau et de
l'Assainissement
PEA : Poste d'Eau Autonome
PO43- : Orthophosphates
POS : Plan d'Orientation
Stratégique
PSAO : Plan Stratégique
d'Assainissement de la ville d'Ouagadougou
RA-BIOTECH : Réseau Ouest Africain de
Biotechnologies
SONABEL : Société Nationale
d'Electricité du Burkina
SQE : Service Qualité Eau
STEP : Station d'Epuration
vi
LISTE DES FIGURES
Figure 1: Organigramme du SQE ..5
Figure 2 : Schéma classique d'une coupe transversale d'un
système classique de lagunage 6
Figure 3 : Schéma de fonctionnement de la station
d'épuration 7
Figure 4: Schéma de fonctionnement d'une station
d'épuration à lagunage aéré 9
Figure 5 : Mécanismes en jeu dans les bassins de lagunage
naturel 12
Figure 6 : pH-mètres 18
Figure 7 : Oxymètre ....18
Figure 8 : DBOmètre . 20
Figure 9 : Spectrophotomètre 21
Figure 10 : Minéralisateur DCO ...21
Figure 11 : Centrifugeuse .22
Figure 12 : Variation moyenne
mensuelle des eaux brutes et traitées de DCO dans le temps
. 26
Figure 13 : Variation moyenne mensuelle des rendements de DCO
...27
Figure 14: Variation moyenne mensuelle des eaux brutes et
traitées de DBO5 dans le temps
..27
Figure 15 : Variation moyenne mensuelle des rendements de DBO5
28
Figure 16 : Variation moyenne mensuelle des eaux brutes et
traitées des MES dans le temps
...29
Figure 17 : Variations moyenne mensuelle des rendements des MES
29
Figure 18: Variation moyenne mensuelle des eaux brutes et
traitées de Nitrates dans le temps
30
Figure19 : Variations moyenne mensuelle des rendements des
Nitrates .31
Figure 20: Variation moyenne mensuelle des eaux brutes et
traitées de orthophosphates dans
le temps 31
Figure 21: Variations moyenne mensuelle des rendements des
orthophosphates ..32
vii
LISTE DES TABLEAUX
TABLEAU I : Caractéristiques des
bassins 6
TABLEAU II : Variation de la DCO dans le
temps 24
TABLEAU III : Variation de la DBO5 dans le
temps 24
TABLEAU IV : Variation des MES dans le temps
25
TABLEAU V : Performances de la STEP de
Kossodo ..32
VIII
Table des matières
Dédiace ii
Remerciements iii
Sigles et abréviations v
Liste des figures vi
Liste des tableaux vii
Résumé x
Introduction generale 1
Chapitre 1: Revue bibliographique ...2
I .Le cadre de l'étude 2
1. La présentation de la structure d'accueil1 2
1.1. L'organisation de l'ONEA 2
1.2. Les missions de L'ONEA 3
1.3. L'ouvrages d'assainissement 3
2. L'organisation et fonctionnement du laboratoire central de
l'ONEA (LCO) 4
II. La station d'épuration de Kossodo 5
1. La situation géographique 5
2. Le fonctionnement des bassins 6
III. L'épuration des eaux usées par le
procédé de lagunage 8
1. L'état des lieux en Afrique de l'ouest 8
2. Le lagunage aéré 8
3. Le lagunage à macrophytes 9
4. Le lagunage à microphytes 10
IV. Les caractéristiques des eaux usées 13
1. Les paramètres physico-chimiques des bassins de
lagunage 13
2. Les paramètres de pollution 14
2.1. La Demande Biochimique en Oxygène (DBO5) 14
2.2. La Demande Chimique en Oxygène (DCO) 15
2.3. Les Matières en Suspension (MES) 15
2.4. L'azote dans les eaux 16
2.5. Le Phosphore dans les eaux 16
Chapitre 2 : matériel et méthodes 17
I. L'échantillonnage 17
1. Le site de prélèvement 17
2. La technique d'échantillonnage 17
ix
3. Le transport et conservation des échantillons 17
II. Les analyses physicochimiques des performances
épuratoires 17
1. La mesure des paramètres physico-chimiques 17
1.1. Le potentiel d'hydrogène (pH) 17
1.2. L'oxygène dissous (O2) 18
1.3. La température 18
2. La détermination de la pollution carbonée
19
2.1. La mesure de la demande biochimique en oxygène
19
2.2. La mesure de la demande chimique en oxygène 20
2.3. La mesure des matières en suspension 21
3. Les nitrates (NO3 -) 22
4. Les orthophosphates (PO43-) 23
Chapitre 3: résultats et discussion 24
1. Les caractéristiques de l'effluent brut 24
2. Les rendements épuratoires 25
2.1. L'élimination de la charge organique 25
2.1.1. La demande chimique en oxygène 25
2.1.2. La demande biochimique en oxygène 27
2.1.3. Les matières en suspensions 28
2.2. L'élimination des nutriments 30
2.2.1. L'élimination de NO3- 30
2.2.2. L'élimination des orthophosphates
(PO43-) 31
3. L'évaluation de l'efficacité du traitement
32
Conclusion et recommandations 33
References bibliographiques 34
Annexe 1 : 36
RÉSUMÉ
Le Burkina Faso, comme les autres pays de la
sous-région, connaissent des problèmes liés à la
gestion des eaux usées domestiques et industrielles. Leurs villes se
sont construites sans véritable plan d'assainissement. Ainsi, pour
remédier ces problèmes, une station d'épuration des eaux
usées a été construite à Kossodo dont un suivi de
ces paramètres révèle nécessaire.
La présente étude a pour objectif
d'évaluer l'état actuel de fonctionnement de la station de
lagunage et dégager pour le futur, les perspectives de gestion du
système.
Pour l'atteinte de cet objectif, nous avons effectué
des prélèvements à l'entrée et à la sortie
de la station et procéder par la méthode de
spectrophotométrie pour déterminer les paramètres
épuratoires.
Ainsi les taux d'abattement des paramètres de pollution
obtenus atteignent 92,64% pour la DBO5, 70,73% pour la DCO et 47,78% pour les
MES ; ces abattements sont bonne dans l'ensemble. Un suivi rigoureux des
paramètres pourrait améliorer davantage la performance
épuratoire de la station d'épuration de Kossodo d'une part et
d'autre part assurer un cadre sain et durable pour la population et surtout les
maraichers dans la réutilisation.
X
Mots clés : Eaux usées,
Performances épuratoires, Gestion, ONEA, Ouagadougou.
1
INTRODUCTION GENERALE
Les pays subsahariens, et singulièrement ceux de la
région soudano-sahélienne vivent avec acuité le
problème de l'assainissement en général et des eaux
usées en particulier (Kiemdé, 2006).
Cet état de fait a entre autres pour causes, la
précarité du régime climatique de la région, la
démographie galopante dont le taux de croissance est relativement
élevé. Au Burkina Faso, la prise de conscience des enjeux de
l'assainissement a débouché sur la mise en place de structures
chargées d'intégrer ces questions dans les stratégies du
développement durable. Cependant, le Plan Stratégique
d'Assainissement de la ville de Ouagadougou (PSAO) a été
initié. Cette initiative dans sa composante « Assainissement
collectif » permet d'opérer la jonction entre les travaux des
stations d'expérimentation et de recherche, menés à petite
échelle et la gestion d'une réalisation à grande
échelle.
En outre les conditions naturelles difficiles et la croissance
démographique incontrôlée, reposent ainsi avec
acuité la problématique du développement humain,
particulièrement dans le contexte du milieu urbain :
accessibilité à l'eau potable ;
accessibilité à des systèmes
d'assainissement ;
accessibilité à des revenus justes et
équitables.
L'épuration des eaux usées de la ville de
Ouagadougou par lagunage à grande échelle, intéresse
à divers niveaux tous les partenaires impliqués dans les
questions d'assainissement : scientifiques, bailleurs de fonds, institutions
politiques, exploitants du système, et mêmes les pays de la sous
région intéressés par cette initiative.
C'est dans ce cadre que s'inscrit notre travail dont le
thème s'intitule : « évaluation de la
performance de la station d'épuration de Kossodo dans le traitement
physicochimique de l'eau ».
L'objectif global de l'étude est d'évaluer
l'état actuel de fonctionnement de la station de lagunage et
dégager pour le futur, des perspectives de gestion du système. A
cet effet, les objectifs spécifiques suivants ont été
définis :
évaluer les paramètres indicateurs de polluants
dans l'eau à l'entrée de la station ;
évaluer les paramètres indicateurs de polluants
dans l'eau à la sortie de la station ;
comparer leurs valeurs aux normes de l'OMS applicables au
Burkina Faso.
2
REVUE BIBLIOGRAPHIQUE
I .Le cadre de l'étude
1. La présentation de la structure d'accueil1
1.1. L'organisation de l'ONEA
Société d'Etat, l'ONEA est placé sous la
tutelle conjointe de trois ministères :
-la tutelle technique du ministère de l'eau de
l'aménagement hydraulique et de l'assainissement ;
-la tutelle financière du ministère des finances
et du budget ;
-la tutelle de gestion du ministère du commerce, de la
promotion de l'entreprise et de
l'artisanat.
L'ONEA est administré par un conseil d'administration qui
est obligatoirement saisi de
toutes les questions d'importance pouvant influencer la marche
générale de la société. Parmi
les administrateurs on peut citer le ministère de
l'environnement et du développement
durable.
Actuellement, l'ONEA gère 46 centres dotés d'un
système d'approvisionnement en eau
potable et un centre équipé de Poste d'Eau
Autonome (PEA). Ces centres sont répartis dans
quatre directions régionales :
-La Direction Régionale de Ouagadougou (DRO) ;
-Le Direction Régionale de Bobo-Dioulasso (DRB) ;
-Le Direction Régionale du Nord-Ouest (DRNO) ;
-la Direction Régionale du Nord-Est (DRNE).
Les quatre directions sont coiffées par la direction de
l'exploitation qui est l'une des six
directions centrales. Les autres directions centrales sont :
-la Direction de l'Assainissement (DASS) ;
-la Direction clientèle (DCL) ;
-la Direction de l'Exploitation (DEX) ;
-la Direction Financière (DF) ;
-la Direction des Ressources Humaines (DRH) ;
-la Direction de Maitrise d'Ouvrage de Ziga (DMOZ) qui assure la
mise en oeuvre du projet
de renforcement de l'approvisionnement en eau potable de
Ouagadougou par le barrage de
Ziga.
L'ONEA assure la production et la distribution de l'eau potable
selon 3 étapes :
-l'exhaure de l'eau à partir des ressources en eau
souterraine et de surface (une source Bobo-
Dioulasso) ;
3
-le traitement de l'eau dans les stations de traitement en
chaine complète (floculation, décantation, filtration,
désinfection) ;
-la distribution par des conduites d'adduction.
Ces trois étapes sont possibles grâce aux
équipements de pompage, aux sources d'énergie (SONABEL et groupes
électrogènes) et aux ouvrages de stockage et châteaux
d'eaux. Dans le domaine de l'assainissement, l'ONEA s'attelle à la mise
en oeuvre des plans stratégiques des villes de Ouagadougou et de
Bobo-Dioulasso dans ses volets d'assainissement autonome (latrines, bacs
à laver et douches raccordés aux puisards), l'assainissement
scolaire (latrines et urinoirs) et l'assainissement collectif. C'est donc dans
le cadre de l'assainissement collectif que l'ONEA a mis en place à
Ouagadougou un réseau d'égout débouchant sur une station
d'épuration au secteur 26 plus précisément dans le village
de Kossodo-Nabisso. La station est fonctionnelle depuis le 19 Janvier 2004.
1.2. Les missions de L'ONEA
L'Office National de l'Eau et de l'Assainissement (ONEA) a
pour mission, la création, la gestion et la production des installations
de captage, d'adduction et de traitement. Il oeuvre dans la distribution d'eau
potable pour les besoins urbains et industriels. L'ONEA travaille aussi
à promouvoir et à améliorer la gestion des installations
d'assainissement collectif et individuel (latrines améliorées,
etc.)
1.3. L'ouvrages d'assainissement
Les principaux ouvrages d'assainissement des eaux usées
domestiques peuvent être regroupés en deux grandes classes : les
ouvrages individuels et les ouvrages collectifs. + Les ouvrages
individuels
Dans cette classe on retrouve :
-les latrines traditionnelles utilisées à
Ouagadougou par environ 57 % des ménages (ONEA) ; -les latrines à
fosses fixes ou étanche utilisées par 24% des ménages
(ONEA) ;
-les WC (Water Close) modernes à chasse
raccordée « toutes eaux » qui sont utilisés dans 13%
des ménages (ONEA).
+ Les ouvrages collectifs
Les infrastructures d'assainissement collectif sont peu
développées. L'assainissement individuel reste dominant. Jusqu'en
Décembre 2010, un seul réseau d'égouts long de 4 km
desservait essentiellement la zone industrielle de Kossodo (brasserie) et une
partie du centre ville (BCEAO et marché central).
4
2. L'organisation et fonctionnement du laboratoire central
de l'ONEA (LCO)
Le laboratoire central de l'ONEA est doté d'un
personnel compétent et formé aux techniques d'analyses de la
qualité de l'eau. Il a pour rôle de contrôler la
potabilité des eaux de boisson, la qualité des eaux de surface,
de puits et de forage et enfin contrôler la qualité des eaux
usées et épurées avant leurs rejets ou
réutilisation.
Celui-ci est subdivisé en cinq sections :
-la section de chimie générale : dans cette
section, seules les analyses physicochimiques y sont faites. Il s'agit entre
autre la mesure du pH, la conductivité, le taux d'alcalinité
complète (TAC), de la dureté totale, le carbone agressif etc ;
-la section de chimie organique : les analyses de cette
section se focalisent sur la détermination des pesticides
présents dans les eaux de boissons par la chromatographie en phase
gazeuse (CPG) ;
-la section de métaux lourds : s'occupe de la
recherche des métaux tels que l'Arsenic, le Plomb, le Fluor, l'Aluminium
etc ;
-la section de microbiologie : dans cette section on
recherche les germes totaux en général et plus
spécifiquement les indicateurs de contamination fécale
(coliformes thermotolérants et les streptocoques fécaux) ;
-la section des eaux usées : cette section s'occupe
exclusivement des analyses des eaux usées. Les principales analyses
effectuées sont : la détermination de la DCO, la DBO5, les MES,
les Nitrates, Phosphores etc.
Ces différentes sections sont bien
détaillées dans la figure n° 1.
Directeur de
l'exploitation
Chef de Service Qualité de l'Eau
Agents d'appui : - Agent de Saisie Laboratoire
- Chauffeur
- Manoeuvre de Laboratoire
|
|
Chef de Section
Chimie Organique
Microbiologie
Chef de section Chimie Générale- Métaux
Lourds-Eaux Usées
5
Agents
Qualité Eau
du
Laboratoire
de
Microbiolo
gie
|
|
Agent
Qualité Eau
du
Laboratoire
de
Chimie
Organique
|
|
Agents
Qualité Eau
du
Laboratoire
de
Chimie
Générale
|
|
Agents
Qualité Eau
du
Laboratoire
de
Métaux
Lourds
|
|
Agent
Qualité Eau
du
Laboratoire
des
Eaux
Usées
|
|
Figure n° 1 : Organigramme du
Service Qualité Eau (SQE)
II. La station d'épuration de Kossodo
1. La situation géographique
La station d'épuration (STEP) des eaux usées de
la ville de Ouagadougou est située à Kossodo à la
périphérie de la zone industrielle au nord-est de la ville
(Annexe 3). Elle a été construite dans le cadre du Plan
Stratégique d'Assainissement de la ville de Ouagadougou (PSAO)
financé par l'Agence Française pour le Développement (AFD)
et la Banque Mondiale. Elle est destinée à l'assainissement
collectif des eaux usées domestiques et industrielles de la ville de
Ouagadougou. Les eaux épurées sont destinées à
être réutilisées en agriculture urbaine.
6
2. Le fonctionnement des bassins
La station d'épuration de Ouagadougou, en
fonctionnement depuis 2004, est une station de lagunage naturel avec 08 bassins
comme l'illustre la figure 4. Les effluents arrivent par un réseau
alternant écoulement gravitaire et stations de refoulement (3 au
total).
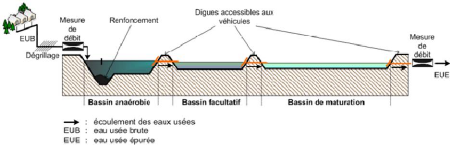
Figure n°2 : Schéma
classique d'une coupe transversale d'un système classique de lagunage
(Source : http//
www.univ-lehavre.fr/cybernat/pages/lagunat)
Les trois premiers bassins, en parallèles, sont
construits de manière à recevoir une lame d'eau de 4 m et
permettent une dégradation de la matière par voie
anaérobie.
Ils sont ensuite reliés à 2 bassins en
parallèles, appelés bassins facultatifs, qui permettent une
dégradation de la matière par voie aérobie et
anaérobie (1,80 m de lame d'eau). Enfin, trois derniers bassins sont en
série et dégradent la matière de façon
aérobie. Une goutte d'eau arrivant dans la station y restera ainsi un
mois avant d'en sortir. Les eaux ainsi traitées sont rejetées
dans un affluent de la Volta. Il a été aussi prévu
qu'elles soient réutilisées pour l'irrigation des champs
avoisinants (Gorse F, 2008).
En plus de ces bassins on a un laboratoire, 2 bâtiments
administratifs et enfin des latrines pour éviter d'éventuelles
pollutions d'origine fécale au sein du site.
Tableau I : Caractéristiques
des bassins
Désignation
|
BA
|
BF
|
BM1
|
BM2
|
BM3
|
Profondeur (m)
|
4
|
1,8
|
1,20
|
1,20
|
1,20
|
Surface (m2)
|
0,37
|
3
|
1,47
|
0,37
|
0,37
|
Volume (m3)
|
18500
|
54000
|
29400
|
7400
|
7400
|
Temps de séjour (j)
|
3
|
16
|
6
|
3
|
3
|
|
Source : Loue, 2005
7
L'ensemble des bassins est prévu pour fonctionner en
deux filières parallèles.
Bassins anaérobies (figure 5)
Au nombre de trois (03), ces bassins doivent permettre un
fonctionnement normal même lors du curage des bassins qui est fait en
théorie tous les deux (02) ans.
Le BA1 déverse toujours dans le BF1, le BA3
déverse toujours dans le BF2, le BA2 est prévu pour
déverser soit dans le BF1, soit dans le BF2. De ce fait, les BA ne sont
pas équipés de bypass.
Bassins facultatifs (figure 5)
Ces bassins au nombre de deux (02) fonctionnent en
parallèles. Lors des vidanges qui sont prévues tous les dix (10)
ans en moyenne, l'ensemble des influents est prévu pour transiter dans
un seul BF.
Les sorties de ces deux bassins sont en série,
assurant ainsi le passage de la totalité des effluents en tête du
BM1.
Bassins de maturation (figure 5)
Ces bassins au nombre de trois (03), sont en série,
avec chacun un by-pass en tête de bassin, permettant de mettre
hors circuit l'un ou l'autre des bassins.
Sur l'ensemble des huit bassins, seul le bassin facultatif
1(matérialisé en noir au niveau du schéma ci-dessous)
n'est pas fonctionnel compte tenu du niveau de charges hydrauliques
actuelles.
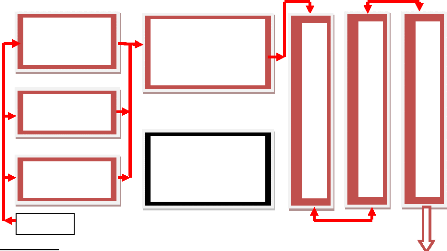
Figure n°3: Schéma de fonctionnement
de la station d'épuration de Kossodo
ENTREE
ANAEROBIE 3
ANAEROBIE 2
ANAEROBIE 1
FACULTATIF1
FACULTATIF2
MATURATION1
MATURATION 2
MATURATION 3
Source : ONEA, 2004
|
SORTIE
|
|
8
III. L'épuration des eaux usées par le
procédé de lagunage
1. L'état des lieux en Afrique de l'ouest
Le lagunage a été introduit en Afrique de
l'Ouest depuis 30 ans avec l'aide des agences françaises et suisses de
coopération et d'aide au développement. Plusieurs pays tels que
le Sénégal en 1976, le Burkina Faso et la Cote d'Ivoire ont eu
l'occasion de le tester entre 1985 et 1989 (Koné, 2002).
C'est à partir de l'observation de
l'écosystème des étangs qu'est né le principe du
lagunage. La technique est basée sur des phénomènes
d'autoépuration naturelle dans les mares et les étangs. Ces
phénomènes sont basés sur des facteurs physiques
(rayonnement solaire, température, sédimentation etc) et
biologiques (prédation, parasitisme, antagonismes, compétition
etc). Le principe de fonctionnement s'inspire donc de celui des
écosystèmes rencontrés dans les zones humides naturelles
(Radoux ,1989). Il présente certains avantages (simplicité et
économie de fonctionnement, adaptation aux variations de charge,
efficacité de désinfection, production de boue réduite).
Les eaux usées pouvant être traitées par lagunage sont les
eaux usées urbaines et industrielles des industries agroalimentaires
(abattoirs, laiteries, sucreries, distilleries, conserveries etc).
2. Le lagunage aéré
Dans ce système l'oxygène est apporté
mécaniquement par un aérateur de surface ou une insufflation
d'air. Ce principe ne se différencie des boues activées que par
l'absence de système de recyclage des boues. En situation de sous charge
importante, la nitrification peut être complète avec une
dénitrification partielle. Dans la partie d'aération, les eaux
à traiter sont en présence de micro-organismes qui vont consommer
et assimiler les nutriments constitués par la pollution à
éliminer.
Dans la partie de décantation, les matières en
suspension que sont les amas de microorganismes et de particules
piégées, décantent pour former les boues.
D'après (Deronzier et al., 2001), ce
système est composé principalement de deux bassins dont la
population bactérienne se présente comme suit :
une densité de bactéries faible et à un
temps de traitement important pour obtenir le niveau de qualité requis
;
une floculation peu importante des bactéries, ce qui
contraint à la mise en place d'une lagune de décantation
largement dimensionnée.
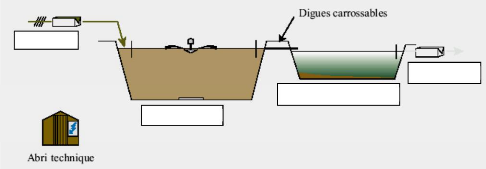
Eau brute
Lagune aéré
Lagune de décantation
Eau traitée
9
Figure n°4 : Schéma de
fonctionnement d'une station d'épuration à lagunage
aéré (Source : Deronzier et al.,
2001)
Le lagunage aéré est très sensible aux
variations climatiques et le taux d'élimination de l'azote et du
phosphore reste limité à l'assimilation bactérienne de
l'ordre de 25 à 30% (Satin et Selmi, 1999). Le niveau de qualité
de l'effluent est bon au niveau de la charge organique avec plus de 80 %
d'abattement, la filière se prête aisément à
l'apport complémentaire d'adjuvants physico-chimiques en vue
d'éliminer les orthophosphates.
3. Le lagunage à macrophytes
Le procédé utilise des végétaux
supérieurs, flottants ou fixés. Ces végétaux encore
appelés macrophytes servent de supports à d'autres
microorganismes intervenant dans l'épuration. Les performances
intrinsèques des bassins à macrophytes en Afrique sont
très peu étudiées et la laitue d'eau demeure la plante la
plus utilisée dans les bassins d'épuration (Charbonnel et Simo,
1986 ; Koné, 2002). Le lagunage à macrophytes est effectué
dans des bassins en séries où les plantes cultivées
couvrent les bassins et maintiennent les conditions anaérobies de
dégradation de la matière organique. Les racines des plantes
fournissent l'oxygène au milieu et servent de pièges aux boues
qui remontent en surface. Le lagunage à macrophytes est
généralement utilisé en vue d'améliorer le
traitement sur les paramètres DBO5 ou MES ou de l'affiner les
nutriments, les métaux etc. (Déronzier, 2001).
10
4. Le lagunage à microphytes
Dans le lagunage à microphytes également
nommé le lagunage naturel, l'épuration est assurée par un
temps de séjour prolongé dans plusieurs bassins étanches
disposés en série. Le nombre de bassins est
généralement de trois (03) (Piétrasanta et Bondon, 1994).
Cependant, utiliser une configuration avec quatre, voire six bassins permet
d'avoir un meilleur abattement bactérien. L'un des mécanismes sur
lequel repose le lagunage à microphytes est la photosynthèse. La
tranche d'eau supérieure des bassins est exposée à la
lumière. Ceci permet le développement d'algues qui produisent
l'oxygène nécessaire au développement et au maintien des
bactéries aérobies. Ces bactéries sont responsables de la
dégradation des matières organiques. Le gaz carbonique produit
par les bactéries ainsi que les sels minéraux permettent aux
algues de se multiplier. Il y a ainsi prolifération des deux populations
interdépendantes : les bactéries et les algues planctoniques,
également dénommées « microphytes ».
Dans le fond du bassin où la lumière ne
pénètre pas, ce sont des bactéries anaérobies qui
dégradent la matière organique issue de la décantation. Un
dégagement de gaz carbonique et de méthane se produit à ce
niveau (Perera et Baudot, 2001). Une station de lagunage à microphytes
est constituée de plusieurs combinaisons possibles. La plus commune est
cependant la disposition de trois types de bassins (anaérobie,
facultatif, maturation) (Piétrasanta et Bondon, 1994). Les eaux
usées qui arrivent à la station subissent un prétraitement
physique par dégrillage, déshuilage et dessablage pour
éliminer les matières solides grossières, les graisses et
le sable selon l'origine des eaux à traiter.
Le bassin anaérobie (BA)
Le bassin anaérobie se caractérise
principalement par sa très faible concentration en oxygène
dissous. Cette anaérobiose s'explique par la profondeur de ce bassin
(2-5m) et la forte charge organique associée à une
activité microbienne importante consommatrice d'oxygène (Drapeau
et Jankovic, 1977). Les algues y sont généralement absentes.
Lorsqu'elles sont présentes, leur développement se limite
à la surface. Le bassin anaérobie assure une première
phase de l'épuration, qui consiste principalement à
l'élimination de la matière organique biodégradable
représentée par la demande biochimique en oxygène (DBO).
La charge admissible dans ce bassin est supérieure à 100g de
DBO5/m3/j pour une profondeur de 03 m. La DBO5 est la demande
biochimique en oxygène en 5 jours. La dégradation de la
matière organique se déroule en trois phases :
11
-Une phase de dépolymérisation et
d'acidogenèse, dans laquelle les macromolécules sont initialement
hydrolysées par les microorganismes (Pseudomonas, Cytophaga,
Flavobacterium, Acaligenes) en acide gras, carbohydrates, acides
aminés. Ces produits de dégradation sont ensuite utilisés
comme substrats par les bactéries acidogènes (Clostridium,
Bacteroides, Peptostreptococcus, Peptococcus, Eubacterium, lactobacillus)
qui les transforment en acide gras volatils.
-Une phase d'acetogenèse dans laquelle les
bactéries acetogènes (Syntrophomonas, Syntrophobacter,
Acetobacter) oxydent les acides gras volatiles en acétate, en
dioxyde de carbone (CO2) et en hydrogène moléculaire (H2).
- Une phase de méthanogenèse assurée par
les bactéries méthanogènes (Methanothryx,
Methanosarcina, Methanobrevibacter, Methanobacterium) qui
métabolisent les produits de la phase acetogenèse en
méthane et sulfure d'hydrogène.
La réduction des matières organiques (pollution
carbonée) varie entre 40% et 60% dans une gamme de température
comprise entre 10°C et 20°C (Mara et Pearson, 1998) et pour un temps
de séjour court de 1 à 2,5 jours. Ce temps de séjour ne
permet pas une bonne élimination des microorganismes
pathogènes.
Le bassin facultatif (BF)
Il est divisé verticalement en trois zones comme
l'indique la figure n°3 : une zone aérobie, une zone
anaérobie facultative et une zone anaérobie. Les
mécanismes entrant en jeu dans ce type de bassin sont les suivants :
-dans la zone aérobie, grâce aux sels nutritifs,
au soleil et au gaz carbonique, les algues microscopiques se développent
et produisent de l'oxygène nécessaire aux bactéries
aérobies pour dégrader les matières organiques ;
-dans la zone anaérobie facultative, les
bactéries anaérobies facultatives dégradent
également les matières organiques ;
-dans la zone anaérobie, les matières
organiques sont minéralisées en méthane et en
hydrogène. Dans le cas d'une eau d'origine domestique, environ 90
à 95% des matières biodégradables exprimées en
DBO5, s'échappe sous forme de gaz (Satin et Selmi, 1999).
Ce type de bassin est profond de 1,5 à 2 m et la
réduction de la matière organique est de l'ordre de 60 à
80% avec un temps de séjour de 5 à 10 jours.
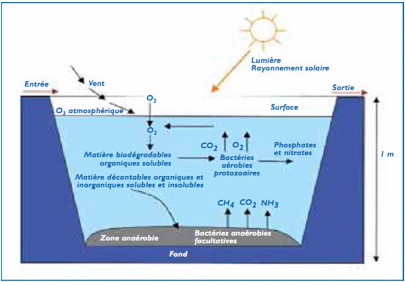
12
Figure n°5: Les mécanismes en jeu
dans les bassins de lagunage naturel (Perera et
Baudot, 2001)
Le bassin de maturation (BM)
Le rôle principal de ce bassin est d'affiner
l'épuration en éliminant en grande partie la pollution
bactérienne notamment les pathogènes d'intérêt
sanitaire. Ce processus épuratoire est régi par un ensemble de
facteurs dont les principaux sont les rayons ultra violets, la
température, l'insuffisance du substrat carboné, le temps de
séjour élevé et la prédation (BCEOM, 1990). Ce
bassin faiblement chargé en matière organique est profond de 1
à 1,5 m. Le volume de liquide est entièrement aérobie et
les microorganismes qui s'y développent sont essentiellement
aérobies ou anaérobies facultatives. Ils utilisent
l'oxygène fourni par la photosynthèse réalisée par
les algues pour se développer et les approvisionnent en sels nutritifs
issus de leur métabolisme. La concentration de l'oxygène augmente
dans la journée avec l'activité photosynthétique et le pH
augmente avec la consommation du CO2 par les algues. Dans la nuit, la
concentration de l'oxygène diminue du fait de la respiration des
bactéries aérobies et de l'absence de photosynthèse tandis
que le pH diminue avec la production du CO2 résultant du
métabolisme des bactéries. Le phytoplancton consomme
également de l'oxygène et rejette du gaz carbonique la nuit. Le
temps de séjour est de l'ordre de 12 à 30 jours avec un rendement
épuratoire de plus de 80% pour la pollution bactérienne
13
exprimée en coliformes thermotolérants. Dans ce
bassin apparait le zooplancton qui se nourrit de bactéries ainsi que des
matières organiques.
L'eau ainsi épurée est rejetée dans les
cours d'eaux ou réutilisée en agriculture après analyses.
IV. Les caractéristiques des eaux
usées
1. Les paramètres physico-chimiques des bassins de
lagunage
Température
La température influence la cinétique des
réactions. En effet, l'activité biologique du milieu est d'autant
plus élevée que la température augmente. Une
température très élevée conduit à
l'épuisement de l'oxygène dissout par abaissement de la valeur de
saturation tout en modifiant l'équilibre biologique du système.
Pour le maintien d'une bonne activité épuratoire, les limites
inférieures et supérieures de la température sont
respectivement de 10°C et 30°C (Guerrin, 1981).
Potentiel d'hydrogène (pH)
Le pH est l'un des paramètres les plus importants de
la qualité de l'eau. Il mesure la concentration en ions hydronium
H3O+ de l'eau et traduit la balance entre acide et base sur une
échelle de 0 à 14. Le pH de neutralité est 7.
Ce paramètre caractérise un grand nombre
d'équilibre, physico-chimique, et dépend de facteurs multiples,
dont l'origine de l'eau.
Le pH des eaux usées domestiques est
généralement voisin de la neutralité (compris entre 6,7
à 7, 2) (Guerrin, 1981). Il doit être étroitement
surveillé au cours de toutes les opérations de traitement.
L'épuration biologique se trouve fortement perturbé pour un pH
< 4,5 ou > 8. Les variations du pH sont en relation avec
l'activité photosynthétique dont la réaction est la
suivante: (CO3H) 2 Ca ? CaCO3 + H2O + CO2
La consommation de CO2 par la réaction de la
photosynthèse tend à déplacer l'équilibre
carbonique dans le sens de sa production et donc à élever le pH.
Ainsi, un pH bas pourrait être l'indice d'une faible productivité
: soit par absence, soit par excès d'algues.
Conductivité
La conductivité mesure la capacité de l'eau
à conduire le courant entre deux électrodes. La plupart des
matières dissoutes dans l'eau se trouvent sous forme d'ions
chargés électriquement (en cations on a par exemple
Ca2+, Mg 2+, K+, Na+ etc et en
anions SO42-, Cl-, HCO3-, PO43-,
NO3- etc). La mesure de la conductivité permet donc
d'apprécier la quantité de sels dissous dans l'eau. La
conductivité est également fonction de la température de
l'eau : elle est plus importante lorsque la température augmente. Elle
est exprimée en microsiemens par
14
centimètre (uS/cm) et est
ramenée à une température de 20 à 25°C. Comme
la température, des variations de conductivité permet de mettre
en évidence des pollutions, des zones de mélanges ou
d'infiltration. La conductivité est également l'un des moyens de
valider les analyses physico-chimiques de l'eau.
Oxygène dissous (O2)
L'eau absorbe autant d'oxygène que nécessaire
pour que les pressions partielles d'oxygène dans le liquide et dans
l'air soient en équilibre. La solubilité de l'oxygène dans
l'eau est fonction de la pression atmosphérique (donc de l'altitude), de
la température et de la minéralisation de l'eau : la saturation
en O2 diminue lorsque la température et l'altitude augmentent. La
variation de la teneur en oxygène peut être également
fonction de la présence des végétaux, des matières
organiques oxydables, des organismes et des germes aérobies ainsi que de
la perturbation des échanges atmosphériques à l'interface
eau-air.
La concentration en oxygène dissous est un
paramètre essentiel dans le maintien de la vie, et donc dans les
phénomènes de dégradation de la matière organique
et de la photosynthèse. C'est un paramètre utilisé
essentiellement pour les eaux de surface. Au niveau de la mer à
20°C, la concentration en oxygène en équilibre avec la
pression atmosphérique est de 8,8 mg/L d'O2 à saturation. Une eau
très aérée est généralement
sursaturée en oxygène (torrent), alors qu'une eau chargée
en matières organiques dégradables par des microorganismes est
sous-saturée.
L'oxygène dissous est un paramètre utile dans le
diagnostique biologique du milieu eau. La dissolution de l'oxygène dans
l'eau est le résultat de deux phénomènes principaux :
l'échange gazeux à l'interface eau-air favorisé par
l'action du vent et l'agitation de surface ; l'activité
photosynthétique du plancton.
2. Les paramètres de pollution
2.1. La Demande Biochimique en Oxygène
(DBO5)
La Demande Biochimique (ou Biologique) en Oxygène
(DBO), représente la quantité d'oxygène qui est
utilisée par les microorganismes aérobies pour la
dégradation de la matière organique biodégradable. La DBO5
permet d'évaluer le contenu en matières organiques
biodégradables d'une eau. Elle constitue donc une mesure indirecte du
degré de pollution d'une eau, par la matière organique. Le
contenu des matières organiques d'une eau est le plus souvent
évalué au bout de 5 jours (DBO en 5 jours d'où le terme
DBO5) pour deux raisons principales : (i) la dégradation complète
des matières organiques peut être relativement longue (plusieurs
semaines) ; (ii) l'oxydation des dérivés ammoniacaux et des
nitrites en nitrates
15
(nitrification), absorbe aussi de l'oxygène. Mais cette
nitrification ne débute qu'au bout de 10 jours. L'adjonction de
1-allyl-2-thiourée (C4H8N2S) permet d'inhiber la
nitrification ; ce qui permet de mesurer la DBO21 qui correspond
à la dégradation complète de la matière organique
biodégradable en 21 jours. La détermination de la DBO5 (mg O2/L)
s'effectue par plusieurs méthodes :
y' méthode de dilution : mesure de l'oxygène
dissous au début et à la fin de l'essai ;
y' méthode manométrique au mercure (lecture
directe) ;
y' méthode OxyTop qui est un système
électronique de mesure (principe de mesure manométrique avec
capteur de pression).
Les tests sont réalisés dans des flacons
standards de 300 mL, à l'obscurité et à 20°C pendant
5 jours en présence de microorganismes. La consommation d'oxygène
permet l'oxydation des matières organiques par les microorganismes.
L'oxydation des matières organiques provoque la formation de CO2 qui est
piégé par le KOH. Ces tests doivent impérativement se
dérouler à l'obscurité, pour prévenir toute
production d'oxygène à travers la photosynthèse en cas de
présence d'algues ou de bactéries photosynthétiques dans
l'échantillon.
2.2. La Demande Chimique en Oxygène (DCO)
La DCO exprime la quantité d'oxygène dissous
nécessaire pour oxyder par voie chimique, sans intervention
d'êtres vivants, toutes les substances oxydables contenues dans un
effluent (sels minéraux oxydables, composés organiques
biodégradables ou non, etc.) Elle est exprimée en mg O2/L. La
demande chimique en oxygène est un critère de pollution
organique. La mesure de la DCO est obtenue par oxydation chimique en milieu
acide, l'acide sulfurique (H2SO4) et le dichromate de potassium
(K2Cr2O7) sont utilisés comme oxydants. Ce dernier a la
propriété de passer du jaune à l'état oxydé
au vert à l'état réduit. On effectue des dilutions avant
ajout de tout réactif pour des échantillons dont la DCO est
susceptible de dépasser 900 mg/L.
2.3. Les Matières en Suspension (MES)
Ce sont les matières solides contenues dans les eaux
usées et qui sont séparables par filtration ou par
centrifugation. Elles sont exprimées en poids de matières
sèches. Les MES comportent des matières organiques et
minérales. Elles constituent un paramètre important qui marque
bien le degré de pollution d'un effluent. La mesure des MES repose sur
le principe suivant : à l'aide d'un équipement de filtration sous
pression (pompe), un volume d'échantillon est filtré sur un
filtre préalablement pesé. Le filtre est ensuite
séché à l'étuve à une température de
105°C pendant 1heure 30 minutes. La masse du résidu retenu sur le
filtre est déterminée par
16
pesée : c'est la différence entre la masse
à vide du filtre et sa masse après séchage. De même,
la mesure des MES peut être réalisée également par
la méthode centrifugation.
2.4. L'azote dans les eaux
L'Azote se trouve dans la nature sous plusieurs formes (Rodier,
1996) :
-N2 : Azote moléculaire sous forme gazeuse dans
l'atmosphère (78 % de l'air) ;
-N : Azote organique dans les composés organiques (acides
aminés, protéine etc) ;
-NH3 : Azote ammoniacal forme réduite soluble ;
-NO3- et NO2 - : l'azote nitrate et nitrique, forme
oxydées respectivement stable et instable. L'azote est le composé
intermédiaire de la transformation de l'ammoniaque en nitrates. L'azote
des eaux usées domestiques provient des déjections humaines
(urée) et de la consommation ménagère des produits
azotés (protéines).
Cet azote organique est transformé en ammoniaque (NH4
+) qui est oxydé en nitrate (NO3 -). Les nitrates sont ensuite
réduits en azote moléculaire.
2.5. Le Phosphore dans les eaux
Dans les eaux, le phosphore est présent sous forme de
phosphore organique et d'ions phosphates ou orthophosphates (PO43-).
Le dosage des orthophosphates s'effectue par la méthode
colorimétrique au molybdovanadate. Pour évaluer le phosphore
total d'un échantillon, il faut d'abord procéder à une
minéralisation du phosphore organique en orthophosphates (par digestion
au persulfate acide), avant de les doser comme précédemment.
17
MATERIEL ET METHODES
Cette étude s'est déroulée à la
station d'épuration des eaux usées de la ville de Ouagadougou
(Kossodo) de, Septembre à Novembre. La mesure des paramètres
physico-chimiques permet d'évaluer les performances épuratoires
de la station par rapport aux normes du Burkina Faso (2001) et de
l'Organisation Mondiale de la Santé (1989).
I. L'échantillonnage
1. Le site de prélèvement
Au niveau de la station d'épuration de Kossodo, nous
avons procédé à des prélèvements d'un litre
d'eau usées sur chacun des points suivants : à l'entrée de
la station (eau brute : E.B) et à la sortie de la station (eau
traitée: E.T).
2. La technique d'échantillonnage
Le prélèvement sur les différents points
a été effectué chaque Jeudi matin durant trois mois. Les
échantillons ont été prélevés à
l'entrée de la station et à la sortie de la station à
l'aide d'une perche. Ces échantillons ont été
conditionnées dans des bouteilles d'un litre ; ces bouteilles sont
ensuite codifiées et placées à 4°C dans des armoires
réfrigérées avant qu'elles ne parviennent au laboratoire.
Certains paramètres tels que l'oxygène dissous, la
température, la conductivité et le pH sont mesurés in
situ.
3. Le transport et conservation des échantillons
Les échantillons ainsi prélevés sont
placés au frais à 4°C lors du transport au laboratoire pour
éviter que certains composés ne se détériorent. Au
laboratoire les échantillons sont immédiatement rangés
dans des armoires réfrigérés (4°C) jusqu'au moment de
leur analyse (Apha, 1985).
II. Les analyses physicochimiques des performances
épuratoires
1. La mesure des paramètres physico-chimiques
1.1. Le potentiel d'hydrogène (pH)
La mesure est faite in situ à l'aide d'un
pH-mètre de marque WTW équipé de sondes spécifiques
pour chaque paramètre. L'électrode utilisée pour la mesure
du pH est de type sentix 41/T avec compensation automatique de
température. La figure n°6 illustre le pH-mètre que nous
avons utilisé.
18
Figure n°6 : photo du
pH-mètre (Sawadogo, 2013)
1.2. L'oxygène dissous (O2)
La mesure de l'oxygène dissous est faite in situ
à l'aide d'une sonde à oxygène de type cello X325 WTW
du multimètre, avec compensation automatique de température. La
lecture est directe et est donnée en mg O2/L comme
présenté sur la figure n°7.

Figure n°7 : photo de
l'Oxymètre (Sawadogo, 2013)
1.3. La température
La mesure est faite in situ au moment de la mesure de
l'oxygène dissous avec un multi paramètre. La lecture est directe
et est donnée en degré Celsius (°C).
19
2. La détermination de la pollution
carbonée
Les méthodes de mesure des paramètres classiques de
la qualité des eaux (DBO5, DCO, MES Nitrates, Phosphates, etc) sont
mentionnées dans les normes françaises (AFNOR, 1997).
2.1. La mesure de la demande biochimique en oxygène
Principe
L'échantillon d'eau introduit dans une enceinte
thermostatée est mis sous incubation. On fait la lecture de la masse
d'oxygène dissous, nécessaire aux microorganismes pour la
dégradation de la matière organique biodégradable en
présence d'air pendant cinq (5) jours. Les microorganismes
présents consomment l'oxygène dissous qui est remplacé en
permanence par l'oxygène de l'air, contenu dans le flacon provoquant une
diminution de la pression au dessus de l'échantillon. Cette
dépression sera enregistrée par une OxyTop.
Mode opératoire
Les échantillons ont été d'abord
dilués avant leur répartition dans des flacons de DBO (flacons
ombreux), y ajouter 1 mL d'allyl-2 thiourée puis mettre un barreau
magnétique. Ces flacons possèdent des godets en caoutchoucs dans
leurs goulots dans laquelle sont placées chacun 2 pastilles de soude.
Chaque flacon a été vissé par un OxyTop puis appuyer
simultanément les touches S et M jusqu'à l'apparition deux 00.
Enfin les flacons ont été placés sur l'agitateur dans une
armoire thermostatique à 20°C pendant 5 jours. La touche S permet
de visualiser les valeurs mémorisées par l'OxyTop. La figure
n°8 illustre l'appareillage de mesure.

20
Figure n°8 : photo du
DBOmètre (Sawadogo, 2013)
2.2. La mesure de la demande chimique en
oxygène
La charge organique globale des échantillons est
déterminée par la Demande Chimique en Oxygène (DCO). La
DCO mesure le caractère réducteur de l'échantillon, en
particulier les matières organiques et aussi toutes les matières
réductrices susceptibles d'être oxydées.
La DCO est concentration exprimée en mg d'O2 / L,
équivalent à la quantité d'un oxydant chimique
(dichromate) consommée par les matières dissoutes et en
suspension lorsqu'on traite un échantillon d'eau avec cet oxydant.
Principe
Le principe de la méthode au dichromates de potassium
consiste à porte à l'ébullition, une prise d'essai de
l'échantillon, en milieu acide, en présence d'une quantité
connue de dichromate de potassium ; de sulfate d'argent joue le rôle d'un
catalyseur d'oxydation et de sulfate de mercure (II) permettant de complexer
les ions chlorures. L'excès de dichromate est dosé par
spectrophotométrie (absorbance 600 nm). La DCO est calculée
à partir de la courbe d'étalonnage.
Mode opératoire
Pour la réalisation pratique, le minéralisateur
a été placé sous la hotte d'aspiration et mis en marche
à 150°C au moins une heure de temps avant la minéralisation.
Ensuite la prise d'essai (étalon, blanc, contrôle ou
l'échantillon), la solution de minéralisation et le
réactif d'acide sulfurique ont été introduits dans les
tubes de minéralisation. Ces tubes ont été portés
à 150°C pendant deux heures (figure n°10). Après
refroidissement à la température ambiante,
l'absorbance des échantillons minéralisés
ont été mesurés à l'aide d'un
spectrophotomètre type DR/3800 à 600 nm (figure n°9).

21
Figure n°9 : photo du
spectrophotomètre Figure n°10 : photo du
minéralisateur DCO
(Sawadogo, 2013)
2.3. La mesure des matières en suspension
Principe
Le dosage des matières en suspension des eaux
usées a été réalisé par un Séchage
à 105°C #177; 2°C et pesée conformément à
la Norme Française NF 90-105-2. (1997).
Mode opératoire
Les échantillons destinés à l'analyse des
MES ont été au préalable bien
homogénéisés avant leur répartition dans des tubes
de 100 mL. Ces tubes ont été ensuite placés dans une
centrifugeuse à 5000 tr/min pendant 20 min (figure n°11).
Après la centrifugation, les culots retenus au fond des tubes ont
été récupérés par rinçage à
l'aide d'une pissette d'eau distillée, dans des coupoles de masse connue
(M0). Ses culots récupérés ont été
séchés dans un dessiccateur à 105°C #177; 2°C
pendant 06 heures. La masse des MES s'obtient par la différence entre M0
et M1.

22
Figure n°11 : photo de la
Centrifugeuse (Sawadogo, 2013)
Expression des résultats
La teneur en matières en suspensions est donnée par
l'équation suivante :
Où :
ñ : est la teneur en matière en
suspension, en milligrammes par litre ;
V : est le volume en millilitres de la prise
d'essai ;
M0 : est la masse en milligrammes de la capsule
à vide ;
M1 : est la masse en milligrammes de la capsule
et son contenu après séchage à 105°C.
3. Les nitrates (NO3 -)
Principe
Le cadmium présent dans la gélule réduit le
nitrate dans l'échantillon en nitrite. L'ion nitrite réagit avec
l'acide sulfanilique pour former un sel de diazonium intermédiaire. Ce
sel réagit avec l'acide gentisique pour former un complexe coloré
ambre. La lecture est obtenue à 500
nm.
Mode opératoire
Les nitrates ont été dosés par la
méthode colorimétrique de reduction au cadnium en utilisant le
Nitraver5 comme réactif. Les nitrates contenus dans 10 mL
d'échantillon réagissent avec une gélule du réactif
(le cadmium) pour donner une couleur ambre. La concentration de
23
nitrates (mg/L) a été lue à l'aide d'un
spectrophotomètre de type DR3800 à une longueur d'onde de 500
nm.
4. Les orthophosphates (PO43-)
Principe
Le dosage des orthophosphates (o-P) par
spectrophotométrie d'absorption moléculaire est fondé sur
la formation, en milieu acide et en présence de molybdate d'ammonium,
d'un complexe phosphomolybdique qui développe une coloration bleue
lorsqu'il est réduit par l'acide ascorbique.
Mode opératoire
Les orthophosphates ont été dosés par la
méthode colorimétrique au molybdovanadate. Les orthophosphates
contenus dans 10 mL d'échantillon réagissent avec le molybdate
présent dans la gélule pour former un complexe mixte
phosphate/molybdate. Ensuite, l'acide ascorbique réduit le complexe,
provoquant une forte coloration bleue de molybdène. Enfin cette
coloration qui a été lue à l'aide d'un
spectrophotomètre de type DR3800 à une longueur d'onde de 880 nm
et il affiche directement la concentration en orthophosphates en mg/L.
24
RESULTATS ET DISCUSSION
1. Les caractéristiques de l'effluent brut
Les valeurs de la DCO et de DBO5 (Tableau III & IV)
traduisent une bonne élimination des paramètres
épuratoires. Mais il y a une forte variabilité de la
qualité de l'effluent admis à la tête de la station avec
des valeurs de pH qui évoluent de [6,4 ; 10,8] ; ce qui est de nature
à favoriser le développement de la flore bactérienne
nécessaire à la dégradation biologique des polluants
organiques.
Tableau II : variation des valeurs de
DCO dans le temps
|
Paramètres
|
Concentration
|
05-Sept
|
13-Sept
|
20-Sept
|
27-Sept
|
Moyenne
|
|
DCO Entrée
|
mg/L
|
2404
|
901,06
|
5758,2
|
1609
|
2668,07
|
|
DCO Sortie
|
mg/L
|
456,5
|
466,2
|
155
|
297
|
343,68
|
|
|
|
|
|
|
|
|
|
04-Oct
|
11-Oct
|
18-Oct
|
25-Oct
|
Moyenne
|
|
DCO Entrée
|
mg/L
|
4961
|
2791
|
3321
|
1566
|
3159,75
|
|
DCO Sortie
|
mg/L
|
559
|
835
|
1375
|
402
|
792,75
|
|
|
|
|
|
|
|
|
|
08-Nov
|
15-Nov
|
22-Nov
|
29-Nov
|
Moyenne
|
|
DCO Entrée
|
mg/L
|
992
|
1270
|
2418
|
1533
|
1553,25
|
|
DCO Sortie
|
mg/L
|
506
|
490
|
588
|
671
|
563,75
|
Le tableau IV présente les concentrations moyennes
mensuelles de la DBO5 enregistrées au cours de notre
expérience.
Tableau III : variation des valeurs de
DBO5 dans le temps
|
Paramètres
|
Concentration
|
05-Sept
|
13-Sept
|
20-Sept
|
27-Sept
|
Moyenne
|
|
DBO5 Entrée
|
mg/L
|
1500
|
1400
|
2000
|
500
|
1350
|
|
DBO5 Sortie
|
mg/L
|
80
|
70
|
80
|
67,5
|
74,38
|
|
|
|
|
|
|
|
|
|
04-Oct
|
11-Oct
|
18-Oct
|
25-Oct
|
Moyenne
|
|
DBO5 Entrée
|
mg/L
|
2275
|
1400
|
800
|
1000
|
1368,75
|
|
DBO5 Sortie
|
mg/L
|
60
|
280
|
113
|
120
|
143,25
|
|
|
|
|
|
|
|
|
|
08-Nov
|
15-Nov
|
22-Nov
|
29-Nov
|
Moyenne
|
|
DBO5 Entrée
|
mg/L
|
500
|
600
|
800
|
900
|
700
|
|
DBO5 Sortie
|
mg/L
|
75
|
45
|
26,3
|
140
|
71,58
|
25
Le tableau V illustre les différentes concentrations
moyennes mensuelles des matière en suspension mesurées.
Tableau IV : variation des valeurs des
MES dans le temps
|
Paramètres
|
Concentration
|
05-Sept
|
13-Sept
|
20-Sept
|
27-Sept
|
Moyenne
|
|
MES Entrée
|
mg/L
|
467
|
268
|
5082
|
200
|
1504,25
|
|
MES Sortie
|
mg/L
|
130
|
137
|
56
|
350
|
168,25
|
|
|
|
|
|
|
|
|
|
04-Oct
|
11-Oct
|
18-Oct
|
25-Oct
|
Moyenne
|
|
MES Entrée
|
mg/L
|
329
|
231
|
253
|
175
|
247
|
|
MES Sortie
|
mg/L
|
128
|
243
|
236
|
207
|
203,5
|
|
|
|
|
|
|
|
|
|
08-Nov
|
15-Nov
|
22-Nov
|
29-Nov
|
Moyenne
|
|
MES Entrée
|
mg/L
|
260
|
160
|
427
|
295
|
285,5
|
|
MES Sortie
|
mg/L
|
231
|
175
|
268
|
87
|
190,25
|
2. Les rendements épuratoires
2.1. L'élimination de la charge organique 2.1.1.
La demande chimique en oxygène
Les résultats obtenus ont permis de construire ces
figures pour distinguer la variation du paramètre (DCO).
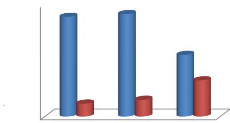
La figure n°12 présente les variations moyennes
mensuelles de la concentration de DCO des eaux brutes et les eaux
traitées, où on observe une diminution nette entre l'effluent
brut et l'effluent traité avec une valeur minimale à la sortie de
343,68 mg/L contre une valeur maximale équivalent à 2739,6 mg/L
à l'entrée. Mais cette valeur minimale reste toujours
supérieure à la norme de l'OMS (150 mg/L). Ce qui pourrait
s'expliquer par une forte accumulation de la matière organique à
l'entrée de la station.
DCO
1647,67
966
446,6
2666,07 2739,6
343,68
0
3000
Concentration (mg/L)
2500
2000
1500
1000
500
Septembre Octobre Novembre Période
DCO Entrée mg/L DCO Sortie mg/L
26
Figure n°12: Variation moyenne
mensuelle de la DCO des eaux brutes et traitées dans le
temps
Taux d'abattement de chaque unité :
Le calcul du taux d'abattement d'un élément (x)
exprimé en % est basé sur la formule suivante :
% d'abattement (x) = [(Ci - Cf)/Ci] x100 avec
Ci : concentration initiale de (x) de l'eau
usée brute
Cf : concentration finale de (x) de l'eau
usée traité
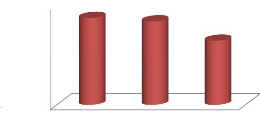
La figure 13 présente une bonne élimination de
la DCO au cours de notre expérience avec des rendements moyens qui
varient entre 64,29% et 84, 11%. Ces résultats sont similaires à
ceux obtenus par Piétrasanta et Bondon en 1994 (80 % et 90%). Cet
important taux d'abattement de DCO est dû à la dégradation
des matières organiques dissout dans l'eau usée par la flore
bactérienne dénitrifiantes.
DCO
64,29
0,00
Taux d'abattement (%)
87,11 83,70
100,00
80,00
60,00
40,00
20,00
Septembre Octobre Novembre
Période
DCO %
27
Figure n°13: Taux d'abattement de la
DCO dans le temps 2.1.2. La demande biochimique en
oxygène
La figure n°14 montre les variations moyennes mensuelles
de la concentration en DBO5 des eaux brutes et des eaux traitées avec
une baisse considérable de la charge entre l'entrée et la sortie.
Malgré cette baisse, la concentration minimale en DBO5 (71,53 mg/L)
demeure légèrement supérieure à la norme
burkinabè de rejet des eaux usées dans les eaux de surfaces qui
fixe la limite à 50 mg/L selon le DECRET n°2001-185 /
PRES/PM/MEE portant fixation des normes de rejet des polluants dans
l'air, l'eau et le sol. Ceci pourrait s'expliquer par l'absence ou une mauvaise
application du système de traitement en amont de la station.
DBO5

1350 1275
700
74,38 81 71,53
0
1400
Concentration(mg/L)
1200
1000
800
600
400
200
Septembre Octobre Novembre Période
DBO5 Entrée mg/L DBO5 Sortie mg/L
Figure n°14: Variation moyenne
mensuelle de la DBO5 des eaux brutes et traitées dans le temps
28
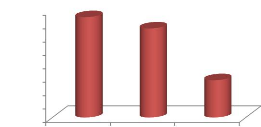
Les valeurs de rendement de DBO5 au cours de la durée
de notre expérience (figure n°15) varient d'un mois à
l'autre où elles atteignent leur maximum au mois de Septembre à
94,49 %, comparable à celui de Maïga en 2006 (95%). Ce qui montre
l'efficacité de la station en matière d'élimination de la
charge organique biodégradable. La décroissance du taux de
rendement moyen au cours de notre expérience pourrait s'expliquer par
des variations du pH et de la température.
DBO5
94,49
95,00
Taux d'abattement (%)
94,00
93,00
92,00
91,00
90,00
89,00
88,00
87,00
93,65
89,78
Septembre Octobre Novembre
Période
DBO5 %
Figure n°15: Taux d'abattement de la
DBO5 dans le temps
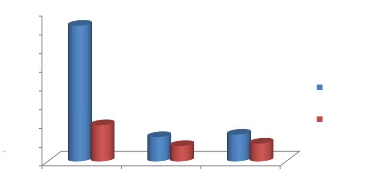
2.1.3. Les matières en suspensions
Les valeurs des MES diminuent de l'amont vers l'aval de la
station. On observe une très forte concentration moyenne des MES des
eaux brutes pendant le mois de Septembre par rapport aux mois ultérieurs
de notre étude (figure n°16). Par contre, les concentrations
moyennes des MES de la sortie enregistrée pendant le mois d'Octobre et
de Novembre sont conformes aux normes (200 mg/L) de l'OMS (1989). Cette
fluctuation pourrait s'expliquer par une augmentation des déchets dans
la station que peut occasionner la saison hivernale.
Septembre Octobre Novembre
Période
1448,25
385,75
259,00 285,5
164,2 190,25
200
Concentration(mg/L)
0
400
600
800
1000
1200
1400
1600
MES
MES Entrée mg/L
MES Sortie mg/L
Figure n°16: Variation moyenne
mensuelle de la MES des eaux brutes et traitées dans le temps
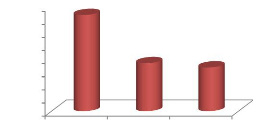
La variation des rendements moyens mensuels des MES (figure
n°17) est en fonction de certains facteurs (la charge organiques des
effluents, climat, saison etc.)
L'augmentation de la charge des MES ne représente pas une
pollution en soi, tant que le milieu récepteur est assez grand.
MES
Septembre Octobre Novembre
Taux d'abattement (%)
40,00
80,00
70,00
60,00
50,00
30,00
20,00
10,00
0,00
73,36
36,60 33,36
Période
MES %
29
Figure n°17 : Taux d'abattement des
MES dans le temps
30
2.2. L'élimination des nutriments 2.2.1.
L'élimination de NO3 -
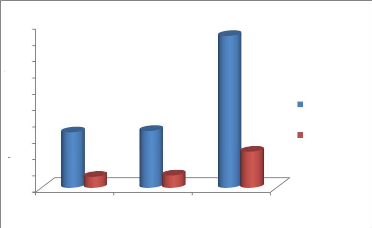
Durant notre expérience, les eaux brutes dont recevait
la station était faiblement chargée en nitrates. On note une
concentration moyenne maximale de 18,63 mg/L (eau brute) au cours du mois de
Novembre (figure n°18). Les valeurs ainsi trouvées après le
traitement à la lagune sont largement inférieures à celle
de la norme burkinabè de rejet des eaux usées dans les eaux de
surfaces qui fixe la limite à 50 mg/L selon le DECRET
n°2001-185 / PRES/PM/MEE portant fixation des normes de rejet des
polluants dans l'air, l'eau et le sol.
NITRATES
6,8 6,98
4,43
1,52
Septembre Octobre Novembre
Période
18,63
1,35
20
18
16
14
12
10
8
6
4
Conncentration (mg/L)
2
0
Nitrates Entrée mg/L
Nitrates Sortie mg/L
Figure n°18: Variation moyenne
mensuelle des Nitrates des eaux brutes et traitées dans le
temps
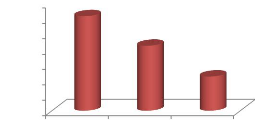
La figure n°19 présente une bonne
élimination des nitrates où les rendements varient entre 76,22%
et 80,15%. L'élimination des nitrates en particulier et de l'azote en
général est due d'abord à la décantation des
matières en suspension dans les bassins anaérobies ensuite
à la volatilisation et enfin à l'assimilation par les
micro-algues.
NITRATES
81,00
Taux d'abattement (%)
80,00
79,00
78,00
77,00
76,00
75,00
74,00
80,15
78,22
76,22
Septembre Octobre Novembre
Période
Nitrates %
31
Figure n°19: Taux d'abattement des
Nitrates dans le temps 2.2.2. L'élimination des orthophosphates
(PO43-)
La figure n°20 présente les variations des
concentrations moyennes mensuelles des orthophosphates des eaux brutes et
traitées. On observe une forte concentration moyenne des eaux
épurées enregistrées au cours du mois de Novembre (30,58
mg/L) par rapport aux autres mois, celle-ci dépasse la valeur moyenne
à l'entrée (24,11 mg/L). Cela induit une production
d'orthophosphates au cours traitement. De même, toutes les valeurs
obtenues après le traitement sont largement supérieures à
la limite tolérable (5 mg/L) proposée par l'OMS (1989).
1122Concentration (mg/L)
35
30
0
0
0
5
5
5
Septembre Octobre Novembre
31,59
6,69 6,26
Orthophosphates
30,58
Période
15,6
24,11
Orthophosphates Entrée mg/L
Orthophosphates Sortie mg/L
Figure n°20: Variation moyenne
mensuelle des Orthophosphates des eaux brutes et traitées dans le
temps
32
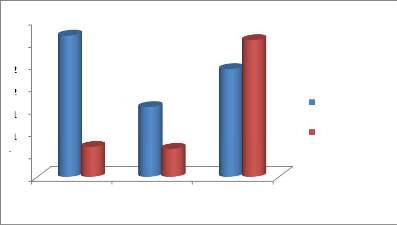
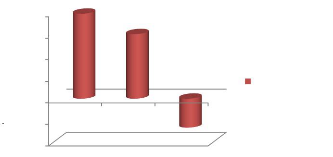
La figure n°21 montre les variations de rendements moyens
des orthophosphates enregistrés au cours de notre expérience. On
observe une diminution progressive du taux moyen des rendements mensuels. Le
mois de Novembre fait une exception puisqu'il enregistre un rendement moyen
négatif (-26,84%).
Orthophosphates
Periode
78,82
59,87
Septembre Octobre Novembre
-26,84
Orthophosphates %
80,00
taux d'abattement (%)
60,00
40,00
20,00
0,00
-20,00
-40,00
Figure n°21 : Taux d'abattement des
Orthophosphates dans le temps 3. L'évaluation de
l'efficacité du traitement
Les rendements moyens d'abattement de la pollution sur la
période de suivi sont de 92,64 % pour la DBO5, 70,73 % pour la DCO et
47,78 % pour les MES (tableau II). Excepté le rendement moyen des MES,
ces résultats sont comparables aux travaux de Kiemdé en 2009. De
même le rendement moyen mensuel de la DBO5 se rapproche aux normes de
l'OMS applicable au Burkina Faso (95% à 99%). Au vu des résultats
nous déduisons que la STEP présente un abattement global
satisfaisant.
Tableau V : les performances de la STEP
de Kossodo
|
Paramètres
|
Septembre
|
Octobre
|
Novembre
|
Moyenne
|
|
Rendement (%)
|
|
MES
|
73,36
|
36,6
|
33,36
|
47,78
|
|
DCO
|
87,11
|
83,7
|
41,37
|
70,73
|
|
DOB5
|
94,49
|
93,65
|
89,77
|
92,64
|
33
CONCLUSION ET RECOMMANDATIONS
A travers ce travail, nous avons tenté d'étudier
les performances épuratoires de la station d'épuration de la
ville de Ouagadougou par un suivi des paramètres globaux de pollution
tel que (DBO5, DCO, MES).
Il ressort des mesures et des analyses
réalisées, une forte variation des paramètres
physicochimiques des effluents bruts à l'entrée de la station
d'épuration. Ces variations qui sont la conséquence du manque de
maîtrise du traitement en amont, reposent sur la difficulté
d'obtenir un échantillonnage correct des effluents bruts lors des
mesures de suivi de la STEP. Concomitamment, les variations des
paramètres atmosphériques, influent sur les processus en cours
dans les bassins. En conséquence, les résultats obtenus sont
fonctions de l'échantillonnage et des périodes de mesure.
Les abattements moyens constatés à la sortie de
la STEP pour la pollution carbonée sont relativement
élevés : DBO5 : 92,64% ; DCO : 70,73 % ; MES : 47,78 %. Ces
niveaux d'abattement traduisent ainsi un bon niveau d'épuration entre
l'entrée des effluents en tête des lagunes et la sortie de la
STEP. Ces performances épuratoires sont assez bonnes pou l'ensemble de
la STEP, mais cela suscite cependant des observations et des recommandations,
qui pourront améliorer le suivi du fonctionnement du système.
A partir de cette étude, nous recommandons :
+ un suivi plus rapproché des paramètres
physico-chimiques des effluents bruts soit une nécessité, car
pouvant expliquer le déroulement des processus dans les
différents bassins ;
+ Résoudre le problème de prolifération
intensive des algues pour augmenter les rendements d'abattement des MES ;
+ Un suivi concomitant et rapproché des effluents
industriels permettra la vérification stricte du respect des normes
d'admission des effluents dans le réseau d'égouts.
Dans le but d'un suivi scientifique du comportement de la
STEP, il est préconisé, l'aménagement sur le site du
lagunage d'un domaine réservé à vocation
pédagogique et de recherche, destiné aux différentes
expérimentations.
34
REFERENCES BIBLIOGRAPHIQUES
Association Française de Normalisation (AFNOR).
1997, Qualité de l'eau, tome 1, Terminologie,
échantillonnage et évaluation des méthodes. 376p. ISBN
2-12-179020-9.
Agences de bassins, 1979. Lagunage naturel et
lagunage aéré : procédés d'épuration des
petites collectivités, CTGREF d'Aix en Provence. 16p.
Apha., 1985. Les méthodes standards
pour l'analyse de l'eau et des eaux usées. American Public Health
Association, Washington, DC. 1268 p.
BCEOM, 1990. Application de
procédé de lagunage naturel au traitement des eaux usées
domestiques des collectivités de petites à moyenne importance.
Rapport, Paris. 36p.
Charbonnel, Y. et Simo, A., 1986.
Procédé et systèmes de traitement biologiques
d'eaux résiduaires. Université de Yaoundé, Brevet OAPI
n° 8320. 11p.
Décret N°2001-185 / PRES/PM/MEE
portant fixation des normes de rejet des polluants dans l'air, l'eau
et le sol au Burkina Faso.
Deronzier G., 2001. Les
procédés extensifs d'épuration des eaux usées
adaptées aux petites et moyennes collectivités. 44 p.
Drapeau A. J. et Jankovic., 1977. «
Manuel de microbiologie de l'environnement », Organisation Mondiale de la
santé, Genève.22-34p.
Deronzier G., Schétrite S., Racault Y., Canler
J.P., Liénard A., Héduit A. et Duchène P., 2001.
Traitement de l'azote dans les stations d'épurations
biologiques des petites collectivités. Document technique FNDAE
n°25. 2ème édition, Cemagref éditions,
Antony. 30p. ISBN 2-285362-555-9.
Gorse F., 2008. La filière
assainissement. n°08, 27p.
Guerrin F., 1981. Etude physico-chimique du
lagunage de Réalmont (Trn), Agence de Bassin Adour - Garonne,
74p.
Kiemdé W. H., 2006. Épuration
des eaux usées par lagunage à grande échelle sous climat
sahélien : bilan de la station de lagunage de la ville de Ouagadougou
à Kossodo après un an
35
de fonctionnement et perspectives d'avenir. Université de
Ouagadougou. Burkina Faso. 130
p.
Koné D., 2002. Épuration des
eaux usées par lagunage à microphytes et à macrophytes en
Afrique de l'ouest et du centre : état des lieux, performances
épuratoires et critères de dimensionnement. Thèse de
Doctorat ès Sciences et Techniques dans les domaines de Sciences et
Ingénierie de l'Environnement. N° 2653 - EPFL (Suisse).193 p.
Organisation Mondial de la Santé (OMS), 1989.
L'utilisation des eaux usées en agriculture et en aquaculture :
recommandations à visées sanitaires. Rapport technique n°
778, Genève. 84 p.
Mara et Pearson., 1998. design Manuel for
waste stabilization ponds in Mediterranean countries. Lagoon International
Technology Ltd., leeds. 112p.
Norme Française 90-105-2., 1996:
Qualité de l'eau- Dosage des matières en
suspension-Méthode par centrifugation. ISO 6107-2. 6-8p.
Perera P. et Baudot B., 2001.
Procédés extensifs d'épuration des eaux
usées. Office international de l'eau.
Piétrasanta Y. et Bondon D., 1994. Le
lagunage écologique. Ed.Economica, Paris, 11p
Radoux M., 1989. Epuration des eaux
usées par Hydrosère reconstituée. Tribune de l'eau 42(8):
62-68p.
Rodier J., 1996. L'analyse de l'eau : Eau
naturelles, eaux résiduelles, eaux de mer. 8ème édition,
Paris, 1384 p.
Salembéré C.A., 2009. Epuration
des eaux usées de Kossodo : analyse des performances épuratoires
de la STEP de Kossodo et analyse des impacts socio-économiques et
sanitaires des maraîchers. Mémoire pour l'obtention du master
d'ingénierie en eau et environnement. 2iE, Ouagadougou. 12p.
Satin M. et Selmi B., 1999. Guide technique de
l'assainissement. 2ème édition. 680p.
Site internet :
-http//
www.univ-lehavre.fr/cybernat/pages/lagunat
-
http://www.oieau.org
36
ANNEXE 1 : DONNEES TECHNIQUES DE LA STATION D'EPURATION
DE KOSSODO
1. Composition
y' 08 bassins de lagunage :
1er étage : 03 bassins anaérobies en
parallèle ; 2è étage : 02 bassins facultatifs en
parallèle ; 3è étage : 03 bassins de maturation en
série ; y' 28 lits de 95 m2 chacun soit 2660 m2
y' 01 laboratoire ;
y' 02 bâtiments administratifs ; y' et des latrines;
2. Dimension
y' 13 hectares de superficie nette y' Volume total : 180 000
m3
|
Désignation
|
Dimensions (LXl)
|
Profondeur(M)
|
Volume (m 3)
|
|
Fond
|
Crète
|
Bassin
|
Eau
|
Bassin
|
Eau
|
|
Bassins anaérorobies
|
88,50 mx19 m
|
108mx37, 80m
|
4,70m
|
4,00m
|
|
18
600
|
|
Bassins facultatifs
|
287,50mx94m
|
298,50mx107m
|
2,50m
|
1,80m
|
|
103
000
|
|
Bassins de maturationN°1
|
202mx62m
|
217mx74, 5m
|
2,7m
|
1,20m
|
|
27
000
|
|
Bassins dematurationN°2
|
142mx42m
|
156,5mx54, 5m
|
2,7m
|
1,20m
|
|
6 850
|
|
Bassins de maturationN°3
|
142mx42m
|
155mx54m
|
2,7m
|
1,20m
|
|
6 850
|
|
Lits de séchage
|
3,80mx25m
|
3,80mx25m
|
0,70m
|
0,40m
|
66,50
|
38,00
|
37
Les normes présentées ci-dessous proviennent du
décret N°2001-185 PRES/PM/MEE portant fixation des normes de rejets
de polluants dans l'air, l'eau et le sol
|
Normes de déversement des eaux usées dans
les égouts
|
|
Paramètres
|
Valeurs limites (mg/L)
|
|
DCO
|
2000
|
|
DBO5
|
800
|
|
Nitrates
|
90
|
|
Phosphates
|
50
|
|
Sulfates
|
600
|
|
MES
|
1000
|
|
pH
|
6.4 - 10.5
|
|
Normes de déversement des eaux usées dans
les eaux de surface
|
|
Paramètres
|
Valeurs limites (mg/L)
|
|
DCO
|
150
|
|
DBO5
|
50
|
|
Nitrates
|
50
|
|
Phosphates
|
5
|
|
Sulfates
|
600
|
|
MES
|
100
|
|
pH
|
6.4 - 10.5
|
ANNEXE 2 : SITUATION GEOGRAPHIQUE DE LA STEP
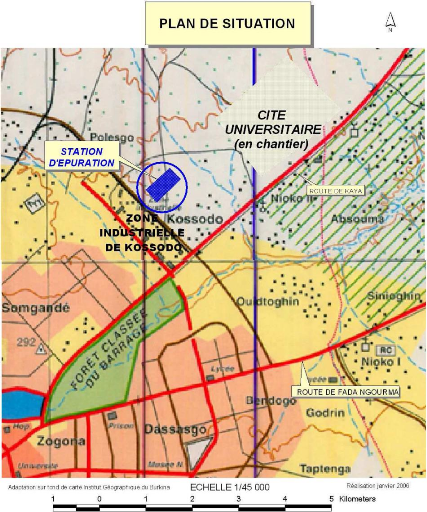
38
Source : ONEA , 2004
| 


