|
UNIVERSITE DE KINSHASA

FACULTE DE MEDECINE
ETUDE
DIAGNOSTIQUE DE L 'HYPERTROPHIE VENTRICULAIRE GAUCHE A L'ELECTROCARDIOGRAPHIE, A
LA RADIOGRAPHIE ET A L 'ECHOCARDIOGRAPHIE CHEZ
LES PATIENTS HYPERTENDUS DE KINSHASA
Par
MALONGA MUNAMA JACQUES A.
Docteur en Médecine
Travail présenté
pour l'obtention
du grade de
spécialiste en Radiologie.
Décembre 2002
DEDICACE
Je dédie ce travail
A mon créateur, le Dieu Tout Puissant
A ma chère et tendre épouse, Docteur Claudine
MOMA KASONGO, pour sa complicité active et sa foi inébranlable
dans l'accomplissement de cette oeuvre.
A mes enfants Louange MALONGA MOMA, Jacques MALONGA KWA
NZAMBI, Elie MALONGA : sachez qu'ici bas toute marche selon la
volonté divine s'accompagne toujours de sa récompense quel que
soit l'obstacle à franchir.
A mon feu père Victor MALONGA MANSANGU et à ma
mère Georgine NZUZI NGOMA, pour tant d'amour et encouragement dans
l'accomplissement de cet édifice.
A mes frères et soeurs de sang et d'alliance, ce
travail est également le votre.
REMERCIEMENTS
Au terme de ce modeste travail, nous tenons à remercier
toutes les personnes morales et physiques qui ont contribuée à
notre formation et à la réalisation de ce mémoire.
Nos remerciements s'adressent particulièrement au
professeur B. LONGO, promoteur de ce travail qui nous a guidé avec une
attention pédagogique particulière.
Notre gratitude va aussi à l'endroit du professeur E.
KINTOKI, co-promoteur de ce travail qui nous a entouré d'un encadrement
pratique en échocardiographie et électrocardiographie tout au
long de ce cheminement.
Nous remercions également le professeur S. MBENDI, Chef
de Département de Médecine Interne, qui nous a ouvert les portes
de son département.
Nous remercions le professeur P. MALENGA , Chef de
service de Radiologie pour nous avoir accueilli avec bienveillance dans son
service et pour nous avoir guidé avec rigueur scientifique et
compétence dans l'apprentissage radiologique.
Nous remercions les professeurs Z. KASHONGWE, T. ODIO , J.M.
KAYEMBE, M. LUTETE, J.M. MBUYI, N. NSEKA ,J.R. MBUYAMBA et SHIKU pour
tout encadrement réçu d'eux.
Au Doyen de la Faculté de Médecine, le
professeur S. LUFUMA ainsi qu'à tous les professeurs de la
faculté de médecine, pour leur précieux encadrement tant
durant notre formation de médecine générale que lors de
notre spécialisation. Le profond respect que nous leur devons est celui
réservé aux maîtres.
Nous remercions également tous les Chefs des travaux de
notre département et en particulier ceux de la radiologie pour leur
encadrement soutenu. Notre gratitude va à l'endroit des Docteurs J.M.
KABEYA , M. LELO, E. NDOMA , A. MOLUA, M. MANSO et J.M. KAMBANGU, qu'ils
trouvent ici notre profonde reconnaissance.
Nous remercions aussi les médecins radiologistes P.
ELOKO, J. MAMUENI, J. MAYAMA et B. NTUMBA qui nous avaient largement
encadré au sein de ce service de Radiologie.
A tous nos collègues assistants, nous disons merci pour
le précieux soutien et moment passé ensemble, votre esprit de
franche collaboration et du renouveau sera toujours contributif au
progrès.
Nous remercions tous les agents du Département de
Médecine Interne et en particulier ceux de la Radiologie, le personnel
soignant et du service informatique de LOMO-MEDICAL de LIMETE, ainsi que
mademoiselle J. MALONGA et messieurs D. BEYA et B. SIMBI pour leur
contribution dans l'élaboration de ce travail.
Des remerciements particuliers sont adressés à
Monseigneur RUNIGA, au père H. FARCY, aux soeurs M. RHEINDEL, J.BROCQUET
du diocèse de MAHAGI, ainsi qu'aux messieurs A..KINGO , H. BILAM et au
Docteur A. MANGBELE pour leur apport logistique ayant conduit à
l'accomplissement de cette oeuvre.
Nos remerciements sont aussi adressés aux familles
Dr.T.NGOY, Dr.G.MAYALA, Dr. H. SESE , Dr. H. MBANDU, Dr. J. NKOY , F.
BOTSWALI, F.FANY, A. NSILULU, B. NZABANI et I. MUTABA pour leur précieux
soutien.
Merci à tous nos frères, soeurs et amis, qui de
loin ou de près d'une manière ou d'une autre, nous ont
apporté leur assistance.
A vous tous qui avez accepté d'endosser des
irradiations pour l'accomplissement de ce travail, nous disons une fois de plus
merci. Ce travail est aussi le votre.
INTRODUCTION
Si hier l'hypertension artérielle (HTA) était
une affection rare en Afrique noire (1), elle constitue aujourd'hui un
réel problème de santé publique (2,3).
L'hypertension artérielle constitue 29 à 44 %
des hospitalisations cardio-vasculaires et un sur cinq malades vus en
consultation cardiologique à Yaoundé (4). La place de l'HTA et
de ses complications a déjà été soulignée
dans la morbi-mortalité aux Cliniques Universitaires de Kinshasa (5) .
Les principales complications de l'HTA sont les accidents vasculaires
cérébraux (AVC), l'insuffisance cardiaque, l'insuffisance
coronaire, l'insuffisance rénale chronique et l'artérite des
membres inférieures.
L'hypertrophie ventriculaire gauche (HVG)
considérée par certains comme une adaptation morpho-fonctionnelle
de réponse à l'HTA (6), est pour la majorité des
chercheurs, une complication fréquente et une conséquence de
l'HTA (7).
Sa prévalence chez l'hypertendu varie avec la
méthode utilisée, depuis la plus ancienne tel que
l'électrocardiogramme (ECG) jusqu'aux plus récentes et
sophistiquées comme la Tomodensitométrie computarisée (CT
Scanner) et l'Imagerie par Résonance magnétique (IRM) en passant
par la radiographie de face et par l'échocardiographie.
En dépit de nombreuses publications relatives à
l'HVG et au risque cardio-vasculaire dans les pays développés
et en Afrique noire (8,9), aucune étude congolaise n'est encore
consacrée à la valeur du pronostic et à la
validité de méthodes diagnostiques de l'HVG chez l'hypertendu.
Cette lacune est liée à l'insuffisance des ressources
financières pour équiper la plupart des centres de santé
d'au moins un électrocardiographe, d'un équipement de radiologie
et d'un échocardiographe.
Il ne faut pas non plus négliger les difficultés
de l'analyse et de comparaison des données fournies par ces trois
méthodes diagnostiques de l'HVG.
En ce qui concerne l'ECG, le diagnostic évocateur d'HVG
porte sur des signes d'hypervoltage des complexes QRS ou la somme des
amplitudes des ondes R+S (10). Si sa spécificité est en
général très bonne (85% à 98 %), sa
sensibilité est en revanche médiocre (20% à 50 %)
(11-18).
Chez l'enfant (19), l'index cardio-thoracique (ICT) n'est pas
correllé aux données échocardiographiques.
Chez les patients Allemands, la sensibilité et la
spécificité de l'ICT dans l'évaluation de l'HVG sont
respectivement de 48,8 % et de 93,6 %, l'échocardiographie étant
le test de référence (20).
Contrairement à l'ECG qui montre une faible
prévalence (moins de 5 %) d'HVG dans une population d'hypertendus
modérés (11), l'échocardiographie bidimensionnelle (2D) et
temps-mouvement (TM) évaluent cette prévalence à des taux
de 30 à 60 % (21-23).
En effet, l'échocardiographie dans des mains expertes
atteint une grande sensibilité (93%) et une grande
spécificité (95%) ( 24).
La géométrie ventriculaire gauche distingue le
ventricule gauche normal, le remodelage ventriculaire concentrique, des
hypertrophies ventriculaires concentrique ou excentrique selon l'indice de
masse ventriculaire gauche (IMVG) et de l'épaisseur pariétale
relative (24).
La faisabilité de ce trois méthodes
diagnostiques diminuent avec l'âge et l'obésité (24).
L'obésité elle-même, ensemble avec la race, le sexe et le
sport, est aussi considérée comme étiologie de l'HVG. (6).
Le médecin spécialiste en Imagerie
médicale doit être capable de faire le tri des informations de
façon aussi rationnelle et pragmatique que possible afin de pouvoir
juger, entre autre, la rigueur de la méthodologie et, donc, la
crédibilité des résultats présentés.
L'évaluation des méthodes diagnostiques
utilisées en imagerie médicale devra tenir compte des
critères suivants :
- disposer d'une bonne qualité technique ;
- obtenir une interprétation reproductible ;
- apporter une information valide ;
- être utile à la prise de décision
médicale ;
- être efficace pour le malade et la population.
Pour répondre à toutes ces
préoccupations, la présente étude est donc
initiée.
L'objet essentiel à long terme de la présente
étude est d'envisager la pertinence du choix de la méthode
diagnostique et du seuil décisionnel dans la définition de l'HVG
chez l'hypertendu congolais et pour atteindre ce but, les objectifs
spécifiques suivants ont été
précisés :
- évaluer l'ECG et la radiographie du thorax comme
méthodes diagnostiques de l'HVG selon des critères
objectifs ;l'échocardiographie étant la méthode de
référence ;
- dégager les principales qualités susceptibles
d'être mesurées dans ces méthodes diagnostiques ;
- estimer la prévalence de l'HVG selon
l'échocardiographie ;
- enfin, proposer des seuils optimaux de l'ECG et de la
radiographie du thorax dans la définition de l' HVG.
CHAPITRE 1.
GENERALITES
1.1. METHODES
DIAGNOSTIQUES
1.1.1. Electrocardiogramme
Durant une grande partie du siècle passé,
l'electrocardiographie a représenté la principale technique
d'investigation des cardiopathies. Elle a acquis une position si sûre en
médecine clinique qu'aucun examen cardiologique ne pourrait
actuellement être considéré comme complet sans ECG.
Les ECG sont devenus si familiers que leur valeur est
considérée comme chose établie plutôt que
jugée de manière critique ; L'électrocardiogramme
n'est qu'un moyen indirect d'enregistrement de la séquence des
modifications électriques ayant lieu dans le coeur au cours de la
systole et de la diastole. Les 12 dérivations enregistrées
normalement à l'extrémité des membres et sur la paroi
thoracique fournissent simplement différents points de vue sur ces
événements.
Ainsi, les dérivations précordiales de V1
à V6 s'étendent autour de la partie gauche du thorax pour
montrer comment les changements électriques se propagent sur les
ventricules droit et gauche. On découvre d'autres aspects de
l'activité électrique cardiaque grâce aux ECG à
l'effort, pendant la vie quotidienne et au moyen de dérivations
spéciales.
Des enregistrements en série sont souvent
particulièrement utiles parce qu'ils permettent de comparer des
observations pendant des jours, des mois ou des années.
L'ECG se présente sous forme des tracés dans les
12 dérivations standards enregistrés consécutivement. La
première déflexion à partir de la ligne de base
représente les changements électriques pendant la contraction
auriculaire ; elle est suivie par le complexe QRS ou ventriculaire, le
segment ST et finalement l'onde T.
La fréquence et la régularité de ces
réflexions, leur amplitude et leur forme, leur durée et les
intervalles sont les principaux critères sur lesquels repose
l'interprétation de l'ECG.
La fréquence cardiaque et la présence ou
l'absence d'arythmies devraient être immédiatement apparentes
sur chaque tracé, quoique la nature et la cause d'une arythmie puissent
demander l'interprétation d'un spécialiste.
Lorsque le tracé présente des déflexions
inhabituelles petites dans toutes les dérivations, il peut s'agir d'un
artefact dû à une mauvaise calibration de l'enregistreur ou
à une atténuation excessive des interférences ;
pourtant des tracés d'amplitude authentiquement réduite
signifient probablement une altération globale de la conduction
électrique à partir du coeur, provoquée par un
épanchement et/ou un épaississement péricardique.
Les différences relatives d'amplitude des ondes peuvent
indiquer ce que l'on appelle une déviation de l'axe à droite ou
à gauche, c'est-à-dire une domination électrique du coeur
gauche ou du coeur droit, ce qui dénote habituellement une dilatation ou
une hypertrophie (21 ).
La figure, la durée et l'amplitude d'autres ondes, et
les intervalles entre elles, permettent des conclusions quant à
l'état du système de conduction et du myocarde -
particulièrement la présence ou l'absence d'ischémie - et
les effets de certains médicaments, digitale.
Bref, l'ECG peut donner des informations sur la
fréquence cardiaque, le rythme, l'équilibre entre coeur gauche
et droit, l'état du péricarde, le système de conduction et
le myocarde, ainsi que les signes d'ischémie et d'effets
médicamenteux.
L'ECG ne fournit pas d'information directe sur des atteintes
valvulaires, une athérosclérose coronarienne ou une
hypertension à moins que ces troubles potentiellement sérieux ne
provoquent déjà une déviation axiale ou ne fassent
apparaître des indices ECG d'ischémie ou d'insuffisance du
myocarde. En d'autres termes, on ne peut le considérer comme un
inducateur précoce des affections cardio-vasculaires responsables de
la majeure partie de la morbidité et de la mortalité.
1.1.2 Radiographie
thoracique.
Pour les affections cardio-vasculaires, la radiographie
thoracique est d'intérêt limité par comparaison à
l'ECG et d'autres examens plus spécifiques. (21)
En effet, cette méthode est rarement diagnostique.
Néanmoins, il s'agit d'un bon examen de dépistage
général : elle aide surtout à exclure des images
pathologiques à symptomatologie initiale analogue ou presque
identique.
La radiographie du thorax renseigne sur la
taille du coeur et des gros vaisseaux, et sur la vascularisation pulmonaire
artérielle et veineuse. La dilatation d'une cavité se traduit
habituellement par des modifications de la taille et des concours de la
silhouette cardiaque. A l'inverse, l'hypertrophie myocardique s'accompagne
souvent d'un épaississement pariétal, qui produit seulement une
discrète modification de la silhouette cardiaque. Elle ne permet pas de
faire de manière formelle une distinction entre une dilatation et une
hypertrophie du ventricule gauche.
1.1.3. Echocardiographie
L'échocardiographie utilise des ultrasons dont la
fréquence se situe entre 2 et 13 MHZ pour visualiser le coeur et
d'autres organes internes. Lorsqu'on a commencé à l'utiliser en
clinique dans les années 50, la technique était
unidimensionnelle ; depuis les années 70, elle est aussi
bidimensionnelle.
Les premiers échographes étaient
unidimensionnels selon l'une de trois modalités suivantes :
· le mode A, rarement utilisé aujourd'hui,
représente l'intensité de l'écho sur l'axe x de
l'oscilloscope et le temps sur l'axe y ;
· le mode B représente l'intensité de
l'écho sur l'axe z (brillance) de l'oscilloscope, et la distance du
traduction sur l'axe y ;
· le mode M présente sur l'axe x, la distance du
transducteur sur l'axe y et l'intensité de l'écho sur l'axe z.
Cette représentation est obtenue soit en faisant défiler le
signal sur l'écran de l'oscilloscope, soit en photographiant
l'écran de l'oscilloscope sur du papier en mouvement.
De nos jours, on utilise d'avantage l'échographie
bidimensionnelle. Avec cette technique, un tracé est enregistré
selon le mode B qui balaie un secteur rapidement et de manière
répétée, afin de fournir des images en temps réel.
Le balayage peut être effectué par voie mécanique ou
électronique .
La réponse de fréquence des balayeurs de secteur
n'est pas aussi bonne que celle de l'échocardiographie en mode M, mais
la possibilité de voir les mouvements du coeur en deux dimensions
représente une compensation suffisante pour la perte de
résolution.
Cette technique a révolutionné l'étude
des cardiopathies congénitales et des lésions valvulaires. Son
aptitude à visualiser la structure et la fonction du coeur la rend
idéale pour l'évaluation de l'ischémie et de l'infarctus
du myocarde. Elle permet une évaluation précise :
- des valvules cardiaques, particulièrement de la
mitrale. A cause de sa position, la valvule pulmonaire n'est pas d'une
évaluation facile ;
- des cardiopathies congénitales ou
acquises ;
- de la cinétique de la contraction ;
- de la taille relative des cavités cardiaques
individuelles. Cela peut être utile pour le diagnostic des
cardiomypathies et des anévrismes ;
- de l'épaisseur du myocarde ;
- des péricardites et des épanchements
péricardiques.
Etant donné que l'os et le gaz pulmonaire
interfèrent avec la transmission des ultrasons, seule une petite zone
du coeur est directement accessible à l'analyse.
Chez les adultes, l'accès au coeur est limité
aux endroits où il est proche des espaces intercostaux. Les ondes
sonores traversent les tissus beaucoup plus lentement que les rayons X :
leur longueur d'onde plus élevée limite la résolution.
Malgré ces limites, l'échocardiographie sous ses
diverses formes représente sans doute une très importante
méthode d'investigation non invansive.
1.2. HYPERTROPHIE
VENTRICULAIRE GAUCHE (HVG)
L'hypertrophie ventriculaire gauche est
considérée comme une conséquence de l'HTA prolongée
et les autres causes sont l'âge, l'obésité et les
sports.
On parle d'HVG échographique :
- lorsque les épaisseurs du septum interventriculaire
et de la paroi postérieure du ventricule gauche sont supérieures
à 11 mm à la fin de la diastole;
- lorsque la masse ventriculaire gauche est supérieure
ou égale à 120 gr/m2 (valeur normale : 70 + 25
gr/m2 ) en tenant compte du fait que cette masse ventriculaire est
variable chez le sujet normal en fonction du sexe, de la race et de
l'âge ;
Il existe plusieurs définitions de l'HVG
radiologique. En épidémiologie, on utilise le rapport
cardio-thoracique classique ou on calcule le volume cardiaque sur base de
radiographie de face et de profil.
Il existe plusieurs définitions de l'HVG
électrocardiographique, essentiellement basées sur les
critères de voltage selon les dérivations
considérées, mais aussi sur des critères de «
strain» (anomalies du segment ST et de l'onde T) tel que rappelés
par Odia et al (8).
Les travaux récents confirment la gravité de l'
HVG détectée à l'échocardiographie (23,25). Sa
présence multiplie par 6 le risque de mort subite de cause
cardio-vasculaire (26) lorsqu'elle se manifeste par des signes
électriques. L'HVG est responsable de coronaropathies, d'un risque
accru d'arythmies et de morts subites. Il s'agit donc d'un marqueur de risque
beaucoup plus important, même s'il ne s'agit que des petites
modifications de la dépolarisation..
Messerli (27) souligne l'augmentation très
significative de la fréquence de l'extrasystole ventriculaire lorsqu'il
existe une HVG.
L'HVG est fréquente dès les premiers stades de
l'HTA, chez les adolescents hypertendus, mais aussi dans l'HTA limite (27) et
dès le stade de l'hypertrophie auriculaire gauche à l'ECG
(28,29).
Lorsqu'il y a surcharge tensionnelle, il est essentiel que la
tension de la paroi ventriculaire augmente. La tension n'est pas seulement
fonction de la pression mais aussi du diamètre et de l'épaisseur
de la paroi. Lorsque la tension de la paroi augmente, le myocyte réagit
par l'opposition parallèle de nouvelles myofribrilles. La paroi
s'épaissit et sa tension a tendance à se normaliser.
Ce processus a une expression variable selon le
mécanisme causal : la paroi est si épaisse que sa tension
est inférieure à la normale et donc l'hypertrophie dont souffrent
les patients avec sténose aortique ne disparaît pas après
chirurgie des valvulopathies. Un hypertrophie marginale est à l'origine
d'une tension insuffisante de la paroi : on remplace la valve mais
l'hypertrophie persiste.
L'hypertrophie à donc pour but de réduire la
tension de la paroi ( 27 ).
1.3. QUALITES MESUREES PAR
UNE METHODE DIAGNOSTIQUE
On doit évaluer les examens d'imagerie selon les
critères objectifs. Cela concerne les méthodes nouvelles avant
leur diffusion, mais aussi les examens anciens. Une technique d'utilisation
courante peut se révéler inutile dans un contexte nouveau .
L'objet de la présente étude est de dégager les
principales qualités susceptibles d'être mesurées dans un
examen d'imagerie.
Ainsi cinq critères peuvent être
proposés :
- avoir une bonne qualité technique ;
- être reproductible dans son
interprétation ;
- apporter une information valide ;
- être utile à la prise de décision
médicale
- être efficace.
1.3.1. Avoir une bonne
qualité technique
La première qualité d'un examen d'imagerie
à évaluer ressort du domaine technique. Le minimum que l'on doit
exiger est que l'examen fournisse une information valable.
Le problème relève du contrôle de
qualité. La technique mesure-t-elle ce pour lequel elle est
utilisée ? Est-elle exacte (absence d'erreur systématique)
et précise (faible variabilité) ?
Montre-t-elle ce qu'elle est censée montrer ?.
L'examen est-il facile à exécuter correctement ?
1.3.2. Avoir une
interprétation
Les examens d'imageries posent le problème de
reproductibilité, de jugement et de variabilité
d'interprétation inter et intra observateurs.
La notion de concordance de réponses est importante
dans un hôpital où un même malade est examiné par
plusieurs médecins, ou lors de sa surveillance au long cours par le
même médecin.
La concordance ou la reproductibilité de lecture peut
se quantifier par le coefficient d'agrément Kappa (32,33).
1.3.3. Apporter une information
valide.
On doit mesurer objectivement la qualité de
l'information fournie par un examen d'imagerie médicale.
Dès l'examen clinique, le clinicien estime les chances
qu'à le sujet d'être atteint de la maladie M. Le rôle de
l'examen complémentaire est de modifier ces probabilités a priori
afin de pouvoir estimer, en fonction des résultats, le risque
d'être malade (valeur prédictive positive) ou de ne pas être
malade (valeur, prédictive négative).
Ces valeurs prédictives dépendent de deux
types de données : qualités intrinsèques de l'examen
(sensibilité et spécificité) et probabilité
primaire à priori, pré-test, ou prévalance de la maladie
à détecter.
On doit, en évaluation, être très
précis dans la définition du signe mis en évidence
à qui on va appliquer la procédure et, surtout, dans la
façon de déterminer si le sujet est réellement malade ou
pas (33).
1.3.3.1. Définition du signe
Le signe peut être soit une variable quantitative
continue, une mesure (ex. diamètre d'un ganglion), soit une variable
qualitative le plus souvent à deux classés (présence ou
absence d'une image). Les signes doivent être parfaitement définis
pour augmenter la concordance de mesure.
1.3.3.2. Définition des patients de l'étude.
L'étude doit être testée dans un groupe de
patients, malades et non malades, représentatif de la population cible,
c'est-à-dire de la population de patients qui sera susceptible, par la
suite de bénéficier de cet examen.
Il importe d'éviter tout biais susceptible de fausser
les estimations.
1.3.3.3. Définition des malades et des non-malades.
La valeur diagnostique d'un examen est mesurée en
comparaison avec le diagnostic réel, ou gold standard. Ce diagnostic
final peut être déterminé soit à partir d'un examen
de référence, soit, au mieux, par l'examen anatomo-pathologique
de la pièce opératoire de la biopsie. On utilise alors un
consensus de spécialistes ou, la simple évolution clinique.
Il est utile de souligner que l'examen de
référence quel qu'il soit, doit être totalement
indépendant de l'examen à évaluer et son résultat
non connu de l'expérimentateur.
De même, l'examen à évaluer ne doit pas
contribuer à la détermination du diagnostic réel.
Les résultats d'une étude sur la valeur
diagnostique d'un examen doivent être rapportés sous forme
d'indices tels que sensibilité et la spécificité. Soit un
groupe de sujets dont on sait, grâce à l'examen de
référence , que certains sont malades et d'autres pas. On
effectue sur ces sujets l'examen d'imagerie dont on veut évaluer
l'apport en informations et dont on suppose que la réponse est binaire,
ou normale.
On présente alors les résultats sous forme de
tableau à quatre cases (contingences).
La sensibilité (ou taux de vrais positifs) est la
proportion de résultats pathologiques chez les sujets malades. C `est la
probabilité que le signe soit présent chez les sujets malades.
La spécificité (ou taux de vrais
négatifs) est la proportion de résultats normaux chez les sujets
non malades. La sensibilité et la spécificité sont des
indices qui ont un avantage et un inconvénient : l'avantage est que
ces mesures sont indépendantes de la prévalence de la maladie et
peuvent donc être utilisées aussi bien pour le dépistage
(prévalence faible) que pour le diagnostic (prévalence
élevée); l'inconvénient est que ces mesures ne sont pas
utilisables en tant que telles.
Le médecin doit connaître en quoi le
résultat d'un examen modifie la probabilité d'un sujet
d'être malade. Il utilise pour sa prise de décision
médicale, les valeurs prédictives.
La valeur prédictive positive est la
probabilité qu'un sujet soit malade si l'examen est positif (le signe
est positif). La valeur prédictive négative est là
probabilité qu'un sujet soit non malade si le signe est absent.
Les valeurs prédictives dépendent de la
sensibilité, de la spécificité et de la prévalence
de la maladie.
Il est donc important de savoir que les valeurs
prédictives calculées dans une étude ne peuvent
être appliquées que dans un environnement où la
prévalence de la maladie est identique à celle de l'étude.
Ce n'est pas toujours le cas.
Comme dans toute estimation, il est souhaitable de
présenter les résultats de la sensibilité, de la
spécificité et des valeurs prédictives en indiquant leur
intervalle de confiance.
1.3.4. Etre utile à la
prise de décision.
La quatrième qualité d'un examen est son
utilité au diagnostic, à la thérapeutique et au pronostic
(32,33). Les questions suivantes doivent être posées :
Cet examen modifie-t-il le comportement médical en
termes de stratégie décisionnelle ? Remplace-t-il d'autres
examens moins performants ou plus onéreux ou vient-il s'ajouter à
la stratégie d'exploration actuelle ? a-t-il modifié le
choix thérapeutique ? va-t-il permettre de prévoir
l'évolution et formuler un pronostic ? La stratégie
optimale dépend de la fréquence de la maladie dans la population
étudiée, de la gravité et des erreurs possibles de
diagnostic et de la rationalité du décideur (36).
Là, l'étude doit prendre en compte le
coût. Son évaluation est du domaine de l'équipe
médicale.
1.3.5. Etre efficace pour le
malade et la population.
Il s'agit de la capacité à produire le maximum
de résultats sur l'état de santé du malade ou de la
population avec le minimum de coût (37,38).
On regroupe dans le coût aussi bien les aspects
financiers que les aspects de santé (probabilité infligée
au malade en cas d'exploration longue ou coûteuse, gravité d'un
incident iatrogène, « coût » de l'erreur ou
l'absence de diagnostic, arrêt de travail...).
Si on raisonne en terme uniquement monétaire, l'analyse
coût-avantage ou coût- bénéfice permet de
répondre à des questions telles que : cette procédure
vaut-elle la peine d'être entreprise ?Son objectif est-il
acceptable ?
Si par contre on raisonne en terme de rendement, l'analyse
coût-éfficacité répond à des questions
comme : quel est le meilleur moyen pour atteindre
l'objectif fixé ? Et quelle est l'utilisation la plus efficace des
ressources limitées ?
CHAPITRE 2. METHODES
2.1. NATURE ET CADRE DE
L'ETUDE
La présente étude transversale, multicentrique,
descriptive et analytique a eu comme cadre les Cliniques Universitaires de
Kinshasa (CUK) et la Clinique LOMO-MEDICAL de la ville de Kinshasa, Congo. Les
CUK sont situées sur le Mont Amba de la commune de Lemba et la Clinique
LOMO-MEDICAL sur la 4ème Rue du côté
résidentiel dans la commune de Limete.
2.2. PATIENTS
Etaient éligibles les patients hypertendus constituant
les séries consécutives prises en charge dans les deux milieux
hospitaliers respectifs, entre janvier 1999 et Mars 2002.
2.2.1. Critères
d'exclusion
Ont été exclus de la présente
étude, les patients présentant les caractéristiques
suivantes :
- histoire médicale personnelle de maladie
cardio-vasculaire et de diabète sucré ;
- présence d'obésité définie par
un indice de masse corporelle (IMC) égale ou supérieur à
30 kilogrammes/mètre-carré ;
- pratique des sports de compétition et exercice
physique vigoureux ;
- présence de grossesse ;
- mauvaise qualité technique des tracés
électrocardiographiques, du cliché radiographique de thorax et
d'échocardiogramme. Un cliché de thorax asymétrique,
réalisé en expiration était jugé de mauvaise
qualité. Un électrocardiogramme non calibré (voltage
inférieur à 10 millivolt) et plein d'artefacts était non
interprétable. L'échocardiogramme était techniquement non
réalisé devant tout thorax déformé ou plein d'air
(exemple patient emphysémateux ou asthmatique).
2.2.2. Critères
d'inclusion
Ont été finalement inclus dans la
présente étude, les patients non exclus et ayant satisfait les
critères suivants :
- avoir été de race noire, de
nationalité congolaise et âgé de 15 ans ou plus ;
- avoir présenter une HTA définie selon les
critères de JNC (39) et de l'OMS (40)
pression artérielle systolique (PAS) à 140 mmHg
et pression artérielle diastolique (PAD) » 90 mmHg.
2.3. EXAMEN CLINIQUE
Réalisé par le médecin traitant, l'examen
clinique a servi à colliger les données concernant
l'identité, le sexe, l'âge, l'anthropométrie et la
pression artérielle. Le poids corporel exprimé en kilogramme, a
été mesuré sur une balance de type pèse personne et
de marque GLAXO ( Pekin , Chine) , préalablement calibré au
début de chaque journée, chez les patients
légèrement habillés et déchaussés. Le poids
a été mesuré au 100 grammes près.
Plaçant le malade avec son dos contre une toise murale
fixée de façon verticale sur un sol dur, la partie
inférieure de l'orbite à hauteur du conduit auditif externe, la
taille a été lue jusqu'au centimètre près.
L'IMC a été obtenu en rapportant le poids en
kilogramme sur la taille en mètre-carré (39).
La pression artérielle des patients a été
mesurée après un repos de cinq minutes en position couchée
en utilisant un sphygmomanomètre automatique de marque OMRON
automatique, HEM-705 CP (Tokyo, Japon).
2.4. EVALUATION DE L'HVG
Dans la mise au point de l'HTA, l'augmentation de la masse, de
la taille et de volume du ventricule gauche (HVG) a été
évaluée par trois méthodes diagnostiques :
l'électrocardiographie, la radiographie du thorax et
l'échocardiographie.
2.4.1. Méthode
Radiologique
2.4.1.1. Appareils et matériels
Les appareils radiologiques de type Multiplanigrap de marque
Siemens (Allemagne) pour la clinique LOMO-MEDICAL et Mobile Speed (Kyoto,
Japon ) pour les Cliniques Universitaires de Kinshasa, ont été
utilisé dans la réalisation des clichés du thorax.
On avait utilisé le statif vertical, une distance
foyer-film d'au moins 180 m, les films à double émulsion de
marque AGFA et de type AGFA-CPBU (Belgique) de dimensions 36x43 ou 35x35. Les
cassettes avec écrans renforçateurs, l'index en plomb, les bains
du révélateur et du fixateur pour le développement manuel
en chambre noire ainsi qu'une imprimante furent utilisés (41).
2.4.1.2. Position et centrage
Le patient debout en position
postéro-antérieure, jambes légèrement
écartées, strictement de face. La tête était en
rectitude, le menton soulevé s'appuyant sur le bord supérieur de
la cassette (ainsi une portion de la cassette était visible des deux
côtés au-dessus de chaque épaule. Les épaules
étaient abaissées et plaquées en avant, le plus au
contact possible de la cassette. Les bras étaient placés en
rotation interne (la paume des mains regardant en arrière) puis les bras
légèrement fléchis, les dos des mains placés sur
les hanches, les coudes étaient portés en avant pour
écarter les omoplates (41).
Le rayon directeur horizontal était centré sur
la ligne des épineuses à la hauteur d'une ligne joignant
l'extrémité inférieure de la pointe des omoplates.
La prise du cliché s'était effectuée chez
le patient en inspiration profonde et en apnée. Le film
exposé était ultérieurement placé en chambre noire
pour un développement manuel.
2.4.1.3. Lecture radiographique des clichés
Utilisant un négatoscope couché de marque WGR (
Bonn , Allemagne ) de la salle de lecture radiologique des CUK , la lecture
des clichés était effectuée par nous-mêmes.
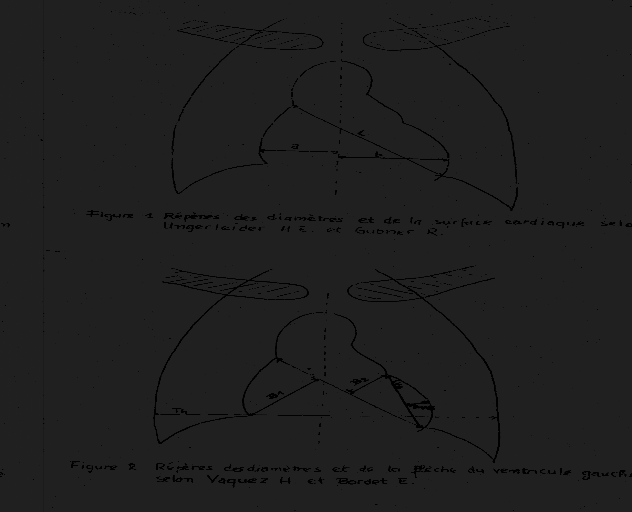
A l'aide d'une règle millimétrique, les
repères des diamètres du coeur en cm et la flèche du
ventricule gauche en cm (FVG) selon VAQUEZ et BORDET ( 42, 43), et pour la
surface cardiaque selon UNGERLEIDER et GUBNER (Figure 2) (44 ) ont
été mesurés.
Après avoir tracé la ligne verticale
médio-thoracique passant par les épineuses, les diamètres
cardiaques médians droit (a) et gauche (b) ont été
déterminés en mesurant la distance du point extrême du
contour cardiaque à droite et à gauche, à la ligne
médiane. La somme (a+b) est appelée diamètre transversal
cardiaque.
Le diamètre longitudinal du coeur (L) a
été déterminé après avoir tracé une
ligne partant de la pointe du coeur (apex) à l'angle formé entre
l'oreillette droite et la veine cave supérieure (ou l'aorte
ascendante).
Le diamètre basal du coeur (B) a été
défini par la ligne qui joint le point le plus bas du bord de
l'oreillette droite au point situé entre l'auricule gauche et le
ventricule gauche.
La longueur du VG (LVG) a été obtenue en reliant
le point de jonction de l'auricule gauche à la pointe du coeur.
La flèche du ventricule gauche (FVG) ou corde du
ventricule gauche correspondait à la perpendiculaire abaissée du
point le plus excentrique du bord inférieur du VG sur la longueur du
ventricule gauche (LVG).
Le diamètre interne trans-thoracique (Th) a
été tracé parallèlement à (a) et à
(b), avec tangence au point le plus haut de la coupole diaphragmatique
droite.
La surface cardiaque a été obtenue selon la
formule suivante :
Surface cardiaque (S ) = (/4) x ( L x
B)
2.4.2. Electrocardiogramme
2.1.1.1. Matériels et enregistrement
Les électrocardiographes AUTO CARDINER FCP - 1454
marque FUKUDA DENSHI (Tokyo, Japon) pour LOMO- MEDICAL et CARDIOFAX (Tokyo,
Japon) pour les Cliniques Universitaires de Kinshasa ont été
utilisés.
En fixant des électrodes aux membres et à la
paroi thoracique, à des positions standards et en s'assurant grâce
à un gel que le contact entre l'électrode et la peau
était bon, l'enregistrement des différences de potentiel
était effectué normalement sur du papier thermosensible
défilant à 25 mm/seconde.
Un papier quadrillé montrait une échelle de
temps horizontale (0,04 seconde par petit carré) et de potentiel
verticale (0,1 mVolt par petit carré).
Les enregistrements étaient effectués pendant
quelques minutes chez un patient au repos et alité, au moyen de douze
dérivations standards.
2.1.1.2. Critères électrocardiographiques
Chaque tracé électrocardiographique a
été analysé pour le dépistage de l'HVG en
appliquant les critères électrocardiographiques cités par
Odia et al (8) et dérivés de la somme des ondes S en V1 ou V2 et
R en V5 ou V6 dans les dérivations précordiales(Tableau 1 ).
Tableau 1 Critères ECG d'HVG utilisés
Critères
|
Caractéristiques
|
|
Mcphie , 1958
|
S+R > 40 mm
|
|
Sokolow-Lyon , 1949
|
S+R > 35 mm
|
|
Wolff , 1956
|
S+R > 30 mm
|
2.4.3. Echocardiogramme
Les mesures échocardiographiques ont été
obtenues en utilisant un échocardiographe de marque BIOSOUNDS
(Indianapolis, USA) pour LOMO MEDICAL avec un transducteur de 2,5 MHZ et un
échocardiographe de marque SONOLINE LS2 Siemens (Allemagne) avec un
transducteur de 3,5 MHZ.
Le transducteur a été placé au niveau du
4ème espace intercostal gauche, le patient étant
couché en décubitus gauche. Il a été
orienté directement vers le dos pour identifier la valve mitrale
(aspect en M) puis pointé dans différentes directions pour mettre
en évidence les mouvements du V.G., de la valvule tricuspide et de
l'oreillette gauche en image bidimensionnelle.
En appliquant les recommandations de l'American Society of
Cardiology(ASE)(45), les paramètres suivants ont été
mesurés en mode TM (en prenant l'image bidimensionnelle comme
repère) :
- le diamètre diastolique du VD = VDDD ;
- le diamètre diastolique du VG =
VGDD ;
- le diamètre systolique du VG =
VGDS ;
- l'épaisseur diastolique du SIV =
SIVED ;
- l'épaisseur systolique du SI V =
SIVES ;
- l'épaisseur diastolique de la PP =
PPED ;
- l'épaisseur systolique de la PP = PPES.
La surface corporelle (SC) en m2, le volume
télédiastolique du VG (VTD) en ml, le volume
télésystolique du VG (VTS) en ml, la post-charge traduite par le
End Systolic Stress (ESS), la masse ventriculaire gauche (MVG) en gramme,
l'index de masse ventriculaire gauche (IMVG) en gr/m2 et
l'épaississement relatif de la paroi postérieure (ERP) sous
forme de ratio, ont été calculé à l'aide des
formules ci-après :
Taille,cm x Poids, kg
* SC = ---------------------------- ;
3.600
7 3
* VTD = ---------------- x VGDD ;
2,4 + VGDD
7 3
* VTS = --------------- x VGDS ;
2,4 + VGDS
0,334 x VGDS x TAPAS
· ESS = ---------------------------- ;
PPES
PPED x (1 x -------- )
VGDS
* MVG = 1,05 (VGDD +SIVED+PPED)3 -
VGDD3] ;
MVG
* IMVG = ----------- ;
SC
2 x PPED
· ERP = ---------------- .
VGDD.
2.5. DEFINITION DE L'HVG ET
DE LA GEOMETRIE VENTRICULAIRE GAUCHE
2.5.1. Définition
radiographique.
Les valeurs de l'ICT, de la FVG et de la surface cardiaque
égales ou supérieures à leurs médianes
tirées de la présente population ont défini l'HVG
radiographique.
2.5.2. Définitions
electrocardiographiques
L'HVG électrique a été respectivement
définie par l'indice de Mcphie > 40 mm, l'indice de
Sokolow-Lyon > 35 mm et l'indice de Wolf f > 30 mm.
2.5.3. Définitions
échocardiographiques.
L'HVG définie par l'échocardiographie (test de
référence ou gold standard) a été
considérée comme le diagnostic réel de cette complication
de l'HTA.
L'IMVG > 125gr/m² a caractérisé l'HVG
à l'échocardiographie;
L'HVG concentrique et l'HVG excentrique ont été
définies par rapport à la géométrie
ventriculaire gauche normale et au Remodelage concentrique, en
considérant le seuil de 0,45 pour l'ERP et celui de 125 g/m² pour
l'IMVG. L'étude de la géométrie ventriculaire a
été réalisée par la combinaison de l'IMVG et de
l'ERP selon le seuil proposé par GANAU et al(45,46). Elle a
distingué la géométrie normale de remodelage ventriculaire
concentrique, des hypertrophies ventriculaires gauches concentrique et
excentrique (Tableau 2).
Tableau 2 Géométrie Ventriculaire Gauche
|
Géomètrie Normale
|
Remodelage Concentrique
|
HVG
Excentrique
|
HVG Concentrique
|
|
ERP
|
< 0,45
|
> 0,45
|
< 0,45
|
> 0,45
|
|
IMVG
|
< 125gr/m²
|
< 125gr/m ²
|
> 125gr/m²
|
> 125gr/m²
|
2.6. VALIDITE DES METHODES
DIAGNOSTIQUES
La validité interne considérée comme la
capacité de poser correctement le diagnostic de l'HVG était
mesurée par la sensibilité, la spécificité, les
valeurs prédictives positive et négative et le rapport de
vraisemblance. La validité externe définie par la
reproductibilité de plusieurs méthodes de diagnostic, indiquait
la probabilité d'obtenir les mêmes résultats.
Pour ce faire, la base des formules a été
établie à partir du quarré latin (Tableau 3).
Tableau 3 Quarré Latin.
|
Test de Référence Echographie
|
|
|
Méthodes de diagnostic :
* Radiographie *ECG
|
+ -
|
Total
|
|
Test +
Test -
|
a = Vrai Positif, VP b= Faux Positif , FP
c = Faux Négatif, FN d = Vrai Négatif,
VN
|
a + b
c + d
|
|
TOTAL
|
a + c b + d
|
a + b + c + d
|
VP a
* Sensibilité = = ;
VP + FN a + c
VN d
* Spécificité = = ;
VN + FP d + b
Sensibilité
LR + =
1 -
Spécificité
* Rapport de vraisemblance
;
1 - Sensibilité
LR - =
Spécificité
VP a
* Valeur Prédictive Positive, VP + = =
;
VP + FP a + b
VN d
* Valeur Prédictive Négative, VP - = =
;
VN + FN d + c
a + d
* Concordance observée = = Po ;
a + b + c + d
(a+c)(a+b) + (b+d)(c + d)
* Concordance attendue sous l'hypothèse
d'indépendance = = Pa ;
( a + b + c + d)2
Po - Pa
* Coefficient KAPPA = .
1 - Pa
La concordance observée a mesuré la
reproductibilité, et le coefficient KAPPA l'accord entre tests pour le
diagnostic de l'HVG (-1 = désaccord, 1 = accord absolu et 0 = accord
dû parfaitement au hasard).
Le rapport de vraisemblance indiquait le pouvoir discriminant
d'un test de classer correctement les malades et les non malades (LR+ tend
vers + , LR - tend vers 0,
si LR 1, alors le test n'est absolument pas informatif).
2.7. ANALYSES
STATISTIQUES
La saisie des données a été
effectuée à l'aide des logiciels EPI-INFO 6.04 et EXCEL Version
6. Les logiciels EPI-INFO 6.04 et SPSS-PC+ ont servi à effectuer les
calculs statistiques. L'analyse descriptive a été
réalisée grâce aux calculs des proportions pour les
variables qualitatives (fréquence, pourcentage), des moyennes et des
écarts-types pour les variables continues.
Les différentes comparaisons de fréquence ont
été faites à l'aide du test Chi-carré de Pearson
ou à l'aide du test de Fisher quand cela était
nécessaire.
Le test t de Student a été utilisé pour
comparer les moyennes des variables continues normalement distribuées et
le test H de KrusKal Wallis (test non paramétrique) pour la comparaison
des moyennes des variables continues asymétriques.
L'évaluation des méthodes de diagnostic de
l'hypertrophie ventriculaire gauche (radiographie, électrocardiographie
et l'échocardiographie comme test de référence) a
été réalisée par leur validité interne et
externe et la mesure de l'accord (efficience ou concordance) et le choix
décisionnel à l'aide des courbes ROC ( Receiver Observer's
Curves)
(48-50).
La valeur de p<0.05 a été
considérée comme seuil de significativité statistique.
CHAPITRE 3. RESULTATS
Au total, les résultats de 137 patients hypertendus
constituant la population de la présente étude dont 81 hommes
(59,1 %) et 56 femmes (40,9%) avec un sexe ratio de 1,5 homme : 1 femme
sont rapportés dans ce chapitre.
3.1. AGE
La figure 3 présente la répartition de la
population d'étude selon l'âge. Cette population d'étude
est normalement distribuée avec le mode, la moyenne et la médiane
confondus dans la tranche d'âge de 45 - 54 ans. En effet, les
extrêmes de l'âge varient entre 26 ans et 79 ans ; l'âge
moyen étant de 52,9 ans plus ou moins 11,7 ans.
%
30,6%
23,4%
18,1%
17%
8%
2,9%
">74"
"65 - 74"
"55 - 64"
"45 - 54"
"35 - 44"
"<34"
Age, ans
Figure 3 Distribution de la population d'étude selon
l'âge.
3.2. PRESSION ARTERIELLE ET
VARIABLES ANTHROPOMETRIQUES
Les caractéristiques générales de la
pression artérielle, du poids, de la taille, de l'indice de masse
corporelle (IMC) et de la surface corporelle sont résumés dans
le tableau 4. Comme il fallait s'y attendre, les chiffres tensionnels moyens
sont caractéristiques d'une population d'hypertendus. Et la valeur
moyenne de l'IMC est suggestive d'une population avec surcharge
pondérale.
En effet, sur 137 patients de la population globale, 57,7 %
(n=79) ont leur IMC compris entre 25 kg/m2 et 29
kg/m2 . Aucun patient n'est défini comme
obèse.
Tableau 4 Pression Artérielle et paramètres
anthropométriques
|
Variables
|
Moyennes + E . T
|
Extrêmes
|
|
Poids, kg
|
69,7 #177; 10,3
|
47 - 100
|
|
Taille, m
|
1,67 #177; 0,8
|
1,5 - 1,9
|
|
IMC, kg/m2
|
25 #177; 2,6
|
17,7 - 29,7
|
|
PAS, mmhg
|
167,7 #177; 29,9
|
113 - 250
|
|
PAD, mmhg
|
99,3 #177; 17,3
|
60-190
|
|
SC, m²
|
1,8 #177; 0,2
|
1,4 - 2,3
|
IMC : Indice de masse corporelle. SC : Surface
corporelle.
3.3. DONNEES
RADIOGRAPHIQUES.
L'Index cardiothoracique (ICT), la surface cardiaque (SC) et
la flèche du ventricule gauche (FVG) considérés comme
variables continues, sont résumés dans le tableau 5. Leurs
valeurs moyennes sont caractéristiques de l'augmentation du volume et de
la surface cardiaque.
Tableau 5 Valeurs moyennes de l'ICT, de la surface
cardiaque et de la flèche du
ventricule gauche
|
Variables
|
Moyenne E . T
|
Extrêmes
|
|
ICT
|
0,53 #177; 0,06
|
0,37 - 0,76
|
|
Surface cardiaque, cm²
|
126,1 #177; 29,5
|
75,6 - 283,1
|
|
FVG, cm
|
1,6 #177; 0,3
|
0,8 - 2,5
|
En effet, considérés comme variables
dichotomiques, les catégories supérieures de l'ICT, de la FVG et
de la surface cardiaque sont respectivement constituées au moins de la
moitié des membres (Tableau 6).
Tableau 6. Augmentation de la taille globale ou partielle du
coeur suggérée par l'anomalie de certains critères
radiologiques du thorax à l'incidence de face ( médianes)
Variables n %
ICT 0,52 72 52,6
FVG 1,5 82 59,9
Surface cardiaque 123,7 cm2 69 50,4
3.4. DONNEES
ELECTROCARDIOGRAPHIQUES
L'axe électrique moyen du complexe QRS est de 10,5
39,6° avec les extrêmes variant entre - 150° et +86°.
La figure 4 repartit la population d'étude selon l'axe
électrique de QRS.
61,3%
%
24,8%
13,9%
-
+
"1° et 86°"
"-29° et 0°"
"-150° et -30°"
Axe QRS
Figure 4 Répartition de la population d'étude
selon l'axe électrique de QRS.
De cette population 38,7 % (n=53) présente un axe
électrique de QRS gauche et hyper-gauche. 13,9 % (n=19) avec un axe
électrique de QRS à -30° souffrent d un hemibloc
antérieur gauche. La surcharge systolique du VG (sous décalage
asymétrique du segment ST) est présente chez 34,3 % de la
population (n=47).
Les taux les plus élevés d'HVG
sont fournis au tableau 7 par l'indice de Wolff pathologique suivi par ceux
définis par l'indice de Sokolow pathologique et enfin par ceux
caractérisés par l'indice de Mcphie pathologique .
Tableau 7 Fréquences d'HVG selon certains
critères électrocardiographiques
|
Indice S+R
|
n
|
%
|
|
Mcphie > 40 mm
|
36
|
26,3
|
|
Wolf f >30 mm
|
76
|
53,3
|
|
Sokolow > 35 mm
|
54
|
39,4
|
3.5. PARAMETRES
ECHOCARDIOGRAPHIQUES
Les données échocardiographiques relatives aux
épaisseurs septale et pariétale, aux diamètres et
à l'index de masse du ventricule gauche (I.MVG) sont
résumées au tableau 8.
Tableau 8 Paramètres échocardiographiques du
ventricule gauche
|
Variables
|
Moyenne #177; E.T
|
Extrêmes
|
|
SIVED, mm
|
12,1 #177; 3,2
|
7 - 22
|
|
SIVES, mm
|
16,6 #177; 3,7
|
7 - 27
|
|
VGDD, mm
|
50,3 #177; 7,1
|
38-75
|
|
VGDS, mm
|
37,8 #177; 9,6
|
21 -66
|
|
PPED, mm
|
10,8 #177; 2,3
|
7,5 -20,5
|
|
PPES, mm
|
15,6 #177;2,8
|
9 - 21
|
|
IMVG, gr/m²
|
159,1 #177; 55,9
|
77,2 - 332,6
|
SIVED : Epaisseur diastolique du SIV ;
SIVES : Epaisseur systolique du SIV
VGDD : Diamètre diastolique du VG; VGDS :
Diamètre systolique du VG
PPED : Epaisseur diastolique de la PP ; PPES
: Epaisseur systolique de la PP
IMVG : Index de masse du VG.
L'étendue ou amplitude de l'index de masse
ventriculaire gauche est très large avec une valeur moyenne nettement
pathologique. Seule l'épaisseur diastolique du SIV est
caractérisée par une valeur moyenne pathologique
(Hypertrophie).
L'HVG estimée à l'échocardiographie selon
l'IMVG > 125 gr/m² est présente chez 70,8 % (n= 97) des
patients de cette population hypertendue.
Concernant la géométrie et le remodelage du
ventricule gauche chez ces hypertendus (Tableau 9), 1/5 de cette population
présente une géométrie normale du VG alors que la
fréquence des patients avec remodelage concentrique est proche de 10 %
(n = 12).
Il est noté plus des cas d'HVG excentrique que ceux
d'HVG concentrique.
En effet de ces 97 cas d'HVG échographique 62 (63,9
%) et 35 (36,1 %) présentent respectivement une hypertrophie
ventriculaire gauche excentrique et une HVG concentrique.
Tableau 9 Géométrie et Remodelage du
ventricule gauche chez les noirs
hypertendus congolais
|
Echo. Coeur
|
IMVG 125gr/m²
|
ERP
|
n
|
%
|
|
Géométrie normale du VG
|
<
|
<
|
28
|
20,4
|
|
Remodelage concentrique
|
<
|
>
|
12
|
8,8
|
|
HVG concentrique
|
>
|
>
|
35
|
25,5
|
|
HVG excentrique
|
>
|
<
|
62
|
45,3
|
Excepté la post-charge évaluée sous forme
d'End Systolic Stress (ESS) avec une valeur moyenne élevée,
l'épaississement relatif de la paroi postérieure, le volume
télédiastolique et le volume télésystolique du VG
sont caractérisés par des valeurs moyennes normales (Tableau
10).
Tableau 10 Post-charge, ERP, VTD et VTS
|
Variables
|
Moyenne #177; E.T
|
|
Post-charge
*End Systolic Stress (ESS) x 10 dynes/cm²
|
145 #177; 61,2
|
|
Epaississement relatif Paroi postérieure VG, ERP
|
0,44 #177; 0,12
|
|
VTD, ml
|
75,1 #177; 22,2
|
|
V.T.S, ml
|
44,2 #177; 23,2
|
3.6. MATRICE DE
CORRELATIONS DANS LA POPULATION D'ETUDE.
Le poids est corrélé de manière positive
et très significative à la taille (r = 0,719, p< 0,001),
à la surface corporelle (r = 0,316, p< 0,001), à l'IMC (r =
0,727, p< 0,001), mais inversement associé à la PAS ( r =
-0,234, p< 0,01).
La taille est associée de manière
négative à la PAS (r = -0.364,p< 0.001), à la PAD (r =
- 0,258, p< 0,01), mais de manière directe au VGDD (r = 0,213, p
< 0,01) et au VG DS ( r = 0,214, p<0,01).
La pression artérielle systolique est
corrélée positivement à ERP (r = 0,247, p< 0.01) et
à ESS (r = 0,209, p< 0.01). L'ICT est corrélé
positivement à la surface cardiaque (r = 0,451, p< 0.001), à
la FVG (r = 0,253, p< 0.01) et au VGDD (r = 0,310, p< 0.001).
L'onde R est corrélée positivement à
l'ICT (r = 0,217, p < 0,01), à la surface cardiaque (r = 0,203, p
< 0,01) et à ESS (r = 0,304, p< 0,001), mais négativement
à l'IMC, (r = - 0,214, p < 0,01). L'onde S est corrélée
positivement au VGDD (r = 0.227, p< 0.01).
L'IMVG est corrélée positivement à la
surface cardiaque (r = 0.294, p < 0,001), à la FVG (r = 0,202,
p< 0,01), au VGDD (r = 0.541, p < 0,001) et au VGDS (r = 0,389, p<
0,001), au SIVED (r = 0.656, p <0,001) au SIVES (r = 0.476, p< 0,001),
à PPED (r = 0,57, p< 0,001) mais négativement à
l'index de Sokolow (r = -0,300, p< 0.001), à l'index de Wolff (r = -
0,224, p < 0,01)
3.7. VALIDITE DES TESTS
DIAGNOSTIQUES DE L'HVG
3.7.1. Radiographie du
Thorax.
Le tableau 11 présente la validité interne de
trois tests radiologiques dans le diagnostic de l'HVG chez l'hypertendu noir,
l' IMVG étant le test de référence.
Si les indices de sensibilité et de
spécificité sont des valeurs relativement bonnes pour l'ICT, la
surface cardiaque et la flèche du ventricule gauche, la valeur
prédictive positive est très bonne pour tous les trois
critères radiologiques.
Par contre, la valeur prédictive négative et la
concordance sont des valeurs médiocres.
En pratique, prenant l'echocardiographie comme
référence, l'ICT, la surface cardiaque et la FVG sont incapables
de bien classer aussi bien les malades que les non- malades.
Tableau 11 Validité diagnostique de la radiographie
du thorax à l'incidence de face dans le
dépistage de l'HVG (IMVG
> 125 gr/m², l'échocardiographie étant le test de
référence)
|
Validité diagnostique
|
ICT > 0,52
|
Surface cardiaque >120cm2
|
FVG>1.5
|
|
Sensibilité, %
|
61
|
54
|
67
|
|
Spécificité, %
|
67
|
58
|
57
|
|
Valeur Prédictive Positive, %
|
82
|
75
|
79
|
|
Valeur Prédictive Négative, %
|
41
|
34
|
41
|
|
Reproductibilité
|
0,54
|
0,46
|
0,57
|
|
LR (+)
|
1,8
|
1,3
|
1.6
|
|
LR (-)
|
0,6
|
0,8
|
0,6
|
|
Kappa, coefficient
|
0,24
|
0,1
|
2,2
|
3.7.2. Electrocardiogramme
(ECG)
Comparé à l'IMVG 125 gr/m²
évalué à l'échocardiographie (Tableau 12), l'ECG
présente une spécificité élevée mais une
faible sensibilité.
Les valeurs prédictives positives de trois indices
électrocardiographiques étudiés sont très
élevées alors que les valeurs prédictives négatives
sont médiocres dans l'ensemble.
L'indice de Wolff, l'indice de Sokolow et l'indice de Mcphie
présentent un désaccord avec l'échocardiographie dans le
diagnostic de l'HVG chez ces hypertendus.
Tableau 12 Validité diagnostique de l' ECG dans
l'évaluation de l'HVG
(l'IMVG > 125g/m² à
l'échocardiographie étant le test de Référence)
|
Validité Diagnostique
|
Indice de Wolff
|
Indice de Sokolow
|
Indice de Mcphie
|
|
Sensibilité, %
|
60
|
46
|
29
|
|
Spécificité, %
|
63
|
76
|
80
|
|
Valeur prédictive(+), %
|
79
|
83
|
78
|
|
Valeur prédictive (-), %
|
39
|
37
|
32
|
|
Reproductibilité
|
0,52
|
0,42
|
0,27
|
|
L.R (+)
|
1,6
|
2
|
1,5
|
|
L.R (-)
|
0,6
|
0,7
|
0,9
|
|
Kappa, coefficient
|
0,2
|
0,2
|
0,2
|
3.7.3. Détermination de
seuil de décision
En faisant varier le seuil décisionnel tout au long des
critères diagnostiques, l' ICT et la somme des amplitudes S en V1 ou V2
et R en V5 ou V6, l'ensemble des points du couple
sensibilité/spécificité dessine la courbe ROC.
3.7.3.1. Choix décisionnel à la radiographie.
La figure 5 représente la courbe ROC établie
entre la sensibilité et la spécificité de
différents seuils de (0,49 ; 0,52 ; 0,56 et 0,64). La
validité de l' ICT dans le diagnostic de l'HVG est sujet à
caution.
En effet, la courbe est très loin de l'angle
supérieur gauche ayant une spécificité à 100 % et
une sensibilité à 100 %.
Néanmoins, le seuil de l'ICT = 0,52 semble optimal
(sensibilité à 61%, spécificité à 68 %).
%
100
50
0
Sensibilité
(d)
(c)
(b)
(a)
100 50 0
%
100 - spécificité
Figure 5 Courbe ROC pour déterminer le seuil
décisionnel de l'ICT ( a, b, c, d) :
a = 0,64 ; b = 0,56 ; c= 0,52 ; d= 0,49.
3.7.3.2. Choix décisionnel de l'ECG
En considérant plusieurs seuils de la somme SVI ou V2
et RV5 ou V6 (a=7, b=30, c=31, d=35, e=40 et f=41), la courbe ROC pour ces
critères électrocardiographiques est aussi loin de l'angle
supérieur gauche (figure 6).
0
50
100
100 - specificité
Sensibilité
(b)
(a)
(c)
(d)
(e)
(f)
100
0
50
%
%
Figure 6 Courbe de ROC pour déterminer le seuil
décisionnel de l'amplitude de S+R
(a, b, c, d, e, f).
Le seuil optimal de l'amplitude S + R est de 30,
critère proposé par Wolff. En effet , comparé
à d'autres critères dont ceux de Sokolow fixé à 35,
l'indice de Wolff montre des valeurs supérieures de sensibilité
à 60 % et de spécificité à 63 %.
CHAPITRE 4.
DISCUSSION
Les directives relatives à la prévention,
à la détection, à l'évaluation et au traitement de
l'HTA données par JNC (39) et l'OMS (40) devraient être
adaptées en fonction des situations locales et individuelles.
En ce qui concerne l'évaluation de l'HTA, la
présente étude définit l'HVG chez les patients noirs
hypertendus, congolais de Kinshasa. Elle permet donc d'identifier les
patients à haut risque cardio-vasculaire (6,7).
La radiographie du thorax à l'incidence de face,
l'électrocardiogramme et l'échocardiogramme sont les trois
procédures diagnostiques de l'HVG retenues dans la présente
étude.
En ce qui concerne l'échocardiographie comme
méthode diagnostique de référence apportant le diagnostic
réel de l'HVG, la radiographie du thorax et l'électrocardiogramme
doivent être considérés comme des examens de
dépistage.
Ces examens de dépistage servent à identifier
les patients hypertendus dont le risque d'avoir l'HVG est élevé.
De cette façon, ces patients peuvent bénéficier de
l'échocardiogramme et du traitement. En effet, certains traitements
anti-HTA entraînent une régression de l'HVG (51).
La présente étude a analysé la
validité et la reproductibilité de la radiographie du thorax et
de l'électrocardiographie dans la définition de l'HVG,
l'échocardiographie étant le test de référence.
4.1. PREVALENCE DE L'HVG
La présente étude démontre que l'HTA est
le principal facteur prédisposant au développement de l'HVG. En
effet, les patients hypertendus obèses, grands sportifs et avec
affections cardiovasculaires susceptibles d'induire l'HVG, ont
été exclus de la présente étude (6).
En dépit de non ajustement pour l'âge, ce
dernier ne peut pas être incriminé dans cette HVG dans une
population des jeunes adultes (âge moyen de 52,9 #177;11,7 ans). L'IMVG
ne montre aucune corrélation significative avec l'âge.
Cette HVG survient précocement chez les hypertendus
congolais, et est observée chez 70,8 % des patients avec HTA
légère à modérée (valeurs moyennes de PAS
égale à 167,7 mmHg à classer dans le grade 2 et valeurs
moyennes de PAD égales à 99,3 mmHg à classer dans le grade
1 selon la classification de l'HTA de JNC/OMS. Ce taux de prévalence
est de loin supérieur à ceux rapportés dans les pays
développés entre 30 et 60 % avant 1990 (21,22) et entre 17 et 39
% en 1995 (51).
Ce taux de prévalence très élevé
d'HVG dans cette population explique l'absence de la prise en charge de l'HTA
avec une approche multifactorielle auprès de patients à
majorité pauvres. L'HTA est souvent méconnue chez 70 %
d'hypertendus (52) et non traitée chez plus de 80 % (53). Cette
prévalence élevée d'HVG confirme l'émergence des
maladies cardio-vasculaires devant être épidémiques autour
de 2020 en Afrique subsaharienne (54).
Dans l'étude de Framingham (9,55),
l'amélioration de l'observance du traitement anti-hypertenseur et de
la prise en charge des patients hypertendus a favorisé une diminution
non seulement de la prévalence de l'HTA de plus de 60 % (taux passant
de 18,5 % à 9,2 % chez l'homme et de 28 % à 7,7 % chez la femme)
mais aussi celle de l'HVG de 4,5 à 2,5 % chez l'homme et de 3,6
à 1,1 % chez la femme.
Il est certain qu'au plan pronostic, ces patients hypertendus
courent dans un proche avenir un grand risque des maladies coronaires,
d'arythmies, d'insuffisance cardiaque et de mort subite tel que prouvé
par l'enquête de Framingham (9, 55, 56).
L'étude de Framingham a montré que le taux de
mortalité à 5 ans des hommes présentant une HVG
démontrée à l'échographie, était d'environ
35 % contre 10 à 15 % à l'absence d'HVG à
l'échographie (57).
La géométrie ventriculaire va aussi influencer
à l'avenir le pronostic de ces hypertendus. Les hypertendus noirs
congolais présentent trois fois plus de remodelage concentrique et
d'HVG excentrique et d'HVG concentrique que les hypertendus caucasiens des
Etats-Unis (58), mais deux fois moins de remodelage concentrique, et d'HVG
concentrique mais cinq fois plus d'HVG excentrique que les noirs
américains (58) (Tableau 13).
Tableau 13 Géométrie ventriculaire gauche au
Congo et aux Etats-Unis
|
Géométrie ventriculaire
|
MALONGA
Congo
n = 137
|
BABATUNDE et al
al
n = 73
|
|
Noirs
|
Noirs
|
Blancs
|
|
Remodelage concentrique du ventricule gauche
|
8,8 %
|
18 %
|
3 %
|
|
HVG concentrique
|
25,5 %
|
38 %
|
20 %
|
|
HVG excentrique
|
45,3 %
|
9 %
|
13 %
|
Dans l'étude américaine (58), le remodelage
concentrique est six fois plus présent chez les noirs américains
que chez les caucasiens. L'HVG concentrique est deux fois plus présente
chez les noirs américains que chez les caucasiens.
Ces variations d'HVG chez les noirs restés en Afrique,
chez les noirs de la diaspora américaine et chez les blancs des
Etats-Unis suggèrent des mécanismes
éthiopathogéniques et des stades évolutifs ou d'adaptation
différents dans l'HTA.
Chez les patients hypertendus avec post-charge très
élevée (EES), les mécanismes résistifs pourraient
intervenir dans l'HVG concentrique (59). Les mécanismes
volumétriques interviendraient dans l'HVG excentrique (60).
L'excès d'HVG excentrique dans la présente
étude est le stade initial de l'évolution de la majorité
des patients hypertendus noirs africains vers une cardiomyopathie
dilatée avec insuffisance cardiaque congestive ; la dysfonction
systolique du VG pour l'HVG excentrique a été déjà
rapportée ailleurs (61). La dysfonction diastolique était
présente dans les HVG concentriques. En plus de différence
raciale intervenant dans la réponse adaptative du VG devant l'HTA (58)
tel que l'absence de la baisse tensionnelle nocturne chez les noirs,
l'environnement pourrait aussi intervenir (plus d'obésité chez
les noirs américains, absence de traitement chez les noirs
africains).
4.2. VALIDITE DIAGNOSTIQUE
DE LA RADIOGRAPHIE DU THORAX
Les données de la présente étude
démontre que la sensibilité de l'ICT et de la FVG est sinon
satisfaisante. La sensibilité de la surface cardiaque est assez bonne.
Seule la spécificité de l'ICT apparaît satisfaisante et
plus élevée en valeur absolue en comparaison avec celle de la
FVG. Mais ces valeurs sont inférieures à celles rapportées
en Allemagne(sensibilité de l'ICT égale à 69.7%,
spécificité égale à 87.4%). La présente
étude et celle de Jung et al (20) démontrent la pertinence
clinique de la radiographie du thorax dans le dépistage de l'HVG. Ceci
s'explique par l'absence de la dilatation des cavités cardiaques gauches
des hypertendus évalués dans la présente étude.
En effet, la radiographie apporte une analyse de la taille et
du volume cardiaque de manière grossière et ne permet pas de
dissocier de manière formelle une dilatation d'une hypertrophie
ventriculaire gauche(62). L'HVG s'accompagne souvent d'un épaississement
pariètal déterminant à peine une légère
modification de la silhouette cardiaque. Ceci est lié au principe
d'obtention des images radiographiques projetées sur un plan(44). La
distance foyer-film peut influer sur la sensibilité de la radiographie
du thorax :seul un télé-coeur permet d'éviter
l'agrandissement de la taille du coeur. L'inspiration insuffisante et/ou
l'expiration entraînent une fausse augmentation de la taille du coeur. La
présente étude a été limitée par l'absence
de clichés thoraciques de profil. Un cliché thoracique de face et
un cliché thoracique de profil auraient permis les calculs du volume
cardiaque. La sensibilité diagnostique est meilleure avec le volume
cardiaque, quand bien même le volume cardiaque radiologique concerne tout
aussi bien le muscle que la cavité gauche(63).
Qu'à cela ne tienne, la présente étude
démontre que l'ICT est corrélé directement au
diamètre diastolique du VG à l' échocardiographie. Ce
diamètre diastolique rendu au cube
exprime grossièrement le volume cardiaque(42,44). L'ICT
est aussi corrélé de manière positive aussi bien à
la surface cardiaque qu'à la FVG. La convexité de l'arc
inférieur gauche cardiaque et son allongement, appréciés
de manière analytique par la FVG , ne sont plus les seuls signes
radiologiques fidèles de l' augmentation de la masse ventriculaire
gauche.
En effet, la courbe ROC démontre une
bonne validité diagnostique de l'ICT (sensibilité égale
à 61% et spécificité égale à 68%) au seuil
optimal de l'ICT égale à 0.52. Il n'est pas encore possible de
doter la plupart des zones de santé d'un échocardiographe. Il
serait utile de généraliser ce seuil optimal de 0.52 pour l'ICT
dans la définition de l'HVG compliquant l'HTA du noir africain.
Toutefois, il convient de retenir que la radiographie(incidence de face) est
incapable de classer correctement l'HVG et un coeur de poids normal. La
concordance et le pouvoir discriminant médiocre du cliché
radiologique de thorax(incidence de face) rend ce dernier un test diagnostique
absolument non informatif.
4.3. VALIDITE DIAGNOSTIQUE
DE L'ECG
Parmi les nombreuses définitions
électrocardiographiques de l'HVG citées par Odia et al(8),trois
de ces critères ont été évalués dans la
présente étude. Il s'agit de critères basés sur le
voltage à partir des dérivations précordiales tel que le
critère de Mcphie, l'indice de Sokolow-Lyon et l'indice de Wolff. En
effet, aucun critère n'est encore universellement accepté.
Comme démontré par d'autres études pour
la plupart de ces critères(8, 10-18, 64), la présente
étude confirme la faible sensibilité (29%-60%) et la haute
spécificité (63%-80%) de l'ECG dans la définition de l'HVG
de ces hypertendus. La valeur la plus élevée de cette
sensibilité a été obtenue par l'indice de Mcphie . Mais la
valeur prédictive est la plus élevée en appliquant
l'indice de Wolff comme seuil décisionnel optimal à 30mm, avec
une sensibilité de 60 % et une spécificité de 63%. Il
serait logique d'exclure l'indice de Sokolw-Lyon et celui de Mcphie dans la
définition de l'HVG due l'HTA des noirs africains au regard de leurs
taux élevés des faux négatifs. D' autres études
africaines ont déjà signalé le faible rendement
diagnostique de l'ECG dans la définition de l'HVG des noirs au Nigeria
(8).
Les résultats décevants de l'ECG devant la
définition de l'HVG ont poussé les spécialistes en
épidémiologie à mettre en avant, en plus de
critères de voltage, le critère de répolarisation (
surcharge systolique sous forme de sous décalage du segment ST). En
effet, la faible sensibilité de l'ECG pour l'HVG, a été
améliorée par la modification de critères standards de
l'ECG (Cornell voltage 2.4 mV et Romhilt-Estes score 5 points)(64).
Le Code de Minnesota (codes III.1 et II .3)
définissant l'HVG par la combinaison des critères de voltage et
des critères de répolarisation, a été
proposé pour améliorer la validité diagnostique de l'ECG
dans les études épidémiologiques(65). Ces critères
de voltage et de « strain » ou surcharge
(anomalie du segment ST et par négativation de l'onde T) ont
été largement exploités au plan
épidémiologique par les études de Framingham(66). Mais on
peut estimer que l'évaluation du segment ST à l'ECG est
cruciale : s'agit-il d'une surcharge ou d' un début
d'ischémie ? L'ECG est inapte pour différencier l'HVG de la
pathologie coronarienne. En effet, l'ECG permet de définir l'HVG sous
forme de variable catégorique limitée uniquement à la
limite supérieure de la distribution de la taille cardiaque
(appréciation qualitative binaire :absence ou présence de
l'HVG). La courbe de ROC transforme cette appréciation qualitative en
estimation quantitative et, permet au seuil optimal décisionnel de
s'approcher de l'échocardiographie. l'échocardiographie
définit donc l'HVG sous forme de l'index de masse ventriculaire gauche
qui est une variable continue.
D'ailleurs, l'onde R et l'onde S, variables continues de
l'ECG, montrent une association avec certaines variables continues de la
radiographie du thorax ou de l'échocardiographie. L'onde R est
directement corrélée à l'ICT, à la surface
cardiaque et à la post-charge (ESS). Cette onde reflète la
sévérité et les répercussions de l'HTA sur le
coeur. Par contre, l'onde S est corrélée positivement au
diamètre télédiastolique du VG(VGDD) à
l'échocardiographie : une grande amplitude de l'onde S est
suggestive de la dilatation du VG chez les hypertendus.
Dans une formation médicale dépourvue de
l'échocardiographe, la mise à profit de l'anthropomètrie,
des données radiographiques et électrocardiographiques, permet de
prédire le diamètre télédiastolique du ventricule
gauche.
En dépit de la précaution prise pour exclure les
sujets obèses de la présente étude, l'onde R montre une
association négative avec l'IMC. L'augmentation de l'IMC (surcharge
pondérale, obésité) peut expliquer la faible
sensibilité des critères électrocardiographiques.
En effet, l'obésité très fréquente chez les
patients hypertendus, peut constituer un facteur confondant dans la relation
existante entre la pression artérielle et la structure cardiaque(67).
A l'instar de la radiographie du thorax et en comparaison avec
l'échocardiographie, l'ECG montre une concordance qui laisse à
désirer. La reproductibilité de lecture doit être de mise
dans une formation médicale où un patient est
évalué par plusieurs médecins.
CHAPITRE 5. CONCLUSIONS ET
RECOMMANDATIONS
5.1. CONCLUSIONS
L'échocardiographie, test de référence,
démontre que l'HTA du noir congolais est greffée d'une
sévérité particulière à travers la
prévalence de l'hypertrophie ventriculaire gauche (HVG), une de ses
complications, estimée à 70,8%.
Cette imagerie ultrasonographique démontre la
physiopathologie de l' HVG sous forme de géométrie
ventriculaire normale chez 20 % des patients, de remodelage concentrique du VG
chez 8,8% des patients, d'HVG concentrique chez 25,5% des patients et d'HVG
excentrique chez 45,3% des patients.
Comparés à ce test de référence,
la radiographie du thorax à l'incidence de face et l'ECG de repos
montrent une faible sensibilité, une bonne spécificité
mais une concordance médiocre. Néanmoins, l'index cardio -
thoracique égale à 0,52 et l'indice de Wolff supérieur
à 30 mm sont identifiés comme seuils décisionnels optimaux
dans la définition de l'HVG des patients hypertendus.
L'index cardio - thoracique est corrélé de
manière significative et positive au diamètre télé
- diastolique du ventricule gauche à l'échocardiographie. L'onde
R est corrélée significativement et directement à la
post - charge estimée par l'ESS à l'échocardiographie.
5.2. RECOMMANDATIONS
Au terme de la présente étude, il est
formulé plusieurs recommandations à différentes personnes
au regard de leurs fonctions respectives suivantes :
5.2.1. A l'autorité
sanitaire étatique
De doter notre système sanitaire au niveau des
hôpitaux de références de zones de santé ainsi que
des hôpitaux universitaires d'un échocardiographe devant permettre
une amélioration de la prise en charge tant diagnostique que
thérapeutique de l'HTA et de ses complications. A défaut d'un
échocardiographe, leur doter au moins d'un appareil radiographique et
d'un électrocardiographe ;
5.2.2. Aux médecins
radiologistes
D'exercer toujours un esprit critique dans l'évaluation
d'une ou des méthodes diagnostiques de l'imagerie médicale,
devant leur permettre de faire le tri des informations de façon
rationnelle et pragmatique que possible, afin de juger, entre autres, la
rigueur de la méthode employée et donc, la
crédibilité des résultats obtenus ;
5.2.3. Aux chercheurs
D'initier ultérieurement d'autres études pour
mieux comprendre la physiopathologie de l'HVG des hypertendus noirs en
général et la pertinence de la prédominance du type HVG
excentrique chez l'hypertendu noir congolais ;
5.2.4. Aux
médecins
D'initier en temps utile, un bon traitement anti -
hypertenseur pour la régression de l'HVG, et par conséquent
réduire son impact sur la morbi-mortalité cardio-vasculaire. Ceci
est possible en vulgarisant l'application du seuil décisionnel de la
courbe ROC dans la définition de l'HVG chez l'hypertendu noir
congolais.
REFERENCES
1. DONNISON C.P.
Blood pressure in the Africain native
Lancet, 1929, 1 : 6 - 7.
2. M'BUYAMBA KABANGU JR., FAGAD R., STAESSEN.J., LITIJNEN.P.,
MBUY wa MBUY. R., LONGO. K., AMERY, A.
Blood pressure in Bantu of Zaire : epidemiological
aspects
Cardiol Trop, n° spécial.
3. BERTRAND. E., COULIBALY A.D., TICOLAT.R.
Statistiques 1988, 1989 et 1990 de l'institut de Cardiologie
d'Abidjan (ICA)
Cardiol Trop 1991, 17 (68) : 151 - 155.
4. MONEKOSSO G.I., HAGBE P. et ANCELLE J.P.
L'Hypertention artérielle en consultation à
Yaoundé
Afr. Med ; 1974, 13 : 991.
5. MBARAGA N., LONGO - MBENZA B., TSHIANI K.A.
Place de l'hypertension artérielle aux Cliniques
Universitaires de Kinshasa
Cardiol Trop 1984 ; 10 : 85 - 89.
6. ROUDOUT R., GOSSE P., AOUISERATE E., DALLACCHIO M.
L'Echoradiogramme dans l'hypertension artérielle
Arch. Mal. Coeur 1987 ; 10 : 1487 - 1495.
7. LEENEN FHH.
Increased risk attributed to left ventricular hypertrophy in
hypertension in : ROBERT ROBERTS (Ed). Curent opinium in Cardiology.
Rapid Science Publishers, Philadelphia 1996 : 469 -
470.
8. ODIA O.J ., FALASE A.O
An evaluation of various criteria for electro - cardiographic
diagnosis of left ventricular hypertrophy, using echocardiography, in adult
nigerians,
Cardiologie Tropical, 1987, 13 : 65 - 70.
9. KANNEL W.B., GORDON T., OFFUT D.
Left ventricular hypertrophy by electrocardiogram.
Prevalence, incidence and mortality in the Framigham Study.
Ann. Intern. Med., 1969, 71 : 89.
10. CASALE P.N et al.
Improved six specific criteria of left ventricular
hypertrophy for clinical and computed interpretation of
electrocardiograms : validation of autopsy fundings.
Circulation, 1987, 7 : 565 - 72.
11. SAVAGE D.D., GARRISION R.J., KANNEL W.B. et la.
The spectrum of left ventricular hypertrophy in a general
population sample. The Framingham Study
Circulation, 1987, 75 (Suppl 1) 26 - 33.
12. DEVEREUX R.B.
Cardiovascular Assessment of the Hypertensive Patient
Dialogues in hypertension, 1984, 1 : 27 - 41.
13. REICHEK., DEVEREUX R.B. :
Left ventricular hypertrophy : Relation of anatomic,
echocardiographic and electrocardiographic findings
Circulation 1981 ; 63 : 1391 - 1398.
14. DEVEREUX R.B., CASALE P.N., EISENBERG R.R et al.
Electrocardiographic detection of left ventricular
hypertrophy : Comparison of standar criteria. Comparated diagnosis and
physician interpretation using echocardiographic left ventricular mass as the
reference standard.
J Am Coll Cardiol, 1984 ; 3 : 82 - 87.
15. DEVEREUX R.B., REICHEK N.,
Repolarisation abnormalities of left ventricular hypertrophy
Relation of echocardiographic, hemodynamic and electrocardiographic findings.
J Electronocardiol 1983 ; 15 : 47 - 53.
16. DEVEREUX R.B., PHILIPS M.C., CASALE P.N. et al.
Geometric determinants of electrocardiographic left
ventricular hypertrophy
Circulation 1983; 67 : 907 - 911.
17. DEVEREUX R.B., CASALE P.N., EISENBERG R.R. et al.
Electrocardiographic detection of left ventricular
hypertrophy : Analysis of criteria using echocardiography and autopsy data
bases
In Laks MM (ed) : computerized Interpretation of the
Electrocardiogram.
Enginnering foudation, 1983 : 41 - 48.
18. CASALE P.N., DEVEREUX R.B., KRIGFRIELD P. et al.
New criteria of electrocardiographic left ventricular
hypertrophy
Clin Res 1983 ; 31 : 173 A.
19. DAVIDSON A., KRULL F, KALLFELZ H.C.
Cardiomegaly. - What does it mean ? A comparison of
electrocardiographic to radiological cardiac dimensions in children
Pediatr cardiol 1990 ; 11 : 181 - 5.
20. JUNG G., LANDWEHR P., SCHANZENBACHER G., FAEBER B.,
LACKNER K.,
Value of thoracic radiography in the assessment of cardiac
size. A comparison with left ventricular cardiography
Rofo Fortschr Geb rontgenstr Neuen Bildgeb verfahr 1995 ;
162 (5) : 368 - 72.
21. DEVEREUX R.B. et al.
Is the electrocardiogram still usefull for detection of left
ventricular hypertrophy?
Circulation 1990 ; 81 : 1114 - 6.
22. SAVAGE D.D. et al.,
Echocardiographic assessment of cardiac anatomy and function
in hypertensive subjects
Circulation 1979 ; 59 : 623 - 26.
23. HARISIOS B., DEMETRIOS M., YOUNG H., ARNOLD M.
Left ventricular mass and systolic perfomance in chronic
systemic hypertension.
Am J Cardiol 1986; 57 : 232 - 237.
24. AMABILE G.
Hypertrophie ventriculaire gauche et risque cardio -
vasculaire de l'hypertendu,
Ann Cardio Angeiol 1998 ; 47 (2) : 86 - 90.
25. CASALE P.N., MILNER M., DEVEREUX R.B. et al.
Value of echocardiographic left ventricular mass in
predicting cardiovascular morbid events in hypertensive men
Circulation (Abstract) 1985 ; 72 :III - 130.
26. GIOVANNI de SIMONE M.D., GIAN FRANSCESCO M.
Left ventricular hypertrophy in arterial hypertension
Hert Beat, Printer (éd.) 1993 ; 4 » 2 -
3.
27. ERIC EBERGEL.
Evaluation de la masse ventriculaire gauche par
échographie en mode M : de la masse à
l'interprétation
Sang Thrombose vaisseaux, vol 7 ; 1995 : 333 - 9.
28. AREND MOSTERD et al.
Trends in the prevalence of hypertension, anthypertensive
therapy, and left ventricular hypertrophy from 1950 to 1989.
N Eng J. Med 1999 ; 340 : 1221 - 7.
29. SAFAR M.E., LEHNER J.P., VINCENT M.I., PLAINFOSSE M.T.,
SIMON A. et al.
Echocardiographic dimensions in bordeline and sustained
hypertension
Am I cardiol 1979 ; 44 : 630 - 6.
30. CLEMENTY J., DANY F. DALLACHIO M.
Etude des tracés externes et des épreuves non
sanglentes
Arch Mal Coeur 1978 ; 17 : 20 - 8.
31. DUNN F.G., CHANDARATNA, de CARVALHO J.G., BASTA L.,
FROHLICH E.
Pathophysiologic assessment of hypertensive heart disease
with echocardiography
Am I cardio 1977 ; 39 : 189 - 93.
32. COHEN J.
A coefficient of agreement for nominal scales
Educat Psychol Measurements 1960 ; 20 : 37 - 40.
33. GREMY F.
Information médicale : Introduction à la
méthodologie en médecine et santé publique
Flammarion médecine - Science, Paris 1987 : 269 -
77.
34. LUSTED L.B
Introduction to medical decision making
Springfiel Thomas, 1968 ; 272.
35. LOOP J.W., LUSTED L.B
American college of cardiology diagnostic efficacy satudies
Am I Radiol 1978 ; 131 : 173 - 9
36. ALPEROVITCH A., LE MINOR M.
Quelques remarques sur la notion de stratégie
diagnostique optimale.
Radiol J CEPUR 1982 ;2 : 33 - 7.
37. BERTRANT P.
Comment évaluer un examen d'imagerie
Rev. Im Med 1991 ; 2 : 399 - 401.
38. GRENIER B.
Décision médicale : analyse et
stratégie de la décision dans la pratique médicale
Masson, Paris 1990 ; 246.
39. The sixth report of the joint National Committee on
prevention detection, evaluation and traitement of high blood pressure (JNC
VI)
Arch Intern Med 1997 ; 157 : 2413 - 2446.
40. Guidelines Subcommittee, 1999 World Health Organisation
Internation Society of hypertension guidelines for the management of
hypertention
J Hypertens 1999 ; 17 : 151 - 183.
41. MONNIER J.P. et al.
Radiodiagnostic
Masson, Paris 1990 ; 5 - 34.
42. VAQUEZ H. et BORDET E.
Radiologie du coeur et des vaisseaux de la base, Paris
1928.
43. BORDET E.,
La dilatation du coeur. Etude radioscopique, Paris, 1929.
44. UNGERLEIDER H.E et GUBNER R.
Evaluation of heart size measurements
Am Heart J, 1942 ; 24 : 24 - 494.
45. SAHN D.J., De MARIA A., KISSLO J., WEYMAN A.
The committee on M-mode standarisation of the American
society of Echocardiography: recommendations regarding quantitation in M-mode
achocardiography results of a survey of echocardiographic methods.
Circulation 1983; 58 : 1072 - 83.
46. GANAU A., DEVEREUX R.B., ROMAN M.J., de SIMONE G.,
PICKERING T.G.,
SERGIO SABA P., VARGUI P., SOMONGINI I., LARAGH J.H.,
Patterms of left ventricular hypertrophy anf geometric
remodeling in essentiel
hypertension
Am Coll Cardiol 1932 ; 19 : 1550 - 8.
47. WEINSTEIN M.C., FINEBERG H.V.
Clinical decision analysis,
WB Sanders Company, Philadelphie 1980 : 121 - 127.
48. METZ Ch. E.
Basic principales of ROC analysis
Sem Nucl Med, 1978 ; 8 : 283 - 298.
49. SWETS J.A.
ROC analysis applied to the evaluation of medical imaging
techniques
Invest radiol 1979 ; 14 : 109 - 121.
50. SWETS J.A., PICKETT R.M., WHITEHEAT S.F. et al.
Assessment of diagnostic technologies
Sciences 1979 ; 205 : 753 - 759.
51. FRANZ I.W. et al.
Long terme studies in regression of left ventricular
hypertrophy. J. Cardiovasc Pharmacol 1991 ; 17 (Suppl. II) ; 87 -
93.
52. M'BUYAMBA - KABANGU J.R., FAGARD R., LIJNEN P., STAESSEN
J., DITU M.S., TSHIANI K.A., AMERY A.
Epidemiologycal study of blood Pressure and hypertension in a
sample of urban Bantu of Zaïre.
J Hypertens 1986; 4: 485 - 91.
53. LONGO-MBENZA B., PHANZU-MBETE L.B., MBUYAMBA-KABANGU
J.R., TONDUANGU K., MVUNZU M., MUVOVA D., LUKOKI-LUILA E. et al.
Hematocrit and stroke in black Africans under tropical
climate and meteological influence.
Ann. Med. Interne 1999; 150 (3); 171 - 177.
54. WORLD HEALTH ORGANIZATION
Non communicable disease: A strategy for the african
region
WHO Regional Office for Africa, Harare, 2000.
55. CASALE P.N. et al.
Value of echocardiographic measurement of left ventricular
mass in prediting cardiovascular morbid events in hypertensive men
Ann Intern Med, 1986 ; 105 : 173 - 8.
56. LEVY D.
Pronostic implacations of echocardiographically determined
left ventricula mass in the Framingham Heart Study
N Engl J Med 1990 : 1561 - 6.
57. KANNEL W.B
Prevalence and natural history of echocardiographic left
ventricular hypertrophy.
Am J Med 1933 ; 75 (Suppl 3 A) : 4 - 11.
58. BABATUNDE O.O., GBADEDO T.D., PORTER V.D., WILKENING B.,
HALL V.D. Racial Differences in Ambulatory Blood Pressure and
Echocardiographie
Left Ventricular Geometry
Am J Med Sci 1998; 315 (2) : 101 - 109.
59. GOURGON R. et al.
Hypertrophie ventriculaire gauche. Avantages et
incovénients Ann Cardiol Argeiol 1986 ; 35 : 607 - 15.
60. De SIMONE G. et al.
Hemodynamic hypertrophied left ventricular patterms in
systemic hypertension.
Am J. Cardio, 1987 ; 60 : 1317 - 21.
61. GOSSE P. et al.
Caractéristiques morphologiques et fonctionnelles du
coeur dans l'hypertension artérielle non traitée
Arch Mal Coeur 1991 ; 84 : 1823 - 6.
62. BROUSTED C., WANGERMEZ J. et al.
Etude comparative des mesures du volume cardiaque par la
méthode de stratigraphie axiale transversale et les méthodes
géométriques téléradiographiques
Journ. Radiologie 1960 ; 41 : 417 - 431.
63. DEVEREUX R.B., CASALE P.N., WALLERSON D.C. et al
Cost-effectiveness of echocardiographiy and
electrocardio-graphy for detection of left ventricular hypertrophy in patients
with systemic hypertension
Hypertension 1987 ; 9 (Suppl II) II - 69 - 76.
64. POST W.S., LEVY D.
New developments in epidemiology of left ventricular
hypertrophy
Curr Opin Cardio 1994 ; 9 : 534 - 541.
65. REICHEK., DEVEREUX R.B.
Left ventricular hypertrophy : relationship of anatomic,
echocardiographic and electrocardiographic findigs
Circulation 1981 ; 63 : 1391 - 8.
66. BLACKBURN H., KEYS A., SIMONSEN E., RAUTAHARJU P.,
PUNSAR. S.
The electrocardiogram in population studies : a
classification system
Circulation 1960 ; 21 : 1160 - 1175.
67. KANNEL W.B., DANNEMBERG A.L., LEVY D.
Population implications of electrocardiography left
ventricular hypertrophy
Am J Cardiol 1987 ; 60 : 851 - 931.
TABLE DES MATIERES
DEDICACE
i
REMERCIEMENTS
ii
INTRODUCTION
1
CHAPITRE 1. GENERALITES
3
1.1. METHODES DIAGNOSTIQUES
3
1.1.1. Electrocardiogramme
3
1.1.2. Radiographie thoracique.
4
1.1.3. Echocardiographie
4
1.2. HYPERTROPHIE VENTRICULAIRE GAUCHE (HVG)
5
1.3. QUALITES MESUREES PAR UNE METHODE
DIAGNOSTIQUE
6
1.3.1. Avoir une bonne qualité technique
6
1.3.2. Avoir une interprétation
7
1.3.3. Apporter une information valide.
7
1.3.4. Etre utile à la prise de
décision.
8
1.3.5. Etre efficace pour le malade et la
population.
9
CHAPITRE 2. METHODES
10
2.1. NATURE ET CADRE DE L'ETUDE
10
2.2. PATIENTS
10
2.2.1. Critères d'exclusion
10
2.2.2. Critères d'inclusion
10
2.3. EXAMEN CLINIQUE
11
2.4. EVALUATION DE L'HVG
11
2.4.1. Méthode Radiologique
11
2.4.2. Electrocardiogramme
14
2.4.3. Echocardiogramme
15
2.5. DEFINITION DE L'HVG ET DE LA GEOMETRIE
VENTRICULAIRE GAUCHE
16
2.5.1. Définition radiographique.
16
2.5.2. Définitions
electrocardiographiques
16
2.5.3. Définitions
échocardiographiques.
16
2.6. VALIDITE DES METHODES DIAGNOSTIQUES
17
2.7. ANALYSES STATISTIQUES
19
CHAPITRE 3. RESULTATS
20
3.1. AGE
20
3.2. PRESSION ARTERIELLE ET VARIABLES
ANTHROPOMETRIQUES
20
3.3. DONNEES RADIOGRAPHIQUES.
21
3.4. DONNEES ELECTROCARDIOGRAPHIQUES
22
3.5. PARAMETRES ECHOCARDIOGRAPHIQUES
23
3.6. MATRICE DE CORRELATIONS DANS LA POPULATION
D'ETUDE.
25
3.7. VALIDITE DES TESTS DIAGNOSTIQUES DE L'HVG
25
3.7.1. Radiographie du Thorax.
25
3.7.2. Electrocardiogramme (ECG)
26
3.7.3. Détermination de seuil de
décision
27
CHAPITRE 4. DISCUSSION
30
4.1. PREVALENCE DE L'HVG
30
4.2. VALIDITE DIAGNOSTIQUE DE LA RADIOGRAPHIE DU
THORAX
32
4.3. VALIDITE DIAGNOSTIQUE DE L'ECG
33
CHAPITRE 5. CONCLUSIONS ET RECOMMANDATIONS
35
5.1. CONCLUSIONS
35
5.2. RECOMMANDATIONS
35
5.2.1. A l'autorité sanitaire
étatique
35
5.2.2. Aux médecins radiologistes
35
5.2.3. Aux chercheurs
36
5.2.4. Aux médecins
36
REFERENCES
37
TABLE DES MATIERES
44
| 


