|
MINISTERE DE L'ENSEIGNEMENT SUPERIEUR ET DE LA
RECHERCHE
SCIENTIFIQUE
UNIVERSITE DE FARHAT ABBAS -SETIF-
FACULTE DES
SCIENCES DE LA NATURE ET DE LA VIE
DEPARTEMENT DE MICROBIOLOGIE
MEMOIRE
En vue d'obtenir le Diplôme des
ETUDE SUPERIEURES
Option : Microbiologie
Présenté par
Bennani
Youcef
LE miLDiou DE LA pommE DE tErrE
Encadreur: Mr Aissaoui Mohamed Ridha.
President: Mme Aliouche Halima.
Session : 2010-2011
Remerciements
Je remercie tout d'abord Allah qui m'a
donné la santé et le courage
pour terminer ce
mémoire.
Je tiens à présenter ma profonde
gratitude et mes sr42cres
vesseur Aissaoui Mohamed qui m'a
fait
bénéficier de son savoir et de ses conseils
éclairés afin de perfectionner ce
travail. Je le remercie
également pour sa disponibilité et son
encouragement.
Je tiens à remercier et
à présenter ma profonde gratitude et
reconnaissance a mes amies
Hicham Wissam Asma Badro
Fatiha Nabila
qui mon guidé tout au
long de ce travail et pour leurs aide, leurs
précieux
conseils.
Dédicace
Dieu tout Puissant merci pour le pouvoir et le courage
que vous m'a donné pour compléter ce travail. Je
dédie ce modeste travail à :
*Ma mère pour son encouragement et
bienveillance.
*Mon père, pour son soutien et aide.
* Mes fr~res et ma soeur chacun par son nom.
*A tous mes coll~gues d'étude
spécialement
*A tous ceux qui aiment la science et la recherche
scientifique.

Sommaire
Résumé
1 #177;
Introduction...........................................................................1
1.1- Le mildiou de la pomme de terre
.............................................2 1.2- La famine Irlandaise de la
pomme de terre...................................2 1.3- utilisation du P.
infestans comme arme biologique..........................2
2 - Origine et migration du Phytophthora infestans
«..................................3« 2.1-L'origine de
Phytophthora
infestans...........................................3« 2.2-
Première migration du
P.infestans.............................................3«
2.3- Seconde migration du
P.infestans..............................................4 2.4-
Diversité des populations du
P.infestans...................................... 5
3 - Biologie du
P.infestans...............................................................
6 3.1- Caractères
morphologiques...................................................... 9 3.2-
Génétique.....................................................................
10
4- L'isolement de
P.infestans..........................................................«
11 4.1- L'isolement de P.infestans du tissu infecté
.................................« 11
4.2- L'isolement de
P.infstans des tubercules infectés ......................... 12
4.3- L'isolement dans la gélose après le transfert des tranches
de pomme de
terre.......................................................................................
12
5- Multiplication de P.infestans
......................................................« 12
5.1- Sur feuilles ou sur tranche de pomme de terre
............................« 13 5.2- La culture pure sur les plaques
agar-agar..................................« 14
6- Cycle de développement et
épidémiologie....................................... 16
7- Symptôme de mildiou
...............................................................« 18
7.1-Les
dommages..................................................................20«
8- Les méthodes de
luttes...............................................................21
8.1 La lutte chimique
.............................................................. 21 8.1.1-
Problèmes de résistance aux fongicides
...........................22
8.2- La lutte génétique
............................................................23
8.3- La lutte
biologique............................................................23 8.3.1-
L'utilisation de Trichoderma........................................
24 8.3.2- L'utilisation de Pseudomonas
«.......................................24
Conclusion................................................................................
26
Références bibliographiques

Résumé
Le mildiou est dû à un champignon microscopique,
phytophthora infestans (Mont) de Bary. Ce parasite
attaque plusieurs espèces de la famille des solanacées en
particulier la pomme de terre et la tomate et certaines morelles.
Le mildiou se manifeste quand le temps est humide et les
températures douces, dans ces conditions, et comme les cycles de
multiplication asexuée sont courts, le développement de la
maladie peut être très rapide et détruit la plantation en
quelques jours seulement et peut tuer le feuillage et les tiges des plantes de
pommes de terre et de la tomate en tout temps durant la saison de croissance.
Le vent favorise la dispersion des sporanges sur plusieurs centaines de
mètres, voire davantage.
La littérature et les observations des
centres de recherches indiquent qu'il existe aussi une forme
sexuée de reproduction du champignon. Quand une forme A1 est
confrontée à une forme A2, dans des conditions propices, les
mycéliums peuvent localement fusionner et produire des oospores; fruits
d'un brassage génétique constituant une source de
variabilité des populations de mildiou; les oospores qui
peuvent survivre quelques années dans le sol.
Pour lutter contre le mildiou, en plus des ressources
intervenant la résistance variétale, l'emploi
répété de produits fongicides s'avere la solution la plus
employée en pratique, donc la priorité de la stratégie de
lutte est d'emprcher autant que possible l'implantation du parasite dans les
espèces hôtes.
Mots-clés: Phytophthora
infestans, mildiou, pommes de terre, épidémiologie,
reproduction asexuée, reproduction sexuée,
mycélium, oospores.
Abstract
Potato late blight caused by the oomycete Phytophthora
infestans; this parasite attacks several families' species of solanaceae
especially the Potato, and the tomato.
The late blight manifests itself when the weather is humid and
temperatures seem to be soft, in these conditions, and as the cycles of
non-sexual multiplication are short the development of disease can be very
quick leading to destroy the planting in few days only, and can exhaust potato
plants foliage and stems as with tomato too during the growth season. The wind
enhances the dispersion of sporangia along several hundred of meters, or even
more.
Literature and observations of research centers point out that
there is also another sexual reproduction's form of the oomycete, when a form
A1 is confronted to another form A2, and in advantageous conditions, mycelium's
can merge together and will produce oospores, like a result of a genetic mixing
to made up a new source of various potato late blight populations like oospores
which can survive some years in the soil.
To fight the late bright, more than one mean using speculation
resistance, the repeated use of fungicidal products is the most used solution
in practice, therefore the strategy having priority to realize this struggle is
to prevent the establishment of the parasite, as many as possible, in the host
species.
Key words: Phytophthora infestans, late
blight, Potato, epidemiology, non-sexual reproduction, sexual reproduction,
mycelium, oospores.

1- Introduction :
Les Phytophthora sont répondus sous toutes les
latitudes ; leur rôle en pathologie végétale est important
car la gamme des plantes auxquelles ils s'attaquent est très large. Dans
le couple ``hôte-parasite'', les deux populations antagonistes ne
s'affrontent pas a armes égales car, si la population des espèces
parasites dispose de moyens extrêmement efficaces pour varier et
s'adapter a toute modification de la population hôte , celle-ci pour des
raison pratiques et économiques ;tend dans l'agriculture moderne, vers
l'uniformisation des variétés a la fois dans le temps et dans
l'espace.
Le pouvoir saprophytique des Phytophtora est tenu
pour être médiocre, ils se maintiennent cependant fort bien dans
le sol sous la forme de spores résistantes (chlamidospores, oospores) ou
plus brièvement sous la forme de sporocystes voire de
mycéliums.
Dans ces conditions, le sol constitue souvent le principal
réservoir d'inoculum pour un grand nombre d'espèces et rend la
lutte par les méthodes agronomique ou chimiques traditionnelles
onéreuses et incomplètement efficaces .la nécessité
d'organiser la lutte sur le plan génétique, en opposant aux
parasites un matériel végétal sélectionné
pour sa résistance, s'est imposée.
Ceci explique que de très nombreux travaux notamment
ceux de Lionian(1925), Waterhouse(1931), Gooding-Lucas(1959), Tarjot(1965)
aient été consacrés a l'analyse du rôle joué
par des facteurs extrêmes comme les constituants du substrat, la
température, l'eau, la composition de l'atmosphère,
l'éclairement, dans la formation des sporocystes et l'émission
des zoospores. Dans les conditions naturelles, ces caractéristiques de
l'environnement sont modifiées, par la présence de plantes
supérieurs .aussi avons-nous tentés de déterminer dans
quelle mesure et de quelle manière les plantes supérieurs
interviennent dans le déroulement du cycle saprophytique des
Phytophthora jusqu'à ce que celui-ci s'achève par
l'entrée en contact du parasites avec son hôte, c'est-a-dire
jusqu'à l'amorce du cycle parasitaire.
1.1- Le mildiou de la pomme de terre :
Le mildiou causé par le champignon Phytophthora
infestans est une maladie qui préoccupe depuis toujours les
producteurs de pomme de terre car cet organisme pathogène de La famille
de Solanacée peut causer des pertes considérables dans cette
culture. Bien que le mildiou puisse affecter la tomate de champ, cette maladie
atteignait rarement des proportions épidémiques au sein de cette
culture. (Andrivon, 1995)
1.2- La famine irlandaise de pomme de terre :
Bien que la pomme de terre ait subi quelques problèmes
avec les maladies elle a été considérée comme une
récolte sûre, mais en 1845 une nouvelle maladie inconnue a fait
son arrivée, en tuant la tige et en détruisant le tubercule dans
les champs. L'apparence dramatique G IIRENYITaSh3M111e1SRP P 111} 13MIFI ARP P
HIlon a appelé cette maladie) en Europe ensuivie dans le
désespoir humain dans beaucoup de pays comme Les Pays-Bas, la Suisse et
la France, mais les conséquences de la maladie dans L'Irlande
était de loin le pire. Les villageois irlandais étaient plus ou
moins complètement la personne à charge sur la pomme de terre
pour produire un régime de subsistance sur leurs petits lots de terrain.
Durant 1845 ~ 1850 la pomme de terre irlandaise récoltée a
rétréci et le manque de graine provoqué par la plaie. La
perte de la récolte de pomme de terre s'est ensuivie dans la famine et
la mort de plus de 1 million de personnes. Cela a, à son tour,
provoqué l'immigration de 1.2 millions d'irlandais, essentiellement aux
Etats-Unis (Eriksson, 1916; Grand, 1946; Salaman, 1949; Bourke, 1991; le
Tourneur, 2005).
1.3- Utilisation comme arme biologique :
Le mildiou de la pomme de terre fut l'un des plus de 17 agents
que les États-Unis ont étudiés comme armes biologiques
potentielles avant que le programme d'armes biologiques soit suspendu. La
France, le Canada, les États-Unis et l'Union soviétique ont
également fait des recherches sur le Phytophthora infestans
comme arme biologique durant les années 1940 et 1950.(
Frédéric Suffert, Émilie Latxague, Ivan Sache,2009).
2- Origine et migrations du Phytophthora infestans :
2.1- L'origine de P. infestans :
Il est cru par la plupart des chercheurs que P.
infestans naît du mexicain pays montagneux. À l'origine,
c'était seulement ici que les types s'accouplant pourraient être
trouvés qu'à un 1:1 de rapport. La population de P.
infestans dans cette région a été trouvé pour
être très divers, tant phénotypiquement que
génétiquement (Goodwin et Drenth, 1997; Grünwald et al.
2001). Aussi, les nombreuses espèces indigènes de
Solanacée résistantes à P. infestans
trouvé dans le Mexique Central indiquent que cette région est la
région d'origine du pathogène (Niederhauser, 1991).
2.2- Première migration du P. infestans :
En Amérique du Nord, le mildiou a été
observé pour la première fois en 1843 près de Philadelphie
aux États-Unis tandis qu'en Europe cette maladie a fait son apparition
en Belgique en 1845. Par la suite, le mildiou atteignait rapidement toutes les
régions productrices de pomme de terre à travers le monde. Les
tubercules de pomme de terre contaminés par P. infestans
représentaient le véhicule de choix pour transporter et
disperser ce champignon phytopathogène. Diverses hypothèses
furent énoncées pour expliquer le lieu d'origine des migrations
du P.infestans vers l'Amérique du Nord et l'Europe. Celle
retenant le plus l'attention, stipule que le centre d'origine du
P.infestans est localisé dans les montagnes du Mexique
central puisque dans cette région la diversité des populations du
champignon est maximale et la reproduction sexuée semble existée
depuis toujours. Ainsi la théorie la plus acceptée aujourd'hui
est donc celle préconisant une migration du P.infestans
à partir du Mexique vers les États-Unis et de là vers
l'Europe. Il n'est également pas exclu que le champignon puisse avoir
été transporté directement du Mexique vers l'Europe.
(Andrivon, 1996)
2.3- Second migration du P. infestans :
En Amérique du Nord, c'est en 1979 qu'une nouvelle
population du P. infestans (connue sous le nom d'US-6) a
été vraisemblablement introduite en Californie aux
États-Unis. Il semble qu'elle est entrée via des fruits de tomate
en provenance de la région du nord-ouest du Mexique. En Californie, le
mildiou n'avait pas été observé sur la tomate depuis 32
ans soit jusqu'à l'avènement de l'épidémie de 1979.
Cette nouvelle population du P. infestans (US-6) est donc
présumée responsable de cette infection sévère sur
la tomate. (Goodwin et al., 1994)
Cependant, cette population du P. infestans (US-6) ne
peut expliquer les épidémies de mildiou que les États-Unis
et le Canada ont connu depuis le milieu des années 1990. L'explication
la plus possible pour justifier l'émergence de ces
épidémies du mildiou en Amérique du Nord est la migration
massive, juste avant ou durant l'année 1992, de nouvelles populations du
parasite comme les lignées US-7 et US-8(Goodwin et al., 1998). L'analyse
de ces nouvelles populations du P. infestans présentes en
Amérique du Nord démontre qu'elles proviendraient des
régions productrices de pomme de terre et de tomate du nord-ouest du
Mexique (Fry et al. ,1993). Les tubercules de pomme de terre ainsi que les
transplants et fruits de tomate infectés permettent le transport sur de
longues distances de l'agent responsable du mildiou. (Legard et Fry, 1995).
2.3- Diversité des populations du P. infestans :
Depuis les annees 1990, le mildiou de la pomme de terre et de
la tomate connaît un nouvel essor aux États-Unis et au Canada. La
cause première de ces graves infections par le mildiou est associee
à la migration recente de nouvelles populations du P. infestans
(Goodwin et al. ,1998). Avant 1980, (1EQaISNe IGIN CSRSXla2IRQN
GX FhaP SLIQRQ GéP RQ2reEqXIXQe1N1X0 1 lignee est presente dans les
diverses regions du monde laquelle est nommee US-1. Une exception existe, soit
le Mexique central où la diversite du P. infestans est
particulièrement grande. En fait la lignee US-1 est issue de la
première migration du P. infestans en Amerique du Nord et en
Europe (Fry et al. ,1993).
La lignee US-E ITN2 SIiQFISD3P 1Q2 Sa2KRTqQ1IFK9 la SRP P 1 Ge
2ILIHEIQ TX'FIONSIX2 occasionnellement infecter la tomate. Cette information
permet de comprendre pourquoi le P 1lGiRX0QAI22eLIQEi2NSIN GeNESIRSRr2ERQN
pSIGbP EqXIN GEQNileNEFXl2XreN Ge12RP a2e avant (IiQ2IRGXF2iRQ GeIQRXNHOeN
lITQéeN. IYIEQ qXEMITQée T18 6-1 dominait aux États-Unis
et au Canada depuis son introduction, elle est desormais rare, voire absente
(Fry et al. ,1993).
( ($ P plI1Xe EGX11 RTGEGeN FIaQJIP IQ2NTRQ2 FRP P eQFé
àIN'IQN2KIDIEGaQN Os populations du P.infestans au debut des
annees 1980 mais les principaux bouleversements prennent place durant les
annees 1990 (Daayf, 2000).
Au Quebec, il apparaît que depuis 1994, la lignee la
plus frequemment identifiee est US-8. Cette nouvelle affQéH 11SrINeQ2M
XQeTP eQaFILSlXN NOINXNe SXiNqX'elle a la FaSaFi2é GI E se propager plus
rapidement et de causer des dommages plus importants. Cette virulence accrue
lui est conferee par les caracteristiques suivantes : developpement de
brûlures foliaires Ge ESRXN gIEQGeN 1GiP eQNiRQN, FESEFi2é
G'IQfeF2erJIeN I2igIN I2 GeIFIXNeIIGeN FREQFrIN, NSRrXG2IRQ davantage abondante
et rapide, germination des spores prompte et accrue. Ces caracteristiques en
plus de la resistance au metalaxyl, ont donc permis à la lignee US-8 de
predominer et de GélRJRIlEREQé11G1RUTIQe118 6-1(Daayf,
2000 ). Bien que la lignee US-8 est principalement rapportee pour causer des
dommages chez la pomme de terre, il demeure que depuis 1997 elle E
é2é 11NR4é0G1éF1aQ216RQN GITSCIQ2N GI
2RP a2e IQ STRIeQTQFe IGe 14 Oe GX 311QFne GRXErG, GI RI Nouvelle-Écosse
et du Quebec (Fry et al. ,1992).
3-La biologie de Phytophthora infestans :
-Classification selon (Mont.) de Bary, 1876: Domaine :
Eukaryota
Règne : Chromalveolata
Division : Stramenopiles
Classe : Oomycetes
Ordre : Peronosporales
Famille : Peronosporaceae
Genre : Phytophthora
Espèce : Phytophthora infestans
- les principales phases du cycle de développement du
champignon et la maladie sont présentées dans la figure 1.
En retard le mildiou est considéré par la
plupart des chercheurs comme une maladie fongique, mais le
Phytophthora, le genre, n'est pas rattaché à de vrais
champignons. Il appartient à l'oomycètes du royaume
Straminopila qui inclut des algues marines par exemple d'or et marron
(de Bary, 1876). Les oomycètes sont caractérisés
par leur capacité de libérer des zoospores asexués
heterokont formés dans les sporanges. Les parois de cellule
d'oomycètes contiennent la cellulose à la
différence des vrais champignons qui contiennent de la chitine .les
Oomycètes sont diploïde pour la partie importante de leur cycle de
vie, et la reproduction sexuelle se produit par le développement
d'oospores. &'est le résultat de l'assemblage d'oogones et
anthéridies (Harrison, 1992; Judelson et Blanco, 2005). Les
oomycètes sont un groupe très varié de micro-organismes
qui incluent saprophytes aussi bien que pathogènes de la plupart des
classes des organismes aux limites des vertébrés et des plantes
à d'autre oomycètes.
Pendant la phase épidémique P.
infestans est étendu par sporanges aéroportés qui
sont formé sur les plantes infectées .Dans les conditions de
température modérée (~20°C) et t'humidité de
Tt'air élevée (RH> de 90 %) un nombre massif de sporanges peut
être formé dans une récolte infectée. Les sporanges
sont d'habitude libérés le matin où le la
température montant provoque une diminution pointue dans
l'humidité de t'IirT(de Bary, 1876; Lacey,
1965; Andrivon, 1995). Les sporanges sont alors étendus
par les mouvements aériens. Quand ils sont déposés sur une
plante hôte susceptible ils iront infecter, dans les conditions moites
(libérez de l'eau sur la surface de feuille) .l'infection peut survenir
par la voie directe par le sporangium lui-même ou par la voie indirecte
via la libération de 5 à 10 motile zoospore par sporangium,
chacun peut à son tour infecter la plante hôte. Le point de
rupture entre la germination directe et indirecte a l'air est autour de
15°C, (Harrison, 1992; Judelson et Blanco, 2005) par la voie indirecte,
étant l][QfITFt[oQIQa plus commune au-dessous de cette
température, par contre l'infection directe domine en-dessus de
15°C. À la germination le sporange et les zoospores forment des
tubes de germe et infectent par la formation d'appressoria et patères de
pénétration. Après la pénétration une
vésicule d'infection est formée et les hyphes grandira tant inter
- qu'intracellulaire et développera l]haustorium pour extraire des
aliments de l'intérieur des cellules de l'hôte, et
détruisent ainsi le tissu vital (Grenville-Briggs et van West, P.
2005). Après une période latente aussi courte que 3
jours (Flier et Turkensteen. 1999; Carlisle et al, 2002) de nouveaux
sporanges sont formés et étendus pour infecter de nouvelles
plantes. La propagation rapide et efficace, ainsi que l'infection et la
colonisation de la plante hôte offre le potentiel de détruire
toutes les parties souterraines.
Quand cela arrive, selon le cycle de développement de
la récolte, le résultat peut être des pertes de production
quantitatives très élevées. Les tubercules de pomme de
terre peuvent aussi être infectés si les sporanges sont
enfoncés dans le sol (de Bary, 1876; Lacey, 1965; Andrivon, 1995).
L'infection de tubercule réduira la qualité de la récolte
et si la grande proportion des tubercules est infectée, il peut
s'ensuivre la perte de récolte totale. Un autre aspect très
important de cela est que les tubercules infectés peuvent fonctionner
comme inoculum pour une autre épidémie à la saison
suivante (Andrivon, 1995). P. infestans à deux types
s'accouplant a désigné A1 et A2 et peuvent d'habitude subir la
reproduction sexuelle seulement si les deux types s'accouplant sont
présents. Les isolats auto fertiles de P. infestans peuvent être
trouvés, mais leur rôle et importance ne sont pas
complètement compris (Élégant et al. 1998).En plus de la
variation génétique augmentée par la recombinaison, la
reproduction sexuelle donne aussi au pathogène la possibilité de
survivre entre les saisons dans le sol sous forme d'oospores (Andrivon,
1995).
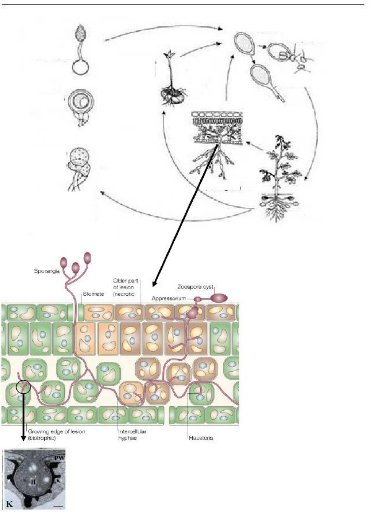
oogonium antheridium
reproduction sexuée
sporulation
sur les feuilles
tube germinatif
plante infectée
Figure 1 :Cycle biologique de P.
infestans
a.
c.
(a) Schumann 1991 ; (b) Judelson et Blanco 2005 ; (c) Hardam
2008
3.1- Caractères morphologiques :
- Les Colonies poussent de façon radiale,
compacte sans marge nette, Le mycélium, elles sont duveteuses et
présentent de courts hyphes aériens.
-Le Sporange : présente une papille
caractéristique. Les sporanges sont terminaux, rarement intercalaires.
Ils sont caduques et portent un court pédicelle (3 um); ils ont une
forme ovoïde, ellipsoïdale à limoniforme.
-Les sporangiophores sont isolés ou
organisés en sporanges arrangés en bouquet. Ses dimensions sont
de 19-55um×16-46um.
-Chlamydospores : Cette souche ne produit pas de
chlamydospores.
-la reproduction : Il existe une reproduction
asexuée qui utilise des zoospores biflagellées. Reproduction
sexuée : Les anthéridies, sphériques à globuleuses,
fécondent l'oogone de façon amphigyne). La fécondation est
hétérothallique. Les oogones, hyalines, présentent une
paroi lisse et sont plérotiques (31-50 um). Les oospores germent en
produisant un sporange ou du mycélium.
Sporangia et sporangiophores de P. infestans,
hautement grossi.
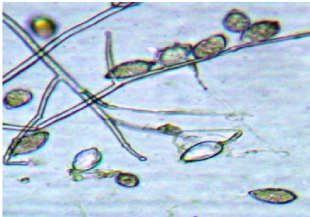
Photo : B. Bushe,2000.
Ces sporangia en forme de citron peuvent germez directement ou
provoquer la libération du nageant zoospores qui peut infecte des tissus
hôtes. Deux des sporanges à la photographie ayez l'air
d'être transparents et être effectivement vides, en ayant
renvoyé leurs contenus. Il est très important de comprendre cette
maladie, qui peut tuer des plantes dans quelques jours.
3.2- Génétique :
Le séquençage du génome de
Phytophthora infestans a été achevé en 2009. On a
constaté que ce génome est considérablement plus grand
(240 Mb) que celui des autres espèces de Phytophthora dont le
génome avait déjà été séquencé
; Phytophthora sojae a un génome de 95 Mb et Phytophthora
ramorum de 65 Mb. Il contient aussi une variété
différente de transposons et de nombreuses familles géniques
codant pour des effecteurs (protéines) qui sont impliqués dans
les propriétés pathogènes de l'oomycète. Ces
protéines sont divisées en deux groupes principaux selon qu'elles
sont produites par l'oomycète dans le symplasme (à
l'intérieur des cellules végétales) ou dans l'apophase
(entre les cellules végétales). Les protéines
formées dans le symplasme comprennent les protéines RXLR, qui
contiennent une séquence arginine-X-leucine-arginine (où X peut
être n'importe quel séquence d'acides aminés) à la
terminaison aminée de la protéine. Les protéines RXLR sont
des protéines d'virulence, ce qui signifie Tu'elles Seu\ent être
détectées par la plante et provoquer une réponse
hypersensible, tuant l'oomycète. On a découvert que
Phytophthora infestans contient environ 60 % de plus de ces
protéines que d'autres espèces de Phytophthora et cela
peut lui permettre de vaincre les défenses de l'hôte plus
rapidement. Celles trouvées dans l'apoplaste comprennent des enzymes
hydrolytiques telles que protéases, lipases et glycosylases qui
dégradent les tissus des plantes, des inhibiteurs d'enzymes pour la
protection contre les enzymes de défense de l'hôte et des toxines
nécrosantes. Globalement, le génome à un contenu
répétitif extrêmement élevé (environ 74 %) et
une distribution des gènes inhabituelle en ce que certaines zones
contiennent de nombreux gènes tandis que d'autres en contiennent
très peu (Brian Haas, et al. 2009) (Sudeep Chand.2009).
4- L'isolement de P. infestans :
Il y a de différentes façons d'isoler P.
infestans du tissu infecté, mais les deux voies communes sont
de :
1) transférer le hyphe fongique et sporange directement
sur le milieu dans une boite Pétri,
2) placer le tissu infecté à l'intérieur
d'un milieu sélectif.
Le premier d'entre ceux-ci implique généralement
de cultiver le champignon sur les tubercules de pomme de terre et le
deuxième sur le tissu de feuille ou le tubercule (Caten, 1968).
Dans notre expérience, les génotypes de pomme de
terre sont plus faciles à isoler avec la méthode 1. En tout cas,
il est toujours plus facile d'isoler d'une infection récente qui
commence juste à sporuler.
P. infestans est relativement facile à
maintenir en vie par les inoculations répétées sur le
tissu vivant. D'autre part, P. infestans est quelquefois difficile
à faire entrer dans la culture pure. Donc, il faut garder votre isolat
vivant sur le tissu vivant jusqu'à ce qu'il soit purifié avec
succès (Caten, 1968).
4.1- L'isolement P. infestans de la pomme de terre
infectée :
1. Les lésions de Sporulation sur le tissu de feuille,
pris du champ, sont lavées à l'eau douce et placées dans
une chambre humide (a inversé la boite de pétri avec la
gélose diluée) tout en exposant le côté axial de la
feuille vers le haut.
2. Les plaques sont incubées à 15-18°C
pendant 1 jour ou jusqu'à ce que la sporulation fraiche apparaisse.
3. De petits morceaux du tissu infecté, de la
frontière de sporulation de la lésion, sont coupés et
placés sous les tranches de pomme de terre dans une boite pétrie
vide.
4. Les boites sont incubées à 15-18°C pendant
1 semaine, jusqu'à ce qu'il y ait sporulation abondante sur le
côté supérieur de la tranche.
5. Pour réinoculer les feuilles, choisissez des
sporanges du haut du tubercule et placez-les dans une goutte d'eau sur une
feuille de pomme de terre ou une autre tranche de tubercule. Vous pouvez
répéter les étapes 2-5 plusieurs fois pour garder votre
isolat vivant.
IV.2- L'isolement de P. infestans des tubercules
infectés :
Pour isoler des tubercules infectés, coupez le
tubercule ouvert où l'infection s'est produite et placez-le dans une
chambre humide jusqu'à ce que la sporulation soit produite ; suivez
alors les mêmes étapes sur la section.
IV.3- L'isolement dans la gélose après le
transfert des tranches de pomme de terre :
Une fois l'inoculum apparaît sur le côté
supérieur d'une tranche de tubercule infectée ou d'une feuille,
les sporanges sont récoltés dans une chambre d'écoulement,
en les recueillant avec une aiguille inoculant et en plaçant le sporange
sur le milieu sélectif, Ne touchez pas la tranche de pomme de terre ou
la feuille avec l'aiguille. L'utilisation d'un stéréoscope est
fortement utile, directement de la feuille infectée ou du tissu de la
tige (Caten, 1968).
Il est possible d'isoler le champignon directement du tissu de
feuille infectée, mais il est conseillé de produire l'inoculum
frais au moins une fois (Caten, 1968 ).
Pour isoler directement, un petit morceau de feuille
infectée de la frontière de sporulation, en incluant un petit peu
du tissu vert, qui est découpé et traversé par un colorant
en solution pendant 30 secondes, ensuite rincé dans de l'eau
distillée stérile deux fois de suite, puis séché
avec du papier filtre stérile. Les morceaux de feuille sont alors
placés sur le haut ou à l'intérieur d'un milieu
sélectif. Les plaques sont incubées à 18°C pendant
5-10 jours, ou jusqu'à ce que le champignon commence à grandir et
se nourrir de la gélose. Les bouts d'Hyphe sont alors
transférés à V8 ou sur les plaques agar agar de Seigle
boiles.
5- La multiplication de P. infestans :
Nous avons deux méthodes proposées pour multiplier
P. infestans, soit sur :
1) les feuilles ou les tranches de pomme de terre.
2) la culture pure sur les plaques agar-agar.
5.1- les feuiles ou les Tranches de Pomme de terre :
Nous multiplions souvent P. infestans sur les
feuilles ou les tranches de pomme de terre; essentiellement pour la production
d'inoculum, mais aussi pour la conservation de ce dernier.
5.1.1 Le fait de récolter de sporange et de
zoospores :
1. les sporanges sont lavés du côté
supérieur d'une lésion sporulant, sur une tranche de pomme de
terre ou une feuille de tomate avec de l'eau distillée, puis
tamisée à l'E1de1d'cn filtre maille de 30 micron pour enlever les
mycéliums et d'autres débris.
2. Le filtrat est alors passé par un filtre de maille
de 10micron, qui piège les sporanges. Ceux-ci sont lavés
plusieurs fois avec de l'eau potable et recueillis ensuite, du filtre avec une
petite quantité d'eau distillée.
3. Cette suspension sporangial est incubée à
6°C pendant 2 heures pour inciter la libération des zoospores. Si
on veut séparer les sporanges des zoospores, la suspension est de
nouveau passée par le filtre de maille de 10micron, dès que les
zoospores ont été libérés et le filtrat, qui en
contenant seulement les zoospores, est recueilli. La suspension de zoospore est
inoculée sur les tranches de tubercule ou les feuilles de pomme de terre
(en cas d'inoculum de pommes de terre) pour garder la croissance de
champignon.
5.1.2 L'inoculation de tubercules :
1. Choisisses des tubercules parmi les variétés
susceptibles, moyennes de grandeur si disponible, sans pourritures ni dommage
sévère ou coloration verte.
2. Laver les tubercules et laisser sécher.
3. stériliser La surface des tubercules en les piquant
dans l'alcool de 70 % durant quelques secondes, et les faire de décaper
au chalumeau.
4. Avec un couteau trempé dans l'alcool et
décapé au chalumeau, coupez la pomme de terre en tranches
épaisses d'environ 1 centimètre. Chaque tranche devrait avoir
deux surfaces de coupe. Débarrassés L'extérieurs la
plupart des parties des tubercules. Placez les tranches de pomme de terre sur
un filet de fil stérilisé dans les boîtes peu profondes de
plastique menus de papier filtre humide au fond. Le filet devrait être
à au moins 1 centimètre au-dessus du fond
du plateau. Deux gouttes de sporange ou de la suspension
zoospore seront placées sur les tranches de tubercule, les boîtes
sont fermées et placées dans une chambre humide et l'incubation
suit à 15-18°C pendant 1 semaine.
5.1.3 L'inoculation de feuilles :
1. Le prospectus de coupe se fait des feuilles
complètement développés de pomme de terre,
cultivées n'ayant pas atteint le stade de la floraison placées
dans de l'eau douce. Les feuilles doivent être en bonne état sans
signes de maladie ou de stress.
2. Rincer les feuilles et tapoter-les pour les
sécher.
3. laisser le côté axial en haut vers les
couvercles de boite pétri, inversés contenant la gélose
diluée, et inoculer avec deux gouttes du sporogone ou de la suspension
zoospore du P. infestans.
4. incubation à 15-18°C pendant 1 jour dans
l'obscurité, ensuite de 6 jours à un cycle de lumière de
14 heures. Pour la conservation de cultures de P. infestans, l'une ou
l'autre de ces deux procédures, peut être
répétée une fois par semaine. Seulement les spores
formés sur le côté non-inoculé des tranches de pomme
de terre ou de feuilles sont récoltées. Pour la production
inoculum, les spores du côté inoculé des tranches ou des
feuilles peuvent aussi être récoltées. Si aucune colonie
bactérienne n'est visible.
Une note sur la contamination! Soyez prudents avec la
contamination de tranches de tubercule (et part dans une certaine mesure) avec
Erwinia et d'autres organismes qui peuvent attaquer la pomme de terre.
Inoculez toujours des tranches de tubercule très propres (la filtration
comme ci-dessus) et diluez les quantités d'inoculum. Une goutte de 10
micron pour environ 50 zoospores fera attention à la contamination.
Comme Aussi, vous pouvez juste transférer des morceaux d'hyphe et de
sporange.
Sur les plaques agar-agar Fondamentalement toutes ces recettes
viennent de Catin et les Mouvements d'esquive (Caten, 1968; Caten, 1970) et
peut avoir été légèrement modifié par le
laboratoire de Bill Fry dans Cornell.
5.2- culture pure sur les plaques agar-agar :
Les milieux sélectifs :
Nous avons deux différents milieux sélectifs, l'un
est utilisé dans Cornell, et l'autre développé
par Hans Hohl (Hohl, 1991).
a) Pour le milieu de Cornell:
Antibiotiques
Vancomycine 100 mg / L
Polymixine B 50mg / L
Ampicilline 200 mg / L
La rifampicine 20mg / L
PCNB (75% WP) 67mg / L
Benlate (50% WP) 100 mg / L
1. Préparer 10% élucidés V8, et laisser les
médias refroidir juste après autoclavage.
2. Ajouter le mélange aux antibiotiques mentionnés
ci-dessus, mélanger et verser sur les plaques.
b) Pour le milieu Hohl:
Antibiotiques
La griséofulvine 20mg / L
Nystatine 19 mg / L
Benlate (50% WP) 10mg / L
Méthoxypurine 5 mg / L
Rifamycine 30 mg / L
L'acide nalidixique 5 mg / L
8-azaguanine 40 mg / L
Néomycine 30 mg / L
1. Préparer Rye B agar et laisser les médias
refroidir juste après autoclavage.
2. Mélanger les antibiotiques dans le DMSO, ajouter les
au milieu, bien mélanger, puis et couler en boîtes.
Vous pouvez également préparer des stocks
d'antibiotiques dans 10 ml de DMSO et entreposer des portions de 1 ml dans le
congélateur. Utiliser 1 ml de mélange pour 1 litre de milieu.
6- Le cycle de développement et
épidémiologie :
Les principales phases du cycle de developpement du champignon et
de la maladie sur la pomme de terre sont :
6-1 Conservation et foyer primaires :
Trois modes de conservation hivernale ont ete envisages chez
P. infestans : -survie dans le sol (en saprophyte ou sous forme
d'oeufs, issue de la phase sexuée
-conservation dans les tubercules infectes restant dans le sol ou
a proximite du champ. -et conservation dans les tubercules utilises comme
semences.
Il est aujourd'hui couramment admis que la survie en
saprophyte du champignon, sous forme de mycelium ou de cystes, est assez
limitee. Le champignon incube au contact de sol non sterilise ne resterait
infectieux que pendant 15 à 77 jours, selon le type et le traitement
expérimental. Cette durée se survie saprophytique limitée
est d'ailleurs un caractère assez general au sein du genre
Phytophthora, très infectieux a l'intervalle entre cultures,
elle ne permet pas d'envisager la présence de formes saprophytes du
champignon comme origine de l`inoculum primaire (P.Rousselle, Y.Robert,
1996).
L'existence de chlamydospores a d'abord été
envisagée, mais la plupart des travaux publies ensuite, ne retiennent
pas cette forme de survie. Par contre, l'existence d'oospores issues de la
reproduction sexuee, est bien etablie chez P.infestans. La
première observation remontent au début de ce siècle, mais
c'est Smoot et al (1958) qui établiront l'existence de deux type de
souche appartenant a des type sexuels opposes sont en presence, Les thalles de
chacun des type sont potentiellement bisexues, produisant a la fois des oogones
et des anthéridies sous l'effet d'hormones produites par les souches de
type oppose (Ko, 1978). Ceci explique que lors de croissement, on obtienne a la
fois des produits d'autofécondation et des hybrides (Shaw, 1987). ce
déterminisme hormonal de l'induction n'est pas spécifique ,
puisqu'il est possible d'induire la production d'organes sexuels chez les
souches A1 de P.infestans par conformation avec des souches A2 de
divers autre espèces , telle P.derechsleri , P.parasitica , P.
palmivora ou P.capsici (Shen et al., 1983).
Un suivie des type compatibilite sexuelle present dans les
populations naturelles de P.infestans a ete realise a la fin des annees 1950 au
Mexique ( Gallegly et Galindo, 1958)
puis dans divers autres pays (Fry et al., 1993). Ces suivies
ont montré, jusqu'au début des années 1980, le type A2
n'était présent qu'au Mexique central, oil il survenait en
proportion sensiblement égales aves le type A1 (Shaw, 1987). cette
observation semblait exclure toute possibilité d'intervention des
oospores dans le cycle biologique du parasite dans les région autres que
le centre du Mexique .des travaux récent montrent toutefois que .
Après l'introduction de souche de type A1 au cours de vingt
dernières années (Spielman et al.1991 ; Fry et al.1992-1993), la
production d'oospores IN VIVO est désormais possible en Europe
(Frinking et al., 1987) et que ces organes sont capable de survivre au hiver eu
champ et de réinfecter ensuite des cultures de pomme de terre (Pittis et
Shattock, 1994).
La source d'inoculum traditionnellement invoquée comme
étant a l'origine des foyers primaires de mildiou est constituée
de sporocystes produit sur des tubercules infectés, Soit restants dans
la parcelle ou a proximité immédiates de celle-ci durant la phase
hivernale (repousses, tas de triage), soit importés au printemps. Les
tas de triage, laissés en bordure de champs, constituent selon Boyd
(1974) la source principale d'inoculum primaire. Une méthode de lutte
prophylactique efficace est donc l'élimination précoce de ces tas
de déchets .concernant les plants , un grand nombre d'étude a
montré que seul une faible proportion des tubercules contaminés
donne des poussée porteuse de mycélium et de fructification du
champignon .Selon Robertson (1991) ,ceci s'explique par le fait que le
mycélium situé trop loin des jeunes pousses ne les atteint pas a
temps pour être entrainé hors de terre lors de la croissance de la
tige . La faible densité de pousses atteint à l'hectare explique
assez aisément le délai souvent important qui sépare
l'apparition de ces pousses et l'apparition des premières taches
foliaires.
7- Symptômes du mildiou :
Les symptômes du mildiou peuvent ~tre observés
sur l'ensemble des organes de la pomme de terre : 1-jeunes pousses (foyer
primaire), 2-feuilles et pétioles (à tous les stades de
l'épidémie) 3- sur les tiges et enfin 4- sur les tubercules.
1- Les jeunes pousses attaquées sont gr~les et
couvertes d'un duvet blanchItre (fructification du parasites) elles sont en
générales détruites très rapidement et donc
rarement détectées huileux ; ces taches brunissent rapidement, et
s'entourent d'un liseré jaune à la face supérieure des
limbes (Figure 1) .sur la face inferieure, le pourtour de la zone
nécrosée laisse apparaitre, en condition de forte
humidité, les fructification du parasite (James et al.,
1972)
2- Le même type de symptôme, nécrose
affecte les pétioles, les attaques sur bouquets terminaux se manifestent
par un brunissement et un léger recroquevillaient des feuilles apicales
; la zone nécrosée s'entent alors le long des tiges, provoquant
un desséchement progressif des folioles (Figure 2)
3- Sur tiges le symptôme typique est une nécrose
brune violacée, s'entent sur 2 à 10 cm a partir d'un noeud. Par
temps humide, cette nécrose couvée d'une pulvérulence
reste souvent rigide, contrairement aux symptômes observés lors de
pourritures bactériennes, mais casse très facilement.
4- Sur tubercules, les attaques surviennent en cas de
précipitation abondante de la phase de grossissement. A la
récolte ou quelque semaine après, le mildiou se
révèle par des plages superficielles irrégulières,
gris bleuâtres, violacées ou brunes. En section, on remarque des
zones marbrée rouille ou brun~tres, s'entendant de manière
diffuse de l'épidémie vers l'intérieur du tubercule. Il
s'ensuit une pourriture sèche (Figure 3) n'évoluant pas en cours
de conservation.
Toutefois, dans la plupart des cas, s'ajoutent à cette
pourriture sèche de la pourriture humide d'origine bactérienne
(Erwinia le plus souvent à qui se propagent aux tubercules
voisins).
La répartition des nécroses sur la plante est
variable. Sauf pour les toutes premières, difficiles a déceler,
les taches apparaissent rarement de façon isolée .Par temps chaud
et humide, elles gagnent rapidement la surface entière des folioles
touchées ; en quelque jours, la totalité du feuillage peut
être ainsi détruit. Les folioles se désarticulent,
retombent le long des
fanes ou se détachent complètement. Au niveau de
la parcelle, la maladie se développe en général à
partir de foyers bien marqués, qui s'agrandissent. Toutefois, certaines
années (telle l'année 1987 dans le Nord de la France), on
observées le début de l'épidémie des taches sur
feuilles et surtout sur bouquets terminaux, affectant un grand nombre de
plantes réparties de manière homogène dans la parcelle.
Figure1 : Description de symptôme Figure
2:Description de symptôme sur les feuilles sur tige

Figure 3 Description de symptôme sur les
tubercules
http://www.plantdepommedeterre.org/pages/maladies/mildiou.htm
7.1- Les dommages :
Les pertes de rendement dues au mildiou sont assez difficiles
à chiffrer. Car elles affectent à la fois la production de
tubercules récoltés et leur qualité. Lors d'un suivi de 96
parcelles canadiennes au cours de la période 1953-1970, James et al
(1972) ont enregistré des pertes de rendement de 24 à 53%, alors
que Shtienberg et al (1983) rapportent des pertes de 50 à 60% aux
Etats-Unis. Pour sa part, Bedin (1986) estime entre 20 et 90% de la
récolte les pertes maximales imputable au mildiou. Les attaques son les
plus dommageable (James et al 1972) .Les attaques plus tardives se traduisent
surtout par des taux de contamination élevés des tubercules
d'où des pertes en conservation, des sur coEts de triage et souvent une
des taux de contamination élevés des tubercules, d'où des
pertes en conservation, des surcouts de triage et souvent une chute des prix de
vente.

http://www.plantdepommedeterre.org/pages/maladies/mildiou.htm(2011)
Figure 4 : un champ de pomme de terre ravagé par
le mildiou
8- Les méthodes de luttes :
8.1- La lutte chimique :
Les premiers essais de lutte chimique, réalisés
vers les années 1880, étaient inspirés des traitements a
la bouillie bordelaise expérimentés avec succès a la
même époque pour lutter contre le mildiou de la vigne. Les travaux
portant jusqu'à la fin de la seconde guerre mondiale sur l'utilisation
des sels de cuivre ont été dirigés par
Viennot-Bourgin (1949) et plus récemment par Schwinn et Margot (1991).
Ces sels sont aujourd'hui largement remplacés par des fongicides de
synthèse, apparus sur le marché au cours des 45 dernieres
années. Trois groupes de matières actives, définis par
leur niveau de translocation dans la plante, sont aujourd'hui disponibles.
Le premier groupe compte des produits de contact, inhibant la
germination des spores en bloquant divers enzymes du champignon. Ces produits
ne sont pas mobilisés par la plante et ne protègent donc que les
organes
traités.la protection
assurée est de l'ordre de 7 à 8 jours, mais peut être
réduite en cas de précipitation supérieurs a 25mm. Dans ce
groupe ON trouve les dithiocarbamates (manébe, propinébe,
métirme de zinc et surtouts mancozébe), ainsi que divers autres
familles de matières actives ; Les phtalimides (folpel, captafol);
phthalonitriles (Schwinn et Margot, 1991) ces fongicides n'ont qu'un effet
préventif, et doivent donc ttre appliqués avant les
contaminations.
Le groupe des matières actives
pénétrantes est réduit au cymoxanil. Ce composé
pénètre dans les organes traités, ne se par la
sève, de par son pouvoir pénétrant, le cymoxanil est
susceptible de détruire le mycélium du champignon jusqu' a 2
jours après la contamination, alors que sa persistance d'action reste
faible (3jours environ). Il est en général associé a des
fongicides de contact et utilisé lorsqu'un programme de traitement
préventif, a base de fongicides de contact, est difficile a mettre en
oeuvre du fait des périodes pluvieuses ou orageuses.
Enfin, le groupe des matières actives
systémiques qui comporte des phénylamides (méta-laxyl,
benalaxyl, ofurace, oxadixyl), des carbamates (propamocarbe) et des
dérivés de l'acide cinnamique (diméthomorphe). Ces
composés sont redistribués dans l'ensemble de la plante
traitée, ce qui leur confère une action curative et la
possibilité de protéger des organes non encore
développés au moment du traitement.
C'est pourquoi les spécialités à base de
matière actives systémiques sont très intéressantes
en conditions de croissance active de la plante. Elles sont en
général composée d'un systémique et d'un contact
(Spécialités dites 2 voies) ou d'un systémique, d'un
contacte et d'un pénétrant (spécialités dites 3
vois).l'intervalle d'application entre deux traitement peut être a 10
jours pour des 2 voies et a 14 jours pour des 3 voies (Schwinn et Margot,
1991).
L'utilisation massive des fongicides systémiques, en
particulier des phénylamines, a très rapidement ressortie des
isolats résistants a ces matières actives, ce qui a rendu ces
traitement inefficaces. Un suivi de la fréquence des
souches résistantes était très étroitement
corrèle avec l'intensité du traitement. En
Bretagne, les souches résistantes étaient majoritaires
mais nettement minoritaires de 1990 a 1992(Andrivon, 1994).
La stratégie actuelle de la lutte chimique contre le
mildiou est donc de limiter à deux
ou à trois le nombre de traitement à base de
matières actives systémiques. Ces traitements seront
réalisés au début du programme seront relayés par
un programme a base de fongicides de contact ou d'association
contact/pénétrant, appliqués préventivement. La
cadence de l'application, en général fixée au début
du programme, peut être modulée de simulation
épidémique.
8.1.1-Problèmes de résistance aux
fongicides :
En raison du risque d'apparition de résistance aux
fongicides systémiques (phénylamides), diverses stratégies
d'utilisation sont recommandées. Il existe un consensus assez
général pour préconiser l'utilisation des fongicides
systémiques 2 ou 3 fois au maximum par saison, et si possible en
alternant différents produits systémiques ayant un
mécanisme de
cours d'une saison. Il n'y a pas de consensus quant au
calendrier de traitement. En dépit de nombreux signalements de
résistance, les phénylamides (métalaxyl, oxadixyl,
ofurace, bénalaxyl) sont toujours utiles contre le mildiou. La
résistance à d'autres fongicides n'a pas été
confirmée chez P. infestans, mais les programmes de
pulvérisation sur pomme de terre doivent toutefois tenir compte du
risque de résistance (Norme OEPP, 1994).
8.2- La lutte génétique :
Les programmes de sélection pour la résistance
au mildiou chez la pomme de terre se sont longtemps basés sur
l'introduction de résistances monogénique issues de
l'espèce Salanum demissum. A l`heure actuelle, onze de ces
gènes (dénommés R1 à R11) ont été
introduits chez S. tubersum mais ils ne représentent
vraisemblablement qu'une petite parti de variabilité disponible (Watie,
1991).
En cultivant des variétés porteuses de tels
gènes, on a rapidement révélé dans les populations
du parasite existant des isolats capables de surmonter ce type de
résistance (Watie, 1991) et entrainent une perte souvent rapide
d'efficacité spécifique dans la lutte contre le mildiou. Les
sélectionneurs s'orientent actuellement vers des résistances non
spécifique à des races du parasite, mais partielles,
polygénique, dont l'effet principal est de réduire la vitesse
d'expansion de la maladie. De plus, le nombre élevé de
gène impliqués dans ces résistances rend leur
sélection difficile, mais offre en général, de meilleures
garanties de durabilité (Watie, 1991).
8.3- La lutte biologique :
La lutte biologique se définie par l'utilisation de
micro-organisme vivants. Ou de leurs produits pour empêcher ou
réduire les pertes ou les dommages causés par l'organisme
pathogène.
Elle consiste à agir sur la régulation des
populations de ces organismes nuisibles pour réduire leurs
dégâts à un seuil économiquement acceptable, en
établissant, au sein de l'agroécosystème, un
équilibre biologique stabilisé (Supudman ,1991).
Les micro-organismes pathogènes peuvent être
neutralisés pas des mécanismes très variés qui
aboutissent à leur destruction, ou à leur modification. On
appelle ce microorganisme les antagonistes (Davet ,1996).
Plusieurs antagonistes peuvent être dans la lutte
biologique .nous citerons l'exemple des bactéries parmi elles le genre
Pseudomonas, et l'exemple des champignons eux le genre
Trichoderma .ces derniers étant les plus
préconisés dans la lutte contre le Phytophthora (Davet
,1996).
8.3.1-La lutte biologique par Trichoderma :
L'utilisation de Trichoderma comme agent de control
biologique, nécessite l'étude de la prolifération, du
mécanisme biologique et les facteurs de l'environnement qui gouverne
l'interaction entre l'antagoniste et le champignon
phytopathogène (Gary.1998).
Le champignon Trichoderma est considéré
comme un facteur essentiel dans la lutte
biologique puis que plupart de ces espèces intervient dans
la lutte des microorganismes
nocifs, surtout pour le champignon comme Phytophthora
infestans .le genre Trichoderma se trouve souvent dans la terre
ou sur les constituants des plantes, et leur croissance est
rapide(Gary.1998).
L'efficacité du genre Trichoderma dans
l'inhibition des organismes pathogènes repose surtout sur leur
capacité à produire plusieurs substances ou antibiotiques tels
que (Viridine, Gliotoxine...). Ces derniers sont considérés comme
des armes contre les organismes phytopathogène (Hauell, Panovic, 1995,
Gary, 1991).le genre Trichoderma produit également des enzymes
(cellulase, chitinaseà qui provoque la lyse du Phytophthora
dans la pomme de terre (Spudman, 1991).
Trichoderma viridae est utilisé pour traiter des
tubercules de pomme de terre, avant la
plantation initiale, ou l'utilisation du traitement dans les
zones de rhizosphères mais le problème indésirable c'est
la compétition aves la microflore indigène (nutriment). Pour
éviter ceci il faut additionner principalement des sources de nutriment
de la chitine, que des sucres, afin d'assurer un bon fonctionnement de
Trichoderma (Spudman, 1991).
8.3.2- L'utilisation de Pseudomonas
Les espèces du genre Pseudomonas utile pour les
plantes sont ce
grande majorité de la microflore rhizosphérique et
qui semble être prése
la pomme de terre (PGPR) (the plant growth promoting
Rhizobacteria)
Les Pseudomonas sont connus pour être d'excellents
agents de la lutte biologique,
exerçant une action antifongique (antibiotique,
enzymatique) est stimulée en présence de forte concentration de
N-acyl-L-homoserin lactone dans les sites intracellulaires (Chin, Woeng et al,
1997).
L'étude de la biologie du Pseudomonas agent
antagoniste de Phytophthora infestans dans la pomme de terre est
basée sur l'étude de la couche suppressive du sol (Spudman
La pénétration du Pseudomonas dans la
plante se fait à partir des racines de la pomme terre puis se propage
dans les tubercules par les ponctuations.
L'arrosage des plantes par une solution de Pseudomonas
diminue l'infection à 50% e le traitement utilisé après la
récolte réduit l'infection a 75% (Spudman ,1991).
Pseudomonas fluorescens se trouve naturellement dans
les racines de la plante de pomme de terre il secrète un pigment
fluorescent (pyoverdine) qui provoque la réduction de
P.infestans (Spudman ,1991).
Les sidérophores (faible poids
moléculaire) synthétisées par pseudomonas sont importantes
dans la suppression de pathogènes des plantes comme Phytophthora sp.
(Leong 1986
L'action protectrice de Pseudomonas fluorescens et
Pseudomonas putuda s'exerce principalement par l'intermédiaire
de sidérophores et des antibiotiques pour contré
l'influence des organismes nuisible ou parasites couramment présents
dans le sol (Davet, 1996).
Appliqués en robage à des tubercules de pomme de
terre avant leur plantation dans le champs expérimentaux ils permettent
des augmentations de rendement allant jusqu'à 17 % (Kloepperet et al,
1980)
Conclusion
Cette synthèse bibliographique sur le mildiou de la pomme
de terre nous à permis de :
- connaitre l'origine et la migration du Phytophthora
infestans ainsi que sa diversité des populations.
-d'en-déduire le cycle biologique du parasite et ces modes
d'infection de la plante hôte. - mettre en évidence les techniques
d'isolement et de multiplication de P. infestans.
-la description des symptômes du mildiou sur l'ensemble des
organes de la pomme de terre. -connaitre l'épidémiologie de la
maladie et les dommages qu'il peut causer.
-rapporter les différentes méthodes de lutte
chimique, génétique et biologique cette dernière est la
mieux adaptée a cause de sa décence de la nature environnante et
la disponibilité de leurs agents antagonistes présents dans la
rhizosphère.
Le développement explosif de
P.infestans en fait un parasite extrêmement difficile
à combattre lorsque l'épidémie est déclarée.
La priorité de la stratégie de lutte est donc d'emprcher autant
que possible l'implantation du parasite au champ cultivé.
References bibliographiques
Andrivon, D. ,1996- The origin of
P.infestans population present in Europe in the 1840s : a critical review of
historical and scientific evidence, Plant pathol, 45: 1027-1035.
Andrivon, D. 1995. Biology,
ecology and epidemiology of the potato late blight pathogenPhytophthora
infestans in soil. Phytopathology 85. 1053-1056.
Andrivon, Det al., 1998. Phytophthora
infestans; des population en evolution. Phytoma 502 : 28-30.
Brian Haas, et al., 2009 «
Genome sequence and analysis of the Irish potato famine pathogen
Phytophthora infestans », dans Nature, vol. 461, p. 393-398.
Carlisle, D.J., Cooke L.R., Watson, S. & Brown,
A.E. 2002. Foliar aggressiveness of
Northern Ireland isolates of Phytophthora infestans on detached leaflets of
three potato cultivars. Plant Pathology 51, 424-434.
Chin, A;Woeng, T.F.C., W. Depriester, A, J. Ronder Bij et
lutenberg. 1997- description of colonisation of gro. W.C.S.365 ,
using scaning collection microscopie. Mal plant, microbe interact. 10,
79-86.
Daayf, F. et H.W (bud), Platt. 2000.
Assessment of variation in Canadian population of the potato late
blight pathogen Phytophthora infestans in 1999; 161,630.
Davet, P.,1976: vie microbienne du sol et
production végétale I.N.R.A. ed, Paris. P 344.
de Bary, H.A. 1876. Researches into
the nature of the potato-fungus- Phytophthora infestans. Royal Agricultural
Society of England. Journal, 12, 239-269.
Donald C. ERWIN and Olaf K. RIBEIRO,
1996. Phytophthora. Diseases Worldwide., APS
Press, St-Paul, Minnesota.pp 245-256.
Eriksson, J. 1916. Det primära
utbrottet av bladmögel (Phytophthora infestans) pá potatisplantan.
In: Kungliga Lantbruks-Akademiens Handlingar och tidskrift för ár
1916. Ivar Hæggströms boktryckeri aktiebolag 1916. 538- 590.
Flier W.G. &Turkensteen L.J.
1999. Foliar aggressiveness of Phytophthora
infestans.in three potato
growing districts in the Netherlands. European Journal of Plant Pathology 105,
381-388.
Frédéric Suffert, Émilie Latxague,
Ivan Sache, 2009, Plant pathogens as agroterrorist weapons:
assessment of the threat for European agriculture and forestry, vol. 1, ,
p. 221#177;232.
Fry .W.E., Goodwin, 1993. A.Historical and
recent migration of Phytophthora infestans: chronology, pathway and
implication.Plant dis., 77 , 653-661.
Fry , W.E. et al., 1992. Population genetics
intercontinental migration of Phytophthora infestans, Rev. Phytopathology. 30:
107-129.
Gary, E.,1998 : Trichoderma et Gliocladium.
Edited byGary E, Harman and Christ ian P.Kubicek, 2. P: 367.
Gellegly M.E,Galindo J.,
1958-Mating types and oospores of Phytophthora infestans
in nature in mexico. Phytopathology 48, 274-277.
Goodwin, S.B. and Drenth A. 1997.
Origin of the A2 mating type of Phytophthora infestans outside Mexico.
Phytopathology, 87, 992-999.
Grenville-Briggs, L.J. & van West, P.
2005. The biotrophic stages of oomycete-plant
interactions. Advances in applied microbiology, 57. 217-242.
Grünwald, N.J., Flier, W.G., Sturbaum, A.K.,
Garay- Serrano, E., van der Bosch, T.B.N., Smart, C.D., Matuzak, J.M.,
Lozoya-Saldaña, H., Turkensteen, L.J. & Fry, W.E.
2001. Population structure of Phytophthora infestans in
the Toluca valley region of central Mexico. Phytopathology 91, 882-890.
Harrison, J. G. 1992. Effects of the aerial
environment on late bligbht of potato - a review. Plant Pathology 41.
384-416.
James W.C., Shih C.S.,Hodson W.N., Callbeck C.L.,
1972- The quantitative relationship between late blight
of potato and loss in tuber yield .Phytopathology62, 92-96.
Judelson, H.S. & Blanco A.B.
2005. The spores of Phytophthora: Weapons of the plant
destroyer. Microbiology ,. 47-58
KO. W.H, 1978 , Heterothallic Phytophthora:
evience for hormonal regulation of sexual reproduction.
J.gen.microbiol.107, 15-18.
Lacey, J.1965. The infectivity of soils
containing Phytophthora infestans. Annals of Applied Biology
56,363-380.
Leong J., 1986- Siderophores : their
biochemistry and possible role in the biocontrol of plant pathogens . Annu.
Rev. Phytopathology. 24, 187-209.
Lzgard,R.D, T.Y. Lee et W.E. Fry. 1995.
Pathogenic specialization in Phytophthora infestans.
Aggressiveness on tomato. Phytopathology 85: 1356-1361.
Niederhauser, JS. 1991.
Phytophthora infestans: The Mexican connection. In:
Phytophthora. Symptoms of the British Mycological Society for Plant Pathology
and the society of Irish Plant Pathologists held at Trinity College.
Patrick Rousselle,Yvon Robert,Jean-Claude Crosnier ,1996 ,La
pomme de terre :production, amélioration, ennemis et maladies,
utilisation p.283-291.
Pittis J.E.,Shattock R.C, 1994 -
Viability, germination and potential of oospores of Phytophthora. infestans .
plant pathol., 43, 387-396.
Robertson N.F., 1991- The challenge of
Phytophthora infestans. In Ingram, Williams Eds., 1991, 1-30.
Schwinn F.J, Margot P., 1991- Control with chemicals
In Ingram, Williams Eds, 1991, 225-265.
Shaw D.S.,1987-The breeding of phytophthora
infestans:the role of the A2 mating type.In genetics and plant pathogenesis
P.RDay, G.J.Jellis, Blackwell.Oxford161-174.
Shtienberg D.,Bergeron S.N., Fry W.E., 1983-
Devlopement of a general model for yield loss assessment in
potatoes .Phyopathology, 80, 466-472.
Smart, C.D, Willman, M.R, Mayton, H, Mitzubuti, E.S.G,
Sandrock, R.W, Muldoon, A.E. & Fry, W.E. 1998. Self-fertility
in two clonal lineages of Phytophthora infestans. Fungal Genetics and Biology
25, 134-142.
Smoot J,J.Gough.F.j,Lamey, H.A,Eichenmuller. J.Gallegly
M.E,1998, Production and germination of oospore of Phytophthora.
Infestans. Phytopathology 48, 165-171.
Spielman L.J., Drenth A., Davidse, Fry W.E,
1991- A second worldwide migration and population displacement of
Phytophthora infestans .Plant pathol., 40, 422-430.
Wastie R.L., 1991- Breeding for resistance. In
Ingram Williams Eds, 1991, 193-224.
| 

