|
OCTOBRE 2024
UNIVERSITE DE LUBUMBASHI
Faculté des Sciences
Agronomiques
Département de Gestion des sols, Eaux et
Assainissement
B.P 1825

Evaluation des effets de la toxicité du Cu et du
Co sur la
croissance du Blé tendre (Triticum aestivum) dans
la région
de Lubumbashi (R.D Congo)
Par
NTAMBWE NTAMBWE Jonas
Travail de fin d'Etude présenté et
défendu en vue de l'obtention du diplôme de Master en Sciences
Agronomiques/Gestion des Sols, Eaux et Assainissement
UNIVERSITE DE LUBUMBASHI
Faculté des Sciences
Agronomiques
Département de Gestion des sols, Eaux et
Assainissement
B.P 1825

Evaluation des effets de la toxicité du Cu et du
Co sur la
croissance du Blé tendre (Triticum aestivum) dans
la région
de Lubumbashi (R.D Congo)
Par
NTAMBWE NTAMBWE Jonas
Travail de fin d'Etude présenté et défendu
en vue de l'obtention du diplôme de
Master en Sciences
Agronomiques/Gestion des Sols, Eaux et Assainissement
Directeur: Prof. Dr. MUYUMBA KAYA Donato
Année-académique 2023-2024
I
Dédicace
A mon père NTAMBWE T. Jonas et ma mère KALUNGA
K. Bibiane, pour votre amour, votre soutient sur tous les plans. Aucune phrase
ne pourra exprimer l'amour que je porte pour vous. Prenez cette oeuvre d'esprit
qui témoigne ma profonde gratitude !
A tous mes frères et soeurs que je porte
précieusement dans mon coeur A ma meilleure amie SIMONETTE KATAMBWE
Rachel A mon combattant de lutte KANGUDIA MANGALA Nathan
II
Remerciements
Au terme de ce travail, nous ne pouvons pas passer sous
silence la joie qui remplit notre coeur en exprimant notre profonde gratitude
à l'endroit de personnes qui, de près ou de loin, ont
contribué à la réalisation de ce travail qui vient de
sanctionner la fin de notre premier cycle académique. Nos remerciements
s'adressent plus particulièrement :
? Au Professeur Associé. KAYA MUYUMBA Donato directeur
de ce travail de fin d'étude, pour avoir accepté de diriger le
présent travail. Qu'il trouve ici le mérite et expression de
notre profonde gratitude.
? Au doyen de la faculté des sciences agronomiques le
professeur ordinaire NGOY SHUTCHA Mylor, au vice-doyen chargé de
l'enseignement le professeur CABALA KAPOMBO KALEBA Sylvestre, au vice doyen
chargé de la recherche le professeur LWALABA WA LWALABA Jonas et a
toutes les autorités académiques et administratives, chefs de
travaux et tous les assistants (e)s de la faculté des sciences
agronomiques pour avoir concouru pour notre bonne formation ;
? En fin notre gratitude est adressée vers le
Très-Haut, le Dieu Tout-Puissant pour ses biens fait à notre
faveur.
III
Résumé
La pollution des sols par les éléments traces
métalliques (ETM) demande une évaluation du risque des effets
toxiques chez les espèces végétales les plus
consommées, notamment le blé tendre (Triticum aestivum). Cette
étude a pour objectif principal d'évaluer l'effet toxique de deux
ETM, Cuivre (Cu) et Cobalt (Co) sur la croissance du blé tendre
(Triticum aestivum).
Deux essaies séparés ont été
adoptés, l'un pour le Cu et l'autre pour le Co. Le dispositif
expérimental adopté était en Blocs aléatoires
complets, comportant quatre traitements (4), avec trois (3)
répétitions.
Les principaux résultats ont montré qu'il y
avait des différences significatives entre les différents
traitements dans tous les deux essaies, et pour tous les paramètres
végétatifs observés notamment le taux de germination ; le
taux de survie ; la hauteur de plantes, le nombre des feuilles ainsi la
longueur des racines, il s'avère que les traitements témoins ont
donné les meilleures moyennes pour tous les paramètres
observés dans les deux essais. Par conséquent nous pouvons dire
que les concentrations croissantes du Cu et Co ont un effet négatif
significatif sur les plantes de blé tendre.
Mots clés : ETM, Cu, Co, pollution,
blé tendre
IV
Abstract
Soil pollution by metallic trace elements (MTE) requires an
assessment of the risk of toxic effects in the most consumed plant species, in
particular soft wheat (Triticum aestivum). The main objective of this study is
to assess the toxic effect of two MTE, copper (Cu) and cobalt (CO) on the
growth of soft wheat (Triticum aestivum).
Two separate attempts were adopted, one for the Cu and the
other for the CO. The experimental device adopted was in complete random
blocks, comprising four treatments (4), with three (3) repetitions.
The main results showed that there were significant
differences between the different treatments in both tries, and for all the
vegetative parameters observed, in particular the germination rate; the
survival rate; The height of plants, the number of leaves as well as the length
of the roots, it turns out that the control treatments gave the best averages
for all the parameters observed in the two trials. Therefore we can say that
the increasing concentrations of Cu and Co have a significant negative effect
on soft wheat plants.
Keys words : MTE, Cu, Co, Pollution, Soft
wheat
V
Table des matières
Dédicace I
Remerciements II
Résumé III
Abstract IV
Table des matières V
Liste des figures VIII
Liste des tableaux IX
Liste des symboles et abréviation X
Introduction 1
Chapitre 1. Revue de la littérature 3
1.1. Eléments traces métalliques 3
1.1.1. Définition des « éléments traces
métalliques » 3
1.1.2. Origine de la contamination des sols par les métaux
lourds 3
1.1.3. Mobilité et biodisponibilité des
éléments traces métalliques 5
1.2. Le Cuivre 6
1.2.1. Le Cuivre dans l'environnement 6
1.2.2. Toxicité du Cuivre 6
1.3. Le Cobalt 7
1.3.1. Mobilité et biodisponibilité en milieu
terrestre 7
1.3.2. Le cobalt et les végétaux 8
1.3.3. Toxicité du cobalt dans les plantes 10
1.4. Généralités sur la culture de
blé 11
VI
1.4.1. Origine du blé 11
1.4.2. Classification botanique et description morphologique
12
1.4.3. Cycle biologique du blé 15
I.1.5. les exigences climatiques 18
1.4.4. Importance de la culture 19
Chapitre 2. Milieu, matériels et méthodes 21
2.1. Milieu d'étude 21
2.1.1. Situation géographique 21
2.1.2. Climat 21
2.1.3. Sol 22
2.1.4. Hydrographie 22
2.1.5. Végétation 23
2.2. Matériels 23
2.2.1. Matériels végétal 23
2.2.2. Matériels non biologiques 23
2.2.1. Matériels chimiques 23
2.3. Méthode 24
2.3.2. Paramètres mesurés 25
Chapitre 3. Interprétation des résultats 27
3.1. Résultats obtenus avec le traitement de Cu 27
3.1.1. Taux de germination (%) 27
3.1.2. Taux de survie (%) 28
3.1.3. Hauteur de plantes (Cm) 29
3.2. Résultats obtenus avec le traitement Co 32
3.2.1. Taux de germination (%) 32
VII
3.2.2. Taux de survie (%) 33
3.2.3. Hauteur de plantes (Cm) 34
3.2.4. Nombre de feuilles 36
3.2.5. Longueur des racines à 40 jours (Cm) 37
4.1. Effet du Cu sur les paramètres
végétatifs du blé tendre 38
4.2. Effet du Co sur les paramètres
végétatifs du blé tendre 39
Conclusion 41
Bibliographie 42
Annexes 1
VIII
Liste des figures
Figure 1. Origine des éléments traces
métalliques dans le sol d'après Robert et Jules 1999 4
Figure 2. Anatomie du grain de blé 14
Figure 3. Localisation du milieu d'étude 21
Figure 4. Schéma du dispositif expérimental
adopté 24
Figure 5. Dispositif expérimentale adopté pour
le CuSO4 5H2O et pour le CoSO4 7H2O
séparément 25
Figure 8. Taux de germination à 10 jours en fonction
des traitements 27
Figure 9. Taux de survie à 15 jours en fonction des
traitements 28
Figure 10. Taux de survie à 40 jours en fonction des
traitements 28
Figure 11. Hauteur des plantes à 20 jours en fonction
des traitements 29
Figure 12. Hauteur des plantes à 40 jours en fonction
des traitements 29
Figure 13. Nombre des feuilles à 20 jours en fonction
des traitements 30
Figure 14. Nombre des feuilles à 40 jours en fonction
des traitements 30
Figure 15. Longueur des racines à 40 jours en fonction
des traitements 31
Figure 16. Taux de germination à 10 jours en fonction
des traitements 32
Figure 17. Taux de survie à 15 jours en fonction des
traitements 33
Figure 18. Taux de survie à 40 jours en fonction des
traitements 33
Figure 19. Hauteur des plantes à 20 jours en fonction
des traitements 34
Figure 20. Variation des hauteurs en fonction des traitements
34
Figure 21. Hauteur des plantes à 40 jours en fonction
des traitements 35
Figure 22. Nombre des feuilles à 20 jours en fonction
des traitements 36
Figure 23. Nombre des feuilles à 40 jours en fonction
des traitements 36
Figure 24. Longueur des racines à 40 en fonction des
traitements 37
IX
Liste des tableaux
Tableau 1. Mobilité et biodisponibilité du Cu et
Co dans les écosystèmes métallifères (Muyumba
et al., 2019 5
Tableau 2. Classification systematique du blé selon
(Van Den Abeelz, 1956) 13
Tableau 3. Quantité de sulfates de cuivre
pentahydraté et de sulfates de cobalt heptahydraté en
gramme qui doit être apportée à chaque pot
24
Tableau 4. Base des données pour le traitement avec le
CuSO4 5H2O 1
Tableau 5. Base des données pour le traitement avec le
CoSO4 7H2O 2
X
Liste des symboles et abréviation
ETM : éléments traces métalliques
Co : Cobalt
Cd : Cadmium
Pb : Plomb
H.P : Hauteur des plantes
N.F : Nombre des feuilles
L.R : Longueur des racines
T.G : Taux de germination
T.S : Taux de survie
C.E.C : Capacité d'échange cationique
CuSO4 5H2O : Sulfates de cuivre pentahydraté CoSO4 7H2O :
Sulfates de cobalt heptahydraté
Eh : potentiel redox
VNM : Valeurs non mesurées
1
Introduction
Les éléments traces métalliques sont
naturellement présents dans les sols à des concentrations faibles
inferieures à 0,1% de la composition de l'écorce terrestre
(Baize, 1997 ; Kabata-pendias et al., 2001).
Bien que certains de ces éléments traces
métalliques soient essentiels pour les plantes, ils deviennent tous
toxiques lorsqu'ils sont présents à des fortes concentrations
(Kupper et al., 2000 ; Baize et al., 2001).
La contamination des sols par les éléments
traces métalliques peut avoir deux conséquences majeures. D'une
part, elle peut favoriser la dispersion des éléments traces
métalliques dans l'environnement vers les eaux de surface par
érosion, vers les eaux souterraines et les nappes par
lixiviation-lessivage et, enfin, par transferts dans la chaine alimentaire par
l'intermédiaire des animaux et plus encore des végétaux
(Adriano, 2001). D'autre part, la contamination des sols par les
éléments traces métalliques peut affecter les
différentes fonctions du sol, celles contribuant aux services
écosystémiques, et en particulier sa fonction de production en
zone agricole (Adriano, 2001).
En République Démocratique du Congo, les
concentrations de Co et de Cu dans certains régions contaminées
peuvent atteindre des milliers de fois supérieures à celle du sol
normal (Lange et al., 2016). Le cobalt (Co), qui n'a pas été
reconnu comme un élément nécessaire aux plantes bien qu'il
ait une fonction biologique ou physiologique distincte dans les
légumineuses, constitue une menace sérieuse pour la croissance et
le développement des plantes une fois qu'il est disponible en grande
quantité dans les sols (Chatterjee, 2003 ; Gopal et al., 2003 ;
Karuppanapandian et Kim, 2013 ; Lwalaba et al., 2017a ;b). D'autre part le
cuivre (Cu) est l'un des micronutriments requis en très petites
quantités par les plantes, une quantité excessive de Cu dans le
substrat peut limiter la croissance des racines en brulant leurs
extrémités, causant ainsi une croissance racinaire
latérale excessive (Bloodnick, 2014).
Nombreuses espèces végétales peuvent
être atteintes par la pollution de métaux lourds, notamment les
espèces céréalières. Aniol et Gustafon (1984) ont
montré que les différentes céréales ne
réagissent pas de la même façon à la présence
des métaux lourds. Ces deux auteurs ont classés, en 1984, le
seigle comme la céréale la plus tolérante, le blé
présentant une tolérance
2
intermédiaire et l'orge comme la plus sensible. Le
blé (Triticum aestivum) a été choisi durant cette
étude comme céréale.
Cette étude a pour objectif principal d'évaluer
les effets de la toxicité du cuivre et du cobalt sur la croissance du
blé tendre dans la région de Lubumbashi. Spécifiquement
l'étude présente a pour objectif de :
? Evaluer la toxicité des différentes doses
croissantes du Cu sur la croissance du blé tendre ; avec comme
hypothèse la croissance du blé tendre serait fonction des
différentes concentrations du Cu
? Evaluer la toxicité des différentes doses
croissantes du Co sur la croissance du blé tendre ; avec comme
hypothèse la croissance du blé tendre serait fonction des
différentes concentrations du Co
La présente étude est subdivisée en
quatre chapitres outre l'introduction et la conclusion notamment : le chapitre
1 consacré à la revue de la littérature ; le chapitre 2
présente le milieu, matériels et méthodes, le chapitre 3
présentation des résultats obtenues et le chapitre 4 discussion
des résultats.
(a) Origine naturelle Les éléments traces
métalliques sont présents naturellement dans les roches, ils sont
libérés lors de l'altération de celles-ci pour constituer
le fond géochimique
3
Chapitre 1. Revue de la littérature 1.1.
Eléments traces métalliques
1.1.1. Définition des «
éléments traces métalliques »
D'un point de vue purement chimique, les
éléments de la classification périodique formant des
cations en solution sont des métaux. D'un point de vue physique, le
terme « les ETM » désigne les éléments
métalliques naturels, métaux ou dans certains cas
métalloïdes (environ 65 éléments),
caractérisés par une forte masse volumique supérieure
à 5 g.cm3 (Adriano, 2001) (Tableau 1). D'un autre point de vue
biologique, on en distingue deux types en fonction de leurs effets
physiologiques et toxiques : métaux essentiels et métaux
toxiques.
(i) Les éléments traces métalliques
essentiels sont des éléments indispensables à
l'état de trace pour de nombreux processus cellulaires et qui se
trouvent en proportion très faible dans les tissus biologiques
(Loué, 1993). Certains peuvent devenir toxiques lorsque la concentration
dépasse un certain seuil. C'est le cas du cuivre (Cu), du nickel (Ni),
du zinc (Zn), du fer (Fe). Par exemple, le zinc (Zn), à la concentration
du millimolaire, est un oligo-élément qui intervient dans de
nombreuses réactions enzymatiques (déshydrogénases,
protéinase, peptidase) et joue un rôle important dans le
métabolisme des protéines, des glucides et des lipides
(Kabata-Pendias et Pendias, 2001).
(ii) Les éléments traces métalliques
toxiques ont un caractère polluant avec des effets toxiques pour les
organismes vivants même à faible concentration. Ils n'ont aucun
effet bénéfique connu pour la cellule. C'est le cas du plomb
(Pb), du mercure (Hg), du cadmium (Cd).
Les éléments traces métalliques, implique
aussi une notion de toxicité. Le terme « éléments
traces métalliques » est aussi utilisé pour décrire
ces mêmes éléments, car ils se retrouvent souvent en
très faible quantité dans l'environnement (Baker et Walker,
1989).
1.1.2. Origine de la contamination des sols par les
métaux lourds
Le problème principal avec les métaux lourds
comme le plomb, le cadmium, le cuivre et le mercure est qu'ils ne peuvent pas
être biodégradés, et donc persistent pendant de longues
périodes dans des sols. Leur présence dans les sols peut
être naturelle ou anthropogénique.
4
(Bourrelier et Berthelin, 1998). La concentration naturelle de
ces métaux lourds dans les sols vaire selon la nature de la roche, sa
localisation et son âge.
(b) Origine anthropique Cependant, la source majeure de
contamination est d'origine anthropique. Au cours des décennies
dernières, l'apport des éléments traces métalliques
au sol dans le monde s'est étendu ; à l'heure actuelle on
l'estime à 22000 tonnes de cadmium, 939000 t de cuivre, 783000 t de
plomb, et 1350000 t de zinc (Singh et al., 2003). Les principaux types de
pollutions anthropiques responsables de l'augmentation des flux de
métaux, sont la pollution atmosphérique (rejets urbains et
industriels), la pollution liée aux activités agricoles et la
pollution industrielle.
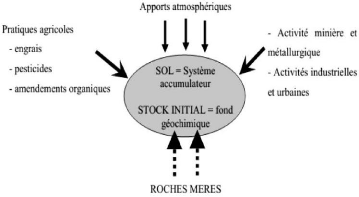
Figure 1. Origine des éléments traces
métalliques dans le sol d'après Robert et Jules 1999
La pollution atmosphérique résulte des
activités industrielles (rejets d'usine) et urbaines (gaz
d'échappement, etc....). Il faut distinguer les apports diffus
aériens d'origine lointaine des apports massifs localisés
d'origine proche. Dans les apports diffus sont classés les
poussières et aérosols provenant des chauffages ainsi que des
moteurs d'automobiles. Les apports massifs localisés résultent
d'apports anthropiques accidentels liés aux activités
industrielles sans protection efficace contre la dispersion dans
l'environnement (Baize, 1997). Certaines pratiques agricoles sont à
l'origine de l'introduction de métaux lourds dans le sol. Les produits
destinés à améliorer les propriétés
physico-chimiques du sol sont souvent plus riches en métaux lourds que
le sol lui-même par exemple les engrais, les composts et les boues de
station d'épuration (Robert et Juste, 1999). La pollution industrielle
provenant des usines de production de l'activité humaine tels que les
matières organiques et graisses (industries agro-alimentaires), les
5
produits chimiques divers (industries chimiques), les
matières radioactives (centrales nucléaires, traitement des
déchets radioactifs) et la métallurgie (Godin et al., 1985). Les
déchets miniers et les terrils industriels sont une source
particulièrement importante de pollution par le zinc, le plomb et le
cadmium.
Le rôle des pratiques industrielles et agricoles dans la
contamination des sols doit être pris en compte : cela concerne une
grande partie du territoire. Leur accumulation et leur transfert constituent
donc un risque pour la santé humaine via la contamination de la
chaîne alimentaire, mais aussi pour le milieu naturel dans son ensemble
(Bourrelier et Berthelin, 1998).
1.1.3. Mobilité et biodisponibilité des
éléments traces métalliques
La toxicité d'un métal dépend de sa
spéciation (forme chimique) autant que des facteurs environnementaux
(Babich, 1980). Dans le sol, les éléments traces
métalliques peuvent exister sous forme d'ion libre ou sous forme
liée à des particules de sol. Cependant, un métal n'est
toxique pour les organismes vivants que s'il est sous forme libre ; il est
alors biodisponible. Comme tout élément chargé
positivement, les cations métalliques peuvent interagir dans le sol avec
toute particule organique ou minérale chargée
négativement. De l'équilibre entre les formes libres et
fixées de l'ion va dépendre sa biodisponibilité,
directement liée à sa toxicité. Enfin, la
biodisponibilité des métaux lourds varie en fonction de plusieurs
facteurs du sol.
Parmi lesquels, la capacité d'échange de cation
(CEC), le pH, le potentiel redox (Eh), la teneur en phosphate disponible, la
teneur en matière organique et les activités biologiques.
Tableau 1. Mobilité et biodisponibilité
du Cu et Co dans les écosystèmes
métallifères
(Muyumba et al., 2019
|
Unité
|
Total (ppm)
HF + HClO4 + HCl
|
Mobilisation (ppm) CH3COONH4 EDTA
|
Mobilisables (ppm) CaCl2
|
|
Témoin
|
Cu
|
Co
|
Cu
|
Co
|
Cu
|
Co
|
|
134
|
49
|
98
|
2,4
|
0,23
|
0,83
|
,,
6
1.2. Le Cuivre
1.2.1. Le Cuivre dans l'environnement
Un des premiers métaux utilisés par l'homme est
le cuivre du fait qu'on le trouve dans des gisements minéraux de
beaucoup de régions du monde, et bien qu'il puisse être facilement
travaillé, il a une résistance élevée à la
corrosion (Angeles Cid, 1995). Le Cuivre est surtout présent dans la
croute terrestre sous forme de sulfure de Cuivre (La chalcocite, Cu2S), de
sulfure de cuivre-fer (la chalcopyrite, CuFeS2), de bonite (CuFeS4), et aussi
comme des minéraux oxydés tels que les carbonates, sulfates et le
cuivre des hydroxyles-silicates (Kiaune et Singhasemanon, 2011). Le Cuivre se
retrouve dans l'eau de surface, l'eau souterraine, l'eau potable et l'eau de
mer mais aussi il est initialement présent sous forme de complexes ou
matière particulaire (A TSDR, 2002).
1.2.2. Toxicité du Cuivre
Le cuivre est un oligo-élément essentiel pour le
fonctionnement des plantes, des microorganismes et des animaux en raison de sin
exigence pour de nombreux processus métaboliques particuliers (ICA,
1995). En particulier, il est essentiel pour de nombreuses fonctions
biochimiques, comme par exemple la catalyse de réactions
d'oxydo-réduction dans le cytoplasme, la mitochondrie et le chloroplaste
des cellules (Fargasoya, 2004), ou bien comme un transporteur
d'électrons durant la respiration (Yruela, 2009). Le cuivre participe
aussi dans la lutte des espèces réactives de l'oxygène
comme la Cu/Zn superoxyde dismutase (SOD) qui convertit l'anion superoxyde en
dioxygène et peroxyde d'hydrogène (ICA, 1995).
Dans le sol, le Cu2+ existe sous plusieurs
espèces chimiques, mais il est principalement absorbé comme un
élément nutritif par les plantes sous forme de Cu2+
(Maksymiec, 1997). L'accumulation du Cu2+ peut atteindre des
concentrations de 20 et 30 ug.g- 1 de poids sec (Pham et al., 2013). La
caractérisation primaire de toxicité du Cu2+ est
l'inhibition de l'élongation des racines et la croissance de la plante
(Tsay et al., 1995).
Les effets du Cu2+ provoquent d'autres
symptômes comme la nécrose, la chlorose et la décoloration
des feuilles (Yruela, 2009). Le changement redox du Cu+ en
Cu2+ induit la formation d'espèces oxydées
radiculaires comme l'oxygène singulet (02-) et le radical
hydroxyle (OH), et ces espèces oxydatives provoquent des dommages aux
macromolécules biologiques, comme l'ADN et l'ARN, les protéines,
les lipides et les glucides (Lombardi et
7
Sebastiani, 2005 ; Yurekli et Porgali, 2006). Il a aussi
été démontré que la toxicité du
Cu2+ induit une réduction de l'activité
photosynthétique par une baisse du rendement quantique du
photosystème II (Alaoui-Sosse et al., 2004 ; Pesko et Kralova, 2013).
Egalement, les êtres humains sont exposés au cuivre par inhalation
de particules de Cu2+, l'ingestion d'eau ou de nourritures
contaminées par le cuivre. Cependant, la toxicité du cuivre pour
l'être humain est relativement faible par rapport aux autres
métaux tels que le Cadmium, le mercure, le plomb et le chrome. Les
effets toxicologiques qui peuvent être induites par les ions cuivre
(Cu2+) peuvent provoquer des dépôts dans le cerveau, le
foie, la peau, le pancréas, et le myocarde (Davis et al., 2000).
1.3. Le Cobalt
1.3.1. Mobilité et biodisponibilité en
milieu terrestre
Sols Le cobalt stable est présent dans les sols
à une concentration variant de 1 à 50 mg.kg-1 sec (Hamilton,
1994) ; des concentrations élevées ont été
observées localement sur des zones hyperminéralisées
(jusqu'à 5 000 mg.kg-1 sec) ou sur des sols formés sur serpentine
(Coughtrey et Thorne, 1983). En France, les concentrations observées
vont de 2 à 23
mg.kg -1 sec avec des valeurs extrêmes
allant jusqu'à 150 mg.kg- 1 sec dans des zones de «
métallotectes » à fortes minéralisations, notamment
dans le Morvan (Baize, 2000). Les sols agricoles de pâture sont souvent
déficients en cobalt (< 1 mg.kg-1 sec) et doivent alors être
supplémentés en cet oligoélément pour assurer une
nutrition correcte du bétail qui s'y nourrit (Hamilton, 1994). De
nombreuses études de spéciation et de sorption-désorption
du cobalt ont été effectuées sur des milieux simples
(oxydes métalliques en particulier) et pour des conditions applicables
à certains stockages profonds (Brooks et al., 1998 ; Brooks et Carroll,
2003 ; Khan et al., 1995 ; Wang et Papenguth, 2001 ; Wang et al., 2003). En
revanche, les études concernant le comportement du cobalt dans des sols
restent plus globales. En termes de spéciation, dans les conditions de
pH et de potentiel redox similaires à celles des sols « moyens
», le cobalt serait essentiellement sous forme de Co2+. Au-delà de
pH 9,5, les hydroxydes de cobalt seraient dominants et tendraient à
précipiter ; les sulfures n'apparaîtraient qu'en conditions
réductrices (Eh < - 300 mV à pH 7) (Krupka et Serne, 2002 ;
Deltombe et Pourbaix, 1966). Le cobalt forme des complexes très stables
avec les ligands organiques, notamment les acides humiques et fulviques (Glaus
et al., 2000), ce qui augmenterait sa mobilité. Il est reconnu que la
chimie de l'élément est étroitement liée à
celle du fer et du manganèse et qu'il est étroitement
associé aux oxy-hydroxydes
8
métalliques. Sa forte affinité pour les oxydes
de fer induit une augmentation de sa mobilité en milieu
réducteur, notamment hydromorphe ; cependant, le contrôle de sa
mobilité dépend des oxy-hydroxydes métalliques, de la
concentration en Ca2+, mais aussi de la présence de ligands organiques
(Bresson et al., 2009 ; Krupka et Serne, 2002). La sorption du cobalt sur des
phases minérales pures est modérée et décroît
avec le pH en l'absence de ligands organiques, alors qu'en présence de
complexant organiques la sorption du cobalt diminue par formation de complexes
anioniques (Krupka et Serne, 2002 ; Wang et al., 2002). Bien que dans les sols,
le cobalt soit moyennement mobile, ses formes complexées sont
très mobiles et facilement disponibles pour les plantes. Il serait
majoritairement, soit faiblement adsorbé sur les argiles, en liaison
avec les oxydes de fer et de manganèse, soit complexé par les
acides humiques. Seuls 5 à 10 % du cobalt total d'un sol sont
hydrosolubles ou facilement extractibles (Colle et al., 1991 ; 1996). Une
évolution notable des fractions échangeables et des fractions
très fortement fixées a été montrée par des
extractions séquentielles sur des sols de rizière : le cobalt de
ces deux fractions tendrait à diminuer en quelques mois, au profit d'une
augmentation du cobalt associé aux oxydes de fer (Tagami et
Uchida,1998). Par ailleurs, l'augmentation de la teneur en argiles s'accompagne
d'une augmentation du Kd : ainsi, Gutierrez et Fuentes (1991) ont
observé, pour des concentrations de cobalt de 1 mg.L-1 dans la solution
du sol, des Kd respectifs de 151 et 318 L.kg-1 sec pour des sols
différant essentiellement par leur teneur en argile, i.e. 16 et 31 %. La
migration du cobalt dépend des caractéristiques du sol : en
termes de pH, la mobilité diminue parallèlement à
l'acidité ; dans les sols à faible capacité
d'échange cationique (sablonneux acides, par exemple), le lessivage est
modéré ; les sols ou horizons riches en matière organique
fixeraient plus fortement et durablement le cobalt. La fraction remobilisable
est dans ce cas d'environ 5 % par an avec une période (demi-vie) dans la
couche humifère variant de 2 à 12 mois (Colle et al., 1991 ;
1996). La structure du sol en place est également un facteur important :
des phénomènes particuliers de migration
préférentielle et une valeur de Kd plus forte du cobalt lorsqu'il
est mesuré en système batch, par rapport à une migration
en lysimètres ont été mis en évidence par Albrecht
et al. (2003).
1.3.2. Le cobalt et les
végétaux
Le cobalt est un oligo-élément qui jouerait un
rôle vis-à-vis des bactéries symbiotiques fixatrices
d'azote et dont l'excès pourrait provoquer une diminution de
chlorophylles et de l'absorption du fer (Chatterjee et Chatterjee, 2000).
L'absorption du cobalt par les plantes est conditionnée par la
concentration du cobalt mobile du sol, de celui présent sur les sites
9
échangeables et par sa forme chimique. Par analogie
avec le nickel, le transporteur dans les plantes semble être l'histidine
(Bresson et al., 2009). À l'exception de quelques plantes
hyper-accumulatrices, la plupart des plantes terrestres ne montrent pas de
bioconcentration du cobalt. Ses teneurs moyennes dans les plantes vont de 0,1
à 115 mg.kg-1 sec. Des concentrations 10 à 20 fois plus
élevées ont été observées dans des
légumineuses sur des sols hydromorphes (Coughtrey et Thorne, 1983) ; sur
des sols riches en cobalt, les concentrations des végétaux
naturels peuvent atteindre de 100 à 1 000 mg.kg-1sec, notamment chez
l'espèce arborée Nyssa sylvatica (Chatterjee et Chatterjee,
2003). Les facteurs de transfert racinaire moyens sont de l'ordre de 0,1
kg.kg-1 (poids secs). Ils varient entre 10-4 et 5. La variabilité pour
un même type de végétal est en moyenne de l'ordre d'un
facteur 10 et elle peut être beaucoup plus forte selon le sol et entre
différents végétaux. L'absorption racinaire est
réputée -- comme pour la plupart des cations -- augmenter
faiblement avec la diminution du pH, ce qui apparaît dans les
résultats de Gerzabek et al. (1994) ; à l'inverse, les
résultats de Ban-nai et Muramatsu (2002) sur des radis cultivés
sur 10 sols modérément acides (pH de 5,5 à 6,5) et ceux de
Gerzabek et al. (1998) ne font pas apparaître de variation significative
du transfert racinaire avec le pH du sol. Le fer, l'aluminium et le calcium
influent sur l'absorption du cobalt par les végétaux par
compétition sur les sites d'échange du sol (capacité
d'échange). Dans une moindre mesure, la texture du sol et sa teneur en
matière organique modifient l'intensité des transferts racinaires
(Colle et al., 1996 ; AIEA, 2010). Le transfert aux dicotylédones est
supérieur (en moyenne d'un facteur 15) au transfert aux
monocotylédones. L'influence d'un apport de cobalt stable au sol a
été mesurée lors des essais de Colle et al. (1991) en
lysimètres de grande taille (16 bacs x 200 kg de sol brun calcaire). Les
conclusions montrent qu'un apport de cobalt stable au sol entraîne une
augmentation du facteur de transfert racinaire. Pour un amendement de 50 g de
cobalt stable par kg de sol sec, le transfert du 60Co est approximativement
multiplié par 8 pour les pailles de céréales et les
gousses de haricots, par 4 pour les grains de céréales et par 2
pour les feuillages de légumes (salades, haricots, carottes). Un
dépôt à la surface du sol augmente également le
transfert comparativement à un apport incorporé de façon
homogène dans la couche racinaire (Colle et al., 1983 ; 1996).
L'étude de l'influence du mode d'apport montre que le dépôt
global sur les organes aériens (aspersion sur les feuillages) est de
loin le plus pénalisant, puisqu'il aboutit à une augmentation des
facteurs de transfert (exprimés en Bq.kg-1 de végétal par
Bq.m-2 de surface cultivée) d'un facteur 102 à 103 relativement
à un apport racinaire de même activité surfacique
équivalente (Colle et al., 1991). Ces résultats sont
cohérents avec ceux de Sabbarese et al., (2002) qui ont comparé
les activités massiques de tomates irriguées par aspersion et
à la
10
raie : le ratio est de 6,5 environ pour les fruits, de 6,2
pour les tiges, de 5,3 pour les feuilles et de 2 pour les racines. Lors d'une
contamination foliaire occasionnelle, les résultats, rares, sont en
outre très variables selon le stade végétatif lors de la
contamination. Lors d'expérimentations sur les céréales
contaminées par aspersion à divers stades
végétatifs, Coughtrey et Thorne (1983) indiquent, classiquement,
que le pourcentage initial de radionucléide retenu par le
végétal au moment de la contamination dépend de la
biomasse à ce stade alors que le pourcentage retenu par le
végétal à la récolte est lié au délai
séparant la récolte de la contamination. La contamination du
grain passe par un maximum lorsque la contamination a lieu pendant la
période de maturation puis diminue, alors que celle de la paille
augmente lorsque la date de contamination s'approche de celle de la
récolte. La translocation vers le grain s'effectuerait ainsi durant une
courte période.
1.3.3. Toxicité du cobalt dans les
plantes
Le cobalt à des concentrations élevées
provoque une cytotoxicité et une phytotoxicité dans les plantes,
qui sont similaires à celles du Cu, du Ni et du %00Zn. La
cytotoxicité est l'inhibition de la mitose et l'endommagement des
chromosomes, ainsi que la perturbation du réticulum endoplasmique des
cellules de l'extrémité des racines (Rauser, 1981 ; Smith et
Carson, 1981 ; Akeel et Jahan, 2020). La phytotoxicité varie en fonction
des espèces végétales et de la concentration de Co dans
les organes végétaux. Les légumineuses présentent
généralement une chlorose ou une couleur blanc pâle sur les
jeunes feuilles, et les tomates présentent soit une chlorose
internervaire, soit une chlorose diffuse sur les jeunes feuilles (Akeel et
Jahan, 2020).
La toxicité du cobalt pour les plantes est rare dans
les sols naturels, mais elle se produit lorsque les plantes poussent dans des
sols contaminés par le Co. La contamination des sols par le Co provient
principalement des activités d'extraction et de fusion, de
l'élimination des boues d'épuration et de l'utilisation d'engrais
chimiques (Hamilton, 1994). Comme indiqué ci-dessus, les plantes peuvent
contrôler l'absorption, le transport et la distribution du Co. Cependant,
lorsque le Co dans les sols contaminés devient hautement disponible, le
Co peut obtenir un avantage compétitif sur le Fe, ce qui entraîne
une plus grande absorption de Co que de Fe par l'IRT1. Avec des concentrations
croissantes de Co à l'intérieur des cellules, FPN2 peut ne pas
être en mesure de séquestrer efficacement le Co dans la vacuole,
ce qui entraîne une plus grande quantité de Co à
transporter des racines aux pousses.
11
1.4. Généralités sur la culture de
blé
Le blé est un terme qui désigne plusieurs
céréales appartenant au genre triticum, ce sont des plantes
annuelles cultivées dans de très nombreux pays. Le mot «
blé » désignait également le « grain »
(caryopse) produit par ces plantes. Le blé tendre (Triticum
aestivum) et le blé dur (Triticum durum) sont les deux
espèces les plus cultivées du genre Triticum dans le monde et le
blé tendre fait partie des trois grandes céréales avec le
maïs et le riz dont il est plus consommé par l'homme avec le riz et
la troisième culture par l'importance de la récolte mondiale
(Tavernier et Lizeaux, 1993).
De tous les types de blés, deux ont une importance
économique majeure :
Le blé dur (Triticum durum) est surtout
cultivé dans les régions sèches et chaudes au sud de
l'Europe et en Afrique du Nord. Riche en gluten, il est employé pour les
semoules et pâtes alimentaires (Clerget, 2011).
Le blé tendre ou froment (T. aestivum), le
plus cultivé, est produit dans les zones plus tempérées
comme le nord de l'Europe et du continent américain pour la confection
de la farine panifiable (Sabbagh, 2006).
1.4.1. Origine du blé
Il y a 10 000 ans, à la fin de la dernière
glaciation, des blés proches de ceux que nous cultivons aujourd'hui
poussaient sur de vastes surfaces au Moyen-Orient, qui remonte au
néolithique (environ 5000 ans avant J.C.) et
peut-être même au mésolithique (7000 avant J.C), (Erroux,
1961).
- Origine géographique
L'origine géographique des blés est un des point
les plus discutés ; à ce sujet plusieurs théorie et
hypothèses ont été émises
(Valdeyron, 1961). En effet selon Laumont et
Erroux (1961), les recherches effectuées depuis fort longtemps sur le
centre d'origine des blés ; basées sur des arguments
archéologiques et phylogénétiques, permettant d'admettre
que les trois groupes d'espèces du genre Triticum aurait trois centres
d'origine distincts.
Selon (Vavilov, Auriau, 1967 et Moule, 1980) ces groupes sont
repartie comme suit :
? Groupes des Diploïdes : dont le centre d'origine est le
foyer SYRIEN et le nord PALISTINIEN.
? Groupes des Tétraploïdes : ayant comme centre
d'origine l'ABYSSINIE.
12
? Groupes des Hexaploïdes : dont le centre d'origine est le
foyer AFGHANO-INDIEN. Pour (Grignac ,1978), le moyen orient ou coexistent, les
deux espèces parentales et où l'on a retrouvé de
nombreuses forme de blé dur, serait le centre géographique.
A partir de cette zone d'origine, l'espèce s'est
différenciée dans trois centre : le bassin occidental, la
méditerranée, le sud de l'ex URSS et le proche orient.
L'Afrique du nord est considérée comme un centre
secondaire de diversification de l'espèce (Bensemra, 1990).
La diffusion des blés vers l'Afrique par la route la plus
ancienne gagna l'Égypte vers 6 000 avant aujourd'hui et se poursuivit
vers le Soudan et l'Éthiopie, au sud, et vers la Libye à l'est.
D'autres voies d'introduction furent maritimes : à partir de la
Grèce et de la Crète, certains blés rejoignirent
également la Libye ; d'autres, en provenance du Sud de la
péninsule italienne et de la Sicile, parvinrent aux côtes de la
Tunisie, du Maroc et de l'Algérie (Bonjean, 2001).
- Origine génétique
Les espèces de blé tirent leur origine
génétique de croisements naturels entre Triticum
monococcum, Triticum urartu et des espèces sauvages
apparentées appartenant à Aegilops (Aegilops
speltoïdes) ; Triticum monococcum et Triticum urartu
sont les premières formes de céréales
cultivées, elles sont de constitution génomique 2n = 14. (Feldman
et Sears, 1981).
1.4.2. Classification botanique et description
morphologique
- Classification botanique :
Le blé est une plante herbacée,
monocotylédone appartenant au groupe des céréales à
paille. Il est une monocotylédone classée de la manière
suivante :
13
Tableau 2. Classification systematique du blé
selon (Van Den Abeelz, 1956)
|
Taxon
|
Noms
|
|
Espèce
|
Triticum aetivum
|
|
Genre
|
Triticum
|
|
Tribu
|
Triticeae
|
|
Famille
|
Poaceae
|
|
Ordre
|
Poales
|
|
Classe
|
Liliopsida
|
|
Embranchement
|
Magnoliophyta
|
|
Règne
|
Plantae
|
- Description morphologique :
? Le grain de blé : le grain est un
caryopse, c'est un fruit sec indéhiscent, il est de couleur jaune
ambrée à violacée selon l'espèce blé dur ou
blé tendre et selon la variété. Il présente une
partie plane (ventrale) et une partie dorsale légèrement
bombée. La base élargie contient le germe est le sommet est garni
de petits poils (la brosse), la partie ventrale est fondue par un sillon qui
pénètre profondément dans le grain, cependant la partie
dorsale présente une arête plus ou moins prononcée (Gond et
al., 1986 in Oudjani, 2009). Chez le blé dur comme la plupart
des graminées possèdent un fruit sec (caryopse), celle-ci
distingué par un grain étroit allongé à sillon
profond à brosse peu développé et à texture souvent
vitreuse (Bachir Bey Ilhem et al 2015). Elle est entourée d'une
matière végétale qui la protège des influences
extérieures. Elle est constituée d'un germe ; la partie
essentielle du fruit permettant la reproduction de la plante: il se
développe et devient à son tour une jeune plante et d'une amande
avec 65 à 70% d'amidon ainsi qu'une substance protéique (le
gluten) dispersée parmi les grains d'amidon (Bebba 2011).
14
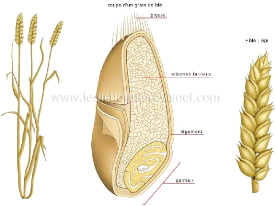
Figure 2. Anatomie du grain de blé
? La tige : La tige commence à prendre
son caractère au début de la montaison, c'est-à-dire prend
sa vigueur et porte 7 à 8 feuilles, elle présente des bourgeons
auxiliaires que servent à l'origine des talles, elle s'allonge
considérablement à la montaison. (Alismail et al.,
2017).
? Les feuilles : les feuilles sont à
nervures parallèles. Le limbe possède souvent à la base
deux prolongements aigus embrassant plus ou moins complètement la tige :
les oreillettes ou stipules ; à la soudure du limbe et de la gaine peut
se trouver une petite membrane non vasculaire entourant en partie le chaume
(Belaid, 1986). La feuille terminale a un
rôle primordial dans la reproduction (Soltner,
1988).
? Les racines du blé sont fibreuses :
à la germination la radicule ou racine primaire, et un entre-noeud
sub-coronal émergent du grain. Le système racinaire secondaire
peut être assez développé, s'enfonçant à des
profondeurs atteignant jusqu'à deux mètres. Il apporte les
éléments nutritifs à la plante
(Soltner, 1988). Les racines
de blé sont de type fasciculé peu développé dont on
peut distinguer des racines primaires qui assurent la croissance de la plantule
jusqu'au tallage tandis que les racines secondaires ou adventices sont
émises à partir du plateau de tallage. Celles produites par la
plantule durant la levée sont des racines séminales tandis que
ces adventives se forment plus tard à partir des noeuds à la base
de la plante et constituent le système racinaire permanent (Maamri,
2011). La profondeur des racines est variable selon le travail du sol ainsi que
l'humidité du sol. Pour Bachir Bey et al., (2015), 50% du poids
total des racines se trouvé entre 0 - 25 cm, 10% entre 20 - 50 cm mais
elles peuvent atteindre 1m à 1.2m
15
dans un sol bien profond. Cependant pour Fritas, (2012), 55 %
du poids total des racines se trouve entre 0 et 25 cm de profondeur.
? Les fleurs : sont regroupées en une
inflorescence composée d'unités morphologiques de base : les
épillets. Chaque épillet compte deux glumes (bractées)
renfermant de deux à cinq fleurs distiques sur une rachéole
(Soltner, 1988). Elles sont groupées
en inflorescence ou épillets qui s'attachent à l'axe ou rachis de
l'épi portant de 15 à 25 épillets par épis
(Benderradji, 2013) et comportant de 3 à 5 fleurs, tandis que chaque
fleur est enveloppée de deux glumelles l'une à l'intérieur
et l'autre à l'extérieur dont chacune compte trois
étamines à anthères biloculaires, ainsi qu'un pistil
à deux styles à stigmates plumeux qui peut produire un fruit
à une seule graine, soit le caryopse (Maamri, 2011). Au cours de la
fécondation, les anthères sortent des fleurs tandis que le grain
est à la fois le fruit et la graine (Bebba 2011). La fécondation
de la fleur a lieu à l'intérieur des glumelles, avant la sortie
des étamines à l'extérieur (Benderradji ; 2013).
1.4.3. Cycle biologique du blé
1. La période
végétative
Elle se caractérise par un développement
strictement herbacé et s'étend du semis jusqu'à la fin de
tallage (Bada., 2007).
- La germination-levée
Cette phase comprend une période de l`imbibition de la
graine, libération des enzymes et dégradation des réserves
assimilables par la graine, ensuite c'est la phase de croissance
caractérisée par l`allongement de la radicule (Hennouni, 2012).
C'est un passage de la semence de l'état de vie lente à
l'état de vie active (Benchikh , 2015). Le grain de blé absorbe
au moins 30% de son poids en eau (Fritas, 2012). Juste à la
levée, les premières feuilles déclenchent la
photosynthèse. On parlera de levée lorsque 50 % des plantes
seront sorties du sol (Ait Slimane AitKaki, 2008).
Les téguments se déchirent, la racine principale
est couverte d'une enveloppe appelée coleorhize apparaît, suivie
par la sortie de la première feuille, couverte d'une enveloppe
appelée coléoptile (Fritas., 2012). Ces organes jouent un
rôle protecteur et mécanique pour percer le sol (Ait Slimane
AitKaki, 2008).
Au cours de la germination la coléorhize
s'épaissit en une masse blanche et brise le tégument de la graine
au niveau du germe, c'est le début de l'émission des racines
primaires, garnis de poils absorbants, tandis que le coléoptile gainant
la première vraie feuille, s'allonge vers la
16
surface, où il laisse percer la première
feuille, c'est la levée alors que la deuxième et la
troisième feuille suivent bien après (Laala, 2011) et une tige
sur le maitre brin à l'aisselle de la feuille la plus âgée
se lance à la surface du sol (Belagrouz, 2013), puis apparaissent
d'autres racines et feuilles. La durée de cette phase varie avec la
température de 8 à 15 jours (Fritas, 2012).
La date de levée est définie par l'apparition de
la première feuille qui traverse la coléoptile, cependant la
germination de la graine dépend de trois facteurs importants ; l'eau,
l'aération et la température (l'optimum de la germination de
15/25°C) (Bachir Bey, et al 2015). Le blé germe dès
que la température dépasse le 0 °C (Bebba, 2011).
Le rythme d'émission des feuilles est
réglé par des facteurs externes comme la durée du jour et
la température tandis que la somme de température séparant
l'apparition de deux feuilles successives est estimée à
100°C et varie entre 80 °C pour le semis tardif et à 110
°C pour un semis précoce (Bebba 2011).
Les plus grosses graines lèvent les premières et
donnent des plantules plus vigoureuses cependant, la composition des
réserves (teneur en protéines) agit favorablement sur la vitesse
de la germination-levée (Nadjem, 2011).
- Tallage
Cette phase s'amorce à partir de la quatrième
feuille. La formation de la première talle se fait au stade 3 feuilles.
La première talle primaire (maitre-brin) apparaît à
l'aisselle de la première feuille du blé. La
2ème et la 3ème talle apparaissent à
l'aisselle de la 2ème et la 3ème feuille
(Hamadache, 2013 et Salmi,
2015). Le fin tallage est celle de la fin de la période
végétative, elle marque le début de la phase reproductive,
conditionnée par la photopériode et la vernalisation qui
autorisent l'élongation des entrenoeuds (Gate,
1995 et Salmi, 2015).
Le début du tallage est caractérisé par
:
? la formation de nouvelles racines (la plante possède
de 5 à 6 racines primaire) (Bachir Bey et al., 2015).
? stade de formation du plateau de tallage : c'est le
phénomène de "pré-tallage" dans lequel le deuxième
entre noeud qui porte le bourgeon terminal s'allongé à
l'intérieur de la coléoptile, il cesse de remonter à 2 cm
sous la surface (Laala, 2011), quelle que soit la profondeur du semis, à
ce niveau on assiste à l'apparition d'un renflement : c'est le futur
plateau de tallage (Benchikh, (2015) il se forme presque au niveau de la
surface du sol ( Bachir Bey et al., 2015).
? stade d'émission des talles : Des valeurs de la
variance fortement significatives et positives pour le nombre d'épillets
par épi ont été retrouvées chez tous les
croisements
17
effectués par Emir (2010) et qui exhibent aussi un
hétérobeltiosis significatif et positif. Bachir Bey et
al., (2015) à l'aisselle des premières feuilles du
blé des bourgeons axillaires entre, alors en activité pour donner
de nouvelles pousses: les talles. Bencheikh, (2015), la première talle
se forme à la base de la première feuille et la deuxième
talle à la base de la deuxième feuille. Ouanzar (2012), les
bourgeons axillaires à l'aisselle des feuilles des talles donnent
naissance à l'émission de talles secondaires. Il apparaît
à partir de la base du plateau de tallage, des racines secondaires ou
adventives, qui seront à l'origine de l'accroissement du nombre
d'épis. Le stade fin tallage c'est-à-dire au stade "épi
à 1 cm du plateau de tallage, est caractérisé par une
croissance active des talles. Le plant de blé a besoin, durant cette
phase, d'un important apport d'engrais azotés (Bebba 2011).
L'importance du tallage dépendra de la
variété de, la densité de semis, la densité
d'adventices et de la nutrition azotée cependant, le tallage marque la
fin de la période végétative et le début de la
phase reproductive, qui est conditionnée par la photopériode et
la vernalisation qui autorisent l'élongation des entre-noeuds (Ait
Slimane AitKaki, 2008).
2. Période de reproduction
- Phase de la montaison
Au cours de cette phase pour Fritas (2012), les talles
montantes entrent en compétitions pour les facteurs du milieu avec les
talles herbacées qui de ce fait n'arrivent pas à monter en
épis à leur tour. Ces dernières régressent et
meurent (Laala, 2011). Ce phénomène se manifeste chez un certain
nombre de talles herbacées qui commence (jeunes talles) par une
diminution de la croissance puis par un arrêt de celle-ci alors que,
d'autres se couronnent par des épis (Laala, 2011). Pendant cette phase
de croissance active, les besoins en éléments nutritifs notamment
en azote sont accrus (Ait Slimane AitKaki, 2008). Non seulement deviennent
très importants mais aussi déterminent le nombre d'épis,
le nombre de grain par épi et le poids maximal du grain (Benchikh 2015).
La montaison s'achève à la fin de la sortie de la dernière
feuille et le début du gonflement qui engaine les épis dans la
gaine (Nadjem, 2011).
- Phase de l'épiaison et de
fécondation
Elle est marquée par la méiose pollinique,
l'éclatement de la gaine avec l'émergence de l'épi. C'est
au cours de cette phase que s'achève la formation des organes floraux et
s'effectue la fécondation (Soltner, 2005).
18
La vitesse de croissance de la plante est maximale. Cette phase
correspond à l'élaboration d'une grande quantité de la
matière sèche, cette phase dépend étroitement de la
nutrition minérale et de la transpiration qui influence le nombre final
de grains par épi (Masale, 1980 ; Soltner, 2005). - La
maturation du grain
Au cours de cette phase, l'embryon se développe et
l'album se charge de substances de réserve. On observe une augmentation
du volume du poids des graines (stade laiteux). Ensuite, le poids frais des
grains continue à augmenter alors que celui des tiges et des feuilles
diminue (stade pâteux). Puis les grains deviennent durs et leur couleur
devient jaunâtre (Boufnar-Zaghoune et Zaghouane, 2006).
I.1.5. les exigences climatiques
Pour être rentable, la production des
céréales nécessite une connaissance accrue du
développement de la culture. Selon Djermoun, (2009) les facteurs
climatiques ont une action prépondérante sur les
différentes périodes de la vie du blé. Parmi ces facteurs
on citera principalement :
- Température
La germination commence dès que la température
dépasse 0°C, avec une température optimale de croissance
située entre 15 à 22° C. Les exigences globales en
température sont assez importantes et varient entre 189o et
24 °C selon les variétés.
De même la température agit sur la vitesse de
croissance, elle ne modifie pas les potentialités
génétiques de croissance, c'est la somme de température
qui agit dans l'expression de ces potentialités. Chaque stade de
développement du blé nécessite des températures
particulières (Ondo., 2014).
- L'humidité
Les besoins en eau de la culture du blé varient entre
450 et 650 mm selon le climat et la longueur du cycle végétatif
(Baldy, 1974).
- La photopériode
Le rayonnement solaire et la durée du jour consolide
l'effet positif de la température sur le rendement quand elle n'est pas
très élevée et accentue son effet négatif dans le
cas contraire. La photopériode affecte aussi la durée de chacune
des périodes de développement citées. Les
variétés du blé diffèrent quant à leur
sensibilité à la photopériode (Kalarasse., 2018).
19
- L'eau
L'eau est un facteur limitant de la croissance du blé. Ce
dernier exige l'humidité permanente durant tout le cycle de
développement. Pendant les différentes phases de son cycle, les
besoins sont plus élevés au vu des conditions climatiques
défavorables (Bennai et Benabbas, 2007).
- La lumière
La lumière est le facteur qui agit directement sur le bon
fonctionnement de la photosynthèse et le comportement du b lé. Un
bon tallage est garanti si le blé est placé dans les conditions
optimales d'éclairement (Felliet, 2000).
1.4.4. Importance de la culture
Historiquement, le blé est l'une des premières
céréales cultivées et consommées dans le monde avec
une production annuelle d'environ 600 millions de tonne (Ricroch et
al., 2011). Les échanges qui se multiplient entre les
régions du monde font de cette céréale l'un des principaux
acteurs de l'économie mondiale (Laberche, 2004).
La production du blé est surtout localisée dans
le bassin méditerranéen d'une part (Europe du Sud, Moyen orient,
Afrique du Nord), et en Amérique du Nord d'autre part (Canada central et
Nord des USA), où est produit le quart du blé dur mondial
(Clerget, 2011).
Depuis la nuit des temps les céréales
nourrissent l'humanité, produire mieux et plus a été
nécessaire pour répondre aux besoins d'une population
grandissante. Nos ancêtres ont dû apprendre à
améliorer progressivement les techniques de production,
sélectionner des semences avec un meilleur potentiel
génétique. Depuis longtemps, les céréales,
notamment le blé est devenu un produit de première
nécessité à l'échelle mondiale. Son importance
dépasse le rôle traditionnel considéré comme aliment
(Ammar, 2015).
L'amidon du blé tendre est également
utilisé depuis plusieurs années comme matière
première pour la fabrication de biocarburants (Clément, 2010). En
2018, la production mondiale de blé a atteint 762 millions de tonnes
contre 732 millions de tonnes pour 2019 (CIC, 2019). Au cours la compagne
agricole 2018-2019, les principaux producteurs de blé mondiaux sont, par
ordre décroissant, sont l'Union Européenne (137.600 milliers de
tonnes), la Chine (131.430 milliers de tonnes), l'Inde (99.700 milliers de
tonnes), la Russie (71.600 milliers de tonnes), les Etats Unies (51.287
milliers de tonnes) et le Canada (31.800 milliers de tonnes) (Statista, 2019).
Le marché mondial du blé est segmenté en différents
groupes de pays qui ont diverses capacités de production et de
consommation de blé, ce qui rend ce marché plus propice à
la volatilité des
20
prix. Seulement 20% de la production mondiale du blé
est échangée et il s'agit d'un marché de surplus et
d'excédents. Cependant ce commerce mondial du blé a
été multiplié par trois entre 1961 et 2005 et le
blé conforte ainsi sa place de céréale « la plus
échangée » dans le monde. (CIC, 2019).
21
Chapitre 2. Milieu, matériels et méthodes
2.1. Milieu d'étude
2.1.1. Situation géographique
Le présent travail a été
réalisé dans la région de Lubumbashi, située au
Sud-est dans la province du Haut-Katanga en République
démocratique du Congo ; à une altitude d'environ 1250 m et elle
est située entre 11° 20' et 12° de latitude Sud et 27°
10' et 27° 40' de longitude Est.
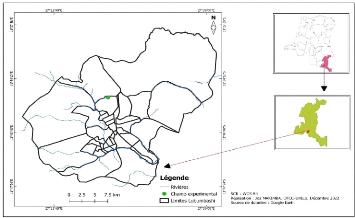
Figure 3. Localisation du milieu
d'étude
2.1.2. Climat
La ville de Lubumbashi appartient au type du climat Cw6
d'après la classification de Koppen. Ce climat est
caractérisé par une alternance de deux saisons durant 6 mois
chacune avec une période de transition au mois d'Avril (la saison des
pluies et la saison sèche). Les précipitations annuelles varient
entre de 1270 mm et de 1770 mm (FAO, 2005).
Le climat de la ville de Lubumbashi est donc tropical humide,
caractérisé par une alternation des deux saisons : (1) la saison
sèche qui dure 6 mois et 7 mois ; elle débute, en moyenne, le 20
avril et prend fin vers le 20 octobre ; (2) la saison des pluies qui dure 6
mois, du mois d'Octobre à Avril (soit 230 à 240 jours de pluie ;
Kasongo, 2009 ; Mukalay, 2016). Durant la saison des pluies, il tombe une
moyenne de 1200 mm, ce qui signifie qu'il ne pleut presque pas durant la saison
sèche.
22
La température moyenne annuelle varie autour de
20°C. Les mois les plus chauds sont ceux d'octobre et novembre avec une
moyenne maximum journalière de 32°C et une température
moyenne mensuelle de 23°C. Par contre, le mois de juillet est le mois le
plus froid avec la moyenne minimum journalière de 8°C, la
température moyenne mensuelle étant de 17°C (FAO, 2005 ;
Mpundu, 2010). Le taux d'humidité moyenne annuelle est de 68 % avec les
niveaux d'humidité mensuelle dont les moyennes varient d'un minimum de
47% en saison sèche (septembre) et un maximum de 86% durant la saison
des pluies (février) (Mpundu, 2010).
2.1.3. Sol
Le Haut-Katanga, étant une province minière, est
caractérisée par les sols polygéniques, qui proviennent
principalement du socle précambrien de Lubumbashi synclinal
dominé en grande partie des schistes de la série de Kundelungu
(Kasongo, 2009). Les sols du Haut-Katanga font partie des sols
latéritiques désaturés jaune-rouge. Ils sont
caractérisés par une abondance des matériaux argileux
(Kaolinite) avec une faible capacité d'échange cationique (CEC),
du Fer, des sesquioxydes d'Aluminium et un pHeau flottant à 5,2 (Kasongo
et al., 2013).
Les sols du Haut-Katanga sont très diversifiés
par leur nature. La carte des sols élaborée par l 'ISRIC (Van
Engelen et al., 2006 in Kasongo 2009) dans le cadre de la base des
données SOTER montre, la dominance de groupes des sols de
référence suivants : Ferralsols, Vertisols, Cambisol et
Fluvisols.
Les Ferralsols orthiques, Vertisols, Combisols et Gleysols
sont les principaux groupes qui constituent les différentes classes des
sols dans le Haut-Katanga, ils font partie des sols tropicaux récents et
terres noires tropicales de la classification de l'INEAC (Kasongo, 2009). Le
relief est caractérisé par les chaines des montagnes de Mitwaba,
Kundelungu et d'Upemba.
2.1.4. Hydrographie
Ville située sur plusieurs confluents. Le principal,
plus proche du centre historique et définissant la position du plateau
sur lequel est posée la ville, est celui de la Kafubu avec la
Lubumbashi, son affluent, au sud du noyau urbain originel. Les autres
confluents dans l'agglomération ont lieu entre la Lubumbashi et la
Karavia au centre-ouest de la ville, la Kafubu et la Ruashi à l'est, et
entre la Kafubu et la Naviundu, au sudouest. Des dembos (savannes
saisonnièrement inondées) sont formés dans certains fonds
de vallée des petits affluents. Un lac de retenue a été
aménagé sur la Lubumbashi, dans la partie nord de
l'agglomération (Vranken, 2010).
23
2.1.5. Végétation
Les principales unités de végétation dans
le Haut-Katanga sont : les forêts denses sèches, les forêts
denses édaphiques, les forêts claires, les savanes et les milieux
aquatiques (Muganguzi, 2016). Le Haut-Katanga et ses environs sont
caractérisés par des savanes arborées anthropiques, ce qui
entraîne la dégradation des forêts de Miombo en savane et
arbustive et finalement en savane herbeuse (Malaisse, 1997). La forêt
claire du type Miombo s'impose comme l'écosystème le plus
dominant, il a fait l'objet des nombreuses études, tant botaniques,
phytosociologiques, zoologiques qu'écologiques (Meerts et Hasson, 2016 ;
Malaisse, 2018).
Les forêts dans le Haut-Katanga se distinguent en quatre
types principaux ci-après : la forêt claire (Miombo), la
forêt dense tropicale (Mushitu), et la forêt sèche
sempervirente (Muhulu) (Malaisse et al., 1972), et les forêts denses
marécageuses des hauts plateaux qui sont méconnues (Malaisse,
2018). La forêt claire à Brachystegia appelée « Miombo
» est le biome dominant caractérisé par de
termitières occupant aussi une grande surface terrière, elle
couvre plus de 80% du territoire et constitue une ressource économique
très importante pour la province (Mujinya et al., 2014).
2.2. Matériels
2.2.1. Matériels végétal
> La variété du blé choisie
appelée « 59/26 » est une variété qui provient
du Mexique, elle a un cycle végétatif de 120 jours, elle peut
atteindre une hauteur de 120cm et donne un rendement de 1 à 2t/ha.
2.2.2. Matériels non biologiques
> Une latte
> Des pots avec sous-plats
> Un stylo
2.2.1. Matériels chimiques
Pour notre étude nous avons utilisé les
réactifs ci-après que nous avons contaminés au sol.
> Le sulfate du cuivre pentahydraté : CuSO4 5H2O
> Le sulfate de cobalt heptahydraté : CoSO4 7H2O
Figure 4. Schéma du dispositif expérimental
adopté
24
2.3. Méthodes
Deux essaies séparés sont adoptés, l'un
pour le Cu et l'autre pour le Co. les substrats reçoivent 4 traitements
en utilisant le sulfates de cuivre pentahydraté (CuSO4 5H2O) et le
sulfates de cobalt heptahydraté (CoSO4.7H2O), elles sont
mélangées directement au sol dans les pots. Les doses initiales
étaient respectivement de T0 : 0 ppm ; T1 : 50 ppm ; T2 : 100 ppm ; T3 :
200 ppm (mg.kg-1), lorsque les grains ont été mises en
terre, il n'y avait aucun grain qui a germé sauf dans le traitement
témoin, sur ce nous avons dilué la concentration de chaque
traitement 3 fois, et nous avons eu des concentrations diluées suivantes
: T0 : 0 ppm ; T1 : 16 ppm ; T2 : 33 ppm ; T3 : 66 ppm.
Tableau 3. Quantité de sulfates de cuivre
pentahydraté et de sulfates de cobalt
heptahydraté en gramme
qui doit être apportée à chaque pot.
|
TO
|
T1
|
T2
|
T3
|
|
Doses (ppm)
|
0
|
16
|
33
|
66
|
|
CuSO4 5H2O (g)
|
0
|
5,5
|
13
|
26,2
|
|
CoSO4 7H2O (g)
|
0
|
8
|
16
|
32
|
Le dispositif expérimental adopté est en Blocs
aléatoires complets et comporte quatre traitements (4), avec trois (3)
répétitions.

BLOC 1
BLOC 2
BLOC 3
T0R1 T1R1 T2R1 T3R1
T3R2 T2R2 T1R2
T2R3 T3R3 T0R3 T1R3
T0R2
T0 : 0 ppm ; T1 : 16 ppm ; T2 : 33 ppm ; T3 : 66 ppm.
> Le nombre de feuilles par plantes : le nombre des thalles a
été prélevé au 20eme et au 40eme jour.
25

Figure 5. Dispositif expérimentale adopté
pour le CuSO4 5H2O et pour le CoSO4 7H2O séparément
2.3.1. Conduite de l'essai
+ Prélèvement du sol
expérimental
Le sol expérimental a été
prélevé dans la foret da Miombo, et 4 échantillons
composites ont été prélevé sur une superficie de
1ha, et les échantillons ont été
homogénéiser et après conditionné dans les pots.
+ Le semis
Nous avons effectué un semis direct dans les pots, et les
pots avaient une capacité de contenir 1kg de sol, à raison de 4
grains par pot, disposé systématiquement.
+ L'arrosage
En ce qui concerne l'arrosage, elle se faisait dans les
sous-plats pour éviter le tassement du sol à la surface du
sol.
2.3.2. Paramètres mesurés
? Paramètres morphologiques
> Le taux de survie : le taux de survie en (%) a
été prélevé au 15eme jour ainsi que au 30eme
jour.
> La hauteur des plantes : la hauteur des plantes en (Cm) a
été mesure au 20eme et au 40eme jour.
26
? La longueur des racines : après la récolte des
plantes nous avons mesuré la longueur de racines en (Cm).
2.3.2. Analyses statistiques
Les analyses de la variance (ANOVA) pour les paramètres
végétatifs notamment (le taux de germination, le taux de survie,
la hauteur de plantes, le nombre de feuilles, la longueur de racine) du
blé ont été réalisées à l'aide du
logiciel R. Le test de Tukey a été utilisé en vue de
comparer les différentes moyennes à l'aide du logiciel MINITAB,
nous avons utilisé Excel 2019 pour la réalisation des
graphiques.
27
Chapitre 3. Interprétation des résultats
3.1. Résultats obtenus avec le traitement de Cu
3.1.1. Taux de germination (%)
En ce qui concerne le taux de germination, l'analyse de la
variance montre qu'il y a des différences significatives entre les
différents traitements (P < 0,05). En effet, le taux de germination
des grains de blé tendre tend à diminuer de manière
inversement proportionnelle aux concentrations croissantes du Cu comme la
figure (8) l'illustre.
MOYENNE
A
120
|
T.G 10 jours
|
100
80
|
|
|
|
|
|
|
AB
|
|
|
|
60
40
|
|
BC
|
|
|
20
0
|
|
C
|
|
|
|
|
|
|
Temoin 16 ppm de Cu 33 ppm de Cu 66 ppm de Cu
Traitements
Figure 6. Taux de germination à 10 jours en
fonction des traitements
Figure 8. Taux de survie à 40 jours en fonction
des traitements
28
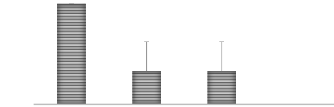
3.1.2. Taux de survie (%)
L'analyse statistique révèle un effet
significatif (P < 0,05) sur le taux de survie des plantes de blé
tendre à 15 jours, la moyenne la plus élevée a
été observée au traitement témoin avec une valeur
de 100% et la moyenne les plus faibles ont été observées
avec tous les traitements ayant reçu du Cu (figure 9).
MOYENNE
A
120
Temoin 16 ppm de Cu 33 ppm de Cu 66 ppm de Cu
Traitements
T.S 15 jours
100
40
80
60
20
0
B B
B
Figure 7. Taux de survie à 15 jours en fonction
des traitements
MOYENNE
120
Temoin 16 ppm de Cu 33 ppm de Cu 66 ppm de Cu
Traitements
T.S 40 jours
100
40
80
60
20
0
B
B B
A
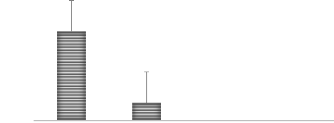
Egalement l'analyse statistique révèle une
différence significative entre les différents traitements, en ce
qui concerne le taux de survie à 40. La moyenne la plus
élevée a été observé au traitement
témoin comme la figure (10) l'illustre.
Figure 10. Hauteur des plantes à 40 jours en
fonction des traitements
29
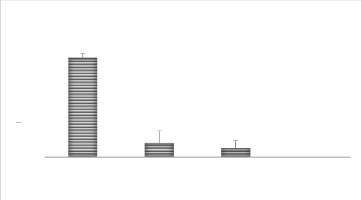
3.1.3. Hauteur de plantes (Cm)
La figure (11) met en évidence l'effet des
différentes concentrations du Cu sur la hauteur moyenne des plantes de
blé tendre après 20 jours de traitement. Une diminution nette de
la hauteur des blés cultivés sur des traitements au Cu comme le
montre la figure 11.
A
30
25
H.P 20 jours
20
15
10
5
0
B B
B
Temoin 16 ppm de Cu 33 ppm de Cu 66 ppm de Cu
Traitements
MOYENNE
Figure 9. Hauteur des plantes à 20 jours en
fonction des traitements
H.P 40 jours
Temoin 16 ppm de Cu 33 ppm de Cu 66 ppm de Cu
Traitements
MOYENNE
35
30 A
Pour la hauteur de plantes à 40 jours, l'analyse
statistique montre qu'il y a une différence significative entre les
différents traitements témoin d'une part et tous les traitements
avec le Cu.(P < 0,05), la moyenne la plus élevée étant
observée dans le traitement témoin comme l'illustre la figure
12.
Figure 12. Nombre des feuilles à 40 jours en
fonction des traitements
30
3.1.4. Nombre de feuilles
Pour le nombre de feuilles à 20 jours, l'analyse
statistique montre qu'il y a plus de feuilles sur le blé du traitement
témoin qu'il y en a sur les traitements au Cu. Une différence
significative entre les deux tendances (P < 0,05), une fois de plus les
traitements au Cu affiche la valeur la plus faible que celle du témoin
(figure 13).
|
N.F 20 jours
|
5
4
3
2
|
|
B
|
B
|
|
|
|
|
|
1
0
|
|
B
|
|
|
|
|
|
Temoin 16 ppm de Cu 33 ppm de Cu 66 ppm de Cu
Traitements
MOYENNE
7
6 A
Figure 11. Nombre des feuilles à 20 jours en
fonction des traitements
N.F 40 jours
MOYENNE
7
A
Temoin 16 ppm de Cu 33 ppm de Cu 66 ppm de Cu
Traitements
Au quarantième jour l'analyse statistique dégage
une différence significative entre les traitements témoin et les
traitements au Cu. Le nombre de feuilles du traitement témoin
s'avère plus élevé que celles des traitements qui ont
reçu le Cu. (Figure 14).
31
3.1.5. Longueur des racines (Cm)
La figure (15) met en évidence l'effet des
différentes concentrations du Cu sur la longueur moyenne des racines de
blé tendre après 40 jours de traitement. Nous constatons une
diminution de la longueur moyenne des racines inversement aux ayant reçu
le Cu. Cette diminution est significative (P < 0,05) chez les plantés
traitées avec le Cu.
L.R 40 jours
Temoin 16 ppm de Cu 33 ppm de Cu 66 ppm de Cu
Traitements
MOYENNE
16
14
12 A
Figure 13. Longueur des racines à 40 jours en
fonction des traitements
32
3.2. Résultats obtenus avec le traitement
Co
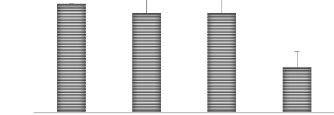
3.2.1. Taux de germination (%)
En ce qui concerne le taux de germination, l'analyse de la
variance montre qu'il y a des différences significatives entre les
traitements témoin, la dose 1 et 2 d'une part et le traitement T3 (P
< 0,05). En effet, le taux de germination des grains de blé diminue
significativement dans la dose la plus élevée comme le montre la
figure (16).
MOYENNE
A
120
Temoin 16 ppm de Co 33 ppm de Co 66 ppm de Co
Traitements
T.G 10 jours
100
40
80
60
20
0
A A
B
Figure 14. Taux de germination à 10 jours en
fonction des traitements
Figure 16. Taux de survie à 40 jours en fonction
des traitements
33
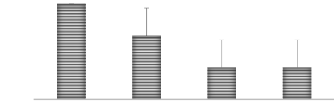
3.2.2. Taux de survie (%)
L'analyse statistique révèle un effet
significatif (P < 0,05) sur le taux de survie des plantes de blé
tendre à 15 jours, la moyenne la plus élevée a
été observée au traitement témoin tandis que les
valeurs les plus faibles s'observent dans le traitement avec 33 ppm de Co et
avec 66 ppm de Co et la valeur la plus élevée revient au
traitement témoin. Le traitement avec 16 ppm étant
intermédiaire entre ces deux tendances comme l'exprime la figure 17.
MOYENNE
A
120
Temoin 16 ppm de Co 33 ppm de Co 66 ppm de Co
Traitements
T.s 15 jours
100
40
80
60
20
0
AB
B B
Figure 15. Taux de survie à 15 jours en fonction
des traitements
MOYENNE
120
100
A
|
T.S 40 jours
|
80
60
40
|
|
AB
|
|
|
20
0
|
|
B B
|
|
|
|
|
Temoin 16 ppm de Co 33 ppm de Co 66 ppm de Co
Traitements
L'analyse de la variance montre une différence
significative entre les traitements en ce qui concerne le taux de survie
à 40 jours, et la moyenne la plus élevée a
été observée au traitement témoin comme l'illustre
la figure (18).
34
3.2.3. Hauteur de plantes (Cm)
La figure (19) met en évidence deux tendances
différentes concentrations du Co sur la longueur moyenne des racines de
blé. La valeur la plus élevé s'observe dans les
traitements témoin et les plus faibles dans les doses ayant reçu
le Co.
MOYENNE
35
30
Temoin 16 ppm de Co 33 ppm de Co 66 ppm de Co
Traitements

H.P 20 jours
25
20
15
10
5
0
B
B B
A
Figure 17. Hauteur des plantes à 20 jours en
fonction des traitements

Figure 18. Variation des hauteurs en fonction des
traitements
35
Pour la hauteur de plantes à 40 jours, l'analyse
statistique montre qu'il y a une différence significative entre les
différents traitements (P < 0,05), la moyenne la plus
élevée observée au traitement témoin et les
moyennes les plus ont été observées avec les traitements
(33 et 66 ppm).
H.P 40 jours
Temoin 16 ppm de Co 33 ppm de Co 66 ppm de Co
Traitements
MOYENNE
45
40
35 A
Figure 19. Hauteur des plantes à 40 jours en
fonction des traitements
Figure 21. Nombre des feuilles à 40 jours en
fonction des traitements
36
3.2.4. Nombre de feuilles
Pour le nombre de feuilles à 20 jours, l'analyse
statistique montre qu'il y a une différence significative entre les
différents traitements (P < 0,05), la moyenne la plus
élevée observée au traitement témoin et les
moyennes les plus faibles ont été observées avec les
traitements (33 et 66ppm de Co).
|
N.F 20 jours
|
5
4
3
|
|
B
|
|
|
2
1
0
|
|
B B
|
|
|
|
|
Temoin 16 ppm de Co 33 ppm de Co 66 ppm de Co
Traitements
MOYENNE
7
6 A
Figure 20. Nombre des feuilles à 20 jours en
fonction des traitements
N.F 40 jours
Temoin 16 ppm de Co 33 ppm de Co 66 ppm de Co
Traitements
MOYENNE
14
12 A
L'analyse statistique dégage une différence
significative entre les traitements pour le nombre de feuilles à 40
Jours, et la moyenne la plus élevée a été
observée au traitement témoin comme la figure (23) l'illustre.
37
3.2.5. Longueur des racines à 40 jours
(Cm)
La figure (23) met en évidence l'effet des
différentes concentrations du Co sur la longueur moyenne des racines de
blé tendre après 40 jours de traitement. Les résultats
montrent une diminution de la longueur moyenne des racines inversement aux
concentrations croissantes du Co par rapport aux témoins. Cette
diminution est significative (P < 0,05) chez les plantés
traitées avec par la concentration de 16, 33, et 66 ppm de Cu.
MOYENNE
14
Temoin 16 ppm de Co 33 ppm de Co 66 ppm de Co
Traitements

L.R 40 jours
12
10
4
8
6
0
2
B
B B
A
Figure 22. Longueur des racines à 40 en fonction
des traitements
38
Chapitre 4. Discussion
4.1. Effet du Cu sur les paramètres
végétatifs du blé tendre
Les résultats montrent les concentrations en Cu ont
exercés un effet négatif significatif sur le processus
germinatif, ce qui s'est traduit par une diminution du pourcentage et de la
cinétique de germination. En effet l'inhibition de la germination des
graines de blé peut-être due à la capacité qu'a le
Cu à se lier aux groupements d'acides aminés, ce qui entrainerait
une inhibition de l'activité des enzymes essentielles (Ferfar, 2017).
Les mêmes constatations ont été rapportées par
Benali et Bouguettaia (2020) qui ont étudié l'effet de
différentes concentrations de nanoparticules de ZnO sur la germination
du blé tendre « Triticum aestivum ». Ces auteurs
expliquent la raison de la diminution de la germination à des
concentrations élevées par augmentation de l'absorption et
l'accumulation des nanoparticules à la fois dans l'espace
extracellulaire et à l'intérieur des cellules, entrainant ainsi
une réduction de la division et une élongation cellulaires et
l'inhibition des enzymes hydrolytiques impliquées dans la mobilisation
des réserves au cours du processus de germination des graines.
Les résultats obtenus dans cette étude en ce qui
concerne la hauteur des plantes, l'analyse statistique montre qu'il y a des
différences significatives entre les différents traitements. En
effet nous constatons que la hauteur de plantes de blé tendre tend
à diminuer de manière inversement proportionnelle aux
concentrations croissantes du Cu, ces résultats sont en accord avec ceux
de Alam et al. (2015) et Woo-mi (2008) qui ont mis en évidence une
inhibition de la germination et de la croissance des plantes de blé
après exposition aux fortes concentrations des nanoparticules de fer et
de Cuivre, respectivement. L'application du Cu au sol diminue la hauteur des
plantes et cause des réductions de 39 à 50%, en comparaison avec
le témoin (Sonmer et Woolhouse, 2006). D'après kaplan (2010), la
hauteur des plantes de tomates a été affectée
significativement par l'application du Cu au sol qui a causé un
décroissement à des doses croissantes.
En ce qui concerne la longueur des racines, la longueur
diminue significativement inversement proportionnelle aux concentrations du Cu,
ces résultats vont dans le même sens que ceux trouvés par
Lexmond et Vorm (1981) qui ont signalé que l'application des niveaux
élevés du Cu inhibe usuellement la croissance des racines avant
d'affecter la production de biomasse aérienne. Cependant, ce ne signifie
pas nécessairement que les racines sont plus sensibles à des
concentrations élevées du Cu, mais probablement, due en
réalité que les racines sont dans un
39
environnement ou le Cu est en excès. D'après
Pahlsson (1989), le Cu généralement atteint le
développement racinaire par l'inhibition de la croissance racines
latérales et de l'initiation de la croissance des racines des jeunes
plantes. Ainsi Ouzounidou (1994) a montré que les concentrations
supérieures du Cu (80 et 160 uM) en solution de culture, mais pas les
inferieures, conduisent à une réduction significative de la
croissance des racines. Lidon et Henriques (1992) ont reporté que la
toxicité du Cu, est exprimée par la taille réduit des
racines, apparait comme le résultat directe de l'accumulation du Cu en
excès dans les tissus.
4.2. Effet du Co sur les paramètres
végétatifs du blé tendre
Les résultats montrent que le les concentrations de Co
ont exercés un effet négatif significatif sur les
différents paramètres morphologiques de la culture de blé,
les mêmes constats ont été faits par Li et al. (2020) qui
ont montré que les concentrations de Co dans les pousses d'orge, de
colza et de tomate étaient linéairement corrélées
avec le Co de la solution du sol. Par conséquent, un excès de Co
dans les pousses peut initialement provoquer un stress oxydatif, entrainant une
augmentation des activités enzymatiques antioxydants (Tewari et al.,
2002). A mesure que les stress progresse, le Co peut entrer en
compétition avec le Fe ou le Mg dans le chloroplaste en diminuant la
teneur en chlorophylle (Lwalaba et al., 2017), ce qui entraine une carence en
Fe et une couleur jaunâtre des nouvelles feuilles en croissance, comme
l'on reporté Sree et al. (2015), le Co est capable d'inhiber
l'activité des enzymes impliquées dans la biosynthèse des
intermédiaires de la chlorophylle, ce qui réduira les
activités photosynthétiques nettes.
Les études de Gopal (2003) montrent que l'excès
du Co à entrainer chez la tomate des symptômes de chlorose diffuse
des jeunes feuilles a partir de la base et des taches nécrotiques
ultérieures sont apparues sur les zones chlorotiques. Ces effets
étaient plus graves à 0,5 mM et l'intensité des
symptômes diminuait progressivement avec une diminution de l'apport de Co
de 0,5 Mm à 0,05 mM.
Le cobalt affecte également négativement la
translocation de P, S, Cu, Mn et Zn des racines aux pousses (Chatterjee et al.,
2000). Tous ces facteurs, agissant ensemble, peuvent entrainer une
phytoxicité et réduire considérablement la croissance des
plantes. Différentes plantes présentent des capacités
différentes à tolérer le Co. Les plantes d'ivoine ont
été affectés négativement lorsqu'ils ont
été cultivés dans une solution de sol contenant 0,14 mg/l
de Co (Anderson et al., 1973). Les plantes de riz développeraient des
symptômes toxiques lorsqu'ils
40
sont cultivés dans des sols dont la teneur en Co
variait entre 25 et 50 mg/kg (Kitagishi et Yamane, 1891). Les études de
chatterjee, 2003 ; Gopal et al., 2003 ; Karuppanapandian et Kim, 2013 ; Lwalaba
et al., 2017) montrent l'effet toxique du Co sur les plantes, plus
précisément sur la culture de l'orge lors d'une exposition
à court terme pouvait être atténué en ajoutant du Cu
au milieu nutritif.
41
Conclusion
La présente étude avait comme objectif principal
d'évaluer les effets de la toxicité du cuivre et du cobalt sur la
croissance du blé tendre dans la région de Lubumbashi. Deux
essaies séparés ont été adoptés, l'un pour
le Cu et l'autre pour le Co. Le dispositif expérimental adopté
était en Blocs aléatoires complets, comportant quatre traitements
(4), avec trois (3) répétitions.
Les principaux résultats ont montré qu'il y
avait des différences significatives entre les différents
traitements dans tous les deux essaies, et pour tous les paramètres
végétatifs observés notamment le taux de germination ; le
taux de survie ; la hauteur de plantes, le nombre des feuilles ainsi la
longueur des racines, il s'avère que les traitements témoins ont
donné les meilleures moyennes pour tous les paramètres
observés dans les deux essais. Par conséquent nous pouvons dire
que les concentrations croissantes du Cu et Co ont un effet négatif
significatif sur les plantes de blé tendre.
N'ayant pas l'intention de limité la recherche dans ce
domaine, les prochaines études pourront multiplier le nombre de
traitements ainsi que de répétition pour justement affirmer ou
infirmer les théories avancées dans cette étude.
42
Bibliographie
Adriano, D.C. (2001). Trace éléments in
terrestrial environments: Biochemistry, bioavailability and risks of metals.
Springer-Verlag, New York. Antosiewicz, D.M. (2005). Study of calcium-dependent
lead-tolerance on plants differing in their level of Ca-deficiency tolerance.
Environ. Pollut. 134, 23-34.
AIEA (2010). Handbook of parameter values for the prediction
of radionuclide transfer in terrestrial and freshwater environments. Technical
reports series 472. AIEA, Vienne. 194 p.
Ait Kaki S., 2008. Contribution à l'étude de
l'interaction génotype x milieu, pour la qualité technologiques
chez le blé dur en Algérie. Thèse doctorat,
Université de Annaba, 174 p.
Alaoui-Sosse, B., Genet, P., Vinit-Dunand, F., Toussaint, M.
L., Epron, D. et Badot, P. M. (2004). Effect of copper on growth in cucumber
plants (Cucumis sativus) and its relationships with carbohydrate accumulation
and changes in ion contents, Plant Science, 166, 5, 1213-1218.
Albrecht A., Schultze U., Bugallo P.-B., Wydler H., Frossard
E. et Fluhler H. (2003). Behavior of a surface applied radionuclide and a dye
tracer in structured and repacked soil monoliths. J Environ Radioactiv, 68(1):
47-64.42
Alismail W et al., (2017). Influence de la densité de
semis sur la production du blé dur dans la zone semi-aride du Haut
Cheliff. Thèse de mastère. Univ de Khemis-Miliana.51p.
Angeles Cid, C. H., Enrique, T. et Julio, A. (1995). Copper
toxicity on the marine microalga Phaeodactylum tricornutum: effects on
photosynthesis and related parameters. Aquatic Toxicology, 31, 165-174.
Bebba S., (2011). Essai de comportement de deux
variétés de blé dur (Triticum durum L.var.Carioca et
Vitron). Conduite sous palmier dattier au niveau de la région de
Ouargla. Mémoire d'Ingénieur d'Etat en Agronomie Saharienne,
Université Kasdi Merbah-Ouargla. 71p.
43
Babich, H. and Stotzky, G. (1980). Environmental factors that
influence the toxicity of heavy metals and gaseous pollutants to
microorganisms, Crit. Rev. Microbiol. 8, 99-145.
Bachir Bey I, Soumatia N., (2015). Contribution à
l'étude de l'effet de la fréquence d'irrigation sur la production
du blé dur sur les sols lourds en zone-aride ; Mémoire de Master
; Université Djilali Bounaama Khemis Miliana, 67p.
Bada Leila., (2007). Variabilité génotypique du
blé dur (Triticumdurum Desf.) vis à vis de la
nuisibilité directe.
Baize D. and Sterckeman T., (2001): Of the necessity of
knowledge of the natural pedogeochemical background content in the evaluation
of the contamination of soils by traces elements. Sci. Tot. Environ. 264:
127-139.43
Baize D. (1997). Teneurs totales en éléments
traces métalliques dans les sols (France). INRA. Paris. 410 p.
Baize D. (2000). Teneurs totales en « métaux
lourds » dans les sols français. Résultats
généraux du programme ASPITET. Le Courrier de l'environnement,
INRA, N° 39. (Disponible sur internet :
http://www.inra.fr).43
Baker, A.J.M. and Walker, P.L. (1989). Ecophysiology of metal
uptake by tolerant plants. In: Heavy metal tolerance in plants - Evolutionary
aspects. Shaw, A. (Eds). CRC Press, 155-177.
Belagrouz A., (2013). Analyse du Comportement du Blé
Tendre, Variété El WIFAK (Triticum aestivum L.) Conduite
en Labour Conventionnel, Travail Minimum et Semis Direct sur Les Hautes Plaines
Sétifiennes. Mémoire Magistère, université Ferhat
Abbas Setif. 88p.
Baldy C., (1974). Contribution à l'étude
fréquentielle des conditions climatiques. Leurs influences sur la
production des principales zones céréalières
d'Algérie. INRA (France)-CCCE (France)-Projet céréales
(Algérie).
Belaid D., (1986). Aspect de la céréaliculture
algérienne, ed- O.P.U, 217
Clerget., (2011). Biodiversité des
céréales et leur utilisation par l'homme. Origine et
évaluation, bulletin 2001 de la société d'histoire
naturelle du pays de Montbéliard.
44
Benchikh C., (2015). Valorisation de la qualité de 3
variétés locales de blé dur (Triticum durum Desf)
cultivées en région semi-aride. Mémoire magistere.
Université EL Hadj Lakhdar- Batna. 149p
Bennai et Benabbas., (2007). L'amélioration des
rendements des céréales par une fertilisation adaptée aux
conditions pédologiques algériennes.
Ban-nai T. et Muramatsu Y. (2002). Transfer factors of
radioactive Cs, Sr, Mn, Co and Zn from Japanese soils to root and leaf of
radish. J Environ Radioactiv, 63(3): 251-264.44
Ben semra N., (1990). Effet de la fertilisation azotée
et de la densité du semis sur le rendement de la variété
de blé dur « Waha » cultivée en zone sub
humide.Thèse. ing. INA.
Benderradji L., (2013). Selection in vitro pour la
tolérance aux stresses salin et thermique chez le blé tendre.
Mémoire doctorat, Université Constantine. 143p.
Bonjean,A (2001); «Histoire de la culture des
céréales et en particulier celle du blé tendre (Triticum
aestivum L)», Eds, Le Perches, Guy P et Fraval A, Agriculture et
biodiversité des plantes, Dossier de l'environnement de l'INRA,
n°21, 29-37. 44
Bourrelier P.H. et Berthelin J. (1998). Contamination des sols
par les éléments traces: les risques et leur gestion. Rapport
n°42. Ed. Technique et documentation. Paris. 438p.44
Bresson C., Ansoborlo E., Malard V., Eyrolle F. and Fievet B.
(2009). Cobalt. In: H.-. Lavoisier (Editor), Toxicologie nucléaire
environnementale et humaine. Edition Tec&Doc, pp. 748.44
Brooks, R. R. (1998). Plants that
Hyperaccumulate Heavy, Metals: Their Role in Phytoremediation, Microbiology,
Archaeology, Mineral Exploration and Phytomining. Oxon: CAB International.44
Brooks S.-C. et Carroll S.-L. (2003). Geochemical reactions
governing the fate of Co-NTA in contact with natural subsurface materials. Appl
Geochem, 18(3): 423-433.44
Chatterjee, J., Chatterjee, C., (2003). Management of
phytotoxicity of cobalt in tomato by chemical measures. Plant Sci. 164,
793-801.44
98108.
45
Colle C., Siclet F. et Saas A. (1983). Principaux facteurs de
transfert sol-plante obtenus en France pour des sols prélevés
à proximité des sites PWR. In: Séminaire sur le transfert
à l'homme des radionucléides libérés dans
l'environnement par les installations nucléaires, Bruxelles, Belgique,
17-21 octobre 1983, 371-387.
Colle C., Grauby A. et Delmas J. (1991). Dépôt
des radionucléides sur le sol et la végétation. In :
Euratom Radiation Protection Programme 1985-1989. EUR 15295 1 : 636-639.45
Colle C., Roussel-Debet S. et Réal J. (1996).
Transferts du radiocobalt en milieu terrestre. Radioprotection, 31(3):
43-354.45
Coughtrey P.-J. et Thorne M.-C. (1983). Cobalt. In:
Radionuclide distribution and transport in terrestrial and aquatic ecosystems:
a critical review of data. Volume II. Rotterdam. AA Balkema, 156-217.45
Davis, J. A., Volesky, B. et Vierra, R. (2000). Sargassum
seaweed as biosorbent for heavy metals, Water Research, 34, 17, 4270-4278.
Djermoun., (2009). La production
céréalière en Algérie : les principales
caractéristiques.
Deltombe E. et Pourbaix M. (1966). Cobalt. In: Pourbaix M.
Atlas of electrochemical equilibria in aqueous solutions. Pergamon Press,
London, 323-329.45
Emir E, EytukTonk F. and Tosun M., 2010. Heterosis for Yield
and its Components
in
Bread Wheat Crosses Among Powdery Mildew Resistant and
Susceptible Genotypes, Pak.
Erroux J., 1960. Introduction au catalogue de blé dur
cultivé en Algérie.35p. étude des caractères de
production et d'adaptation. Mémoire de magistere.
Fefarr M , (2017). Toxicité et bioaccumulation de
pesticides sur quelques variétés de blé dur (T.
durumDesf.). Thèse de doctorat : Département de biologie. Annaba.
373p.45
Feillet P. (2000). Le grain de blé. Composition et
utilisation, INRA éditions 308 p.
Feldman, M. & Sears, E.R. (1981). The wild gene resources of
wheat. Sci.Am. 244:
Hennouni N., (2012). Evaluation du métabolisme
respiratoire et enzymatique des racines de blé dur (Triticum durum
Desf) issues de plantes infectées par les maladies
46
FAO, (2005). New LocClim: Local Climate Estimator. FAO
Environment and Natural Resources Working Paper, N° 2046
Fargasova, A. (2004). Toxicity comparison of some possible
toxic metals (Cd, Cu, Pb, Se, Zn) on young seedlings of Sinapis alba L, Plant,
Soi! and Environment, 50, 1, 33-38.
Fritas S., (2012). Etude bioécologique du complexe des
insectes liés aux cultures
céréalières
Gate P., (1995). Ecophysiologie du blé. Ed. ITCF.
Technique et Documentation. Lavoisier. Paris. P. 419-425.
Gerzabek M.-H., Strebl F. et Temmel B. (1998). Plant uptake of
radionuclides in lysimeter experiments. Environ Pollut, 99(1): 93-103.
Glaus M.-A., Hummel W. et Van Loon L.-R. (2000). Trace
metal-humate interactions. I. Experimental determination of conditional
stability constants. Appl Geochem, 15(7): 953-973.46
Godin, P. M., Feinberg, M.H. & Ducauze, C.J. (1985).
Modelling of soil contamination by
airborne lead and cadmium around several emission sources.
Environ. pollut. 10, 97-114.
Gond, 1986 in Oudjani, (2009). Diversité de 25
génotypes de blé dur (triticum durum Desf.) :
Gopal, R., Dube, B.K., Sinha, P., Chatterjee, C., (2003).
Cobalt toxicity effects on growth and metabolism of tomato. Commun. Soil Sci.
Plant Anal. 34, 619-628.46
Grignac. P, 1978. «Le blé. Monographie
succincte». Annale de l'INR. Paris. 83-98. Gutierrez M. et
Fuentes H.-R. (1991). Competitive adsorption of cesium, cobalt and strontium in
conditioned clayey soil suspensions. J Environ Radioactiv, 13(4): 271-282.46
Hamadache, A. (2013). Eléments de phytotechnie
générale : Grandes Culture- Tom I : Le blé.
1éreédition. Mohamed Amrani. 49-69.
Hamilton, E. I. (1994). The geobiochemistry of cobalt. Sci.
Total Environ. 150, 7- 39. doi: 10.1016/0048-9697(94)90126-046
47
cryptogamiques et de plantes traitées avec un fongicide
(ARTEA EC 330). Mémoire de Doctorat, université Badji Mokhtar
Annaba. 142p.
Laala Z., 2011. Analyse en chemin des relations entre le
rendement en grains et les composantes chez des populations F3 de blé
dur (Triticum durum Desf.) Sous conditions semi-arides. 97p.
Laberche, J.C., 2004. La nutrition de la plante in. Biologie
Végétale. Ed. Dunod. Paris. P. 154-163.
Lange, B., Pourret, O., Meerts, P., Jitaru, P., Cances, B.,
Grison, C., Faucon, M.P., (2016). Copper and cobalt mobility in soil and
accumulation in a metallophyte as influenced by experimental manipulation of
soil chemical factors. Chemosphere 146, 75-8447
Laumont P. & Erroux J., (1961). Inventaire des blés
durs rencontrés et cultivés en Algérie. Mémoires de
la société d'Histoire Naturelle de l'Afrique du Nord.
Imprimerie «La typaLitho» et Ju es. Carbonel, 5-15.
Lexmond T.M., Van Der Vorm P.D.J.. (1981). The effect of pH on
copper toxicity to hydroponically grown maize. Netherlands Journal of
Agricultural Science, v.29, p.217-238.
Li, H., Liu, Y., Qin, H., Lin, X., Tang, D., Wu, Z., et al.
(2020). A rice chloroplast-localized ABC transporter ARG1 modulates cobalt and
nickelhomeostasis and contributes to photosynthetic capacity. New Phytol. 228,
163-178. doi: 10.1111/nph.16708
Lidon FC. and Henriques FS. (1992). Copper toxicity in rice:
Diagnostic criteria and effect on tissue Mn and Fe. Soil Sci. 154, 130-135.
Lombardi, L. et Sebastiani, L. (2005). Copper toxicity in
Prunus cerasifera: growth and antioxidant enzymes responses of in vitro grown
plants, Plant Science, 168, 3, 797-802. 47
Loué, A. (1993). Oligo-éléments en
agriculture. Ed. Nathan (ed), 45-177.
Lwalaba, J.L.W., Zvobgo, G., Fu, L., Zhang, X., Mwamba, T.M.,
Muhammad, N., Mundende, R.P.M., Zhang, G., (2017a). Alleviating effects of
calcium on cobalt toxicity in two barley genotypes differing in cobalt
tolerance. Ecotoxicol. Environ. Saf. 139, 488-495.
48
Lwalaba, J.L.W., Zvobgo, G., Mwamba, M., Ahmed, I.M., Mukobo,
R.P.M., Zhang, G., (2017b). Subcellular distribution and chemical forms of Co2+
in three barley genotypes under different Co2+ levels. Acta Physiol. Plant. 39,
102.48
Kabata-Pendias, A. and Pendias, H. (2001). Trace elements in
soils and plants. CRC Press, London.
Kabata-Pendias A. (2011). Trace Elements in Soils and Plants.
Fourth ed. CRC Press, Boca Raton, Taylor & Francis Group, LLC. 505 p.
Kaplan M. Sonmez S., Sonmez NK. and Kaya H. (2010). Influence of
copper and sulphur applications on the growth and nutrient contents of tomato
plants. Journal of Food, Agriculture & Environment Vol.8 (3&4):
728-732.
Karuppanapandian, T., Kim, W., (2013). Cobalt-induced oxidative
stress causes growth inhibition associated with enhanced lipid peroxidation and
activates antioxidant responses in Indian mustard (Brassica juncea L.) leaves.
Acta Physiol. Plant. 35, 2429-2443.48
Kasongo, L., Mwamba, M., Tshipoya, M., Mukalay, M., Useni, S.,
Mazinga, K., Nyembo, K., (2013). Réponse de la culture de soja (Glycine
max L. (Merril) à l'apport des biomasses vertes de Tithonia diversifolia
(Hemsley) A. Gray comme fumure organique sur un Ferralsol à Lubumbashi,
R.D. Congo. Journal of Applied Biosciences 63, 4727.4848
Kitagishi, K., and Yamane, I. (1981). Heavy Metal Pollution in
Soils of Japan. Tokyo: Japan Science Society Press.48
Khan S.-A., Reman RU et Khan M.-A. (1995). Adsorption of
Cs(I), Sr(II) and Co(II) on Al2 O3. J Radioan Nuc Chem Ar, 190(1): 81-96.48
Krupka K.-M. et Serne R.-J. (2002). Geochemical Factors
Affecting the Behavior of Antimony, Cobalt, Europium, Technetium, and Uranium
in Vadose Sediments. Rapport PNNL 14126, US. Department of Energy, Pacific
Northwest Laboratory, Washington.48
Küpper H., Lombi E., Zhao F. J. & McGrath S. P.,
(2000). Cellular compartmentation of cadmium and zinc in relation to other
elements in the hyperaccumulator Arabidopsis halleri. Planta, 212, 75-84
Pahlsson A.B. (1989). Toxicity of heavy metals (Zn,Cu, Cd, Pb)
to vascular plants: A literature review. Water Air and Soil Pollution, 47,
287-319.
49
Maamri K., (2011). Stabilité du critère de la
discrimination du carbone isotopique en relation avec le poids
spécifique de la feuille drapeau chez quelques variétés de
blé dur cultivées en milieu semi-aride. Mémoire de
magister. Faculté SNV. UFA, Sétif.
Malaisse F. (2018). Anthropisation des paysages Katangais.
Prologue : Le Katanga, une mosaïque d'écosystèmes en
mutation : une approche globale. 23 p49
Masale MJ., (1980). L'élaboration du nombre
d'épi chez le blé d'hiver. Influences de différentes
caractéristiques de la structure du peuplement sur l'utilisation de
l'azote et de la lumière. Thèse doctorat. ING. INA, Paris
Grignon, 274 p.
Mpundu M.M., (2010). Contaminations des sols en
éléments traces métalliques à Lubumbashi (Katanga
RDC). Évaluation des risques de contamination de la chaine alimentaire
et choix des solutions de remédiation. Thèse de doctorat,
Université de Lubumbashi, 401 49
Mukalay, (2016). Identification et classification des sols
sous les nouvelles normes et étude de bio-identification et de
restauration des unités dégradées dans la zone agricole du
Haut-Katanga RD-Congo. UNILU. Lubumbashi 212p49
Mujinya B.B., Adam M., Mees F., Bogaert J., Vranken I., Erens
H., Baert G., Ngongo M., Van Ranst E., (2014). Spatial patterns and morphology
of termite (Macrotermes falciger) mounds in the Upper Katanga, D.R. Congo.
Catena 114, 97-106.49
Nadjem (2011). Contribution à l'étude des effets du
semis direct sur l'efficience d'utilisation de l'eau et le comportement
variétal de la culture de blé en région semi-aride.
Ondo EO., (2014). Caractérisation d'une collection de
variétés anciennes de blé pour leur réponse
à la mycorhization et impact sur la qualité du grain.
Thèse de doctorat.Université de Bourgogne.157p.
Ouanzar S., (2012). Etude comparative de l'effet du semis direct
et du labour conventionnel sur le comportement du blé dur (Triticum
durum Desf.). Mémoire de Magistère, Université Ferhat
Abbas Setif, 70p.
Tagami K. et Uchida S. (1998). Aging effect on bioavailability
of Mn, Co, Zn and Tc in Japanese agricultural soils under waterlogged
conditions. Geoderma, 84(1-3): 3-13.
50
Pham, A. N., Guowei, X., Christopher, J. M. et David, T.
(2013). Waite. Fenton-like copper redox chemistry revisited: Hydrogen peroxide
and superoxide mediation of copper-catalyzed oxidant production. Journal of
Catalysis, 301 , 54-64. 50
Ricroch A., Dattée Y., & Fellous M., (2011).
Biotechnique végétale : environnement, alimentation,
santé. Ed du Vuibert. Paris. 170-182p.
Robert M. and Juste C. (1999). Dynamique des
éléments traces de l'écosystème sol. In
Spéciation des métaux dans le sol, pp. 15-37, Les Cahiers des
Clubs CRIN, (Eds), Paris.50
Sabbarese C., Stellato L., Cotrufo M.-F., D'Onofrio A., Ermice
A., Terrasi F. et Alfieri S. (2002). Transfer of 137Cs and 60Co from irrigation
water to a soil-tomato plant system. J Environ Radioactiv, 61(1): 21-31.50
Salmi M., (2015). Caractérisation morpho-physiologique
et biochimique de quelques générations F2 de blé dur
(Triticum durum Desf.) sous conditions semi-arides. L.Thèse de
magistère. Univ. ferhatabbas-setifufas
Singh, O. V., Labana, S., Pandey, G., Budhiraja, R., and Jain
R. K. (2003). Phytoremediation: an overview of metallic ion decontamination
from soil. Appl. Microbiol. Biotechnol. 61, 405-412.
Smith, S.R., (2009). A critical review of the bioavailability
and impacts of heavy metals in municipal solid waste composts compared to
sewage sludge: review article. Environ. Int. 35, 142-156.
Smith, I. C., and Carson, B. L. (1981). Trace Metals in the
Environment. Ann Arbor, MI: Ann Arbor Science Publishers.50
Sonmez S, Kaplan M, Sonmez NK, Kaya H and Uz I. (2006). High
level of copper application to soil and leaves reduce the growth and yield of
tomato plants. Sci. Agric. (Piracicaba, Braz.), v.63, n.3, p.213-218
Soltner P., (2005). Les bases de la production
végétales: La plante et son amélioration.4èmeEd.
Collection et Techniques Agricoles. 248p.
51
Tsay, C. C., Wang, L. W. et Chen, Y. R. (1995).
Plantresponse to Cu toxicity, Taiwana, 40, 2, 173-181.
Valdeyron L., (1961). Ressources
génétique des blés. Revue scientifique française
p27-38.
Van Den Abeele, 1956. Les principales cultures
du Congo-Belge, 9emeEd. Bruxelles.
Van Engeleen V. W. P. ; Verdoodt, A., Dijkshoorn,
K.&Van Ranst, E., (2006). Soil and Terrain Data Ba e of Central
Africa: D R Congo-Burundi and Rwanda. (SOTERCAF, version 1.0), UGent-FAO
ISRIC.22 p.
Vranken (2010). Pollution et contamination
des sols aux métaux lourds dus à l'industrie métallurgique
à Lubumbashi. Université de Bruxelle.118p51
Wang, Q. R., Cui, Y. S., Liu, X. M., Dong, Y. T.,
Christie, P. (2003). Soil contamination and plant uptake of heavy
metals at polluted sites in China. J. Environ. Sci. Health Part AToxic/Hazard.
Subst. Environ. Eng. 38, 823-838.
Wang Y. et Papenguth H.-W. (2001). Kinetic
modeling of microbially-driven redox chemistry of radionuclides in subsurface
environments: coupling transport, microbial metabolism and geochemistry. J Cont
Hydrol, 47(2-4): 297-309.
Woolhouse HW and Walkers S (1981). The
physiological basis of copper toxicity and copper tolerance in higher plants.
In: Copper in soils and plants (Loneragan JF, Robson AD & Graham RD Eds).
Academic Press, pp. 235-262
Woo-MI Lee., Youn-Joo AN., Hyeon Yoon., and Hee-Seok
Kweon. (2008). Toxicity and bioavailability of copper nanoparticles to
the terrestrial plants mung bean (phaseolus radiatus) and wheat (triticum
aestivum): plant agar test for water-insoluble nanoparticles. Environmental
Toxicology and Chemistry, Vol. 27, No. 9, pp. 1915- 1921.51
1
Annexes
Tableau 4. Base des données pour le traitement
avec le CuSO4 5H2O
|
Traitements
|
T.G à 10jrs (%)
|
T.S à 15 jrs (%)
|
H.P à 20 Jrs (cm)
|
Nbre F à 20 jrs
|
T.S à 40 jrs (%)
|
H.P à 40 Jrs (cm)
|
Nbe de F à 40jrs
|
Longueur racines 40jrs (cm)
|
|
Témoin
|
100
|
100
|
27
|
6
|
100
|
28
|
6
|
10
|
|
Témoin
|
100
|
100
|
25
|
5
|
50
|
26
|
6
|
9
|
|
Témoin
|
100
|
100
|
26
|
5
|
100
|
32
|
6
|
15
|
|
16 ppm de Cu
|
100
|
50
|
6,1
|
3
|
50
|
7
|
3
|
1
|
|
16 ppm de Cu
|
75
|
50
|
5
|
3
|
0
|
0
|
0
|
0
|
|
16 ppm de Cu
|
25
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
33 ppm de Cu
|
50
|
50
|
3
|
2
|
0
|
0
|
0
|
0
|
|
33 ppm de Cu
|
25
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
33 ppm de Cu
|
25
|
50
|
4
|
2
|
0
|
0
|
0
|
0
|
|
66 ppm de Cu
|
25
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
66 ppm de Cu
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
66 ppm de Cu
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
2
Tableau 5. Base des données pour le traitement
avec le CoSO4 7H2O
|
Traitement
|
T.G à 10jrs (%)
|
T.S à 15 jrs (%)
|
H.P à 20 Jrs (cm)
|
Nbre de F à 20 jrs
|
T.S à 40 jrs (%)
|
H.P à 40 Jrs (cm)
|
Nbre de F à 40 jrs
|
L racines 40jrs (cm)
|
|
Témoin
|
100
|
100
|
27,5
|
6
|
50
|
30
|
6
|
10
|
|
Témoin
|
100
|
100
|
26,5
|
5
|
100
|
40
|
7
|
13
|
|
Témoin
|
100
|
100
|
20
|
5
|
100
|
30
|
6
|
12
|
|
16 ppm de Co
|
100
|
50
|
7
|
2
|
0
|
0
|
0
|
0
|
|
16 ppm de Co
|
75
|
50
|
5
|
2
|
50
|
9
|
3
|
4
|
|
16 ppm de Co
|
100
|
100
|
8
|
3
|
50
|
12
|
5
|
4
|
|
33 ppm de Co
|
100
|
50
|
4
|
2
|
0
|
0
|
0
|
0
|
|
33 ppm de Co
|
100
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
33 ppm de Co
|
75
|
50
|
5
|
2
|
0
|
0
|
0
|
0
|
|
66 ppm de Co
|
50
|
0
|
0
|
0
|
0
|
0
|
0
|
0
|
|
66 ppm de Co
|
50
|
50
|
5,5
|
2
|
0
|
0
|
0
|
0
|
|
66 ppm de Co
|
25
|
50
|
3
|
2
|
0
|
0
|
0
|
0
|
| 


