3.2) Résultats dans les classes
expérimentales
3.2.1) Description du cours avec activités
expérimentales
Les activités sont réalisées au
lycée Chaminade dans la seconde C12 et C10. Le test d?identification des
ions fait partie du chapitre de la Réaction Chimique, et l?enseignant a
développé le premier objectif général qui demande
de caractériser les ions en solution aqueuse et le second de
caractériser un ion pour son identification. Les activités se
sont déroulées au cours d?une séance de
deux heures (2) dans les deux classes. L?effectif des élèves dans
chacune des classes est de vingt cinq (25) élèves. Les
différentes photos des expériences réalisées par
les élèves sont présentées à l?annexe.
Le début de la séance a été
précédé par un entretien préalable avec
l?enseignant pour lui préciser nos attentes et lui suggérer une
stratégie. Il faut souligner que dans les deux classes
expérimentales nous avons travaillé avec le même
enseignant. Nous avons ensemble avec l?enseignant monté le protocole
expérimental et les différentes étapes de la leçon.
Dans cet entretien nous avons donné des précisions à
l?enseignant sur les stratégies de la manipulation à savoir :
v' l?évaluation écrite avant l?enseignement ;
v' le contrôle de pré-requis ;
v' la présentation de la situation problème ;
v' la phase des explications ;
v' la présentation des manipulations ;
v' la consolidation des notions ;
v' l?évaluation écrite après
l?enseignement.
L?enseignant a respecté son cheminement habituel :
salutation, contrôle des présences...à l?exception des
éléments ou stratégies précités.
3.2.2) Evaluations diagnostiques
1) Classe 1
Question 1 : qu'est ce qu'un ion ?
Les résultats obtenus montrent que 19
élèves ont donné une réponse exacte à la
question et cinq (5) élèves ont donné des réponses
inexactes que nous présentons dans le tableau XIII.
Tableau XIII : Réponses inexactes de
l?évaluation diagnostique pour la question n°1
|
Réponses inexactes
|
Nombre d'élèves
|
|
Un ion est un anion qui a gagné les électrons
|
2
|
|
Un ion est un cation qui a perdu les électrons
|
3
|
Question 2 : La solution de nitrate d'argent
contient quels types d'ions ?
Les résultats obtenus montrent que 17
élèves ont donné une réponse exacte soit un taux de
68% ; dans le tableau XIV nous avons présenté les
différentes réponses inexactes données par les
élèves. Ici le taux de réponses neutres est de 8%.
Tableau XIV: Différentes réponses inexactes
dans la classe exp.1 pour la question n°2.
|
Réponses inexactes
|
Nombre d'élèves
|
|
La solution de nitrate d?argent contient les ions
Ag2+,2NO4 -
|
5
|
|
La solution de nitrate d?argent contient les ions Ag, NO3
|
1
|
Question 3 : La solution de sulfate de cuivre
contient quels types d'ions ?
Le nombre des élèves donnant une réponse
exactes est de 15, soit un taux de 60% dans cette classe, mais il est de 10
élèves des réponses inexactes, sort un taux de 40% et ces
différentes réponses inexactes sont présentées dans
le tableau XV.
Tableau XV : Réponses inexactes de
l?évaluation diagnostique pour la question n°3.
|
Réponses inexactes
|
Nombre d'élèves
|
|
La solution de sulfate de cuivre contient les ions
Cu3+,3SO4 -
|
6
|
|
La solution de sulfate de cuivre contient les ions
Cu,SO4
|
4
|
Question 4 : L'addition de la solution de
nitrate d'argent (Ag+,NO3-) à une solution
contenant les ions chlorure (Cl-) donne quel précipité
?
Les résultats obtenus montrent que 10
élèves ont donné une réponse exacte soit un taux de
40%. Les différentes réponses inexactes dont le taux est de 48%
sont présentées dans le tableau XVI et le taux de réponses
neutres est de 12%.
Tableau XVI: réponses inexactes, évaluation
diagnostique dans la classe expérimentale 1 pour la question
n°4.
|
Réponses inexactes
|
Nombre d'élèves
|
|
Donne un précipité rose de chlorure d?argent
AgCl
|
7
|
|
Donne un précipité vert de chlorure d?argent
AgCl
|
5
|
Question 5 : L'addition de la solution
d'hydroxyde de sodium Na+, OFF- à une solution
contenant les ions cuivre II Cu2+ donne quel précipité
?
Les résultats obtenus montrent que 10
élèves ont donné une réponse exacte soit un taux de
40%. Les différentes réponses inexactes sont
présentées dans le tableau XVII et ont atteint 36%, ici le taux
de réponses neutres est de 24%.
Tableau XVII : les réponses inexactes de
l?évaluation sommative sur la question n°5.
|
Réponses inexactes
|
Nombre d'élèves
|
|
Donne un précipité vert de d?hydroxyde de cuivre
Cu(OH)2
|
4
|
|
Donne un précipité blanc de d?hydroxyde de cuivre
Cu(OH)2
|
5
|

Synthèse des résultats de
l'évaluation diagnostique dans la classe expérimentale
1
Les résultats généraux de
l?évaluation diagnostique avec les différentes catégories
des réponses, sont traduits par figure 4 suivant.
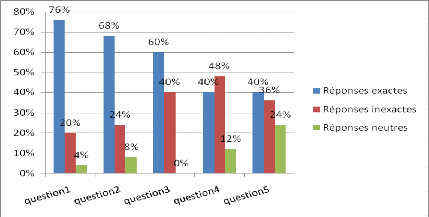
Figure 4 : résultats de l'évaluation
diagnostique dans la classe 1 (la première classe
expérimentale).
NB : les réponses neutres expliquent le
choix de deux réponses par les élèves pour une question ou
bien le non choix à la question.
Les résultats obtenus et traduit par la figure 4,
montrent qu?au niveau de la première question à savoir
la définition d'un ion 19 élèves
ont répondus exactes à la question sur les 25 soit un taux de
76%. Il y a eu juste 5 élèves qui ont donné de
réponses inexactes et 1 neutre.
Au niveau de la deuxième question n°2 et de la
troisième n°3 le nombre d?élèves donnant une
réponse exacte à baisser jusqu?à 60% soit 15
élèves par rapport à la première question n°1.
Par contre, le taux de réponse inexacte s?élève et croit
jusqu?à atteindre 40% soit 10 élèves. A partir de la
question n°4 le taux de réponses inexactes est en hausse et atteint
environ 50% soit 12 élèves. Par contre le taux de réponses
exactes atteint à peine 40% soit 10 élèves. A la question
n°5 nous avons à peu près les mêmes remarques
qu?à la 4ème question, cependant qu?ici les taux de
réponses exactes et inexacte sont moyennement égaux.
Il faut souligner que le taux de réponses neutres, qui
était quasiment inexistant aux questions n°1, 2 et 3, connait une
hausse exponentielle partir de la 4ème question
jusqu?à la 5ème question où il a atteint
environ 25%.
Au regard de cette analyse, le taux de réponses exactes
élevé au niveau de la question n°1 s?explique par le fait
que, les élèves ont des connaissances antérieures sur la
définition d?un ion : la notion ion est enseigné depuis la classe
de la cinquième dans le chapitre intitulé les
éléments chimiques.
A partir des questions n°2 et 3, le taux de
réponses exactes baisse tout simplement parce que les
élèves pour donner la formule d?un ion ont eu des conceptions sur
la notion.
Le taux de réponses inexactes est élevé
à partir de la question n°4 parce que la plupart des
élèves n?ont pas des connaissances y relatives. Cela est aussi
valable pour la question n°5. Nous remarquons ici, pour la justification
de la raison, qu?au niveau des questions n°4 et 5 (couleur du
précipité) la courbe de réponses neutres est en forte
croissance parce que les élèves, une fois de plus, n?ont pas des
connaissances y relatives, et ils n?ont pas voulu se prononcer sur les
questions.
| 


