II-Objectif de la manipulation :
C'est de faire l'extraction des pigments majoritaires de paprika
puis faire une séparation de ces pigments à l'aide d'une
chromatographie sur colonne liquide dans le but de faire l'identification et(
la caractérisation de colorant qu'elle contient ( la capsanthine) cette
caractérisation consiste à déterminer le RF par une
méthode dite chromatographie sur couche mince et de déterminer
également la longueur d'onde d'absorption maximale du colorant cette
dernière étape est réalisée par la méthode
de spectroscopie UV .
III-Mode opératoire : la manipulation se
déroule par 4 étapes :
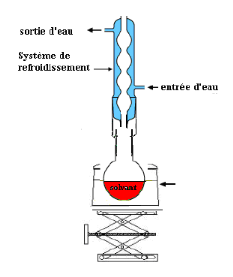
ETAPE 1-EXTRACTION des pigments majoritaires de paprika
On a placé dans un ballon 0,5 grammes de
paprika commercial et 15 mL
de dichlorométhane. On fait un chauffage à reflux
pendant quelques minutes
Selon le protocole suivant
Chauffe ballon
![]() On filtre, la solution obtenue renferme
tous les pigments du paprika qui ont été extraits par le
dichlorométhane. On filtre, la solution obtenue renferme
tous les pigments du paprika qui ont été extraits par le
dichlorométhane.
Concentration de l'extrait par le vapeur
rotatif pour déterminer sa masse obtenue.
ETAPE2-Chromathographie sur micro colone :
séparation des pigments contenues
dans l'extrait Cette étape se passe par 3
procédés
Chromatographie sur couche mince de l'extrait brut (en
mélange)
2-Dépôt de l'échantillon
1- préparation de la micro-
colonne :
3-Alimentation de la colonne en éluant
Ces trois étapes de la Chromathographie sur micro
colonne sont expliquées comme ce qui suit :
· Préparation de la micro- colonne
:
On maintient une pipette pasteur verticalement à l'aide
d'une pince fixée à une potence Dans cette pipette on met ce qui
suit :
Ø Un petit morceau de coton.
Ø 1mm de sable.
Ø On introduit la poudre de silice dans la pipette
à l'aide d'une seringue.
Ø On met une autre souche de sable juste après la
silice.
Remarque important : le remplissage se fait sous vide.
· Dépôt
de l'échantillon
A l'aide d'une pipette pasteur, prélever un peu de
solution à chromatographier et la déposer sur le dessus de la
colonne de silice
· Alimentation la
colonne en élution:
Lorsque le dépôt a bien imprégné la
silice, on verse un peu d'éluant (dichlorométhane) sur la
colonne, très doucement sur la paroi de la pipette. On
Ajoute régulièrement de l'éluant dans la
colonne.
Remarque : le niveau d'éluant dans
la pipette doit rester au dessus de celui de la silice jusqu'à la fin du
développement.
· Récupération des
fractions :
On laisse couler l'éluant et on récupère des
fractions (12 fractions) dans des tubes à essai on change le tube
chaque 5 min.
L'ensemble des étapes est présenté
sur la figure 1.
Pince
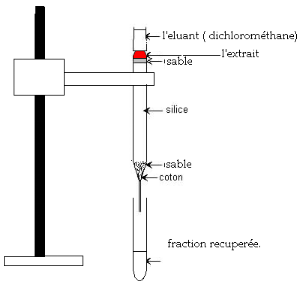
Figure 1 :Chromathographie sur micro colone :
séparation des pigments
Dessin d'une colonne de chromatographie
liquide
Figure 2 : Dessin d'une colonne de chromatographie
liquide
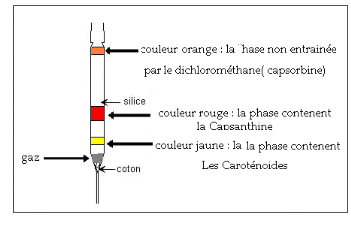
ETAPE 3- CHROMATOGRAPHIE SUR COUCHE MINCE
(détermination du RF)
On fait un dépôt de chaque fractions
récupérées (séparées par la chromatographie
liquide sur colonne) sur une plaque de chromatographie tout en marquant
l'endroit ou on a met ce dépôt à l'aide d'un trait, on met
les plaques dans les cuves qui contiennent le solvant)
Apres un temps on voit qu'il y migration sur la plaque, on
arrête la chromatographie une fois le solvant arrive au front de la
plaque.
On fait la révélation des taches puis en calcule
les RF de ces taches.
ETAPE 4- SPECTROSCOPIE (détermination de la
longueur d'onde maximale. On cherchera à étudier
l'absorbance du l'extrait brut et les différentes fractions
séparées pour des longueurs d'ondes (entre 350 nm et 470
nm).
Protocole expérimental :
- On Dilue les différents colorants à
étudier avec le Méthanol
- Verser les solutions diluées dans différentes
cuves.
- Avant de mesurer l'absorbance des solutions, pour chaque
longueur d'onde, faire le `blanc'
-On Relève l'absorbance environ tous 10 nanomètres
entre 350 nm et 470 nm et on trace les courbes.
Résultats :
1- Calcule de rendement l'extraction des
pigments:
· Echantillon peser au départ : 0,5 g de la
poudre du colorant pour séparer les pigments.
· La masse du Ballon vide pour l'extraction
=59,18g.
· La masse du Ballon après concentration
=59,37g.
La masse se calcule comme ce qui suit :
59,37-59,18=0,19g
Donc 0,19g est la quantité extraite.
Le rendement de cette extraction est le
suivant :
(m ex / m ech) x 100 = (0,19/0,5)
x100=38%
m ex : La masse de l'extrait en
(g) .
m ech: la masse de
l'échantillon du départ en (g).
2- Migration par CCM : Calcule du RF
On a fait une CCM pour l'échantillon complet
c'est-à-dire avant la séparation des pigments, de la même
manière on a fait La CCM également pour les différentes
fractions récupérées les résultas obtenues sont les
suivantes :
2-A- CCM pour l'extrait de départ
Apres migration par CCM, l'observation du
papier a montré qu'on a trois taches différentes voir figure
3 :
· la première tache orange (au bas de la plaque)
: RF = (0 ,9/3,6) =0,25.
· La deuxième tache rouge intense :
RF= (2,6/3,6) =0,72.
· La troisième tache jaune (en haut
de la plaque) : RF= (3,1/3,6) =0,86.
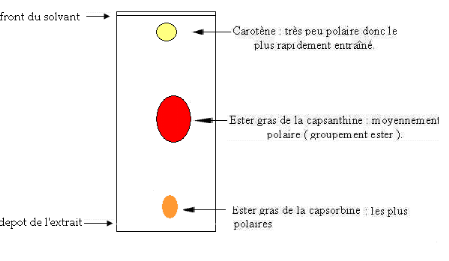
Figure 3 : dessin d'une plaque de CCM
2-B-CCM pour les fractions
récupérées :
On a eu trois types de fractions qui sont
présentées sur le tableau suivant :
|
Fraction
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
12
|
|
Couleur
|
B
|
J
|
J
|
R
|
R
|
R
|
Org
|
Org
|
Org
|
Org
|
J
|
J
|
B : blanc : cette
fraction ne contient aucun colorant
J : jaune
R : rouge
Org : orange
Calcule des RF ces fractions
· La fraction jaune :
RF = (3,2/3,6) =0,89
· La fraction rouge :
RF= (2,7/3,6)=0,75
· La fraction orange :
RF = (1/3,5)=0,28
Interprétation et observation
On observe bien que l'ordre de sortie de la colonne est le
même que l'ordre de migration sur la plaque de CCM :
Le colorant
jaune (fraction jaune) migrant le plus haut sur la plaque on le trouve
essentiellement dans la fraction 2 et 3, cette phase
contient les caroténoïdes, peu polaire et
qui sont les plus rapidement
entraînées.
Le colorant donnant la tache rouge
intense (fraction rouge qui contient la capsanthine se trouve
surtout dans les fractions 4 et 5.
A partir de la
fraction 6, le colorant rouge disparaît progressivement, les
autres fractions donnant un groupe de taches en bas sur la plaque, ces taches
présentent les ester gras de la capsorine et qui sont très
polaires.
3- Détermination de la longueur d'onde optimale
par SPECTROSCOPIE
Résultas du balayage à la spectroscopie
ultra visible pour :
Ø L'extrait du départ
Cette opération est utilisée pour déterminer
l'onde maximale d'absorption pour le résidu extrait : on fait varier la
longueur d'onde à partir du 350 jusqu'à 470 nm
et chaque fois on fait la mesure de l'absorbance les résultas sont
présentées sur le tableau suivant :
|
ë(nm)
|
350
|
360
|
370
|
380
|
390
|
400
|
410
|
420
|
430
|
440
|
450
|
460
|
470
|
|
A
|
0,70
|
0,647
|
0,615
|
0,598
|
0,634
|
0,72
|
0,783
|
0,876
|
0,929
|
0,973
|
0,900
|
0,892
|
0,880
|
Voici la courbe la longueur d'onde en fonction de
l'absorbance
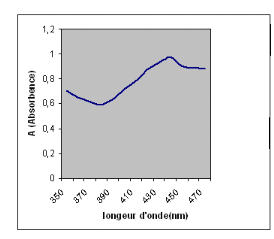 Figure 2 : longueur d'onde en fonction de
l'absorbance pour l'extrait (mélange) Figure 2 : longueur d'onde en fonction de
l'absorbance pour l'extrait (mélange)
Ø Pour les fractions séparées :
-la fraction jaune :
|
ë(nm)
|
350
|
360
|
370
|
380
|
390
|
400
|
410
|
420
|
430
|
440
|
450
|
460
|
470
|
|
A
|
0,11
|
0,113
|
0,145
|
0,127
|
0,16
|
0,21
|
0,23
|
0,29
|
0,308
|
0,367
|
0,400
|
0,370
|
0,377
|
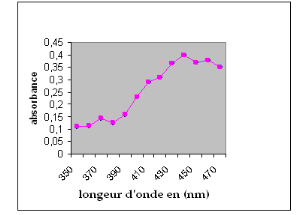
Figure 3 : longueur d'onde en fonction de
l'absorbance pour la fraction jaune
-fraction rouge :
|
ë(nm)
|
350
|
360
|
370
|
380
|
390
|
400
|
410
|
420
|
430
|
440
|
450
|
460
|
470
|
|
A
|
0,7
|
0,77
|
0,832
|
0,912
|
1,090
|
1,340
|
1,690
|
1,90
|
2,12
|
2,50
|
2,16
|
2,17
|
2,24
|
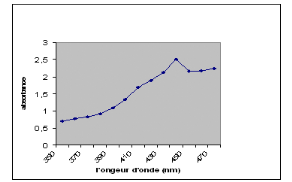
Figure4 : longueur d'onde en fonction de
l'absorbance pour la fraction rouge
-fraction orange :
|
ë(nm)
|
350
|
360
|
370
|
380
|
390
|
400
|
410
|
420
|
430
|
440
|
450
|
460
|
470
|
|
A
|
0,75
|
0,75
|
0,862
|
0,962
|
1,02
|
1,14
|
1,309
|
1,41
|
1,512
|
1,81
|
1,619
|
1,62
|
1,6
|
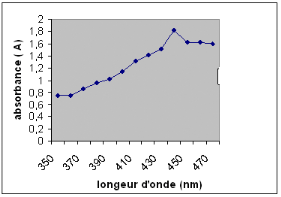
Figure5 : longueur d'onde en fonction de
l'absorbance pour la fraction orange
Interprétation des
résultas :
Ø L'extrait
D'après les résultas de balayage on a
trouvé que la longueur d'onde optimal pour l'extrait avant la
séparation par chromatographie liquide sur colonne est égale
à ë = 440nm.
Ø La fraction jaune : ë =
450nm.
Ø La fraction rouge : ë = 440nm.
Ø La fraction orange : ë =
440nm
Calcul du RF pour le colorant : on sait
bien Le colorant capsanthine donnant la tache
rouge intense se trouve dans fraction rouge son RF est déjà
calculé :
RF = 0,75 dans la fraction rouge alors au
départ on a trouvé un RF = 0,72 dans le
mélange (l'extrait avant la séparation des colorants)
d'après ces résultas on peut dire que la tache rouge s'agit de
la capsanthine et son RF est le suivant
RF=0,75
I- Caractérisation du colorant
D'après les résultas obtenu le long de la
manipulation on a eu les caractéristiques suivantes :
Ø En réalisant la chromatographie liquide sur
colonne on trouvé que La capsanthine se trouve dans la
fraction rouge qui englobe les pigments majoritaires du paprika et qui sont
responsable de la couleur rouge.
Ø D'après les résultas du balayage par
spectroscopie la longueur d'absorbance maximal
ë = 440nm.
Ø D'après les résultas de la chromatographie
sur couche mince (CCM) la capsanthine est moyennement
polaire son RF = 0,75

| 


