III- PROCEDES DE POLYMERISATION ET DE MISE EN FORME
Plusieurs substances interviennent dans une réaction de
polymérisation : les amorceurs, les précurseurs, les solvants,
les catalyseurs. Ils ont une influence sur les procédés de
polymérisation.
III 1 Amorceur de polymérisation
Un amorceur de polymérisation est une substance qui
possède au moins une liaison chimique labile, c'est-à-dire qui se
rompt facilement, capable de générer soit des radicaux libres par
rupture homolytique, soit des espèces ioniques très
réactives.
Les moyens physiques d'amorçage de
polymérisation cationique sont des radiations ionisantes tels les rayons
á, la photolyse,...
Certains monomères ne sont polymérisés
que par un seul type d'amorceur. Ainsi l'isobutadiène ne se
polymérise qu'en présence d'amorceurs cationiques, tandis que le
cyanure de vinylidène (CH2=C (CN)2) demande un amorceur anionique. Par
contre un certain nombre de monomère comme le styrène ou le
buta-1,3-diène polymérisent avec des amorceurs cationiques ou
avec des amorceurs anioniques. Mais il n'existe actuellement aucun
procédé industriel de polymérisation de
l'éthylène et du propylène utilisant un amorceur ioniques.
Ces monomères, de grande importance économique sont très
peu réactifs. Ils sont en partie (éthylène) ou en
totalité (propylène) polymérisés par des
catalyseurs basés sur les métaux de transition [3-4].
III 2 - Polymérisation ionique.
Elle s'effectue par l'intermédiaire d'espèces
réactives ioniques (carbocations et carbanions). C'est une
réaction d'addition en chaîne qui suit les trois étapes
suivantes : l'amorçage, la propagation, la terminaison et / ou le
transfert. Les monomères porteurs de substituants hydroxyles qui
réagissent avec l'amorceur pour former des produits inactifs ne
polymérisent pas par voie ionique [3-4].
III 2-1 - Polymérisation cationique.
Le centre actif est porteur d'une charge positive et est en
général associé à un contre ion négatif ou
bien constitué d'une liaison fortement polarisée. Les
composés tels que le BF3, le Ticl4, HClO4 sont des amorceurs de ces
réactions.
Les centres actifs sont des acides de Lewis. Cette
polymérisation peut être considérée comme une
réaction acide-base, le monomère étant la base de
Lewis.
Les principaux types de centres actifs sont :
-les ions carbénium C +
22
Mémoire présenté et soutenu par Jacques
Nkongo Dim
Les polymères dans l'industrie
+
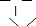
-les ions oxonium O
+
-les ions aziridium N
Ou bien les esters polarisés correspondants.
Si nous envisageons la réaction de
polymérisation de l'isobutène en présence de trifluorure
de bore, le mécanisme est [12] :
Amorçage
BF3 + H2 0 H+ + + BF3 OH -
CH3 CH3
H+ + BF3 0H- + CH2 = C CH3 - C + + BF3 OH
CH3 CH3
Propagation
|
CH3 CH3
|
CH3 CH3
|
|
|
|
CH3 - C + + n CH2 = C H- CH2 - CH2 - C
|
CH2 - C +
|
|
|
CH3 CH3 CH3 CH3
n
Terminaison- Transfert
CH3
CH3
CH3 CH3
CH2 - CH2 - C - CH2 - C + H
CH2- CH2-C
CH=C + H+
H
CH3 CH3 CH3
En réalité la deuxième étape de
cette polymérisation a un mécanisme plus complexe. Les
réactions de terminaison ou de transfert sont concurrentielles.
D'une façon générale la
polymérisation cationique n'est pas
stéréospécifique. Lorsque les substituants du centre actif
sont encombrants comme dans le cas de l'?-méthylstyrène, cette
réaction donne lieu à une configuration
préférentiellement syndiotactique .
23
Mémoire présenté et soutenu par Jacques
Nkongo Dim
Les polymères dans l'industrie
Illustration
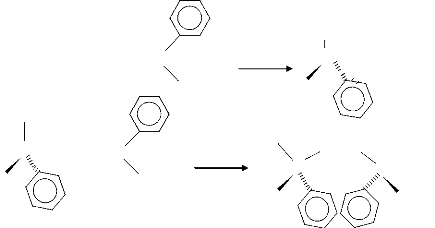
CH3
H+ + BF3OH- + CH2 = C C+ + BF3OH
CH3 CH3
CH3
CH3
CH3
C+ + CH2 = C
CH3
CH3
CH3 CH2
C C+
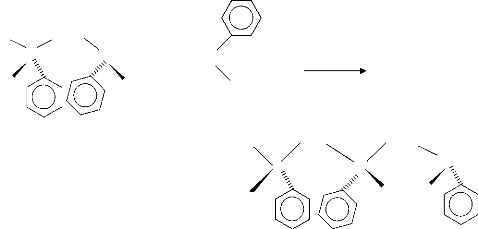
CH3
CH2
CH2
C+
C C
CH3
CH3
CH3
CH3 CH2
C C + + CH2 = C
CH3 CH3
CH3
Le caractère atactique est obtenu dans le cas de la
polymérisation des hétérocycles.
Ces réactions se produisent en général
dans des solvants polaires qui influencent la dissociation des paires d'ions,
mais aussi dans la réaction de transfert.
| 


