Soit une réaction de premier ordre :
A B
Si 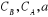 et et 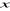 sont
respectivement ; la formalité de B, la formalité de A, la
concentration actuelle de a et la concentration actuelle de b : sont
respectivement ; la formalité de B, la formalité de A, la
concentration actuelle de a et la concentration actuelle de b :
Au temps t=0 : 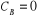 et et 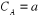 (1)
(1)
Et au temps t>0 : 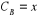 et et 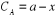 (2)
(2)
La vitesse de formation de B
est : 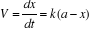 (3)
(3)
En intégrant cette vitesse,
on obtient : 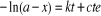 (4)
(4)
Aux les conditions initiales, x=0
pour t=0, on obtient : 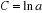 (5) (5)
On obtient enfin pour la loi de
vitesse de réaction de premier ordre :
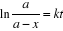 (6)
(6)
k est la constante de vitesse.
L'équation (6) peut
s'écrire aussi : 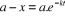 ou ou 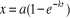 (7) (7)
Ou encore 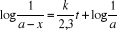
Les équations écrites en (6) donnent l'allure
des courbes de formation de B et de disparition de A.
CHAPITRE II. L'ACIDE CYANHYDRIQUE
ET LA TOXICITE DU MANIOC
II.1. L'acide cyanhydrique et la
toxicité du manioc
Cet acide ne se trouve pas à l'état libre dans
les tissus végétaux, mais sous forme de composés chimiques
qui peuvent être des glycosides cyanogénétiques ou des
cyanolipides.
Les glycosides cyanogénétiques sont des â-
glycosides constitués d'un sucre non hydrolysable et d'un
aglycone : linamarine et lotaustraline ( ou
méthyllinamarine).(Monique L, et. Al ; 1992)
Le principe toxique essentiel qui existe en quantités
variables dans toutes les parties de la plante de manioc est un composé
chimique appelé linamarine. Il coexiste souvent avec son homologue
méthylique appelé méthyllinamarine ou lotaustraline.
Figure 1: Structure des glucosides
cyanogénétiques de manioc (15)
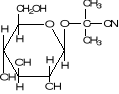 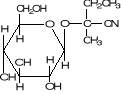
LINAMARINE
LOTAUSTRALINE
Identiques sur le plan de la qualité, ces glucosides
sont présents dans le manioc dans le rapport 93% à 97% pour la
linamaroside contre 7 à 3% de la lotaustraloside (6)
Leur biosynthèse semble impliquer l'acide aminé
L-valine pour la linamaroside et l'acide aminé L-isoleucine pour la
lotaustraloside comme précurseurs, selon le schéma proposé
par Conn et Butler, mentionnés par Rukiya (1988).
Figure 2: Etapes de la
biosynthèse d'un glucoside cyanogénétique (11)
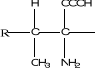
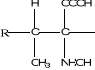
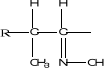
Amino acide
N-Hydroxylaminoacide Aldoxime
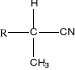
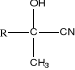
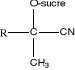
Nitrile á -
Hydroxynitrile glucoside
cyanogénétique
La linamarine est un glucoside cyanogénétique
qui est transformé en acide cyanhydrique toxique ou acide prussique
lorsqu'il entre en contact avec la linamarase, une enzyme qui est
libérée quand les cellules des racines de manioc se rompent a
linamarase est une enzyme endogène qui a son optimum d'activité
à pH 5,5 - 6. Elle est détruite à72°C. c'est une
ß- glucosidase (Bourdoux et al ; 1980)
Figure 3: Dégradation
enzymatique de la linamarine (4)
+
Linamarase
+ H2O
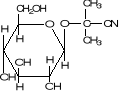
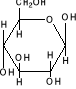 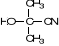
Linamarine
Glucose
Cyanohydrine
Oxynitrilase
+ HCN
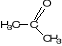
Acetone
acide cyanhydrique
La linamarine est par ailleurs un composé assez stable
qui n'est pas modifié durant la cuisson du manioc. Si elle passe de
l'intestin dans le sang comme glucoside intact, elle est probablement
excrétée inchangée dans l'urine sans dommage pour
l'organisme (Philbrick, et al. 1977).
Cependant la linamarine ingérée peut
libérer du cyanure dans l'intestin durant la digestion.
L'acide cyanhydrique (HCN) est un composé volatil. Il
s'évapore rapidement dans l'air à des températures
supérieures à 28°C et se dissout facilement dans l'eau. Il
peut aisément être perdu durant le transport, l'entreposage et
l'analyse des échantillons. La teneur normale en cyanogène des
tubercules de manioc se situe normalement entre 15 et 400 mg de HCN/kg de poids
frais (7).
La concentration varie largement entre les
variétés de même qu'avec les conditions écologiques
et culturelles. La concentration des glucosides cyanogénétiques
augmente du centre vers la périphérie du tubercule (Bruijn,
1973). Généralement, la teneur en cyanure est beaucoup plus
élevée dans la peau (écorce) du manioc.
Les méthodes traditionnelles de transformation et de
cuisson du manioc. Si elles sont appliquées avec soin, peuvent
réduire la teneur en cyanure jusqu'à des niveaux non toxiques.
Une méthode de transformation efficace libérera
la linamarase en désintégrant la microstructure de la racine de
manioc. En amenant cette enzyme en contact avec la linamarine, le glucoside est
transformé en acide hydrocyanique. Le cyanure libéré se
dissout dans l'eau quand la fermentation est provoquée par un trempage
prolongé et s'évapore quand le manioc fermenté est
séché.
Le séchage au soleil de petits morceaux de manioc frais
pendant une courte durée n'est pas un bon procédé de
détoxication. Le cyanure ne sera pas complètement
libéré et l'enzyme sera détruite pendant le
séchage.
Les techniques de transformation par séchage au soleil
ne réduisent que de 60% à 70% la teneur totale en cyanure durant
les deux premiers mois de conservation. Les résidus de cyanure peuvent
être très importants dans les tubercules secs, de 30 à 100
mg/kg (Casadei, 1988). La simple cuisson à l'eau de morceaux de racine
fraîche n'est pas toujours une garantie de non-toxicité car le
cyanure ne pourrait être que partiellement libéré, et une
fraction seulement de la linamarine passerait dans l'eau de cuisson.
La réduction des cyanures varie si le produit est mis
dans l'eau froide (27°C) ou directement dans l'eau bouillante
(100°C).
Après 30 minutes de cuisson, les cyanures ne sont plus,
dans le premier cas, que 8% de leur valeur initiale, et dans le seconde cas
environ 30% (Essers, 1986).
Plusieurs auteurs ont suggéré différents
niveaux minimaux pour la toxicité. Rosling (1987) a exprimé
l'opinion qu'une dose de plus de 20 mg pour 100 g de manioc est toxique, tandis
que Bolhis (1954) a établi la dose toxique de 50 à 60 mg par
jour pour un adulte Européen.
| 


