3.2. TAILLE DU CONFINEMENT
Le choix de la taille du confinement est d'une très
grande importance, et la gamme de pores que nous allons choisir doit être
déterminée en relation avec les échelles existantes dans
le monde du vivant. L'idée n'est pas de reproduire à l'identique
une membrane, qui serait beaucoup trop complexe voire impossible à
étudier par QENS, mais plutôt d'extraire dans un premier temps les
dimensions caractéristiques afin de réaliser un modèle
simple qui « imiterait » une membrane.
Une membrane cellulaire se compose d'une bicouche de
phospholipides dans laquelle des protéines membranaires, dites
protéines de transport spécifiques, permettent le transport des
ions ou des molécules à travers les couches lipidiques. En
moyenne, l'épaisseur d'une membrane cellulaire classique mesure environ
5 à 10 nm. (Figure 25)
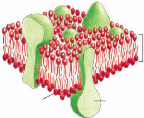
-- 5-10nm membrane
protéine
lipide
Figure 25 : Représentation schématique d'une
membrane cellulaire.
Afin d'élargir le choix dans les matrices de
confinement, nous chercherons à obtenir des diamètres de
pores
compris entre 2 et 20nm, des tailles qui sont du même ordre de grandeur
que l'espace
intermembranaire. Parmi les différents types de silices
poreuses, nous nous sommes dirigés vers des gels de silice aqueux
(hydrogels), et une silice mésoporeuse de type MCM-41, que nous avons
adapté à cette étude. Ces deux silices sont
complémentaires : la première présente des pores
interconnectés, non-organisés avec un diamètre de pore
moyen ; la deuxième, quant à elle, est composée de pores
calibrés et organisés. Ainsi, ces deux types de silice nous
permettront de juger de l'impact de la forme des pores sur la dynamique. Les
synthèses des hydrogels et des MCM-41 sont assez différentes,
d'autant que la synthèse de la silice mésoporeuse a
été spécialement développée pour
répondre à nos contraintes. De ce fait, nous allons
développer la synthèse des hydrogels dans la suite de ce chapitre
alors que celle des MCM-41 sera traitée dans le chapitre 6.
3.3. SYNTHESE DE GELS DE SILICE AQUEUX (HYDROGELS)
Les gels de silice aqueux ont été
synthétisés à l'aide du procédé «
sol-gel », qui permet par simple polymérisation de
précurseurs moléculaire en solution, d'obtenir des
matériaux vitreux sans passer par l'étape de fusion. Très
utilisé dans la fabrication des verres, des films et des fibres, il
permet également de synthétiser des particules de taille et de
forme contrôlées.101,102,103,104,105,106,107,108
3.3.1. Principes généraux
La méthode « sol-gel » a pour principe la
gélification d'un sol, qui est une dispersion stable de particules
solides dans un liquide. Le gel, qui en résulte, est moins
évident à définir puisqu'il s'agit d'un état
intermédiaire de la matière situé entre l'état
solide et l'état liquide. Un gel peut être vu comme un
réseau tridimensionnel solide qui s'est expansé au travers d'un
liquide.
La synthèse par voie « sol-gel » se fait
généralement à partir de précurseurs alcoxydes (ou
alcoolates) de formule brute M(OR)m où M est un atome
métalique et R un groupement alkyl CnH2n+1. (Nous nous limiterons ici au
cas du silicium, c-à-d M = Si). Les réactions chimiques à
la base du procédé se déclenchent lorsque les
précurseurs sont mis en présence d'eau : l'hydrolyse des
groupements alkoxy intervient alors, suivie par la condensation des produits
hydrolysés qui conduit au phénomène de
gélification.
- L'hydrolyse est une réaction de substitution
nucléophile, qui peut se répéter sur tous les groupements
-OR de l'alcoolate. Elle conduit à la formation de l'acide silicique
(Si-(OH)4) et libère des molécules d'alcool (ROH) (Eq. 19). Son
mécanisme, qui présente une vitesse minimale à pH ~ 7, est
activé par catalyse acide ou basique :
Si-(OR)4 +
4H2O?-*
Si-(OH)4 + 4ROH
(Eq. 19)
- La condensation est également une réaction de
substitution nucléophile. Elle se traduit soit par une expulsion d'eau
par réaction entre deux groupements silanols (Eq. 20), soit par le
départ d'alcool par réaction entre un groupe silanol et un groupe
alkoxy (Eq. 21). Cette étape de condensation conduit à la
formation de ponts siloxanes (-Si-O-Si-) qui constituent l'unité de base
du polymère inorganique.
HO -Si-O-H H-O-Si- OH ? HO -Si-O-Si- OH H O (Eq. 20)
3 3 3 3 2
Si- OR +2H O ? SiO +4ROH (Eq. 21)
4 2 2
La chimie des alcoolates du silicium conduit à des gels
polymériques ou colloïdaux selon que les conditions de pH soient
en-dessous ou au-dessus du point isoélectrique (pH ~ 2,5)*
et/ou la proportion d'eau utilisée pendant la réaction.
Gels polymériques:
Dans des conditions de catalyse acide (pH < 2,5) et
pour de petites quantités d'eau (H2O:Si < 5), la cinétique
d'hydrolyse est prépondérante devant celle de la condensation, et
les effets stériques confèrent à cette attaque une
difficulté croissante quand l'oxygène appartient successivement
à un monomère, une extrémité de chaîne ou un
milieu de chaîne. De ce fait, la condensation se fera
préférentiellement en bout de chaîne. Il y a alors
apparition de polymères linéaires ou faiblement ramifiés
(Figure 26(a)), qui s'enchevêtrent (b), et forment de nouvelles
ramifications donnant lieu au phénomène de gélification
(c).
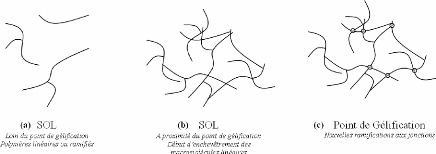
Figure 26: Croissance du polymère et formation d'un gel
dans les systèmes à catalyse acide, en fonction de l'avancement
de la réaction.103
* Le point isoélectrique est également
appelé point de charge nulle, et correspond à une charge
électrostatique nulle à la surface de la particule.
Gels colloïdaux :
Dans des conditions de catalyse basique (pH > 2,5)
et/ou en présence d'une grande quantité d'eau, les
réactions d'hydrolyse et de condensation se produisent
simultanément. La rapidité de la réaction conduit à
la formation d'agrégats très fortement ramifiés qui ne
peuvent s'interpénétrer et vont donc exister en tant
qu'entités discrètes (Figure 27(a)). Cependant, les clusters vont
se lier les uns aux autres pour former un gel colloïdal. Les
agrégats, en se liant les uns aux autres (b), vont former un
réseau tridimensionnel de particules enchevêtrées à
l'origine de la gélification (c).
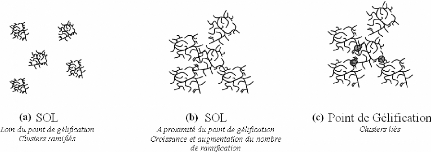
Figure 27 : Croissance du polymère et formation d'un gel
dans les systèmes à catalyse basique en fonction de
l'avancement de la réaction.103
| 


