3.3.2. Synthèse des hydrogels en présence de
monosaccharides
Les gels aqueux de silice contenant des solutions de D-glucose
ont donc été synthétisés à l'aide de ce
procédé « sol-gel ». La synthèse, en
collaboration avec Dr A. Douy du CRMHT, s'est fortement inspirée d'un
protocole expérimental décrit dans la
littérature.109 Cette synthèse110
nécessite les réactifs suivants : du D-glucose (C6H12O6), du
tetraéthoxysilane (Si-(OC2H5)4 (TEOS), = 98%), de l'urée
(CO(NH2)2, = 99%) de l'acide nitrique (HNO3, 67%) et de l'eau lourde
(D2O)*.
Pour cette nouvelle étude, nous nous sommes
limité à l'étude de la dynamique moléculaire du D-
glucose, et comme dans le cas des solutions volumiques, nous avons
utilisé du D2O et du D-glucose partiellement deutéré
(C6D5H7O6). Pour ce faire, le sucre (10 g) a été dissout en
boîte à gants (He) avec 30 mL d'eau lourde.** La
solution obtenue est agitée pendant quelques heures, avant d'être
placée dans une étuve à vide à 30°C pour
évaporer le solvant. Après complet séchage, le D-glucose
partiellement deutéré (C6D5H7O6) se présente
sous forme d'une poudre blanche prête à l'emploi.
* Tous ces produits chimiques proviennent de chez Sigma Aldrich,
exceptée l'eau lourde qui provient de chez Cambridge Isotope
Laboratory.
** Si l'on calcule le nombre d'atomes de deutérium par
molécule de D-glucose, nous trouvons 60:1, correspondant
à 60 D pour 5 H (en ne considérant que les hydrogènes
échangeables).
Le protocole expérimental pour la synthèse des
gels est le suivant. Dans un premier temps, le TEOS (1,5 g) est ajouté,
en boîte à gants, à une solution de D2O (20 mL)
acidifiée à l'acide nitrique (2- 3 gouttes). Puis, lorsque
l'hydrolyse du TEOS est terminée, c'est-à-dire lorsque la
solution est redevenue translucide, l'urée (0,1 g) et une
quantité donnée de D-glucose C6D5H7O6 (x g) sont ajoutées
à la solution. Après agitation, le sol est placé dans un
porte échantillon scellé à l'indium, puis vieilli entre 15
et 20 heures à 70-80 °C. La thermolyse de l'urée va
générer de l'ammoniac de manière homogène, qui, par
un processus catalytique et en augmentant le pH du sol, va faire polycondenser
l'acide silicique. Avec l'avancement de la réaction de polycondensation,
un réseau tridimensionnel de ponts siloxanes va s'étendre dans
tout le volume de la solution pour finalement former un gel. La solution de
sucre se retrouve alors confinée dans un squelette siliceux. (Figure
28)
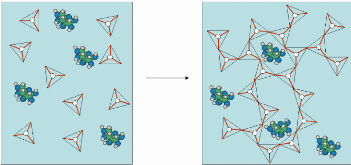
Figure 28 : Schéma représentatif de l'expansion du
réseau tridimensionnel siliceux dans tout le volume de la solution de
D-glucose.
Nous avons préparé des gels présentant
des fractions molaires glucose:eau = 0, 1:55 et 1:20. Il s'agit des ratios que
nous avons utilisés dans l'étude des solutions volumiques de
D-glucose (Cf. Chapitre 2). Elles correspondent à des concentrations
massiques de:
- 0, 13,4 et 30 wt.% dans des solutions intégralement
hydrogénées*,
**
- 0, 14,2 et 31,6 wt.% si l'on ne prend en compte que l'eau et le
sucre.
Le récapitulatif des échantillons est
présenté dans le tableau 20, dans lequel les ratios glucose:eau
sont donnés entre parenthèses.


*Lespourcentages massiques en sucre ont
été calculés de la manière suivante: wt.%msucre
mtotal ** Dans ce cas, wt.%msucre msucremeau
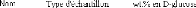

Tableau 20 : Tableau récapitulatif des gels de silice
synthétisés.
Le gel obtenu maintient parfaitement le liquide en son sein
(Figure 29), mais une fois sa surface brisée, le gel ne présente
plus aucune rigidité macroscopique et des écoulements de solution
apparaissent. C'est pour cette raison qu'il est absolument nécessaire de
synthétiser ces gels directement dans les porte-échantillons.

Figure 29 : Photographie d'un gel de silice aqueux.
| 


