3.3.3. Caractérisation Raman
Comme nous venons de le voir, le protocole expérimental
nécessite une montée en température de la solution pour
activer la thermolyse de l'urée. Ce chauffage, bien que
modéré (~ 80 °C), pourrait dégrader le
monosaccharide. Afin de s'assurer de l'intégrité des
molécules de D-glucose après gélification, des mesures de
spectrométrie Raman ont été réalisées en
collaboration avec Dr A. Desmedt du LPCM (Université Bordeaux 1).
La spectroscopie Raman permet de sonder les transitions
vibrationnelles, qui sont caractéristiques d'une molécule dans un
environnement donné. Les mesures en Raman confocal ont été
réalisées sur un spectromètre Labram II (Jobin-Yvon), dont
la source excitatrice est un laser Ar/Kr opérant à 514,5 nm et
avec une résolution spectrale de 6 cm-1. Un microscope
équipé d'un objectif 50× avec une ouverture numérique
de 0,75 et un trou confocal de 700 um ont été utilisés
pour faire converger le faisceau sur l'échantillon. Un filtre Notch a
également été utilisé pour filtrer la diffusion
Rayleigh. Les gels A1, A2 et A3, et une solution de D-glucose à 14 wt.%
ont été mesurés entre 100 et 4200 cm-1 à
la température ambiante. Les spectres sont présentés dans
la figure 30.
12
10
Solution 14 wt.%
8
6
4
2
A3
A2
Al
0
500 1000 1500 2000 2500 3000 3500 4000
Déplacement Raman (cm~1)
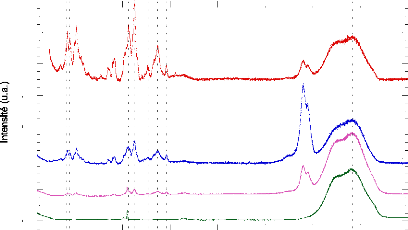
Figure 30: Spectres Raman pour les gels A1, A2 et A3, et pour une
solution de D-glucose à 14 wt. %. Les lignes en pointillés
marquent la position des pics Raman du D-glucose.
Les gels A2 et A3 présentent un nombre important de
pics dans la région spectrale comprise entre 250 et 1500
cm-1. Ces raies, que l'on observe très clairement dans la
solution, correspondent aux différents types de vibrations existantes
dans la molécule de D-glucose. Les attributions des différentes
raies sont listées dans le tableau 21. La coïncidence des raies,
sans décalage en fréquence, témoigne de la présence
du monosaccharide dans son intégrité structurale. Notons
également que l'on retrouve des pics de déformation pour les deux
variétés allotropiquesetdu D-glucose, ce qui confirme qu'il n'y a
pas eu de discrimination d'une variété par rapport à
l'autre durant la synthèse.
Un autre point est également à noter:
l'évolution de la bande des -OH entre 2700 et 3800 cm-1.
Lorsque l'on augmente la concentration en sucre, la bande des -OH diminue de
manière importante. Cette observation traduit l'augmentation du nombre
de liaisons hydrogène entre le monosaccharide et l'eau et donc, par voie
de conséquence, la diminution des liaisons hydrogène entre
molécules d'eau. Donc lorsque la concentration augmente, le sucre
«déstructure » le réseau aqueux.
On pourrait se demander, pourquoi n'observe t'on pas de
déplacement en fréquence, puisque nos solutions sont
confinées? En fait, la résolution instrumentale (6
cm-1) ne nous permet pas de déconvoluer deux pics
séparés de quelques cm-1. De plus, dans le cas
où les molécules de sucre interagissent avec la matrice
hôte, la proportion de molécules interagissant est si faible, que
le décalage en fréquence est masqué par les autres
vibrations plus nombreuses et donc plus intenses.
|
Espèce
concernée
|
Déplacement
Raman (cm-1) Type Attribution
|
170 vh2) élongation de la liaison
hydrogène
450 vL1) libration (inter)
780 vL2) libration (inter)
Eau 1650 v2a1 déformation symétrique
(intra)
3240 v, élongation symétrique
3400 v3 élongation asymétrique
3600 - groupements OH non interagissant
|
D-glucose
|
425 CCC) déformation -C-C-C-
450 CCO)endo déformation -C-C-O-
518 C2-C1-O1) déformation -C2-C1-O1- de la forme
540 C2-C1-O1) déformation -C2-C1-O1- de la forme
585 C6-C5-O5) déformation -C6-C5-O5-
710 O5-C1-O1) déformation -O6-C1-O1- de la forme
770 O5-C1-O1) déformation -O6-C1-O1- de la forme
842 vCC) élongation -C-C- de la forme
860 vCH) élongation -C-H- de la forme
893 vCC) élongation -C-C- de la forme
910 vCH) élongation -C-H- de la forme
1018 C-O-H) déformation -C-O-H-
1060 C-O-H) déformation -C-O-H-
1124 vCO) élongation -C-O-
1260 zCH2) twisting du groupement -CH2
1336 zCH2) twisting du groupement -CH2
1372 wCH2) wagging du groupement -CH2
1445 CH2) déformation du groupement -CH2
2900 vCH) élongation
2946 vCH) élongation
|
Tableau 21 : Affectation des fréquences observées
dans le spectre du D-glucose en solution aqueuse et dans
les gels A1, A2 et A3.111,112,113,114,115
La synthèse semble donc répondre à toutes
nos attentes : confinement, concentration, conservation de la structure
moléculaire de sucre, mais il nous reste une inconnue à
déterminer : le diamètre moyen des pores ... Afin de
répondre à cette question, nous avons étudié ces
trois mêmes gels à l'aide de la diffusion des neutrons aux petits
angles (SANS).
| 


