III. Classification des minéraux argileux
Les travaux de l'A.I.P.E.A. (Association Internationale
Pour l'Etude des Argiles) (19661972) et plus tard, ceux de
Pédro (1994), ont permis d'aboutir à une classification
(Tableau I1) qui repose sur l'utilisation des critères suivants [8]
:
- Type de feuillets 2/1 ou 1/1;
- Charge globale du feuillet;
- Nature des cations inferfoliaires.
Il existe différentes classifications des argiles. La
plus classique est basée sur l'épaisseur et la structure du
feuillet. On distingue ainsi 4 groupes :
- Minéraux à 7
Å : Le feuillet est constitué d'une couche
tétraédrique et d'une couche octaédrique. Il est
qualifié de T/O ou de type 1/1. Son épaisseur est d'environ 7
Å ;
- Minéraux à 10
Å : Le feuillet est constitué de deux couches
tétraédriques et d'une couche octaédrique. Il est
qualifié de T/O/T ou de type 2/1. Son épaisseur est d'environ 10
Å ;
- Minéraux à 14
Å : Le feuillet est constitué de l'alternance de feuillets
T/O/T et de couches octaédriques interfoliaires ;
- Minéraux
interstratifiés : L'épaisseur du feuillet est variable. Ces
minéraux résultent du mélange régulier ou
irrégulier d'argiles appartenant aux groupes ci-dessus.
La valeur de la charge permanente du feuillet a servi de
critère pour établir une classification des phyllosilicates 2/1
(Tableau I-1). Cette classification est déduite des travaux de
McKenzie (1975) et Brindley (1996) [8].
Chapitre-I- Etude bibliographie
Année : 2012/2013 PFE - Master - Chimie Fondamentale
Page 16
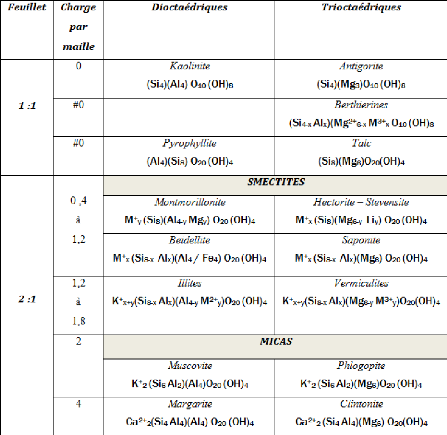
Tableau I-1 : Classification des
minéraux argileux selon la charge globale du feuillet et de la
composition de sa couche octaédrique [9].
IV. Structure des principaux minéraux argileux ?
Structure de la kaolinite :
La kaolinite est constituée d'une succession de couches
alternées de feuillets en tétraèdre (Silice) et de
feuillets en octaèdre (Aluminium), qui explique donc que l'on
considère la kaolinite comme un minéral argileux 1/1. Sa formule
théorique est Si4Al4O10(OH)8. Les deux feuillets sont
liés de telle manière qu'ils forment une seule couche
d'épaisseur d'environ 7 ? (0,7 nm) qui s'étend
indéfiniment dans les deux autres directions [2].
Chapitre-I- Etude bibliographie
Année : 2012/2013 PFE - Master - Chimie Fondamentale
Page 17
La liaison entre deux feuillets adjacents est assurée
par des liaisons hydrogènes. Ces liaisons s'établissent entre les
hydroxyles de la couche octaédrique et les oxygènes de la couche
tétraédrique. Elles entraînent un rapprochement des
feuillets adjacents, empêchant toute pénétration de
molécules d'eau, de molécules organiques ou d'ions
minéraux [10]. Il n'existe donc aucune possibilité de
gonflement ou de rétraction des feuillets. La faible capacité
d'échange des kaolinites est due à des sites de surface
amphotères.
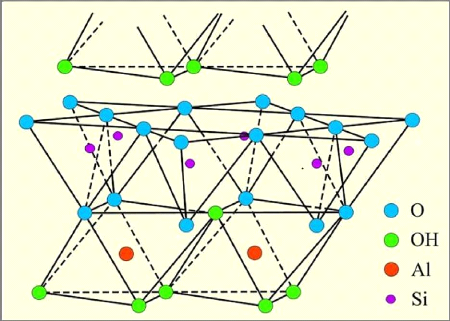
Figure I-7 : Représentation
schématique de la structure de kaolinite [11] ?
Structure de l'illite :
L'illite est constituée d'une couche octaédrique
(O) intercalée entre deux couches tétraédriques (T). Sa
formule théorique est : (Si4-xAlx) (Al2) O10 (OH)2
(K)x avec x voisin de 0,5 [1].
Les illites sont des minéraux argileux à
feuillet de type 2/1 et à équidistance basale stable à
10 Å. Elle présente des substitutions fréquentes
de Si4+ par Mg2+, Fe2+ ou Fe3+, les
défauts de charge de la maille sont compensés en
général par des ions K+ logés dans les
cavités hexagonales des couches tétraédriques
[1]. Ces gros cations assurent la liaison ionique des feuillets
adjacents et bloquent l'écart réticulaire à 10 Å
quelque soit l'état d'hydratation.
Chapitre-I- Etude bibliographie
Année : 2012/2013 PFE - Master - Chimie Fondamentale
Page 18
L'argile illitique renferme de faibles quantités d'eau
zéolithique et par conséquent ne présente pas de
phénomène de gonflement [10].
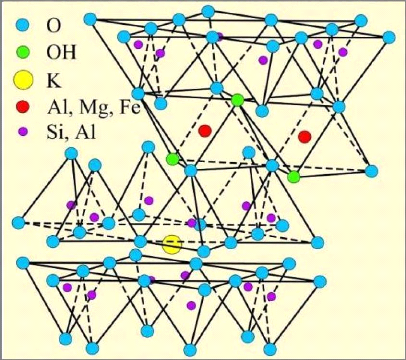
Figure I-8 : Représentation
schématique de la structure de l'illite [11] ?
Structure de chlorite :
Le chlorite est un terme qui a désigné au
début les minéraux phylliteux de couleur verte et riche en fer
ferreux [1]. Le feuillet élémentaire est de type 2/1/1,
avec en position interfoliaire une couche continue de nature hydroxylique
(couche octaédrique) déterminant une équidistance basale
très stable à 14 Å. La structure des chlorites correspond
donc à l'association d'un feuillet 2/1 de type micacé avec une
couche interfoliaire supplémentaire et indépendante,
constituée d'hydroxyde de magnésium ou de fer ferreux. Les
feuillets 2/1 sont liés entre eux par cette couche hydroxylique : les
charges négatives provenant de substitutions diverses dans le feuillet
2/1 sont en effet compensées par les charges positives
développées dans la couche octaédrique hydroxylée
au sein de laquelle se produisent des substitutions bivalent/trivalent (par
exemple : Mg2+/Al3+, Mg2+/Fe3+,
Fe2+/Fe3+) [12].
Chapitre-I- Etude bibliographie
Année : 2012/2013 PFE - Master - Chimie Fondamentale
Page 19
La couche hydroxylique, appelée couche ou feuillet
brucitique, a donc une composition mixte, ferromagnésienne ; du fait de
la compensation des charges, elle assure à l'édifice cristallin
une très grande stabilité [12].
La formule structural de chlorite est : Mg5 (Al, Fe) (OH)8 (Al,
Si)4 O10
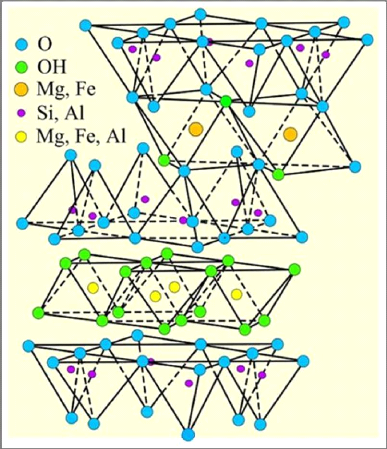
Figure I-9: Représentation
schématique de la structure de chlorite [11] ?
Structure de vermiculite :
Ce sont des minéraux à aspect de mica et sont
proches des illites et chlorites mais avec la propriété
d'être gonflants. Ils se caractérisent par la présence de
cations hydratés dans l'espace interfoliaire. Le complexe interfoliaire
comprend généralement des cations Mg ou Ca
Chapitre-I- Etude bibliographie
Année : 2012/2013 PFE - Master - Chimie Fondamentale
Page 20
et 2 couches de molécules d'eau. Ainsi, si ces
minéraux sont chauffés, ils perdent leur eau interfoliaire et
leur distance inter-réticulaire rétrécit à 10
Å. Les vermiculites dioctaédriques résultent
généralement de l'altération des micas (illite ou
muscovite) et sont abondantes dans les sols des zones tempérées.
Les vermiculites trioctaédriques sont plutôt issues de
l'altération des chlorites ou néoformées [13].
La formule générale des vermiculites est :
(Mg.CaX) (Si(8-X).AlX) (Mg.Fe)6 O20 .
yH2O avec X= 1 à 1,4 et y de l'ordre de 8.
Mg2+ et Ca2+ sont les cations compensateurs très
facilement échangeables [1].
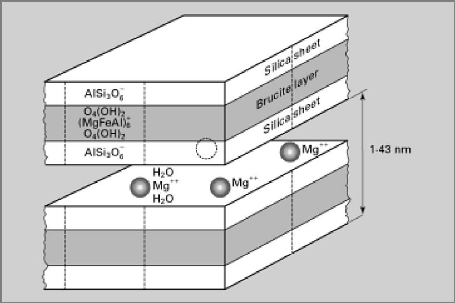
Figure I-10 : Représentation
schématique de la structure de vermiculite [30] ?
Structure de smectite :
Les smectites sont des phyllosilicates de type 2/1 (ou TOT),
constituées de deux couches tétraédriques encadrant une
couche octaédrique. Les minéraux smectites diffèrent selon
que les substitutions isomorphiques sont prédominantes dans les couches
tétraédriques et/ou octaédriques ainsi que selon la
composition chimique de leurs couches octaédriques, autrement dit
suivant que si le minéral est dioctaédrique ou
trioctaédrique [7].
Le tableau I-2 reporte la classification des différents
minéraux argileux formant la classe des smectites.
Chapitre-I- Etude bibliographie
Année : 2012/2013 PFE - Master - Chimie Fondamentale
Page 21
Chapitre-I- Etude bibliographie
Tableau I-2 : Les différents
types de smectites [14].
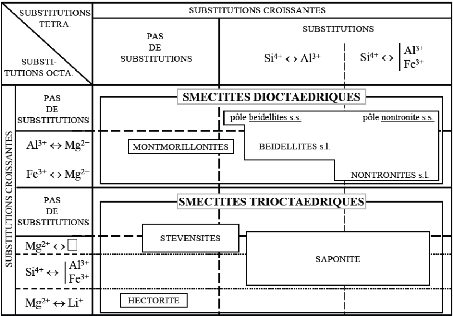
Il existe deux sous-groupes : les smectites
trioctaédriques (saponite, stevensite) et les smectites
dioctaédriques (beidellite, montmorillonite et nontronite) :
? Les smectites trioctaédriques correspondent
aux saponites ou aux stévensites dont la couche octaédrique
contient essentiellement Mg2+. Les substitutions sont alors
majoritairement tétraédriques : Si4+ remplacé
par Al3+ ou Fe3+ dans la saponite et négligeables
dans la stévensite.
? Les smectites dioctaédriques sont les
beidellites, les nontronites et les montmorillonites. Dans l'idéal, les
beidellites et les nontronites ont un déficit de charge
tétraédrique comme les saponites (Si4+
substitué par Al3+), alors que les montmorillonites ont
un déficit de charge octaédrique (Al3+
substitué par Mg2+ essentiellement). En fait, les
smectites dioctaédriques possèdent le plus souvent à la
fois des déficits de charges tétraédriques et
octaédriques et c'est cette tendance qui les classe parmi les
montmorillonites ou les beidellites. Les nontronites sont des beidellites
contenant du fer dans la couche octaédrique et éventuellement
dans la
Année : 2012/2013 PFE - Master - Chimie Fondamentale
Page 22
couche tétraédrique [4]. La
montmorillonite est la smectite la plus connue et la plus
étudiée; sa structure est schématisée sur la figure
I-11.
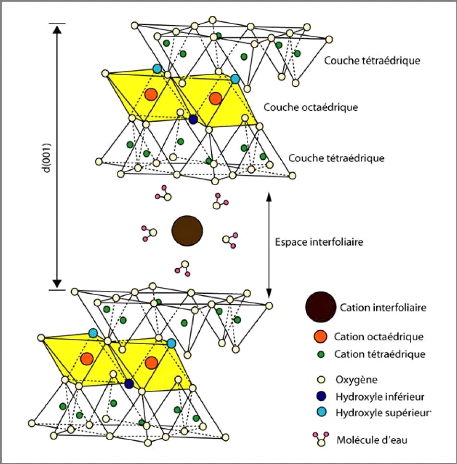
Figure I-11 :
Représentation schématique de la structure
d'une montmorillonite [4].
Les formules structurales sont très variables d'une
smectite à l'autre, même au sein d'une même espèce.
Il est donc difficile de proposer une formule structurale
générale [14]. On peut quand même donner les
formules structurales de quelques espèces parmi les plus courantes:
- Montmorillonite Rx(Al2-x
Mgx)O (Si4)T O10(OH)2,
nH2O (R=Na+ ou 1/2Ca2+, x 0,3-0,7)
- Beidellite Nax+y (Al2-x-t
Fe3+ t Mgx)O (Si4-y Aly)T
O10 (OH)2, nH2O
- Nontronite Ky (Fe3+
2-x Alx)O (Si4-y Aly)T O10(OH)2,
nH2O
Chapitre-I- Etude bibliographie
Année : 2012/2013 PFE - Master - Chimie Fondamentale
Page 23
- Saponite (Mg) Nay
(Mg3)O (Si4-y Aly)T
O10 (OH)2, nH2O
Par ailleurs, la couche interfoliaire est également de
nature variable (cations mono ou divalents avec 1 ou 2 couches d'eau). Les
cations qui assurent la compensation du déficit de charge du feuillet
T/O/T. sont principalement Na+, Ca2+, Mg2+ et
K+ [7]. Ils se localisent en général
au-dessus du centre des cavités hexagonales de la couche
tétraédrique, à des cotes variables en fonction de leur
taille, de leur sphère d'hydratation et du déficit de charges du
feuillet [7].
| 


