I.1. Principe physico-chimique :
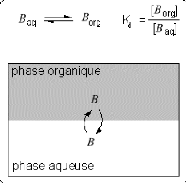
une phase organique non-miscible a l'eau. Lorsque les deux phases
liquides sont en contact il s'etablit l'equilibre de partage suivant pour B
(figure 1) :
Retire 1.1) Equilibre
de partage d'un solute B entre deux phases liquides non-miscibles
(aqueuse
et organique).
Cet equilibre est caracterise par une constante
thermodynamique Kd appelee le coefficient de partage :
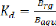
L'extraction sera d'autant plus efficace que le coefficient de
Distribution est grand, on choisit, lorsque cela est possible, un solvant
d'extraction dans lequel le solute est tres soluble
[5].
1.2. Equilibre liquide-liquide d'un system ternaire
:
Les equilibres liquide-liquide ternaire mettent en jeu trois
constituants : diluant (A), solute (B) et solvant ( C). L'introduction du
solvant dans le mélange soluté-diluant provoque l'apparition de
deux phases liquide, la premiere riche en diluant qui l'on appelle raffinat, la
seconde riche en solvant dite extrait [6].
1.2.1. Representation triangulaire :
La presence des trois constituants dans le mélange
liquide, le solute B et les deux constituants A et C, nous conduit a adopter
une presentation graphique au moyen des triangles
équilatéraux.
Chaque sommet représente un constituant pur A, B ou C.
Sur chaque coté du triangle on peut indiquer la composition des
mélanges binaires (entre 0 % et 100 %) A-B, B- C, A- C. Chaque point au
cceur du triangle représente un mélange ternaire A-B- C. Il
s'agit donc de positionner le point représentatif en fonction de la
proportion de chaque constituant sachant que % A + % B + C % = 100 %.
[7].
La figure (I- 2) rappelle les regles de lecture du diagramme.
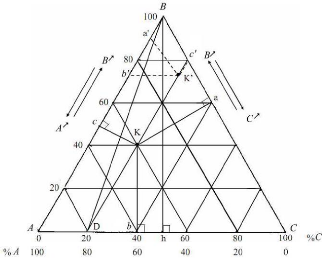
Figure I .2) : Principe de
lecture des compositions sur les diagrammes ternaires. [7] I.2.2.12egle
des mélanges : relation barycentrique
Considérons un mélange ternaire (A + B + C) de
masse R kg qui est mélangé a un mélange ternaire (A + B +
C) de masse E kg mais de composition distincte. Le point M représentatif
du ternaire (A + B + C) final a une composition intermédiaire entre R et
E qui se situe graphiquement en un point de la droite RE dont on peut
déterminer la position en écrivant les bilans massiques a l'aide
de la figure( I.3).
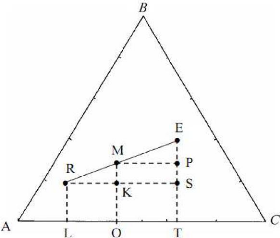
Ileum 1.3) : Relation
barycentrique entre les compositions de M, R et E.
· Bilan massique global :
R + E = M (II-1)
R : masse (kg) du mélange R ;
E : masse (kg) du mélange E ;
M : masse (kg) du mélange M.
· Bilan massique sur le constituant C :
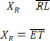
Ou : = = pourcentage de C dans R ;
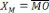
= pourcentage de C dans E ;
= pourcentage de C dans M.
Soit ;
Les relations dans les triangles semblables donnent :
(II-4) + (II-5) conduit a la regle des phases ou regle des
segments inverses :
Cette relation permet de positionner le point M a partir des
masses R et E. Ainsi lorsque :
E/R > 1, le point M est plus proche de R que de E.
Si E/R < 1, le point M est plus proche de E que de R.
· Les bilans massiques sur les trois constituants
conduisent aux relations qui traduisent le fait que le point M est le
barycentre des points R et E affectés de coefficients égaux aux
masses totales des mélanges correspondants. [7]
1.2.3. Courbe de distribution et droites de conjugaison
(conodales) :
Tout mélange liquide ternaire ayant une composition
globale se situant a l'intérieur du domaine de démixtion
génére la formation de deux phases liquides non miscibles de
compositions distinctes. Celles-ci sont régies par la thermodynamique
des mélanges a l'équilibre.
Les constituants du ternaire de composition M (fig. I-3-a) se
répartissent dans l'extrait E riche en C et dans le raffinat R riche en
A. Dans le cas retenu, le soluté B est en concentration
supérieure en E qu'en R. La relation barycentrique obtenue a partir des
bilans massiques fait que les points R, M et E sont alignés. Tout autre
mélange de départ situé sur cette droite RE conduit a des
phases non miscibles de même composition. Cette droite RE est la droite
de conjugaison représentant l'équilibre de composition des deux
phases. De la même faRon le mélange M' conduit a la formation de
deux phases non miscibles de composition R' et E'. Bien que sur le diagramme
ternaire (fig. I.3.a) on ai représenté que quatre conodales, il y
a en réalité une infinité de droites dans le domaine
biphasique. Ces droites sont rarement paralléles et leurs pentes varient
progressivement dans un sens ou dans l'autre. Dans de trés rares cas la
pente s'inverse en passant par une
droite de conjugaison horizontale pour laquelle la teneur en
solute est alors identique dans les deux phases.
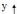
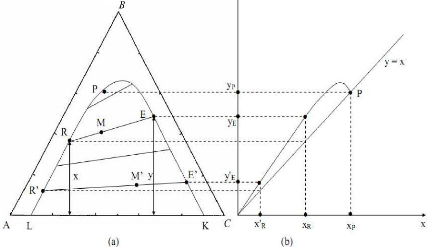
Retire 1-4): Courbe de
distribution (b) obtenue a partir des droites de conjugaison du
ternaire
liquide dont le binaire A- C est partiellement miscible.
Le point P est le point critique (droite conjuguee reduite a
un point) traduisant la limite de passage du domaine biphasique au domaine
monophasique. Au point P les courbes de limite de solubilite des solutions
riches en A et celles riches en B se rejoignent.
Le point P est generalement distinct de celui representant la
teneur maximale de B sur la courbe binodale.
La courbe de distribution (fig. I-3-b) represente a
l'equilibre la concentration du solute dans l'extrait (y) en fonction de la
concentration du solute dans le raffinat (x). Ainsi si dans le diagramme
ternaire (fig. I-3-a) l'equilibre thermodynamique est represente par une droite
(la conodale RE) sur la courbe de distribution, chaque equilibre est represente
par un point de coordonnees (R,E) = (x,y).
Compte tenu des pentes des conodales, la courbe de
distribution se situe au-dessus de la bissectrice y = x qui traduit bien que le
constituant B se concentre preferentiellement dans l'extrait. Inversement
lorsque la courbe se situe sous la bissectrice, le solute se concentre dans le
raffinat et les pentes des droites de conjugaison sont negatives.
Le choix d'un solvant C consiste tout d'abord a
vérifier que le coefficient de distribution d = y/x a l'équilibre
soit le plus grand possible ce qui limitera d'autant la quantité de
solvant nécessaire a l'extraction. [7]
| 


