|
Céramiques
Généralités
En science des matériaux est un
céramique tout élément solide, inorganique et non
métallique.

On distingue les céramiques bio-inertes qui
ne développent pas de lien avec le tissu osseux, et les
céramiques bioactives qui elles créent un lien entre l'os et le
matériau par la formation in vivo d'une couche d'apatite
carbonatée. Les céramiques inertes sont utilisées comme
matériau de frottement, les céramiques bioactives comme
matériau de comblement ou d'accrochage en recouvrement de surface.
Figure 3 : Structure macroporeuse d'une céramique
biphasée.
Céramique inertes
Alumine
A la suite des travaux de dentistes
comme Sandhaus, Boutin fut le premier à utiliser ce matériau en
orthopédie. Il implante la première prothèse
alumine-alumine en 1970. Il fut suivi par des auteurs germaniques (Griss,
Mittelmeier, Salzer), japonais (Shikita, Kawahara), italiens (Pizzoferato). De
cette période (en particulier pendant la période 1970-1977)
à aujourd'hui des améliorations ont permis d'augmenter la
fiabilité de ce matériau en améliorant sa qualité
ainsi que ses systèmes de fixation. L'alumine est obtenue par frittage
(compression à chaud [1 600 à 1 800 °C]) de poudre d'oxyde
d'alumine pur ou de mélange d'oxydes. Le frittage permet d'obtenir une
forte liaison entre les particules. Ainsi est réalisé un
matériau dense à structure polycristalline très fine,
chimiquement inerte et thermodynamiquement stable donc quasi insensible
à la corrosion.
Caractéristiques mécaniques
L'alumine haute densité est normalisée (AFNOR,
ISO). L'alumine dite de qualité médicale est pure, dense,
polycristalline. Elle est particulière par sa pureté
supérieure à 99.7, par sa densité supérieure
à 3.94. Il est essentiel que la taille des grains soit petite et qu'ils
soient régulièrement répartis. De plus, leur mise en forme
doit être particulièrement soigneuse (vitesse de rotation des
instruments tranchants ou perforants, contrôles qualité
permanents). C'est de l'ensemble de ces exigences que dépendra la
sécurité de l'alumine orthopédique. Les
caractéristiques des principales alumines. De ces
caractéristiques brutes, un certain nombre d'observations et de
conclusions doivent être faites sur trois principaux
éléments : les résistances mécaniques, le
comportement dans le frottement, et le vieillissement.
Résistance
mécanique
Elle est excellente en compression et relativement
faible en tension, ce qui caractérise les matériaux à
comportement « fragile ». Il est cependant possible de
réaliser des matériaux pour lesquels on contrôle
suffisamment l'existence de fissures initiales et surtout la taille de ces
fissures initiales. La facilité et la rapidité de propagation
d'une fissure - une fois celle-ci initiée - est une
caractéristique essentielle de ce matériau, elle est
exprimée par la constante K1c. La faible taille des grains (et surtout
la faible dispersion dans la taille des grains), le contrôle
qualité, la disparition des fissures lors du frittage, et une meilleure
connaissance du matériau ont rendu ce risque de fracture pratiquement
nul. En dehors des qualités intrinsèques du matériau
d'autres paramètres interviennent ce sont :
La taille de la tête fémorale (32 mm est une
sécurité, 28 mm est possible, 26 mm est risqué) ;
la fixation de la tête à la queue fémorale
qui est au mieux assurée par un cône-mors à rugosité
élevée permettant une meilleure répartition des charges
par augmentation de la surface de contact ;
Les précautions de stérilisation qui
devront éviter les refroidissements rapides après chauffage ;
Enfin, les précautions lors de l'implantation
chirurgicale (pas d'impaction forcée au marteau de la tête sur le
cône.
Biocompatibilité
La céramique d'alumine est un des
matériaux les plus biocompatibles, elle est souvent utilisée
comme matériau témoin. L'évaluation dans les tissus mous
et dans l'os peut être résumée comme suit :
La réaction après implantation dans les muscles
est faible aboutissant à long terme à une capsule fibreuse
paucicellulaire et riche en fibres collagènes ; les macrophages,
témoins de la permanence de l'irritation sont absents à long
terme ;
Après implantation en tissu osseux non chargé,
l'alumine est rapidement entourée d'os tissé non mature ; en 2
à 4 mois, cet os se différencie en tissu osseux mature qui vient
en contact étroit avec l'implant. A long terme, les résultats
sont inconstants avec pour certains des implants entourés de tissu
fibreux ou chondroïde. Des implantations sous forme de spacers ou de
prothèses ont montré que les zones chargées en compression
présentaient un contact osseux étroit
Zircone
Dans le cadre des prothèses de
hanche, l'alumine a donné satisfaction. Son caractère fragile, sa
faible résistance aux contraintes en traction imposent toutefois un
diamètre de tête fémorale minimal (28 ou 32 mm selon les
auteurs) pour éliminer les risques de fracture. C'est pourquoi des
céramiques plus résistantes ont été
développées ; parmi celles-ci la zircone est apparue
particulièrement intéressante.
Caractéristiques
mécaniques
Résistance mécanique
Elle est excellente, ceci s'explique par ses
caractéristiques physicochimiques. L'oxyde de zircone se présente
sous trois phases possibles : la phase cubique est stable mais fragile, la
phase tétragonale est résistante mais instable pouvant se
transformer en phase monoclinique. A 1100 °C la zircone se transforme en
phase tétragonale puis à partir de 2000 °C en phase cubique.
Le changement de phase est associé à des variations de volume.
L'addition d'oxyde de calcium, de magnésium ou d'ytrium permet d'aboutir
à une stabilisation du matériau. La zircone stabilisée par
l'oxyde d'ytrium est particulièrement intéressante car obtenue
par frittage à des températures qui correspondent à la
phase tétragonale (donc résistante). De plus, lors de
l'initiation d'une fissure, les grains à structure tétragonale se
transforment en fond de fissure en grains à structure monoclinique plus
volumineux permettant un arrêt de la propagation de la fissure. Cette
caractéristique explique que les têtes fémorales en zircone
présentent une résistance à l'impact quatre à huit
fois supérieure quand elles sont comparées à des
têtes en alumine. Les principales caractéristiques
comparées de la zircone et de l'alumine.
Biocompatibilité
Elle a été étudiée
quantitativement par Christel et coll. En tissu mou et en tissu osseux : la
réaction observée est superposable à celle observée
au contact de l'alumine. Toutefois, on ne dispose pas pour ce matériau
d'étude à long terme ni d'étude de la réaction aux
particules d'usure qui sont beaucoup plus petites que les particules d'alumine
(0,1 ìm contre 2 ìm).
Céramiques bioactives
Hydroxyapatite et phosphate tricalcique
L'hydroxyapatite (HA) est le constituant naturel
anorganique de la matrice osseuse. Sa formule chimique est :
Ca10(PO4)6(OH)2. Il peut être
synthétisé, mais présente alors avec l'HA naturelle des
différences (présence en très faible quantité
d'ions Mg, Na, K, Cl, et F dans l'os ; taille des cristaux). L'HA et ses
dérivés ont en commun la propriété
d'ostéoconduction au contact du tissu osseux. Selon le rapport P/Ca et
la structure on distingue :
ü phosphates tricalciques â (â TCP) :
Ca3(PO4)2 ;
ü hydroxyapatite (HA) :
Ca10(PO4)6(OH)2 ;
ü composites (HA + â-TCP) ;
ü d'autres composés comme la brushite, le
phosphate octocalcique ou le phosphate tétracalcique existent, mais nous
ne les détaillerons pas.
Les blocs massifs de céramiques de phosphate
de calcium sont préparés par compaction d'une poudre suivie d'un
frittage à très haute température (> 1000 °C). Ils
induisent une ostéoconduction, c'est-à-dire qu'ils servent de
support aux cellules ostéoformatrices et sont colonisés de
façon centripète par un néotissu osseux. L'os
néoformé en contact étroit avec le matériau prend
progressivement la place du matériau qui est le siège d'une
dégradation par un mécanisme cellulaire de phagocytose et
extracellulaire de dissolution.
La porosité et la solubilité sont des
paramètres fondamentaux. En effet, la repousse osseuse ne peut
s'effectuer qu'avec une porosité de 40 à 50 % et une taille de
pores située entre 100 et 300 ìm. Ces céramiques
présentent une microporosité intrinsèque ( < 100
ìm) et une macroporosité (100 ìm < < 100
ìm) et une macroporosité (100 ìm <  < 600
ìm) à la base de la néoformation osseuse. Quant à
la solubilité, elle dépend du rapport Ca/P. Il est égal
à 1,5 pour les âTCP qui sont solubles et entièrement
dégradables et à 1,67 ou plus pour les HA qui sont insolubles et
peu ou pas dégradables. < 600
ìm) à la base de la néoformation osseuse. Quant à
la solubilité, elle dépend du rapport Ca/P. Il est égal
à 1,5 pour les âTCP qui sont solubles et entièrement
dégradables et à 1,67 ou plus pour les HA qui sont insolubles et
peu ou pas dégradables.
L'utilisation de ces biocéramiques est
limitée par des propriétés mécaniques faibles
(fragilité due à la porosité, résistance
mécanique faible). En pratique, certaines conditions doivent être
respectées de façon stricte par le chirurgien, ce qui limite
leurs indications. Ces conditions sont :
ü contact étroit avec l'os ;
ü absence de contrainte et de mouvements à
l'interface.
Bioverres
Les bioverres sont une des classes de
céramiques bioactives. Un lien chimique est donc recherché entre
l'os et le matériau. C'est depuis les années 1970 que Hench a
étudié et développé différents types de
bioverres. D'autres auteurs ont ensuite recherché des formulations
différentes ayant la même action de liaison à l'os.
La caractéristique commune à tous les
bioverres quelle que soit leur composition est de présenter à
l'interface des modifications qui aboutissent à la formation, à
la surface du bioverre, d'une couche d'hydroxyapatite carbonatée qui
chimiquement et structurellement est identique à la phase
minérale de l'os, cette équivalence serait responsable du lien
entre os et matériau. Les études les plus poussées ont
été réalisées sur des verres à base de
silice (verres de Hench). Histologiquement, l'interface est formée de
l'implant à l'os d'une couche riche en silice et d'une couche
d'hydroxyapatite carbonatée ; une zone composite de 100 ìm
d'épaisseur en moyenne est formée de fibres collagènes
venant du tissu osseux et d'hydroxyapatite. L'interface composite est similaire
à celle que l'on observe à la jonction tendon-os entre un
matériau à module d'Young faible et un matériau à
module d'Young plus élevé. Mécaniquement, le lien entre os
et matériau est suffisamment solide pour que lors des tests
mécaniques, la rupture intervienne préférentiellement soit
dans l'os, soit dans le bioverre mais pas à l'interface.
Les verres bioactifs les plus étudiés et
utilisés sont composés principalement d'oxydes de silicium
(SiO2), de sodium (Na2O), de calcium (CaO) et de
Phosphore (P2O5). Le verre le plus utilisé et
le plus bioactif est le verre noté bioverre 45S5 de L.L.
Hench (composé en % massique de 45% de SiO2, 24,5% de
Na2O, 24,5% de CaO et 6% de P2O5). Ce bioverre
est classé sur toute la gamme des matériaux bioactifs
dans la classe A, qui correspond à l'indice de
bioactivité le plus élevé. Cette bioactivité
est due à la capacité du bioverre lorsqu'il est
immergé dans le milieu physiologique, de former de l'hydroxyapatite
carbonatée (HAC). Cette couche HAC permet un accrochage chimique en
environ 12 heures de l'implant à l'os. La bioactivité du
bioverre 45S5 lui confère des propriétés
d'ostéoconduction, d'ostéostimulation et de résorption.
Propriété structurale : Les phases
cristallines
La cristallographie des bioverres joue un rôle
important sur leur bioactivité et leur résistance
mécanique. Le bioverre a été traité thermiquement
à différente température puis analysé par
diffraction des rayons X afin d'identifier les phases cristallines en fonction
de la température comme représenté sur la figure
ci-dessous :
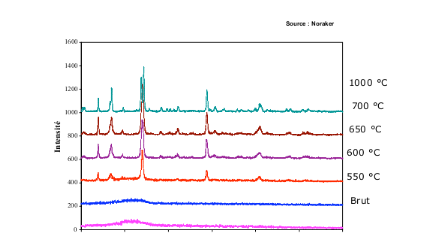
Figure X : Diagrammes de diffraction X du bioverre 45S5 en
fonction de la température du traitement thermique.
L'analyse des diagrammes de diffraction X (Figure 00) indique
que le bioverre présente une structure amorphe jusqu'à
550°C. Au delà de cette température, le traitement
thermique provoque l'apparition de deux phases cristallines, la
première, majoritaires apparaît à partir de 600°C :
Na2Ca2(SiO3)3 et la seconde
à partir de 700°C : Na2CaSi3O8.
Le bioverre 45S5 est un Matériau bioactif qui permet
l'Ostéointégration (ostéoproduction) et
l'ostéoconduction. Il est biocompatible, 100 % Synthétique et
entièrement Biorésorbable. Cependant malgré les nombreuses
propriétés de ce matériau, des limites technologiques sont
identifiable et notamment au niveau de niveau de sa fragilité et de sa
mise en forme. Afin de lever le verrou technologique, la tendance est
d'associer une phase polymère résorbable à une phase
minérale.
Les propriétés mécaniques des
bioverres sont modestes, en particulier la résistance en flexion, aussi,
l'utilisation sous forme massive est-elle réservée à des
zones peu ou pas sollicitées. Ainsi le Bioglass a une résistance
en flexion de moins de 7 kg/mm2 qui est améliorée
après cristallisation ; le Cervical présente une
résistance en flexion de 10 kg/mm2 ; la vitrocéramique
d'apatite-wollastonite est la plus résistante avec une
résistance en flexion de 23 kg/mm2. Plusieurs approches
permettent IV- Elaboration des bio- verres poreux à visée
orthopédique
Les substituts osseux biphasés en hydroxyapatite
et phosphate tricalcique sont considérés comme l'alternative
majeure aux greffes autologues. Contrairement à l'os autologue,
ces matériaux ont plusieurs inconvénients. D'une part, ils sont
partiellement résorbables, d'autre part, ils sont
ostéoconducteurs mais pas ostéoinducteurs. De plus, le
comportement mécanique de ces matériaux reste très
fragile.
Le développement d'une nouvelle structure poreuse
d'implants à partir de bio-verre pour application de substitution
osseuse permet de remédier à ces inconvénients. Une
alternative prometteuse est alors la réalisation de bio- verres
poreux, plus facilement résorbables en surface, et qui permettent
alors les processus de dissolution de Calcium et Phosphore, puis de re-
précipitation en surface d'hydroxyapatite de composition plus proche de
la partie minérale de l'os. Ces verres bios- actifs, sont
déjà utilisés dans le domaine dentaire comme
granulés et dans le revêtement de prothèses
métalliques. Ils ne sont cependant pas encore utilisés en
orthopédie pour la réalisation de substituts poreux, à
cause de verrous technologiques à leur fabrication. La
société NORAKER développe un procédé de
fabrication permettant de réaliser des bio-verres poreux, dans des
gammes de porosités identiques aux substituts osseux en
hydroxyapatite. Ce procédé permet de réaliser des
substituts osseux avec une porosité contrôlée, à
l'échelle nanométrique, micrométrique et macroscopique.
Les résultats montrent des propriétés mécaniques
supérieures à celles des hydroxyapatites poreuses pour un
même taux de porosité, ainsi que des propriétés
biologiques plus intéressantes, de part la formation d'hydroxyapatite
naturelle à leur surface.

Figure 8 : Exemple de substituts osseux
développé par la société NORAKER.
d'utiliser les propriétés biologiques des
bioverres : le recouvrement de matériaux ayant de meilleures
qualités mécaniques (céramiques, métaux), ou
l'utilisation de composites faits de fibres métalliques dans un substrat
de bioverre.
Quelques applications cliniques ont été
réalisées à l'aide de ces matériaux. Il faut citer,
le remplacement vertébral, le comblement osseux après
exérèse tumorale ou la réalisation de butée
d'épaule pour luxation récidivante.
Phosphates de calcium
Les phosphates de calcium sont des céramiques
biocompatibles. Ils sont ostéoconductifs grâce à leur
ressemblance avec la phase minérale de l'os. Ils
possèdent aussi la propriété d'être
biodégradables. Parmi les phosphates de calcium, l'hydroxyapatite
(HA) et le â-tricalcium phosphate (â-TCP) sont souvent
utilisés comme matériaux de comblement osseux. Ils peuvent
être utilisés sous forme de particules macroporeuses pour
améliorer l'ostéointégration et la
biodégradation en augmentant la surface spécifique. En
effet, la macroporosité favorise la repousse de l'os en permettant
l'invasion par des précurseurs vasculaires et des cellules osseuses
(Knabe et al. 2008). Ils peuvent aussi être implantés sous forme
de blocs de taille millimétrique avec macroporosité
interconnectée (Weiss et al., 2003). Il existe de nombreuses autres
formes de phosphates de calcium (les plus importants sont
rassemblés dans le Tableau III -Mihailescu IN et al., 2010).
Certains de ces phosphates de calcium, dont le DCPD (brushite), DCPA,
OCP, â-TCP et ACP sont parfois trouvés dans les tissus
vivants dans des conditions normales ou pathologiques.
Utilisation du phosphate tricalcique â
Les céramiques de phosphate de calcium sont de plus en
plus utilisées en chirurgie osseuse.
En particulier, Le phosphate tricalcique â a
été utilisé en traumatologie dans 24 cas. La
classification du GESTO (Association pour l'étude des greffes et
substituts tissulaires en orthopédie) prenant en compte le type, la
nature et la taille de la perte de substance a été couplée
à une échelle qualitative de l'intégration.
Le phosphate tricalcique â apparaît comme un
substitut osseux de choix pour le comblement des pertes de substance osseuse
modérées observées en traumatologie.
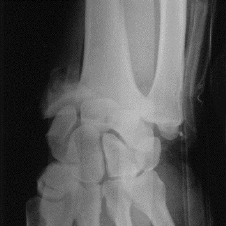
Figure X : Homme de 48 ans. Fracture comminutive du
poignet.
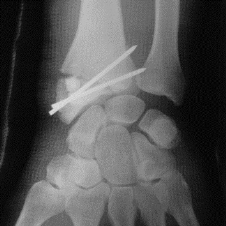
Figure X : Comblement de la perte de substance
osseuse styloïdienne par deux 2 cubes de
5 × 5 × 5 mm de Biosorb et
ostéosynthèse par embrochage.
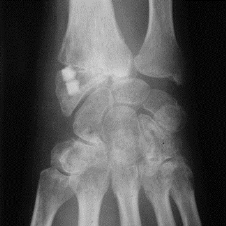
Figure X : Cinq mois postopératoires. Ablation des
broches. Intégration périphérique des implants.
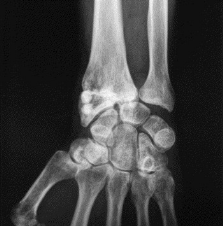
Figure X : Neuf mois postopératoires. Bonne
intégration des implants prenant un aspect floconneux.
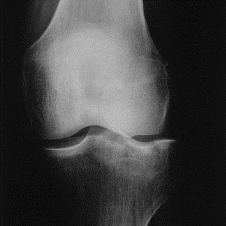
Figure X : Femme de 63 ans. Fracture enfoncement du
plateau tibial externe.
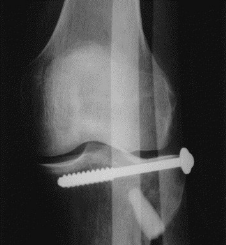
Figure 6 : Aspect postopératoire.
Relèvement du plateau tibial et comblement de la perte de substance
osseuse par un implant de Biosorb qui sert d'étai sous-chondral.
Ostéosynthèse par vis.
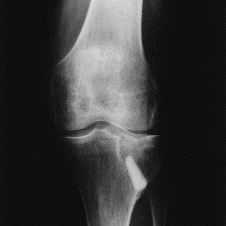
Figure X : Dix mois après l'opération.
Ablation du matériel. Aspect radiographique du substitut
inchangé.
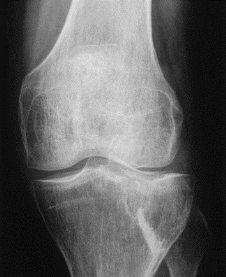
Figure X : Vingt-cinq mois après
l'opération. Bonne intégration du substitut qui est presque
totalement résorbé.
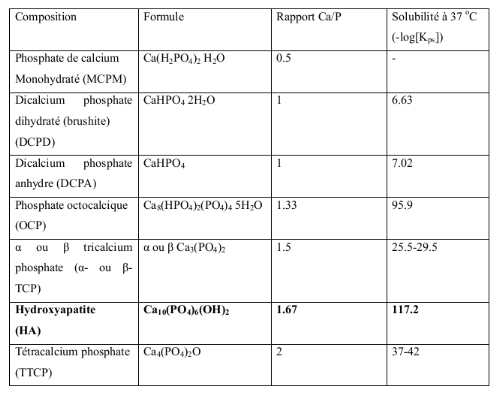
Tableau III : Différents phosphates de calcium :
formules chimiques, rapport Ca/P et solubilité.
| 

