
REPUBLIC OF CAMEROON Peace - Work -
Fatherland
RÉPUBLIQUE DU CAMEROUN
Paix -Travail -
Patrie
******
UNIVERSITÉ DE YAOUNDÉ
I
******
ÉCOLE NORMALE
SUPÉRIEURE
******
DÉPARTEMENT DE
CHIMIE
******
******
THE UNIVERSITY OF YAOUNDE I
******
HIGHER TEACHER TRAINING COLLEGE
******
DEPARTMENT OF CHEMISTRY
*****
LABORATOIRE DE CHIMIE INORGANIQUE
LABORATORY OF INORGANIC CHEMISTRY
CONTRIBUTION À L'ÉTUDE DE
L'APPORT
CALCIQUE ET MAGNÉSIQUE DES EXTRAITS À
L'EAU ET
À L'ACIDE CHLORHYDRIQUE 0,1M DE
L'AFRAMOMUM DANIELLII ET DU
FAGARA
XANTHOXYLOÏDES (ÉPICES CONSOMMÉES
AU
CAMEROUN)
Mémoire rédigé et soutenu
publiquement en vue de l'obtention du Diplôme de Professeur de
l'Enseignement Secondaire, Deuxième Grade
(DI.P.E.S. II)
Par :
MATANGOUO SONKOUE Baudelaire
Licencié en chimie
inorganique
Matricule : CM04-07SCI0523 Sous la
direction de : NGANSOP René
Chargé de cours (ENS)
Juin 2013
CERTIFICATION DU DIRECTEUR
|
Je soussigné Dr. NGANSOP René,
certifie que les travaux effectués par l'étudiant
MATANGOUO SONKOUE Baudelaire, matricule
CM04-07SCI0523, portant sur :
« Contribution à l'étude de
l'apport calcique et magnésique des extraits à l'eau et à
l'acide chlorhydrique 0,1M de l'aframomum daniellii et du fagara
xanthoxyloïdes (épices consommées au Cameroun)
», ont été réalisés sous ma direction
au Laboratoire de Chimie Inorganique de l'École Normale
Supérieure de Yaoundé. Ce travail n'a jamais été
présenté devant un jury dans le cadre d'une thèse ou d'un
mémoire.
En foi de quoi la présente attestation lui est
établie pour servir et valoir ce que de droit.
Fait à Yaoundé le
Le Directeur de Mémoire
NGANSOP René
Chargé de Cours (ENS)
DÉDICACES
À la mémoire de mon feu père FOMETIO
Maurice
À ma mère NZANGUIM Marthe
À mes frères et soeurs.
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 i
REMERCIEMENTS
Je tiens à témoigner ma gratitude :
· Au Dr. NGANSOP René, pour m'avoir accueilli
chaleureusement dans son équipe de recherche et pour m'avoir
initié à la recherche.
· À tous les enseignants des Départements
de Chimie et de Physique de l'Ecole Normale Supérieure de
Yaoundé, pour la qualité de formation.
· À la grande famille FOMETIO Maurice, pour tous
les efforts consentis tout au long de ma formation.
· À TADJUI Blaise, pour tout le soutien qu'il m'a
apporté.
· Aux familles IMMATA, DOUANLA, SOKENG, pour l'accueil,
le soutien et le réconfort qu'ils ont manifesté à mon
endroit.
· À KOKEA Chantal, MELI Sylviane, SAHA Clovis,
Papa KENNE David, FOMENE Yves, FOMETIO Roselin, TATSAWOUM Sidoin, FOMETIO
Jerry, MBOGNING Gaurès, FOMETIO Maurice pour tout le soutien et les
encouragements qu'ils ont su m'apporter.
· À mes amis NGUELA Rodrigue, TACGANG Alain,
FUMBA Gaston, ESSOMBA Serge, TCHOUALA Alex, KEUBOU Alex, TATANG Miterand,
MOULIOM Emmanuel, KAGHO Donald, MBA Martin, YOMI Chimène pour leur
soutien multiforme et leur sincère amitié.
· À tous mes camarades de promotion et en
particulier ceux de laboratoire, MAZONGUI Annie, DJAMOU Alain, TAKOUKAM Bertin,
MISTE Pamela, ZOCK André, pour l'esprit d'équipe.
· À Tous ceux qui ont oeuvré de
près ou de loin à la confection de ce mémoire.
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 ii
LISTE DES ABRÉVIATIONS
EDTA ou Y : Ethylène diamine tétra
acétique
T.A : Tampon ammoniacal
NET : Noir Eriochrome T
VEDTA : Volume d'EDTA
RPR : Réactif de Patton et Reeder
H2Y2- : Forme anionique de l'EDTA
pH : Potentiel hydrogène
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
iii
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 iv
LISTE DES TABLEAUX
Tableau I : Apports conseillés en
calcium en mg par jour 13
Tableau II : Valeurs magnésiques de
quelques aliments ..15
Tableau III : Apports conseillés en
magnésium en mg par jour 16
Tableau IV : Concentrations molaires totales
en ions Ca2+ et Mg2+ de l'aframomum
daniellii en fonction du solvant et du temps
d'extraction ..26
Tableau V : Concentrations totales en ions
Ca2+ et Mg2+ de l'aframomum daniellii sous
agitation constante en fonction du solvant et du temps
d'extraction ..27
Tableau VI : Concentrations molaires totales
en ions Ca2+ et Mg2+ du fagara
xanthoxylïodes en fonction du solvant et du
temps d'extraction 28
Tableau VII : Concentrations totales en ions
Ca2+ et Mg2+ du fagara xanthoxylïodes
sous agitation constante en fonction du solvant et du temps
d'extraction ..29
LISTE DES FIGURES
|
Figure 1 : Plante d'aframomum daniellii
|
9
|
|
Figure 2 : Fruits d'aframomum daniellii
|
9
|
|
Figure 3 : Fruits de fagara
xanthoxyloïdes
|
...10
|
Figure 4 : Organigramme du mode
opératoire pour la détermination des titres totaux en
ions Ca2+ et Mg2+ 23
Figure 5 : Organigramme du mode
opératoire pour la détermination des titres totaux en
ions Ca2+ et Mg2+ lorsque la suspension est
agitée .24
Figure 6 : Évolution de la concentration
en ions Ca2+ et Mg2+ de l'aframomum daniellii
en fonction du solvant et du temps d'extraction . ..30
Figure 7 : Évolution de la concentration
en ions Ca2+ et Mg2+ de l'aframomum daniellii en
fonction du solvant sous agitation constante et du temps
d'extraction .30
Figure 8 : Évolution de la concentration
en ions Ca2+ et Mg2+ du fagara
xanthoxylïodes en fonction du solvant et du temps
d'extraction 31
Figure 9 : Évolution de la concentration
en ions Ca2+ et Mg2+ du fagara xanthoxylïodes
en fonction du solvant sous agitation constante et du temps
d'extraction .31
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 v
SOMMAIRE
DÉDICACES i
REMERCIEMENTS ii
LISTE DES ABRÉVIATIONS ii
LISTE DES TABLEAUX iv
LISTE DES FIGURES v
SOMMAIRE vi
RESUMÉ viii
ABSTRACT ix
INTRODUCTION 1
CHAPITRE I :GÉNÉRALITÉS ET REVUE DE LA
LITTÉRATURE SUR LES
ÉPICES 4
I. GÉNÉRALITÉS SUR LES ÉPICES 5
I. 1.Définitions 5
I.2. Historique 6
I. 3 Étude pharmacologique 7
I. 4 Épices et santé 7
II. ÉTUDE DE QUELQUES ÉPICES
CONSOMMÉES AU CAMEROUN 8
II.1. Famille des Zingiberaceae : Aframomum Daniellii 8
II.1.1. Description 8
II.1.2. Ethnobotanique et utilisation 9
II.2. Famille des Rutaceae : Fagara xanthoxyloïdes 9
II.2.1. Description 9
II.2.2. Ethnobotanique et utilisations 10
III GÉNÉRALITÉS SUR LE CALCIUM ET LE
MAGNÉSIUM 11
III.1. Élément calcium 11
III.1.1. Sources du calcium 11
III.1.2. Absorption du calcium 12
III.1.3. Importance du calcium dans l'organisme 12
III.1.4. Symptômes d'un manque en calcium 13
III.2. Élément magnésium 14
III.2.1. Sources du magnésium 14
III.2.2. Absorption du magnésium 15
III.2.3. Importance du magnésium dans l'organisme 15
III.2.4. Symptômes d'un manque en magnésium 17
III .3 Dosage des ions calcium et magnésium 17
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 vi
III.3.1. Dosage des ions calcium 17
III.3.2. Dosage des ions magnésium 18
III.3.3 Dosage des ions calcium et magnésium dans la
même solution 18 CHAPITRE II :MATÉRIAUX, MATÉRIEL,
RÉACTIFS ET MÉTHODES
EXPÉRIMENTALES 20
I. MATÉRIAUX 21
I.1. Origine 21
I.2. Conditionnement 21
II. MATÉRIEL 21
III. RÉACTIFS UTILISÉS 21
IV. MÉTHODE EXPÉRIMENTALE 22
IV.1. Principe 22
IV.2 Mode opératoire 22
CHAPITRE III :RÉSULTATS ET INTERPRÉTATION 25
I. RESULTATS 26
II. INTERPRÉTATION 32
INTÉRÊTS.PÉDAGOGIQUES 33
CONCLUSION 35
RÉFÉRENCES BIBLIOGRAPHIQUES 37
ANNEXES 40
Annexes I : Préparation des solutions 41
Annexe II Formules semi-développées du NET et de
l'EDTA 44
Annexe III : Calcul des concentrations 45
Annexe IV : Calcul de 46
Annexe V : Épices et condiments de la sauce jaune et du
«Nkui» 47
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
vii
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 viii
RESUMÉ
Dans le présent travail, les teneurs en ions
alcalino-terreux (calcium et magnésium) des extraits à l'eau
distillée et à l'acide chlorhydrique 0,1M de l'aframomum
daniellii et du fagara xanthoxylïodes (épices
consommées au Cameroun) sont analysées. Cette analyse a
été menée en dosant par complexométrie les ions
calcium et magnésium contenus dans lesdits extraits.
L'étude montre qu'après un temps de
macération de 12 h, les concentrations en ions calcium et
magnésium sont de 8,64 mmol/L et 12,52 mmol/L par 50 g d'aframomum
daniellii respectivement dans l'eau distillée et dans l'acide
chlorhydrique 0,1 M. Elles sont de 7,39 mmol/L et 12,97 mmol/L par 50 g de
fagara xanthoxylïodes respectivement dans l'eau distillée
et dans l'acide chlorhydrique 0,1 M. Ces concentrations varient lorsque la
suspension est agitée : 8,97 mmol/L et 13,81 mmol/L par 50 g
d'aframomum daniellii respectivement dans l'eau distillée et
dans l'acide chlorhydrique 0,1 M ; et 6,86 mmol/L et 15,69 mmol/L par 50 g de
fagara xanthoxylïodes respectivement dans l'eau distillée
et dans l'acide chlorhydrique 0,1 M.
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 ix
ABSTRACT
In the present piece of work, concentrations of calcium and
magnesium ions contained in extracts from distilled water and chlorhydric acid
of aframomum daniellii and of fagara xanthoxyloïdes
(spices consumed in Cameroon) are analysed. This analysis has been made by
complexometric titration of calcium and magnesium ions contained in the given
extracts.
The analysis reveals that after some macerated time of 12
hours, concentrations of calcium and magnesium ions are of 8.64 mmol/L and of
12.52 mmol/L per 50g of aframomum daniellii respectively in distilled
water and 0.1M chlorhydric acid and of 7.39 mmol/L and of 12.97 mmol/L per 50g
of fagara xanthoxyloïdes respectively in the distilled water and
0.1M chlorhydric acid. Those concentrations change when the suspension is
troubled: 8.97 mmol/L and 13.81 mmol/L per 50g of aframomum daniellii
respectively in the distilled water and 0.1M chlorhydric acid and of 6.86
mmol/L and 15.69 mmol/L per 50g of fagara xanthoxyloïdes
respectively in the distilled water and 0.1M chlorhydric acid.

INTRODUCTION
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 2
De par leur popularité ancestrale, les aliments
épicés ont non seulement de valeurs sensorielles, mais sont aussi
porteurs, dans plusieurs contrées, des valeurs culturelles des
populations qui les utilisent. La sauce jaune et la sauce gluante (Nkui)
apparaissent comme un exemple de cette valeur culinaire, sociale et culturelle
des épices. Elles sont consommées traditionnellement dans l'Ouest
du Cameroun et leur préparation intègre un complexe de 6 à
18 épices. La valeur culturelle et sociale de ces sauces tient à
leur utilisation comme symbole de reconnaissance et d'estime lors des
réceptions de hautes personnalités et invités de marque.
Sur le plan de la santé, on leur attribue un rôle d'induction de
la lactation, de revitalisant, d'aphrodisiaque, d'agent bactéricide et
de détoxifiant. Cette valeur thérapeutique viendrait des
épices qui entrent dans leur composition.
Malgré l'importance socioculturelle et
thérapeutique des épices de la sauce jaune et de la sauce
gluante, les études sur l'apport calcique et magnésique de
celles-ci restent très peu menées. On peut toutefois relever dans
la limite de nos connaissances, les travaux de Tchiégang et Mbougueng
(2005) qui ont porté sur la composition chimique des épices
consommées à l'Ouest Cameroun, et de Yangoué (2008) sur
l'apport calcique et magnésique des extraits à l'eau de
l'aframomum daniellii et de fagara xanthoxyloïdes.
Dans l'objectif d'améliorer la consommation des
bio-ressources du milieu naturel Camerounais, un projet de recherche a
été initié au laboratoire de chimie inorganique de
l'École Normale Supérieure de Yaoundé sur la
physico-chimie des coquilles d'oeufs et des épices susceptibles
d'être source de calcium et de magnésium en médecine
alternative. Le présent travail s'inscrit dans ce cadre et porte sur la
contribution à l'étude de l'apport calcique et magnésique
des extraits à l'eau et à l'acide chlorhydrique 0,1M de
l'aframomum daniellii et du fagara xanthoxyloïdes. En
effet, Yangoué (2008) lors de ses travaux sur ces épices a
utilisé l'eau distillée comme solvant d'extraction sans aucune
agitation permanente de la suspension (solvant et poudre d'épice) alors
que le milieu stomacal est acide et en perpétuelle agitation. Cette
opposition soulève une problématique : l'influence de la nature
du solvant et de l'agitation du milieu réactionnel sur les
quantités d'ions calcium et magnésium des extraits des
épices. C'est
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 3
pour cette raison que nous avons repris ce travail dans le but
d'étudier l'influence des paramètres suscités tout en nous
familiarisant avec les techniques complexométriques.
Pour mener à bien ce travail, nous l'avons organisé
en trois chapitres. Le premier porte sur les généralités
et revue de la littérature sur les épices, le deuxième sur
la démarche expérimentale et le troisième sur les
résultats et discussions.
CHAPITRE I :
|
|
GÉNÉRALITÉS ET REVUE DE
LA
|
|
LITTÉRATURE SUR LES ÉPICES
|
|
|
|
I. GÉNÉRALITÉS SUR LES
ÉPICES
I. 1.Définitions
A l'exception du sel, substance minérale, les
épices et les aromates sont des substances d'origine
végétale, ayant pour fonction essentielle d'assaisonner les mets.
La popularité dont jouissent encore les épices de nos jours est
liée aux propriétés et vertus qui leur sont
attribuées. L'existence de la pluralité des mets dans le monde
est en partie due au simple fait que l'homme dans sa perpétuelle
recherche de nouvelles saveurs fait recours aux épices
traditionnelles.
Le mot épice provient du latin « species
» signifiant espèce ou substance. Les épices sont des
parties séchées ou non des plantes aromatiques : feuilles,
boutons floraux, graines, écorces, fruits, racines. Utilisées
seules ou mélangées, elles sont destinées à
relever, à parfumer, à colorer tout en communiquant une saveur
particulière. D'après Nevellier et Jolivet (1965) le terme «
épice » s'applique aux produits naturels végétaux ou
mélange de ceux-ci, sans matières étrangères qui
sont utilisés soit en entier, soit en poudre pour donner de la saveur et
de l'arôme et pour assaisonner les aliments. Cette définition
s'accorde avec celle du Petit Larousse(2005) qui définit l'épice
comme une substance aromatique d'origine végétale utilisée
pour assaisonner les mets.
L'encyclopédie définit les épices comme
étant des substances aromatiques tirées de certains
végétaux (écorces, racines, feuilles, fleurs, gousses,
graines, fruits) originaires de l'Inde, de l'Afrique tropicale, de
l'Amérique. On les emploie comme condiments pour relever la saveur des
mets, pour parfumer les boissons ou activer les fonctions de l'estomac.
(Youmbi, 2011)
Dans la langue romaine, les épices sont définies
comme étant des « substances d'origine indigène ou exotique,
aromatique, à saveur chaude ou piquante, employées pour rehausser
le goût des aliments ou y ajouter les principes stimulants qui y sont
contenus ».
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 5
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 6
La particularité des épices est qu'elles sont
souvent obtenues après séchage de la plante et/ou transformation
(fermentation, blanchiment, stabilisation), contrairement aux aromates, qui
sont généralement consommées sans aucune transformation.
L'assaisonnement « aromatique » est souvent plus doux, le goût
est alors beaucoup moins relevé que celui des épices au
caractère plus affirmé. Quant aux condiments, ils servent
également à accompagner les plats, la différence
essentielle tenant au traitement culinaire préalable à l'usage :
ils peuvent se présenter en conserve, sous leur forme naturelle, ou
être préparés en pâte ou sauce.
I.2. Historique
D'histoires tragiques en épopées
extraordinaires, les épices ont de tout temps suscité convoitise
et fascination : que de fortunes fabuleuses, d'expéditions à
travers les siècles et les continents, de crimes et de conquêtes
ont été initiées pour ces substances autrefois plus
précieuses que l'or. C'est presque l'histoire de l'humanité qui
défile à travers la quête des épices : Grecs,
Romains, Arabes, Vénitiens, Portugais, Hollandais, Français,
Anglais se sont succédés tour à tour pour obtenir le
privilège de parsemer leur cuisine de parfums incomparables et remplir
leur cuisine, leur coffre grâce à cette manne providentielle.
Au XVe siècle, la recherche de nouvelle
route vers le pays conducteurs d'épices est l'un des principaux enjeux
des grandes découvertes. A l'époque, l'augmentation de la
consommation de viande impose le recours à d'importantes
quantités d'épices, importées d'Afrique (malaguette de
guinée, poivre du Bénin) et de maigre qualité. Vendus en
Tripolitaine, au débouché des routes transsahariennes, ces
produits sont distribués en Europe par les Vénitiens.
Au début du XVIe siècle, la fermeture
de la méditerranée après la conquête turque modifie
les routes commerciales, qui empruntent dès lors les voies maritimes qui
contournent l'Afrique. Le commerce avec les Indes orientales, principale
réserve d'épices, est d'abord contrôlé par les
Portugais, jusqu'à l'intervention des Espagnols puis, au
XVIIe siècle, des Néerlandais et des Français ;
les grands ports d'importateurs, pour le Nord de l'Europe, seront Lisbonne et
Anvers. Les épices étaient moins chères,
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 7
plus accessibles et de ce fait moins utilisées par les
riches car elles n'étaient plus considérées comme un objet
de noblesse.
A la fin du XVIIe siècle, des épices,
des fruits et l'ail étaient mis en bouteille avec du vinaigre pour
améliorer leur préservation. Aujourd'hui les épices font
partie de notre vie quotidienne.
I. 3 Étude pharmacologique
Outre leur utilisation en cuisine, certaines de ces
épices présentent des activités thérapeutiques :
diurétique (Allium sativum, hibiscus sabdariffa, Tétrapleura
Tetraptera par la scoppoletine) ; anticonvulsif, aphrodisiaques (Aframomum
melegueta, Mondia whitei, pentadiplandra brazzeana, piper guineense) ;
anti-athérome (Echinops giganteus) ; hématopoète (piper
guineense) ; stimulant, stomachique (Mondia whitei, Capsicum, Allium, Zingiber
officinale, les apiacées, les lamiacées) ; hypoglycémiant,
bactériostatique (Allium porum) ; fébrifuges (Cymbopognon
citratus, Allium Sativum). (Youmbi, 2011)
I. 4 Épices et santé
Depuis longtemps, les épices représentent une
part importante de la nourriture humaine. A côté des fibres
alimentaires et des vitamines, on a récemment identifié, dans les
fruits, légumes et épices, d'autres composés comme les
phénols et les flavonoïdes qui pourraient avoir des effets
bénéfiques pour la santé (Groff et Gropper, 2000). En
effet, à côté de leur fonction dans la plante comme
protecteurs contre les agresseurs de l'environnement, on attribue à ces
composés des fonctions salutaires pour l'homme, comme la
réduction de maladies vasculaires et cardiaques (Hertog et al.
1993).
C'est pourquoi, ces dernières années ont
été marquées par la recherche d'antioxydants et de sels
minéraux. Certaines épices facilitent la digestion des mets
lourds, soit par les tanins contenus qui favorisent la sécrétion
biliaire, soit parce qu'elles contiennent des lipases ou des protéases
qui pré-digèrent les aliments qu'elles accompagnent.
(Tchiégang et Mbougueng, 2005).
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 8
II. ÉTUDE DE QUELQUES ÉPICES
CONSOMMÉES AU CAMEROUN
II.1. Famille des zingiberaceae : aframomum daniellii
*Synonymes: aframomum daniellii, aframomum
afzelii, aframomum angustifolium
*Noms vernaculaires: Esson (Beti), Besak
(Bangwa), Atsoo (Foto), Kichione (Yambassa), Etutu (Douala).
II.1.1. Description
Aframomum daniellii est une plante pérenne, de
longueur comprise entre 3-4 m. Les feuilles (figure 1) larges ont une longueur
de 7-10 cm et une largeur de 30-50 cm ; les fleurs ont 2 cm de large et de
couleur rouge orangée, encombrées et bractées. Les fruits
sont de couleur rouge et de forme ovoïde, avec des capsules arrondies
à la base et pointées à l'apex dans les bouquets
dressés. L'intérieur de la capsule possède une pulpe
blanche qui protège les graines (figure 2). Ces dernières ont une
longueur de 4 à 6 mm, de forme pyramidale avec une surface lisse ; ces
graines ont un parfum aromatique et une saveur acide. Cette famille de grandes
herbes à larges feuilles est bien représentée dans la zone
de forêt dense humide, moins bien en savane. Ce sont des plantes qui, par
froissement des feuilles ou par des rhizomes, dégagent une odeur
aromatique très particulière.
Les zingiberaceae portent parfois des inflorescences compactes
aux extrémités de tiges feuillées, mais fréquemment
ces inflorescences naissent directement sur le rhizome et se dressent
verticalement en épi. Le fruit est charnu, de teinte rouge à
maturité, avec des graines enfermées dans une pulpe
acidulée. Les aframomum sont des espèces africaines
endémiques dont certaines graines sont utilisées comme
condiments. C'est une plante qu'on retrouve en Afrique de l'Ouest et en Afrique
Centrale (Guinée, Sud du Nigeria, Guinée Equatoriale, Cameroun,
Gabon). (Abdou Bouba, 2009)

Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 9
Figure 1 : plante a. daniellii
Figure 2 : fruits a. daniellii
(Matangouo, 2013) (Matangouo, 2013)
II.1.2. Ethnobotanique et utilisation
Les feuilles d'aframomum daniellii sont
utilisées comme aromates dans les repas. Les tiges et les feuilles sont
utilisées pour la construction des huttes chez les pygmées. Les
fruits sont mangeables et peuvent avoir des propriétés laxatives.
Les graines servent d'une part comme épices au Cameroun et d'autre part
comme appâts dans la pêche (Noumi, 1984). Au Congo, elles sont
employées comme laxatifs ; des rhizomes sont utilisés comme
purgatifs (Bouquet, 1969). Les travaux d'Odukoya et al. (1999)
montrent que les huiles essentielles des graines d'aframomum daniellii
ont une action inhibitrice sur l'enzyme 5-lipoxygénase du soja et
met ainsi en exergue son activité anti-inflammatoire.
II.2. Famille des Rutaceae : fagara xanthoxyloïdes
*Synonymes : zanthoxylum polyganum
Schum, zanthoxylum sénégalense A. Chev, fagara
sénégalensis A. Chev, zanthoxylum
xanthoxyloides.
*Noms vernaculaires: Ngna'a tchou (Ngiemboon)
qui signifie bouche ouverte.
II.2.1. Description
Arbuste atteignant 12 m de hauteur ; cime plus ou moins en
boule ; tronc garni de mamelons ligneux surmontés d'un dard
acéré, rameaux épineux avec des aiguillons crochus
atteignant 1 cm de longueur, de teinte brune. Feuilles alternes, atteignant 20
cm ; rachis garni d'aiguillons ; 5-9 paires de folioles ; limbe atteignant 10 x
4 cm,
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 10
sommet arrondi, emarginé ou garni d'un large mucron
triangulaire, bords souvent retournés vers le dessous et coriaces.
Fleurs pentamères, unisexuées ; calices à lobes
triangulaires ; corolle blanchâtre. Les fleurs mâles ont 5
étamines et pistil rudimentaire, un disque central épais et
convexe à 5 lobes. Quant aux fleurs femelles elles ont un disque
cylindrique peu élevé supportant un carpelle globuleux. Les
fruits (figure 3) sont des follicules subglobuleux d'environ 5mm de
diamètre. La graine, unique par follicule, est bleue sombre et
luisante.

Figure 3 : Fruits de fagara
xanthoxyloïdes (Matangouo, 2013)
II.2.2. Ethnobotanique et utilisations
Les fruits de fagara xanthoxyloïdes sont des
épices indispensables pour la préparation du «Nkui» et
la sauce jaune. C'est une plante qui est considérée comme un
parasiticide polyvalent interne (vermifuge) et externe (plaie suppurante) d'une
activité indéniable (Noumi, 1984).
Pour le traitement des dysenteries, les diarrhées
profuses, les vers intestinaux et les urétérites ; les wolofs
(Sénégal) en font un grand usage. Les préparations des
racines sont très utiles en usage externe pour les plaies suppurantes,
les morsures de serpents. L'écorce des racines à saveur piquante
est sialagogue (augmente la production de la salive) et est prescrite comme
anti-odontalgique (Noumi, 1984). Les feuilles sont également
recommandées pour les stomatites (inflammation de la muqueuse buccale),
les gingivites (inflammation des gencives), les caries. En aromathérapie
contre les migraines et les névralgies (douleurs au niveau des nerfs)
selon diverses modalités (applications sur la tête ou le front)
les feuilles, les écorces des tiges et surtout des
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 11
racines sont utilisées après qu'elles soient
fractionnées et plus ou moins froissées (Kerharo et Adam, 1974).
Selon le professeur Sofowora (Jazet, 1993), la plante empêcherait
l'hémolyse des globules rouges et plus de trente publications ont
précisé l'action anti-drépanocytaire de celle-ci,
c'est-à-dire le pouvoir important qu'elle possède de redonner aux
globules rouges des malades leur forme ronde et de permettre un meilleur apport
d'oxygène. Le principe actif de la plante a été
isolé et des comprimés préparés au Nigeria. Les
travaux d'Issac et al. (1975) montrent qu'il n'existe aucune
toxicité de cette plante.
III GÉNÉRALITÉS SUR LE CALCIUM ET
LE MAGNÉSIUM
III.1. Élément calcium
Le calcium est un élément chimique, de symbole
Ca et de numéro atomique 20.
C'est un métal alcalino-terreux qui ne se trouve jamais
à l'état de corps pur dans la nature. Il est le cinquième
élément le plus abondant de la croûte terrestre (plus de 3
%).
Élément métallique le plus abondant dans
notre organisme, le calcium représente 2% du poids corporel. Il se
concentre à près de 90% dans les os et les dents. La petite
proportion restante joue un rôle primordial au près des cellules
musculaires (celles du coeur entre autres) et nerveuses, en plus de participer
aux fonctions rénales, aux mécanismes de la coagulation sanguine
ainsi qu'à plusieurs processus enzymatiques.
III.1.1. Sources du calcium
Le calcium est présent dans plusieurs aliments de
consommation courante. Les produits laitiers constituent la principale source
de calcium alimentaire (plus des deux tiers des aliments consommés) des
pays occidentaux. Le calcium y est présent sous une forme permettant une
bonne absorption intestinale (de l'ordre de 30 %) et n'augmentant pas
l'excrétion urinaire, permettant finalement une bonne
biodisponibilité. D'autres aliments contiennent du calcium :
épices, eaux minérales, amandes, pistaches, dattes, persil,
cacao, oranges, haricots secs, jaune d'oeuf, graines de sésame, choux,
épinard, certains poissons.
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 12
III.1.2. Absorption du calcium
Le pourcentage d'absorption du calcium varie suivant
l'âge et la nature des aliments. Ainsi, la capacité d'absorber le
calcium devient altérée avec l'âge. Une alimentation trop
riche en fibres s'oppose à l'absorption intestinale, du calcium. La
vitamine D favorise l'absorption du calcium tout d'abord dans le tractus
intestinal, puis au niveau des dents et des os. En fait, la vitamine D augmente
l'absorption du calcium jusqu'à 80%. Le calcium d'origine
végétale est le plus souvent moins absorbable car il est en
grande partie insolubilisé de façon irréversible sous
forme d'oxalates (épinard, cacao). Ainsi l'absorbabilité du
calcium de l'épinard ne dépasserait pas 5%. Pour
l'évaluation de la biodisponibilité réelle, il faut aussi
tenir compte des facteurs alimentaires qui influencent la perte urinaire du
calcium absorbé. Ainsi l'absorption simultanée de phosphore
diminue l'excrétion urinaire de calcium. A l'opposé, les
composants «acidogènes » du régime, comme les sulfates
(en particulier dans les eaux minérales sulfatées calciques),
augmentent la calciurie (élimination de calcium par voie urinaire).
III.1.3. Importance du calcium dans l'organisme
Le calcium est majoritairement entreposé dans les os,
dont il fait partie intégrante. Le calcium joue aussi un rôle
essentiel dans la coagulation sanguine, le maintien de la pression sanguine et
la contraction des muscles du coeur. De plus, il intervient dans les
échanges cellulaires et est, de ce fait, vital. Son taux sanguin
(calcémie) est extrêmement régulé, pour
éviter des variations fatales à l'organisme. Le calcium
intervient dans la contraction musculaire par l'intermédiaire de l'ion
calcium Ca2+. Le calcium est stocké dans le muscle dans des
citernes et est libéré sous l'influx nerveux pour activer les
molécules d'actine qui vont permettre la contraction musculaire. Le
calcium est un activateur d'enzyme, agit comme promoteur de structuration
(stabilisation de la structure des protéines) et acide de Lewis.
Ca2+ est présent sous forme d'hydroxyapatite
(Ca5(PO4)3OH) constituant majeur des os et des dents (biomatériaux de
structures dures).
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 13
Le tableau I donne quelques indications sur les apports
journaliers conseillés en France
Tableau I: Apports conseillés en calcium en
mg par jour. (
www.servicevie.com/02Sante/Dossier/
Dossier30103684.html)
|
Enfants de 1 à 3 ans
|
500
|
|
Enfants de 4 à 9 ans
|
800
|
|
Adolescents de 10 à 14 ans
|
1200
|
|
Adolescents de 15 à 18 ans
|
1200
|
|
Adultes
|
900
|
|
Femmes de plus de 55 ans
|
1200
|
|
Hommes de plus de 65 ans
|
1200
|
|
Femmes enceintes
|
1000
|
|
Femmes allaitantes
|
1000
|
|
Femmes après allaitement
|
1000
|
Nos besoins en calcium devraient pouvoir être couverts
par notre alimentation mais l'on a parfois besoin des additifs pour combler des
carences inévitables.
III.1.4. Symptômes d'un manque en calcium Les
symptômes les plus courants sont les suivants :
? Fragilisation osseuse
? Déminéralisation osseuse au profit des autres
besoins en calcium de l'organisme entraîne une perte progressive et
accélérée du capital accumulé.
? Risque de fracture augmenté (poignet,
fémur...)
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 14
Les symptômes les plus sévères sont les
suivants :
? Tétanie ? Spasme
? Troubles cardiaques
III.2. Élément magnésium
Le magnésium est un élément chimique, de
symbole Mg et de numéro atomique 12
Le magnésium, profondément lié au
calcium, puisqu'il assure sa fixation, est l'un des principaux aliments de la
cellule nerveuse. Le magnésium est le 8e
élément le plus répandu sur notre planète (2% de la
croûte terrestre ; 1,25g/l dans la mer). Il est présent
dans tous les organismes vivants, végétaux (chlorophylle),
animaux et chez l'homme. C'est un minéral essentiel, non
synthétisé, ni transformé dans l'organisme, et dont tout
l'apport est d'origine externe. Le magnésium est un minéral
essentiel au bon fonctionnement de l'organisme humain. Il participe à
plus de 300 réactions métaboliques dans le corps.
III.2.1. Sources du magnésium
Dans le tableau II suivant, sont listées les masses de
magnésium contenues dans 100g de quelques aliments. (
www.Wikipedia.org)
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 15
Tableau II : Valeurs magnésiques de
quelques aliments. (
www.Wikipedia.org)
|
Aliments
|
Masse en mg de Mg pour 100g
|
|
Fruits de mer
|
410
|
|
|
Mélasse
|
197
|
- 242
|
|
Cacao
|
150
|
- 400
|
|
Céréales
|
100
|
- 150
|
|
Epinards
|
50 - 100
|
|
Poisson
|
25 - 50
|
Quelques autres aliments contenant du magnésium :
épices, légumes verts, fèves, amandes, banane, graines de
maïs, pomme de terre, arachides.
III.2.2. Absorption du magnésium
Le magnésium est un élément dont ont
besoin toutes les cellules de notre corps. La moitié du magnésium
dans le corps humain se trouve dans les cellules des tissus et des organes et
l'autre moitié est combinée avec le calcium pour faciliter son
absorption.
III.2.3. Importance du magnésium dans
l'organisme
Le magnésium est impliqué dans l'énergie
du métabolisme du corps humain et dans la synthèse des
protéines. Le corps humain a besoin du magnésium pour le
métabolisme du calcium, de la vitamine C, du sodium et du phosphore. Le
magnésium active les enzymes impliquées dans la conversion du
sucre du sang en énergie.
Le magnésium aide le corps humain dans le combat de la
dépression, favorise un système cardio-vasculaire plus sain, aide
dans la prévention des crises cardiaques, apporte le soulagement de
l'indigestion, lutte contre le stress.
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 16
Les besoins en magnésium varient en fonction de
l'âge et du sexe. Ils augmentent particulièrement chez les femmes
enceintes, les femmes allaitantes et chez les personnes âgées. En
cas d'activités physiques intenses, les besoins sont aussi plus
élevés car la sueur entraîne une élimination
importante de magnésium. Le tableau III regroupe quelques masses de
magnésium conseillées selon l'âge par l'agence
française de Sécurité Sanitaire des aliments,
3e édition, Ed. Tec & Doc.
Tableau III : Apports conseillés en
magnésium en mg par jour.
(
www.servicevie.com/02Sante/Dossier/
Dossier30103600.html)
|
Enfants de 1 à 3 ans
|
80
|
|
Enfants de 4 à 6 ans
|
130
|
|
Enfants de 6 à 9 ans
|
200
|
|
Enfants de 10 à 12 ans
|
280
|
|
Adolescents de 13 à 16 ans
|
370
|
|
Adolescents de 16 à 19 ans
|
410
|
|
Adolescentes de 16 à 19 ans
|
370
|
|
Hommes adultes
|
420
|
|
Femmes adultes
|
360
|
|
Femmes enceintes (3e trimestre)
|
400
|
|
Femmes allaitantes
|
390
|
|
Hommes de plus de 65 ans
|
420
|
|
Femmes de plus de 55 ans
|
360
|
|
Personne de plus de 75 ans
|
400
|
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 17
III.2.4. Symptômes d'un manque en
magnésium
Le déficit en magnésium entraîne la
fragilité des dents exposées à la carie, des ongles qui
deviennent cassantes. Dans le cas de carie dentaire, le calcium n'a que peu
d'influence, alors que l'influence du magnésium est
prédominante.
D'autres symptômes sont :
? hyperexcitabilité neuromusculaire : crises de
tétanie se caractérisant par la contracture des membres
supérieurs et du visage ;
? troubles immunologiques ; atteintes cardio-vasculaires et,
dans les cas extrêmes, infarctus ;
? fatigabilité musculaire ; irritabilité,
nervosité, insomnie ; ? troubles digestifs : diarrhées,
nausées ;
? crampes, tremblements ;
III .3 Dosage des ions calcium et magnésium
III.3.1. Dosage des ions calcium
Pour doser le calcium dans une solution, on utilise comme
indicateur coloré de l'ion Ca2+ le réactif de Patton
et Reeder, et on comme agent complexant le sel de l'EDTA.
Considérons une certaine quantité d'ions
Ca2+ se trouvant en solution aqueuse. Si on ajoute du réactif
de Patton et Reeder (RPR) à cette solution, il se forme en milieu
basique un complexe rouge :
Ca2+ + PR (bleu) [Ca-PR] 2+ (rouge)
Si on ajoute de petites quantités d'EDTA à cette
solution, l'ion H2Y2- réagit avec Ca2+ pour donner
un complexe plus stable en milieu alcalin :
[Ca-PR] 2+ (rouge) + H2Y2-
CaY2- + PR (bleu) + 2H+
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 18
Cette équation s'écrit simplement :
Ca2+ + H2Y2- CaY2- +
2H+
Tant qu'il reste du Ca2+ libre dans la solution,
celle-ci reste rouge. À partir du moment où l'on a ajouté
suffisamment de H2Y2- pour que tout le calcium soit passé
à l'état de complexe CaY2-, le réactif de
Patton et Reeder libéré reprend sa couleur bleue à ce pH.
La fin du dosage est donc mise en évidence par le virage de la solution
du rouge vineux au bleu.
III.3.2. Dosage des ions magnésium
En milieu légèrement basique, le
magnésium réagit avec l'EDTA pour donner un complexe stable
suivant l'équation :
Mg2+ + H2Y2- MgY2- +
2H+
La fin de la réaction est observée au moyen d'un
indicateur de concentration de Mg2+, le noir eriochrome T (NET) qui
est rouge vineux en présence de Mg2+ et bleu en son absence
(à pH 10). En effet, en absence de l'EDTA, les ions Mg2+
réagissent sur le NET selon la réaction suivante :
Mg2+ + NET (bleu) [Mg-NET] 2+ (rouge)
L'ajout de la solution de l'EDTA dans la solution se traduit
par la formation d'un complexe stable entre ce ligand et les ions
Mg2+ selon le schéma :
[Mg-NET] 2+ (rouge) + H2Y2-
MgY2- + NET (bleu) + 2H+
III.3.3 Dosage des ions calcium et magnésium
dans la même solution
On réalise un premier dosage en milieu alcalin en
éliminant de la solution les ions Mg2+ selon la
réaction de précipitation suivante :
Mg2+ + 2OH- Mg(OH) 2 (S)
On dose ensuite le calcium restant avec la solution de l'EDTA
en présence du réactif de Patton et Reeder.
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 19
Un deuxième dosage effectué en présence
du NET (qui est un indicateur des deux ions Mg2+ et Ca2+)
en milieu ammoniacal permet de doser la somme (Mg2+ +
Ca2+) car le complexe Ca(II) est plus stable que celui de Mg(II).
On peut également éliminer de la solution les
ions Ca2+ en les précipitant sous forme d'oxalate de calcium
conformément à l'équation :
Ca2+ + C2O42- CaC2O4 (S)
CHAPITRE II :
MATÉRIAUX, MATÉRIEL,
|
|
|
RÉACTIFS ET MÉTHODES
|
|
|
|
|
EXPÉRIMENTALES
|
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 21
Ce chapitre nous présente successivement les
matériaux, le matériel, et les méthodes
expérimentales utilisées.
I. MATÉRIAUX
I.1. Origine
Dans le présent travail, les échantillons
d'épices d'Aframomum daniellii et de Fagara
xanthoxyloïdes sont achetés sur le marché de Dschang,
chef-lieu du département de la Menoua, région de l'Ouest
Cameroun.
I.2. Conditionnement
Les épices sont séchées jusqu'à
poids constant, puis écrasées, tamisées et stockées
en lot de 50g dans des bocaux en verre pour les différentes analyses.
II. MATÉRIEL
En dehors de la verrerie courante de laboratoire
(éprouvette, pipette, fiole jaugée, bécher, burette
à zéro automatique...), nous avons utilisé :
· Un Moulinex à sec ;
· Un agitateur ;
· Des bouteilles plastiques ;
· Un tamis de la ménagère ;
· Une balance de précision 10-1 g.
III. RÉACTIFS UTILISÉS
· Poudres d'épices d'Aframomum daniellii et
de Fagara xanthoxyloïdes.
· Solution d'acide chlorhydrique 0,1M préparé
à partir de HCl 33%
· Solution d'EDTA 0,0083M, préparée à
partir de l'EDTA disodique de pureté 98%.
· Tampon ammoniacal (T.A) préparé à
partir des cristaux de chlorure d'ammonium et de la solution d'ammoniaque.
· Indicateur métallochrome noir Eriochrome
T(NET)
· Eau distillée
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
22
IV. MÉTHODE EXPÉRIMENTALE
Pour notre travail, nous avons utilisé la technique
des dosages complexométriques pour la détermination du titre
total en ions calcium et magnésium, pour les raisons
d'accessibilité et de mise en oeuvre facile.
IV.1. Principe
Le principe consiste en un tirage direct de la
totalité des ions alcalino-terreux (Ca2+ et Mg2+)
à partir de l'EDTA comme agent complexant, suivant la réaction ci
- dessous :
2H2Y2- + Ca2+ + Mg2+
MgY2- + CaY2- + 4H+
Le dosage effectué avec l'EDTA en présence du
NET en milieu ammoniacal permet de doser la somme Mg2+ +
Ca2+ car le complexe de Ca2+ est plus stable que celui de
Mg2+ ; et le NET est à la fois indicateur de concentration de
Mg2+ et de Ca2+ en milieu ammoniacal, pH # 9,2.
IV.2 Mode opératoire
Dans un réacteur, 500mL de HCl 0,1M ou d'eau
distillée et 50g de poudre d'épices sont introduits. Après
agitation à des intervalles de temps de 30min, 1h, 1h30min, 2h, 2h30min,
3h, 6h, 9h, 12h, un prélèvement de 5mL de suspension est
effectué.
Aux 5mL de suspension préalablement
prélevés, on ajoute 5mL de tampon ammoniacal et une pincée
de NET. On fait descendre progressivement dans cette solution l'EDTA 0,0083M
contenue dans la burette à zéro automatique.
Le point équivalent est repéré par le
virage de la solution du rouge vineux au bleu. Le volume d'EDTA noté est
celui nécessaire pour doser le mélange Ca2+ +
Mg2+. Ce protocole peut être résumé par les
organigrammes des figures 4 et 5.
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
23
50g d'épices
|
1°) 500mL de HCl 0,1M
2°) 500mL d'eau
distillée
|
|
|
Mélanger dans un réacteur de 1500mL, fermer
puis
homogénéiser
Attendre 30min, 1h, 1h30min, 2h, 2h30min, 3h, 6h, 9h, 12h
Prélever 5mL de suspension et doser par l'EDTA en
milieu
tampon ammoniacal, en présence du NET, puis
homogénéiser
avant la 2ème prise
Noter le volume d'EDTA au point équivalent qui est
repéré par
le virage de la solution du rouge vineux au bleu
Figure 4 : Organigramme du mode
opératoire pour la détermination des titres totaux en ions
Ca2+ et Mg2+
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
24
50g d'épices
|
|
1°) 500mL de HCl 0,1M 2°) 500mL d'eau
distillée
|
|
|
|
|
|
|
|
Mélanger dans un bocal en verre de 500mL, puis
soumettre le
mélange à l'agitation constante de l'agitateur
Attendre 30min, 1h, 1h30min, 2h, 2h30min, 3h, 6h, 9h, 12h
Prélever 5mL de suspension et doser par l'EDTA en
milieu
tampon ammoniacal, en présence du NET, puis
homogénéiser
avant la prise suivante
Noter le volume d'EDTA au point équivalent qui est
repéré par
le virage de la solution du rouge vineux au bleu
Figure 5 : Organigramme du mode
opératoire pour la détermination des titres totaux en ions
Ca2+ et Mg2+ lorsque la suspension est agitée.

CHAPITRE III :
RÉSULTATS ET
INTERPRÉTATION
Mémoire de DIPES II présenté par MATANGOUO
SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 26
I. RÉSULTATS
Les volumes d'EDTA obtenus au point équivalent ont
permis de calculer les concentrations totales en ions Ca2+ et
Mg2+ contenus dans 50 g d'épices et les résultats sont
consignés dans les tableaux IV, V, VI et VII. Les figures 6, 7, 8 et 9
donnent les représentations graphiques.
Tableau IV : Concentrations molaires totales en ions
Ca2+ et Mg2+ d'aframomum daniellii en fonction
du solvant et du temps d'extraction.
Solvant
|
Temps (heures)
|
VEDTA (mL)
|
([Ca2+]+[Mg2+])×
10-3mol/L
|
|
0,5
|
3,2 #177; 0,1
|
5,4 #177; 0,2
|
Eau distillée
|
1
|
3,6 #177; 0,1
|
6,1 #177; 0,2
|
|
1,5
|
3,7 #177; 0,1
|
6,3 #177; 0,2
|
|
2
|
3,9 #177; 0,1
|
6,7 #177; 0,2
|
|
2,5
|
4,1 #177; 0,1
|
7,1 #177; 0,2
|
|
3
|
4,5 #177; 0,1
|
7,9 #177; 0,2
|
|
6
|
4,4 #177; 0,1
|
7,8 #177; 0,2
|
|
9
|
4,7 #177; 0,1
|
8,4 #177; 0,3
|
|
12
|
4,8 #177; 0,1
|
8,6 #177; 0,3
|
|
0,5
|
5,9 #177; 0,1
|
9,9 #177; 0,2
|
|
1
|
6,3 #177; 0,1
|
10,7 #177; 0,2
|
HCl 0,1 N
|
1,5
|
6,6 #177; 0,1
|
11,3 #177; 0,3
|
|
2
|
6,5 #177; 0,1
|
11,2 #177; 0,3
|
|
2,5
|
6,8 #177; 0,1
|
11,8 #177; 0,3
|
|
3
|
6,8 #177; 0,1
|
12,0 #177; 0,3
|
|
6
|
6,7 #177; 0,1
|
11,9 #177; 0,3
|
|
9
|
6,9 #177; 0,1
|
12,4 #177; 0,3
|
|
12
|
6,9 #177; 0,1
|
12,5 #177; 0,3
|
|
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
27
Tableau V : Concentrations totales en ions
Ca2+ et Mg2+ d'aframomum daniellii sous
agitation constante en fonction du solvant et du temps
d'extraction.
Solvant
|
Temps (heures)
|
VEDTA (mL)
|
([Ca2+]+[Mg2+]) x10-3 mol/L
|
|
0,5
|
4,1 #177; 0,1
|
6,9 #177; 0,2
|
|
1
|
4,3#177; 0,1
|
7,3 #177; 0,2
|
Eau distillée
|
1,5
|
4,4#177; 0,1
|
7,5 #177; 0,2
|
|
2
|
4,4#177; 0,1
|
7,6 #177; 0,2
|
|
2,5
|
4,6#177; 0,1
|
8,0 #177; 0,2
|
|
3
|
4,8#177; 0,1
|
8,4 #177; 0,2
|
|
6
|
4,7#177; 0,1
|
8,4 #177; 0,3
|
|
9
|
4,9#177; 0,1
|
8,8 #177; 0,3
|
|
12
|
4,9#177; 0,1
|
8,9 #177; 0,3
|
|
0,5
|
6,7#177; 0,1
|
11,2 #177; 0,2
|
|
1
|
6,8#177; 0,1
|
11,5 #177; 0,3
|
HCl 0,1 N
|
1,5
|
7,1#177; 0,1
|
12,1 #177; 0,3
|
|
2
|
7,1#177; 0,1
|
12,3 #177; 0,3
|
|
2,5
|
7,5#177; 0,1
|
13,1 #177; 0,3
|
|
3
|
7,8#177; 0,1
|
13,7 #177; 0,3
|
|
6
|
7,7#177; 0,1
|
13,6 #177; 0,3
|
|
9
|
7,6#177; 0,1
|
13,7 #177; 0,3
|
|
12
|
7,6#177; 0,1
|
13,8 #177; 0,3
|
|
Tableau VI : Concentrations molaires totales en ions
Ca2+ et Mg2+ du fagara xanthoxylïodes en
fonction du solvant et du temps d'extraction.
Solvant
|
Temps (heures)
|
VEDTA (mL)
|
([Ca2+]+[Mg2+]) X10-3 mol/L
|
|
0,5
|
2,9 #177; 0,1
|
4,9 #177; 0,2
|
|
1
|
3,0#177; 0,1
|
5,1 #177; 0,2
|
Eau distillée
|
1,5
|
3,3#177; 0,1
|
5,6 #177; 0,2
|
|
2
|
3,4#177; 0,1
|
5,9 #177; 0,2
|
|
2,5
|
3,7#177; 0,1
|
6,4 #177; 0,2
|
|
3
|
3,8#177; 0,1
|
6,7 #177; 0,3
|
|
6
|
4,1#177; 0,1
|
7,2 #177; 0,3
|
|
9
|
4,0#177; 0,1
|
7,1 #177; 0,3
|
|
12
|
4,1#177; 0,1
|
7,4 #177; 0,3
|
|
0,5
|
6,9#177; 0,1
|
11,6 #177; 0,3
|
|
1
|
7,1#177; 0,1
|
12,0 #177; 0,3
|
HCl 0,1 N
|
1,5
|
7,2#177; 0,1
|
12,3 #177; 0,3
|
|
2
|
7,5#177; 0,1
|
12,6 #177; 0,3
|
|
2,5
|
7,6#177; 0,1
|
12,7 #177; 0,3
|
|
3
|
7,9#177; 0,1
|
12,8 #177; 0,3
|
|
6
|
8,1#177; 0,1
|
12,9 #177; 0,3
|
|
9
|
8,3#177; 0,1
|
12,9 #177; 0,3
|
|
12
|
8,2#177; 0,1
|
13,0 #177; 0,3
|
|
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
28
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
29
Tableau VII : Concentrations totales en ions
Ca2+ et Mg2+ du fagara xanthoxylïodes sous
agitation constante en fonction du solvant et du temps
d'extraction.
Solvant
|
Temps (heures)
|
VEDTA (mL)
|
([Ca2+]+[Mg2+]) x10-3 mol/L
|
|
0,5
|
3,4#177; 0,1
|
5,7 #177; 0,2
|
|
1
|
3,6#177; 0,1
|
6,1 #177; 0,2
|
Eau distillée
|
1,5
|
3,7#177; 0,1
|
6,3 #177; 0,2
|
|
2
|
3,9#177; 0,1
|
6,7 #177; 0,2
|
|
2,5
|
4,0#177; 0,1
|
7,0 #177; 0,2
|
|
3
|
4,3#177; 0,1
|
7,5 #177; 0,3
|
|
6
|
4,2#177; 0,1
|
7,4 #177; 0,3
|
|
9
|
3,9#177; 0,1
|
7,0 #177; 0,3
|
|
12
|
3,8#177; 0,1
|
6,9 #177; 0,3
|
|
0,5
|
7,3#177; 0,1
|
12,2 #177; 0,3
|
|
1
|
7,6#177; 0,1
|
12,9 #177; 0,3
|
HCl 0,1 N
|
1,5
|
7,8#177; 0,1
|
13,3 #177; 0,3
|
|
2
|
8,2#177; 0,1
|
14,1 #177; 0,3
|
|
2,5
|
8,3#177; 0,1
|
14,4 #177; 0,3
|
|
3
|
8,7#177; 0,1
|
14,8 #177; 0,3
|
|
6
|
8,8#177; 0,1
|
15,1 #177; 0,3
|
|
9
|
8,8#177; 0,1
|
15,5 #177; 0,3
|
|
12
|
8,9#177; 0,1
|
15,7 #177; 0,3
|
|
H2O HCl
([Ca2+]+[Mg2+])×10-3mol/L
|
14 12 10 8 6 4 2 0
|
|
|
|
0 2 4 6 8 10 12 14
|
|
Temps (heures)
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
30
Figure 6 : Évolution de la
concentration en ions Ca2+ et Mg2+ d'aframomum
daniellii en fonction du solvant et du temps d'extraction.
H2O HCl
([Ca2+]+[Mg2+])×10-3mol/L
|
16 14 12 10 8 6 4 2 0
|
|
|
0 2 4 6 8 10 12 14
Temps (heures)
Figure 7 : Évolution de la
concentration en ions Ca2+ et Mg2+ d'aframomum
daniellii en fonction du solvant sous agitation constante et du temps
d'extraction.
H2O HCl

0 2 4 6 8 10 12 14
Temps(heures)
14
12
10
8
6
4
2
9[Ca2+]+[Mg2+])×10-3mol/L
0
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
31
Figure 8 : Évolution de la
concentration en ions Ca2+ et Mg2+ du fagara
xanthoxylïodes en fonction du solvant et du temps d'extraction.
0 2 4 6 8 10 12 14
Temps(heures)
|
16
|
|
|
|
|
|
([Ca2+]+[Mg2+])×10-3mol/L
|
14 12 10 8 6 4 2 0
|
|
|
|
|
|
|
|
|
|
|

H2O HCl
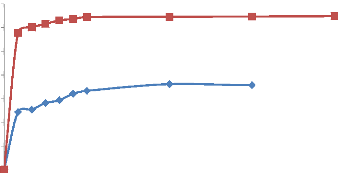
Figure 9 : Évolution de la
concentration en ions Ca2+ et Mg2+ du fagara
xanthoxylïodes en fonction du solvant sous agitation constante et du
temps d'extraction.
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 32
II. INTERPRÉTATION
Les résultats des tableaux IV, V, VI et VII montrent
que le volume d'EDTA nécessaire pour doser les ions calcium et
magnésium contenus dans 50 g de poudre d'épices varie en fonction
du temps de macération des épices.
L'allure de l'évolution des courbes
représentant les concentrations totales en ions Mg2+ et
Ca2+ en fonction du solvant, de l'agitation et du temps d'extraction
permet de dégager les tendances suivantes :
? Entre 0 et 30 min (0,5 heure), l'extraction est une
fonction linéaire du temps quelles que soient les conditions
expérimentales (solvant, effet de l'agitation).
? L'extraction est plus importante dans l'acide chlorhydrique
que dans l'eau distillée.
? L'extraction est plus importante lorsque la suspension est
agitée constamment.
? Après un temps d'extraction maximale, la
concentration en ions calcium et magnésium reste constante (13,6 mmol/L
et 15,1 mmol/L respectivement pour aframomum daniellii et pour
fagara xanthoxyloïdes) et a tendance à diminuer dans
certains cas. Cette diminution pourrait être due au
phénomène d'adsorption.
Les quantités de matière d'ions
Ca2++Mg2+ obtenues par Tchiégang et Mbougueng
(2005) sont systématiquement plus élevées (40,7 mmol pour
aframomum daniellii et 31,5 mmol pour fagara
xanthoxyloïdes) que celles obtenues dans nos différentes
épices avec des valeurs de 13,6 mmol et 15,1 mmol respectivement pour
aframomum daniellii et pour fagara xanthoxyloïdes. Ceci
pourrait s'expliquer par le fait que dans nos suspensions on ne trouve que les
ions libres ou libérés alors que Tchiégang et Mbougueng
(2005) intègrent le magnésium calcium et le liés en
calcinant ces épices à 550o C. En effet, le calcium et
le magnésium se trouvent dans les fibres organiques des épices
sous forme d'oxalates ou de phtalates plus ou moins solubles selon les
solvants. Leur calcination conduit à la libération totale du
calcium et du magnésium.

INTÉRÊTS
PÉDAGOGIQUES
Ce travail de recherche nous a permis de développer des
compétences nouvelles entre autres :
· La maitrise des techniques complexométriques ;
· Le dosage acido-basique ;
· L'identification des ions ;
· La préparation des solutions ;
· La maitrise de l'outil informatique ;
· L'esprit critique ;
· L'ouverture d'esprit ;
· La recherche de l'information, chose indispensable pour
les enseignants.
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
34

CONCLUSION
Mémoire de DIPES II présenté
par MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013
36
Cette étude avait pour but de déterminer par
complexométrie l'apport calcique et magnésique des extraits
à l'eau et à l'acide chlorhydrique 0,1M de l'aframomum
daniellii et du fagara xanthoxyloïdes (épices
consommées au Cameroun), il ressort que :
· après 3 heures de temps de macération, on
tend progressivement vers une extraction maximale (13,6 mmol et 15,1 mmol
respectivement pour aframomum daniellii et pour fagara
xanthoxyloïdes).
· les concentrations en ions Ca2+ et
Mg2+ sont plus élevées avec l'acide chlorhydrique
comme solvant d'extraction qu'avec l'eau distillée.
· les concentrations en ions Ca2+ et
Mg2+ sont plus élevées lorsque la suspension est
agitée.
· fagara xanthoxyliodes est plus riche en ions
alcalino-terreux (15,1 mmol/L) qu'aframomum daniellii (13,6
mmol/L).
Dans le souci d'améliorer ce travail, nous proposons,
pour les recherches futures, les travaux suivants :
· Effectuer l'extraction à chaud, afin de voir
l'influence de la température.
· Déterminer la teneur de ces épices en
d'autres éléments tels que le fer et le phosphore.
· Calciner ces épices afin de déterminer les
concentrations totales en ions calcium et magnésium.
RÉFÉRENCES
BIBLIOGRAPHIQUES
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 38
Abdou Bouba Armand (2009). Contribution
à l'étude du développement d'un aliment fonctionnel
à base d'épices du Cameroun : caractérisation
physico-chimique et fonctionnelle. Thèse de Doctorat, ENSAI
Ngaoundéré, 288 p.
Bouquet (1969). Féticheurs et
médecine traditionnelle du Congo (Brazzaville). ORSTOM, Paris (France),
36: 282-294.
Groff J. and Gropper S. (2000). Advanced
nutrition and human metabolism, 3rd Ed. Belmont: Wadsworth.
Hertog M. G. L., Feskens E. J. M., Hollman P. C. H.,
Katan M. B. and Kromhout D. (1993). Dietary antioxidant flavonoids and
risk of coronary heart disease: the zupthen elderly study. The lancet 342:
1007-1014.
Issac S. W. A., Sofowora E. A., Williams A. O., Marquis
V. O., Adekunle A. A. and Anderson C. O. (1975). Extract of Fagara
xanthoxyloides roots in sickle cell anemia. Acta haematological, 53 p.
Jazet Dongmo P. M. (1993). Extraction et
analyse des huiles essentielles de deux plantes aromatiques et à
épices de la famille des rutacées : Zanthoxylum leprieurii
Guill et Perr et Zanthoxylum xanthoxyloides Watern.
Mémoire de maîtrise, Université de Yaoundé I, 46
p.
Kerharo J. et Adam J. G. (1974). La
pharmacopée Sénégalaise traditionnelle, plantes
médicinales et toxiques, Vigot frères, Paris 712 p.
Nevellier P. et Jolivet H. (1965). Epices,
aromates, herbes et condiments. Modificateurs des caractères
organoleptiques des denrées. Annale de la nutrition et de
l'alimentation, 19(5), 449-480.
Noumi E. (1984). Les plantes à
épices, à condiments et à aromes du Cameroun :
Thèse de Doctorat 3e cycle en sciences biologiques.
Faculté des sciences, Université de Yaoundé, Cameroun, 165
p.
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 39
Odukoya O. A., Houghton P. J. and Raman A.
(1999). Lipoxygenase inhibitors in the seeds of Aframomum
daniellii. Phytomedecine, Int. J. Phytother. Pharmacol. , 6(4), 251256.
Tchiégang C. et Mbougueng D. (2005).
Composition chimique des épices utilisées dans la
préparation du Nah poh et du Nkui de l'Ouest Cameroun.
Tropicultura. 23,4. 193-200.
Youmbi Y. B. (2011). Contribution à
l'étude de l'apport calcique et magnésique de Tetrapleura
Tetraptera et Afrostyrax Kamerunensis (épices
consommées au Cameroun). Mémoire de DIPES II, ENS
Yaoundé.
Yangoue P. (2008). Techniques
complexométriques : application à l'étude de l'apport
calcique et/ou magnésique de quelques épices consommées au
Cameroun. Mémoire de DIPES II, ENS Yaoundé.
http://www.wikipedia.org/épice
(consulté le 12 Novembre 2012).
http://www.servicevie.com/02Sante/Dossier/Dossier30103684.html
(consulté le 12 Novembre 2012).
http://www.servicevie.com/02Sante/Dossier/Dossier30103600.html
(consulté le 12 Novembre 2012).

ANNEXES
Annexes I : Préparation des solutions
1 Préparation de 3 L d'une solution d'EDTA de
concentration 0,0083M
La masse molaire de l'EDTA est 372,25 g/mol
? Masse d'EDTA à peser pour préparer 1 L d'une
solution de 0,025M
? On prépare 1 L de la solution en introduisant 9,306g
d'EDTA dans une fiole
jaugée de 1000mL, puis on complète avec de l'eau
distillée jusqu'au trait de
jauge et on homogénéise.
? Ensuite, dans un récipient on ajoute à la
solution préparée 2 L d'eau distillée à
l'aide de la fiole jaugée de 1000 mL pour obtenir la
solution de 3 L d'EDTA
0,0083 M.
P? ?100?m
P ? m
m
0 0
? p = =
m = p x
V
0 0
100 V 0
2 Préparation d'un litre d'une solution de tampon
ammoniacal
On dispose d'une solution commerciale de NH3 28%. ?? =
0,597??/??
Soient m0 la masse de la solution, m
la masse du soluté, ?? la densité de la
solution
? m ?
??P?V
0
m
m0
n= =
C ?
V
0 0
M NH 3
or
?
1000???P
100 NH ? M
3
C0 ?
m
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 41
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 42
Dilution au 5ème de la solution
V =114 mL ? ? =
1 2
?
V 570ml
On dissout 60 g de chlorure d'ammonium (NH4Cl) dans un minimum
d'eau dans une fiole jaugée de 1000mL, on y ajoute 570 mL d'ammoniaque
concentrée (1,96 mol/L) et on ajuste avec l'eau distillée
jusqu'au trait de jauge.
3 Préparation d'une solution d'acide chlorhydrique
0,1 M
On dispose d'une solution commerciale de HCl 37% p =
1,18??/??
? Calcul de la concentration C0 de cette
solution Considérons un volume de la solution V0 = 1000
mL
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 43
Soient m0 la masse de la solution, m
la masse du soluté, ?? la densité de la solution Le
pourcentage massique P = 37%.
Or
? Calcul du volume V0 d'acide nécessaire
pour préparer 5 L de HCl 0,1M
Equation de dilution
=
CV
1 1
C0
C V = CV =
V
0 0 1 1 0
0,1 x 5000
A . N :
V = = 42 mL
0 11,96
? Le volume Ve d'eau à ajuster
On introduit 42 mL de HCl 11,96 M dans une fiole jaugée
de 1000 mL, on complète avec de l'eau distillée jusqu'au trait de
jauge, on le retourne dans une bonbonne de 5 L ; on complète ensuite
avec de l'eau distillée, quatre (04) fois avec la fiole jaugée de
1000 mL.
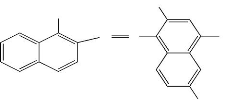
Annexe II Formules semi-développées du
NET et de l'EDTA
1 Noir d'Eriochrome T:
3-Hydroxy-[1-hydroxy-(2-naphtalenyl) azo] 7-nitro-naphtaleno-sulfonate
de sodium
SO3Na
OH
N N
NO2
HO
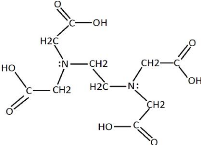
2 Éthylène diamine tétra
acétique
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 44
Annexe III : Calcul des concentrations
|
1
|
2
|
3
|
...
|
9
|
|
|
|
|
...
|
|
|
5
|
5
|
5
|
...
|
5
|
|
V 1000
p
|
V 1000
p
|
V 1000
p
|
...
|
|
|
|
|
|
...
|
|
|
|
|
|
...
|
|
|
|
|
|
|
r 1
C V
|
r 1
C V
|
r 1
C V
|
...
|
? ?
C V
|
|
E 1
? ? ? ?
V V V
? ?
0 p 1
1000 ? ? V p ? ?
|
E 2
? ? 2 ) + + ?
V V V V
?
0 p 1 2
1000 ? ? V
p ? ?
|
E 3
? ? 3 ? ? ?
V V V V V ?
? ?
0 p 1 2 3
1000 ? ? V p ? ?
|
E 9
? ? 9 ? ? ? V
V V V ?
? ?
0 1 .... 9
p
1000 ? ? V p ? ?
|
|
|
|
|
...
|
|
|
|
|
|
...
|
|
|
? ?
C V
E 1
? ? ? ?
V V V
? ?
0 p 1
V V V
0 ? ? ?
p p ? ?
|
C r V ?
E 2
? ?
V 2 V ? V ?
V ?
? ?
0 p 1 2
V 2 V V
0 ? ? ?
p p ? ?
|
C r V ?
E ? ?
V 3 V ? V ?
V ? V ?
3 ? ?
0 1 2 3
p
V 3 V V
0 ? ? ?
p p ? ?
|
C ? V ?
E 9
? ? ? V
V 9 V ? V ?
?
? ?
....
0 1 9
? ? p
9
V V V
0 p ? p ? ?
|
|
|
|
|
...
|
|
|
|
|
|
Ct
s
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 45
est le volume prélevé.
Vst est le volume de la solution
à un instant t.
Ct est la concentration des ions et dans le
volume prélevé.
n, est le nombre de moles des ions et restants.
nP est le nombre de moles des ions et dans
l'échantillon à doser.
nt est le nombre de moles total des ions et
en solution à un instant t du
dosage.
Cs est la concentration totale des ions et en solution
à un instant t du
dosage.
? VE ? 0,1 mL
Annexe IV : Calcul de
Au point équivalent
s
C . V
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 46
? ?
V
s
t t t E E
C V C V C V
. ? . ? ?
E E s s s t
? ?
C . V
E E
ln C t t t
ln ln ln . ? ln
s ? ? ? ? C ? C V
V
t s E E s
?lnC t ln t
? C
?lnV ?lnV
s E E s
?
t t t t
dC dC dV dV ? C ?C
?V ?V
s E E s s E E s
? ? ? ? ? ? ?
Ct CE VE Vt Ct CE VE Vt
s
? V
|
Or
|
|
0
|
|
CE
|
|
?
|
? CE
V
E s
C s C s
V t
? V
E s ?
|
|
V
? ? ? ? ?
t t ? ? ? ?
t 1
Avec =
Vt 300
|
t
et
|
Mémoire de DIPES II présenté par
MATANGOUO SONKOUE Baudelaire E.N.S Yaoundé 2012/2013 47
Annexe V : Épices et condiments de la sauce
jaune et du Nkui
|
Noms scientifiques
|
Noms français et descriptif
|
Partie utilisée
|
|
Aframomum daniellii
|
Maniguette sucrée
|
Fruit
|
|
Aframomum sulcatum
|
Maniguette des singes
|
Fruit
|
|
Dorstensia psilurus
|
Chasse serpent
|
Racine
|
|
Echinops giganteus
|
Racine tubéreuse
|
Racine
|
|
Fagara leprieurii
|
Grappe odoriférante
|
Fruit
|
|
Fagara xanthoxyloïdes
|
Bouche béante
|
Fruit
|
|
Hypodaphnis zenkeri
|
Ecorce rouge
|
Ecorce
|
|
Mondia whitei
|
Racine sucrée
|
Racine
|
|
Pentadiplandra brazzeana
|
Liane blanche
|
Racine
|
|
Piper guineesse
|
Poivier
|
Fruit
|
|
Scleria striatinux
|
Racine de chaume
|
Rhizome
|
|
Scorodophloeus zenkeri
|
Arbre à ail
|
Graine
|
|
Solanum melongena
|
Aubergine
|
Fruit
|
|
Tetrapleura tetraptera
|
Fruit à quatre ailes
|
Fruit
|
|
Xylopia parviflora
|
Poivre de sédhiou
|
Fruit
|
Source : Noumi E. (1984). Les plantes
à épices, à condiments et à aromates du Cameroun,
Thèse de Doctorat 3e cycle, Université de
Yaoundé, Cameroun.



