II.4.1. DOSAGE DES ÉLÉMENTS EN TRACES
MÉTALLIQUES
II.4.1.1. TRAITEMENT DES ÉCHANTILLONS
La méthode appliquée pour le traitement des
échantillons est celle proposée par UNEP/IAEA (1985a, 1985b et
1986) qui s'effectue à partir des opérations suivantes :
Lyophilisation : La lyophilisation
est une technique permettant la déshydratation de l'échantillon
congelé par sublimation à basse température (-55°C)
et sous vide (0,1 bar) pendant 48 heures. Au bout de 24 h les
échantillons sont retirés du lyophilisateur (Fig.II.9.A) pour
être remués à l'aide d'une spatule en acier inoxydable afin
de permettre leur déshydratation complète si nécessaire.
La lyophilisation est préférable à la
déshydratation à l'étuve car cette dernière
entraine une perte des ETM les plus volatiles en particulier le mercure.
Broyage: Les sédiments
lyophilisés sont broyés à l'aide d'un mortier en
porcelaine. Pour le matériel biologique, les échantillons
d'oursin sont broyés en fine poudre à l'aide d'un mortier en
agate et les rhizomes à l'aide d'un broyeur centrifuge à billes :
Centrifugal Ball Mill, S 100. RETSCH® (Fig.II.9.B).

A B
Figure II.9 : (A) Lyophilisateur ; (B) Broyeur
centrifuge à billes
Homogénéisation : Le
sédiment est constitué de particules diverses, l'affinité
avec l'ETM est en fonction de la taille et de la nature de la particule
sédimentaire, ainsi dans le but d'uniformiser la répartition des
particules sédimentaires au sein de l'échantillon le lyophilisat
est récupéré et homogénéisé pendant
48 heures.
II.4.1.2. NETTOYAGE DES INSTRUMENTS
Les ETM se trouvent à l'état de traces dans le
milieu marin. Une contamination est plus que probable si les conditions
optimales d'applications et de propreté de tout instrument et de
verrerie utilisés pendant le traitement et le stockage des
échantillons ne sont pas réunies. Pour cela tout le
matériel utilisé doit subir préalablement les
opérations d'un nettoyage spécifique détaillé en
annexe I.
II.4.1.3. MINÉRALISATION DES
ÉCHANTILLONS
La minéralisation (digestion) est une opération
d'extraction et de solubilisation des ETM après décomposition des
échantillons qui s'effectue soit :
> en milieu acide : l'opérateur doit
nécessairement manipuler sous une hôte aspirante et se munir du
matériel de protection adéquat (masque à gaz, lunettes et
gants) ;
> à chaud et sous colonne à reflux ;
> par voie humide : celle-ci permet la
récupération maximale des métaux traces (PINATA, 1979).
Nous avons réalisé l'analyse des ETM au
laboratoire Régional Centre « LRC Ben Aknoun » de
l'Observatoire National de l'Environnement et du Développement Durable
« l'ONEDD» après leur minéralisation au laboratoire de
l'annexe de l'ENSSMAL de SidiFredj. Nous avons réalisé quatre
différentes minéralisations en milieu acide selon
l'élément recherché : mercure et autres métaux
traces ; et la matrice étudiée : sédiment, matériel
biologique (rhizome de posidonie et gonade d'oursin commun) comme suit :
A- Digestion du sédiment et du matériel
biologique pour la détermination du mercure total par
spectrophotométrie d'absorption atomique avec système d'hydrures
(CV-AAS)
Principe:
Ces méthodes sont applicables pour des
échantillons de sédiment ou de matériel biologique. La
forte digestion acide permet de décomposer les échantillons,
ainsi que d'oxyder et convertir toutes les formes de mercure en mercure
inorganique.
Réactifs:
- HNO3 (65% pour analyse, ISO, Merck) ;
- H2SO4 (95-97%, pour analyse, faible en mercure,
Merck) - pour le sédiment ; - K2Cr207 (10 %, pour analyse,
faible en mercure, Merck) ;
- Eau déionisée Milli-Q (>18 Mc cm,
Millipore).
Matériel:
> Tubes en Téflon avec bouchons (60 ml, Savillex) et
tubes gradués en polypropylène avec bouchons (50 ml, Sarstedt)
nettoyés suivant les procédures 1 et 3 (annexe I) ;
> Fiole jaugée de 500 ml (classe A) nettoyée
suivant la procédure 3 (annexe I) ; > Spatules en plastiques
nettoyées suivant la procédure 1 (annexe I) ;
> Balance de précision (DENVER INSTRUMENT®.
M-220D) et micropipette (Finn pipette) ;
> Plaque chauffante (Ceran 500, 22SR) et bloc en aluminium.
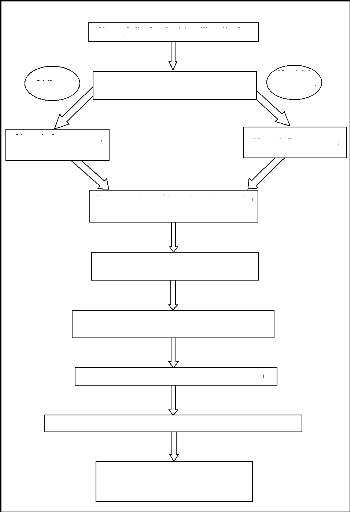
Procédure:
Ajout de 4 ml d'HNO3
et 2 ml d'H2SO4
Sédiment
Ajout d'1ml de K2Cr207 puis dilution
jusqu'au trait de jauge (50 ml)
Transfert dans les tubes de 50 ml en
polypropylène
Refroidissement à température ambiante
avant
ouverture des tubes sous une hotte aspirante
Fermeture hermétique des tubes et
mise
à température ambiante pendant 1h
Chauffage des tubes pendant 3h à
90°C
sur plaque chauffante + bloc
Homogénéisation des échantillons (2
min)
Décantation avant
analyse
(généralement toute une nuit
ou 30 minutes dans un
bac à ultrason)
Pesée de 0,5 g d'échantillon sec
dans
les tubes en Téflon (60ml)
Ajout de 5 ml d'HNO3
Matériel
Biologique
Figure II.10. : Procédure de digestion
du sédiment et du matériel biologique
pour la
détermination du mercure total par CV-SAA
B- Digestion du sédiment et du matériel
biologique pour la détermination de Plomb, et Zinc par
spectrophotométrie d'absorption atomique (SAA)
Principe:
Les échantillons sont minéralisés dans
des « bombes » en téflon fermées à l'aide de
l'acide nitrique pour le matériel biologique et d'une combinaison
d'acide fluorhydrique (HF) et d'eau régale pour le sédiment.
L'utilisation d'HF est nécessaire pour la
décomposition complète des silicates. Pour les métaux
étudiés, son utilisation a été substituée
par de l'eau régale.
Réactifs:
- HNO3 (65% pour analyse, ISO, Merck) ;
- HCL (30%, supra-pur, Merck) - pour le sédiment ;
- Eau déionisée Milli-Q (>18 Mc cm,
Millipore).
Matériel:
- Bombes en Téflon avec bouchons (50 ml, Nalgène)
et tubes gradués en polypropylène
avec bouchons (50 ml,
Sarstedt) nettoyés suivant les procédures 1 et 2 (voir annexe I)
;
- Spatules en plastiques nettoyées suivant la
procédure 1 (voir annexe I) ;
- Balance de précision (DENVER INSTRUMENT®. M-220D)
et micropipette (Finnpipette) ;
- Plaque chauffante (Ceran 500, 22SR) et bloc en aluminium.
Procédure : Voir figure II. 11.
| 


