II.4.2.3. DOSAGE DE NITRATE
Selon (WOOD et al., 1967 in LOURGUIOUI,
2006), Le passage des échantillons dans une colonne de cadmium
traité au cuivre permet la réduction de nitrate ( ~) en nitrite (
~). Ces dernières ( ~ initiaux + ~ réduits) seront ensuite
dosées par colorimétrie selon la méthode
précédemment décrite. D'après (RODIER et al.,
1996), les concentrations de nitrate sont obtenues après la
soustraction des concentrations de nitrite déterminés,
antérieurement, avant le passage des échantillons dans la colonne
réductrice.
II.4.2.4. DOSAGE D'ORTHOPHOSPHATE
Le principe du dosage d'Orthophosphate selon la méthode
de (MURPHY et RILEY, 1962 in LOURGUIOUI, 2006) repose sur la
réaction de l'anion Orthophosphate (P ~ ~) avec l'ion molybdate
d'ammonium et l'ion oxydrate de potassium (Antimoine) en milieu acide pour la
formation de l'acide phosphomolybdique. Cet acide est réduit par l'acide
ascorbique en bleu de molybdène dont l'absorbance à 880 nm est
proportionnelle à la concentration de l'ion orthophosphate
présent dans un échantillon.
II.4.2.5. DOSAGE DU SILICIUM DISSOUS
Présent à 95 % sous forme d'acide orthosilicique
Si(OH) (AMINOT et CHAUSSEPIED, 1983), le silicium dissous réagit avec le
molybdate d'ammonium en milieu acide pour former un complexe silicomolybdique
qui réduit par l'acide ascorbique donne un composé coloré
en bleu absorbant à 810 nm (MULLIN et RILEY, 1955 in
LOURGUIOUI, 2006). L'ajout de l'acide oxalique évite
l'interférence de phosphate.
Etalonnage, mesure et calcul
L'étalonnage nécessite, pour chaque sel à
doser, la préparation d'une solution mère et d'une solution fille
(voir annexes IV à VII). Une fois la solution fille prête, nous
employons le principe de neutralisation pour préparer d'autres solutions
filles plus diluées (standards), qui constitueront une gamme
étalons (annexe VIII).
Le signal d'absorption mesuré en continu par le
spectrophotomètre est traduit sous la forme d'un pic sur un ordinateur
interfacé. La hauteur du pic est proportionnelle à la
concentration du sel dans l'échantillon. La mesure de standards de
concentrations connues permet de calculer une droite de régression (de
la forme Y = a X + b) qui est utilisée pour
déterminer les concentrations inconnues. Les pics sont mesurés
par rapport à une ligne de base constituée d'eau de mer
oligotrophe (épuisée de nutriments).
Le logiciel intégré de l'appareil utilisé
réalise automatiquement tous les calculs nécessaires pour nous
permettre d'obtenir les droites d'étalonnage ci-après.
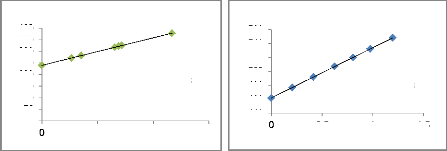
0
2 4 6
[NH4+] umol/l
50
abs = 29,605 [NH4+] +
239,98
R2 = 0,9998
400
350
Absorbance
300
250
200
150
100
0,5 1 1,5
[NO2-] umol/l
Absorbance
560
540
520
500
y = 71,781x + 462,08
R2 = 1
440
480
460
Fig. II.17 : Droite d'étalonnage
Fig. II.18 : Droite d'étalonnage
de l'Ammonium de Nitrite
0 1 2 3
[NO3-] umol/l

Absorbance
560
540
520
500
y = 31,823x + 465,94
R2 = 1
480
460
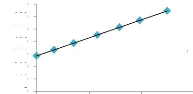
700
y = 289,54x + 284,55
R2 = 1
0
Absorbance
600
500
400
300
200
100
0 0,5 1 1,5
[PO43-] umol/l
Fig. II.19 : Droite d'étalonnage
Fig. II.20 : Droite d'étalonnage
de Nitrate d'Orthophosphate
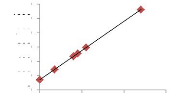
1200
1000
y = 204,07x + 141,86
R2 = 1
0
Absorbance
800
600
400
200
0 2 4 6
[SiO2] umol/l
Fig. II.21 : Droite d'étalonnage du
Silicium dissous
| 


