1.3. A partir de composés nitrosés :
1.3. a. Réaction de cétone et du
1-chloro-1-nitrosocyclohexane
Oppelzer et al35,36,37 ont
réussi à synthétiser la nitrone cyclique qui est un
intermédiaire pour la synthèse du (-)allosedamine, un agent
potentiel dans le traitement de SIDA ( syndrome immunodéficitaire
acquis). Ces auteurs ont utilisé comme catalyseur le composé
chiral le plus connu. La nitrone obtenue, après attaque de
l'énolate qui est généré par traitement basique sur
le 1-chloro-1- nitrosocyclohexane, est énantiomériquement pure.
L'addition de l'acide chlorhydrique conduit à l'hydroxylamine et
à l'aldéhyde dont la condensation entre eux donne la nitrone
cyclique (schéma 17).
NaN(SiMe3)2
Aux O O
Aux
O
Aux
O
O
N
H
OH
N
O
O O
O
O
O
H
Aux O O
H
H
O
Aux
Aux
O
O
NHOH O N
Aux O
N
O
O O
O
O O
N
H
H
H
Cl
O
Aux
Aux
O
N
OH
O H
N
O
O
Cl
O
O
O
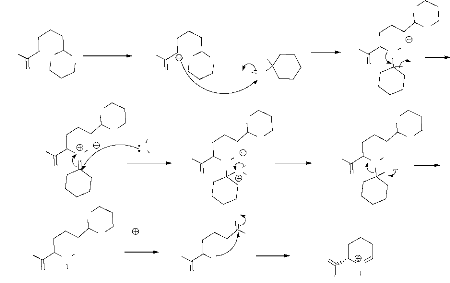
Le mécanisme d'obtention de la nitrone est montré
dans le schéma 18.

- Schéma 18 -
1.3. b. A partir de méthylène activé
et de composé nitrosé :
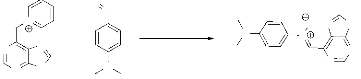
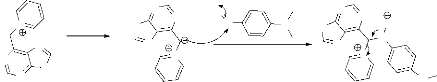
Les composés qui possèdent un
méthylène activé, par un bon groupe partant, réagit
en présence d'une base avec les composés aromatiques
nitrosés, pour donner les nitrones Narylsubstituées. Ce
procédé est plus connu sous le nom de réaction de
Kröhnke (schéma 19)38.
NaOH 2N
N
Pyridine anhydre
N
ON
N
NH
N
N
N
N
N N H
+
O
N
N
94%

N
N
N
N
N NaOH HN N N
O
N
N
HN
O
N
N
N
N
N
N
N
NH
NH
ON
N
N
N
N
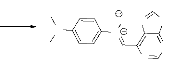
- Schéma 20 -
1.4. A partir de nitroarénes:
La réaction des aldéhydes avec les
nitroarénes s'effectue en milieu aqueux et en présence de l'agent
réducteur le zinc. Elle se déroule en deux étapes
simultanément, à savoir, la réduction de la fonction nitro
en hydroxylamine et l'attaque de cette dernière sur l'aldéhyde.
Nous obtenons la nitrone correspondante avec des rendements
acceptables39 (schéma 21).

O
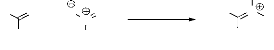
O O O NH4Cl ,Zn
+ N
Ar
N
H
R
Ar
R
H
EtOH , H2O 16 h
12 - 65%
- Schéma 21-
1.5. A partir d'amine secondaire :
a. L'oxydation d'amine secondaire utilisant le
complexe (MTO/Urée, H2O) 40 a montré
son efficacité et sa non-toxicité pour la préparation des
nitrones a partir des amines secondaires.
Les rendements sont excellents (schéma 22).
R
R1 N
H
CH3ReO3 (0.5%)

urée, H2O2,CH3OH, 2.5h
R
R1 N
O
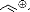

50 - 91%
- Schéma 22 -
b. L'oxydation des produits organiques,
telles que les amines, par l'oxygène41 en
présence du perchlorate de 5-éthyl-3-méthyllumiflavinium
comme catalyseur et l'hydrazine monohydraté conduit aux nitrones avec de
très bons rendements (schéma 23).

O2
(1 atm)
CF3CH2OH
, 60°C, 3h
flavin 5mol
1.1eq hydrazine/eau
NH
N
O
85 %
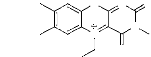
flavin:
N
N
O
O
ClO
N
N
- Schéma 23 -
1.6. A partir d'imines.
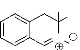
a. Larson et al42
ont développé une méthode de synthèse des nitrones
cyciques à partir des imines correspondantes. Ces composés ont
une activité anti-stroke (endommagement cellulaire) potentiel. La
procédure consiste en la réduction de l'imine en amine avec le
borohydrure de sodium, suivie de l'oxydation par l'eau
oxygénée. Le résultat de la réaction est la
formation de la nitrone cyclique (schéma 24)
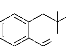
R1
R2
N
R1
N
R2
O
1)NaBH4
2) H2O2 , Cat NaWO4
- Schéma 24 -
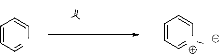
b. Le couple urée/eau
oxygéné43 est stable peu
coûteux et facilement manipulable. Ce réactif est utilisé
dans l'oxydation efficace des différentes molécules organiques
(schéma 25).
c.
87%
-schéma 25-
N
85°C, 25min
N O
O
H2N NH2
, HOOH
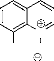
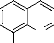
L'oxydation par l'acide
méta-chloroperbenzoïque44 de la
8-hydroxyquinolèine, en présence du 1,2dibromoéthane et du
dichlorométhane, en phase fluorée (C6F14) fournit une
nitrone stable (schéma 26).
CH2Cl2, C6F14
BrCH2CH2Br
1,5eq. m-CPBA, TA, 72h
N
O
OH
N
OH
- Schéma 26 -
d. La N-oxydation, des imines
aromatiques, donne directement la fonction nitrone. La réaction a lieu
généralement par l'intermédiaire de peracides
(schéma 27)45.


O
N
H
oxone
KHCO3
(CH3)2CO ou CH3CN
2H2O
O
O
N
H
97%
Oxone : 2KHSO5.KHSO4.K2SO4
- Schéma 27 -
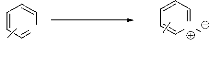
e. Oxydation par perborate de sodium.
Le Perborate de sodium est un réactif très efficace
pour l'oxydation des imines conjugués en leur N-Oxydes
(schéma 30)46.
60-70%
1.1eq SPB
CH3CO2H 40°C, 3-4 h
N
R O
N
R
- Schéma 30 - Les résultats obtenus sont
illustrés dans le tableau suivant. Tableau
|
Produits
|
O
N
|
O
N
HO
|
N O
NC
|
|
Rdt (%)
|
75
|
73
|
60
|
1.1.7. A partir des oxaziranes:
La réaction entre les imines et l'eau
oxygénée a été employée pour la
synthèse de grandes variétés de dérivés de
3-aryloxazirane. Le réarrangement thermique des dérivés
de3-aryloxazirane donne les nitrones correspondantes avec des rendements qui
varient entre 50 et 100 %. L'isomérisation thermique des
oxaziranes47,48 autres que les 3-aryloxaziranes ne
donnent pas des nitrones, mais d'autres produits, généralement
des amides (schéma 31).

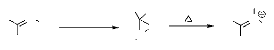
R N
Ar
R1 H2O2
R Ar
O
N
R1
O
R
Ar
N
R1
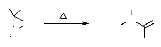
R
R
R R N O
R1
N O
R1
- Schéma 31-
Résultats
Comme nous l'avons mentionné dans la première
partie, en ce qui concerne la préparation des nitrones, les
méthodes de condensation entre les composés carbonylés et
les hydroxylamine-Nsubstituées sont les plus souvent
employées pour la synthèse de ces
produits13,14,15.
Nous avons pu préparer quelques nitrones à
partir de différents composés de départ tels que les
aldéhydes (aliphatiques, et aromatiques para substitués, et non
substitués) et les hydroxylaminesN- Substituées. En
plus, nous avons utilisé différents procédés de
synthèse en tenant compte de la structure des produits de
départ.
Les hydroxylamines utilisées sont les suivantes :
CH3NHOH , HCl PhNHOH
1 2
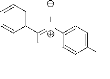
Nous avons également synthétisé une nitrone
9 à partir de la condensation entre le parahydroxynitro
benzène et le benzaldéhyde.
O
N
H
OH
9
1. Synthèse de nitrones à partir de la
condensation entre un aldéhyde et l'hydrochlorure
de-N-méthylhydroxylamine.
Cette réaction nous a permis d'aboutir aux
différentes nitrones aliphatiques et aromatiques par des manipulations
relativement simples. En effet, nous procédons à l'addition d'une
base en l'occurrence la triméthylamine, qui a pour rôle de
libérer l'hydroxylamine, dans le but de former le sel correspondant, que
nous séparons ensuite par filtration sous vide. Les molécules
d'eau générées au cours de la réaction ont
été éliminées par le Dean Stark pour éviter
la réaction inverse.
a. Réaction avec le propanaldéhyde.
La réaction de l'hydrochlorure de
N-méthylhydroxylamine 1 avec le
propanaldéhyde à reflux du toluène pendant une trois
heures du temps donne la nitrone 3 (schéma 1). Le
rendement est estimé à 71 % (d'après le brut), ce produit
est instable et décompose par le contacte avec des solvants polaires ou
portiques, nous pensons que ce ci est dû à l'absence de
conjugaison. Donc on a pas pu l'identifié avec les méthodes
spectroscopiques usuelles.

H3CH2C
H
O + 1
NEt3

toluène,reflux 3h
H3CH2C
H
N
+ HNEt3,Cl + H2O
CH3
3
- Schéma 1-
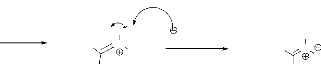
Le mécanisme réactionnel s'effectue selon le
schéma suivant :

CH3NHOH,HCl + NEt3 CH3NHOH + HNEt3 ,Cl
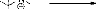
O
H3CH2C H
H H
- Schéma 2 -
H
O
OH
CH3
-H2O
H3CH2C N CH3
H3CH2C N O
CH3NHOH O
H3CH2C N
H
OH H3CH2C N
CH3
OH
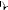
CH3
Le doublet de l'atome d'azote, de l'hydroxylamine,
formée à partir de l'hydrochlorure d'hydroxylamine de
départ, attaque le carbone du carbonyle. Après élimination
d'une molécule d'eau, nous obtenons la nitrone 3
(schéma 2).
| 


