1.2. Historique :
En 1839 William GROVE décrit la première pile
à combustible. Elle fonctionne à l'hydrogène et à
l'oxygène, à basse température, avec des électrodes
de platine et de l'acide sulfurique comme électrolyte [1, 2].
Dans son expérience, il utilisait un tube en U avec
deux électrodes en platine. Grâce à un courant
électrique, il parvint à obtenir de l'hydrogène et de
l'oxygène: c'est ce que l'on appelle
l'électrolyse. Mais en coupant ce courant, il constata
que ces gaz donnaient lieu à un courant électrique de sens
inverse au premier.
Cependant, cette technique resta ensuite plus ou moins dans
l'oubli tandis que se développaient les machines thermiques, les
accumulateurs et les piles électriques. Pourtant des chercheurs
continuèrent de s'intéresser à cette technologie:
· En 1889, L. Mond et C. Langer introduisent les
catalyseurs (platine) et perfectionnent l'électrolyte,
· en 1921, E. Baur découvrant l'importance de la
cinétique et construit une cellule fonctionnant à haute
température (1000°C),
· Au début du siècle, l'électrolyte
est amélioré: introduction de nouveaux matériaux:
carbonates fondus, oxydes solides, acide phosphorique qui seront la base des
différents types des piles d'aujourd'hui.
Mais le progrès essentiel est marqué pour
Francis T. Bacon qui construit une pile avec un
électrolyte alcalin. Cette pile fonctionnait entre 80 et
2000.
On site une chronologie de développement des piles
à combustible :
+ 1839: Découverte de la pile à combustible par
WILLIAM grove. + 1945: les allemands et les russes débutent la
recherche.
+ 1960: Utilisation par la NASA pour alimenter les
fusées.
+ 1991: Commercialisation d'un moteur GPL fonctionnant au
méthanol
+ Novembre 1998: Grand système allemand de pile à
hydrogène et solaire (Evaluation du prototype).
+ Septembre 2000: La NASA lance une étude d'avions
à hydrogène, incluant des cellules de carburant.
+ Février 2001: Agence des nations unies lance le projet
d'autobus de cellule de carburant dans cinq pays en voie de
développement.
+ 2002-2003: bus équipé d'une pile à
combustible par Irisbus.
> Perspective future:
+ 2007-2008: la pile à combustible sera
compétitive sur le marché des autobus.
+ 2010: le surcoût de la pile à combustible sera
inférieur à 10% par rapport à un bus diesel. [9].
1.3. Principe de fonctionnement :
Une pile à combustible est un assemblage de cellules
élémentaires, en nombre suffisant pour assurer la production
électrochimique d'électricité dans les conditions de
tension et courant voulues. Chaque cellule est constituée de deux
compartiments différents alimentés chacun par les gaz
réactifs. Les deux électrodes, séparées par
l'électrolyte, complètent le dispositif. De façon
générale, le fonctionnement électrochimique d'une cellule
unitaire de pile à combustible peut se schématiser sous la forme
donnée dans la figure (1.2) [2, 3,4].
+
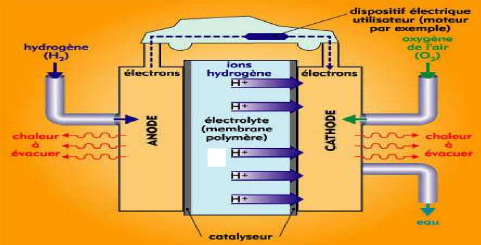
Figure (1.1): Principe de fonctionnement d'une
cellule ?? pile à combustible H2/O2 [1, 8].
Les électrodes sont exposées à un flux
de gaz qui fournit aux électrodes l'apport en carburant et en oxydant,
soit l'hydrogène et l'oxygène, respectivement. Les
électrodes doivent être perméables à ces gaz et
elles possèdent donc une structure poreuse. La structure et la
composition des électrodes peuvent être complexes et
requièrent donc d'être optimisées pour des applications
pratiques. L'électrolyte, pour sa part, doit posséder une
perméabilité aussi faible que possible aux gaz. Pour les piles
à combustible avec un électrolyte conducteur de protons (PEMFC),
l'hydrogène est oxydé à l'anode et les protons sont
transportés à travers l'électrolyte vers la cathode selon
la réaction suivante [1,2] :
2 H+ + 2 e- (1.1)
et à la cathode, l'oxygène est réduit selon
la réaction:
O2+4e- 2O-2 (1.2)
Les électrons circulent par le circuit externe durant ces
réactions. Une fois arrivés à la cathode, les protons se
recombinent avec les ions oxygène pour former de l'eau selon la
réaction:
2
1 O2 + 2 H+ + 2e- H2O (1.3)
Le bilan donne donc:
H2 + 1 O2 H2O + chaleur + électricité
(1.4)
2
Ces réactions d'oxydation de l'hydrogène
(à l'anode) et de réduction de l'oxygène (à la
cathode) s'effectuent à l'interface électrolyte/électrode
en présence d'un catalyseur (platine), en des points appelés
« points triples » figure (1.2) :
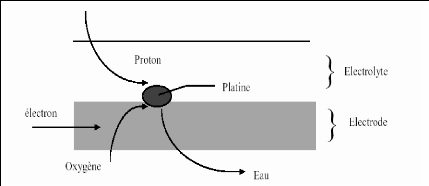
Figure (1.2): Schéma d'une zone active
de cellule de pile à combustible H2/O2 [1, 8].
En ces points, nous trouvons, autour de la particule de
catalyseur :
· Une continuité physique avec l'électrolyte
pour assurer la conduction des protons H+.
· Une continuité physique avec le conducteur
électronique qu'est l'électrode, pour assurer la conduction des
électrons eÎ.
· Une structure poreuse capable d'assurer la diffusion
de l'hydrogène ou de l'oxygène moléculaire.
· Une structure hydrophobe pour assurer
l'élimination de l'eau formée, dans le cas de la cathode.
· Une structure thermiquement conductrice pour assurer
l'évacuation de la chaleur de réaction.
· Nous pouvons ainsi apprécier la
difficulté de réalisation de cette interface qui
représente un point clé de la réalisation de l'ensemble
Electrode-Membrane-Electrode, appelé souvent EME.... [4]
| 


