3.4.7 Application des disques imprégnés
d'antibiotiques
Les antibiotiques utilisés pour l'antibiogramme
provenaient des disques Bio Mérieux et Bio Rad. Ils ont
été placés individuellement avec des pinces
stériles. Le nombre des disques par boite de pétri devait
être de telle sorte que les zones d'inhibitions ne se coupaient pas afin
de permettre la lecture des diamètres dans plusieurs directions. Le
nombre de disque choisi variait entre 6 à 7 par boite de 90
millimètres.
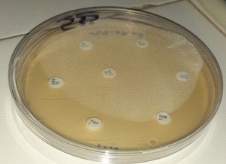
Photo 16 : Disposition de
disque d'antibiogramme
3.4.8. Lecture et interprétation
Après 24 heures d'incubation, les zones d'inhibition
circulaires autour de chaque disque ont été mesurées
à l'aide d'une règle graduée et comparées aux zones
d'inhibition standard. Les diamètres critiques ont été
proposés par le fabricant conformément au NCCLS. (Performances
standards for Antimicrobiolsucceptibillitytesting).
1.5. Méthodes Manuelles
par l'hémoculture
Le diagnostic des bactériémies repose sur une
mise en culture des bactéries éventuellement présente dans
le sang, appelée hémoculture (diagnostic au laboratoire
des bacteriémie, 2023). En règle générale, une
hémoculture correspond à une paire de flacon aérobie et un
flacon anaérobie (diagnostic au laboratoire
des bacteriémie, 2023).
La prescription des hémocultures se justifient dans les
cas suivants :
· Présence des signes de sepsis (hyperthermie >
38.5°, hypothermie < 36.5°, · frissons...)
· Suspicion d'endocardite infectieuse (fièvre,
souffle au coeur.) ;
· Existence d'une fièvre inexpliquée chez
une femme enceinte, un nouveau-né ou un patient
immunodéprimé ;
· Patients à risque (aplasie par exemple).
Le prélèvement doit répondre
à 3 objectifs :
· Limiter au maximum le risque d'exposition au sang du
préleveur (VHB, VIH) ;
· Limiter au maximum la contamination microbienne du
prélèvement ;
· Prélever une quantité de sang
suffisante.
Les hémocultures inoculées sont
acheminées au laboratoire sans tarder.
Lorsque le laboratoire utilise
un automate d'hémoculture, pour éviter que la croissance
bactérienne débute avant le dépôt des flacons dans
l'automate, il est recommandé de ne pas placer les flacons
ensemencés à 37°C.
Pour faire l'incubation on doit homogénéiser le
sang et le bouillon par retournement des flacons puis on va incliner 5
à10 minutes le flacon aérobie afin de recouvrir et ainsi
ensemencer la partie et ainsi ensemencer la partie. L'incuber à
37°C en position verticale le flacon d'hémoculture.
Examen visuel des flacons 1 à 2 fois par jour pendant
10 jours. Chaque jour, on inspecte les flacons pour rechercher les signes
témoignant d'une croissance visible. Sur la gélose
présence des colonies et dans le bouillon apparition d'un trouble ou
d'une hémolyse.
Un flacon négatif montrera un culot globulaire rouge
vif et le bouillon reste limpide et un résultat positif s'observe
lorsque le mélange sang bouillon dépasse le manchon de
l'indicateur de croissance.
Dans le cadre de la démarche qualité, et pour
une bonne traçabilité, les prélèvements
reçus au laboratoire sont inscrits dans les registres de laboratoire et
saisis sur support informatique. Volume sanguin : le nombre de bactéries
par ml de sang étant en général faible, il importe de
prélever une quantité suffisante de sang :
ü Pour l'adulte, 10 ml par ponction veineuse
périphérique. La veine du pli du coude est la plus
indiquée.
Chez l'enfant ou le nouveau-né, le volume de sang
à prélever doit être déterminé par le
médecin traitant. Pour le nouveau-né, il est souvent difficile
d'obtenir plus d'1 à 2 ml de sang. Chez l'enfant 2 a 5 ml de sang
peuvent suffire. Un volume de 5 ml de sang est prélevé sur le
patient et injecte directement dans les flacons d'hémoculture et
incubé à l'étuve pendant une semaine. Lorsqu'on constate
après une semaine des turbidités dans le flacon
d'hémoculture, on va faire le gram, si c'est les bactéries
à Gram négatif qui sont observées, la
référence est faite à l'organigramme ainsi qu'il suit si
le micro- organisme pousse sur la gélose au sang, faire un test
d'oxydase et inoculer une galerie API 20 E. Les Enterobacteriacea (tels que
Salmonella, Shigella) sont oxydase- négatifs. Pour le test
d'oxydase l'aide de pince une goutte de réactif d'oxydase a
été déposée sur le papier buvard, placé sur
une lame porte objet. Ensuite une colonie bien isolée et
représentative a été prélevée à
l'aide de l'anse, puis frottée doucement sur le papier buvard. Le test
est positif lorsqu' une coloration violette apparait dans un délai de 30
secondes. En absence de coloration ou coloration au-delà de 30 secondes
le test est négatif (Paul, 2004). Dans ce test les
caractéristiques des Salmonella, Shigella ont : oxydase (-).
Si les micro-organismes isoles sont identifiés comme
étant Salmonella, Shigella et confirmer par la galerie
API 20E, À l'aide d'une pipette, ont été introduit la
suspension bactérienne dans les microtubes de la galerie. L'incubation
s'est faite à 37°C pendant 24 heures. La lecture de ces
réactions se faits à l'aide du tableau de lectureet
l'identification des souches est obtenue à l'aide du tableau
d'identification du catalogue analytique et faire l'antibiogramme pour les
sensibilités des germes.


Figure 16: Hemoculture Negative
Figure 17: Hemoculture Positive
| 


