2.3. Caractéristiques histologiques
Le type histologique le plus fréquemment
diagnostiqué chez les patientes était l'adénocarcinome
(87%), suivi du carcinome épidermoïde (13%) (Tableau 1).
La confirmation histologique a été
réalisée par biopsie scannoguidée chez 61% des cas, par
bronchoscopique chez 18.2% des cas, par biopsie osseuse chez 14.2% des cas, par
biopsie ganglionnaire sus-claviculaire chez 3% des cas et chez 1.2% des cas,
elle a été réalisée par
|
biopsies cérébrale, hépatique et
péricardique (Tableau 2). Tableau 2: Méthodes de
confirmation histologique des CPNPC
|
|
|
|
Méthodes utilisées
|
n=77
|
%
|
|
Biopsie scannoguidée
|
47
|
61
|
|
Bronchoscopie
|
14
|
18.2
|
|
Biopsie osseuse
|
11
|
14.2
|
|
Biopsie ganglionnaire sus-claviculaire
|
2
|
3
|
|
Biopsie cérébrale
|
1
|
1.2
|
|
Biopsie hépatique
|
1
|
1.2
|
|
Biopsie péricardique
|
1
|
1.2
|
2. Données radiologiques
Sur base de la Tomodensitométrie
Thoraco-Abdomino-Pelvienne (TDM TAP), les tumeurs étaient localement
avancées dans la majorité des cas. Ainsi, les tumeurs T4
représentaient 40.4% et l'envahissement ganglionnaire N2 était
retrouvé dans 41.4% des tumeurs (Tableau 3).
En se basant sur la 8ème édition de la
classification TNM (Annexe 2), le stade radiologique le plus fréquent
était le stade IV chez 90.9% des patientes. Le stade III était
présent chez 7.8% des patientes et une seule patiente a
été diagnostiquée au stade I (1.3%) (Tableau 4).
70% de nos patientes avaient plus d'un site
métastatique. Les localisations métastatiques les plus
fréquentes étaient celles au niveau pleural, osseux, pulmonaire,
hépatique et cérébral (Tableau 5).
Tableau 3: Répartition des tumeurs selon
les classifications TNM
|
Classification
|
n
|
%
|
|
T
|
|
|
|
T1
|
10
|
19.2
|
|
T2
|
10
|
19.2
|
|
T3
|
11
|
21.2
|
|
T4
|
21
|
40.4
|
|
N
|
|
|
|
N0
|
18
|
31
|
|
N1
|
7
|
21.1
|
|
N2
|
24
|
41.4
|
|
N3
|
9
|
15.5
|
|
M
|
|
|
|
M0
|
7
|
9.1
|
|
M1
|
70
|
90.9
|
|
M1a
|
48
|
68.57
|
|
M1c
|
22
|
31.43
|
Tableau 4: Stades radiologiques
Stadesa n Pourcentage
(%)
1.3
1 1.3
7.8
2 2.6
4 5.2
Stade I IA-2
Stade III
IIIA IIIB

24
Stade IV IVA
a. 8ème classification TNM.

25
Tableau 5: Répartition des
différentes localisations métastatiques
Localisations métastatiques n
Pourcentage (%)
Pleurale 39 55.7
Osseuse 31 44.3
Pulmonaire 21 30
Hépatique 12 17.1
Cérébrale 10 14.3
Surrénalienne 6 8.6
Péricardique 5 7.1
3. Profil moléculaire
Le test de mutation de l'EGFR (Epithelial Growth Factor
Receptor) a été réalisé chez 27 patientes (35% des
cas), revenant positif chez 13 patientes (48.1%) et négatif chez 14
patientes (51.9%). Les mutations étaient prédominantes sur l'exon
19 (9 patientes soit 69.2%), suivies par la mutation L858 sur l'exon 21 (4
patientes soit 30.8%) (Tableau 6).
La mutation ALK (Anaplastic Lymphoma
Kinase) qui a été recherchée chez 8 patientes
(soit 29.6% des cas), a été positive chez une patiente, celle qui
était au stade IA-2 (soit 12.5%). La recherche de la mutation ROS1
(Reactive Oxygen Species) a été réalisée chez 2
patientes (7.4%) et était négative dans les deux cas (Tableau
6).
La recherche de l'expression du PD-L1 (Programmed Death-Ligand
1) a été effectuée chez 6 patientes. Une faible
positivité (<50%) a été retrouvée chez 5
patientes représentant 83.3% des cas et une forte positivité
à 60% a été noté chez une seule patiente
(16.7%).
Tableau 6: Statut des mutations EGFR, ALK et
ROS1
|
n
|
Pourcentage %
|
|
Mutation de l'EGFR
|
|
|
|
Réalisée
|
27
|
35
|
|
Positive
|
13
|
48.1
|
|
Mutation sur :
|
|
|
|
Exon 19
|
9
|
69.2
|
|
L858 sur l'exon 21
|
4
|
30.8
|
|
Mutation ALK
|
|
|
|
Réalisée
|
8
|
29.6
|
|
Positive
|
1
|
12.5
|
|
Mutation ROS1
|
|
|
|
Réalisées
|
2
|
7.4
|
|
Positive
|
0
|
0
|

26
4. Prise en charge thérapeutique
Le délai entre la confirmation histologique et le
début du traitement des patientes dans notre étude était
de 2.1 mois en moyenne, il était variable entre 6 jours et 13.8 mois.
Parmi les 77 patientes, 13 ont été perdues de
vue (16.8%) et 6 patientes (7.8%) avaient reçu des soins de support
palliatifs exclusifs (BSC : Best Supportive Care). 1 seule patiente (stade
IA-2) a été adressée pour chirurgie (1.3%) puis perdue de
vue, 3 patientes stade IIIB (4%) avaient reçu une chimiothérapie
néoadjuvante suivie d'une radiochimiothérapie concomitante (RCC)
puis mise sous surveillance et 54 patientes stade IV (70.1%) avaient
reçu un traitement systémique palliatif en première ligne.
Parmi celles-ci, 46 avaient reçu une chimiothérapie à base
de sels de platine (dont 5 EGFR muté) (85.2%) et 8 EGFR muté
(14.8%) un traitement par anti-EGFR (Figure 1).
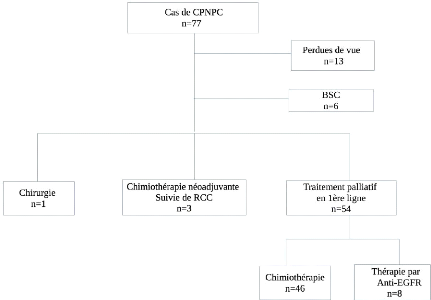
Figure 1: Schéma des traitements
utilisés chez les patientes atteintes de CPNPC
La figure 2 présente les protocoles utilisés en
première ligne chez les patientes au stade IV. L'acide zoledronique a
été associé au traitement systémique palliatif chez
13 patientes (16.9%

27
Protocoles de 2ème ligne
Docétaxel
Gemcitabine monothérapie Navelbine monothérapie
Etoposide monothérapie Carbo-Paclitaxel Carbo-Navelbine
Paclitaxel Pemetrexed Erlotinib
|
n=20
|
Pourcentage (%)
|
|
6
|
30
|
|
3
|
15
|
|
2
|
10
|
|
2
|
10
|
|
1
|
5
|
|
1
|
5
|
|
1
|
5
|
|
1
|
5
|
|
3
|
15
|
des cas) et le bevacizumab chez 3 patientes (4% des cas). Le
nombre moyen de cycles de chimiothérapie reçu était de 3.8
[extrêmes : 1 - 7]. Pour la thérapie par anti-EGFR, le nombre
moyen de cycles était de 15.9 [extrêmes :6 - 40]. Parmi les 46
patientes ayant reçu une chimiothérapie, 16 patientes n'ont pas
pu être évaluées pour la réponse au traitement car
perdues de vue au cours du suivi. L'évaluation de la maladie a
été basée sur les critères RECIST
présentés en annexe 3. Parmi les 30 patientes ayant une maladie
évaluable, 1 patiente (3.3%) a eu une réponse partielle, 6
patientes (20%) ont eu une stabilité et 23 patientes (76.6%) avaient une
progression. Concernant le traitement par anti-EGFR (n=8), 1 patiente a
été perdue de vue (12.5%), 1 patiente avait une réponse
partielle (12.5%), 5 patientes présentaient une stabilité (62.5%)
et 1 patiente avait une progression (12.5%).
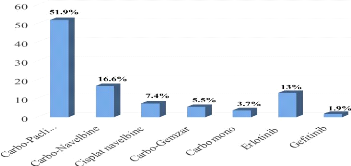
Figure 2: Protocoles utilisés chez les
patientes en 1ère ligne
Après progression, 20 patientes ont reçu un
traitement systémique de 2ème ligne. 17 patientes, (soit 85%) ont
reçu la chimiothérapie et 3 patientes (15%) ont reçu
l'anti EGFR (Tableau 7).
Tableau 7: Protocoles utilisés chez les
patientes en 2ème ligne

28
La radiothérapie palliative a été
réalisée chez 23 patientes, décompressive sur le rachis
chez 10 patientes, cérébrale chez 9 patientes, de consolidation
et antalgique sur le col du fémur chez 2 patientes et sur
l'humérus chez 1 patiente et enfin une radiothérapie palliative
pulmonaire a été réalisée chez 1 patiente.
5. Survie
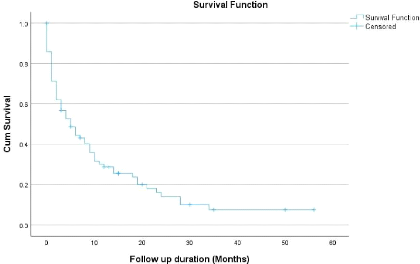
Dans notre série, le suivi médian était
de 5 mois [extrêmes : 0-56], la survie globale (SG) médiane
était de 5 mois IC 95% [2.2-7.7]. La survie sans progression (SSP)
médiane était de 5 mois IC 95% [3.6-6.4]. Par ailleurs, les taux
de survie globale à 6 et 12 mois étaient de 44.4% et 28.7%
respectivement et les taux de survie sans progression (SSP) à 6 et 12
mois étaient de 38.5% et 7.7% respectivement (Figures 3 et 4).

29
Figure 3: Courbe de Kaplan-Meier
représentant la survie globale des patientes
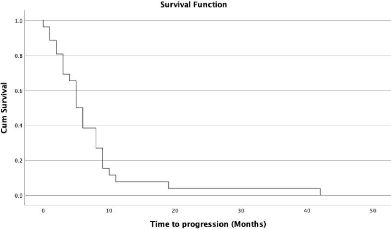
Figure 4: Courbe de Kaplan-Meier
représentant la survie sans progression des patientes

30
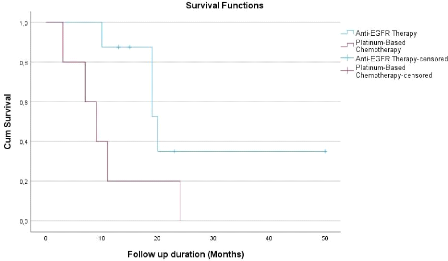
La survie globale (SG) médiane dans le groupe des
patientes EGFR muté traitées par anti EGFR était de 20
mois IC 95% [12.6-27.4] et dans le groupe EGFR muté traité par
chimiothérapie à base de sels de platine, elle était de 9
mois IC 95% [4.7-13.3]. Cette SG médiane chez le groupe thérapie
anti EGFR était significativement plus longue que celle dans le groupe
chimiothérapie à base de sels de platine avec une valeur de
p=0.05 (Figure 5).
De même, la survie sans progression (SSP) médiane
dans le groupe des patientes EGFR muté traitées par anti EGFR
était de 19 mois IC 95% [8.3-29.7] alors que dans le groupe des
patientes mutées pour l'EGFR traité par chimiothérapie
à base de sels de platine, celle-ci était de 5 mois IC 95%
[0.7-9.3]. La SSP médiane chez le groupe thérapie anti EGFR
était aussi significativement plus longue que celle chez le groupe
chimiothérapie aux sels de platine avec une valeur de p=0.028. On a
noté également que les courbes de la survie globale et celle de
la survie sans progression du traitement par chimiothérapie ont
chuté plus rapidement par rapport à celles du traitement par anti
EGFR signifiant que le décès des patientes s'est produit
très rapidement sous chimiothérapie (Figure 6).

31
Figure 5: Courbe de Kaplan-Meier
représentant la survie globale des patientes EGFR muté
traitées par anti EGFR et par chimiothérapie à base de
sels de platine
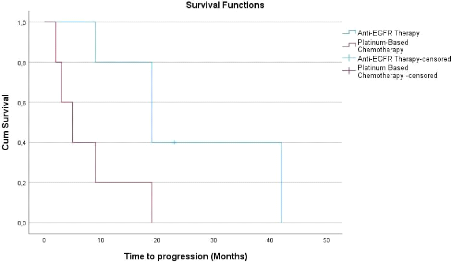
Figure 6: Courbe de Kaplan-Meier
représentant la survie sans progression des patientes
EGFR
mutées traitées par anti EGFR et par chimiothérapie
à base de sels de platine

32
Discussion

33
| 


