Partie
Expérimentale
Quatrième
Chapitre
Matériels et
méthodes
Chapitre. IV. Matériels et méthodes
1. Choix des échantillons de miel
Nous avons travaillé sur 9 échantillons de miel
des années 2008 et 2009 provenant de différentes régions
de la wilaya de Djelfa et 1 échantillon provenant de la région de
la Mitidja et 4 autres échantillons des miels importés, à
chaque échantillon, il à été attribué un
code désignant :
- l'origine géographique du miel ;
- l'origine florale présumée ;
- la date de récolte ;
- mode d'extraction.
Tableau 10: Présentation des
échantillons du miel étudiés
|
N° de
l'échantillon
|
Date de
récolte
|
Lieu de récolte
|
Origine florale
présumée
|
Type
d'extraction
|
|
Miels locaux
|
01
|
Aout 2008
|
Messâad (Oued
Djdey)
|
Jujubier
|
Mécanique
|
|
02
|
Avril 2009
|
Messâad (El
gahera)
|
Toutes fleurs
|
Manuel
|
|
03
|
Juin 2008
|
Amn Ouassara
(Sersou)
|
Toutes fleurs
|
Mécanique
|
|
04
|
Juin 2008
|
Amn el-bel
|
Toutes fleurs
|
Manuel
|
|
05
|
Juin 2008
|
Amn Ouassara
(Sersou)
|
Toutes fleurs
|
Mécanique
|
|
06
|
Juin 2009
|
Messâad (Tamdit)
|
Toutes fleurs
|
Mécanique
|
|
07
|
Juin 2009
|
Messâad (Mlaga)
|
Les épineux
|
Mécanique
|
|
08
|
Juin 2009
|
Hassi bahbah
|
Toutes fleurs
|
Mécanique
|
|
09
|
Mai 2009
|
Amn Ouassara
(Sersou)
|
Toutes fleurs
|
Mécanique
|
|
10
|
Juin 2009
|
Mitidja (Boufarik)
|
Les agrumes
|
Mécanique
|
|
Miels import&
|
11
|
Juin 2008
|
Espagne
|
Toutes fleurs
|
Mécanique
|
|
12
|
Juin 2008
|
Arabie saoudite
|
Toutes fleurs
|
Mécanique
|
|
13
|
Juin 2008
|
Inde
|
Toutes fleurs
|
Mécanique
|
|
14
|
Juin 2008
|
Mali
|
Toutes fleurs
|
Mécanique
|
2. Le Protocole expérimental
Nous avons adopté le protocole expérimental
présenté au niveau de l'organigramme ci
après :
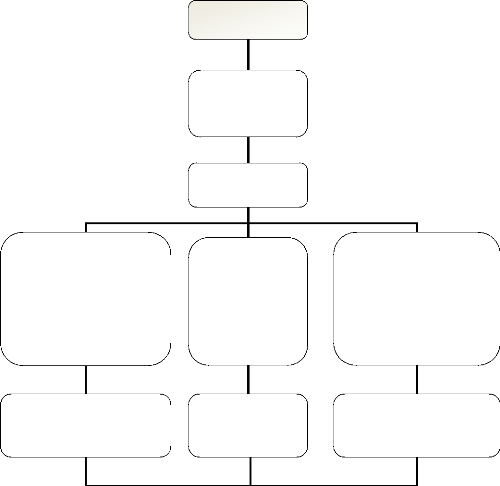
Miels purs
Répartition en flacons et
conservation à
l'abri de
l'humidité et de
la
lumière
Analyses physico-
chimiques et polliniques
Analyses polliniques
Teneur en eau, Degré brix,
l'HMF,
les protéines, l'acidité.
Analyses chimiques
Indice de réfraction,
Absorbance,
Densité,
pH, Conductibilité
électrique
Analyses physiques
- Examen microscopique de la
présence des grains de
pollen
(quantité), des différentes formes
de grains de
pollen.
- Prise des photos
Caractérisation chimique
Caractérisation
physiques
Identification du pollen et
estimation de
l'origine florale
Evaluation de la qualité et
comparaison des miels
Figure 6 : Le protocole expérimental
3. Analyse physique 3.1. La densité
La densité est obtenue en calculant le quotient de la
masse volumique d'un miel et de la même masse volumique
d'eau distillée.
On pèse 5 mg d'eau distillée et on
note le poids, également pour l'échantillon
à analyser dont on note le poids aussi, La densité est
exprimée par la relation:
D = M / M'
Où:
M : Masse du volume du miel;
M' : Masse de même volume
d'eau distillée. 3.2. Le pH
Selon LOUVEAUX (1985), le pH est mesuré en solution dans
l'eau à 10%, à l'aide
d'un pH-mètre. (figure 7 et 8)
Le pH (ou potentiel hydrogène ou indice de
Sorênsen) est défini comme le cologarithme de la concentration en
ions H dans une solution. Pour le miel, c'est un indice de la
« réactivité acide »
du produit.
Le miel est mis en solution à 10 % dans
l'eau distillée. Il suffit de plonger la pointe de
l'électrode dans le liquide la valeur du pH
s'affiche au potentiomètre au centième
d'unité. Le pH-mètre doit être
étalonné avant son utilisation à. l'aide
des solutions tampons (de 7 et 4 par exemple).

Figure 7 : Préparation des Solutions du
miel Figure 8 : Le pH-mètre utilisé
3.3. La conductibilité
électrique
Selon LOUVEAUX (1985), la mesure de la conductibilité
électrique se fait au moyen d'un conductimètre
dans une solution de miel à 20 % de matière sèche (figure
n° 9). On opère à
20°C. La mesure est rapide, mais la préparation de
la solution exige une pesée précise et une mesure de la teneur en
eau.
Cette méthode a pour objet de vérifier si la valeur
de la conductivité électrique du miel analysé est
compatible avec son appellation florale.
Pour la mesure de la conductibilité électrique, il
suffit de préparer une solution à 20% de miel avec de
l'eau distillée, puis plonge la pointe de
l'électrode du conductimètre
électrique.
Lire directement sur l'écran la valeur de
la conductivité électrique.

Figure 9 : Le conductimètre
électrique utilisé 3.4. L'absorbance
La mesure de l'absorbance a été
faite selon la méthode de la FAO (1969). Peser 5g de miel et dissoudre
dans 100 ml d'eau distillée pour une solution de 5% de
concentration. La mesure de l'absorbance est
réalisée à l'aide d'un
spectrophotomètre à 575 nm après avoir étalonner
l'appareil avec de l'eau distillée.
4. Analyse chimique 4.1. Teneur en eau
Selon LOUVEAUX (1982), la mesure de la teneur en eau se fait
très simplement au moyen d'un refractomètre. Le
miel à analyser doit être parfaitement liquide.
La goutte de miel est déposée sur la platine du
prisme d'un réfractomètre de type Abbé
à thermomètre incorporé et répartie en couche
mince. La lecture est faite à travers l'oculaire au
niveau de la ligne horizontale de partage entre une zone claire et une zone
obscure. Cette ligne coupe une échelle verticale graduée
directement en pourcentage d'humidité dans le miel. La
température du prisme est notée.
En se rapportant au Tableau de CHATAWAY (1932) (tableau
n°6), nous obtenons le pourcentage d'eau
correspondant à l'indice de réfraction à
20°C.

Figure 10 : Refractomètre spécial
pour le miel
4.2. Degré brix
Grâce à la méthode de
réfractométrie, on peut évaluer le taux de matière
sèche.
La lecture est faite sur l'échelle qui
indique la teneur en matière sèche ou degré brix qui se
trouve en parallèle avec l'échelle de
l'indice de réfraction.
4.3. Dosage des protéines
Le dosage de protéine s'effectue selon la
méthode de BIURET, en réalisant la gamme
d'étalonnage à partir d'une
solution étalon en SAB de 10g/L. (voir annexe n°
3)
A partir d'une solution de 10% de miel, 1 ml
est versé dans un tube à essai, et on ajoute 4 ml de
réactif de Gornall, on met le mélange dans une cuvette au
spectrophotomètre réglé à une longueur
d'onde X = 540 nm. Le
spectrophotomètre doit être étalonné par une
solution composée par 4 ml de réactif de Gornall et 1 ml
d'eau physiologique (comme blanc).
La teneur en protéine est exprimée comme suite :
= x 2.163 x 10
A : absorbance, 2.163 : le coefficient de correction
retiré à partir la courbe
d'étalonnage.
4.4. La détermination de
l'acidité
L'acidité libre est obtenue en
traçant la courbe de neutralisation du miel par une solution
d'hydroxyde de sodium et la détermination du pH du
point équivalent.
Pour cela, 5g de miel sont pesé et dissout dans
quelques millilitres d'eau distillée et la solution est
amenée à un volume de 50 ml dans une fiole jaugée. Avec
une pipette, 25 ml sont prélevés et versés dans un
bécher. Le liquide est agité à l'aide
d'un agitateur magnétique puis dosé à
l'aide d'un potentiomètre avec
l'hydroxyde de sodium à 0,05 N. Le pH doit être
noté immédiatement après chaque addition
d'hydroxyde de sodium.
Lorsque les variations de pH deviendront minimes, pH compris
entre 8,5 et 9, le volume de l'hydroxyde de sodium
versé dans le bécher doit être calculé pour
déterminer l'acidité libre.
L'acidité libre est exprimée en
milliéquivalent d'hydroxyde de sodium nécessaire
pour porter le pH au point équivalent E, pour 1000 grammes de miel.
|
1000 x x
Acidité libre =
|
|
|
Où:
|
|
|
|
V : le volume en milliéquivalents
d'hydroxyde de sodium verse pour atteindre le pH du point
équivalent (E) lors de la neutralisation du miel;
N : la normalité de l'hydroxyde de sodium
(0,05); M : prise d'essai (5 g).
4.5. La détermination de la teneur en HMF
:
L'HMF est un dérivé de déshydratation des
sucres ; qui apparaît par réaction chimique naturelle lors du
vieillissement ou du chauffage des miels.
L'analyse a été effectuée selon la
méthode de WINKLER parue dans le rapport de la commission international
du miel (2002). Cette mesure de la teneur en HMF est basée sur la mesure
de l'absorbance de cette molécule par spectrophotométrie
réglée à une longueur d'onde de 550nm, en présence
d'acide barbiturique et de la paratoluidine.
Dans une fiole jaugée de 100 ml, on dissout 500 mg
d'acide barbiturique dans 70 ml d'eau distillée au bain marie, on
refroidit et en complète avec de l'eau distillée jusqu'au trait
de jauge.
Solution de paratoluidine :
Dans une fiole jaugée de 250 ml, on dissout 25 g de
paratoluidine dans 50 ml de isopropanole, on ajoute 25 ml d'acide
acétique cristallisable puis on complète jusqu'au trait de jauge
avec le isopropanole.
Laisser la solution de paratoluidine à l'obscurité
24 heures avant son utilisation. Dissoudre 2 g de miel dans 10 ml d'eau
distillée (2tubes par échantillon).
Le dosage est réalisé selon le tableau suivant :
|
Essai Réactifs
|
Tube d'essai
|
Tube témoin
|
|
Solution de miel
|
1 ml
|
1 ml
|
|
Réactif de la paratoluidine à 10%
|
2,5 ml
|
2,5 ml
|
|
Solution d'acide
barbiturique à 0,5%
|
0,5 ml
|
-
|
|
Eau distillée
|
-
|
0,5 ml
|
La préparation du tube à essai ne doit pas
dépasser deux minutes. Expression des résultats
:
L'absorbance d'essai est mesurée par rapport au blanc
à 550 nm dans les trois à quatre minutes en maximum.
La teneur en HMF est exprimée en mg pour 1 kg de miel,
elle est donnée par la formule suivante :
HMF (mg/kg)= (192 x A x 10) / prise d'essai en g
Dont :
192 : facteur de dilution et coefficient d'extinction, obtenue
expérimentalement à partir de l'HMF pur. A : absorbance.
5. Analyse pollinique
L'analyse pollinique des miels donne une
information précise sur les principales plantes mellifères et
permet de caractériser les miels par leur origine botanique ou
géographique. Elle apporte des informations importantes sur le
comportement de butinage des abeilles. Par ailleurs, la teneur en pollen des
miels permet de contrôler leur qualité, augmentant ainsi leur
valeur économique.
Méthode classique
Nous avons utilisé la méthode classique
donnée par LOUVEAUX et al. (1970), 10 g de miel (pesés exactement
à 0,1 g près) sont dissous dans 20 ml d'eau
chaude (ne pas dépasser 40 °C). La solution
obtenue est centrifugée pendant cinq minutes et le liquide restant est
séparé du sédiment; le liquide peut être
versé ou aspiré. Pour une meilleure élimination des sucres
du miel il est recommandé de reprendre le dépôt par 10 ml
d'eau distillée, de le transvaser dans un tube à
centrifugation plus petit et de centrifuger à nouveau pendant cinq
minutes.
On porte le dépôt (au moyen
d'une anse de platine ou d'une fine baguette
de verre), autant que possible de façon quantitative, sur une lame
porte-objet et on le répartit sur une surface d'environ
20 X 20 mm.
Après séchage (plus avantageusement à la
chaleur mais sans excéder 40 °C) on
l'inclut dans la glycérine-gélatine et on
recouvre d'une lamelle. La glycérine-gélatine
est préalablement liquéfiée au bain- marie à 40
°C (MAURIZIOU, 1970).
La détermination de l'origine
géographique et de l'origine botanique repose sur
l'identification des pollens et des autres constituants du
sédiment d'un miel ainsi que sur leur
dénombrement. L'identification se fait avec
l'aide des données tirées des publications
spécialisées comme ceux de Mm NAAS. O (2006), et au moyen de
préparations de comparaison. (Voir les figures 11 à 15)

Figure 11: Centrifugeuse de type SIGMA

Figure 12: Les calibres de la Centrifugeuse

Figure 13: Solution du miel
après
centrifugation (le dépôt de pollens)

Figure 15 : Microscope optique a
appareil
photo numérique

Figure 14 : Lames préparées et
séchées
6. Analyse statistique :
Dans l'analyse statistique nous sommes
basé sur l'analyse de la variance (ANOVA), à
travers cette analyse, nous avons essayé de comparer entre les
différents échantillons du miel, ainsi entre les miels locaux et
les introduits.
Lors de cette analyse, nous avons établi le test de
NEWMAN-KEULS, qui est un test de comparaison de moyennes par paires,
pratiqué à l'issue d'une ANOVA.
(Annexe n°2)
Pour cela nous avons utilisé le logiciel de Statistica
version 6.1.
Cinquième
Chapitre
Résultats et
discussions
| 


